Экспериментальное обоснование возможности применения акустических ударных волн низких энергий в терапии различных урологических заболеваний
- Гарилевич Б.А. – д.м.н., профессор, врач-уролог урологического отделения РУДДК – Филиала № 1 ФГБУ «Главный военный клинический госпиталь имени академика Н.Н. Бурденко» МО РФ
- Кирпатовский В.И. – д.м.н., проф., гл. научный сотрудник НИИ урологии и интервенционной радиологии им. Н.А.Лопаткина – филиал ФГБУ «НМИЦ радиологии» МЗ РФ
- Семенов А.А. – начальник урологического отделения Филиала № 1 ФГБУ «Главный военный клинический госпиталь имени академика Н.Н. Бурденко» МО РФ
- Кудрявцева Л.В. – ассистент кафедры патологической анатомии Медицинского института РУДН
 3703
3703 Дистанционная ударно-волновая литотрипсия уже не одно десятилетие используется как метод неинвазивного удаления камней почек и мочеточников. Сфокусированная акустическая волна высокой мощности способна создавать в области-мишени резкий подъем давления, вызывающий деструкцию камня. При смещении фокуса воздействия можно получить повреждение ткани почки с образованием гематомы или развитием острого пиелонефрита. Однако при уменьшении мощности воздействия можно добиться не повреждающего, а стимулирующего эффекта, подобного физиотерапевтическому воздействию. Это было доказано путем оценки влияния низкоинтенсивного ударно-волнового воздействия (НУВВ) на параметры метаболизма в различных тканях. Этот биологический эффект ударных волн низкой интенсивности может быть полезен для лечения и реабилитации пациентов при различных, в том числе урологических заболеваниях.
Рядом исследований было доказано, что воздействие ударных волн способствует ускорению образования костной мозоли и срастания переломов, более быстрому заживлению кожных ран, приводит к усилению регенеративно-репаративных процессов и стимуляции метаболизма в тканях и клетках [1,2].
В урологической практике была доказана эффективность НУВВ при лечении болезни Пейрони, эректильной дисфункции и хронического простатита [3-9]. При воздействии на предстательную железу НУВВ способствует уменьшению отека, лейкоцитарной инфильтрации, оказывает сосудорасширяющее действие [3,6,10,11]. В экспериментальных исследованиях отмечается повышение проницаемости предстательной железы для антибиотиков и их кумуляция в ткани железы после НУВВ [12].
Показано, что комплексное лечение хронической тазовой боли с применением НУВВ по сравнению с изолированной фармакотерапией оказывает более выраженное обезболивающее и противовоспалительное действие на фоне усиления максимальной систолической скорости кровотока в органе [5,11,13].
Биологические эффекты ударных волн, реализуемые на уровне клеток и тканей, многообразны и опосредуются путем превращения механических импульсов в биохимические реакции. Совокупность клеточных механизмов формируют следующие процессы на уровне тканей: усиление реваскуляризации тканей и коллатерального кровообращения, стимуляцию микроциркуляции и лимфооттока, ускорение репаративных процессов, оказывает обезболивающее, противовоспалительное и противоотечное действие [14-16].
Этот спектр действия НУВВ позволяет предполагать, что данный метод терапии может быть полезен не только для лечения заболеваний предстательной железы, но и при других патологических состояниях. Однако этот вопрос в научной литературе оказался практически не освещен.
Это послужило основанием для проведения данного исследования.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование выполнено на базе Филиала № 1 ФГБУ «ГВКГ им. Н.Н.Бурденко» МО РФ и отдела экспериментального моделирования урологических заболеваний НИИ урологии и интервенционной радиологии им. Н.А.Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России. Все исследования проводились в соответствии с «Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей».
Для подбора параметров стимулирующего воздействия ударных волн на ткань почек проведены экспериментальные исследования по изучению воздействия акустических ударных волн на интактную почку и действие НУВВ с этими параметрами было изучено при моделировании гидронефротической трансформации, острого и хронического пиелонефрита.
Наркотизацию животных производили путем внутрибрюшинного введения 5% раствора тиопентала натрия или гексенала в дозе 45- 60 мг/кг. После завершения экспериментов эвтаназию животных производили путем интраперитонеального введения тиопентала натрия либо гексенала в дозе 300-400 мг/1 кг.
Серия экспериментальных исследований проведена на 43 белых беспородных крысах обоего пола массой 280-320 г. и на 30 кроликах новозеландской породы массой 3- 3,5 кг, у которых моделировали гидронефротическую трансформацию, острый и хронический пиелонефрит.
Весь экспериментальный материал был разделен на 4 группы.
В 1 й группе экспериментов (28 интактных крыс) исследования проводили с целью изучения биологического воздействия ударных волн различной мощности на почки с целью выбора оптимальных параметров, не вызывающих повреждения органа. Экспериментальные исследования проведены на ударно-волновом комплексе «Урат-П2», с электрогидравлической системой генерации ударных волн. Сравнивали эффект ударно-волнового воздействия при работе генератора в режиме высоких и низких энергий в двух вариантах – при С = 0,05 и 0,02 мкФ, U = 18 кВ (по 10 крыс в каждой подгруппе). При этих режимах генератора ударных волн амплитуда давления в фокусе составляла 900 и 400 атм. соответственно, при длительности импульса менее 1 мкс. В каждом режиме на почку подавали 1000 ударно-волновых импульсов. Восемь интактных крыс служили контролем для гистоферментохимических исследований.
Через 1, 7, 14 и 30 суток оценивали эффект ударно-волнового воздействия на почку. Эвтаназию животных проводили передозировкой наркотического вещества. Производилась макроскопическая оценка почек, окружающих органов и тканей, а также забор ткани почки для проведения гистологического и гистоферментохимического исследований.
Для гистологического исследования ткань почки фиксировали в нейтральном формалине, готовили парафиновые срезы по стандартной методике и окрашивали их гематоксилином и эозином.
Гистоферментохимическое исследование проводили для определения активности оксидоредуктаз – сукцинадегидрогеназы (СДГ), являющейся одним из ключевых ферментов цикла Кребса, и лактатдегидрогеназы (ЛДГ), характеризующей активность гликолитических процессов, по общепринятым методиками. Ткань удаленной почки замораживали в жидком азоте и хранили до момента исследования. Готовили криосрезы, в которых определяли активность ферментов с помощью набора реактивов для ферментохимического анализа с последующей обработкой тетразолием-синим. Интенсивность выпадения гранул диформазана в клетках характеризовала активность изучаемого фермента [17]. Изменение активности ферментов под влиянием ударно-волнового воздействия выражали в процентах превышения их уровня в интактной почке, не подвергавшейся ударно-волновому воздействию.
Во 2-й, 3-й и 4-й группах в опытах на крысах и кроликах исследовали действие акустических ударных волн низкой энергии на ткань почек при моделировании урологической патологии (гидронефроз, острый и хронический пиелонефрит). Ударно-волновое воздействие проводили на экспериментальном комплексе «Румелит» с электромагнитной системой генерации ударных волн и параметрами стимулирующего их действия, определенными в опытах предыдущей серии. При этом производили расфокусировку ударных волн с амплитудой давления до 100 атм. и длительностью импульса до 4 мкс с целью уменьшения потенциального повреждающего действия. С этой же целью количество импульсов было уменьшено до 500 на каждый сеанс.
Моделирование гидронефротической трансформации
Моделирование гидронефротической трансформации осуществляли у 15 кроликов путем криодеструкции стенки мочеточника. Для этого в условиях тиопенталового наркоза из лапаротомического доступа выделяли участок мочеточника на границе средней и нижней трети (примерно 1 см), брали его на держалки и отгораживали от окружающих тканей салфетками. К выделенному участку прикладывали небольшой тупфер, смоченный жидким азотом, на 1 минуту с последующим спонтанным оттаиванием замороженного участка. В течение 2 недель у животных формировалась стриктура мочеточника с развитием гидронефроза, что подтверждали рентгенологическим исследованием (экскреторная урография) (рис. 1).
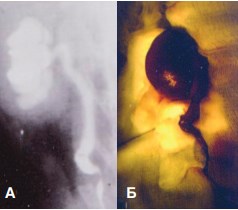
Рис. 1. Экскреторная урограмма кролика (А) и внешний вид почки (Б) через 2 недели после моделирования гидронефротической трансформации
Этих животных разделили на 2 подгруппы:
Контрольную подгруппу составили 3 животных, которым воздействия акустическими ударными волнами не осуществлялось. Опытную подгруппу составили 12 кроликов, которым через 2 недели после моделирования осуществлялось воздействие низкоэнергетическими ударными волнами в количестве 500 импульсов однократно (4 кролика), в 3 сеанса по 500 импульсов (4 кролика) и в 5 сеансов по 500 импульсов (4 кролика) с интервалом 3-4 дня. Через 7 дней после завершения терапии животных выводили из эксперимента путем передозировки наркотического вещества. Почки удаляли и подвергали гистологическому исследованию по стандартной методике.
Моделирование острого пиелонефрита
Моделирование острого пиелонефрита проведено у 15 кроликов, которым под тиопенталовым наркозом пункционно в лоханку вводили 1 мл суспензии Е.соIi в концентрации I09 микробных тел в 1 мл. Контрольную подгруппу составили 3 животных, у которых моделировали пиелонефрит без дальнейшего воздействия ударных волн. Опытную группу составили 12 животных, которым осуществляли ударно-волновое воздействие в различных режимах:
- на 3-и сутки после введения возбудителя однократное воздействие ударными волнами (500 импульсов);
- на 3-и сутки и далее через каждые 4 дня 3-кратное воздействие ударными волнами в количестве 500 импульсов в каждый сеанс:
- на 3-и сутки и далее через каждые 4 дня 5 сеансов ударно-волнового воздействия по 500 импульсов в каждый сеанс.
Через 7 дней после последнего НУВВ производили эвтаназию животных путем передозировки наркотического средства, удаляли почки и проводили их гистологическое исследование по стандартной методике.
Моделирование хронического пиелонефрита
Моделирование хронического пиелонефрита проводили у 15 самок крыс по методике, разработанной в НИИ урологии и интервенционной радиологии им. Н.А.Лопаткина. В условиях тиопенталового наркоза выполняли срединную лапаротомию и осуществляли скелетизацию мочеточников с целью ухудшения условий транспорта мочи. Через неделю катетеризировали мочевой пузырь по уретре и внутрипузырно вводили суспензию культуры E.coli 109 микробных тел в мл в объеме, превышающем емкость мочевого пузыря (примерно 1 мл). При этом за счет пузырно-лоханочного рефлюкса происходил заброс инфекционного агента в лоханки почек, что инициировало воспалительный процесс. Процедуру повторяли троекратно с интервалом 7 дней. Сочетание повторного инфицирования почки и нарушения уродинамики приводило к хронизации воспалительного процесса. Пять крыс составили контрольную группу (у них воздействий не проводили), а 10 животных – экспериментальную группу. Им после завершения процесса моделирования хронического пиелонефрита проводили 5 сеансов ударно-волновой терапии с интервалом 3-4 дня по 500 импульсов в каждый сеанс.
Через 1 неделю после завершения терапии животных выводили из опыта путем передозировки наркоза, удаляли почки и проводили их гистологическое исследование.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Морфо-функциональное состояние интактных почек после воздействия акустических ударных волн разной мощности
При использовании ударноволнового воздействия с параметрами для дробления конкрементов (С=0,05 мкФ) в ближайшие сутки отмечали выраженные альтеративные изменения вплоть до очагов некробиоза и некроза в области терапевтического фокуса размером до 0,3 мм (рис. 2А). В отдельных экспериментах этой группы выявляли развитие субкапсулярного кровоизлияния на фоне выраженных дистрофических изменений в эпителии почечных канальцев. Альтеративные изменения в виде гидропической дистрофии эпителия канальцев с явлениями фокального некроза эпителиоцитов сохранялась весь срок наблюдения (до 30 суток) (рис. 2 Б).
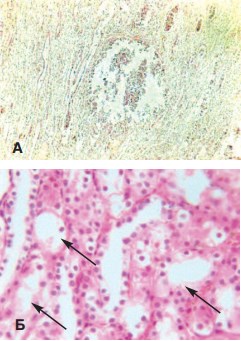
Рис. 2. Участок деструкции ткани почки, развившейся через сутки после воздействия сфокусированными ударно-волновыми импульсами в режиме дробления мочевых камней (С=0,05 мкФ) (А, окраска гематоксилином и эозином, Ув. 100х) и сохраняющаяся через 30 суток гидропическая дистрофия эпителия почечных канальцев с явлениями фокального некроза эпителиоцитов (указано стрелками) (Б, окраска гематоксилином и эозином, Ув. 400х)
В то же время при использовании ударно-волнового воздействия с меньшей энергией (С=0,02 мкФ), не выявляли признаков повреждения почки. При этом уже через сутки отмечали интенсификацию микроциркуляции, проявляющееся в полнокровии как капилляров клубочков, так и перитубулярных капилляров коркового и мозгового вещества (рис. 3). Полнокровие сосудов сохранялось до 14 суток наблюдения.
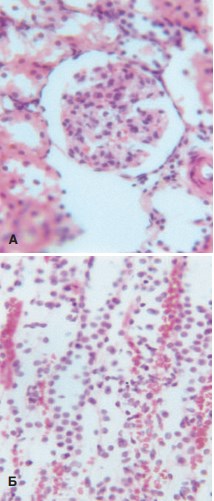
Рис. 3. Полнокровие клубочковых капилляров (А) и перитубулярных капилляров (Б) через сутки после низкоинтенсивного ударно-волнового воздействия (С=0,02 мкФ). Окраска гематоксилином и эозином. Ув. 200х
При гистохимическом исследовании ткани почек этой серии крыс отмечались изменения, свидетельствующие об активации аэробных метаболических процессов на фоне гиперемии внутриорганного сосудистого русла, что проявлялось в изменении соотношения активностей маркерных ферментов цикла Кребса и гликолиза. Гистоферментохимическое исследование выявило увеличение активности СДГ, являющегося одним из ключевых ферментов цикла Кребса, в эпителии почечных канальцев с одновременным снижением активности ЛДГ, являющейся маркером активности гликолитических процессов, активирующихся при неблагоприятных для организма условиях. При этом выявляли прогрессивную интенсификацию аэробного метаболизма до 14 суток наблюдения, тогда как к 30-м суткам отмечали тенденцию к восстановлению исходного соотношения аэробного и анаэробного метаболизма (рис. 4).
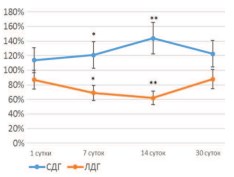
Рис. 4. Динамика активности СДГ и ЛДГ в ткани почек после НУВВ (% к активности в интактных почках)
Эти изменения свидетельствуют, что после НУВВ происходит стимуляция активности энергетически более обоснованного пути синтеза АТФ – цикла Кребса с одновременным некоторым снижением активности значительно менее эффективного гликолиза, являющегося резервным путем синтеза АТФ. С нашей точки зрения, активация аэробных процессов после НУВВ является отражением повышения резервных функциональных и регенераторных возможностей органа и может повышать его устойчивость к повреждающим факторам.
Это предположение мы изучили в последующих экспериментах с влиянием НУВВ на поврежденную почку в условиях моделирования различной урологической патологии.
Результаты воздействия акустических ударных на ткань почек при моделировании гидронефротической трансформации
Воздействие низкоэнергетическими ударными волнами приводило к двум группам изменений. Интенсивность их проявлений имела прямо пропорциональную зависимость с количеством сеансов воздействия низкоэнергетическими ударными волнами. Во-первых, отмечалась выраженная регенерационная активность лейомиоцитов мышечной оболочки мочеточника, способствуя ее гипертрофии, за счет которой возрастала способность транспортировать мочу через область стриктуры (рис. 5).
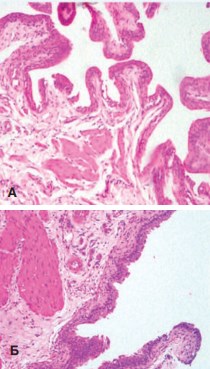
Рис. 5. Умеренно выраженная гипертрофия мышечной оболочки мочеточника в контрольной серии опытов (А) и выраженная ее гипертрофия при воздействии НУВВ (Б). Окраска гематоксилином и эозином. Ув. 200х
Вследствие этого в опытной группе в меньшей степени были выражены явления нефрогидроза и дистрофические изменения эпителиальных клеток. Выраженность различий возрастала с увеличением сеансов ударно-волнового воздействия. Нефрогидроз в контрольной группе к моменту окончания эксперимента был выражен до II, а в отдельных участках до III степени (рис. 6 А), в то время как после проведения 5 сеансов воздействия, нефрогидроз затрагивал в незначительной степени лишь выводные протоки собирательных трубочек, тогда как расширение извитых канальцев было незначительно ( рис. 6 Б).
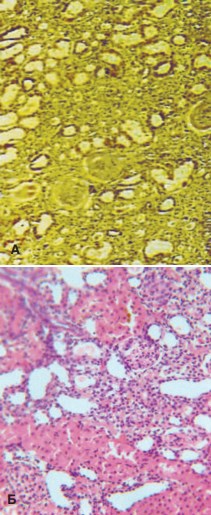
Рис. 6. Выраженный нефрогидроз канальцев коркового вещества, гиалиноз клубочков и диффузная инфильтрация интерстиция почек контрольной серии (А). Умеренно выраженный нефрогидроз и незначительная очаговая лимфогистиоцитарная инфильтрация интерстиция почек после завершения ударно-волновой терапии в 5 сеансов. (Б). Окраска гематоксилином и эозином. Ув. 100х (А) и 200х (Б)
В опытной серии отмечали признаки регенерации поврежденного канальцевого эпителия. В эпителии проксимальных и дистальных канальцев выявляли наличие двуядерных эпителиоцитов, что свидетельствовало об активной регенерации канальцевого эпителия. Если в контрольной группе были выраженные явления отека интерстиция, то в экспериментальной группе у животных с однократным применением НУВВ отечные явления наблюдали преимущественно в мозговом слое и частично в области петли Генле, а после 3-5 сеансов ударно-волнового воздействия отек практически отсутствовал. Инфильтрация интерстиция клетками воспаления также была менее выражена в меньшей степени в опытной серии.
Эти данные свидетельствуют, что воздействие ударно-волновыми импульсами с низкой энергией приводит, во-первых, к стимуляции регенеративной гипертрофии гладкомышечных клеток, во-вторых, к развитию компенсаторно-приспособительных процессов в ткани почек и, в-третьих, улучшает дренажную функцию интерстиция, что должно положительно сказываться на функции почек даже в условиях затруднения пассажа мочи.
Результаты воздействия акустических ударных волн низкой интенсивности на ткань почек при моделировании острого пиелонефрита
При сравнении степени выраженности воспалительной реакции в экспериментальных и контрольных группах обращает на себя внимание тот факт, что в первые 3 суток в контрольных опытах при гистологическом исследовании выявляли массивную инфильтрацию клетками воспаления подслизистого слоя почечной лоханки и интерстиция почечной паренхимы. Целостность эпителиальной выстилки была нарушена. В просвете лоханки обнаруживали скопления десквамированного эпителия, полиморфноядерных лейкоцитов и клеточный детрит. Такая картина сохранялась до конца периода наблюдения, хотя и в меньшей выраженности (рис. 7 А). В тоже время в группе животных с применением НУВВ, хотя и выявлялись воспалительные лейкоцитарные инфильтраты в лоханке и почечной паренхиме, но их выраженность была существенно меньше. У животных, которым проводили 5-кратное ударно-волновое воздействие, к концу срока наблюдения эпителиальная выстилка была полностью сохранена, воспалительные инфильтраты локализовались лишь в подслизистом слое лоханки, тогда как паренхима почки была полностью сохранена. В просвете лоханки не выявляли элементов клеточной деструкции (рис. 7 Б).
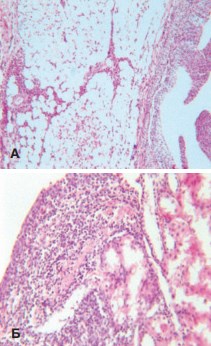
Рис. 7. Массивные полиморфноядерные инфильтраты подслизистого слоя лоханки. Скопление десквамированного эпителия, клеточного детрита и полимфорфноядерных лейкоцитов в просвете лоханки (А). Окраска гематоксилином и эозином. Ув. 100х. Выраженная инфильтрация подслизистого слоя почечной лоханки. Относительно сохранные прилежащие почечные канальцы. Окраска гематоксилином и эозином, Ув. 200х
Таким образом, НУВВ на почку при моделировании острого пиелонефрита приводит к выраженной редукции воспалительного процесса.
Хотя в почечной лоханке сохраняются признаки активного воспаления, но в прилежащей почечной паренхиме они присутствуют в минимальной степени.
Результаты воздействия акустических ударных волн на ткань почек при моделировании хронического пиелонефрита
В эксперименте c моделированием хронического пиелонефрита установлено, что в ткани почек крыс, которым применяли НУВВ, отмечается уменьшение выраженности воспалительных инфильтратов по сравнению с животными контрольной группы. При этом в клеточном составе инфильтратов в опытной группе преобладали макрофаги и гистиоциты, а также активированные фибробласты, количество которых в контрольной группе было значительно ниже, что свидетельствовало о большей активности репаративных процессов при НУВВ. В опытной серии в меньшей степени были выражены дегенеративные изменения в почечных клубочках извитых канальцах. В то же время степень склерозирования интерстициальной ткани почек в контрольной и экспериментальной группах, была практически равнозначна (рис. 8 А,Б).
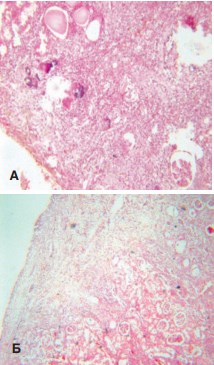
Рис. 8. Почка крысы с хроническим пиелонефритом без терапии (А) и при терапии НУВВ (Б). Уменьшение выраженности клеточной инфильтрации и лучшая сохранность клубочков и канальцев в опытах с ударно-волновым воздействием при выраженном склерозе интерстиция в обеих сериях. Окраска гематоксилином и эозином. Ув. 100х
Таким образом, НУВВ при хроническом пиелонефрите способствует уменьшению выраженности воспалительной реакции, что положительно сказывается на сохранности элементов нефрона, и это косвенно может указывать на лучшую сохранность фильтрационной функции почек. В то же время НУВВ не оказывают существенного действия на степень склерозирования интерстиция почки, который играет важную роль в формировании окончательной мочи [11].
ЗАКЛЮЧЕНИЕ
Полученные нами результаты свидетельствуют, что воздействие НУВВ на почки при моделировании различных урологических заболеваний (гидронефроз, острый и хронический пиелонефрит) в определенных нами технических параметрах (расфокусированные ударные волны с амплитудой давления менее 100 атм., при длительности импульса до 4 мкс., подаче 500 импульсов) оказывает терапевтическое действие за счет интенсификации микроциркуляции в органе, и стимуляции аэробных окислительных процессов, энергетически обеспечивающих реализацию компенсаторно-приспособительных процессов. Это, в свою очередь, способствует уменьшению выраженности воспалительного повреждения ткани и сохранению структур нефрона, что позволяет предполагать лучшую функциональную сохранность почки при изученных патологических состояниях.
Терапевтическое действие НУВВ продемонстрировано в клинике, главным образом, при хроническим бактериальном и абактериальном простатите и синдроме тазовой боли [3-6,10,14]. Проведенное нами исследование свидетельствует о возможности значительного расширения области применения этого метода при других заболеваниях и патологических состояниях, поскольку его действие основано на неспецифическом стимулировании собственных защитно-приспособительных реакциях организма [1,2].
ЛИТЕРАТУРА
- Гарилевич Б. А., Кудрявцев Ю. В., Дзеранов Н. К. Этапы научных разработок в области применения ударных волн. Материалы Пленума правления Российского общества урологов. М. 2003:106-108.
- Гарилевич Б. А., Захаров В. Н., Кудрявцев Ю. В., Кирпатовский В. И. Способ стимуляции метаболических процессов в тканях. Патент № 2076641; заявлено 16.12.1992 г.; опубл. 10.04.1997. Бюл. № 10. – 6 с.
- Гарилевич Б. А., Ротов А. Е., Олефир Ю. В. Первый опыт применения ударно-волновой терапии при лечении больных хроническим простатитом. Вопросыкурортологии,физиотерапии и лечебной физической культуры 2007;(3):43 – 45.
- Кульчавеня Е. В., Шевченко С. Ю., Брижатюк Е. В. Экстракорпоральная ударно-волновая терапия при хроническом простатите. Урология 2016;(2):77-81.
- Кумачев К. В. Применение ударно-волновой терапии в реабилитации мужчин с синдромом хронической тазовой боли при хроническом простатите. Автореф. дис. … к.м.н. М., 2014: 24 с.
- Ротов А. Е. Применение ударно-волновой терапии в комплексном лечении и реабилитации больных хроническим простатитом. Автореф. дис. … к.м.н. М., 2008: 22 с.
- Гарилевич Б. А. Способ лечения хронического простатита. Патент № 2400269; заявлено 13.01.2009; опубл. 27.09.2010. Бюл. № 27. – 3 с.
- Palmieri A, Imbimbo C, Longo N, Fusco F, Vrze P, Mandriapia F et al. A first prospective, randomized, double-blind, placebo-controlled clinical trial evaluating extracorporeal shock wave therapy for the treatment of Peyronie,s disease. Eur Urol 2009;56(2):363-369. doi: 10.1016/j.eururo.2009.05.012.
- Shimpi R K, Jain RJ. Role extracorporeal shock wave therapy in management of Peyronie’s. Urol Ann 2016;8(4):409-417. doi: 10.4103/0974/192/100.
- Руденко И. И., Рапопорт Л. М., Газимиев М. А.,Демидко Ю.Л., Байдувалиев А. М. Первый опыт применения ударно-волновой терапии умужчин с синдромом хронической тазовой боли. Урология 2015; (6): 26-29.
- Ходырева Л. А., Дударева А. А., Мудрая И. С., Маркосян Т. Г. Ревенко С.В., Кумачев К.В., и др. Оценка эффективности ударно-волновой терапии пациентов с тазовой болью методом гармонического анализа пенильного биоимпендаса. Бюллетень экспериментальной биологии и медицины 2013;(2): 259-262.
- Гарилевич Б.А., Кирпатовский В.И., Кудрявцев Ю.В., Синюхин В.Н. Экспериментальное изучение влияния ударно-волновой терапии на проникновение антибиотиков в ткань предстательной железы. Экспериментальная и клиническая урология 2015;(2): 26-29.
- Ходырева Л.А.,Дударева А. А.,Кумачев К. В.,Логвинов Л. А.,Дегтярев С.С., Попов С.В. Новые физические факторыв лечении хронического абактериального простатита/ синдрома хронической тазовой боли. Справочник врача общей практики 2012; (3):23-28.
- Семевский А.Е., Чистов В.В., Серов Д.Д., Баранов М.С. Новейший опыт применения терапии ударными волнами в различных областях медицины. Доктор Ру 2009; (7):32-40.
- Улащик В. С. Ударно-волновая терапия: новые направления использования. Здравоохранение (Минск) 2010;(6): 28-32.
- Gerdesmeyer L, von Eiff C, Horn C, Henne M, Roessner M, Diehl P, et al. Antibakterial effects of extracorporeal shock wave. Ultrasound Med Biol 2005;18(1):115-119.
- Лилли Р. Патогистологическая техника и практическая гистохимия. Мир, М.1969. 646 с.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 1.96 Мб |















































































