Факторы риска формирования обструктивных осложнений эндоскопического лечения пузырно-мочеточникового рефлюкса с использованием кополимера полиалкоголя полиакрилата DOI: 10.29188/2222-8543-2019-11-1-128-131
 3906
3906 Эндоскопическая коррекция (ЭК) пузырно-мочеточникового рефлюкса (ПМР) предложена в начале 80-х годов E. Matouschek [1]. Ее эффективность в лечении ПМР ниже по сравнению с реимплантацией мочеточника. Но ЭК получила широкое распространение благодаря высокой безопасности и низкой травматичности.
Тридцатилетний опыт использования различных имплантатов сформировал убеждение, что развитие обструкции уретеровезикального сегмента (ОУВС) после ЭК – редкое осложнение с частотой менее 1% [2, 3]. Уверенность в безопасности ЭК позволила разработать и внедрить в практику технологии инъекции импланта (HIT и Double HIT), которые повышают эффективность метода [4,5].
Результаты ЭК ПМР демонстрировали недостаточную эффективность методики даже после двух процедур, составляя 59,2-85% [6-8]. Это послужило причиной поиска новых объеомбразующих препаратов, которые могли обеспечить большую эффективность, стабильность введенного объема с сохранением существующего уровня безопасности.
Первые сообщения об использовании кополимера полиалкоголя полиакрилата (КПП) появились в 2010 году. Авторы публикации сообщали о высокой эффективности (83,6-92,7%) нового объемобразующего препарата [9,10].
Однако достаточно скоро появились сообщения, демонстрирующие повышение риска развития ОУВС при использовании КПП [11,12]. За истекшее десятилетие накоплен обширный клинический материал, касающийся частоты ОУВС и факторов риска их формирования. Нами проанализирован собственный опыт использования КПП в пяти клиниках с целью формирования алгоритмов, снижающих вероятность ОУВС и уточняющих программу послеоперационного ведения пациентов с учетом особенностей, характерных для КПП.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование основано на ретроспективном анализе опыта лечения 774 пациентов (1133 почечных единиц (ПЕ)) в период 2012-2017гг., которым в качестве импланта для ЭК ПМР был введен КПП. Среди пациентов было 449 (58,0%) девочек и 325(42,0%)мальчиков. Правосторонний ПМР выявлен у 180 (23,3%) пациентов, левосторонний – у 235 (30,4%) детей, билатеральный процесс – у 359 (46,4%) пациентов. Медиана возраста (мес) [Q1; Q3] пациентов составила 39 [17; 78] мес.
Первая степень рефлюкса диагностирована в 32(2,8%) ПЕ, II степень – в 281 ПЕ (24,8%), III степень – в 568 (50,2%) ПЕ, IV степень – в 214 (18,9%) ПЕ, V степень – в 38 (2,3%) ПЕ. Медиана степени рефлюкса [Q1; Q3] равнялась 3 [2,3]. Технология STING (subureteral polytetrafluoro-ethylene injection) использована у 685 (88,5%) пациентов (1010 (89,1%) ПЕ), техника HIT (hydrodistention implantation technique) – у 89 (11,5%) детей (123 (10,9%) ПЕ).
Всем пациентам ультразвуковое исследование почек (УЗИ) выполнялось через сутки после проведения эндоскопического лечения. Проводился мониторинг активности инфекционного воспалительного процесса в мочевых путях с помощью клинического и бактериологического исследований мочи. При отсутствии признаков обструкции к концу первых суток после операции повторное УЗИ выполняли через три месяца после операции. Контрольную микционную цистографию проводили через 4-6 месяцев после эндоскопического лечения. При наличии признаков обструкции по данным ультразвукового исследования пациентам выполняли изотопную диуретическую ренографию.
В дальнейшем все пациенты находились под наблюдением уролога в течение 5 лет, которое включало в себя ультразвуковой мониторинг не менее двух раз в год даже после документированного устранения рефлюкса и ремиссии инфекции мочевых путей.
К ОУВС относили случаи, когда у пациентов выявляли по данным реносонографии стойкое расширение мочеточника, лоханки и чашечек, превышающее значения, зарегистрированные до эндоскопического лечения, и признаки обструкции по результатам диуретической ренографии.
Показанием к хирургическому лечению ОУВС считали наличие стойких клинических проявлений обструкции и неэффективность консервативной терапии, снижение в динамике почечной функции на стороне обструкции, выявляемые на любом сроке после эндоскопического лечения.
С целью устранения ОУВС выполняли реимплантацию мочеточника и рассечение слизистой мочевого пузыря над имплантом с последующей его эвакуацией.
На основании анализа результатов ЭК детей с ПМР нами сформированы две группы пациентов. I группа – больные без ОУВС и группа II - дети с ОУВС после ЭК. В I группу включены 733 ребенка, 435 (59,3%) девочек и 298 (40,7%) мальчиков. Медиана возраста - 41 месяцев [18,0;81,0]. Техника STING использована у 668 (91,1%) детей (993 (91,0%) ПЕ), HIT у 65 (8,9%) пациентов (98 (9%) ПЕ).
Группа II включила 41 (5%) пациента, медиана возраста - 21,5 месяцев [12,0;43,0], мальчиков – 27 (65,9%), и 14 (34,1%) девочек. После первого введения ОУВС развились у 34 (82,9%) пациентов, после второго у 7 (17,1%). Технология STING применена у 18 (41,5%) больных, HIT у 23 (58,5%) детей.
Статистическая обработка данных проведена с использованием непараметрического критерия Манна-Уитни и критерия Хи-квадрат с поправкой Йейтса.
РЕЗУЛЬТАТЫ
При сравнении возраста пациентов I и IIгрупп выявлено, что пациенты в группе с ОУВС младше детей в группе без обструкции (p=0,002) (рис. 1).
Среди пациентов I группы медиана степени ПМР [Q1; Q3] - 3 [2;3]. В группе детей с ОУВС медиана степени ПМР [Q1; Q3] - 3,5 [3;4]. Мы изучили в сравнении частоту выявления различных степеней ПМР у пациентов обеих групп и выявили, что у больных с ОУВС чаще диагностировали более высокие степени рефлюкса (p<0.001) (рис. 2).
Гендерное распределение пациентов в группах представлено в таблице 1.
Анализ гендерного состава пациентов I и II групп демонстрирует, что вероятность формирования ОУВС у мальчиков существенно выше, чем у девочек (p=0,003).
При сравнении вероятности обструкции в результате применения различных технологий введения импланта выявлено повышение риска ОУВС при использовании технологии HIT (р<0,001) по сравнению с техникой STING (табл. 2).
Вторая инъекция КПП выполнена 82 (10,6%) пациентам в связи с рецидивом рефлюкса. ОУВС после первой инъекции выявлены у 34 (4,4%) пациентов. Среди детей, которым выполнялась вторая ЭК обструкция диагностирована в 7 (8,5%) случаях.
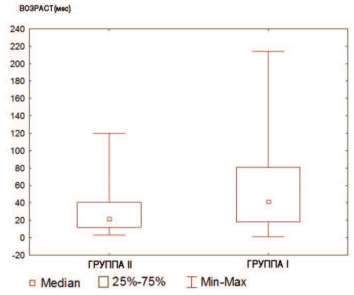
Рис.1. Возраст пациентов I и в II групп
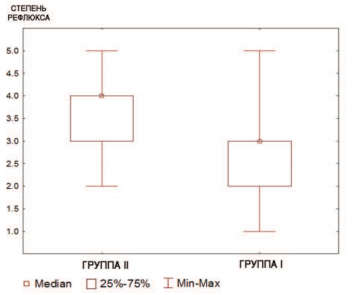
Рис. 2. Степень рефлюкса у пациентов I и II групп
Таблица 1. Гендерное распределение пациентов
| ВСЕ БОЛЬНЫЕ | I ГРУППА | II ГРУППА | ||||
|---|---|---|---|---|---|---|
| абс | % | абс | % | абс | % | |
| Мальчики | 685 | 42,0 | 298 | 40,7 | 27 | 65,9 |
| Девочки | 449 | 58,0 | 435 | 59,3 | 14 | 34,1 |
| p=0,003 | ||||||
Таблица 2. Частота использования техники HIT и STING среди больных обеих групп
| ВСЕ БОЛЬНЫЕ | I ГРУППА | II ГРУППА | ||||
|---|---|---|---|---|---|---|
| абс | % | абс | % | абс | % | |
| STING | 325 | 88,5 | 668 | 91,1 | 18 | 41,5 |
| HIT | 89 | 11,5 | 65 | 8,9 | 23 | 58,5 |
| p=0,003 | ||||||
Однако, несмотря на то, что частота выявлена ОУВС в группе больных после второй ЭК почти в два раза выше, достоверного влияния на вероятность обструкции кратность инъекции не оказывает (р>0,05). ОУВС сформировались в интервале от 1 до 41 мес. после последнего введения импланта. Больше половины случаев (29(70,7%)) обструкции были выявлены в течение первого года после ЭК (рис. 3). При этом все пациенты с ОУВС систематически наблюдались с частотой реносонографии не менее 1 раза в 6 месяцев, что дает возможность нам утверждать, что обструкция может сформироваться даже через 35-41 мес. после эндоскопического лечения.
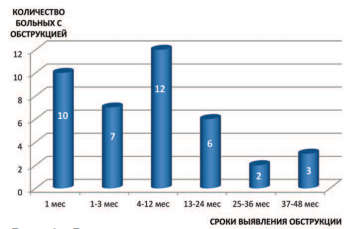
Рис. 3. Распределение пациентов по срокам выявления обструкции
Среди пациентов II группы инфекция мочевых путей выявлена у 12 (28%) больных. Симптоматическая инфекция выявлена в течение первых 6 месяцев у 5 (42%) детей, бессимптомная у 7 (58%) человек через 3-36 месяцев после эндоскопического лечения.
ОБСУЖДЕНИЕ
Достаточно высокая частота развития ОУВС при использовании КПП является существенным противовесом его высокой эффективности и ограничивает его применение.
Понимание, что прямая проекция накопленного ранее опыта ЭК с использованием других имплантов является неправильной стратегией пришло достаточно быстро и в первую очередь коснулось объема вводимого импланта. Если в одной из первых работ [13], посвященных результатам использования КПП, B.Chertin и коллеги сообщают о среднем объеме введенного импланта 0,8 мл, через два года другой авторский коллектив под руководством J.P. Corbetta [14] сообщает о среднем использованном объеме 0,6 мл, то в опубликованном в том же году мультицентровом исследовании [15] S. Kocherov и соавт. сообщают об уменьшении среднего объема болюса до 0,4 мл. Таким образом, уменьшение объема КПП позволяет сохранить высокую вероятность устранения рефлюкса и снижает вероятность формирования ОУВС.
Одним из важнейших условий полноценного понимания особенностей ОУВС при использовании КПП является длительность наблюдения в послеоперационном периоде. Чем длительнее период наблюдения, тем выше частота выявленных ОУВС. Так по данным S. Warchoł и соавт. опубликовавших результаты 5 летнего наблюдения за больными после эндоскопического лечения, ОУВС выявлены у 8% пациентов в интервале 1,1-2,9 лет, при этом авторы сообщают, что ультразвуковое сканирование каждые 6 мес. после операции является обязательным компонентом в алгоритме наблюдения за детьми [16]. С другой стороны, по данным мультицентрового исследования, при наблюдении в течение 3 лет после операции частота ОУВС составила 1,2% [15].
Учитывая полученные нами данные, демонстрирующие возможность выявления ОУВС через 4 года после операции, стратегия наблюдения должна включать непрерывный ультразвуковой мониторинг всех детей после ЭК с использованием КПП.
Гипотеза о том, что высокая степень ПМР, как фактор риска ОУВС при ЭК ПМР представлена в публикации D. Ben-Meir и соавт. [17]. Авторы изучили особенности ОУВС у 9 больных, при ЭК у которых использовали КПП и кополимер гиалуроновой кислоты. Полученные нами данные на основании исследования 41 пациента с обструкцией, позволившие нам сделать аналогичные выводы, являются весомым аргументом подтверждающим гипотезу израильских коллег.
Известно, что для пациентов мужского пола характерно выявление более высокой степени рефлюкса, по сравнению с девочками. Возможно, что выявленные нами гендерные различия, демонстрирующие более высокую частоту выявления обструкции у мальчиков, ассоциированы с повышенным риском обструкции у пациентов с рефлюксом высокой степени.
Только в одной из известных нам публикаций отражена связь техники введения импланта на частоту обструкции [18]. S.C. Karakus и соавт. обструктивные осложнения выявлены у 7 (14%) пациентов, 6 из которых имплант вводили с использованием технологии Double HIT. Результаты нашего исследования демонстрируют, что осторожно должна использоваться даже техника HIT при введении КПП.
В этой же публикации делается вывод о повышенном риске развития ОУВС у детей раннего возраста [18]. Авторы находят объяснение своей находки в малых размерах мочеточника и функциональной незрелостью нижних мочевых путей.
ВЫВОДЫ
Ранний возраст, мужской пол, высокая степень рефлюкса, использование технологии HIT являются дополнительными к известным (большой объем импланта) факторами риска формирования ОУВС после ЭК рефлюкса с использованием качестве импланта КПП. Повышенного внимания требуют пациенты после второго введения КПП, частота выявления обструкции у этих пациентов в два раза выше, чем в группе больных, которым выполнялась первая инъекция. Пациенты после ЭК с использованием КПП должны мониторироваться не менее 4-5 лет с целью выявления отсроченного развития ОУВС.
ЛИТЕРАТУРА
- Matouschek E. Treatment of vesicorenal reflux by transurethral teflon-injection. Urologe A. 1981 Sep; 20(5): 263-4.
- Puri P, GranataC. Multicentersurvey of endoscopic treatment of vesicoureteralreflux using polytetrafluoroethylene. J Urol 1998;160:1007-11. https://doi.org/10.1016/S0022-5347(01)62683-1
- Vandersteen DR, Routh JC, Kirsch AJ, Scherz HC, Ritchey ML, Shapiro E, et al. Postoperative ureteral obstruction aersubureteral injection of dextranomer/hyaluronicAcid copolymer. J Urol 2006; 176(4 Pt 1): 1593-5. https://doi.org/10.1016/j.juro.2006.06.101
- Kirsch AJ, Perez-Brayfield M, Smith EA, Scherz HC. e modified STING procedure to correct vesicoureteralreflux: improved resultswith submucosal implantationwithin the intramural ureter. J Urol 2004; 171(6 Pt 1): 2413-6. https://doi.org/10.1097/01.ju.0000127754.79866.7f
- Cerwinka WH, Scherz HC, Kirsch AJ. Dynamic hydrodistention classification of the ureter and the double HIT method to correct vesicoureteral reflux. Arch Esp Urol 2008; 61(8): 882-7. https://doi.org/10.4321/s0004-06142008000800005
- ElderJS, Diaz M, Caldamone AA, Cendron M, Greenfield S, Hurwitz R, et al. Endoscopic therapy for vesicoureteral reflux: a meta-analysis. I. Reflux resolution and urinary tract infection. J Urol 2006; 175: 716–22. https://doi.org/10.1016/S0022-5347(05)00210-7
- Holmdahl G, Brandström P, Läckgren G, Sillén U, Stokland E, Jodal U, et al. the Swedish reflux trial in children: II. Vesicoureteral reflux outcome. J Urol 2010;184(1): 280-5. https://doi.org/10.1016/j.juro.2010.01.059
- Routh JC, Inman BA, Reinberg Y. Dextranomer/hyaluronic acid for pediatric vesicoureteral reflux: systematic review. Pediatrics 2010; 125(5):1010-9. https://doi.org/10.1542/peds.2009-2225
- Ormaechea M, Ruiz E, Denes E, Gimenez F, Dénes FT, MoldesJ, et al. New tissue bulking agent(polyacrylate polyalcohol)fortreating vesicoureteralreflux: preliminary resultsin children. J Urol 2010;183(2):714-7. https://doi.org/10.1016/j.juro.2009.10.047
- Chertin B, Arafeh WA, Zeldin A, Ostrovsky IA, Kocherov S. Endoscopic correction of VUR using vantris as a new non-biodegradable tissue augmenting substance: three years of prospective follow-up. Urology 2013;82(1): 201-4. https://doi.org/10.1016/ j.urology.2013.01.024
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 343.1 кб |















































































