Фокальная криоаблация предстательной железы
 8931
8931 Отношение к лечению рака предстательной железы (РПЖ) значительно изменилось с конца 1980-х гг., когда анализ на ПСА был введен в качестве скрининга этого заболевания, что впоследствии повлекло за собой увеличение процента выявления ранних форм рака предстательной железы. Это позволило предлагать пациентам различные методы лечения РПЖ: радикальную простатэктомию (РПЭ), дистанционную лучевую терапию (ДЛТ), брахитерапию, аблятивные технологии (криотерапию, высокоинтенсивный сфокусированный ультразвук, фотодинамическую терапию и лазерную интерстициальную термотерапию). Увеличение процента выявления небольших опухолей на ранних стадиях чаще с унифокальным или унилатеральным поражением, а также развитие методов визуализации в совокупности с прогрессом в изучении энергии воздействия позволяет применять потенциально новый метод лечения фокальную криоаблацию предстательной железы (ПЖ). Фокальная криоаблация является модификацией стандартного метода криотерапии, основной задачей которой является удаление всех фокусов рака (или фокусов с наибольшей вероятностью прогрессии или метастазирования) с минимальным риском повреждения структур, обеспечивающих нормальное мочеиспускание, сексуальную функцию и, как следствие, улучшение качества жизни пациен-тов [1]. На сегодняшний день из фокальных методов лечения РПЖ наиболее изучена фокальная криоаблация.
Предпосылкой к выполнению фокальной терапии является выявление основного очага РПЖ («index lesion») опухоли наибольшего объёма, имеющей, как правило, наибольшую сумму баллов по Глисону и коррелирующей с риском рецидива РПЖ [2, 3]. По данным большинства авторов, именно «ведущая опухоль» определяет развитие онкологического процесса и является источником метастазирования [4]. Эффективная аблация данного участка может привести к полному уничтожению опухолевого очага, предотвращению местного распространения и метастазирования (рис. 1). «Неосновные» очаги опухоли чаще имеют высокую дифференцировку, менее агрессивны, склонны к медленному развитию и, как следствие, минимально влияют на риск рецидива РПЖ [5].
Системный ответ организма в ответ на разрушение опухолевых клеток может привести к снижению секреции иммуносупрессивных факторов, индуцированию противоопухолевой иммунной реакции и активации незрелых дендритных клеток, способных уничтожать оставшиеся опухолевые клетки [6, 7].
Оптимальные критерии отбора пациентов для фокальной криоаблации четко не определены. В 2006 году появились первые критерии Consensus Conference on Focal Treatment [8], включающие ожидаемую продолжительность жизни менее 5 лет, клиническую стадию РПЖ T1, уровень ПСА < 15 нг/мл, а также отсутствие метастатического поражения. Согласно «Guidelines» Европейской ассоциации урологов 2013 г., оптимальным кандидатом для фокальной криоаблации является пациент с локализованным РПЖ низкого и среднего риска с изолированным унифокальным или унилатеральным поражением. Предпочтение отдается пациентам с ПСА < 10 нг/мл, суммой баллов по Глисону < 7, клинической стадией РПЖ < Т2b, положительными фрагментами при биопсии < 4 и процентным распространением опухоли < 50% в одном кусочке [9]. К потенциальным кандидатам могут быть отнесены пациенты с РПЖ низкого риска, которым показано активное наблюдение [10]. В таком случае при рецидиве заболевания сохраняется возможность повторного проведения фокальной терапии или радикального лечения. Пациенты с клинической стадией РПЖ T3 (экстракапсулярная инвазия, инвазия в семенные пузырьки) по мнению Bahn DK. и Silverman PD. [11] могут быть условными кандидатами для фокальной криоаблации при условии установления одностороннего процесса и понимания пациентами рисков операции.могут быть условными кандидатами для фокальной криоаблации при условии установления одностороннего процесса и понимания пациентами рисков операции.
Наряду с дифференциацией рисков (по данным шкалы D΄Amico, номограммы Kattan, таблицы Partin, критериям National Comprehensive Cancer Network и пр.), необходимо учитывать уровень ПСА и степень злокачественности опухоли по Глисону [12, 13, 14]. Перед операцией должны быть визуализированы все фокусы рака и степень распространения опухоли, а также оценена степень злокачественности.
Трансректальная биопсия простаты из ≥ 12 точек позволяет оценить объем, локализацию и степень злокачественности опухоли [15]. Тем не менее, последние исследования показывают нередкое расхождение между данными биопсии и патогистологическим заключением после операции. Трансперинеальная шаблонная биопсия была предложена как метод белее точного картирования опухоли и в настоящее время является обязательной в отборе пациентов для процедуры фокальной криотерапии [16].
Ультразвук в течение долгого времени остается одним из основных методов визуализации ПЖ. Последние технологические достижения позволили усовершенствовать методику «обыденного» УЗИ. Комбинация УЗИ с контрастным усилением, 3D, цветным и Допплеровским картированием, эластографией и спектроскопией позволяет значительно повысить чувствительность и специфичность данного метода [17, 18]. Ультразвуковая допплерография позволяет определить вовлеченность в процесс сосудисто-нервного пучка [19]. Применение магнитно-резонансной (МР) спектроскопии, диффузно-взвешенных изображений, а также динамического контрастирования, значительно повышает качество визуализации простаты [20]. МР томография с динамическим контрастированием позволяет оценить анатомическое расположение ПЖ, экстракапсулярное прорастание, а также вовлеченность в опухолевый процесс прилежащих структур (семенных пузырьков, мочевого пузыря, парапростатической ткани, лимфатических узлов и т.д.) [21]. По данным различных авторов, чувствительность и специфичность данного метода колеблется в пределах 81%-90% и 84%-91% соответственно [22, 23]. Совместное применение МРТ с молекулярными методиками, такими как позитронноэмиссионная томография (ПЭТ) с холином, улучшает выявление локализации опухоли и стадирование лимфоузлов [24]. Также по показаниям могут быть проведены остеосцинтиграфия и тазовая лимфаденэктомия для более точного стадирования опухолевого процесса.
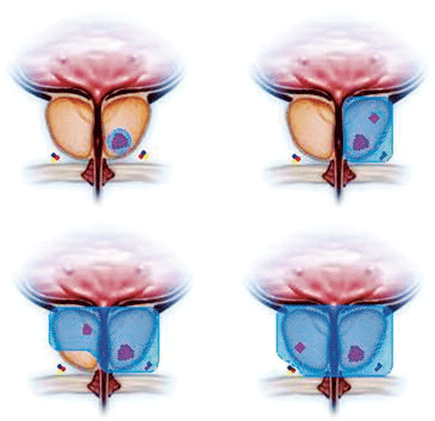
Рис. 1. Схематическое изображение вариантов фокальной криоаблации: А) фокальная криоаблация; Б) гемиаблация; В) аблация ¾ предстательной железы с сохранением одного сосудисто-нервного пучка; Г) криоаблация предстательной железы с сохранением одного сосудисто-нервного пучка
Компьютер-ассистированная ультрасонографическая система HistoScanning позволяет оценивать морфологические изменения ПЖ посредством сопоставления полученного ультразвукового (УЗ) сигнала с данными патогистологических исследований. Чувствительность и специфичность метода варьирует в зависимости от объема опухоли и составляет 80%-87% и 90%-93% соответственно [25, 26, 27].
Методика проведения фокальной криоаблации схожа с таковой при тотальной криоаблации и включает проведение не менее 2 циклов замораживания-оттаивания при помощи аргона и гелия, использование термодатчиков для контроля температуры внутри ледяного шара и в окружающих тканях, а также катетера для согревания уретры [28, 29]. В большинстве случаев процедура фокальной криоаблации выполняется под эпидуральной или спинномозговой анестезией под контролем трансректальной ультрасонографии в двух проекциях. Сонографические характеристики замороженной и незамороженной ткани существенно различаются, что позволяет адекватно контролировать ход лечения и границу «ледяного шара». Сокращение числа криодатчиков и возможность их позиционирования позволяет выполнять криоаблацию не только отдельного участка (доли) ПЖ, но и прилегающих тканей (при необходимости) (рисунок 2, 3).
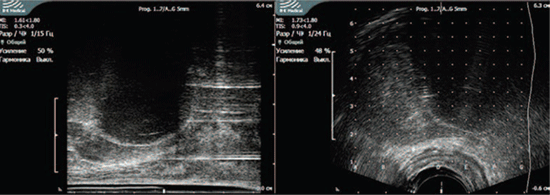
Рис. 2. Формирование ледяного шара (сагиттальная и аксиальная проекции), распространяющегося на левую долю предстательной железы
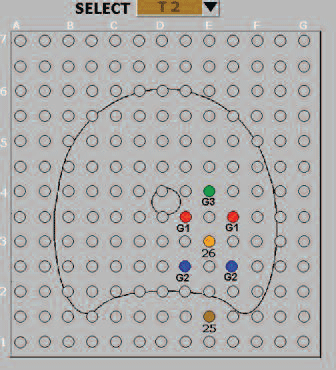
Рис. 3. Схематическое расположение криоигл и термосенсоров в ходе фокальной криоаблации
Протокол наблюдения за больными в послеоперационном периоде по рекомендации большинства авторов включает определение уровня ПСА через различные интервалы времени после операции, а также проведение биопсии ПЖ под контролем ТРУЗИ. В настоящее время в клинике урологии МГМСУ накоплен наибольший опыт проведения тотальной и фокальной криоаблации ПЖ. Протокол наблюдения за больными, перенесшими фокальную криоаблацию ПЖ, которая была выполнена 5 пациентам в России, в нашей клинике включает определение уровня ПСА каждые 3 месяца в течение первого года после операции, проведение биопсии ПЖ под контролем ТРУЗИ через 1 год после операции (независимо от уровня ПСА), заполнение опросников (IIEF, UCLA PCI, ICIQ-SF и др.).
Ухудшение эректильной функции (ЭФ) и недержание мочи наиболее распространенные осложнения любого метода радикального лечения РПЖ. Они в значительной степени влияют на качество жизни пациента. Введение в клиническую практику аппаратов для криоаблации 3-го поколения, специальных термодатчиков, катетера для согревания слизистой уретры, а также мониторирование всего процесса криотерапии в режиме реального времени позволило минимизировать осложнения криоаблации. Тем не менее, в результате смещения границы ледяного шара на перипростатическую ткань может возникнуть риск развития эректильной дисфункции. После операции у большинства пациентов развивается отёк мошонки и полового члена, а также петехии на промежности, в области корня мошонки и пениса.
Осложнения после фокальной криоаблации встречаются значительно реже по сравнению с тотальной криоаблацией. По данным ряда исследований, у пациентов, перенесших фокальную криоаблацию, ЭФ сохраняется в 71-89% случаев и, в большинстве случаев, пациентам не требуется применение ингибиторов фосфодиэстеразы 5 типа (ФДЭ 5) [30, 31]. Недержание мочи у больных, перенесших фокальную криоаблацию, выражено в незначительной степени или отсутствует полностью. Несмотря на значительные преимущества фокальной криоаблации, у данной методики есть свои недостатки: неполная аблация опухоли, недостаточная визуализация опухоли, отсутствие стандартизированного протокола наблюдения за пациентами после операции.
На сегодняшний день не существует единого мнения относительно определения биохимической безрецидивной выживаемости после фокальной криоаблации. Применение надира ПСА 0,2-0,4 нг/мл после радикальной простатэктомии не подходит, т.к. остается нелеченая ткань ПЖ. По мнению большинства авторов, применение надира ПСА +2 нг/мл может быть использовано в протоколе наблюдения за больными после фокальной криоаблации.
В 2002 г. Onik GМ. и соавт. опубликовали первую работу о фокальной односторонней нервосберегающей криоаблации ПЖ [32]. При среднем сроке наблюдения 36 мес у всех наблюдавшихся пациентов (n=9) не отмечалось роста уровня ПСА. Спустя год после операции 6 пациентам была выполнена контрольная биопсия ПЖ, не выявившая рецидива РПЖ. 7 из 9-и пациентов отметили удовлетворительную половую функцию. В 2008 г. авторы представили результаты наблюдения за 48 пациентами, перенесшими фокальную криотерапию РПЖ. В течение двух лет после лечения уровень ПСА оставался стабильным у 94 % пациентов, составив в среднем 2,19 нг/мл. Через 1 год 24 пациентам была выполнена контрольная биопсия ПЖ, не выявившая РПЖ ни в одном случае [33].
Ward JF. и Jones J.S. [34] представили данные регистра COLD (Cryo On-LineDatabase) за период с 1997 по 2007 гг. Из 5853 пациентов, входящих в регистр 1160 была выполнена фокальная криоаблация ПЖ (19,8%). Биохимическая безрецидивная 3летняя выживаемость составила 75,7 % (критерий ASTRO). В последующем у 43 пациентов (3,7%) при контрольной биопсии был выявлен рецидив заболевания. Полное удержание мочи отмечено в 98,4% случаев, спонтанная эрекция в 58,1% наблюдений. Задержка мочи наблюдалась у 6 пациентов (1,1%). Ректоуретральный свищ выявлен у 1 пациента (0,1%).
Truesdale MD. и соавт. [35] представил результаты лечения 77 больных, перенесших фокальную криоаблацию предстательной железы в период с 2002 по 2009 гг. В исследование не включались пациенты, перенесшие лучевую и (или) гормональную терапию. Средний возраст больных составил 69,5 лет, медиана наблюдения 24 (0-87) мес, средний уровень ПСА перед операцией 6,5 нг/мл. По данным биопсии ПЖ средний балл по шкале Глисона – 6 (5-8). По шкале D'amico в группу низкого, среднего и высокого риска были включены 44, 31 и 2 пациента соответственно. В послеоперационном периоде всем пациентам спустя год после операции выполнялась биопсия ПЖ, уровень общего ПСА контролировался 1 раз в 3 мес. В последующем 22 пациентам после операции в связи с подозрением на рецидив была выполнена биопсия простаты: у 10 пациентов (45,5%) диагноз был подтвержден. Биохимическая безрецидивная и раковоспецифическая выживаемость составили 72,7% и 87% соответственно.
Bahn D. и соавт. [36] представили результаты наблюдения за 73 пациентами, перенесшими фокальную криоаблацию ПЖ в период с 2002 по 2011 гг. До операции каждому пациенту проводились ТРУЗИ с допплерографией, а также трансректальная и промежностная биопсии, подтвердившие односторонний процесс заболевания. Послеоперационное наблюдение включало определение уровня ПСА каждые 36 мес, проведение трансректальной биопсии через 6 и 12 мес после операции и заполнение валидизированных опросников. Медиана наблюдения за пациентами составила 3,7 (1-8,5) лет, уровень ПСА до операции 5,9 нг/мл. По данным биопсии простаты сумма баллов по Глисону 6 и 7 имела место у 30 и 43 пациентов соответственно. После операции уровень ПСА снизился на 70% и составил в среднем 1,6 нг/мл (p< 0,001). Из 48 пациентов, которым была выполнена биопсия простаты после операции, у 36 (75%) результат был отрицательным. Прогрессия заболевания была отмечена у 12 пациентов: рак определялся в контралатеральной доле (n=11) и в пролеченной доле (n=1). Полное удержание мочи и сохранение эректильной функции было отмечено у 100% и 86% пациентов соответственно. Сравнивая полученные результаты с результатами лечения пациентов, перенесших РПЭ, авторами был сделан вывод о сопоставимости онкологических и функциональных результатов.
ЗАКЛЮЧЕНИЕ
В результате лучшего понимания процесса криодеструкции опухоли на молекулярном уровне, усовершенствования техники криоаблации и улучшения отбора пациентов, результаты фокальной криотерапии являются многообещающими. Учитывая наличие серьезных осложнений радикального лечения рака предстательной железы, а также тот факт, что многие мужчины отвергают возможность выжидательной тактики или активного наблюдения, проведение фокальной терапии для таких пациентов является альтернативным решением. В результате отсутствия валидизированных опросников для больных, перенесших фокальную криоаблацию, рекомендовано использование существующих методов самооценки состояния здоровья для того, чтобы сравнить результаты с другими методами лечения (международная шкала оценки эректильной функции (IIEF), шкала международного общества по удержанию мочи, функциональная оценка терапии рака простаты, Европейский опросник качества жизни (EuroQoL) и др.). Биопсию простаты под контролем ТРУЗИ рекомендуется проводить через 12 месяцев после фокальной криоаблации ПЖ. Необходимо определять уровень ПСА через 3-месячный интервал в течение первого года после операции и через 6-месячный интервал в последующем.
Усовершенствование методов визуализации опухоли, ее степени распространения и дифференцировки, могут значительно улучшить отбор пациентов, которым показана фокальная криоаблация, а также стандартизировать протокол периода наблюдения.
В России криоаблация предстательной железы с использованием системы 3-го поколение (производитель – компания Galil Medical) применяется с 2010 года. В настоящее время наибольший опыт проведения криоаблации ПЖ (5 пациентов) имеется в клинике урологии МГМСУ. Ряд других лечебных учреждений продолжают осваивать данную современную методику.
ЛИТЕРАТУРА
1. Eggener SE, Scardino PT, Carrol PR. Focal therapy for localized prostate cancer: A critical appraisal of rationale and modalities. // J Urol. 2007. Vol. 178. Р. 2260-2267.
2. Ahmed HU, Emberton M. Benchmarks for success in focal therapy of prostate cancer: cure or control? // World J Urol. 2010. Vol. 5. Р. 577-582.
3. Murphy DG, Walton TJ, Connolly S. Focal therapy for localised prostate cancer: are we asking the correct research questions? // BJU. 2012. Vol. 1. Р. 1-3.
4. Karavitakis M, Ahmed HU, Abel PD. Margin status aer laparoscopic radical prostatectomy and the index lesion: implications for preoperative evaluation of tumor focality in prostate cancer. // J Endourol. 2012. Vol. 5. Р. 503-508.
5. Mouraviev V, Mayes JM, Sun L. Prostate cancer laterality as a rationale of focal ablative therapy for the treatment of clinically localized prostate cancer. // Cancer. 2007. Vol. 4. Р. 906-910.
6. Joosten JJ, Muijen GN, Wobbes T, Ruers TM. In vivo destruction of tumor tissue by cryoablation can induce inhibition of the secondary tumor growth: an experimental study. // Cryobiology. 2001. Vol. 41. Р. 49-58.
7. Sabel MS, Nehs MA, Su G, Lowler KP, Ferrara, italy, JL, Chang AE. Immunologic response to cryoablation of breast cancer. // Breast Cancer Res Treat. 2005. Vol. 90. Р. 97-104.
8. Bostwick D., Waters D., Bahn D. Group consensus reports from the consensus conference on focal treatment of prostatic carcinoma. // Urology. 2007. Vol/ 6. Р. 42-44.
9. EAU Guidelines on prostate cancer, Heidenreich A. 2013. Р. 72-73.
10. Turpen R, Rosser CJ. Focal therapy for prostate cancer: revolution or evolution. // BMC Urology. 2009. Vol. 9. Р. 2.
11. Bahn DK, Silverman PD. Focal cryoablation of prostate: review. // e scientific world journal. 2008. Vol. 8. Р. 486-491.
12. D΄Amico AV, Whittington R, Malkowicz SB. Biochemical outcome aer radical prostatectomy, external beam radiation therapy, or interstitial radiation therapy for clinically localized prostate cancer. // JAMA. 1998. Vol. 280. Р. 969-974.
13. Kattan MW, Eastham JA, Wheeeler TM. Counseling men with prostate cancer: A nomogram for predicting the presence of small, moderately differentiated, confined tumors. // J Urol. 2003. Vol. 170. Р. 1792-1797.
14. Scherr D, Swindle PW, Scardino PT. National Comprehensive Cancer Network guidelines for the management of prostate cancer. // Urology. 2003. Vol. 61. № 1. Р. 14-24.
15. Abouassaly R, Lane BR, Jones JS. Staging saturation biopsy in patients with prostate cancer on active surveillance protocol. // Urology. 2008. Vol. 71. Р. 573–577.
16. Eggener SE. Focal therapy for prostate cancer: possibilities and limitations. // Eur Urol. 2010. Vol. 58. № 1. Р. 57-64.
17. Wink M, Frauscher F, Cosgrove D. Contrast-enhanced ultrasound and prostate cancer; a multicentre European research coordination project. // EurUrol. 2008. Vol. 54. Р. 982–993.
18. Pallwein L, Mitterberger M, Struve P. Comparison of sonoelastography guided biopsy with systematic biopsy: impact on prostate cancer detection. // EurRadiol. 2007. Vol. 17. Р. 2278–2285.
19. Frauscher F, Klauser A, Volgger H. Comparison of contrast enhanced color Doppler targeted biopsy with conventional systematic biopsy: impact on prostate cancer detection. // J Urol. 2002. Vol. 167. Р. 1648–1652.
20. Tareen B., Godoy G., Sankin A. Laterality alone should not drive selection of candidates for hemi-ablative focal therapy. // J Urol. 2009. Vol. 181. Р. 1082-1090.
21. Nogueira L, Wang L, Fine SW. Focal treatment or observation of prostate cancer: pretreatment accuracy of transrectal ultrasound biopsy and T2-weighted MRI. // Urology. 2010. Vol. 75. Р. 472–477.
22. Haider MA, van der Kwast TH, Tanguay J. Combined T2weighted and diffusion-weighted MRI for localization of prostate cancer. // AJR Am J Roentgenol. 2007. Vol. 189. Р. 323–328.
23. Zelhof B, Lowry M, Rodrigues G, Kraus S, Turnbull L. Description of magnetic resonance imaging-derived enhancement variables in pathologically confirmed prostate cancer and normal peripheral zone regions. // BJU Int. 2009. Vol. 104. Р. 621–627.
24. Oyama N, Akino H, Suzuki Y, et al. Prognostic value of 2-deoxy-2[F-18] fluoro-D-glucose positron emission tomography imaging for patients with prostate cancer. // MolImagingBiol. 2002. Vol. 4. Р. 99–104.
25. Simmons L.A., Autier P., Zatura F. Detection, localization and characterization of prostate cancer by Prostate HistoScanning (TM). // BJU Int. 2012. Vol. 110. № 1. Р. 28-35.
26. Braeckman J, Autier P, Soviany C. The accuracy of transrectal ultrasonography supplemented with computer-aided ultrasonography for detecting small prostate cancers. // BJU Int. 2008. Vol. 102. Р. 1560–1565.
27. Dinter DJ, Weidner AM, Wenz F. Imaging diagnostics of the prostate. // Urol. 2010. Vol. 49. № 8. Р. 963-975.
28. Onik GM, Cohen JK, Reyes GD. Transrectal ultrasoundguided percutaneous radical cryosurgical ablation of the prostate. // Cancer. 1993. Vol. 72. № 4. P. 1291-1299.
29. Cytron S, Green D, Witzsch U. Cryoablation of the prostate: technical recommendations. // Prostate cancer prostatic dis. 2009. Vol. 129. № 4. P. 339-346.
30. Ellis DS, Manny TB, Rewcastle JC. Focal cryosurgery followed by penile rehabilitation as primary treatment for localized prostate cancer: initial results. // Urology. 2007. Vol. 12. Р. 9-15.
31. Bahn DK, Silverman P, Lee FSr. Focal prostate cryoablation: initial results show cancer control and potency preservation. // J Endourol. 2006. Vol. 9. Р. 688-692.
32. Onik GM, Narayan P, Vaughan D. Focal «nerve-sparing» cryosurgery for treatment of primary prostate cancer: a new approach to preserving potency. // Urol. 2002. Vol. 60. № 1. P. 109-114.
33. Onik GM, Vaughan D, Lotenfoe R. The «male lumpectomy»: focal therapy for prostate cancer using cryoablation results in 48 patients with at least 2-year follow-up. // Urol Oncol. 2008. Vol. 26. № 5. P. 500-505.
34. Ward JF., Jones JS. Focal cryotherapy for localized prostate cancer: a report from the national Cryo On-Line Database (COLD) Registry. // BJU Int. 2012. Vol. 6. Р. 1648-1654.
35. Truesdale MD, Cheetmanp J, Hruby GW. An evaluation of patient selection criteria on predicting progression-free survival after primary focal unilateral nerve-sparing cryoablation for prostate cancer: recommendations for follow up. // Cancer J. 2010. Vol. 9-10. Р. 544-549.
36. Bahn D, de Castro Abreu AL, GillI S. Focal Cryotherapy for Clinically Unilateral, Low-Intermediate Risk Prostate Cancer in 73 Men with a Median Follow-Up of 3.7 Years. // EurUrol. 2012. Vol. 7. Р. 55-63.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 379.19 кб |















































































