Инновационные стратегии снижения риска хирургической раневой инфекции
 11281
11281 Хирургические раневые инфекции (Surgical site infection SSI) являются источником многих осложнений и причиной высокой летальности, особенно у пациентов, относящихся к группам риска. Вероятность развития послеоперационных SSI определяется рядом внутренних и внешних факторов, действующих во время операции. В США ежегодно регистрируется от 750 000 до 1 000 000 случаев SSI, которые увеличивают продолжительность пребывания пациентов в стационаре на 3.7 млн. суток и являются причиной дополнительных расходов в размере US $1.6 млрд. в год. Основными направлениями снижения риска SSI считаются: совершенствование хирургической техники, своевременная и адекватная антимикробная профилактика, эффективное и длительное применение кожных антисептиков, а также поиск дополнительных методов снижения контаминации раны и оптимизации процесса заживления. В историческом плане контроль SSI проводился в ретроспективном режиме, однако попытки внедрения адекватных и эффективных программ контроля за развитием инфекционного процесса требуют проспективного междисциплинарного подхода в целях идентификации селективных и неселективных SSI, а также быстрого внедрения соответствующих подходов, направленных на снижение риска развития SSI. В США, проводимые на национальном уровне исследования и разработки по снижению частоты осложнений и летальности, связанных с SSI, стали основанием для принятия Проекта по улучшению хирургической помощи, который призван сосредоточить усилия на 4 доказательных интервенционных подходах, включая контроль гликемии у пациентов кардиохирургического и сосудистого профиля, адекватное удаление волосяного покрова, своевременную и качественную антимикробную профилактику и поддержание нормальной температуры тела у пациентов с колоректальными опухолями. В будущем работа по снижению риска SSI потребует целенаправленной многоотраслевой концентрации усилий и объединения доказательных подходов с эффективными инновационными технологиями.
ВВЕДЕНИЕ
В США ежегодно выполняется 30-35 миллионов хирургических операций. Согласно данным Центров контроля и профилактики заболеваний (CDC) Национальной сетевой программы по безопасности здравоохранения хирургическая раневая инфекция (SSI) является третьим по частоте осложнением, связанным с оказанием медицинской помощи [1, 2]. В ряде исследований показано, что SSI ведёт к увеличению как продолжительности пребывания пациента в клинике (в среднем на 7.3 суток), так и расходов на стационарное лечение.
Уже более 100 лет основным патогеном являеться Staphylococcus aureus, который является причиной разнообразных гнойных и токсигенных процессов. В течение последних 40 лет штаммы метициллинрезистентного S. aureus (MRSA) быстро распространились по больницам, и теперь 20-60% изолятов S. aureus, выделяемых у стационарных пациентов, обладают устойчивостью к метициллину [3]. Более того, недавно проведенное CDC исследование показало, что в США частота госпитализации, связанной с MRSA, отличается крайней изменчивостью: среди пациентов в возрасте до 14 лет она составляет 13.1, а среди лиц в возрасте >65 лет достигает 63.6 на 1000 выписанных пациентов [4]. Новейшими исследованиями установлено, что с MRSA-инфекциями связана не только повышенная заболеваемость, но и значительная экономическая нагрузка, источниками которой выступают продолжительность пребывания пациентов в клинике и расходы на стационарное лечение [5, 6].
Научно-обоснованное снижение рисков в эпоху государственного регулирования
Снижение степени риска развития SSI требует понимания того, что факторы риска у конкретного пациента могут играть существенную роль в усилении микробной вирулентности в хирургической ране. Неполный перечень внутренних и внешних факторов риска, способствующих развитию послеоперационных SSI, представлен в таблице 1 [7]. Методы профилактики послеоперационных SSI предусматривают тщательный контроль инфекции и адекватную технологию лечения. Недавняя попытка в США снизить степень риска развития SSI привела к принятию национальной стратегии по данному вопросу в виде Проекта по улучшению хирургической помощи (SCIP). SCIP представляет собой результат сотрудничества специализированных и правительственных организаций на национальном уровне, целью которого является улучшение качества хирургической помощи за счет существенного (25%) снижения заболеваемости и летальности к 2010 году. Разработаны SCIP-критерии для профилактики венозных тромбоэмболий, нарушений деятельности сердца, инфекционных и респираторных осложнений. Представлены основные меры профилактики этих осложнений (таблица 2). Эти меры были определены на основании доказательных критериев практической медицины, способных реально снизить послеоперационную летальность и частоту осложнений [8]. Научно-обоснованные мероприятия по антимикробной профилактике включают введение профилактической дозы соответствующего препарата за 1 час до выполнения разреза, а так же выбор средства в соответствии с принятыми опубликованными принципами и прекращение введения выбранного препарата через 24 часа после окончания операции [9, 10]. Оставшиеся 3 направления (контроль уровня глюкозы в крови у пациентов при операциях на сердце и сосудах, надлежащее удаление волосяного покрова (с использованием специальных инструментов или без них) и поддержание нормальной температуры тела у пациентов после колоректальных вмешательств) завершают комплекс доказательных мероприятий, являющихся ключевыми моментами программы профилактики инфекций в рамках SCIP [11-16].
Таблица 1. Факторы риска развития послеоперационной хирургической раневой инфекции [7].
| Внутренние факторы (пациент) | Внешние факторы (манипуляции) |
| Возраст | Отсутствие гигиенической обработки кожи (водной процедуры) перед операцией |
| Диабет (заболевание обмена веществ) | Бритье кожи в зоне операции накануне вечером |
| Периоперационная гипергликемия | Увеличенная длительность операции |
| Курение | Недостаточная антисептическая обработка кожи |
| Сопутствующая инфекция (отсроченная) | Недостаточная хирургическая профилактика |
| Ожирение | Дефекты асептики |
| Пониженное питание (иммунная недостаточность) |
Гипотермия или гипоксия |
| Низкий уровень сывороточного альбумина перед операцией | Периоперационная гемотрансфузия |
| Прием стероидов | Хирургическая техника: неадекватный гемостаз или избыточная травматизация тканей |
| Продолжительный срок пребывания в клинике до операции | |
| Предшествующее облучение области операционного поля | |
| Колонизация Staphylococcus aureus |
В условиях рыночной экономики больницы стремятся улучшить исходы путём повышения репутации учреждения, влияния на рыночное положение организации. В связи с этим Федеральный акт о сокращении бюджетного дефицита от 2005 г. дал право Центрам программ медицинской помощи Medicare и Medicaid (CMS) отказывать в возмещении расходов тем учреждениям, которым не удается уменьшить число неблагоприятных исходов для стационарных пациентов. CMS представляет собой агентство Федерального министерства здравоохранения и социального обеспечения, ответственное за управление программами Medicare и Medicaid, а также Государственной программой медицинского страхования детей и рядом других программ здравоохранения в США. По состоянию на 1 октября 2008 г. CMS не возмещали расходы на лечение некоторых, таких осложнений как инфекции, связанные с установками центрального сосудистого доступа, катетер-ассоциированные инфекции мочевыводящих путей и SSI, включая медиастиниты после аорто-коронарного шунтирования. В 2009 году этот ощутимый недостаток финансовых поступлений, связанный с вышеперечисленными причинами, еще более увеличился за счет расширения перечня неоплачиваемых послеоперационных осложнений на ряд ортопедических и бариатрических вмешательств [17]. Конечно, быть может, федеральное правительство США пытается таким образом ликвидировать плохо работающие организации здравоохранения, однако это все же можно считать хорошим стимулом к повышению качества работы. Учреждения, работающие в приемлемом диапазоне условий SCIP, будут реально получать несколько более высокую компенсацию за улучшение качества деятельности [18]. Следовательно, снижение степени риска развития SSI сейчас находится на переднем плане для всех организаций здравоохранения США, и во многих случаях мы видим признаки слияния традиционных подходов к снижению рисков с новыми технологиями в целях улучшения исходов.
Таблица 2. Ключевые SCIP-критерии снижения частоты осложнения развития инфекций и летальности после оперативных вмешательств.
| Профилактика инфекций | Профилактическое назначение антимикробных препаратов в течение 1 часа до выполнения разрезаА |
| Профилактическое применение антимикробных средств в соответствии с принятыми опубликованными принципами | |
| Прекращение применения профилактических антимикробных препаратов в течение 24 часов после окончания операцииВ | |
| Контроль уровня глюкозы в крови у пациентов при кардиохирургических вмешательствах | |
| Адекватное удаление волосяного покрова (с использованием специальных инструментов или без них) | |
| Поддержание нормальной температуры тела у пациентов при колоректальных операциях | |
| Профилактика венозных тромбоэмболий | Профилактические мероприятия в соответствии с действующими правилами |
| Принятие соответствующих мер по профилактике венозных тромбоэмболий в течение 24 часов до или после операции | |
| Профилактика нарушений деятельности сердца | Периоперационное назначение β-блокаторов пациентам, которые принимали их до поступления в клинику |
| Профилактика респираторных осложнений | Поднятие головного конца кровати минимум на 30° для пациентов, находящихся на искусственной вентиляции |
| Профилактика стрессовых язв у пациентов, находящихся на искусственной вентиляции | |
| Реализация стандартного протокола отучения пациентов от искусственной вентиляции |
А для пациентов, нуждающихся в назначении ванкомицина или фторхинолонов для хирургической профилактики, - за 2 часа
до выполнения рузреза
В в кардиохирургии - в течении 48 часов
КЛАССИЧЕСКИЕ И ИННОВАЦИОННЫЕ ПОДХОДЫ К СНИЖЕНИЮ РИСКА SSI
Микрофлора кожи сложна и многообразна (микробное число колеблется от 103 на сухих поверхностях кожи до >106 в таких областях, как пах или промежность) [19]. Многие из этих микроорганизмов гнездятся в сальных железах, по волосяному стержню постоянно выделяются на поверхность кожи и распространяются во внешней среде [20].
Возникает вопрос: есть ли польза от душевой процедуры перед плановой операцией? Доказательный анализ свидетельствует о том, что никаких преимуществ такой подход не дает [21]. Однако по данным критического обзора публикаций Кокрановского сотрудничества методология и дизайн прежних клинических исследований не лишены изъянов. Например, отсутствовала стандартизованная методика проведения гигиенических водных процедур перед операцией (пациенты могли принимать душ один или несколько раз), длительность антисептической водной процедуры не была стандартизована, хирургические вмешательства существенно отличались друг от друга (чистые, условно чистые и контаминированные плановые операции). И, наконец, не был организован контроль приверженности пациентов. В недавнем исследовании мы получили данные о том, что если следовать продуманному и хорошо документированному протоколу, то можно получить стабильно высокие уровни хлоргексидина глюконата (CHG) на поверхности кожи (рис. 1) [22].
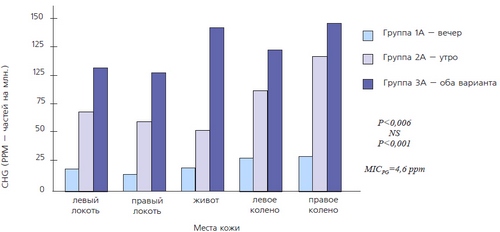
Рис. 1. Графическое отображение данных проспективного рандомизированного исследования: концентрации хлоргексидина на поверхности кожи 5 анатомических областей после 3 различных схем обработки 4% хлоргексидином (накануне вечером, утром и оба варианта - двукратная обработка) перед взятием проб [22].
Практика поощрения пациентов в отношении принятия двух душевых процедур перед плановыми операциями имеет свои достоинства. Во-первых, антисептический душ или гигиеническая процедура снижает микробное представительство на поверхности кожи, особенно на участках с повышенным увлажнением.
Во-вторых, тактика двух процедур обеспечивает наличие на поверхности кожи высоких концентраций CHG, которые сохраняются даже на некотором протяжении послеоперационного периода. Стоимость такого метода снижения степени риска минимальна (<US $1.50 за 4 жидких унции на 1 пациента), тогда как другие подходы, например контроль гликемии, могут потребовать привлечения значительных ресурсов учреждения. Наконец, целесообразность и простота такого подхода имеют большое значение для медперсонала хирургических отделений, которые непосредственно проводят предоперационную подготовку пациентов [23].
В ходе реализации SCIP- инициативы выяснилось, что, несмотря на относительную простоту концепции периоперационной антимикробной профилактики, внедрение эффективной программы с обеспечением своевременного применения надлежащего препарата в адекватной дозе и прекращением его использования по истечении 24 часов зачастую требует существенных изменений в области культуры (психологии) хирургов, анестезиологов, фармацевтов и сестер. Достижение эффективного результата в объеме 95% приверженности инициативам SCIP требует безоговорочного сосредоточения усилий на междисциплинарном уровне. Каждая хирургическая специальность представляет собой уникальную область практической медицины, поэтому режимы профилактики следует соответствующим образом адаптировать, чтобы обеспечить проведение мероприятий до начала хирургического вмешательства. В различных областях хирургии понятие «времени от прибытия пациента до разреза» может быть очень разным. Например, в кардиохирургии этот интервал может достигать 80 минут, а в ортопедии может быть менее 25 минут. В связи с этим, если пациенту до операции необходимо назначить ванкомицин или фторхинолон, то лучше всего это сделать в предоперационной, нежели в операционном зале. Эти разграничения имеют большое значение, однако для реализации всех этих мероприятий необходим междисциплинарный подход [24]. Второстепенная проблема, находящаяся в поле зрения некоторых практических врачей - это проблема дозирования по массе тела. Исторически сложилось так, что максимальная профилактическая доза цефазолина составляет 2 г и обычно назначается пациентам с массой тела >70 кг. Однако при высоких значениях индекса массы тела (ИМТ), что характерно для населения многих индустриально развитых стран, эта доза может оказаться недостаточной для достижения нужного эффекта в периоперационном периоде.
В литературе содержится недостаточное количество работ, касающихся выбора дозы при высоком ИМТ. В 2004 г. хирурги Висконсинского медицинского колледжа изучили динамику концентрации цефазолина в сыворотке крови и тканях после его назначения в периоперационном периоде в дозе 2г бариатрическим пациентам. Пробы тканей и сыворотки крови получали на протяжении всей операции (обходной желудочнокишечный анастомоз по Ру [Roux- en-Y]) у 38 пациентов. В результате анализа взятых проб выяснилось, что менее чем у 29% пациентов концентрация препарата в тканях была достаточной для противодействия S. aureus или Staphylococcus epidermidis в хирургической ране [25]. Эти находки позволили сделать заключение о том, что при высоком ИМТ (>40) 2 г β-лактамного антибиотика являются субоптимальной дозой. Пришло время рассмотреть вопрос о повышении периоперационной дозы цефазолина при высоком ИМТ у пациентов при плановых операциях.
Как уже отмечалось выше, факторы риска можно разделить на внутренние (присущие пациенту) и внешние (связанные с процедурами). При этом фактор самой операционной в отношении риска SSI рассматривался как некий пассивный момент. Как правило, в конструкции современных операционных залов предусмотрена многократная смена атмосферы (20-25 раз в течение 60 минут), и это считается эффективным методом снижения контаминации воздушной среды жизнеспособными микроорганизмами. Некоторые авторы, однако, считают, что этого недостаточно для снижения риска интраоперационной контаминации, особенно при операциях, связанных с имплантацией биомедицинских устройств. В одном исследовании 1999 г. было выявлено, что присутствие в операционном зале персонала повышает активность микробного распространения в 40 раз [26]. Более того, 40 лет назад были получены сведения о том, что 20-30% медицинских работников являются потенциальными носителями S. aureus в полости носа, а некоторые лица способны распространять микроорганизмы с поверхности своей кожи со скоростью 10 000 бактерий/мин-1 [20, 26, 27]. Роль воздуха в операционной в этиологии SSI до настоящего времени неясна, но в недавних исследованиях выяснилось, что биомедицинские устройства-имплантаты могут оказаться весьма уязвимыми объектами контаминации и стать причиной развития инфекций [28].
Поздние инфекции, связанные с сосудистыми шунтами (от 5 до 41 месяца после имплантации), случаются нечасто, но считаются грозными осложнениями. В отличие от острых инфекций, связанных с сосудистыми имплантатами и обусловленными S. aureus, эти поздние инфекции вызываются S. epidermidis и обычно приводят к возникновению псевдоаневризмы анастомоза, образованию наружного свища и ухудшению функционирования имплантата. Сканирующая электронная микроскопия наружной поверхности инфицированного имплантата после его удаления часто выявляет наличие обильного покрытия из пленкообразующих стафилококков [29]. Этиология этих инфекций остается предметом серьезных разногласий. Изучая культуры микроорганизмов, взятых с поверхности кожи пациентов с сосудистыми заболеваниями, Levy с сотрудниками в 1989 г. опубликовали данные о том, что с поверхности кожи в области планируемого хирургического разреза можно высеять множество пленкобразующих штаммов коагулазо-негативных стафилококков. Это значит, что интраоперационная контаминация имплантата может быть обусловлена в том числе и собственной микрофлорой кожи пациента [30]. В недавнем исследов ании с применением методов молекулярной эпидемиологии было выявлено, что распространение микроорганизмов из носоглотки одного из ассистентов хирурга привело к контаминации хирургической раны и развитию послеоперационных SSI у пациентов после аорто-коронарного шунтирования [31].
Данные исследований, проведенных в отделении сосудистой хирургии Висконсинского медицинского колледжа с применением инновационной технологии с непрерывным взятием проб воздуха неподалеку от операционной раны, показали, что все члены хирургической бригады были активными распространителями носоглоточной флоры. В течение 38-50% времени периода контроля из зон, находящихся поблизости от операционной раны, высевались S. aureus и/или S. Epidermidis, а также другие типы бактерий (рис. 2).
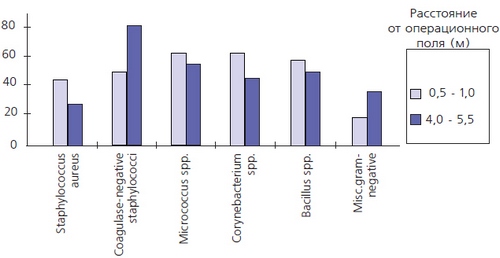
Рис. 2. Средние данные по 70 различным операциям на кровеносных сосудах с получением грамположительных и грамотрицательных микробных аэрозолей из
воздуха операционной.
Более того, с помощью молекулярных методов анализа удалось идентифицировать конкретных членов операционной бригады как распространителей микроорганизмов, ставших причиной контаминации раны [32]. Эти исследования также показали, что защитные свойства обычных хирургических масок с течением времени снижаются, и уже через 90 минут появляется высокая вероятность выделения микроорганизмов во внешнюю среду по краям маски за счет «вентиляции». Утверждение о том, что воздушно-капилярный путь может быть важным фактором захвата и диссеминации микроорганизмов для стационарных пациентов, рассматривается с известной долей скептицизма. Тем не менее, в исследованиях было показано, что носоглоточное распространение является обычным явлением, которое еще более усиливается в условиях сопутствующей риновирусной инфекции [33,34]. Действительно, наш собственный опыт свидетельствует о том, что насморк у сотрудника, присутствующего в операционной, способен значительно увеличить микробную нагрузку на окружающую среду помещения [32].
С учетом растущего числа фактов, свидетельствующих в пользу роли аэрозолей в развитии инфекций, связанных с медицинскими процедурами, FDA (Управление по контролю качества продуктов питания и лекарственных препаратов США) в 2007 г. создало экспертную группу по разработке альтернатив обычной хирургической маске с соответствующими техническими и функциональными характеристиками. Следующее поколение хирургических масок будет, вероятно, совсем другим. Имеются предложения ввести в материал маски антимикробное вещество, эффективно уничтожающее бактерии до их выделения (распространения) в окружающую среду. Еще одно предложение связано с модификацией нынешней респираторной маски N-95 в направлении повышения удобства для пользователя с сохранением защитных свойств изделия. Доработка маски N-95 представляется наиболее жизнеспособным вариантом, направленным на снижение степени риска попадания носоглоточной флоры в атмосферу операционной. Воздушный путь передачи считается важным путем распространения вирусов и некоторых патогенов, таких как Mycobacterium tuberculosis, однако сообщество специалистов в области контроля инфекций несколько сомневается в том, что такой механизм может участвовать в распространении госпитальных инфекционных патогенов, например MRSA. В недавнем отчете по результатам Австралийского исследования, проведенного с применением механических пробоотборников воздуха и осадительных пластин, сказано, что MRSA выделялся из воздуха 80% палат в концентрациях от 1 до 128 колониеобразующих единиц [35]. Эти данные четко указывают на воздух как на важный источник микробной контаминации воздуха больничных палат и операционных. К сожалению, участие этого механизма в развитии инфекций имеет зачастую катастрофическое значение для хирургов и пациентов, поскольку инфекции, связанные с имплантатами, почти всегда ведут к хирургическому удалению устройств, повышению расходов на лечение, ухудшению состояния пациентов и исходов в целом.
КАКОВА РОЛЬ ИМПРЕГНАЦИОННЫХ ТЕХНОЛОГИЙ В ХИРУРГИИ?
Технологии импрегнации в качестве метода снижения степени риска возникновения инфекций, связанных с оказанием медицинской помощи, существуют уже более 15 лет и применяются при изготовлении самых различных медицинских устройств, включая урологические катетеры, устройства центрального сосудистого доступа, раневые повязки, а также некоторые ортопедические и урологические имплантаты [36-41]. В нескольких исследованиях доказательного уровня была подтверждена эффективность таких изделий, импрегнированных (покрытых) антимикробными средствами, у некоторых групп пациентов. Последняя инновация в области импрегнационных технологий в хирургии - шовный материал с триклозановым покрытием. При рассмотрении вопросов, связанных с этими технологиями необходимо учитывать два фундаментальных вопроса: действительно ли шовный материал является источником инфекции?; какие имеются клинические свидетельства эффективности таких изделий? Из литературы известно, что если шовный материал подвергся контаминации (рис. 3), то местные механизмы деконтаминации раны, опосредуемые гранулоцитами, становятся неэффективными [42, 43]. Помимо всего прочего, структурный состав нити и тканевая реактивность также влияют на инфицирующую способность, при этом плетеная нить в большей степени уязвима для микробной контаминации, чем моноволоконная [44, 45]. Следовательно, внедрение в практику плетеного материала с триклозановым покрытием, очевидно, можно считать полезным дополнением к попыткам снизить риск SSI.

Рис. 3. Сканирующая электронная микрофотография плетеной лигатуры, контаминированная метициллинрезистентным Staphylococcus aureus. При контакте шовного материала с кровью и/или тканевыми белками контаминация его поверхности ускоряется.
Однако прежде чем полностью внедрять эту технологию в практику, необходимо получить ответ на несколько вопросов. Во-первых, безопасны ли эти изделия, и не увеличит ли наличие триклозана в организме риск развития резистентности к другим патогенам, присутствующим в клиниках? Во-вторых, каков спектр антимикробной активности этих нитей, и будут ли они активно противостоять именно той флоре, которая чаще всего встречается в хирургической практике?
Для клинической пользы применения любого изделия с антимикробным покрытием (импрегнацией) первый вопрос, имеющий ключевое значение, состоит в том, где именно в организме будет находиться имплантат. Хирургическая рана представляет собой динамическую систему взаимодействия микробных контаминантов и защитных средств организма. Помещение импрегнированного изделия в эту среду не должно неблагоприятно влиять на течение процессов воспаления и созревания, имеющих основополагающее значение для нормального заживления раны. Модельные эксперименты с тканями животных показывают, что плетеные нити с триклозановым покрытием не препятствуют заживлению раны [46]. Кроме того, в клинических исследованиях с участием педиатрических пациентов нити из полиглактина 910, покрытые триклозаном, не оказывали неблагоприятного влияния на заживление ран после операций общехирургического профиля [47].
Вопрос возможного развития устойчивости также представляется проблематичным, особенно для изделий, остающихся в ране в течение длительного периода времени. Триклозан является антисептиком широкого спектра действия с доказанной активностью в отношении грамположительных и грамотрицательных бактерий [48]. Результаты двух исследований свидетельствуют о том, что субингибиторное или длительное воздействие триклозана не вызывает снижения активности препаратов или повышения антимикробной устойчивости при использовании минимальных ингибиторных концентраций [49, 50]. Эти исследования доказали, что учитывая данные минимальных ингибиторных концентраций, уровень резистентности микроорганизмов к триклозану очень невелик. Однако не следует забывать о том, что некоторые популяции бактерий, такие как Pseudomonas aeruginosa, устойчивы к многим антисептикам, включая триклозан, и, следовательно, потенциальный риск формирования клинической резистентности к триклозану нельзя считать нулевым.
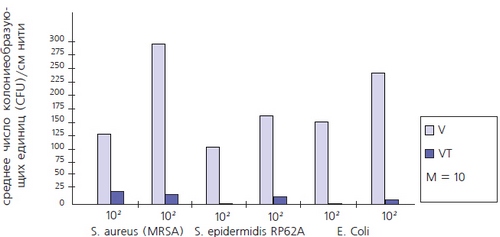
На рисунке 4 представлены сведения об активности плетеных нитей с триклозановым покрытием в адгезионной модели in vitro с хирургическими изолятами MRSA, S. epidermidis и штамма Escherichia coli с расширенным спектром устойчивости к β-лактамам, выделенными из инфицированной раны после абдоминальной гистерэктомии. При сравнении с контрольными изделиями без покрытия, триклозановый материал способствовал снижению (P < 0,01) микробной адгезии на плетеной поверхности [51]. В дальнейших исследованиях было показано, что при контаминации поверхности нити сывороточными белками, снижения антимикробной активности не происходит, а анализ активности триклозана в течение 96 часов не выявил существенных различий (снижения) его эффективности на 4-й день по сравнению с 1-м. Исследования in vitro подтверждают как спектр активности триклозана в отношении отдельных хирургических патогенов, так и ее поддержание в течение времени, необходимого для устранения контаминации раны и заживления.
Результаты посевов: стандартные нити из полиглактина 910 (V) и плетеные нити из полиглактина 910, покрытые триклозаном (VT) [51].
|
Рис. 4. Результаты изучения бактериальной адгезии: шовный материал с трикло зановым покрытием существенно снижает (P < 0.01) адгезию клинических изолятов MRSA, штамма Staphylococcus epidermidis, образующего биопленки, и штамма Escherichia coli, устойчивого к β-лактамазе в сравнении с обычными плетеными нитями без покрытия в двух различных инокулятах. |
Лабораторные исследования подтверждают решения FDA, однако окончательное суждение о клинической эффективности остается за результатами независимых клинических исследований. Данные двух таких исследований в настоящее время обсуждаются в медицинской литературе (одно в кардиохирургии, другое в детской нейрохирургии). В кардиохирургическом исследовании приняли участие 479 пациентов (у 103 был применен шовный материал с триклозановым покрытием, а у 376 - обычный). В исследовании был применен перспективный принцип «случай-контроль», в котором использование триклозанового шовного материала рассматривалось как «воздействие», а обычных плетеных нитей - как контроль. Пациенты были стратифицированы по критериям риска Национальной сетевой программы по безопасности здравоохранения. Состояние каждого пациента контролировалось в течение 2-15 месяцев (у некоторых пациентов были применены имплантируемые изделия). Необходимо отметить, что на протяжении всего исследования антимикробная профилактика проводилась по стандартизованной методике. В контрольной группе выявлено 24 случая инфекций, вызванных как чувствительными, так и резистентными ко многим препаратам штаммами MRSA, в то время как среди пациентов, у которых был применен шовный материал с триклозановым покрытием, случаев инфекций зарегистрировано не было. По данным экономического анализа дополнительные расходы, связанные с применением антимикробного шовного материала, оказываются ничтожными, «если удается предотвратить хотя бы один случай инфекции» [52]. Во втором проспективном двойном слепом рандомизированном контролируемом исследовании участвовали педиатрические пациенты, которым выполнялась имплантация шунтирующих устройств для отвода ликвора. Частота инфекций шунтов после установки составила 5-15%, причем большинство хирургов считает, что при интраоперационной контаминации этот показатель увеличивается [53, 54]. В этом исследовании пациенты были рандомизированы по группам антимикробного и обычного шовного материала. Главной конечной точкой была определена частота инфекций шунта через 6 месяцев после операции, которая в контрольной группе составила 21%, а в опытной - 4.3% (P = 0.038). При этом ни в одной из групп не было выявлено случаев неблагоприятных явлений, связанных с шовным материалом. Авторы сделали заключение о том, что применение шовного материала с антимикробным покрытием было «безопасным и эффективным и, возможно, способствовало снижению степени риска инфицирования шунта после операции» [55].
Данные этих двух независимых исследований, проведенных с участием пациентов, для которых послеоперационная инфекция означала серьезное ухудшение состояния и повышение риска летального исхода, свидетельствуют о том, что в плане стратегии снижения риска инфекционных осложнений применение антимикробного шовного материала для закрытия раны является безопасным и эффективным.
Следует, однако, обратить внимание на один важный момент: пользу, которую можно извлечь из импрегнационных технологий в плане снижения степени риска инфекций у хирургических пациентов, следует всегда рассматривать как дополнительную перспективу. В настоящее время, усилия по снижению частоты инфекций, связанных с установкой центрального венозного доступа, или пневмоний, обусловленных искусственной вентиляцией, привели к тому, что клиники на доказательной основе начали разрабатывать «пакетные» методики, однако в области профилактики SSI никаких подобных консенсусных мер не существует. Снижение степени риска для хирургических пациентов представляет собой задачу значительно более высокого уровня согласованности, решение которой требует не только создания межотраслевых рабочих групп, но также умения классифицировать большое количество факторов риска, влияющих на исходы лечения. Поэтому импрегнированные изделия, такие как шовный материал с триклозановым покрытием, не являются «чудодейственным» средством, а скорее важным дополнительным элементом исчерпывающей доказательной системы снижения степени риска.
СИТУАЦИЯ ПРОЗРАЧНА ИЛИ МЫ НЕДООЦЕНИВАЕМ ЗНАЧЕНИЕ ПРОБЛЕМЫ?
В 2007 г. в хирургической литературе появились 4 отдельных публикации, которые заслуживают обсуждения по следующим причинам:
- прозрачность;
- дискуссия по раневой инфекции, начатая по инициативе хирургов;
- осознание того, что повышение ИМТ и снижение активности гранулоцитов являются важными факторами риска;
- признание того, что частота случаев раневой инфекции во всех областях хирургии фактически выше тех значений, которые называют правительственные организации, такие как Национальная сетевая программа по безопасности здравоохранения.
Исследователи из Далласа (Техас) опубликовали свои данные, согласно которым частота инфекций после колоректальных операций в течение 4 лет составила 25%, и идентифицировали ряд факторов риска, независимо влияющих на возникновение инфекций в области разреза и инфекций внутренних структур, одним из которых является ИМТ [56].
Исследователи из Гейнсвилла (Флорида) сообщили, что у женщин после органосохраняющих операций по поводу ранних стадий рака молочной железы частота случаев инфекции колеблется в широких пределах и зависит от способа закрытия раны. При поверхностном закрытии раны частота инфекций составила 11.7%, а при полнослойном - 5.7%. Это весьма примечательное наблюдение с учетом того, что большинство врачей считают мастэктомию чистой (I класс) операцией. Очевидно, что это не так [57].
По данным группы хирургов, занимающихся лечением воспалительных заболеваний кишечника, частота послеоперационных инфекций у этих пациентов превышает 15% [58]. У большинства таких пациентов на момент операции активность гранулоцитов в ране оказывается сниженной из-за длительного приема лекарственных препаратов, таких как кортикостероиды или метотрексат. Акушеры-гинекологи провели исследование с целью выявления истинной частоты SSI после операций кесарева сечения в соответствии с определением CDC и идентификации независимых факторов риска для этих осложнений. Общая частота случаев инфекций в течение 30 дней после операции составила 8.9%, а на момент выписки - 1.8%. Продолжительность операции оказалась важной переменной риска, а ИМТ >30 был в равной степени важным фактором, как при плановых, так и при экстренных операциях кесарева сечения. Более того, авторы делают вывод о том, что ныне принятый (CDC) показатель частоты инфекций после кесарева сечения занижен относительно истинного, и в действительности эти осложнения наносят значительный вред здоровью женщин [59].
ЗАКЛЮЧЕНИЕ
Следует отметить, что наблюдаемая в США тенденция к открытому обсуждению вопросов инфекционных осложнений в медицине диктует необходимость объединения междисциплинарных ресурсов и коллегиальных усилий, направленных на разработку эффективных и научнообоснованных путей снижения риска SSI у наиболее подверженных им пациентов [60].
Ключевые слова: хирургическая раневая инфекция, факторы риска, периоперационная профилактика, микрофлора кожи, инфецированность воздуха в операционной, импрегнационные технологии.
Keywords: surgical site infections, risk factors, perioperative care, skin microflora, infection rate the air in the operating room, impregnation technology.
ЛИТЕРАТУРА
- Graves EJ, Gillum BS. Detailed diagnoses and procedures, National Hospital Discharge Survey, 1994. // Vital Health Stat 13. 1997. Vol. 127. P. 1-145.
- Emori TG, Gaynes RP. An overview of nosocomial infections, including the role of the microbiology laboratory. // Clin Microbiol Rev. 1993. Vol. 6, N 4. P. 428-432.
- Zinn CS, Westh H, Rosdahl VT. An international multicenter study of antimicrobial resistance and typing of hospital Staphylococcus aureus isolates from 21 laboratories in 19 countries or states. // Microb Drug Resist. 2004. Vol. 10, N 2. P. 160-168.
- Kuehnert MJ, Hill HA, Kupronis BA, Tokars JI, Solomon SL, Jernigan DB. Methicillin- resistant Staphylococcus aureus hospitalizations, United States. // Emerg Infect Dis. 2005. Vol. 11, N 6. P. 868-872.
- Engemann JJ, Carmeli Y, Cosgrove SE, Fowler VG, Bronstein MZ, Trivette SL, Briggs JP, Sexton DJ, Kaye KS. Adverse clinical and economic outcomes attributable to methicillin resistance among patients with Staphylococcus aureus surgical site infection. // Clin Infect Dis. 2003. Vol. 36, N 5. P. 592-598.
- Cosgrove SE, Sakoulas G, Perencevich EN, Schwaber MJ, Karchmer AW, Carmeli Y. Comparison of mortality associated with methicillin-resistant and methicillin-susceptible Staphylococcus aureus bacteremia: a meta analysis. // Clin Infect Dis. 2003. Vol. 36, N 1. P. 53-59.
- Mangram AJ, Horan TC, Pearson ML, Silver LC, Jarvis WR. Guideline for Prevention of Surgical Site Infection, 1999. Centers for Disease Control and Prevention (CDC) Hospital Infection Control Practices Advisory Committee. // Am J Infect Control. 1999. Vol. 27, N 2.P. 97-132.
- Lin DM. Surgical care improvement project: improve performance, reduce complications, and comply with CMS. Marblehead, MA: HC Pro, Inc; 2007.
- Bratzler DW, Houck PM. Antimicrobial prophylaxis for surgery: an advisory statement from the National Surgical Prevention Project. // Clin Infect Dis. 2004. Vol. 38, N 12. P. 1706-1715.
- Itani KMF, Wilson SE, Awad SS, Jensen EH, Finn TS, Abramson MA. Ertapenem versus cefotetan prophylaxis in elective colorectal surgery. // N Engl J Med. 2006. Vol. 355, N 25. P. 2640-2651.
- Zerr KJ, Furnary AP, Grunkemeier GL, Bookin S, Kanhere V, Starr A. Glucose control lowers the risk of wound infection in diabetics after open heart operations.// Ann Thorac Surg. 1997. Vol. 63, N 2. P. 356-361.
- van den Berghe G, Wouters P, Weekers F, Verwaest C, Bruyninckx F, Schetz M, Vlasselaers Ferdinande P, Lauwers P, Bouillon R. Intensive insulin therapy in the critically ill patients. // N Engl J Med. 2001. Vol. 345, N 19. P. 1359-1367.
- Latham R, Lancaster AD, Covington JF, Pirolo JS, Thomas CS. The association of diabetes and glucose control with surgical-site infections among cardiothoracic surgery patients. // Infect Control Hosp Epidemiol. 2001. Vol. 22, N 10. P. 607-612.
- Kurz A, Sessler DI, Lenhardt R. Perioperative normothermia to reduce the incidence of surgical-wound infection and shorten hospitalization. // N Engl J Med. 1996. Vol. 334, N 19.P. 1209-1216.
- Ko W, Lazenby WD, Zelano JA, Isom OW, Krieger KH. Effects of shaving methods and intraoperative irrigation on suppurative mediastinitis after bypass operations. // Ann Thorac Surg. 1992. Vol. 53, N 2. P. 301-305.
- Horgan MA, Piatt JH Jr. Shaving of the scalp may increase the rate of infection in CSF shunt surgery. // Pediatr Neurosurg. 1997. Vol. 26, N 4. P. 180-184.
- Ferman JH. Payments will be based on quality not quantity. CMS plans to stop paying for secondary infections. // Healthc Exec. 2008. Vol. 23, N 2. P. 52-54.
- Centers for Medicare and Medicaid Services (CMS), HHS. Medicare program; hospital outpatient prospective payment system and CY 2007 payment rates; CY2007 update to the ambulatory surgical center covered procedures list; Medicare administrative contractors; and reporting hospital quality data for FY 2008 inpatient prospective payment system annual payment update program-HCAHPS survey, SCIP, and mortality. Final rule with comment period and final rule. // Fed Regist. 2006. Vol. 71, N 226. P. 67959-8401.
- Edmiston CE, Seabrook GR, Johnson CJ, Paulson DS, Beausoleil C. Comparison of a new and innovative 2% chlorhexidine impregnated cloth with4%chlorhexidine as topical antiseptic for preparation of the skin prior to surgery.// Am J Infect Control. 2007. Vol. 35, N 2. P. 89-96. 20.
- Schaal KP. Medical and microbiological problems arising from airborne infection in hospitals.// J Hosp Infect .1991. Vol. 18, Suppl. A. S.451-459.
- Webster J, Osborne S. Preoperative bathing or showering with skin antiseptics to prevent surgical site infection (review). The Cochrane Collaboration. London: J Wiley & Sons; 2006. P. 1-21.
- Edmiston CE, Krepel CJ, Seabrook GR, Lewis BD, Brown KR, Towne JB. The preoperative shower revisited: can high topical antiseptic levels be achieved on the skin surface prior to surgical admission? // J Am Coll Surg. 2008. Vol. 207, N 2. P. 233-239.
- Pottinger JM, Starks SE, SteelmanVM. Skin preparations. // Perioperative Nurs Clinics. 2006. Vol. 1. P. 203-210.
- Zvonar RK, Bush P, Roth B. Practice changes to improve delivery of surgical antibiotic prophylaxis. // Healthc Q 2008. Vol. 11, N 3 Spec. P. 141-144.
- Edmiston CE, Krepel C, Kelly H, Larson J, Andris D, Hennen C, Nakeeb A, Wallace JR. Perioperative antimicrobial prophylaxis in the gastric bypass patient: do we achieve therapeutic levels? // Surgery. 2004. Vol. 136, N 4. P. 738-747.
- Ritter MS. Operating room environment. // Clin Orthop Relat Res. 1999. Vol. 369. P. 103-109.
- Berard F, Gandon J.Postoperative wound infections: the influence of ultraviolet irradiation of the operating room and of various other factors. // Ann Surg. 1964. Vol. 160, Suppl. 2. P. 1-92.
- Clarke MT, Lee PT, Robert CP, Gray J, Keene GS, Rushton N. Contamination of primary total hip replacement in standard and ultraclean operating theaters detected by polymerase chain reaction. // Acta Orthop Scand. 2004. Vol. 75, N 5. P. 544-548.
- Hasanadka R, Seabrook GR, Edmiston CE. Vascular graft infections. In: Rello J, KollefM, Diaz M, RodriguesA(eds.) Critical care infectious diseases, 2nd edition. Boston: Kluwer Academic Publishers; 2007. pp. 531-41.
- Levy ME, Schmitt DD, Edmiston CE, Bandyk DF, Krepel CJ, Seabrook GR, Towne JB. Sequential analysis of staphylococcal colonization by body surface cultured on patients undergoing vascular surgery. // J Clin Microbiol. 1990. Vol. 28, N 4.P. 664-669.
- Faibis F, Laporte C, Fiacre A, Delisse C, Lina G, Demachy M-C, Botterel F. An outbreak of methicillin-resistant Staphylococcus aureus surgical site infections initiated by a healthcare worker with chronic sinusitis. // Infect Control Hosp Epidemiol. 2005. Vol. 26, N 2. P. 213-215.
- Edmiston CE, Seabrook GR, Cambria RA, Brown KR, Lewis BD, Sommers JR, Krepel CJ, Wilson PJ, Sinski S, Towne JB. Molecular epidemiology of microbial contamination in the operating room environment: is there a risk for infections? // Surgery. 2005. Vol. 138, N 4. P. 572-588.
- Sherertz RJ, Reagan DR, Hampton KD, Robertson KL, Streed SA, Hoen HM, Thomas R, Gwaltney JM Jr. A cloud adult: the Staphylococcus aureus-virus interaction revisited. //Ann Intern Med. 1996. Vol. 124, N 6. P. 539-547.
- Bischoff WE, Bassetti S, Bassetti-Wyss BA, Wallis ML, Tucker BK, Reboussin BA, D’Agostino RB Jr, Pfaller MA, Gwaltney JM Jr, Sherertz RJ. Airborne dispersal as a novel transmission route of coagulase-negative staphylococci: interaction between coagulase negative staphylococci and rhinovirus. // Infect Control Hosp Epidemiol. 2004. Vol. 25, N 6. P. 504-511.
- Beckingham W, Senanayake S, Collignon P, McKenzie G. Is methicillin-resistant Staphylococcus aureus aerosolized when healthcare workers carry out activities for patients. // Healthc Infect. 2008. Vol. 13, N 3. P. 77-82.
- Crnich CJ, Maki DG. Are antimicrobial-impregnated catheters effective? Don’t throw the baby out with the bath water. // Clin Infect Dis. 2004. Vol. 38, N 9. P. 1287-1292.
- Stensballe J, Tvede M, Looms D, Lippert FK, Dahl B, Tonnesen E, Rasmussen LS. Infection risk with nitrofurazone-impregnated urinary catheters in trauma patients: a randomized study.// Ann Intern Surg. 2007. Vol. 147, N 5. P. 285-293.
- Paddock HN, Fabia R, Giles S, Hayes J, Lowell W, Adams D, Besner GE. A silver- impregnated antimicrobial dressing reduces hospital costs for pediatric burn patients. // J Pediatr Surg. 2007. Vol. 42, N 1. P. 211-213.
- Walenkamp GH, Keijn LL, de Leeuw M. Osteomyelitis treated with gentamicin-PMMA beads: 100 patients followed for 1-12 years. // Acta Orthop Scand. 1998. Vol. 69, N 5. P. 518-522.
- Darouiche RO, Mansouri MD, Zakarevicz D, AlSharif A, Landon GC. In vivo efficacy of antimicrobial-coated devices.// J Bone Joint Surg Am. 2007. Vol. 89, N 4. P. 792-797.
- Carson CC. Efficacy of antibiotic impregnation of inflatable penile prostheses in decreasing infection in original implant. // J Urol. 2004. Vol. 171, N 4. P.1611-1614.
- Rodeheaver GT, Kurtz LD, Belamy WT, Farrs H, Edlich RB. Biocidal braided sutures. // Arch Surg. 1983. Vol. 118, N 3. P. 322-327.
- Uff CR, Scott AD, Pockley AG, Phillips RK. Influence of soluble suture factors on in vitro macrophage function. // Biomaterials. 1995. Vol. 16, N 5. P. 355-360.
- Scher KS, Bernstein JM, Jones CW. Infectivity of vascular sutures. //Am Surg. 1985. Vol. 51, N 10. P. 577-579.
- Shuhaiber H, Chugh T, Burns G. In vitro adherence of bacteria to sutures in cardiac surgery. // J Cardiovasc Surg (Torino). 1989. Vol. 30, N 5. P. 749-753.
- Storch M, Perry LC, Davidson JM,WardJJ. A28-day study of the effect of coated Vicryl Plus antibacterial suture on wound healing in guinea pig linear skin wounds.// Surg Infect (Larchmt). 2002. Vol. 3, Suppl. 1. P.89-98.
- Ford HR, Jones P, Gaines B, Reblock K, Simpkins DL. Intraoperative handling and wound healing: controlled clinical trial comparing coated Vicryl Plus_antibacterial suture (coated polyglactin 910 suture with triclosan) with coated Vicryl_ suture (coated polyglactin 910 suture). // Surg Infect (Larchmt). 2005. Vol. 6, N 3. P. 313-321.
- Jones RD, Jampani HB, Newman JL, Lee AS. Triclosan: a review of effectiveness and safety in health care setting. // Am J Infect Control. 2000. Vol. 28, N 2. P. 184-196.
- Suller MTE, Russell AD. Triclosan and antibiotic resistance in Staphylococcus aureus. // J Antimicrob Chemother. 2000. Vol. 46, N 1. P. 11-18.
- Aiello AE, Marshall B, Levy SB, Dell-Latta P, Larson E. Relationship between triclosan and susceptibility of bacteria isolates from hands in the community.// Antimicrob Agents Chemother. 2004. Vol. 48, N 8. P. 2973-2979.
- Edmiston CE, Goheen MP, Krepel C, Seabrook GR, Johnson CP, Lewis BD, Brown KR, Towne JB. Bacterial adherence to surgical sutures: is there a role for antibacterial-coated sutures in reducing the risk of surgical site infections? // J Am Coll Surg. 2006. Vol. 203, N 4.P. 481-489.
- Fleck T, Moidl R, Blacky A, Fleck M, Wolner E, Grabenwoger M, Wisser W. Triclosan- coated sutures for the reduction of sternal wound infections: economic considerations. // Ann Thorac Surg. 2007. Vol. 84, N 1. P. 232-236.
- Ammirati M, Raimondi AJ. Cerebrospinal fluid shunt infections in children. A study on the relationship between the etiology of hydrocephalus, age at the time of shunt placement, and infection rate.// Childs Nerv Syst. 1987. Vol. 3, N 2. P. 106-109.
- McGirt MJ, Zaas A, Fuchs HE, George TM, Kaye K, Sexton DJ. Risk factors for pediatric ventriculoperitoneal shunt infection and predictors of infectious pathogens. // Clin Infect Dis. 2003. Vol. 36, N 7. P. 858-862.
- Rozzelle CJ, Leonardo J, Li V. Antimicrobial suture wound closure for cerebrospinal fluid shunt surgery: a prospective, double-blinded, randomized controlled trial. // J Neurosurg Pediatrics. 2008. Vol. 2, N 2. P. 111-117.
- Blumetti J, Luu M, Sarosi G, Hartless K, McFarlin J, Parker B, Dineen S, Huerta S, Asolati M, Varela E, Anthony T. Surgical site infections after colorectal surgery: do risk factors vary depending on the type of infection considered? // Surgery. 2007. Vol. 142, N 5. P. 704-711.
- Indelicato D, Grobmyer SR, Newlin H, Morris CG, Haigh LS, Copeland EM 3rd, Mendenhall NP. Association between operative closure type and acute infection, local recurrence, and disease surveillance in patients undergoing breast conserving therapy for early-stage breast cancer. // Surgery. 2007. Vol. 141, N 5. P. 645-653.
- Alves A, Panis Y, Bouhnik Y, Pocard M, Vicaut E, Valleur P. Risk factors for intraabdominal septic complications after a first ileocecal resection for Crohns disease: a multivariate analysis in 161 consecutive patients. // Dis Colon Rectum. 2007. Vol. 50, N 3.P. 331-336.
- Op0ien HK, Valb0 A, Grinde-Andersen A, Walberg M. Post-cesarean surgical site infections according to CDC standards: rates and risk factors.Aprospective cohort study. // Acta Obstet Gynecol Scand. 2007. Vol. 86, N 9. P. 1097-1102.
- McKibben L, Horan T, Tokars JI, Fowler G, Cardo DM, Pearson ML, Brennan PJ. Guidance on public reporting of healthcare-associated infections: recommendations of the Healthcare Infection Control Practices Advisory Committee. // Am J Infect Control. 2005. Vol. 33, N 4. P. 217-226.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 1.98 Мб |