Криотерапия рака предстательной железы
 16790
16790 В последние годы, благодаря выраженному техническому прогрессу в области ультразвуковой и рентгенологической визуализации, резко возросла частота выявления таких грозных заболеваний, как рак почки и предстательной железы. Онкопатология выявляется на ранних стадиях, что позволяет выполнять радикальное лечение. Наряду с традиционными и хорошо зарекомендовавшими себя хирургическими и лучевыми методами все большее распространение получают малоинвазивные методики: брахитерапия, HIFU-терапия, радиочастотная и криоабляция. Все они разрабатывались с целью минимизировать объем хирургического вмешательства с сохранением органа, но без потери онкологической эффективности. Многие из них могут выполняться в амбулаторных условиях, с минимально выраженными побочными эффектами и практически не влияют на физическую и социальную активность пациента, что в последнее время особенно актуально. У соматически отягощенных пациентов, для которых само по себе проведение открытых или лапароскопических вмешательств представляет большой риск, подобные процедуры являются едва ли не единственным радикальным методом лечения.
Имея в своем арсенале современные хирургические методы лечения рака почки (открытая и лапароскопическая резекция почки и нефрэктомия), все разнообразие органоуносящих и малоинвазивных методов лечения рака предстательной железы (открытая и лапароскопическая радикальная простатэктомия, брахитерапия, HIFU-терапия), в НИИ урологии внедряется новый высокотехнологичный малоинвазивный способ лечения криоабляция, применяющаяся как при раке простаты, так и доброкачественных и злокачественных опухолях почки. В марте 2010 г. в НИИ урологии одновременно с кафедрой урологии МГМСУ проведены первые в России операции криоабляции при новообразованиях этих органов. Несмотря на инновационность методики, она имеет богатую историю.
ИСТОРИЯ
Применению низких температур в медицине положил начало Джеймс Арнотт в 1845-1851 гг., который с целью обезболивания и лечения опухолевых заболеваний кожи, матки и груди применял аппликации из солевых растворов, смешанных со льдом, достигая температуры до -24оС [1, 2]. Метод получил дальнейшее развитие с применением жидкого СО, который охлаждался при переходе в газообразное состояние, образуя хлопья «снега». Спрессованный в специальные аппликаторы «снег» применялся для лечения заболеваний кожи до 1960х годов. Внедрение внутритканевых металлических аппликаторов позволило применять метод и для лечения опухолей мозга и внутренних органов.
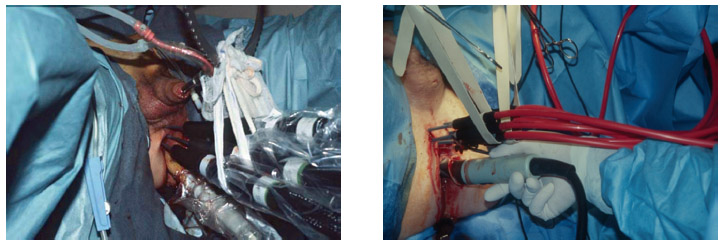
Рисунок 1. Криоаппараты первых поколений. Хорошо видна большая толщина криоигл, ограничивавшая их количество, а значит, и аккуратность заморозки.
В ХХ веке широкое применение приобрел жидкий азот, температура аппликатора достигала -196°С. Первые попытки применения сверхнизких температур при раке простаты были сделаны в 60-х годах прошлого столетия Soanes [3]. В качестве криоагента использовался жидкий азот, а образование льда контролировалось через открытый доступ либо трансуретрально, причем метод применялся как для злокачественных, так и для доброкачественных опухолей. Основным недостатком криохирургических аппаратов того времени (позже их стали называть криомашинами первого поколения) был большой размер криозондов, который вкупе с ограниченными возможностями по их установке и контролю за процессом заморозки в режиме реального времени фактически привел к неприятию метода урологическим сообществом ввиду колоссального количества осложнений [4, 5].
Интерес к криохирургии возродился в начале 90-х годов, чему, безусловно, способствовал технический прогресс в области ультразвуковой визуализации, а также развитие компьютерной техники. Основным отличием второго поколения криохирургической аппаратуры было использование трансректальных ультразвуковых датчиков для контроля за процессом установки криозондов и дальнейшего промораживания. Системы для трансперинеального введения криозондов обозначили перспективность метода, хотя уровень осложнений был все еще достаточно высоким, что объяснялось сложностью контроля за охлаждающим действием жидкого азота, неэффективностью систем подогрева уретры, а также отсутствием данных о температуре тканей [6]. Тем не менее, прогресс не стоял на месте, и вскоре были получены обнадеживающие результаты операций, выполнявшихся с использованием экспериментальных систем прогрева уретры, а также внутритканевых термодатчиков, позволявших контролированно достигать целевую температуру тканей -40 C[7, 8].
В 2000 г. появилось третье поколение криохирургических машин, действие которых основывается на эффекте Джоуля-Томпсона. Суть эффекта заключается в изменении температуры окружающей среды при расширении некоторых газов. Так, аргон при переходе из состояния высокого давления (20 Мпа в баллоне) в низкое давление (0,1 Мпа на кончике криозонда) способен охлаждаться до -185oG Криозонд представляет собой закрытый контур, и аргон возвращается в криомашину, откуда выходит в окружающий воздух. Гелий в тех же условиях, наоборот, нагревается до 67oQ позволяя производить активное оттаивание после каждого из циклов заморозки [9] (рисунок 2). Оба газа инертны и не представляют опасности для находящихся в операционной.
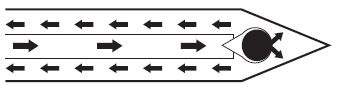
Рисунок 2. Газ под высоким давлением идет по внутреннему контуру, на конце которого проходит через узкое устье, попадает в зону относительно большего объема на кончике термозонда, где и происходит его охлаждение (аргон) или нагревание (гелий). Газ по внешнему контуру возвращается в криомашину, откуда стравливается в окружающую атмосферу.
С этого момента исторически высокие показатели побочных явлений пошли на спад, а разработка термодатчика с точечным термосенсором на конце иглы позволила контролировать и корректировать процесс заморозкив режиме реального времени. Вместе с тем, было разработано компьютерное обеспечение, дававшее возможность предоперационного моделирования роста «ледяного шара» и внесения определенных корректив до введения криозондов в тело пациента.
Американская урологическая ассоциация (AUA) исключила криоабляцию простаты из списка экспериментальных методов в 1996 г., и с этого момента она начала использоваться в основном для лечения пациентов с рецидивом заболевания после лучевой терапии [10]. С накоплением опыта процедура стала все шире применяться у первичных больных и сегодня занимает заслуженное место среди малоинвазивных методик лечения рака предстательной железы.
В настоящее время в аппаратах 3-го поколения толщина криозондов составляет 17Ga, что соответствует диаметру биопсийной иглы. Маленький размер позволяет разместить до 12-14 криозондов в промежности, а вариабельный объем заморозки обеспечивает достаточно точный захват опухоли или органамишени с минимальным воздействием на здоровые ткани. Контроль температуры осуществляется трансректальным УЗ-датчиком, термосенсорами, измеряющими температуру как в зоне интереса, так и в окружающих тканях, таким образом, возможна интраоперационная коррекция степени промораживания, способствующая сохранению невовлеченных в опухолевый процесс структур. Дополнительно при криоабляции простаты по уретре устанавливается специальный обогревающий катетер, предотвращающий некроз тканей мочеиспускательного канала.
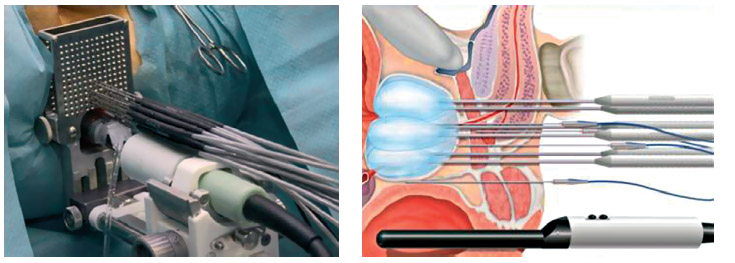
Рисунок 3. Аппарат 3-го поколения. Криозонды 17G установлены через стандартную решетку для брахитерапии. На схеме справа хорошо виден термосенсор (нижняя из игл), установленный в области фасции Денонвилье, контроль температуры в этой зоне позволяет избежать последующих осложнений, связанных с прямой кишкой.
КРИОБИОЛОГИЯ
Повреждающий эффект обусловлен обязательным чередованием фаз замораживания (быстрое) и оттаивания (медленное) и основывается на сочетании трех патогенетических механизмов.
1. Непосредственный цитотоксический эффект
При снижении температуры до -15°С во внеклеточном пространстве формируются ледяные кристаллы, что повышает осмотическое давление дегидратированной экстрацеллюлярной жидкости. Внутриклеточная жидкость устремляется наружу, формируя гиперосмолярную токсичную среду внутри клетки, разрушающую нормальную жизнедеятельность клетки. При дальнейшем снижении температуры до -40^ формируется внутриклеточный лед, разрывающий мембраны органелл и самой клетки. До 90% клеточных мембран необратимо разрушаются уже после первой заморозки. При последующем оттаивании клетки с гиперосмолярным содержимым, чьи мембраны еще способны к транспорту воды, набирают жидкость и разрушаются либо под воздействием гипергидратации, либо от формирования внутриклеточного льда в следующем цикле заморозки. При этом приоритетный механизм клеточной гибели также зависит от скорости заморозки: чем выше скорость, тем больше количество клеток, погибших от внутриклеточной кристаллизации. Тем не менее, независимо от скорости ее достижения, температура -40^ является летальной, особенно цитотоксический эффект выражен у опухолевых клеток, для которых характерен более высокий обмен веществ. Размораживание, наоборот, должно происходить медленнее, т.к. при этом клеточная дегидратация выражена в большей степени [11, 12, 13, 14, 15].
2. Сосудистые реакции
Впервые корреляцию между замораживанием и повреждающей сосудистой реакцией выявил Cohnheim в 1877 г. [16]. Он предположил, что некроз в замороженной, а затем оттаявшей ткани был вызван тромбозом после оттаивания. Позднее его предположения были подтверждены Lewis [17] и другими учеными, доказавшими, что именно такие явления, как повышенная отечность тканей, стаз и дальнейший тромбоз мелких сосудов приводят к некрозу после цикла заморозки/ оттаивания опытного образца ткани.
Marzella на экспериментах с замораживанием ушей кроликов обратил внимание на важную роль холодового повреждения эндотелия в развитии дальнейшей сосудистой реакции [18]. Эндотелий разрушался при заморозке, а при оттаивании отмечалась немедленная тромбоцитарная агрегация, одновременно с которой начиналось накопление межклеточной жидкости и активация нейтрофилов. Через 6 часов начиналась экстравазация эритроцитов, а через сутки расслоение эндотелия.
3. Иммунная реакция
Различные авторы предлагают несколько теорий иммунной реакции. Первая это образования антител к опухоли [19].
После гибели опухолевой клетки высвобождаются внутриклеточные антигены, которые захватываются антиген-представляющими клетками иммунной системы. В-лимфоциты со специфическими к этим антигенам антителами трансформируются в плазматические клетки. Выработка антител индуцирует фиксацию комплемента, вызывая хемотаксис нейтрофилов и макрофагов. Эти клетки высвобождают свободные радикалы и ферменты, которые уничтожают оставшиеся опухолевые клетки.
Другая теория предполагает развитие иммунной реакции посредством индуцирования цитотоксических T-лимфоцитов. Обычно внутриклеточные антигены представляются на клеточной мембране и распознаются цитотоксическими T-клетками, которые высвобождают энзимы, убивая клетку. Предполагается, что замораживание тканей сенсибилизирует цитотоксические Т-лимфоциты или усиливает презентацию антигенов. В исследовании Eskandari пик активации Т-клеток приходился на 14-е сутки после криоабляции опухоли R3327 у лабораторных крыс, и остается повышенным по сравнению с контрольной группой [20].
Третья теория предполагает стимуляцию natural killer клеток в результате действия сверхнизкой температуры, хотя корреляция между этими процессами еще недостаточно исследована. Тем не менее, ответ иммунной системы на криохирургию больше похож на клеточно-зависимый. Так, была отмечена реакция на аденокарциному простаты R3327, в то время как для аденокарциномы молочной железы MRMT-1 подобного эффекта зарегистрировано не было [21].
Не исключается, что для формирования иммунного ответа необходимо определенное количество антигена. Если концентрация антигена превышает определенный порог, может возникнуть иммуносупрессия. Так, Roy отметил, что выживаемость животных заметно уменьшалась при увеличении количества вводимого им вещества промороженной опухоли [22].
В настоящее время принята следующая схема проведения криоабляции:
- цикл заморозки (конечная температура не выше -40o0 в таргетной зоне);
- цикл медленного оттаивания (конечная температура +5-10oQ;
- второй цикл заморозки/оттаивания с теми же параметрами.
После первого цикла заморозки/ оттаивания погибает большая часть клеток, оставшиеся клетки становятся крайне уязвимыми вследствие описанных выше процессов, и второй цикл позволяет практически полностью уничтожить все клетки в зоне криовоздейтвия [23].
КРИОАБЛЯЦИЯ ПРОСТАТЫ: ПОКАЗАНИЯ
Показаниями к криоабляции рака простаты являются [24]:
- локализованный рак предстательной железы;
- локальный рецидив после радикальной простатэктомии или лучевой терапии (Salvage therapy);
- лечение местных осложнений (гематурия, обструкция и т.д.) распространенного заболевания.
Результаты криоабляции простаты зависят от тех же факторов, которые определяют успех других видов лечения: стадии заболевания, гистологической градации по Глисону, уровня ПСА до лечения и объема опухоли. Идеальными кандидатами являются больные со стадией T1-T2a, суммой Глисона до 6 и уровнем ПСА до 10 нг/мл [25].
Некоторые исследователи предполагают, что у пациентов с локализованным процессом, но высоким риском экстракапсулярной инвазии (Т2b/T2c, Глисон > 7 или ПСА выше 10 нг/мл) криохирургия может показать результаты лучше, чем радикальная простатэктомия или лучевая терапия, т.к. ледяной шар распространяется и на перипростатическую клетчатку. Метод также предлагается как метод выбора для пациентов с местнораспространенным заболеванием. Тем не менее, в обоих случаях применение неоадъювантной гормональной терапии является обязательным [26, 27].
Еще одним важным критерием отбора является объем простаты. Увеличение железы более 50см3 требует большего количества газа, повышает риск осложнений и увеличивает время процедуры. В этих случаях рекомендуется применение агонистов ЛГРГ на предоперационном этапе с целью уменьшения объема простаты и проведения процедуры в оптимальных условиях [28].
Особую и достаточно большую группу составляют пациенты с рецидивом заболевания после радикальной простатэктомии, лучевых методов или криотерапии. У этих пациентов риск развития осложнений намного выше, что обязывает нас соблюдать строгие критерии применения данного метода и выбирать пациентов, которым этот метод может действительно помочь. Локальный рецидив должен быть подтвержден гистологически или данными томографии (МРТ, КТ). Необходимо исключить генерализацию опухоли, что должно сопровождаться показателями ПСА < 20нг/мл, Глисон < 8, медленным ростом ПСА после лечения, отрицательными результатами остеосцинтиграфии и ожидаемой продолжительностью жизни более 10 лет [29]. Некоторые исследователи предлагают выполнение лапароскопической тазовой лимфодиссекции для точного стадирования болезни [30]. Также криоабляция может использоваться как паллиативное лечение у пациентов с диссеминированным заболеванием в случае возникновения у них массивной гематурии или инфравезикальной обструкции [10].
Относительными противопоказаниями для криоабляции простаты являются стриктуры и воспалительные заболевания прямой кишки, ампутация прямой кишки и ТУР простаты в анамнезе [31].
РЕЗУЛЬТАТЫ
В отличие от лучевой терапии [32] и радикальной простатэктомии [33], биохимические критерии эффективности для криотерапии все еще не определены. Существует несколько публикаций по результатам криохирургии простаты, однако все они используют разные цифры ПСА в качестве опорной точки. Long [34] описывает 5-летние результаты наблюдения за 975 пациентами, прооперированными в различных центрах, в котором критерием безрецидивной выживаемости обозначен уровень ПСА < 0,5 нг/мл и 1,0 нг/мл.
Bahn [24] в качестве контрольных показателей использовал ПСА 0,1 нг/мл и < 0,3 нг/мл и критерий ASTRO (Американское общество лучевых терапевтов и онкологов). Помимо этих, исследователями использовались также критерии Phoenix и ряд других показателей ПСА.
Один из последних отчетов из реестра COLD (Cryo On-Line Data крупнейший реестр больных, подвергшихся криоабляции) указывает на корреляцию между безрецидивной выживаемостью и уровнем послеоперационного ПСА у 2427 первичных пациентов с раком простаты [35]. Анализ полученных данных показал, что 80,2% наблюдаемых достигли послеоперационного уровня ПСА < 0,6 нг/мл. Основываясь на критерии Phoenix, 5-летняя безрецидивная выживаемость для групп низкого, среднего и высокого риска составила 86%, 67% и 51% соответственно. У больных с послеоперационным уровнем ПСА > 0,6нг/мл частота развития биохимического рецидива в течение 2 лет составила 29,5% независимо от группы риска. Cohen [36] проанализировал данные 10-летнего наблюдения за 204 пациентами, для которых криоабляция также использовалась в качестве первичного метода лечения. Используя критерии Phoenix, исследователи получили следующие результаты безрецидивной выживаемости (10 лет): 80,56%, 74,16% и 45,54% для групп низкой, средней и высокой степени риска соответственно. Таким образом, несмотря на отсутствие четких критериев биохимического рецидива, можно отметить, что чем ниже послеоперационный ПСА, тем выше вероятность его дальнейшей стабильности и выше число негативных результатов биопсий.
В начале 1990-х годов криоабляция применялась в основном при рецидиве рака простаты после хирургического и лучевого лечения. Большое количество осложнений «спасительной» простатэктомии заставило многих обратить внимание на этот молодой метод, хотя ранние результаты не были многообещающими послеоперационная обструкция встречалась у 67%, а уровень недержания мочи доходил до 100% [37].
По данным, представленным Pisters, из 150 пациентов, получавших в качестве первичного метода лечения лучевую терапию с/или без неоадьювантной гормональной терапии, у 60% была диагностирована стадия Т3 и выше, а у 59% сумма Глисона 8-10. После криоабляции биохимический рецидив был выявлен у 58%, у 31% ПСА не превышал 0,1нг/мл, у 11% 0,2 нг/мл. При этом биохимический рецидив наблюдался реже в группе, которая получала лучевое лечение в качестве монотерапии (54%), в то время как у пролеченных комбинированной терапией (+гормональное лечение) рецидивирование отмечалось достоверно чаще (71%) [10].
Izawa в своем исследовании эффективности криоабляции у 131 больного с рецидивом рака получил схожие результаты: безрецидивная выживаемость после монотерапии была выше, чем после комбинированной (48% против 22% соответственно). Пятилетняя безрецидивная выживаемость в среднем составила 40% [38].
Bahn представил анализ 7-летнего наблюдения за 59 пациентами с рецидивом после лучевой и комбинированной терапии. Безрецидивная выживаемость (определяемая по ПСА) составила 59% (ПСА < 0,5) и 69% (ПСА < 1,0нг/мл) [39].
Таблица 1. Безрецидивная выживаемость первичных больных в зависимости от критериев биохимического рецидива, выбранных разными авторами
| Исследование | Количество пациентов | Критерий (ПСА) | Безрецидивная выживаемость для разных степеней риска (%) | Время наблюдения (мес.) |
| Levy et al 2009 | 2427 | Phoenix <0,1 <0,5 >0,6 |
Низкая 91,8 Средняя 76 Высокая 71 Низкая 86 Средняя 67 Высокая 51 Низкая 70.5 Средняя 56 Высокая 47 |
60 |
| Jones et al 2008 | 1198 | ASTRO Phoenix |
Низкая 85 Средняя 73 Высокая 75 Низкая 91 Средняя 79 Высокая 62 |
60 |
| Prepelica et al 2005 | 65 | ASTRO <0,4 <1,0 |
Высокая 82 Высокая 50 Высокая 35 |
72 |
| Long et al. 2001 | 975 | <0,1 <0,5 |
Низкая 76 Средняя 71 Высокая 61 Низкая 60 Средняя 61 Высокая 36 |
60 |
| Bahn et al 2002 | ASTRO <0,1 <0,3 |
Низкая 92 Средняя 89 Высокая 89 Низкая 87 Средняя 79 Высокая 71 Низкая 61 Средняя 68 Высокая 61 |
84 | |
| Cohen et al. 2008 | 204 | Phoenix | Низкая 81 Средняя 74 Высокая 46 |
120 |
Таблица 2. Безрецидивная выживаемость больных, перенесших «спасительную» криоабляцию
| Количество пациентов | Безрецидивная выживаемость, % (мес. наблюдения) | Критерий (ПСА) | |
| Izawa et al. | 131 | 40 (60) | < 2 |
| Bahn et al. | 59 | 59 (72) 69 (72) |
< 0,5 < 1 |
| Ghafar et al. | 38 | 86 (12) 74 (24) |
< 0,3 < 0,3 |
ОСЛОЖНЕНИЯ
Самые подробные данные об осложнениях содержатся в реестре COLD. В случае использования криоабляции у первичных больных задержка мочи наблюдалась у 43 из 1198 пациентов (3,6%). У 18 из 43 проблема была решена при помощи катетеризации, а оставшимся 25 (2,1%) была выполнена ТУР простаты для удаления некротизированных «бахромчатых» тканей. Уретроректальный свищ зарегистрирован у 0,4%, а недержание составило 4,8%, при этом прокладками пользуются 2,9%. Самым частым осложнением является импотенция. Из 354 пациентов, имевших потенцию до процедуры, 25,2% продолжили половую жизнь, но только 8,8% способны провести половой акт без фармакологической или иной поддержки [35].
У пациентов с биохимическим рецидивом заболевания после других методов лечения криоабляция вызывает большее количество осложнений, что ожидаемо. Так, если считать даже незначительное подтекание мочи недержанием, то при использовании систем обогрева уретры в первый год данное осложнение
встречается в 47% случаев, но имеет тенденцию к снижению с течением времени [40]. Обструкция вследствие образования «бахромчатой» уретры, по данным разных авторов, наблюдается в пределах 3-9%, а формирование уретроректального свища в 0-3% случаев [9, 37].
ЗАКЛЮЧЕНИЕ
Благодаря постоянному развитию технического обеспечения криохирургических операций, количество осложнений значительно уменьшилось по сравнению с ранними результатами, тем не менее, в связи с высоким риском развития эректильной дисфункции метод в большей степени применим к пациентам более старшего возраста. Будучи относительно новой методикой лечения рака предстательной железы, криоабляция показала свою эффективность с хорошими результатами специфической выживаемости и биохимического контроля заболевания. Большинство авторов не пришли к консенсусу по биохимическим критериям успешности процедуры, разработка этих критериев является первостепенной задачей. Следует отметить возможность проведения повторных процедур криоабляции, а также применимость в случае рецидива после других методов (хирургических, лучевых). Эффективность во многом зависит от правильного отбора пациентов со строгим соблюдением техники выполнения на всех этапах операции, а также динамическим контролем температуры в зоне операции и окружающих тканях.
Ключевые слова: рак предстательной железы, криоабляция, криохирургическая аппаратура, патофизиология криотерапии, осложнения.
Keywords: рrostate cancer, cryoablation, cryosurgical apparatus, pathophysiology of cryotherapy, complication.
ЛИТЕРАТУРА
- Arnott J. On the Treatment of Cancer by the Regulated Application of an Anaesthetic Temperature./London: Churchill, 1851.
- Bird H. James Arnott, MD (Aberdeen), 1797-1883, a pioneer in refrigeration //Anaesthesia. 1949. Vol.4. P. 10-17.
- Soanes W.A., Gonder M.J., Shulman S. Apparatus and technique for cryosurgery of the prostate // J Urol. 1966. Vol. 96. P. 508-511.
- Gonder M.J., Soanes W.A., Shulman S. Cryosurgical treatment of the prostate // Invest Urol. 1966. Vol. 3. P. 372-8.
- Loening S.A., Bonney WW., Fallon B. Cryotherapy // Prostate. 1984. Vol.5. P. 199-205.
- Chang Z., Finkelstein J.J., Ma H., Baust О. Development of a high-performance multiprobe cryosurgical device // Biomed Instrum Technol. 1994. Vol. 28. P. 383-390.
- Cohen J.K., Miller R.J., Shuman B.A. Urethral warming catheter for use during cryoablation of the prostate // Urology. 1995. Vol. 45. P. 861-864.
- Zisman A., Pantuck A.J., Cohen J.K., Belldegrun A.S. Prostate cryoablation using direct transperineal placement of ultrathin probes through a 17-gauge brachytherapy template technique and preliminary results // Urology 2001. Vol. 58. P.988-993.
- Ghafar M.A., Johnson C.W., de la Taille A., Benson M.C., Bagiella E., Fatal M. Olsson CA, Katz AE. Salvage cryotherapy using an argon based system for locally recurrent prostate cancer after radiation therapy: the Columbia experience // J Urol. 2001. Vol. 166. P.13331338.
- Pisters L.L., von Eschenbach A.C., Scott S.M., Shellie M., Swanson D.A., Dinney C.P., Pettaway C.A., Babaian R.J. The efficacy and complications of salvage cryotherapy of the prostate // J Urol. 1997. Vol. 157. P. 921-925.
- Baust J.G., Gage A.A. The molecular basis of cryosurgery // BJU International. 2005. Vol. 95. P. 1187-1191.
- Rubinsky B. The freezing process and mechanism of tissue damage. / In: Onik G., Rubinsky B., Watson G., et al., editors. Percutaneous Prostate Cryoablation. St Louis: Quality Medical Publishing; 1999.
- Mazur P. Kinetics of water loss from cells at subzero temperatures and the likelihood of intracellular freezing // J Gen Physiol. 1963. Vol. 47. P. 347-369.
- Steponkus P.L., Lynch D. V. Freeze/thaw induced destabilization of the plasma membrane and the effects of cold acclimation // J Bioenerg Biomembr. 1989. Vol. 21. P. 21-41.
- Mazur P. The role of cell membranes in the freezing of yeast and other single cells // Ann NY Acad Sci. 1965. Vol. 125. P. 658-676.
- Cohnheim J. Lectures on general pathology: A handbook for practitioners and students. /London: The New Sydenham Society. 1889 p.
- Lewis T., Love W.S. Vascular reactions of the skin to injury. Part III. Some effects of freezing, of cooling, and of warming //Heart. 1926. Vol. 13. P. 27-60.
- Marzella L., Jesudass R.R., Manson P.N., Myers R.A., Bulkley G.B. Morphologic characterization of acute injury to vascular endothelium of skin after frostbite //Plast Reconstr Surg. 1989. Vol. 83. P. 67-76.
- Grana L., Kidd J., Swenson O. Cryogenic techniques within the tracheobronchial tree // J Cryosurg. 1969. Vol. 2. P. 62-67.
- Eskandari H., Ablin R.J., Bhatti R.A. Immunologic responsiveness & tumour growth of the Dunning R3327 rat prostatic adenocarcinoma following cryosurgery & orchiectomy //Indian J Exp Biol. 1982. Vol. 20. P. 872-874.
- Matsumura K., Sakata K., Saji S., Misao A., Kunieda T. Antitumor immunologic reactivity in the relatively early period after cryosurgery: Experimental studies in the rat // Cryobiology. 1982. Vol. 19. P. 263-272.
- Roy A., Lahiri S., Lahiri P., Pal S., Ghosh S., Roy B. Immunologic and survival studies in mice immunised with cryodestroyed ascites fibrosarcoma (AFS) cells // Indian J ExpBiol. 1990. Vol. 28. P. 1026-1030.
- Gage A.A., Baust J. Mechanisms of tissue injury in cryosurgery // Cryobiology. 1998. Vol. 37. P. 171.
- Bahn D.K., Lee F., Badalament R., Kumar A., Greski J., Chernick M. Targeted cryoablation of the prostate: 7-year outcomes in the primary treatment of prostate cancer // Urology. 2002. Vol. 60, suppl 2A. P. 3-11.
- Han K.R., Belldegrun A.S. Third-generation cryosurgery for primary and recurrent prostate cancer // BJU. 2004. Vol. 93. P. 14-18.
- Prepelica K.L., Okeke Z., Murphy A., Katz A.E. Cryosurgical Ablation of the Prostate: High-Risk Patient Outcomes // Cancer. 2005. Vol. 103. P.1625-1630.
- Koppie T.M., Shinohara K., Grossfeld G.D., Presti J.C., Carroll P.C. The efficacy of cryosurgical ablation of prostate cancer: the University of California San Francisco experience // J Urol. 1999. Vol. 162. P. 427-432.
- Rees J., Patel B., Macdonagh R., Persad R. Cryosurgery for prostate cancer //BJU. 2004. Vol. 93. P. 710-714.
- Ahmed S., Lindsey B., Davies J. Salvage cryosurgery for locally recurrent prostate cancer following radiotherapy // Prostate Cancer and Prostatic Diseases. 2005. Vol. 8. P. 31-35.
- Da la Taille A., Katz A.E. Cryosurgery: is it an effective option for patients failing radiation? // Curr Opin Urol. 2000. Vol. 10. P. 409-413.
- Shinohara K. Prostate cancer: cryotherapy // Urol Clin N Am. 2003. Vol. 30. P. 725-736.
- Roach M. 3rd, Hanks G., Thames H. Jr., Schellhammer P., Shipley WU., Sokol G.H., Sandler H. Defining biochemical failure following radiotherapy with or without hormonal therapy in men with clinically localized prostate cancer: recommendations of the RTOGASTRO Phoenix Consensus Conference // Int J Radiat Oncol Biol Phys. 2006. Vol. 65. № 4. P. 965-974.
- Cookson M.S., Aus G., Burnett A.L. Variation in the definition of biochemical recurrence in patients treated for localized prostate cancer: the American Urological Association Prostate Guidelines for Localized Prostate Cancer Update Panel report and recommendations for a standard in the reporting of surgical outcomes // J Urol. 2007. Vol. 177. № 2. P. 540-545.
- Long J.P., Bahn D., Lee F., Shinohara K., Chinn D.O., Macaluso J.N. Jr. Five-year retrospective, multi-institutional pooled analysis of cancer-related outcomes after cryosurgical ablation of the prostate // Urology. 2001. Vol. 57. № 3. P. 518-523.
- Levy D.A., Pisters L.L., Jones J.S. Primary cryoablation nadir prostate specific antigen and biochemical failure // J Urol. 2009. Vol. 182. № 3. P. 931-937.
- Cohen J.K., Miller R.J. Jr., Ahmed S., Lotz M.J., Baust J. Ten-year biochemical disease control for patients with prostate cancer treated with cryosurgery as primary therapy // Urology. 2008. Vol. 71. № 3. P. 515-518.
- Bales G.T., Willians M.J., Sinner M., Thisted R.A., Chodak G.W. Short-term outcomes after cryosurgical ablation of the prostate in men with recurrent prostate carcinoma following radiation failure // Urology. 1995. Vol. 46. P. 676-680.
- Izawa J.I., Madsen L.T., Scott S.M., Tran J.P., McGuire E.J., von Eschenbach A.C, Pisters L.L. Salvage cryotherapy for recurrent prostate cancer after radiotherapy: variables affecting patient outcome // J Clin Oncol. 2002. Vol. 20. P. 2664-2671.
- Bahn D.K., Lee F., Silverman P., Bahn E., Badalament R., Kumar A, Greski J., Rewcastle J.C. Salvage cryosurgery for recurrent prostate cancer after radiation therapy: a sevenyear follow-up // Clin Prostate Cancer. 2003. Vol. 2. P. 111-114.
- Perrotte P., Litwin M.S., McGuire E.J., Scott S.M., von Eschenbach A.C., Pisters L.L. Quality of life after salvage cryotherapy: the impact of treatment parameters // J Urol. 1999. Vol. 162. P. 398-402.















































































