Необходимость комплексного подхода к обследованию и лечению больных хроническим абактериальным простатитом
 3416
3416 В последние годы много внимания уделяют хроническому простатиту (ХП) — заболеванию, имеющему наряду с медицинским огромное социальное значение. Больные ХП — преимущественно активные мужчины репродуктивного возраста. ХП не представляет непосредственной угрозы жизни, но существенно снижает ее качество, поскольку отрицательно влияет на семейные взаимоотношения, работоспособность и т.д. ХП составляет до 40% в структуре урологического приема частных медицинских центров [1]. Несмотря на многокомпонентную длительную терапию, заболевание склонно к рецидивированию [2].
Согласно классификации Национального Института Здоровья (NIH) США, ХП категории III-а подразумевает наличие клинической и лабораторной симптоматики ХП, т.е. в секрете предстательной железы (ПЖ) присутствует повышенное количество лейкоцитов, хотя роста микробной флоры нет. Сам факт асептического воспаления в данном случае весьма сомнителен, скорее всего имеет место неполное оснащение бактериологических лабораторий [3, 4]. Кроме того, пациенты, относящиеся к категории III-а, в своей жизни получили не один курс антибактериальной терапии, что могло привести к трансформации микроорганизмов в L — формы, не дающие роста на обычных стандартных средах и персистенции их в паренхиме железы [5-7].
Считается, что в структуре ХП до 80-90% приходится на абактериальную форму заболевания (категория III-а). Для признания хронического простатита бактериальным необходимо обнаружение в специфическом для ПЖ материале (секрет, порция мочи после массажа, эякулят) при повторных обострениях (рецидивах) преимущественно одного и того же патогенного бактериального возбудителя (в особенности — отличного от микрофлоры уретры и других отделов мочевого тракта) [8].
Однако в последнее время эта точка зрения пересматривается. Во-первых, появились новые технологии, позволяющие обнаружить новые микроорганизмы в дериватах половых желез (правда, пока что их патогенная роль не доказана) [3,9-11]. Во-вторых, стали признавать внутриклеточных возбудителей этиологическим фактором ХП [2,7,12-13].
Кроме того, отсутствие роста банальной микрофлоры при воспалении любого отдела урогенитального тракта может свидетельствовать о туберкулезе [14]. В Российской Федерации эпидемическая ситуация в отношени туберкулеза во многих регионах остается напряженной [15-18], и диагностическое значение «асептического воспаления» не утратило своей актуальности.
Иммуномодуляторы широко применяют в лечении многих инфекционных заболеваний урогенитального тракта [19], а в случае, например, вируса папилломы человека они являются препаратом выбора, поскольку этиотропной терапии для аногенитального папилломатоза не существует [20]. Любое хроническое воспаление сопровождается снижением иммунитета. Иммунотропные препараты позволяют компенсировать этот дефект, что подтверждено многими исследованиями [21-25]. Однако эффективность комплексного лечения больных хроническим абактериальным простатитом с использованием иммуномодуляторов изучена недостаточно.
Цель исследования — доказать присутствие того или иного патогена в деривате половых желез у больных хроническим абактериальным простатитом и эффективность комплексной терапии с использованием иммуномодулятора (панавир) у этих больных.
Дизайн исследования: нерандомизированное сравнительное двунаправленное случай-контроль.
МАТЕРИАЛ И МЕТОДЫ
В исследование включили две группы больных абактериальным ХП категории III-а по 28 пациентов в каждой. Основную группу (ОГ) набирали проспективно, группу сравнения (ГС) — ретроспективно.
Критерии включения:
- Возраст от 18 до 60 лет;
- Сумма баллов по шкале NIH-CPSI (National Institute of Health Chronic Prostatitis Symptom Index) не менее 15 в течение не менее шести месяцев;
- Наличие в нативном препарате секрета ПЖ, полученном путем изгоняющего массажа предстательной железы, не менее 15 лейкоцитов в поле зрения при световой микроскопии;
- Отсутствие роста патогенной микрофлоры в секрете ПЖ / эякуляте;
- Согласие на участие в исследовании (для ОГ).
Критерии исключения:
- Возраст моложе 18 и старше 60 лет;
- Любые онкологические заболевания;
- Любые соматические заболевания в стадии обострения или декомпенсации;
- ВИЧ-инфекция в любой стадии;
- Алкоголизм и наркомания;
- Наличие инородных тел в мочевом пузыре;
- Бессимптомное течение заболевания или сумма баллов по шкале NIH-CPSI менее 15;
- Рост патогенной микрофлоры в секрете ПЖ / эякуляте в титре более 103 КОЕ/мл.
Все пациенты проходили стандартное обследование, включавшее определение простатоспецифического антигена (ПСА), 3-стаканную пробу мочи, биохимический анализ мочи, пальцевое ректальное исследование (ПРИ) ПЖ. Всем выполняли клиническое и бактериологическое исследование секрета ПЖ. Также больные самостоятельно заполняли опросник NIH-CPSI, переведенный на русский язык.
Видовую идентификацию микроорганизмов проводили методом время пролетной масс-спектрометрии и на микробиологическом анализаторе Phoenix 100 (BectonDickinson, США). Исследование соскоба уретры на Chlamydia trachomatis, Mycoplasma genitalium, Ureaplasma parvum и urealythicum, на Mycobacterioum tuberculosis, а также на вирусы (вирус герпеса и папилломы человека без типирования) выполняли методом полимеразной цепной реакции (ПЦР).
Все пациенты, у которых были выявлены внутриклеточные возбудители, получали антибактериальную терапию доксициклином (юнидокс солютаб) в дозе 300 мг однократно в первый день, и затем по 100 мг дважды в день в течение 14 дней. Девять больных, у которых был обнаружен вирус герпеса, принимали фамцикловир (фамилар) по 250 мг трижды в день в течение 10 дней. Учитывая выраженную интенсивность боли, все пациенты также принимали кетопрофен (фламакс-форте) по 100 мг однократно в день в течение 7 дней. С целью миорелаксации и улучшения аггрегации эритроцитов пациенты обеих групп принимали бенциклон (галидор) по 100 мг дважды в день в течение двух недель. Таким образом, базовая этиопатогенетическая терапия была идентичной.
Также пациентам основной группы дополнительно был проведен курс лечения панавиром внутривенно по 5 мл болюсно, по схеме:
первые 3 инъекции через 24 часа, 4-5 инъекции — через 48 часов. То есть панавир вводили пациентам основной группы в 1-й, 3-й, 5-й, 8-й и 11-й день лечения.
Обследование проводили до начала лечения, через 10±1 дней для оценки переносимости панавира, через 15±2 дня для оценки непосредственных результатов комплексного лечения, через 90±3 дней для оценки результатов. При контрольном обследовании через две недели исследовали секрет ПЖ методом световой микроскопии нативного мазка и анализировали повторно заполненные опросники, а весь спектр обследования повторяли через 3 месяца, степень эрадикации возбудителя оценивали методом ПЦР.
Статистическая обработка результатов проведена на персональном компьютере с помощью пакетов статистических программ Microsoft Ехсеl 2007 и StatistiGa for Windows 6.0. Определяли среднюю арифметическую (х), отклонение от средней арифметической, рассчитывали среднеквадратическое отклонение (а) и среднюю ошибку относительной величины (m). Для решения вопроса о случайности расхождений наблюдаемых средних (относительных) величин производили расчет средней ошибки разности двух средних. Полученные результаты представляли как среднее ± ошибка средней (M±m). Посредством сравнения средних значений двух выборочных совокупностей (М1 и М2) вычисляли t-критерий Стьюдента и определяли уровень значимости р. Статистически значимыми считали различия при р<0,05.
РЕЗУЛЬТАТЫ
Под нашим наблюдением находилось 58 пациентов в возрасте от 24 до 47 лет (в среднем 36±6,9). Давность заболевания колебалась от 4 до 17 лет, в среднем 7,4±2,6 года. Все это время больные наблюдались у уролога с диагнозом «ХП» (без указания категории). Судя по
выпискам из амбулаторных карт, доступных для анализа, при стандартном посеве секрета ПЖ и/или эякулята у всех пациентов результат был отрицательный в течение как минимум шести месяцев до включения в исследование.
При включении в исследование больные отвечали критериям диагноза «хронический простатит категории Ш-а», поскольку у всех пациентов число лейкоцитов в секрете ПЖ превышало 15 в поле зрения, в дериватах половых желез патогенная микрофлора не была обнаружена. Однако молекулярно-генетическими методами у всех пациентов обнаружили ДНК внутриклеточных патогенов: Chlamydia trachomatis (17 пациентов), Ureaplasma urealyticum (15 больных), Mycoplasma genitalium (22 пациента), а также virus Herpes (9 пациентов) и вирус папилломы человека (ВПЧ) у 5 больных (табл. 1). Эти возбудители формально не относятся к этиологическим факторам ХП, тем не менее, поддерживают воспаление в ПЖ.
Таблица 1. Виды внутриклеточных возбудителей, выделенных у пациентов обеих групп до лечения
| Возбудитель | 1-я группа (основная) n=28 | 2-я группа (гр. сравнения) n=28 | Р | ||
|---|---|---|---|---|---|
| абс | % | абс | % | ||
| Chlamydia trachomatis | 9 | 32,1 | 8 | 28,6 | >0,05 |
| Ureaplasma parvum | 5 | 17,6 | 8 | 28,6 | <0,05 |
| Ureaplasma urealiticum | 8 | 28,6 | 7 | 25 | >0,05 |
| Mycoplasma genitalium | 1200,00% | 4290,00% | 1000,00% | 3570,00% | >0,05 |
| Virus Herpes 1 -2 | 900,00% | 3210,00% | 600,00% | 2140,00% | <0,05 |
| Virus Papilloma humanis spp | 5 | 17,6 | 3 | 10,7 | >0,05 |
Сумма выделенных микроорганизмов/вирусов в каждой группе превышает число пациентов/100%, поскольку практически у всех присутствовала ассоциация различных патогенезов, причем у 7 пациентов наряду с уропатогенами был найден вирус герпеса, у двух — вирус герпеса и вирус папилломы человека, у трех — вирус папилломы человека в сочетании с другими внутриклеточными паразитами. У 8 пациентов урогенитальный герпес проявлялся характерными высыпаниями, а у одного была латентная форма инфекции. Все пятеро инфицированных ВПЧ ранее подвергались деструкции папиллом (трое — трижды, двое — дважды); на момент включения в исследование видимые папилломы отсутствовали. Несмотря на существенные различия в частоте выявления Virus Herpes 1-2 и Ureaplasma parvum, мы сочли группы сопоставимыми, поскольку ассоциация патогенов нивелировала это различие.
Ведущей жалобой при обращении была боль в области промежности с иррадиацией в органы мошонки, боль при эякуляции. Интенсивность боли по шкале NIH-CPSI составила в среднем 8,7 балла в группе ОГ и 8,3 — в группе ГС, нарушение мочеиспускания больные оценили в среднем в 4,6 баллов в группе ОГ и в 4,7 балла — в гр. ГС. Качество жизни по шкале симптомов составило 7,6 и 7,8 баллов соответственно. Сумма баллов по шкале NIH-CPSI была в ОГ 20,9, и в группе сравнения — 20,8. Различия результатов анкетирования между группами статистически не достоверны (р>0,05). Сопоставление выраженности симптоматики представлено на рисунке 1.
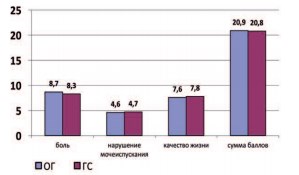
Рис. 1. Выраженность симптомов в баллах по шкале NIH-CPSI у больных ХП
Таким образом, по выраженности симптоматики обе группы больных были идентичны.
Комплексную терапию в течение двух недель завершили все пациенты; незначительные побочные эффекты, не потребовавшие отмены доксициклина, были отмечены у одного пациента в ГС; все пациенты основной группы перенесли внутривенное вливание панавира хорошо.
Через две недели была отмечена положительная динамика по всем параметрам, более выраженная в ОГ. Достоверные различия получены по параметрам «боль», «качество жизни» и по сумме баллов; мочеиспускание улучшилось в обеих группах одинаково. При контрольном обследовании через три месяца вновь достоверно лучшие показатели были отмечены в ОГ. Ни у одного пациента, получавшего иммунотропную терапию, не было обострения заболевания, в то время как в группе сравнения таковых было двое (табл. 2).
Таблица 2. Результаты анкетирования по шкале NIH-CPSI
| Домен | Основная группа | Группа сравнения | р | ||||
|---|---|---|---|---|---|---|---|
| исходно | через 2 нед. | через 3 мес | исходно | через 2 нед. | через 3 мес | ||
| Боль | 8,7 | 3,5* | 2,7** | 8,3 | 4,6* | 4,7** | р1 > 0,05 р2< 0,05 |
| Нарушение мочеиспускания | 4,6 | 2,9* | 1,8** | 4,7 | 3,0* | 3,5 | р1> 0,05 р2< 0,05 |
| Качество жизни | 7,6 | 5,1* | 3,4** | 7,8 | 5,8* | 8,1 | р1> 0,05 р2< 0,05 |
| Сумма баллов | 20,9 | 11,5* | 7,9** | 20,8 | 13,4* | 16,3 | р1> 0,05 р2< 0,05 |
Через три месяца интенсивность боли по шкале NIH-CPSI составила в среднем 2,7 балла в ОГ и 4.7 — в ГС, нарушение мочеиспускания больные оценили в среднем в 1.8 баллов в основной группе и в 3,5 балла — в ГС. Качество жизни по шкале симптомов составило 3,4 и 8,1 баллов соответственно. Сумма баллов была в основной группе снизилась с 20,9 до 7,9, и в группе сравнения — с 20,8 до 16,3.
В ОГ через три месяца после завершения терапии идентифицировали патогены у 5 пациентов (17,8%): ДНК хламидии была обнаружена у двух больных (7,1%), микоплазмы — у трех (10,7%), у одного (3,6%) сохранялся ВПЧ в ассоциации с микоплазмой. В ГС инфекционный агент был найден у 12 больных (42,8%): хламидии по-прежнему присутствовали у трех пациентов (10,7%), уреаплазма суммарно — у 7 (25,0%), и микоплазма -у 4 (14,3%); в 5 случаях сохранялась ассоциация микроорганизмов, том числе в трех — с ВПЧ. Вирус герпеса не определялся ни у одного пациента как в основной, так и в контрольной группе. Эрадикация ВПЧ наступила у трех пациентов из пяти в ОГ, в ГС этот вирус по-прежнему присутствовал у всех пациентов, вошедших в исследование.
Таким образом, в основной группе больных ХП курс комплексной этиопатогенетической терапии привел к эрадикации инфекционного агента у 23-х больных; эффективность лечения составила 82,1%. В группе сравнения у 12 пациентов элиминации возбудителя добиться не удалось; эффективность лечения составила 57,1% (р< 0,05).
ОБСУЖДЕНИЕ
Реальная частота абактериального простатита не известна, поскольку уровень оснащения бактериологических лабораторий и подходы к обследованию пациентов различны не только в разных регионах, но существенно отличаются между государственными клиниками и частными медицинскими центрами. Недооценка внутриклеточных возбудителей и вирусов как этиологического фактора ХП ведет к хронизации заболевания и неудачам в лечении.
Включение в схему этиопатоге-нетической терапии иммуномодулятора существенно повысило эффективность лечения.
Аналогичные эффекты были зарегистрированы при лечении больных папилломавирусной инфекцией (ПВИ) гениталий, которая характеризуется полиморфными многоочаговыми поражениями кожи и слизистых оболочек генитального тракта [2631]. Проведенное нами ранее исследование показало высокую эффективность иммуномодулятора изопринозина у больных хроническим простатитом, инфицированных ВПЧ [20].
Полученные нами данные позволяют утверждать, что, во-первых, под маской абактериального простатита протекает латентно инфекционный. Назвать его бактериальным неправомочно, поскольку выявленные патогены не относятся к классу бактерий. Микоплазма — это грамотрицательный одноклеточный микроорганизм, который является представителем класса молликутов. Он занимает промежуточное положение между грибами, вирусами и бактериями. К классу микоплазм относят и уреаплазмы. Не относятся к бактериям и вирусы. Складывается странная ситуация: возбудители есть, воспаление присутствует, но, поскольку собственно бактерии не выявляют, простатит считается абак-териальным — фактически являясь инфекционным. Таким больным показан особый подход к лечению, поскольку микоплазмы и уреаплазмы располагаются внутриклеточно, и доступны воздействию далеко не каждого антибиотика, в отношении вирусов антибиотики вооще не эффективны. Положение усугубляется преобладанием ассоциаций микроорганизмов; моноинфекция встречается редко. Сказанное выше обусловливает выбор антибактериальных препаратов, способствующих проникать внутрь клетки, в сочетании с иммуномодулатором, способствующим выработке эндогенного интерферона.
ВЫВОДЫ
Больных хроническим абактериальным простатитом категории III-а необходимо обследовать на внутриклеточные инфекции и вирусы, которые также могут поддерживать воспаление ПЖ;
Включение иммуномодулятора в схему стандартной этиопатогенетической терапии больных хроническим «абактериальным» простатитом, ассоциированным с внутриклеточными инфекциями и вирусами, обусловило повышение эффективности на 25,0%.
ЛИТЕРАТУРА
1. Кульчавеня Е.В., Холтобин Д.П., Шевченко С.Ю., Потапов В.В., Зулин Я.В. Частота хронического простатита в структуре амбулаторного урологического приема. Экспериментальная и клиническая урология 2015;(1):16-18.
2. Gasperi M, Krieger JN, Forsberg C, Goldberg J, Buchwald D, Afari N. Chronic prostatitis and comorbid non-urological overlapping pain conditions: A cotwin control study. J Psychosom Res 2017;102:29-33. doi: 10.1016/j.jpsychores.2017.09.005.
3. Xiao J, Ren L, Lv H, Ding Q, Lou S, Zhang W, Dong Z. Atypical microorganisms in expressed prostatic secretion from patients with chronic prostatitis/chronic pelvic pain syndrome: microbiological results from a case-control study. Urol Int 2013;91(4):410-6. doi: 10.1159/000350934.
4. Cai T, Bartoletti R. Re: Park. The presence of Chlamydia is associated
with increased leukocyte counts and pain severity in men with chronic pelvic pain syndrome. Urology 2015;85(6):1522-3. doi: 10.1016/ j.urology.2015.03.023.
5. Pasini M, Kotarski V, Skerk V, Markotic A, Andrasevic AT, Lepej S2, et al. The significance of Chlamydia trachomatis in prostatitis syndrome. J Chemother 2014;26(6):382-4. doi: 10.1179/1973947814Y.0000000165.
6. Cai T, Pisano F, Magri V. Chlamydia trachomatis infection is related to premature ejaculation in chronic prostatitis patients: results from a crosssectional study. J Sex Med 2014;11(12):3085-92. doi: 10.1111/jsm.12699.
7. Park H, Sim SM, Lee G. The presence of Chlamydia is associated with increased leukocyte counts and pain severity in men with chronic pelvic pain syndrome. Urology 2015;85(3):574-9. doi: 10.1016/ j.urology.2014.11.008.
8. Naber KG, Bergman B, Bishop MC, Bjerklund Johansen TE, Botto H, Lobel B, et al. EAU Guidelines on urinary and male genital tract infections. 2002. P. 49-55. URL: https://uroweb.org/wp-content/uploads/ URINARY-AND-MALE-GENITAL-TRACT-INFECTIONS-2001.pdf
9. Olin SJ, Bartges JW Urinary tract infections: treatment/comparative therapeutics. Vet Clin North Am Small Anim Pract. 2015;45(4):721-46. doi: 10.1016/j.cvsm.2015.02.005.
10. La Vignera S, Vicari E, Condorelli RA, Franchina C, Scalia G, Morgia G et al. Prevalence of human papilloma virus infection in patients with male accessory gland infection. Reprod Biomed Online 2015;30(4):385-91. doi: 10.1016/j.rbmo.2014.12.016.
11. Naumenko V, Tyulenev Y, Kurilo L, Shileiko L, Sorokina T, Evdokimov V et al. Detection and quantification of human herpes viruses types 4-6 in sperm samples of patients with fertility disorders and chronic inflammatory urogenital tract diseases. Andrology. 2014;2(5):687-94. doi: 10.1111/j.2047-2927.2014.00232.x.
12. Papes D, Pasini M, Jeroncic A, Vargovic M, Kotarski V, Markotic A, Skerk V. Detection of sexually transmitted pathogens in patients with chronic prostatitis/chronic pelvic pain: a prospective clinical study. Int J STD AIDS 2017;28(6):613-615. doi: 10.1177/0956462417691440.
13. Sanchez LR, Breser ML, Godoy GJ, Salazar FC, Mackern-Oberti JP, Cuffini C, et al. Chronic infection of the prostate by chlamydia muridarum is accompanied by local inflammation and pelvic pain development. Prostate 2017;77(5):517-529. doi: 10.1002/pros.23291.
14. Кульчавеня Е. В., Краснов В.А., Мордык А.В. Альманах внелегоч-ного туберкулеза. Новосибирск: Сибпринт, 2015. — 247 с.
15. Kulchavenya E. Extrapulmonary tuberculosis: are statistical reports accurate? Ther Adv Infect Dis 2014; 2(2) 61-70: doi: 10.1177/2049936114528173
16. Осадчий А.В., Кульчавеня Е.В., Рейхруд Т.А., Нарышкина С.Л., Кожевникова Е.В., Хомяков В.Т. Социально-демографическая характеристика больных туберкулезом легких и внелегочных локализаций. Туберкулез и болезни легких 2015;(2):46-48.
17. Кульчавеня Е.В., Ковешникова Е.Ю., Жукова И.И. Клинико-эпидемиологические особенности современного туберкулезного спондилита. Туберкулёз и болезни лёгких 2013;(1):41-45.
18. Figueiredo AA, Lucon AM, Srougi M. Urogenital Tuberculosis. Microbiol Spectr 2017;5(1). doi: 10.1128/microbiolspec.TNMI7-0015-2016. Review.
19. Tse BN, Adalja AA, Houchens C, Larsen J, Inglesby TV, Hatchett R. Challenges and Opportunities of Nontraditional Approaches to Treating Bacterial Infections. Clin Infect Dis 2017;65(3):495-500. doi: 10.1093/ cid/cix320.
20. Бреусов А.А., Кульчавеня Е.В., Брижатюк Е,В., Филимонов П.Н. Оптимальный подход к комбинированному лечению больных урогенитальным папилломатозом. Урология 2015;(5):118-123.
21. Балабанова Р., Егорова О., Сажина Е. Панавир при ревматоидном артрите, ассоциированном с герпетической инфекцией. Врач 2009;(12):49-53.
22. Гребнева Г., Гребнева О., Ишмулова О. Панавир для ускорения элиминации вирусов при хроническом гепатите. Врач 2010;(7):36-37.
23. Ковчур П.И., Бахлаев И.Е. Эффективность препарата «Панавир» в лечении хронических папилломавирусных заболеваний шейки матки. Вестник РУДН, серия Медицина 2011;(1):24-28.
24. Стовбун С., Сафронов Д., Кучеров В. Панавир: эффективность в регенеративной терапии дуоденальных язв. Врач 2011;(10):51-52.
25. Трубицина И., Чикунова Б., Стовбун С., Сафронов Д., Кучеров В. Специфическая активность препарата Панавир в заживлении экспериментальной язвы желудка. Врач 2011;(10):63-67.
26. Suligoi B, Vittori G, Salfa MC, Timelli L, Corsini D, Fattorini G et al. Prevalence and incidence of external genital warts in a sample of Italian general female population. BMC Infect Dis 2017;17(1):126. doi: 10.1186/ s12879-017-2202-6.
27. Dhumale SB, Sharma S, Gulbake A. Ano-genital warts and HIV status-a clinical study. J Clin Diagn Res 2017;11(1):WC01-WC04. doi: 10.7860/ JCDR/2017/24610.9171.
28. Cortes-Gutierrez EI, Davila-Rodriguez MI, Fernandez JL, de la O-Perez LO, Garza-Flores ME, Eguren-Garza R, Gosalvez J.The presence of human papillomavirus in semen does not affect the integrity of sperm DNA. Andrologia 2017 Mar 6. doi: 10.1111/and.12774.
29. Kim SM. Human papilloma virus in oral cancer. J Korean Assoc Oral Maxillofac Surg 2016;42(6):327-336. doi: 10.5125/jkaoms.2016.42.6.327.
30. Smelov V, Bzhalava D, Arroyo Muhr LS, Eklund C, Komyakov B, Gorelov A, Dillner J, Hultin E. Detection of DNA viruses in prostate cancer. Sci Rep 2016;6:25235. doi: 10.1038/srep25235.
31. Роговская С., Подзолкова А., Оламова Н. Генитальные кондиломы: терапия и профилактика. Врач 2010;(12):46-49
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 272.86 кб |















































































