Особенности вегетативной регуляции функции и кровоснабжения мочевого пузыря и предстательной железы у старых крыс с возрастной гиперплазией предстательной железы в патогенезе ДГПЖ и СНМП
 7746
7746 Доброкачественная гиперплазия предстательной железы (ДГПЖ) является одним из наиболее распространенных урологических заболеваний мужчин пожилого возраста [1-4]. Патогенез развития ДГПЖ до настоящего времени вызывает дискуссию, поскольку накапливающиеся научные данные расширяют спектр факторов, играющих роль в развитии этой патологии. Помимо возрастных изменений гормонального фона, связанных с повышенной трансформацией тестостерона в метаболически более активный дигидротестостерон за счет усиления активности фермента 5α-редуктазы [5, 6], на активность пролиферации клеток предстательной железы (ПЖ) могут влиять концентрация эстрогенов и увеличение соотношения эстрогены/андрогены [7, 8], усиление секреции инсулина и инсулиноподобного фактора роста, пролактина[9-11], а также хроническое нарушение кровоснабжения ПЖ, приводящее к тканевой гипоксии [12-15].Сложность интерпретации данных о патогенезе ДГПЖ усугубляется тем, что не имеется четких данных о корреляции концентрации андрогенов и эстрогенов в крови и их концентрации в ткани ПЖ [6, 16, 17], о причинах повышения активности 5α-редуктазы [18, 19] в связи с разнонаправленным влиянием активации αи β-рецепторов эстрогенов на пролиферативную активность клеток [20, 21], а также практически отсутствием данных о взаимосвязи этих факторов с ухудшением кровоснабжения ПЖ. Неясны также механизмы, ведущие к формированию симптомов нижних мочевых путей (СНМП) у больных ДГПЖ, которые нередко являются основной причиной обращения пациента к врачам, – насколько они обусловлены гормональными факторами или ухудшением кровоснабжения тазовых органов [22-25].
Экспериментальные исследования на животных могут внести существенный вклад в уточнение патогенеза ДГПЖ. Используемую большинством исследователей модель индукции ДГПЖ большими дозами препаратов тестостерона [26-28] нельзя признать физиологичной. В связи с этим мы исследовали возможность использования возрастных изменений в ПЖ и мочевом пузыре (МП) старых крыс в качестве модели ДГПЖ и сопутствующих расстройств мочеиспускания, и на этой модели изучить особенности регуляции кровоснабжения и нейрогенной регуляции МП и ПЖ.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Эксперименты проведены на 15 самцах белых беспородных крыс двух возрастных групп. 1-ю группу составили молодые половозрелые крысы в возрасте 5-6 мес. массой тела 180-260 г (n=7), а 2-ю группу составили старые крысы в возрасте двух лет с массой тела 380-440 г (n=8).
В условиях эфирного наркоза путем нижнесрединной лапаротомии выделяли МП и ПЖ. МП катетеризировали в области верхушки укороченным внутривенным полипропиленовым катетером № 20G, соединенным через 3-ходовой кран с датчиком давления и системой для инфузии мочевого пузыря.
Состояние кровоснабжения и нейрогенной вегетативной регуляции МП и ПЖ исследовали методом гармонического анализа биоимпеданса [29, 30]. Для этого подшивали диагностические электроды в область верхушки и шейки МП, а также к боковым долям ПЖ (рис. 1).
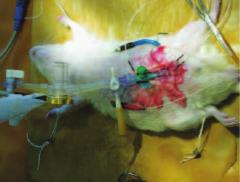
Рис. 1. Катетерированный МП и наложенные диагностические электроды на МП и ПЖ крысы
Регистрацию параметров данса и их анализ проводили с помощью оригинального аппаратно-программного комплекса, разработанного в НИИ урологии Минздрава России совместно с НПФ «Биола». Амплитудные спектры колебаний биоимпеданса автоматически вычислялись методом быстрого преобразования Фурье в частотной полосе 0.05–15.0 Гц. Полученные спектры содержали низкочастотный пик Майера М1 (0.2 Гц), респираторный пик R1 на частоте дыхания крыс (0,8-1 Гц), кардиальный пик С1 на частоте их сердцебиения (3,5-5 Гц), а также последующие гармоники этих пиков меньшей амплитуды (рис. 2). В соответствии с современными представлениями и ранее проведенными исследованиями принимали, что пики М1 и R1 отражают уровень активности регионарных симпатических и парасимпатических влияний соответственно, а пик С1 состояние кровообращения в исследуемом органе [29, 30].
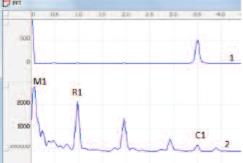
Рис. 2. Типичный спектр ЭКГ (1) и колебаний импеданса (2) МП интактной крысы. М1 – пик Майера, R1 –респираторный пик, С1 – кардиальный пик, совпадающий по частоте с частотой сердечных сокращений (пик на спектре ЭКГ)
Импеданс МП и ПЖ регистрировали одновременно с внутрипузырным давлением при естественном постепенном наполнении МП мочой, а затем во время инфузионной цистометрии через цистостомический катетер. По достижении максимальной емкости МП у наркотизированных крыс происходило мочеиспускание, при котором лишь часть мочи, и в дальнейшем при продолжающейся инфузии осуществлялось ее дробное выделение при сохранении повышенного давления (рис. 3).
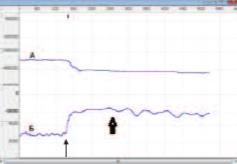
Рис. 3. Пример записи базового импеданса мочевого пузыря (А) и внутрипузырного давления (Б) до и во время его инфузии. Начало инфузии указано тонкой стрелкой, начало мочеиспускания – толстой стрелкой
В конце эксперимента удаляли ПЖ и МП, определяли их массу взвешиванием и брали образцы тканей для проведения гистологического исследования, которое осуществляли по стандартной методике с окраской гистологических срезов гематоксилином и эозином.
Цифровые данные обрабатывали статистически с оценкой достоверности различий в исследуемых группах по методу Стьюдента с использованием t-критерия.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
На первом этапе мы изучили насколько возрастные морфологические и функциональные изменения ПЖ и МП старых крыс соответствуют изменениям, характерным для ДГПЖ.
Результаты исследования показали, что у старых крыс (2-я группа) масса ПЖ оказалась достоверно больше по сравнению с молодыми крысами (1-я гр.), как в абсолютных величинах (1,69±0,07 г. и 0,82±0,04 г. соответственно, p< 0,001), так и относительно массы тела животного (0,41±0,02% и 0,27±0,01% соответственно, р< 0,001), что свидетельствует о развитии возрастной гиперплазии ПЖ. Гистологическое исследование также выявило морфологические признаки, характерные для ДГПЖ, заключающиеся в увеличении количества и размеров ацинусов с гиперплазированным эпителием, клетки которого содержали полиморфные гиперхромные ядра, расположенные в несколько рядов и образующие сосочковые структуры, вдающиеся в просвет ацинусов (рис. 4).
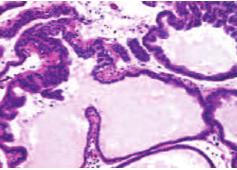
Рис. 4. Гистологическая картина ПЖ старых крыс (2-я гр.). Окраска гематоксилином и эозином. Ув. 200х
Масса МП была больше у 5 из 8 крыс 2-й группы (0,23±0,04 г) по сравнению с 1-й гр. (0,08±0,01 г, p< 0,01). При гистологическом исследовании выявили признаки умеренной гипертрофии детрузора, проявляющиеся в утолщении мышечной оболочки с более массивными пучками гладкомышечных волоМежду пучками лейомиоцитов появлялись выраженные прослойки соединительной ткани. У остальных 3-х крыс масса МП и гистологическая картина не отличались от нормы, выявляемой у молодых крыс 1-й группы.
Результаты цистометрии показали, что в фазу накопления мочи исходное внутрипузырное давление (Pdet) и амплитуда его спонтанных колебаний у старых крыс были достоверно выше, чем у молодых крыс (табл. 1). При инфузионной цистометрии начало мочеиспускания у 5 из 8 старых крыс (62,5%) происходило при более высоком Pdet, чем у молодых животных (42,3-50 и 31,239,5 см. водн ст., соответственно), что отражало повышение тонуса сфинктера уретры и ее сопротивления току мочи. У 3-х других старых крыс Pdet при начале мочеиспускания не отличалось от нормы (31,839,8 см водн. ст), в связи с чем различия по группе в целом оказались статистически недостоверными. Именно у этих крыс не было отмечено признаков гипертрофии детрузора. Увеличенная амплитуда спонтанных колебаний Pdet наблюдалась у всех крыс 2-й гр. независимо от наличия или отсутствия признаков повышения сопротивления уретры и гипертрофии детрузора. На фоне продолжающейся инфузии колебания Pdet у крыс 1-й гр. увеличивались, но не достигали таких высоких значений, как во 2-й гр.
Таблица 1. Показатели цистометрии у крыс разного возраста (см. водн. ст.)
| Молодые крысы (1-я гр.) |
Старые крысы (2-я гр.) |
Р | |
|---|---|---|---|
| Pdet исходное | 11,7±0,4 | 15,3±0,3 | <0,001 |
| Pdet при мочеиспускании | 38,4±2,1 | 42,8±2,6 | >0,05 |
| % крыс с Pdet при мочеиспускании >40 см. вод. ст. |
0% | 62,5% | <0,01 |
| Колебания Pdet в фазу накопления |
2,1±0,3 | 11,8±0,4 | <0,001 |
| Колебания Pdet в фазу постоянной инфузии |
4,5±0,3 | 8,2±0,5 | <0,001 |
Совокупность этих данных позволила нам считать, что возрастные изменения в ПЖ и МП старых крыс в целом соответствуют патофизиологическим процессам, сопровождающим развитие ДГПЖ у человека, а именно: увеличение массы ПЖ с гистологическими признаками ДГПЖ, повышение сопротивления уретры, умеренная гипертрофия МП и усиление самопроизвольной активности. Это дало нам основание для дальнейшего изучения возрастных изменений состояния вазомоторной и нейровегетативной регуляции в этих органах с целью уточнения их роли в патогенезе ДГПЖ.
Развитие возрастной ДГПЖ сопровождалось существенными изменениями регуляции кровоснабжения, как в этом органе, так и в МП. Кардиальный пик импедансного спектра ПЖ, характеризующий состояние интраорганного кровообращения, при физиологическом наполнении МП у крыс 1-й гр. составляла 9,4±0,5 мОм, а во 2-й гр. – 8,9±0,5 мОм, но при переполнении МП во время инфузионной цистометрии в 1-й группе этот показатель возрастал более чем в 2,5 раза (достигая 26,2±2,6 мОм), тогда как у крыс 2-й группы он уменьшался до 7,2±0,4 мОм (рис. 5А). Различия между группами оказались высоко достоверными (p< 0,001). Схожие изменения происходили и в регуляции кровообращения МП. При его физиологическом наполнении кардиальный пик в 1-й и 2й группах составлял 48,7±3,4 и 35,8±2,9 мОм соответственно, но при его переполнении во время инфузионной цистометрии у молодых крыс кровообращение интенсифицировалось (пик С1 возрастал до 148,6±11,8мОм), тогда как у старых крыс отмечалась лишь недостоверная тенденция к росту пика С1 (43,7±3,8 мОм) (рис. 5Б). Различия между группами также оказались высоко достоверными (p< 0,001).
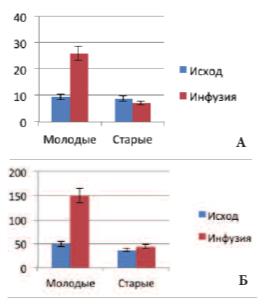
Рис. 5. Изменение кардиального пика С1 импедансного спектра ПЖ (А) и МП (Б) у крыс разных возрастных групп до и на фоне инфузионной цистометрии (мОм)
Таким образом, увеличение функциональной нагрузки, связанной с эвакуацией мочи, у старых крыс не сопровождалось интенсификацией кровоснабжения ПЖ и МП, наблюдаемой в норме у молодых крыс, а наоборот, вызывало его ухудшение, что указывало на существенные возрастные изменения сосудистой вегетативной регуляции этих органов.
Различия между исследованными группами проявлялись в том, что у молодых крыс исходная активность как симпатического (пик М1), так и парасимпатического (пик R1) отделов автономной нервной системы МП оказалась достоверно выше, чем у старых крыс, а их соотношение указывало на относительное возрастание функциональной значимости парасимпатической активности у старых крыс (уменьшение показателя M1/R1) (табл. 2). Суммарная нейрогенная активность, которую определяли по обоим пикам, отражающим активность симпатической и парасимпатической автономной нервной системы, у крыс 2-й группы была значительно снижена, и не наблюдалось ее интенсификации в фазу мочеиспускания, что было характерно для молодых крыс 1-й группы. Эти данные косвенно свидетельствуют в пользу мнения ряда авторов о частичной функциональной денервации МП при инфравезикальной обструкции, вызванной ДГПЖ [31, 32]. Парасимпатическая стимуляция МП при мочеиспускании у молодых крыс резко возрастала, что соответствует общепринятым представлениям о роли холинэргического звена в инициации мочеиспускания [33, 34], тогда как у старых крыс регионарная парасимпатическая активность достоверно не менялась. В результате, преобладание симпатической активности в фазу накопления мочи (M1/R1>1) у молодых крыс при мочеиспускании менялось на преобладание парасимпатической активности (M1/R1< 1), а у старых крыс во время эвакуаторной фазы преимущество симпатических влияний сохранялось и даже усиливалось (возрастание M1/R1).
Таблица 2.Пики М1 и R1 (мОм) и их соотношение в спектре импедансов МП и ПЖ у крыс 1-й и 2-й групп
| Показатели | Молодые крысы (1-я группа) | Старые крысы (2-я группа) | ||
|---|---|---|---|---|
| Исходн. данные | Инфузия | Исходн. данные | Инфузия | |
| Мочевой пузырь | ||||
| М1 | 821±43 | 582±37 | 392±31*** | 457±34 |
| R1 | 481±29 | 1505±48 | 272±19** | 216±16*** |
| M1/R1 | 1,71±0,11 | 0,39±0,04 | 1,44±0,08* | 2,12±0,12*** |
| MR | 952±38 | 1613±36 | 477±27*** | 506±24*** |
| Предстательная железа | ||||
| М1 | 53±3 | 87±6 | 60±4 | 45±3*** |
| R1 | 45±2 | 81±7 | 66±5* | 76±5 |
| M1/R1 | 1,19±0,08 | 1,08±0,06 | 0,92±0,05* | 0,59±0,03*** |
| MR | 70±3 | 19±5 | 89±4** | 88±3*** |
Примечание. Достоверность разницы результатов между 1-й и 2-й гр.:
* p<0,05, ** p<0,01, *** p<0,001.
В отношении ПЖ достоверных различий по показателям симпатической и парасимпатической нервной активности при функциональном наполнении МП между группами не выявили, тогда как их соотношение было различным: у молодых крыс преобладала симпатическая активность (М1/R1>1), а у старых преобладала парасимпатическая активность (M1/R1< 1). В фазу постоянной инфузии МП активность обоих звеньев вегетативной регуляции ПЖ у молодых крыс возрастала пропорционально, и их соотношение существенно не менялось, тогда, как у старых крыс происходило уменьшение показателя симпатической активности на фоне возрастания парасимпатических воздействий, и, в результате, преобладание парасимпатического звена усиливалось.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Проведенные исследования показали, что формирование ДГПЖ сопровождается выраженными регионарными изменениями нейрогенной и сосудистой регуляции ПЖ и МП в зависимости от функции детрузора. Если в норме при переполнении МП и инициации мочеиспускания наблюдали интенсификацию кровообращения в МП и ПЖ, то у старых крыс с ДГПЖ этого не происходило. Эти изменения сопровождались ослаблением нейрогенной вегетативной активности у крыс с ДГПЖ, как в отношении ПЖ, так и МП. При этом в ПЖ наблюдалось относительпреобладание парасимпатических влияний над симпатическими, тогда как в норме наблюдалась обратная картина, а в МП крыс с ДГПЖ преобладала симпатическая активность как в фазу функционального покоя, так и в фазу инициации мочеиспускания, тогда как в норме при инициации мочеиспускания соотношение адрено-холинэргических влияний сдвигалось в сторону парасимпатикуса. Функциональная значимость выявленных различий состоит в том, что сократительная активность выходного отдела МП и ПЖ опосредуется активацией парасимпатического отдела автономной нервной системы, реализуемой через М3-холинорецепторы [35, 36], в связи с чем преобладание холинэргических влияний на гиперплазированную ПЖ может инициировать повышение ее тонуса, увеличивая сопротивление уретры току мочи, что мы зарегистрировали у части крыс в виде повышения Pdet при инициации мочеиспускания. Отсутствие усиления парасимпатичекой стимуляции МП при мочеиспускании у крыс с ДГПЖ может свидетельствовать об ослаблении эвакуаторной функции детрузора. Однако взаимосвязь между изменением соотношений симпато-вагусной регуляции МП и его функцией может быть сложнее, как показали наши исследования и данные [35] о синэргичном действии симпатической и парасимпатической систем в реализации сокращения выходного отдела МП и ПЖ.
Развитие гиперактивности детрузора при ДГПЖ, проявляющейся в наших опытах усилением спонтанных колебаний Pdet у крыс 2-й группы в фазу накопления мочи, может быть связано с изменениями в системе регуляции кровоснабжения МП. Ухудшение кровоснабжения переполненного МП в экспериментах на животных с моделированием хронической инфравезикальной обструкции, имитирующим уродинамические расстройства при ДГПЖ, сопровождается развитием гиперактивности детрузора [37-40]. При этом в МП находили увеличение количества c-kit-позитивных интерстициальных клеток, способных к генерации ритмичных колебаний трансмембранного потенциала, то есть, обладающих пейсмейкерной активностью, получивших название «интерстициальные клетки, подобные клеткам Кахаля» (в англоязычной литературе «interstitial Cajal-like cells», сокращенно ICC) [41, 42]. Увеличение их количества и активности приводит к интенсификации спонтанных колебаний тонуса гладкомышечных клеток детрузора, вызывая ощущения ургентности и приводя к учащению мочеиспусканий [43]. В ткани гиперактивного МП (как у больных, так и у экспериментальных животных) находили увеличенное количество ICC [44, 45]. Показана также анатомическая и функциональная взаимосвязь интерстициальных ICC с вегетативной нервной системой МП, причем эти клетки могут являться посредниками между интрамуральными нейронами и гладкомышечными клетками детрузора [46-48].
Таким образом, изменения вегетативной регуляции МП и нарушение его кровоснабжения при развитии ДГПЖ могут быть факторами патогенеза дисфункции детрузора, проявляющейся у больных ДГПЖ в виде СНМП.
В наших экспериментах выявилась также тесная функциональная взаимосвязь МП и ПЖ в отношении регуляции кровоснабжения этих органов. В обеих группах выявили однонаправленные изменения их кровоснабжения. Увеличение кровотока в МП молодых крыс при его наполнении сопровождалось усилением кровоснабжения ПЖ, и наоборот, ухудшение кровоснабжения переполненного МП старых крыс сочеталось с ухудшением кровоснабжения гиперплазированной ПЖ. Полученные данные могут указывать на патогенетическую роль ухудшения кровоснабжения ПЖ в развитии ДГПЖ, однако, этот вопрос требует дополнительных исследований.
ЛИТЕРАТУРА
1. Доброкачественная гиперплазия предстательной железы. [Под ред. Н.А. Лопаткина]. М., 1999. 216 c.
2. Пытель Ю.А., Винаров А.З. Этиология и патогенез доброкачественной гиперплазии предстательной железы. // В кн. Доброкачественная гиперплазия предстатель-ной железы. М. 1999. С.21-36.
3. Kirby R. Improving lower urinary tract symptoms in BPH. // Practitioner. 2011. Vol. 255, N 1739. P. 15-19.
4. Stroup SP, Palazzi-Churas K, Kopp RP, Parsons JK. Trends in adverse events of benign prostatic hyperplasia (BPH) in the USA, 1998 to 2008. // BJU Int. 2012. Vol. 109, N 1. P. 84-87.
5. Azzouni F, Godoy A, Li Y, Mohler J. e 5 alpha-reductase isozyme family: a review of basic biology and their role in human diseases. // Adv Urol. 2012. Vol. 2012. doi: 10.1155/2012/530121.
6. Kobayashi H, Gotanda K, Shibata Y, Watanabe J, Nakano Y, Shinbo A, Suzuki K. Suppressive effects of the antiandrogen agent, chlormadinone acetate and the 5alphareductase inhibitor, dutasteride on prostate weight and intraprostatic androgen levels in rats. // Arzneimittelforschung. 2011. Vol. 61, N 9. P. 515-520.
7. Roberts RO, Jacobson DJ, Rhodes T, Klee GG, Leiber MM, Jacobsen SJ. Serum sex hormones and measures of benign prostatic hyperplasia. // Prostate. 2004. Vol. 61, N 2. P. 124-131.
8. Wu JH, Jiang XR, Liu GM, Liu XY, He GL, Sun ZY. Oral exposure to low-dose bisphenol A aggravates testosterone-induced benign hyperplasia prostate in rats. // Toxicol Ind Health. 2011. Vol. 27, N 9. P. 810-819.
9. Vikram A, Jena G. Role of insulin and testosterone in prostatic growth: who is doing what? // Med Hypotheses. 2011. Vol. 76, N 4. P. 474-478.
10. Hammarsten J, Peeker R. Urological aspects of the metabolic syndrome. // Nat Rev Urol. 2011. Vol. 8, N 9. P. 483-494.
11. Wang Z, Olumi AF. Diabetes, growth hormone-insulin-like growth factor pathways and association to benign prostatic hyperplasia. // Differentiation. 2011. Vol. 82, N 4-5. P. 261-271.
12. Kojima M, Ochiai A, Naya Y, Okihara K, Ukimura O, Miki T. Doppler resistive index in benign prostatic hyperplasia: correlation with ultrasonic appearance of the prostate and infravesical obstruction.// Eur Urol. 2000. Vol. 37, N 4. P. 436-442.
13. Berger AP, Horninger W, Bektic J, Pelzer A, Spranger R, Bartsch G, Frauscher F. Vascular resistance in the prostate evaluated by colour Doppler ultrasonography: is benign pros-tatic hyperplasia a vascular disease? // BJU Int. 2006. Vol. 98, N 3. P.587-590.
14. Abdelwahab O, El-Barky E, Khalil M.M, Kamar A. Evaluation of the resistive index of prostatic blood flow in benign prostatic hyperplasia.// Int. Braz. J. Urol. 2012. Vol 38, N 2. P. 250-255.
15. Tsuru N, Kurita Y, Masuda H, Suzuki K, Fujita K. Role of Doppler ultrasound and resistive index in benign prostatic hypertrophy. // Int J Urol. 2002. Vol. 9, N 8. P. 427-430.
16. Shidaifat F, Lin YC. Testosterone effect on the expression of genes that mediate testosterone metabolism and genes that mediate the effect of those metabolites on the prostate. // Life Sci. 2012. Vol. 91, N 5-6. P. 194-198.
17. Kumar R, Verma V, Sarswat A, Maikhuri JP, Jain A, Jain RK, Sharma VL, Dalela D, Gupta G. Selective estrogen receptor modulators regulate stromal proliferation in human be-nign prostatic hyperplasia by multiple beneficial mechanisms-action of two new agents. // Invest New Drugs. 2012. Vol. 30, N 2. P. 582-593.
18. Li J, Ding Z, Wang Z, Lu JF, Maity SN, Navone NM, Logothetis CJ, Mills GB, Kim J. Androgen regulation of 5α-reductase isoenzymes in prostate cancer: implications for prostate cancer prevention. // PLoS One. 2011. Vol. 6, N 12. doi: 10.1371/journal.pone.0028840.
19. Chang KH, Li R, Papari-Zareei M, Watumull L, Zhao YD, Auchus RJ, Sharifi N. Dihydrotestosterone synthesis bypasses testosterone to drive castration-resistant prostate cancer. // Proc Natl Acad Sci U S A. 2011. Vol.108, N 33. P. 13728-13733.
20. Ho CK, Habib FK. Estrogen and androgen signaling in the pathogenesis of BPH. // Nat Rev Urol. 2011. Vol. 8, N1. P.29-41.
21. Hu WY, Shi GB, Lam HM, Hu DP, Ho SM, Madueke IC, Kajdacsy-Balla A, Prins GS. Estrogen-initiated transformation of prostate epithelium derived from normal human prostate stem-progenitor cells. // Endocrinology. 2011. Vol. 152, N 6. P. 2150-2163.
22. Кирпатовский В.И., Плотников Е.Ю., Мудрая И.С., Хромов Р.А., Ревенко С.В., Зоров Д.Б. Ишемия мочевого пузыря, как причина его дисфункции после острой задержки мочи. // Экспериментальная и клиническая урология.2012. №3. C. 9-14.
23. Shigehara K, Sugimoto K, Konaka H, Iijima M, Fukushima M, Maeda Y, Mizokami A, Koh E, Origasa H, Iwamoto T, Namiki M. Androgen replacement therapy contributes to improving lower urinary tract symptoms in patients with hypogonadism and benign pros-tate hypertrophy: a randomised controlled study. // Aging Male. 2011. Vol. 14, N 1. P. 53-58.
24. Shinbo H, Kurita Y, Nakanishi T, Imanishi T, Otsuka A, Furuse H, Mugiya S, Ozono S. Resistive index: a newly identified predictor of outcome of transurethral prostatectomy in patients with benign prostatic hyperplasia. // Urology. 2010. Vol. 75, N 1. P. 143-147.
25. Mitterberger M, Pallwein L, Gradl J, Frauscher F, Neuwirt H, Leunhartsberger N, Strasser H, Bartsch G, Pinggera GM. Persistent detrusor overactivity after transurethral resection of the prostate is associated with reduced perfusion of the urinary bladder. // BJU Int. 2007. Vol. 99, N 4. P. 831-835.
26. Jang H, Ha US, Kim SJ, Yoon BI, Han DS, Yuk SM, Kim SW. Anthocyanin extracted from black soybean reduces prostate weight and promotes apoptosis in the prostatic hy-perplasia-induced rat model. // J Agric Food Chem. 2010. Vol. 58, N 24. P.12686-12691.
27. Shin IS, Lee MY, Ha HK, Seo CS, Shin HK. Inhibitory effect of Yukmijihwangtang, a traditional herbal formula against testosterone-induced benign prostatic hyperplasia in rats. // BMC Complement Altern Med. 2012. Vol. 12. P. 48.
28. Nahata A, Dixit VK. Ganoderma lucidum is an inhibitor of testosterone-induced prostatic hyperplasia in rats. // Andrologia. 2012. Vol. 44, Suppl 1. P. 160-174.
29. Мудрая И.С., Ибрагимов А.Р., Кирпатовский В.И., Ревенко С.В., Нестеров А.В., Гаврилов И.Ю. Оценка функционального состояния мочевого пузыря методом Фурье-импедансной цистометрии. // Экспериментальная и клиническая урология. 2010. №3. C. 21-26.
30. Кирпатовский В.И., Мудрая И.С., Ревенко С.В., Нестеров А.В., Гаврилов И.Ю., Хромов Р.А., Баблумян А.Ю.Оценка интрамурального кровотока и нейрогенной регуляции в интактном и гипертрофированном мочевом пузыре с помощью гармонического анализа биоимпеданса. // Бюлл. экспер. биол. мед. 2012. Т. 153, №4. С. 422-427.
31. Zhou Y., Ling E.A. Nitric oxide syntase Its distribution and alteration in the intramural ganglia of the urinary bladder in normal and urethra-obstructed guinea pigs.// Ann Acad. Med. Singapore. 1999.Vol. 28, N 1.P. 49-61.
32. Sibley GN. A comparison of spontaneous and nerve-mediated activity in bladder muscle from man, pig and rabbit. // J Physiol. 1984.Vol. 354. P. 431–443.
33. Fetscher C, Fleichman M, Schmidt M, Krege S, Michel MC. M(3) muscarinic receptors mediate contraction of human urinary bladder. // Br J Pharmacol. 2002. Vol. 136, N 5. P. 641–643,
34. Choppin A. Muscarinic receptors in isolated urinary bladder smooth muscle from different mouse strains. // Br J Pharmacol. 2002. Vol. 137. P. 522–528.
35. Roosen A, Blake-James BT, Wood D, Fry CH. Clinical and experimental aspects of Adreno-muscarinic synergy in the bladder base and prostate. // Neurourol Urodyn. 2009. Vol. 28, N8. P. 938-43. doi: 10.1002/nau.20742.
36. White CW, Short JL, Haynes JM, Matsui M, Ventura S. Contractions of the mouse prostate elicited by acetylcholine are mediated by M(3) muscarinic receptors. // J Pharmacol Exp fter. 2011. Vol. 339, N3. P. 870-7. doi: 10.1124/jpet.111.186841.
37. Drake MG, Hedlund P, Harvey IJ, Pandita RK, Andersson KE, Gillespie JL. Partial outlet obstruction enhances modular autonomic activity in the isolated rat bladder. // J Urol. 2003. Vol. 170. P. 276-279.
38. Kwak TI, Lee JG. Inhibitory effects of propiverin, atropine and oxybutinin on bladder instability in rats with infravesical outlet obstruction. // BJU. 1998.Vol. 82, N 2. P. 272-277.
39. Chai TC, Gemalmaz H, Andersson KE, Tuttle JB, Steers WD. Persistently increased voiding frequency despite relief of bladder outlet obstruction. // J Urol. 1999.Vol. 161, N 5.P. 1689-1693.
40. Berggren T, Uvelius B. Cystometrical evaluation of acute and chronic overdistension of the urinary bladder. // Urol Res. 1998.Vol. 26, N 5. P. 325-330.
41. McСloskey KD. Interstitial cells of Cajal in the urinary tract. // Handb Exp Pharmacol. 2011. Vol. 202. P. 233-254.
42. Okada S, Kojima Y, Kubota Y, Mizuno K, Sasaki S, Kohri K. Attenuation of bladder overactivity in KIT mutant rats. // BJU Int. 2011.Vol. 108, N 2, Pt 2. P. 97-103.
43. Brandling AF. A myogenic basis for the overactive bladder. // Urol. 1997.Vol. 50. P. 57-67.
44. Biers SM, Reynard JM, Doore T, Bradling AF. Functional effects of a c-kit tyrosine inhibitor on guinea-pig and human detrusor. // BJU Int. 2006.Vol. 97. P. 612-616.
45. Hashitani H. Interaction between interstitial cells and smooth muscles in the lower urinary tract and penis. // J Physiol. 2006.Vol. 576, N 3. P. 707-714.
46. McCloskey KD. Interstitial cells in the urinary bladder – localization and function. // Neurosci Urodyn. 2010. Vol. 29, N 1. P. 82-87.
47. Johnston L, Carson C, Lyons AD, Davidson RA, McCloskey KD. Choliergic-induced Ca2+ signaling in interstitial cells of Cajal from the guinea pig bladder. // Amer J Physiol, Renal Physiol. 2008.Vol. 294, N 3. P. 645-655.
48. Fang Q, Yang J, Pan JH, Li WB, Shen WH, Li LK, Wang YQ, Fang JL, Ding LL, Song B. Morphological study on the role of ICC-like cells in detrusor neuro-modulation of rat urinary bladder. // Zhonghua Wai Ke Za Zhi. 2008.Vol. 46, N 20. P. 1542-1545.















































































