Применение анастомотической уретропластики у пациентов с инфравезикальной обструкцией
 9633
9633 Одной из основных причин инфравезикальной обструкции у пациентов старше 50 лет, является доброкачественная гиперплазия предстательной железы. Хирургическая тактика данного состояния широко изучена [1]. В то же время, у более молодых пациентов одной из ведущих причин обструктив- ной симптоматики является стриктура мочеиспускательного канала [2].
По данным нашего исследования, в этиологии стриктур уретры превалировали травматические (18 пациентов) и ятрогенные (4 пациента) повреждения, однако в некоторых случаях этиология оставалась неизвестной и стриктура рассматривалась как «идиопатическая» (2 пациентов).
По нашему мнению, какие либо манипуляции на поврежденной уретре можно предпринимать не ранее чем через 3 месяца после травмы. Этот срок необходим для полного формирования рубцовой ткани в зоне повреждения, что снижает риск рецидива заболевания вследствие неполной резекции измененных тканей [3].
Наиболее распространенной и широко применяемой методикой коррекции дефектов уретры является анастомотическая уретропластика [4], основанная на принципах, предложенных Марион-Хольцовым, и ее различные модификации [5]. Некоторые отечественные авторы [6] склоняются в пользу зарубежных методик уретро- пластики, являющихся по сути модификацией операции Марион-Хольцова. В связи с вышесказанным, нами была поставлена задача оценить эффективность открытой анастомотической уретропластики и обосновать необходимость расширения показаний к ее применению.
МАТЕРИАЛЫ И МЕТОДЫ
На базе нашего центра выполнено проспективное исследование эффективности анастомотической уретропластики при стриктурах бульбо- мембранозного отдела уретры у 24 пациентов, оперированных в период с сентября 2008 по декабрь 2010 года. Из исследования были исключены пациенты с непротяженными первичными стриктурами, коррекция которых могла быть выполнена эндоскопически, а так же пациенты с протяженными стриктурами, наложение анастомоза без натяжения у которых не представлялось возможным.
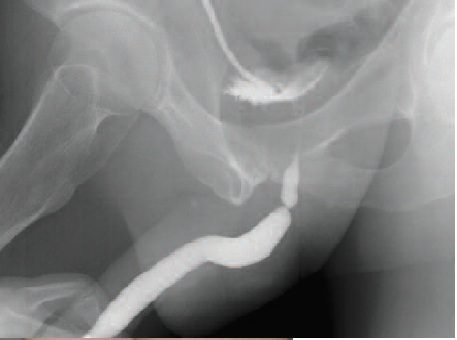
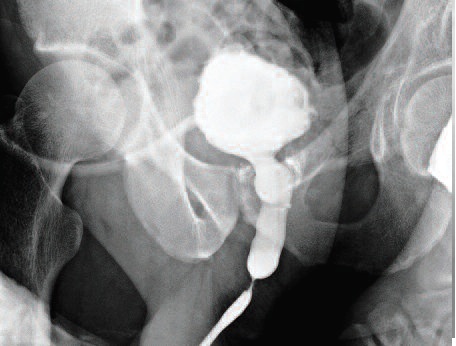
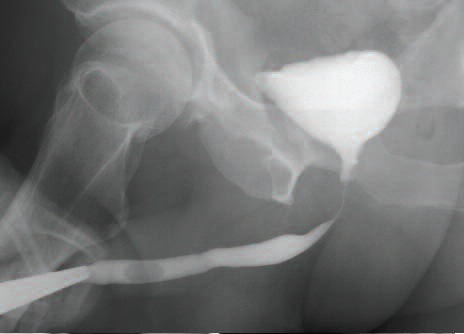
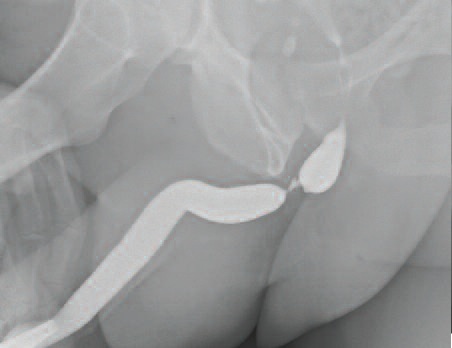
С целью визуализации протяженности стриктуры на предоперационном этапе всем пациентам выполнялось рентгенологическое исследование (рис.1). Протяженность дефектов составляла 1,5-6 см. Так же пациентам выполнялась урофлоуметрия. Скорость мочеиспускания составляла 5-12 мл/с. Перед операцией выполнялось ультразвуковое исследование на предмет наличия остаточной мочи и ретенционных изменений верхних мочевых путей.
 |
 |
| A | Б |
 |
 |
| В | Г |
| А. Ретроградная уретроцистограмма. Рецидивная стриктура бульбозного отдела уретры. В. Ретроградная уретрограмма. Протяженная стриктура бульбомембранозного отдела уретры. |
Б. Комбинированная уретроцистограмма. Посттравматическая стриктура на границе бульбозного и пенильного отделов уретры. Г. Ретроградная уретрограмма. Стриктура бульбозного отдела уретры. |
| Рис 1. Рентгенологическое исследование уретры | |
ОПЕРАТИВНАЯ ТЕХНИКА
Цель операции — создание широкого анастомоза без натяжения. Протяженность и расположение стриктуры являются лимитирующими факторами. Учитывая растяжимость пенильной части уретры во время эрекции, протяженность резекции ограничена возможным послеоперационным искривлением полового члена. Зоны спатуляции по 1 см с каждой стороны и резекция, 2 см стриктуры, приведут в общей сложности к укорочению уретры в пределах 4 см, что может быть неприемлемо для большинства пациентов.
Более того, стриктуры пенильного отдела чаще бывают множественными и протяженными. Поэтому применение анастомотической уретропластики при стриктурах пенильного отдела уретры ограничено [7]. В отличие от пенильного отдела уретры бульбозный отдел может быть широко мобилизован: проксимально до мочеполовой диафрагмы и дистально до пеноскро- тального угла. Бульбозная уретра имеет достаточно хорошее кровоснабжение: от бульбозной и уретральной артерий (проксимально), ретроградным током от головки полового члена и перфорантных артерий, ветвей кавернозных и дорсальных артерий (дистально). При мобилизации собственная эластичность уретры может заместить без натяжения дефект до 4 см. При более протяженных дефектах возможно расправить естественную кривизну бульбозной уретры, образующуюся между ножек полового члена. С этой целью разделяются ножки полового члена, дистальная часть уретры укладывается между ними. Так же сократить диастаз между резецированными краями уретры можно посредством наложения пликационных швов на мягкие ткани промежности в зоне анастомоза. При помощи вышеуказанных манипуляций возможно сопоставить без натяжения дефект до 6-7 см. Таким образом, наиболее обосновано применение анастомотической уретропластики для коррекции стриктур бульбомембранозного отдела уретры от 1 до 4 см, учитывая спатуляцию по 1 см с каждой стороны.
Для интраоперационного удобства, а так же снижения риска позиционных осложнений ноги пациента фиксировались стременами Аллена. Использовался промежностный доступ. Чаще применялся продольный, либо перевернутый Y-образный разрез (рис. 2а).
После вскрытия фасции Коллиса в уретру вводился катетер (для удобства её идентификации и выделения). Локализация стриктуры определялась по наличию фиброза и сокращению спонгиозного тела по типу песочных часов. Дистальная граница сужения выявлялась по введенному в полость уретры катетеру. Для уточнения проксимальной границы резекции ретроградно через цистостомический свищ можно провести уретральный буж, избегая перфорации и дилатации уретры. Если у хирурга возникает сомнение в возможности наложения анастомоза, выполняется продольный разрез через место сужения, который продляется проксимально и дистально до достижения здоровых тканей. Если получившийся дефект слишком велик для наложения анастомоза тактика может быть изменена на заместительную пластику. При мобилизации уретры существует вероятность повреждения пенильных артерий, поэтому пациенты должны быть информированы о возможном развитии эректильной дисфункции.
Зона стеноза полностью иссекалась до здоровых тканей. Для калибровки дистального и проксимального конца применялись уретральные бужи 28-30 Ch (рис. 2б). Невозможность калибровки концов резецированной уретры говорит о наличии резидуального спонгиофиброза, который требует дополнительного иссечения. Недооценка зоны резекции является ключевой причиной рецидива заболевания.
Анастомоз накладывался, по возможности, в 2 слоя: первый ряд швов - непосредственно на слизистую уретры (рис. 2в), вторым рядом - зона анастомоза герметизировалась тканями спон- гиозного тела (рис. 2г). Применялся монофиламентный, рассасывающийся шовный материал 4-0 - 5-0.
Для отведения мочи использовались уретральные катетры 16-18 Ch, которые фиксировались к головке полового члена во избежание их выпадения, а при необходимости, оставлялся цистостомический дренаж. Предпочтительнее использовать полностью силиконовые катетеры вследствие меньшей воспалительной реакции. Количество страховых дренажей зависит от интраоперационной ситуации. Однако, учитывая высокую вероятность образования послеоперационных гематом, желательно оставлять дренаж на протяжении нескольких первых суток. В послеоперационном периоде всем пациентам проводилась антибактериальная (согласно посеву мочи), симптоматическая терапия. Уретральный катетер удалялся на 10-16 сутки. Сроки удаления уретрального катетера являются дискутабельными и часто остаются на усмотрение оперирующего хирурга. После удаления уретрального катетера выполнялась контрольная уретрограмма. Цистостомический дренаж удалялся не позднее 3-х суток до предполагаемого срока удаления уретрального катетера.
 |
 |
| А | Б |
 |
 |
| В | Г |
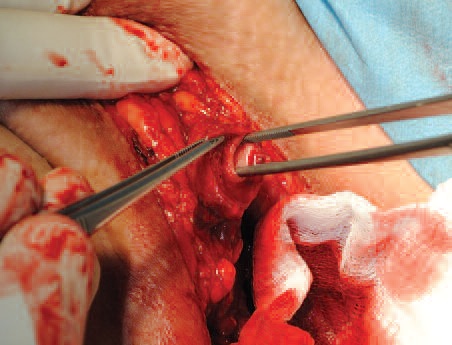
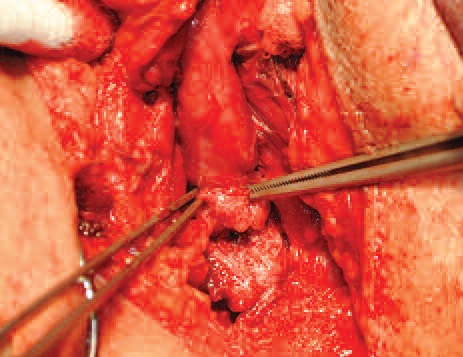
| А. Мобилизация бульбозного отдела уретры. Б. Калибровка зоны резекции. |
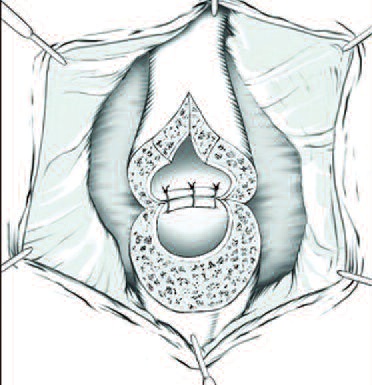
В. Схема наложения 1-го ряда швов. Г. Наложение 2-го ряда швов. |
| Рис 2. Техника наложения анастомоза | |
 |
 |
| А | Б |
 |
 |
| В | Г |
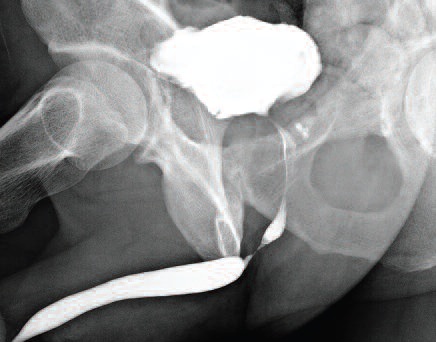
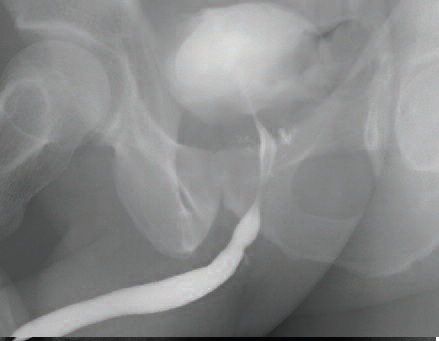
| А. Комбинированная уретроцистограмма. Стриктура бульбозного отдела уретры. Б. Ретроградная уретроцистограмма. Год после оперативного лечения. |
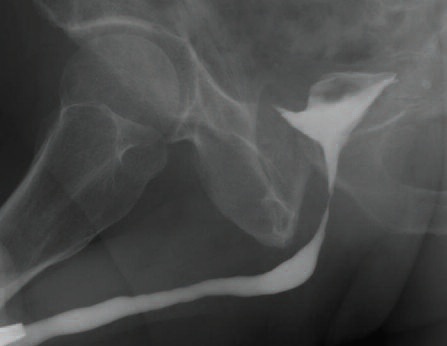
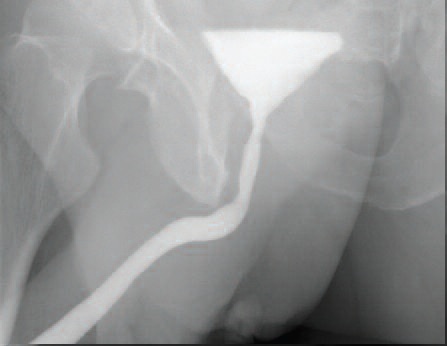
В. Ретроградная уретроцистограмма. Стриктура уретроцистоанастомоза. Г. Микционная уретрограмма. Полгода после оперативного лечения. |
| Рис 3. Контрольное рентгенологическое обследование уретры | |
РЕЗУЛЬТАТЫ
Стоит отметить, что семи пациентам из 24 обследованных ранее, производилась как минимум одна внутренняя уретротомия. Одиннадцать пациентов поступили с функционирующим цистостомическим дренажем, при этом самостоятельное мочеиспускание полностью отсутствовало у пяти из них. Повреждения бульбомембранозного отдела уретры были выявлены у 4 больных, что потребовало наложения им уретропро- статоанастомоза.
В результате проведенного лечения после удаления уретрального катетера самостоятельное мочеиспускание восстановилось у 100% пациентов. Однако в сроки от 5 до 7 месяцев рецидив стриктуры возник у 9,1% (2) пациентов. Этиология стриктур в этих случаях была связана с постлучевыми изменениями тканей (на фоне дистанционной лучевой терапии), что по нашему мнению, и привело к рецидиву. Одному пациенту была произведена повторная операция по той же методике в сроки 6 месяцев после предшествующей (в дальнейшем рецидива заболевания у данного пациента выявлено не было). Второй пациент от предложенного повторного вмешательства отказался. Также у одного пациента при мобилизации уретры была пересечена левая кавернозная артерия, что привело к эректильной дисфункции, и было скоррегировано посредством реваскуляризации полового члена через 8 мес. после оперативного лечения. Значение максимальной скорости мочеиспускания составляло у всех обследованных больных в пределах 19-35 мл/сек за всё время наблюдения. Значимое укорочение полового члена отмечено у 1 пациента, но данный факт не сказался на общей удовлетворенности от лечения (пациент не живёт половой жизнью).
У всех больных в ближайшие (до года) катамнестические сроки после операции не было отмечено недержания мочи, даже при манипуляциях на мембранозном отделе уретры. Таким образом, положительный эффект от оперативного лечения через год наблюдения составил 98%.
Таблица 1. Результаты оперативного лечения стриктур уретры методом анастомотической уретропластики
| Фамилия автора |
Число пациентов |
Протяженность, см |
% успеха |
Продолжительность наблюдения, мес. |
| Eltahawy EA et al. (4) | 213 | 1,9 | 98,5 | 40,5 |
| Santucci RA et al. (8) | 168 | 1,7 | 95,2 | 72 |
| Andrich DE et al. (9) | 82 | 0,5-3 | 86 | 180 |
| Martinez-PiЦeiro JA et al. (10) | 69 | <3 | 88 | 44,4 |
| Jakse G et al. (11) | 60 | 1-4 | 93,3 | 45 |
| Lindell O et al. (12) | 49 | <2,5 | 95,9 | 12-48 |
| Barbagli G et al. (13) | 20 | <2 | 95 | 54,5 |
| Ковалев В.А. и соавт. | 24 | 1,5-6 | 98 | 3-18 |
| Всего: | 685 | – | 93,7 | - |
ОБСУЖДЕНИЕ
Методика анастомотической уретропластики позволяет достигнуть высокого процента успеха и надежности с минимальным количеством осложнений, что сопоставимо с данными других авторов (табл. 1). Eltahawy EA и соавт. периодически сообщает результаты лечения самой обширной группы пациентов на сегодняшний день, перенесших анасто- мотическую пластику. Из 260 пролеченных больных, с последующим катамнестическим наблюдением до 4 лет, рецидив заболевания выявлен всего в 2% случаев. Было отмечено незначительное число осложнений (около 5%), таких как инфекция мочевыводящих путей, саморазре- шающиеся позиционные осложнения, эректильная дисфункция, скро- талгия. По общепринятым стандартам, данная методика идеально подходит для стриктур бульбозного отдела уретры протяженностью от 1 до 4 см. Однако, как показало наше исследование, в некоторых, тщательно отобранных случаях, эта техника может с успехом применяться для лечения стриктур протяженностью до 6 см.
В то же время, применение анастомотической техники при стриктурах пенильного отдела уретры - ограничено, т.к. может вызвать значительное укорочение и вентральное искривление полового члена при эрекции. Возникновение рецидива стриктуры связано, в основном, с ишемией (в том числе вследствие чрезмерного натяжения зоны анастомоза) или неполной резекцией фиброзно-измененных тканей. В большинстве случаев эти изменения успешно коррегируюся внутренней уретротомией, доводя успешность лечения до 100%.
ЗАКЛЮЧЕНИЕ
Таким образом, анастомотиче- ская уретропластика не потеряла своей актуальности до настоящего времени и, при возможности выполнения, является методом выбора при стриктурах уретры 1-4 см, а в некоторых случаях методика может быть использована для коррекции дефектов протяженность до 6 см. Также следует отметить, что выбор метода репарации должен определяться хирургом исходя из интраоперационной картины. Всегда нужно быть готовым, при необходимости, изменить тактику лечения.
Литература
- Доброкачественная гиперплазия предстательной железы. /Под ред. Н.А. Лопаткина. М.: 1997. 216 с.
- Blandy JP, Fowler C. Urethra and penis inflammation. Urology. Oxford: Blackwell Science, 1996. 477 р.
- Andrich DE, Mundy AR. Urethral strictures and their surgical management // Br J. Urol. 2000. Vol. 86. P. 571–580.
- Eltahawy EA, Schlossberg SM, McCammon KA, Jordan GH. Long term follow up for excision and primary anastomosis in anterior urethral strictures // J. Urol. 2005. Vol. 173, Suppl. P. 87.
- Хольцов В.Н. Частная урология. Л.: Практическая медицина. 1927.
С. 389-390. - Живов А.В., Лоран О.Б., Богданов А.Б., Котов С.В., Македонская Т.П., Плеханов А.Ю. Особенности применения методики анастомотической уретропластики при посттравматических стриктурах бульбомембранозной уретры // Урология. 2010. №5. С. 41-46.
- Rosen MA, McAninch JW. Stricture excision and primary anastomosis for reconstruction of anterior urethral stricture // in Traumatic and reconstructive urology. Philadelphia: W.B. Saunders, 1996. P. 565–569.
- Santucci RA, Mario LA, McAninch JW. Anastomotic urethroplasty for bulbar urethral stricture: analysis of 168 patients // J. Urol. 2002. Vol.167. P.1715–1719.
- Andrich DE, Dunglison N, Greenwell TJ, Mundy AR. e long-term results of urethroplasty // J. Urol. 2003. Vol.170. P.90–92.
- Martinez-Piñeiro JA, Carcamo P, Garcia Matres MJ, Martinez-Pineiro L, Iglesias JR experience with 150 cases // Eur Urol. 1997. Vol.32. P.433–441.
- Jakse G, Marberger H. Excisional repair of urethral stricture. Follow-up of 90 patients // Urol. 1986. Vol.27. P.233.
- Lindell O, Borkowski J, Noll F, Schreiter F. Urethral stricture repair: results in 179 patients // Scand J. Urol Nephrol. 1993. Vol.27. P.241–245.13. Barbagli G, Palminteri E, Bartoletti R, Selli C, Rizzo M. Long-term results of anterior and posterior urethroplasty with actuarial evaluation of the success rates // J. Urol. 1997. Vol.158. P.1380–1382.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью в pdf формате | 364.82 кб |















































































