Сравнительная характеристика результатов деривации мочи после радикальной цистэктомии путем формирования толстокишечного кондуита и модифицированной уретеросигмостомии
 12872
12872 М.Н. Тилляшайхов, Д.К. Абдурахманов, Ш.А. Шукруллаев, М.И. Болтаев, Ш.Т. Хасанов, О.Н. Эргашев
Онкологический научный центр МЗРУз, Узбекистан, Ташкент
Современная тенденция в лечении больных с инвазивным раком мочевого пузыря характеризуется стремлением к радикальному избавлению пациента от опухоли цистэктомии с последующей реконструктивной операцией, направленной на восстановление отведения мочи в наиболее физиологическом варианте. Последнее достигается формированием артифициального мочевого пузыря с естественным мочеиспусканием по уретре (ортотопический мочевой пузырь, варианты Studer, Hautmann, Kock, Camey, Mainz pouch I) или с сохранением только накопительной функции и выведением мочи самокатетеризацией (континентные мочевые резервуары по Kock, Indiana pouch, Mainz pouch II).
В мировой литературе прослеживается тенденция к увеличению частоты формирования континентных мочевых резервуаров и относительному уменьшению операций по формированию артифициального мочевого пузыря. Это обусловлено тем, что качество жизни больных с обоими вариантами деривации мочи практически не различается [1-3] или даже имеется преимущество континентных кондуитов [4].
Одной из альтернативных континентных методик является отведение мочи в непрерывный кишечник путем формирования резервуара низкого давления из сигмовидной кишки и уретеросигмостомии с удержанием мочи за счет анального сфинктера (Mainz pouch II и ряд модификаций этого метода). Данные литературы свидетельствуют о достаточно благоприятных функциональных результатах этого типа реконструкции мочевых путей [5-7].
В нашем исследовании мы проанализировали в сравнительном аспекте эффективность двух вариантов континентного отведения мочи после цистэктомии:
- путем формирования толстокишечного кондуита и отведения мочи в непрерывный кишечник;
- с формированием резервуара из сигмовидной кишки и уретеросигмостомии.
Материал и методы исследования
В анализ вошли истории болезни 79 больных раком мочевого пузыря, из которых 30-ти была выполнена радикальная цистэктомия с одновременным формированием мочевого резервуара из илеоцекального угла и восходящей толстой кишки (I группа) и 49 больным была проведена операция модифицированной уретеросигмостомии (II группа).
Возраст больных в I группе колебался от 35 до 60 лет (в среднем 47,3 ± 2,5 лет), во II от 28 до 72 лет (в среднем 48,8 ± 3,6 лет). В трудоспособном возрасте (до 60 лет) было 87% больных в I группе и 74% больных во II группе (различия статистически недостоверны).
У всех больных I группы был переходно-клеточный рак, во II группе помимо этой гистологической формы, выявленной у 46 больных, наблюдали по 1 случаю аденокарциномы, плоскоклеточного и недифференцированного рака. Распределение больных по стадиям опухолевого процесса представлено в таблице 1. Существенным различием между группами оказалось преобладание случаев с наличием метастазов в регионарные лимфоузлы во II группе (16,7% в I группе и 38,8% во II). По степени злокачественности более благоприятная ситуация была во II группе, где было достоверно меньше больных с низкодиффенцированными опухолями (p < 0,05) (Таблица 2).
Таблица 1. Распределение больных в зависимости от стадии опухолевого процесса
| Группы больных | T2N0 | T2N1-2 | T3N0 | T3N1-2 | T4N0 | T4N1-2 |
| I группа Толстокишечный мочевой резервуар | 5 | 2 | 14 | 3 | 6 | - |
| II группа Уретеросигмостомия | 4 | 3 | 20 | 12 | 4 | 6 |
Таблица 2. Распределение больных по степени злокачественности опухоли
| Группы больных | G1 | G2 | G3 | Всего |
| I группа | 9 (30,0%) | 9 (30,0%) | 12 (40,0%) | 30 |
| II группа | 20 (40,8%) | 17 (34,7%) | 12 (24,5%) | 49 |
Методика формирования континентного толстокишечного мочевого резервуара
Этот вариант континентной деривации мочи, по сути, представляет модифицированную методику операции «Indiana pouch». Суть модификаций заключается в следующем:
- отказ от детубуляризации кишечного резервуара, т.к. имеются публикации о сохранении спонтанных сокращений, несмотря на ее осуществление [8-11];
- изменение методики уретеро-резервуарного анастомоза, который осуществляли путем формирования широкого анастомоза спатулированных мочеточников, сшитых в одну трубку, с кишечным резервуаром для профилактики стеноза уретеро-кишечных анастомозов;
- сохранение аппендикса, через который формировали доступ для эвакуации мочи путем самокатетеризации резервуара, выводя его на переднюю брюшную стенку через пупочное кольцо. Последняя модификация объясняется тем, что в литературе имеются описания сложностей, возникающих при катетеризации мочевого резервуара Indiana-pouch, сформированного по классической методике.
Методика формирования резервуара из сигмовидной кишки с уретеросигмостомией
Использованная нами методика является модифицированным вариантом методики Ellabbady [12], заключающаяся в пересечении сигмовидной кишки на 30 см проксимальнее перитонеального перегиба, формировании из дистального отдела кишки детубуляризированного резервуара низкого давления, в который имплантируются мочеточники. Восстановление непрерывности кишечной трубки производилось путем анастомозирования проксимального отрезка сигмовидной кишки с прямой. Нами был внесен в методику операции ряд модификаций:
- отказ от хирургической «детубуляризации» резервуара сигмовидной кишки по причинам, указанным выше;
- формирование «шейки» мочевого резервуара у места его впадения в кишечную трубку производилось путем гофрирования стенки на протяжении 2-2,5 см, что препятствовало забросу содержимого прямой кишки в мочевой резервуар [13].
Методы обследования больных
Всем больным проводили традиционное общеклиническое и урологическое обследование: физикальный осмотр, общеклинический анализ крови и мочи, биохимическое исследование крови, бактериологическое исследование мочи, рентгенологическое исследование, включающее обзорную рентгенографию брюшной полости, экскреторную урографию, восходящую или нисходящую цистографию, ультразвуковое исследование мочевого пузыря, цистоскопию с биопсией стенки мочевого пузыря.
По показаниям для уточнения распространенности опухолевого процесса и вовлечения регионарных лимфатических узлов проводили компьютерную и магнитно-резонансную томографию с контрастированием мочевого пузыря.
У ряда больных в послеоперационном периоде выполняли резервуароскопию, что позволяло визуально оценивать изменения слизистой оболочки мочевого резервуара, оценить функцию анастомозов, осуществлять биопсию слизистой для динамического контроля и проводить функциональное исследование состояния резервуара.
Статистическая обработка материала производилась с помощью компьютерной программы Statistica.6, используя непараметрические критерии, рекомендуемые для медико-биологических исследований с малыми выборками.
Таблица 3. Госпитальная летальность и частота осложнений
| Группы больных | Госпитальная летальность | Ранние осложнения | Поздние осложнения | Повторные операции |
| I группа | 0% | 13,3% | 10% | 13,3% |
| II группа | 10,2%* | 69,4%* | 59,2%* | 18,4% |
Результаты и обсуждение
Сравнение результатов операции в обеих группах выявило достоверно меньшее количество осложнений в I группе, в том числе и осложнений, приведших к летальному исходу (Таблица 3).
В I группе госпитальной летальности не наблюдали, во II группе умерло 5 больных, 3 из них от желудочного кровотечения, 2 от тромбоэмболии легочной артерии.
В раннем послеоперационном периоде в I группе у 4 пациентов развилось 5 осложнений. У одного больного наблюдался парез желудочно-кишечного тракта, успешно разрешившийся на фоне проводимой консервативной терапии и не повлекший нарушений метаболизма. У второго пациента сформировалась стриктура мочеточнико-резервуарного анастомоза, вызванная рубцовым процессом в окружающих тканях и приведшая к развитию острого левостороннего пиелонефрита, что потребовало экстренной пункционной нефростомии с реконструкцией анастомоза. У третьего пациента развился декомпенсированный метаболический ацидоз, потребовавший кратковременной ощелачивающей терапии. У четвертого больного после удаления катетера, дренирующего мочевой резервуар через аппендикостому, возникли существенные трудности самокатетеризации, в связи с чем выполнена экстренная операция по коррекции аппендикостомы с благоприятным результатом.
У выживших больных II группы в раннем послеоперационном периоде наблюдали 29 случаев осложнений. В 11 случаях отмечен длительный парез кишечника, купированный медикаментозной терапией, у 3 больных несостоятельность межкишечного или мочеточнико-резервуарного анастомозов, у 10 развился острый пиелонефрит, у 2 нагноение операционной раны, у 2 пациентов острая язва желудка и 12-перстной кишки (по 1 больному) и у 1 пациента развилась пневмония.
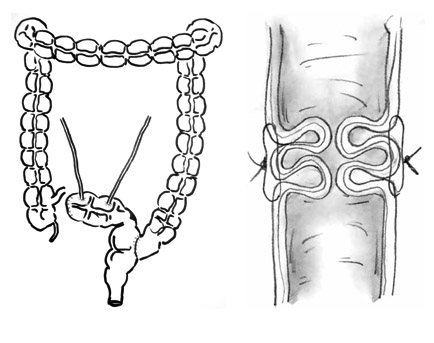
Рисунок. Схема сформированного мочевого резервуара из изолированного сегмента сигмовидной кишки (А) и «шейки» мочевого резервуара (Б).
В отдаленном послеоперационном периоде в I группе зарегистрированы осложнения у 3 больных (10%). У одного больного через 6 месяцев после операции сформировалась стриктура мочеточнико-резервуарного анастомоза, потребовавшая оперативной коррекции, у другого больного развился острый пиелонефрит без признаков нарушения пассажа мочи по мочевым путям. Атака пиелонефрита была купирована консервативной терапией. У третьего пациента наблюдался длительно незаживающий надлобковый свищ, который в последующем самостоятельно закрылся.
Во II группе различные поздние осложнения наблюдались у 19 пациентов: у 14 развитие декомпенсированного гиперхлоремического ацидоза, потребовавшего ощелачивающей терапии, у 9 больных развитие острого пиелонефрита, купированного антибиотикотерапией, у 4 пациентов развитие динамической кишечной непроходимости, купированной консервативными мероприятиями и у 2 пациентов возникновение послеоперационной грыжи передней брюшной стенки.
Обращает на себя внимание, что, несмотря на высокую частоту осложнений во II группе в раннем и отдаленном послеоперационных периодах, большинство из них удалось купировать консервативными методами и лишь 18,4% пациентам потребовались повторные операции, что недостоверно отличалось от этого показателя в I группе больных (13,3%) (Таблица 3).
При динамическом рентгенологическом и ультразвуковом обследовании пациентов в отдаленном периоде у 50% больных I группы и 71,4% больных II группы выявляли нормализацию уродинамики и рентгенологической картины, уменьшение степени пиелокаликоэктазии отмечено у 50% и 28,6% больных соответственно I и II групп. У четырех пациентов I группы с исходными нарушениями функции почек в послеоперационном периоде показатели функции нормализовались, в то время как у четырех больных II группы с аналогичными нарушениями функции почек показатели достоверно улучшились, но превышали верхнюю границу нормы.
Оценивая функциональный эффект примененной операции с точки зрения адекватности восстановления функции мочеотведения, следует отметить, что в раннем послеоперационном периоде у всех больных I группы отмечались частые эпизоды спонтанного подтекания мочи через стому. С увеличением продолжительности послеоперационного периода эти явления уменьшались: через 6 месяцев все пациенты удерживали мочу в течение дня при самокатетеризации с интервалом в 3-4 часа. В ночное время, как правило, больным приходилось вставать до 2-3 раз для опорожнения резервуара. При увеличении времени между мочеиспусканиями больные отмечали подтекание мочи и были вынуждены использовать прокладки.
Таблица 4. Параметры функционального состояния мочевого резервуара
| Показатели | 3 мес. | 6 мес. | 9 мес. | 1 год | До 2 лет |
| I группа | |||||
| Функциональный объем (мл) | 268 ± 32 | 472 ± 46 | - | 502 ± 49 | - |
| Внутрирезервуарное давление (см водн. ст.) | 36 ± 5 | 31 ± 3 | - | 26 ± 3 | - |
| II группа | |||||
| Функциональный объем (мл) | 374 ± 33 | 576 ± 44 | 587 ± 39 | 593 ± 37 | 606 ± 42 |
| Внутрирезервуарное давление (см водн. ст.) | 32 ± 3 | 30 ± 2 | 24 ± 2 | 28 ± 3 | 24 ± 2 |
Во II группе в раннем послеоперационном периоде также наблюдались частые эпизоды недержания мочи и кала. К 6 месяцам после операции симптомы раздражения кишечника стихали, больные вырабатывали оптимальный режим опорожнения прямой кишки. К этому же сроку почти все больные ночью спали. Днем мочеиспускание через прямую кишку осуществлялось каждые 4-6 часов. К этому сроку у больных формируется раздельное выделение кала и мочи: кал выделяется 1 раз в сутки, моча каждые 4-6 часов. Только 1 больной отмечал небольшой дискомфорт в ночное время.
Эффект удержания мочи в мочевом резервуаре во многом зависит от его функционального объема и внутрирезервуарного давления. Измеренная функциональная емкость мочевого толстокишечного резервуара у больных I группы в первые 3 месяца после операции оказалась достаточно низкой 250-300 мл (Таблица 4). По нашему мнению это связано с последствиями операционной травмы, вызывающей длительный спазм мышечной оболочки кишечной стенки и раздражающим действием мочи на неадаптированную кишечную стенку. К 6-12 месяцам после операции емкость возрастала до 450-520 мл. Увеличение функциональной емкости резервуара, по нашему мнению, определяло улучшение его континентности и урежение эпизодов недержания мочи.
У больных II группы в ранние сроки после операции (3 месяца) функциональный объем мочевого резервуара, как правило, не превышал 400 мл при достаточно высоком внутрирезервуарном давлении (Таблица 4). В более отдаленном периоде объем резервуара возрастал в среднем до 600 мл, а внутрирезервуарное давление постепенно снижалось. Такую динамику мы также связываем с постепенной ликвидацией спазма мускулатуры кишки, вызванной операционной травмой и постоянным контактом с такой агрессивной средой, какой является моча, а также адаптацией кишечного резервуара к новой функции и контакту с мочой.
Сравнение зарегистрированных параметров не выявили достоверных различий между двумя исследуемыми группами. Как в I, так и во II группах объем резервуаров в течение 6-12 месяцев достигал необходимых функциональных величин. Внутрирезервуарное давление во все сроки наблюдения в обеих группах не превышало 40 см водн. ст., что было ниже критических значений, потенциально опасных в плане ухудшения функции почек [14, 15].
Все больные I и II групп в отдаленном периоде социально реабилитированы. 8 пациентов I группы смогли вернуться к трудовой деятельности. Во II группе 4 больных вернулись к своей прежней специальности, еще 8 человек также сохранили работоспособность, но трудятся на более легкой работе.
Итак, обе анализируемые нами методики континентной деривации мочи способны обеспечить хорошие функциональные результаты и социальную реабилитацию большинства больных. Методика формирования толстокишечного резервуара с аппендикостомой обеспечивала наименьшую частоту осложнений и не сопровождалась госпитальной летальностью пациентов. Высокая частота осложнений у больных с уретеросигмостомией, безусловно, утяжеляет течение послеоперационного периода, однако, в большинстве случаев их удается купировать консервативно. Среди осложнений преобладают осложнения воспалительного (острый пиелонефрит) и метаболического (гиперхлоремический метаболический ацидоз) характера. Относительно высокая летальность при уретеросигмостомии, по нашему мнению, не связана с методикой операции, а обусловлена недооценкой исходной тяжести состояния пациентов.
Заключение
Исходя из проведенного анализа, считаем, что методика деривации мочи путем формирования толстокишечного кондуита является предпочтительным методом у больных трудоспособного возраста, нуждающихся в качественной социальной реабилитации, не имеющих серьезных сопутствующих заболеваний, препятствующих выполнению кишечной цистопластики (выраженные заболевания сердечно-сосудистой системы, легких и желудочно-кишечного тракта). Наш опыт показывает, что данный метод деривации мочи может быть успешно применен даже при 3-4-й стадии опухолевого процесса и при тотальном поражении мочевого пузыря при отсутствии регионарных метастазов. Степень дифференцировки опухоли также не оказывала существенного влияния на функциональный исход операции.
Ключевые слова: рак мочевого пузыря, методы деривации мочи, континентный толстокишечный мочевой резервуар, уретеросигмостомия.
Keywords: urinary bladder cancer, urine derivation methods, continental ileocecal conduit, ureterosigmostomy.
Литература
- Oncological and functional outcome of radical cystectomy in patients with bladder cancer and obstructive uropathy / Gupta N.P., Kolla S.B., Seth A., Hemal A.K., Dogra P.N., Kumar R. // J. Urol. 2007. Vol. 178, № 4. P. 1206- 1211.
- Morbidity and quality of life in elderly patients receiving ileal conduit or orthotopic neobladder after radical cystectomy for invasive bladder cancer / Sogni F., Brausi M., Frea B., Martinengo C., Faggiano F., Tizzani A., Gontero P. // Urology. 2008. Vol. 71. № 5. P. 919-923.
- Health related quality of life after radical cystectomy: comparison of ileal conduit to continent orthotopic neobladder. / Autorino R., Quarto G., Di Lorenzo G., De Sio M., Perdonà S., Giannarini G., Giugliano F., Damiano R. // Eur. J. Surg. Oncol. 2009. Vol. 35. № 8. P. 858-864.
- Measuring health-related quality of life outcomes in bladder cancer patients using the Bladder Cancer Index (BCI) / Gilbert S.M., Wood D.P., Dunn R.L., Weizer A.Z., Lee C.T., Montie J.E., Wei J.T. // Cancer. 2007. Vol. 109. № 9. P. 1756-1762.
- Даренков С.П., Соколов А.Е., Оччархаджиев С.Б. Ближайшие и отдаленные результаты уретеросигмостомии с формированием резервуаров Mainz pouch II и Хасана // Урология. 2004. № 2. C. 7-12.
- Матвеев Б.П., Фигурин К.М., Карякин О.Б. Рак мочевого пузыря. М. 2001. 243 с.
- Переверзев А.С., Петров С.Б. Опухоли мочевого пузыря. Харьков: «Факт». 2002. 301 с.
- Перепечай В.А. Обоснование ортотопической сигмопластики для восстановления мочевого пузыря: Дис. … канд. мед. наук. Ростов-на-Дону. 2000. 171 с.
- Continence mechanism of the orthotopic neobladder: urodynamic analysis of ileocolic neobladder and exyernal urethral sphincter function / Kakizaki H., Shibata T., Ameda K., Shinno Y., Nonomura K., Koyanagi T. // Int. J. Urol. 1995. Vol. 2. № 4. P. 267-272.
- Nocturnal enuresis in men with an orthotopic ileal reservoir: urodynamic evaluation. / El Bahnasawy M.S., Osman Y., Gomha M.A., Shaaban A.A., Ashamallah A., Ghoneim M.A. // J. Urol. 2000. Vol. 164. № 1. P. 10-13.
- Compartomiento urodinamico de las neovejigas intestinales; nuestra experiencia // Lorenzo Romero J.G., Segura Martin M., Salinas Sanchez A., Hernandez Millan I., Martinez Martin M., Virseda Rodriguez J. // Arch. Esp. Urol. 2001. Vol. 54. № 2. P. 139-144.
- A simple technique of urinary diversion: the dismembered detubularized rectosigmoid bladder with distal colorectostomy / Elabbady A.A., Elabbasy W.I., Arafa A.F., Atta M.A., Abdel-Rahman M. // J. Urol. 1998. Vol. 160. № 3. P. 714-715.
- Тилляшайхов М.Н. Хирургические и физиологические аспекты выбора метода деривации мочи после радикальной цистэктомии по поводу рака мочевого пузыря. Дисс. ... д-ра мед. наук. Ташкент. 2008.
- Churchill B.M., Gilmour R.F., Williot P. Urodynamics // Pediatr. Clin. North Amer. 1987. Vol. 34. P. 1133-1157.
- The type of urinary diversion after radical cystectomy significantly impacts on the patient's quality of life /McGuire M.S., Grimaldi G., Grotas G., Russo P. // Ann. Surg. Oncol. 2000. Vol. 7. № 1.P. 4-8.
| Прикрепленный файл | Размер |
|---|---|
| Статья в формате PDF | 361.19 кб |















































































