Влияние переменного магнитного поля на растворимость органоминералов человека в водных растворах мочевины in vitro
 9647
9647 В работе Попкова В.М. с соавт. [1] приведены результаты эксперимента по определению влияния переменного магнитного поля (ПМП) в диапазоне 2-22 Гц на растворимость находящегося в воде диспергированного органоминерала из организма человека. С помощью спектрофотометрических и ареометрических измерений авторами [1] было установлено, что максимальный отклик системы на воздействие ПМП при растворении органоминералов в условиях in vitro наблюдался при частоте ~2 Гц и был на 14% выше, чем в контроле (без воздействия ПМП). Авторы отмечали, что влияние магнитного поля (МП), регистрируемое также по изменению величины плотности в этих суспензиях, связано с растворением органической составляющей этих минералов и выходом мочевины в состав растворителя. Следует отметить, что мочевина оказывала существенное влияние на изменение плотности этих растворов.
Возникает вопрос о влиянии мочевины на общий ход реакции растворения в присутствии ПМП. Как известно, мочевина, находясь в составе водного раствора, является эффективным растворителем как органических, так и неорганических веществ [2]. Задача настоящего исследования – установить степень влияния мочевины в составе водного раствора, в том числе предварительно обработанного ПМП частотой 2 Гц, на процесс растворения органоминералов человека in vitro.
МАТЕРИАЛЫ И МЕТОДЫ
В экспериментах использовались органоминералы (оксалатного типа), предоставленные кафедрой урологии Саратовского государственного медицинского университета, мочевина ЧДА ГОСТ 6691-71. В качестве опытных растворов использовали водные растворы мочевины различной концентрации, в которые помещались образцы мочевых камней. Контрольный раствор на дистиллированной воде с мочевым камнем находился в той же лаборатории при фоновых уровнях МП, характерных для места проведения опытов. Во всех экспериментах (контрольных и опытных) использовались образцы от одного донора.
Исходные образцы мочевых камней взвешивались на аналитических весах фирмы OHAUS Corp. RV214 с точностью 0,0001 г. Приготовленные растворы мочевины, используемые в опытах, обрабатывались магнитным полем при частоте поля 2 Гц с индукцией 50 мТл в течение 1 часа [3]. Растворимость органоминерала в опытах определяли по выходу в раствор органической составляющей мочевых камней спектрофотометрическим методом, а также весовым методом. Регистрацию проводили через каждые 60 мин воздействия ПМП на спектрофотометре Shimadzu UV-1700 (Япония) при комнатной температуре в кварцевых кюветах размером 1×1×4,5 см. Спектры анализировали в максимумах поглощения матричных белков мочевых камней при длине волны 289-293 нм [1]. Нерастворенную часть суспензий промывали дистиллированной водой, а затем обсушивали на фильтре под струей горячего воздуха. Окончательную дегидратацию мочевых камней проводили в СВЧполе с использованием генератора типа Г4-141, после чего проводили взвешивание на аналитических весах. Дальнейшее фотометрирование проводили с надосадочным раствором.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Для того чтобы исследовать влияние концентрации мочевины на процесс растворения мочевых камней, был проведен следующий эксперимент. Предварительно измельченный органоминерал помещался в водные растворы мочевины с различной концентрацией на 1 час. В качестве контрольного раствора использовались водные растворы мочевины без камня. На рисунке 1 приведены результаты зависимости оптической плотности D от концентрации мочевины на длине волны 290 нм. Как следует из приведенных результатов, максимальная растворимость белковой фракции органоминерала наблюдалась при концентрации мочевины 10.36 г на 100 мл воды. Именно такое значение концентрации мочевины было выбрано нами для дальнейших исследований, что соответствует величинам, используемым при исследованиях in vivo (0,4 – 30 г на 100 мл воды) [4]. Следует отметить, что оптическая плотность контрольного раствора на длине волны 290 нм незначительно изменялась при изменении концентрации мочевины.
Дальнейшие эксперименты проводили с исходно целыми органоминералами.
На рисунке 2 приведена зависимость величины оптической плотности D на длине волны максимума поглощения белковой фракции 290-292 нм растворов мочевых камней от способов их приготовления и времени воздействия ПМП. Из полученных результатов следует, что уже спустя 1 час после начала эксперимента наблюдалось достоверное увеличение оптической плотности опытных растворов мочевины с камнем и мочевины с камнем обработанной ПМП с частотой 2 Гц по сравнению с контрольным раствором камня в воде. Величина оптической плотности продуктов растворения органоминералов в растворе мочевины при одновременном воздействии ПМП после 4-х часового растворения примерно в 21,5 раз превышала величину оптической плотности при растворении в обычной дистиллированной воде, а для случая, когда воздействия ПМП на раствор не осуществлялось примерно в 20,4 раза по сравнению с контрольным раствором. Различие в оптической плотности опытных растворов мочевины с камнем, на которые осуществлялось воздействие ПМП, и растворов мочевины с камнем без МП, с течением времени становилось менее выраженным: в течение 1-го часа отношение оптической плотности растворов с камнем, мочевиной и полем к оптической плотности растворов с камнем и мочевиной составило 1,46 раза; через 2 часа – 1,15; через 3 часа – 1,07 и через 4 часа 1,06 раза соответственно. Уменьшение этого отношения можно объяснить увеличением эффективности воздействия мочевины как химического фактора при длительном процессе растворения мочевых камней над ПМП. Необходимо отметить, что результаты измерений, полученные спектральным методом, дают лишь качественную оценку влияния воздействующих факторов на исследуемые растворы в силу того, что при реакции в раствор выходит мелкодисперсная взвесь, влияя при этом на величину оптической плотности. В связи с этим, для определения количества растворенного вещества органоминерала был проведен прямой весовой метод, результаты измерений которого приведены на рисунке 3.
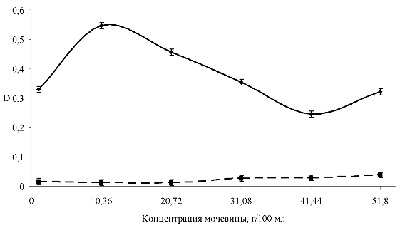
Рис. 1. Зависимость оптической плотности растворов мочевины от ее концентрации
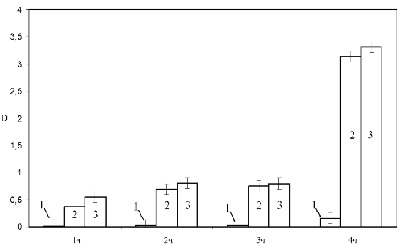
Рис. 2. Зависимость величины оптической плотности растворов мочевых
камней от способов их приготовления и времени воздействия ПМП:
1 – дистиллированная вода с камнем
2 – водный раствор мочевины с камнем
3 – водный раствор мочевины + ПМП 2 Гц + камень
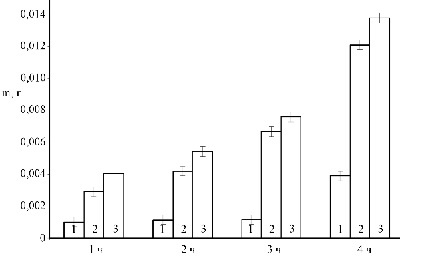
Рис. 3. Весовой метод определения количества растворенного вещества органоминерала при
различной пробоподготовке и времени воздействия ПМП:
1 – дистиллированная вода с камнем; 2 – водный раствор мочевины с камнем
3 – водный раствор мочевины + ПМП 2 Гц + камень
Для этого были выбраны три исходно целых органоминерала от одного донора близкие по массе. Первый органоминерал, исходная масса которого до опытов составляла 0,0479 г, растворялся затем в обычной дистиллированной воде. Второй органоминерал с исходной массой 0,0417 г растворялся в растворе мочевины, а третий с исходной массой 0,0443 г – в растворе мочевины, обработанным ПМП частотой 2 Гц. Согласно полученным результатам растворенная часть мочевого камня при его растворении в обработанном ПМП растворе мочевины превышает значения растворенной части минерала в растворе мочевины без воздействия поля, в ~1,4 раза после 1-го часа растворения, в ~1,3 раза после 2-го часа, в ~1,13 раза после 3-го часа и в ~1,14 раза после 4-го часа соответственно. Также в результате 4-х часового растворения минералов обнаружено, что в обычной воде растворилось 8,14% от исходной массы образца, в растворе мочевины без воздействия поля 29,02%, а в предварительно обработанном ПМП частотой 2 Гц растворе мочевины – 31,15%.
ЗАКЛЮЧЕНИЕ
Результаты проведенных исследований с помощью фотометрического и весового методов свидетельствуют об эффективности применения мочевины для усиления процесса растворения мочевых камней человека in vitro, как в присутствии ПМП, так и в его отсутствии. Максимальная растворимость мочевых камней наблюдалась при предварительной обработке раствора мочевины с помещенным в него мочевым камнем ПМП с частотой 2 Гц в течение 4 часов.
Резюме:
В настоящее время изучается вопрос о влиянии мочевины на общий ход реакции растворения в присутствии переменного магнитного поля (ПМП). Как известно, мочевина, находясь в составе водного раствора, является эффективным растворителем как органических, так и неорганических веществ.
Задача настоящего исследования заключалась в установлении степени влияния мочевины в составе водного раствора, в том числе предварительно обработанного ПМП частотой 2 Гц, на процесс растворения органоминералов человека in vitro. Для этого растворимость органоминерала в опытах была определена по выходу в раствор органической составляющей мочевых камней спектрофотометрическим методом, а также весовым методом. Показано, что величина оптической плотности продуктов растворения органоминералов в растворе мочевины при одновременном воздействии ПМП после 4-х часового растворения примерно в 21,5 раза превышала величину оптической плотности при растворении в обычной дистиллированной воде, а для случая, когда воздействия ПМП на раствор не осуществлялось примерно в 20,4 раза по сравнению с контрольным раствором. Также в результате 4-х часового растворения минералов весовым методом обнаружено, что в обычной воде растворилось 8,14% от исходной массы образца, в растворе мочевины без воздействия поля 29,02%, а в предварительно обработанном ПМП частотой 2 Гц растворе мочевины – 31,15%.
Это свидетельствует об эффективности применения мочевины для усиления процесса растворения мочевых камней человека in vitro, как в присутствии ПМП, так и в его отсутствии.
ЛИТЕРАТУРА
1. Попков В.М., Усанов Д.А., Усанов А.Д., Ребров В.Г., Верхов Д.Г., Буланов В.М. Влияние низкочастотного магнитного поля на растворимость органоминералов человека оксалатного типа в воде in vitro. // Саратовский научно-медицинский журнал. 2012. Т. 8, N 3. С. 735-738.
2. Зотов А.Т. Мочевина. М.: Гос. науч.-техн. изд-во хим. литературы, 1963. 173 с.
3. Устройство для воздействия магнитным полем на биообъекты. Патент на полезную модель. А61N2/00 (2006.01), опубл. 20.01.2008. Сучков С.Г., Усанов Д.А., Сергеев А.А., Усанов А.Д., Сучков Д.С., Селифонов А.В.
4. Cook WH, Alsberg CL. Preparation of glutenin in urea solutions. // Canad J Res. 1931. Vol. 5, N 3. P. 355-374.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 129.78 кб |















































































