Возможности эхографии на этапах лечения рака предстательной железы методом ультразвуковой абляции (HIFU)
 9970
9970 В настоящее время рак предстательной железы (РПЖ) является одной из наиболее значимых медицинских проблем у мужчин. Ежегодно в мире регистрируется более 500 000 новых случаев РПЖ. В России же РПЖ занимает 4-е место среди всех опухолевых заболеваний у мужчин после рака легких, желудка и кожи. За последние годы отмечается значительный рост заболеваемости РПЖ. Так абсолютный прирост впервые выявленных случаев за 10 лет превышает 75%, а по темпам ежегодного прироста данная нозология вышла на первое место в структуре онкологических заболеваний [1, 2, 3]. Именно поэтому диагностике и лечению РПЖ в последнее время уделяется все больше внимания, как за рубежом, так и в Российской Федерации.
По статистике около 75% всех случаев РПЖ обнаруживается у мужчин старше 65 лет. В этом возрасте большинство пациентов имеет осложненный интеркуррентный фон, что не позволяет проводить им радикальное хирургическое лечение. Для этих пациентов, а также для тех, кто отказался от открытой операции из-за возможных осложнений, предложен ряд альтернативных методик, одной из которых является трансректальная высокоинтенсивная фокусированная ультразвуковая абляция предстательной железы (HIFU – High Intensity Focused Ultrasound) [4].
В клинических испытаниях было показано, что HIFU способен разрушать заданный объем предстательной железы (ПЖ) в результате локальной гипертермии и развивающегося коагуляционного некроза, при этом не повреждая окружающие ткани [5, 6, 7].
Несмотря на целый ряд статей, посвященных данному методу лечения РПЖ, до сих пор уточняются показания к HIFU-терапии, изучается эффективность сочетания с другими методами, оцениваются различные схемы мониторинга пациентов после процедуры.
Поэтому, целью нашего исследования явилась оценка возможностей эхографии на этапах лечения рака ПЖ методом ультразвуковой абляции; определение эхографических особенностей ПЖ после HIFU-терапии, а также оценка роли ультразвуковой томографии в мониторинге пациентов после вмешательства.
МАТЕРИАЛЫ И МЕТОДЫ
Проанализированы результаты исследования 41 пациента в возрасте от 50 до 79 лет (средний возраст 66±7 лет), пролеченных методом HIFUтерапии. Диагноз РПЖ (локализованная форма, Т1-Т2N0M0) был выставлен в результате стандартного обследования по поводу повышенного уровня ПСА от 6 до 38 нг/мл (13,3±7,9 нг/мл), которое включало пальцевое ректальное исследование; трансректальное ультразвуковое исследование (ТРУЗИ); мультифокальную пункционную биопсию ПЖ под ультразвуковым контролем.
На дооперационном этапе всем пациентам ТРУЗИ проводилось на аппарате Acuson «S 2000» (Siemens, Германия) c использованием внутриполостного конвексного датчика (с частотами 4-8 МГц) по стандартной методике. При этом определялся объем, оценивались эхоструктура и васкуляризация ПЖ с целью выявления гипоэхогенных участков, либо зон гиперваскуляризации, требующих проведения прицельной пункционной биопсии, а также исключалась раковая инфильтрация стенки прямой кишки и измерялась ее толщина.
Трансректальная мультифокальная пункционная биопсия ПЖпроводилась из 12 точек и при необходимости дополнительно прицельно из 1-4 точек с раздельной маркировкой всех полученных фрагментов тканей [2,4].
Также всем пациентам (100%) на дооперационном этапе были выполнены магнитно-резонансная томография органов малого таза для исключения метастатического поражения регионарных лимфатических узлов и сцинтиграфия костей скелета для исключения отдаленных метастазов.
Практически всем мужчинам (n=40, или 98%) перед сеансом HIFU проводилась биполярная трансуретральная резекция (ТУР) ПЖ. Цель данного вмешательства заключалась в уменьшении объема железы, а также для снижения риска острой задержки мочи и инфекционных осложнений после сеанса HIFU [4]. Рекомендуемый объем ПЖ для HIFU-терапии 20-30 см3.
Процедура HIFU выполнялась посредством роботизированной системы Ablatherm® (EDAP, Франция). В качестве наведения в данном аппарате использовался ультразвук. В процессе HIFU лечения применялся режим «обстрела» по типу единичного выстрела с фокусом эллипсоидной формы до 1,9–2,4 см в длину и около 0,17 см в диаметре. Продолжительность одного импульса составила 5 с, перерыв между импульсами – 5 с. При лечении ПЖ со средним объемом 15-25 см3 требовалось около 400-600 импульсов. Вся процедура занимала около 2-3 часов [4, 5].
Среднее время наблюдения после ультразвуковой абляции – 9 мес. Уровень ПСА после сеанса HIFU-терапии определялся через 1, 3, 6 и 9 мес., ультразвуковое исследование ПЖ проводилось через 3, 6, и 9 мес. При этом оценивались степень редукции объема ПЖ, ее эхоструктура и васкуляризация.
Полученные результаты обрабатывались стандартными методами статистики. Значения непрерывных величин представлялись в виде M±SD, где M – выборочное среднее арифметическое и SD – стандартное отклонение. В случаях нормального распределения, а также равенства выборочных дисперсий, для сравнения выборок использовали t-критерий Стьюдента.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
По данным ТРУЗИ до ультразвуковой абляции объем ПЖ варьировал от 26 до 64 см3 (ср. объем 40,9±9,3 см3). Гипоэхогенные участки, требующие проведения прицельной пункционной биопсии, в В-режиме визуализировались у 11 (27 %) обследованных мужчин, преимущественная локализация данных фокусов (n=10, или 91%) – периферические отделы ПЖ. У одного (9%) пациента гипоэхогенный узел лоцировался в центральной эхозоне. Еще у двух (5%) человек отмечались диффузные изменения ПЖ с отсутствием дифференцировки между эхозонами. У 25 (61%) пациентов РПЖ сочетался с ДГПЖ.
Диффузное повышение васкуляризации от умеренно выраженного до значительного в режимах цветового допплеровского картирования (ЦДК) и энергетического допплеровского картирования (ЭДК) было выявлено у 12 (29%) пациентов. Еще у 5 (12%) человек определялись участки гиперваскуляризации, совпадающие с гипоэхогенными зонами в В-режиме.
По результатам морфологического исследования биопсийного материала во всех случаях опухоль имела строение аденокарциномы разной степени дифференцировки.
На этапе подготовки к HIFU-терапии после ТУР объем ПЖ варьировал от 13,5 до 40 см3 (среднее значение 25,3±7,2 см3).
При ультразвуковом мониторинге во время процедуры HIFU отмечалось увеличение размеров ПЖ, значительное повышение ее эхогенности, появление признаков кавитации в виде ярких гиперэхогенных вспышек.
Достоверное снижение объема ПЖ было выявлено через 3 мес. после HIFU-терапии (р< 0,001) и составило 59% от первоначального (16,6±6,4 см3) (рис. 1). Также у всех обследованных пациентов определялись нечеткие, неровные контуры ПЖ, усиление неоднородности эхоструктуры за счет участков неравномерного повышения эхогенности, в 65% (n=27) случаев нечеткость контуров между задней поверхностью ПЖ и прямой кишкой (рис. 2). У 31 (76%) пациента была повышена эхогенность перипро-статической клетчатки. В режиме ЦДК и ЭДК у 10 (24%) мужчин сохранялось умеренное повышение васкуляризации по периферии. Участков гиперваскуляризации выявлено не было.
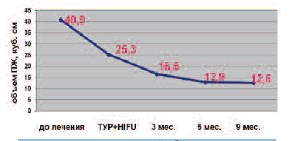
Рис. 1. Динамика изменений объема предстательной железы на этапах лечения методом HIFU-терапии
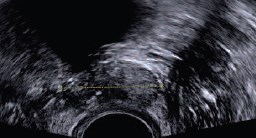
Рис. 2. Эхограмма предстательной железы после сеанса HIFU
Через 6 мес. после лечения редукция объема ПЖ составила 68% от первоначального (12,9±5,9 см3). Изменения эхоструктуры ПЖ в В-режиме практически не отличались от выявленных через 3 мес. после процедуры HIFU. Умеренное повышение васкуляризации по периферии сохранялось у 7 (17%) человек.
Через 9 мес. редукция объема ПЖ составила 70% от первоначального (12,16±5,37 см3). Повышение периферической васкуляризации сохранялось у 5 (12%) пациентов.
На рис. 3 представлена динамика уровня ПСА. Гистологические исследования биоптатов, проведенные через 5 мес. после лечения, выявили полное разрушение железистой ткани и замену ее фиброзной.
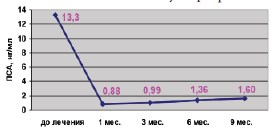
Рис. 3. Динамика уровня ПСА на этапах лечения методом HIFU-терапии
Положительные результаты контрольных мультифокальных биопсий под ультразвуковым наведением, выполненных в интервале 5-9 мес. после лечения, были выявлены у 4-х пациентов. Двум из них проведен повторный сеанс HIFU-терапии, еще двум пациентам с поражением верхушки ПЖ предложены другие методы лечения.
ОБСУЖДЕНИЕ
Эхография, имея огромную диагностическую ценность, применяется на всех этапах лечения локализованных форм рака ПЖ методом ультразвуковой абляции.
Так на дооперационном этапе ультразвуковое исследование позволило измерить объем ПЖ, что имело большое значение при планировании ТУР. Важна роль ТРУЗИ при оценке эхоструктуры и васкуляризации ПЖ с целью выявления прямых, косвенных и допплерографических признаков ракового поражения [8]. Данный метод позволил также исключить признаки местнораспространенного процесса, в том числе и раковую инфильтрацию стенки прямой кишки, что имело большое значение при отборе пациентов для HIFU терапии.
Трансректальная мультифокальная пункционная биопсия под ультразвуковым контролем являлась обязательной процедурой диагностического алгоритма, позволившая более четко локализовать зоны ракового поражения ПЖ [2, 8, 9].
Во время предварительной HIFU– разметки производилось смещение зоны фокуса от левой доли ПЖ к правой, располагая участки абляции один за другим до тех пор, пока не был покрыт весь срез (рис. 4).
Во время процедуры HIFU импульсами высокоинтенсивного ультразвука последовательно проводилось лечение каждого слоя ПЖ. В реальном времени посредством эхографии осуществлялась оценка состояния ПЖ, перипростатической клетчатки, стенок мочевого пузыря и прямой кишки. Оценка эффективности лечения также осуществлялась с помощью ультразвукового исследования в реальном времени. Эхографическими признаками воздействия высокоинтенсивного ультразвука на ткань ПЖ являлись: увеличение размеров ПЖ, неравномерное повышение ее эхогенности, появление ярких гиперэхогенных вспышек.
Редукция объема ПЖ после проведения HIFU-терапии, выявленная при контрольных ТРУЗИ, отмечалась в течение первых 6 месяцев, достигая в среднем 68% от первоначальных значений. Помимо уменьшения объема, были выявлены следующие особенности ультразвуковой картины ПЖ: нечеткость, неровность ее контуров, нечеткость контуров между задней поверхностью ПЖ и стенкой прямой кишки, усиление неоднородности эхоструктуры ПЖ за счет участков неравномерного повышения эхогенности, соответствущих фиброзным изменениям. В ряде случаев отмечалось усиление процесса микрокальцинации, как периуретрально, так и диффузно, а также повышение эхогенности перипростатической клетчатки. Вышеописанные изменения эхоструктуры ПЖ в В-режиме визуализировались через 3 мес. после лечения и практически не менялись при повторных исследованиях.
ЗАКЛЮЧЕНИЕ
Представленные нами данные свидетельствуют о важной роли эхографии на всех этапах лечения РПЖ методом ультразвуковой абляции, а именно:
- на дооперационном этапе с целью диагностики и отбора пациентов для лече-ния;
- во время проведения процедуры с целью оценки ее эффективности;
- в послеоперационном периоде с целью мониторинга результатов лечения.
ЛИТЕРАТУРА
1. Статистика злокачественных новообразований в России и странах СНГ в 2007 г. [Под. ред. Давыдова М.И., Аксель Е.М.]. // Вестник Российского онкологического научного центра им. Н.Н.Блохина РАМН. 2009. Т.20, N 3 (77). 52 c.
2. Аполихин О.И., Сивков А.В., Москалева Н.Г., Солнцева Т.В., Комарова В.А. Анализ урологической заболеваемости и смертности в Российской Федерации в 2010-2011 годах. // Экспериментальная и клиническая урология. 2013. N 2. С. 10-17
3. Аполихн О.И., Сивкоа А.В., Солнцева Т.В., Комарова В.А. Анализ урологиче-ской заболеваемости в Российской Федерации в 2005-2010 годах. // Экспериментальная и клиническая урология . 20121. N 2. С. 4-12.
4. Крупинов Г. Е. Лечение больных раком предстательной железы высокоинтен-сивным фокусированным ультразвуком: Дис. … д-ра мед. наук. М., 2010. 306 с.
5.Назаренко Г.И., Хитрова А.Н. Ультразвуковая аблация опухолей человека или лечение опухолей высокоэнергетическим фокусированным ультразвуком (HIFU). М.: МЦ Банка России. 2008. 32 с.
6. Назаренко Г.И., Чен В.Ш., Хитрова А.Н. Ультразвуковая абляция (HIFU) вы-сокотехнологичная органосохраняющая альтернатива хирургического лечения опухо-лей. – М.:МЦ Банка России. 2008. С.51-54.
7. Kennedy JE, Ter Haar GR, Granston D. High intensity focused ultrasound: surgery of the future? // Br J Radiol. 2003. Vol. 76, N 909. Р. 590-599.
8. Шолохов В.Н., Бухаркин Б.В., Лепэдату П.И. Ультразвуковая томография в диагностике рака предстательной железы. Фирма СТРОМ. 2006. 112 с.
9. Панфилова Е.А. Эластография в дифференциальной диагностике рака пред-стательной железы: Дис. …канд. мед. наук. М., 2011. 130 с.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 792.89 кб |















































































