Выбор метода дренирования мочевого пузыря при HIFU-терапии рака предстательной железы
 8682
8682 Рак предстательной железы (РПЖ) считается сегодня одной из самых серьезных медицинских проблем, связанных с мужским здоровьем. По распространенности заболевание занимает второе место после рака легких у мужчин и третье место в мире среди причин смерти от рака [1]. Совершенствование диагностики позволило выявлять РПЖ на ранней стадии, что привело к внедрению в клиническую практику широкого спектра малоинвазивных методов лечения с целью достижения контроля над заболеванием без значимой потери в качестве жизни пациента. Яркие примеры такого лечения – это брахитерапия, HIFU (high-intensity focused ultrasound)терапия и криоабляция. Радикальная простатэктомия уже давно рассматривается как золотой стандарт лечения пациентов с локализованной формой РПЖ, но, несмотря на хорошие результаты по долгосрочной выживаемости, имеет ряд недостатков. Хирургическое лечение всегда сопряжено с высокой стоимостью операции, длительным послеоперационным периодом и возможностью возникновения серьезных осложнений. Радикальная простатэктомия не показана пациентам, ожидаемая продолжительность жизни которых составляет менее 10 лет и пациентам со значительной сопутствующей патологией. Данный вид лечения, также как и лучевая терапия, показал негативное влияние на качество жизни пациентов с большим количеством осложнений, связанных с мочеиспусканием, сексуальными расстройствами и нарушением функции желудочно-кишечного тракта [2].
Целью любого лечения является увеличение продолжительности жизни при сохранении наилучшего качества жизни. Этого и помогает добиться малоинвазивная хирургия.
HIFU-терапия является классическим примером малоинвазивного метода лечения рака предстательной железы, и рассматривается на сегодняшний день как достойная альтернатива радикальной простатэктомии в лечении локализованного РПЖ [3]. Это относительно новая технология, суть которой заключается в индуцировании мгновенного и необратимого коагуляционного некроза ткани предстательной железы путем термического воздействия (поглощенная ультразвуковая энергия тканью преобразуется в тепло) и кавитации. Ультразвуковые волны, излучаемые датчиком, направлены исключительно на ограниченную, заранее размеченную область предстательной железы, таким образом, отсутствует повреждение окружающих тканей, что является одним из достоинств данного вида лечения.
В настоящее время применение HIFU в лечении РПЖ официально утверждено в Европе, Канаде, Южной Корее, Австралии и т. д. За последнее время проведено довольно много исследований, демонстрирующих эффективность данного вида терапии в плане выживаемости и биохимического рецидива, возможности нервосбережения при поражении опухолью одной доли предстательной железы, описываются возникшие осложнения. Однако существует не так много исследований, затрагивающих проблему профилактики и борьбы с осложнениями данной операции.
К описанным осложнениям и побочным эффектам HIFU-абляции относятся: уретроректальный свищ, ожог/ разрыв прямой кишки или ректальное кровотечение, дискомфорт или боль (например, при мочеиспускании, в сидячем положении, в надлобковой области/ в животе, анальном отверстии и т.д.), позывы к мочеиспусканию или опорожнению кишечника, недержание мочи или кала (риск недержания мочи возрастает у больных после простатэктомии или лучевой терапии), снижение или отсутствие эрекции, пониженная, ретроградная или отсутствующая эякуляция, инфекция мочевых путей (ИМП). Также могут возникнуть такие осложнения, как простатит, эпидидимит и другие инфекции, стриктура уретры, частое мочеиспускание или ноктурия, задержка мочи, в том числе, требующая врачебного вмешательства, геморроидальные боли, кровотечение, в некоторых случаях с образованием сгустков, гематурия или гемоспермия. Из всех перечисленных осложнений, клинически значимыми и требующими в предоперационном периоде профилактики, а в послеоперационном – дополнительной длительной коррекции (лечения) являются инфекционно-воспалительные осложнения (ИВО), дизурические явления, проблемы с эрекцией и ректоуретральные свищи. ИВО являются серьезной проблемой в послеоперационном периоде, так как замедляют процесс восстановления после операции, а также удлиняют период госпитализации. На их долю приходится 12,5% от всех осложнений, и они представлены, в основном, эпидидимитом, пиелонефритом и циститом (рис.1) [4]. И если проблему обструктивных симптомов решает выполнение трансуретральной резекции и послеоперационного дренирования мочевого пузыря, уретроректальных свищей – интегрированная охлаждающая система, то проблема ИВО остается неизменной с момента внедрения HIFU в клиническую практику.
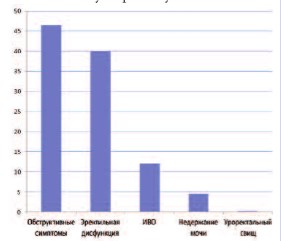
Рис. 1. Основные послеоперационные осложнения HIFU-терапии [4].
Целью нашего исследования являлось определение факторов, предрасполагающих к возникновению ИВО у больных после HIFU.
МАТЕРИАЛЫ И МЕТОДЫ
В клинике урологии Военно-медицинской академии им. С. М. Кирова в период с сентября 2008 по июнь 2013 года выполнены сеансы HIFU-терапии на аппарате Ablatherm (EDAP, Франция) 98 пациентам. Критериями включения пациентов в исследование являлся локализованный РПЖ стадии Т1-Т2N0M0 и местнораспространенная аденокарцинома стадии T3аN0M0. Всем больным проводилось клиническое обследование, включавшее сбор анамнеза, клинический анализ крови и мочи, биохимический анализ крови, посев мочи на флору и чувствительность к антибиотикам, коагулограмма, концентрация простатспецифического антигена (ПСА) в сыворотке крови, пальцевое ректальное и ультразвуковое исследование предстательной железы, органов брюшной полости и забрюшинного пространства, трансректальная мультифокальная биопсия железы, магнитнорезонансная томография малого таза и остеосцинтиграфия.
Всем пациентам проводилась трансуретральная резекция предстательной железы с целью уменьшения объема обрабатываемой при процедуре абляции ткани и улучшения показателей уродинамики после операции.
Исходные данные пациентов представлены в таблице 1.
Таблица 1. Клинико-лабораторные и инструментальные данные обследования пациентов перед HIFU-терапией
| Показатели | |
|---|---|
| Количество пациентов, чел. (%) | 98 (100%) |
| Средний возраст, лет | 66,2 (48 – 73) |
| Объем предстательной железы до ТУР, см3 | 39,5 (20 81) |
| Объем предстательной железы после ТУР, см3 | 22,8 (15 – 36) |
| Объем остаточной мочи, мл | 44,6 (10 – 76) |
| Урофлоуметрия (Q max), мл/сек | 17,2 (8 39) |
| ПСА, нг/мл | 8,8 (0,819,3) |
| Т1-Т2 стадия, чел. (%) | 69 (70,4%) |
| Т3а стадия, чел. (%) | 29 (29,4%) |
Таблица 2. Структура ИВО после HIFU в зависимости от посева мочи на предоперационном этапе
| Группа пациентов | ИВО | Без ИВО |
||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Результат посева мочи | Всего | Эпидидимит | Пиелонефрит | Цистит | ||||||
| абс. | % | абс. | % | абс. | % | абс. | % | абс. | % | |
| Рост м\о (+) (Группа I) | 45 | 46 | 10 | 22,2 | 6 | 13,3 | 8 | 17,8 | 21 | 21,4 |
| Рост м\о () (Группа II) | 53 | 54 | 5 | 9,4 | 3 | 5,7 | 4 | 7,5 | 41 | 48,8 |
Все пациенты были разделены на 2 группы. Первую группу, в которую вошли 45 пациентов, составили мужчины, имеющие положительный посев мочи (т. е. имелся рост микроорганизмов в концентрации ≥ 105 КОЕ/мл). По данным посева мочи в 95% высеялась Escherichia coli, остальные 5% составили Staphylococcus saprophyticus, Enterobacter cloacae, Klebsiella pneumonia, Proteus vulgaris. Всем пациентам была проведена антибиотикотерапия в соответствии с результатом посева мочи. Вторую группу составили 53 пациента с отрицательным посевом мочи (рост микроорганизмов отсутствовал). Каждая из групп была поделена на 2 подгруппы – в одной после абляции был установлен уретральный катетер сроком на 10 суток, во второй – накладывалась эпицистостома с последующим перекрыванием ее на 3-и сутки после абляции с попытками самостоятельного мочеиспускания. В послеоперационном периоде все пациенты получали следующую схему медикаментозной терапии: альфа–адреноблокатор (тамсулозин 0,4 мг в сутки), фторхинолоны (ципрофлоксацин 500 мг два раза в сутки) до 10 дней и нестероидные противовоспалительные препараты (ректальные свечи диклофенак 50 мг) до 5 дней [5].
РЕЗУЛЬТАТЫ
Результаты сравнительной оценки возникновения осложнений в зависимости от результата посева мочи представлены в таблице 2. У пациентов, имеющих стерильную мочу, эпидидимит, пиелонефрит и цистит возникали почти в 2 раза реже, чем у больных с лабораторно значимой бактериурией.
Из сравнительного анализа методов дренирования мочевого пузыря, видно, что при положительном посеве мочи, при наложении эпицистостомы эпидидимит, пиелонефрит и цистит возникает в 2,5-3 раза чаще, чем при установке уретрального катетера. При отрицательном посеве мочи, при наложении эпицистотомы эпидидимит, пиелонефрит и цистит также наблюдался в 1,5-2 раза чаще относительно катетеризации мочевого пузыря (табл. 3).
Таким образом, установка уретрального катетера максимально эффективно предотвращает инфекционновоспалительные осложнения в послеоперационном периоде при HIFU-терапии.
Таблица 3. Сравнительная оценка ИВО в зависимости от метода дренирования мочевого пузыря
| Группа пациентов | Осложнения | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Результат посева мочи | Метод дренирования |
Всего | Эпидидимит | Пиелонефрит | Цистит | ||||
| абс. | % | абс. | % | абс. | % | абс. | % | ||
| Рост м\о (+) (Группа I) | Уретральный катетер | 26 | 57,8 | 3 | 11,5 | 2 | 7,7 | 3 | 11,5 |
| Эпицистостома | 19 | 42,2 | 7 | 36,8 | 4 | 21,1 | 5 | 26,3 | |
| Рост м\о () (Группа II) | Уретральный катетер | 29 | 54,7 | 2 | 6,9 | 1 | 3,4 | 2 | 6,9 |
| Эпицистостома | 24 | 45,3 | 3 | 12,5 | 2 | 8,3 | 2 | 8,3 | |
ОБСУЖДЕНИЕ
HIFU-терапия на сегодняшний день является перспективным направлением в лечении РПЖ, и также, как и любое вмешательство, связано с определенными особенностями ведения преди послеоперационного периода.
В нашем исследовании всем пациентам проводилась трансуретральная резекция предстательной железы. После операции в простатическом отделе уретры имеется раневая поверхность. Как и любая рана, она подвержена большому риску присоединения инфекции. К тому же, почти у половины больных в предоперационном периоде имеется положительный посев мочи. Предшествующая трансуретральная резекция и положительный посев мочи является двумя основными предрасполагающими факторами к появлению инфекций, даже несмотря на проведение соответствующей антибактериальной терапии.
Дренирование мочевого пузыря является неотъемлемой частью при HIFU-терапии, так как имеет место обструкция нижних мочевых путей вследствие отека предстательной железы. Не существует единого мнения относительно метода их дренирования.
Уретральный катетер предохраняет простатический отдел уретры от попадания инфицированной мочи на раневую поверхность после трансуретральной резекции, тем самым снижая риск возникновения осложнений. Полученные нами при сравнении перечисленных методик данные подтверждают, что эпидидимит, пиелонефрит и цистит на фоне эпицистостомы возникают значительно чаще.
ЗАКЛЮЧЕНИЕ
У пациентов, имевших при предоперационном обследовании в посеве мочи рост микроорганизмов, риск появления инфекционно-воспалительных осложнений в послеоперационном периоде выше почти в 3 раза, несмотря на адекватную антимикробную терапию. Установка уретрального катетера с целью дренирования мочевого пузыря в послеоперационном периоде при HIFUтерапии является методом выбора. Наложение эпицистостомы является нецелесообразным, так как связано с большим количеством послеоперационных инфекционно-воспалительных осложнений.
1. Iberti C, Mohamed N, Palese M. A Review of Focal Therapy Techniques in Prostate Cancer: Clinical Results for High-Intensity Focused Ultrasound and Focal Cryoablation. // MedReviews. 2011. Vol.13, №4. P.196-202.
2. Mearini L, Porena M. Transrectal high-intensity focused ultrasound for the treatment of prostate cancer: Past, present, and future. // Indian Journal of Urology. 2010. Vol. 26, №1. P.4-11.
3. Аполихин О.И., Сивков А.В., Шадеркин И.А., Кешишев Н.Г., Ковченко Г.А. HIFUтерапия рака предстательной железы. // Экспериментальная и клиническая урология. 2011. №2-3. С. 4852.
4. Кристиан Шосси. Мировой опыт HIFU-терапии РПЖ. // Экспериментальная и клиническая урология. 2011. №2-3. С. 44-47.
5. Кардиналова В.А., Елоев Р.А., Протощак В.В., Шестаев А.Ю. Инфекционновоспалительные осложнения при HIFU-аблации предстательной железы. // Онкоурология. Материалы VIII конгресса Российского общества онкоурологов. 2013. С. 54.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 668.54 кб |















































































