Резекция почки является общепризнанным стан дартом в лечении больных клинически локализо ванными опухолями почечной паренхимы. Со вершенствование операционной техники привело к накоплению опыта технически сложных орга носохраняющих операций при неудобных для ре зекции опухолях, в том числе – у пациентов с нормальной контралатеральной почкой. Для унифика ции описания анатомических характеристик новообра зований почечной паренхимы предложено использовать несколько нефрометрических шкал, показатели которых коррелируют с результатами резекции почки. Наиболь шее распространение получили классификации PADUA и RENAL. Безопасными считаются резекции почки, вы полняемые при индексе PADUA <8 и/или индексе RENAL <7. При более высоких нефрометрических ин дексах, как правило, выполняется радикальная нефрэ ктомия [1,2]. Небольшое количество наблюдений за больными, подвергнутыми технически сложной резек ции почки при опухолях с высоким нефрометрическим индексом, не дает представления об истинной частоте и тяжести осложнений таких операций, их функциональ ных и отдаленных онкологических результатах. В отде лении урологии НМИЦ онкологии им. Н.Н. Блохина накоплен значительный опыт подобных вмешательств. Целью нашего исследования являлся анализ результатов ре зекций почки у больных опухолями почечной паренхимы с индексом PADUA ≥8 баллов и/или RENAL ≥7 баллов.
Артерии мышечного типа являются внутриорган ными. Это касается коронарных и сегментарных почеч ных артерий. В состав внутренней оболочки артерии входят: эндотелий с базальной мембраной, субэндотели альный слой и внутренняя эластическая мембрана. Эн дотелиальные клетки, расположенные на базальной мембране, вытянуты вдоль продольной оси сосуда, их повреждение приводит к образованию пристеночных тромбов. Кнаружи от субэндотелиального слоя располо жена тесно связанная с ним внутренняя эластическая мембрана. В более крупных артериях мышечного типа эластическая мембрана отчетливо выражена. Средняя оболочка артерии содержит гладкомышечные клетки, расположенные по пологой спирали, между которыми находятся в небольшом числе соединительнотканные клетки и волокна (коллагеновые и эластические). Роль опорного каркаса для миоцитов выполняют коллагено вые волокна. Спиральное расположение мышечных кле ток и их сокращение обеспечивает продвижение тока крови [5]. Эластические волокна стенки артерии на гра нице с наружной и внутренней оболочками сливаются в единый эластический каркас, который придает сосуду эластичность при растяжении и упругость при сдавле нии. Эластический каркас обусловливает постоянное зияние артерий и непрерывность в них тока крови. Бал лонная дилатация артерий травмирует среднюю обо лочку, в которой при гистологических исследованиях обнаруживается инфильтрация нейтрофильных лейко цитов, которые играют роль в процессе воспаления, и рубцевания тканей [6,7].
При выполнении баллонной ангиопластики коро нарных артерий происходит механическое растяжение тканей сосуда, травматизация эндотелия, эластичные слои растягиваются, нередко разрываются. Травматиза ция эндотелия снижает антитромбические функции стенки сосуда, что вызывает образование пристеночных тромбов. Повреждение среднего слоя стенки сосуда при водит к воспалительным процессам, разрастанию фиб розной ткани [4,6,7], вследствие чего может возникнуть стенозирование [6].
Пункция артерии для проведения эндоваскулярной баллонной эмболизации, ввиду отработанности техники и профилактики осложнений, максимально безопасна. По данным Ю.Г. Матчина и соавт., технические ослож нения в виде гематом места пункции, ваготонических реакций, окклюзий артерии регистрировались в единич ных случаях [8]. Такое серьезное осложнение, как пер форация коронарной артерии при проведении ангио пластики, с накоплением опыта и совершенствованием методик также имеет минимальный риск и, как правило, разрешается без оперативного вмешательства [9]. В до ступной нам литературе не нашлось указаний на изме нения стенок интраорганных сосудов ветвей почечной артерии при транслюминальных вмешательствах. Также отсутствуют сведения об изменениях паравазальных тканей почки при суперселективной окклюзии почеч ной артерии. Восполнению этих пробелов посвящено настоящее исследование.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование ретроспективно и проспективно включены медицинские данные 122 больных, подверг нутых резекции почки по поводу опухолей почечной па ренхимы с нефрометрическим индексом ≥8 баллов по шкале PADUA и/или ≥7 баллов по шкале RENAL. Обли гатные показания к органосохраняющему лечению име лись у 65 (53,3%), факультативные – у 57 (46,7%) пациен тов. Облигатные показания к резекции почки включали: опухоль паренхимы единственной почки у 50 (41,0%) (после нефрэктомии с контралатеральной стороны по поводу рака почки – 28 (23,0%), по поводу другого забо левания – 2 (1,6%), нефункционирующая вторая почка – 9 (7,4%), врожденная единственная почка – 9 (7,4%), под ковообразная почка – 2 (1,6%)) и двухсторонние опу холи почек у 15 (12,3%) больных. У 57 (46,7%) пациентов контралатеральная почка функционировала.
Медиана возраста пациентов составила 57 (23-80) лет. Соотношение мужчин и женщин – 1,3:1. При обсле довании у всех пациентов были выявлены опухоли почеч ной паренхимы: одностороннее поражение имело место у 77 (63,1%), двухстороннее – у 43 (36,9%) больных.
Из 43 пациентов с двухсторонними опухолями почек в 28 (23,0%) случаях новообразования почечной паренхимы выявлены метахронно, и с контралатеральной стороны ранее была выполнена нефрэктомия, в среднем, за 56,1 (1 386) месяца до резекции. У 15 (12,3%) больных на момент включения в исследование имелось двухстороннее пора жение, при этом опухоли контралатеральной почки были классифицированы как соответствующие категориям сТ2b-T3aN0M0 и являлись показанием к последующей радикальной нефрэктомии. Показанием к резекции с равной частотой служили опухоли правой (47,5%) и левой почек (52,5%). Подробная нефрометрическая характери стика опухолей почечной паренхимы приведена в таблице 1. Категория сТ1 диагностирована у 99 (81,2%), сТ2 – у 22 (18,0%), сТ3а – у 1 (0,8%) пациента. В 4 (3,3%) случаях вы явлены увеличенные до 1-2,5 см регионарные лимфоузлы (категория сN1). Отдаленных метастазов не диагностиро вано ни у одного больного.
Медиана индекса сопутствующих заболеваний Чарльсона составила 5,0 (2-11). По классификации Аме риканского Общества Анестезиологов (ASA) операцион ный риск оценен как ASA 1-2 у 72,1%, ASA 3-4 – у 27,8% пациентов.
Исходная функция почек оценивалась у всех боль ных. Медиана скорости клубочковой фильтрации (СКФ) в группе составила 81 (26-142) мл/мин/1,73 м2. Всем паци ентам в связи с наличием опухоли почки установлен ди агноз хронической болезни почек (ХБП) (1-2 стадий – 100 (92,0%), 3-4 стадий – 22 (18,0%) больных).
Всем больным выполнили резекцию почки (открытую – 120 (98,4%), лапароскопическую – 2 (0,6%)), в 120 (98,4%) наблюдениях – в условиях ишемии почечной паренхимы (путем пережатия почечных артерии и вены – 67 (54,9%), почечной артерии – 47 (38,5%), сегментарной артерии – 6 (4,9%)). Наружное охлаждение почки ледяной крошкой применялось во время 59 (48,4%) операций. Медиана дли тельности ишемии составила 23,0 (6-78) минуты (тепловой – 22,3 (6-47) минут, холодовой – 27,1 (6-78) минут; р=0,014). Интраоперационное ультразвуковое исследование (УЗИ) почки потребовалось во время 11 (9,0%) операций для уточ нения локализации опухоли. У 7 (5,7%) пациентов обнару жены дополнительные опухолевые очаги, не выявленные до операции (в 2 (1,6%) случаях – при УЗИ). У 113 (92,6%) пациентов удален один, у 9 (7,4%) – более одного опухоле вого узла (2 – 6 (4,9%), 3 – 2 (1,6%), 9 – 1 (0,8%) больному). В 3 (2,5%) наблюдениях выполнена энуклеорезекция, в 119 (97,5%) – истинная резекция почки. 8 (6,5%) пациентам с опухолевым венозным тромбозом сегментарных вен, вы явленным во время резекционного этапа, произведена тромбэктомия. Собирательная система вскрыта в 22 (19,3%) случаях, мочеточниковый стент интраоперационно уста новлен 4 (3,5%) больным. В 5 (4,1%) случаях производилось срочное гистологическое исследование, при этом в 2 (1,6%) препаратах были выявлены клетки опухоли, что послужило показанием к немедленной дополнительной ре зекции почки.
Пятнадцати (12,3%) больным с опухолью контрала теральной почки, в среднем, в течение 3 (2-4) месяцев после органосохраняющего вмешательства выполнена нефрэктомия с другой стороны. Ни одному пациенту после хирургического лечения не проводилось дополни тельное противоопухолевое лечение.
Медиана наблюдения составила 55,0±29,8(4-142) ме сяца. Для статистической обработки все данные о пациентах и результатах их лечения формализованы с помощью разработанного кодификатора и внесены в базу данных, созданную на основе электронных таблиц EXCEL. Степень тяжести осложнений резекции почки оценивалась по классификации Клавьена-Диндо [3]. Почечная функция оценивалась с помощью вычисления расчетной СКФ по формуле the Modification of Diet in Renal Disease study, ее изменения классифицировалась по системе National Kidney Foundation/Kidney Disease Outcomes Quality Initiative (KDOQI) classification до хирургического лечения и в позд нем послеоперационном периоде (>28 дней) [4], по си стеме RIFLE – в раннем послеоперационном периоде (≤28 дней) [5]. Продолжительность жизни рассчитывали от даты хирургического вмешательства до последнего дня на блюдения или смерти. Статистический анализ полученных результатов проводили с помощью известных статистиче ских методов при использовании блока программ «SPSS 16.0 for Windows».
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Медиана длительности резекции почки у 122 паци ентов составила 150 (60-320) мин, медиана объема крово потери – 600 (10-4500) мл. Переливание компонентов крови потребовалось во время 15 (12,2%) резекций почки. Медиана числа перелитых доз эритроцитарной массы со ставила 1 (1-4), свежезамороженной плазмы – 1 (1-4).
Интраоперационные осложнения резекции почки развились у 6 (4,9%) пациентов. Во всех случаях имело место трудно контролируемое кровотечение из зоны ре зекции, сопровождавшееся массивной (>1000 мл) крово потерей. У всех пациентов кровотечение остановлено путем прошивания краев резекции, нефрэктомия не по требовалась ни в одном наблюдении.
Осложнения раннего послеоперационного периода зарегистрированы у 32 (26,2%) больных (1-2 степеней тя жести по Клавьену-Диндо – 25 (20,5%), 3-4 степеней тяже сти – 7 (5,7%)). Летальных исходов (осложнения 5 степени тяжести) не зарегистрировано. У 14 (11,4%) пациентов развились урологические осложнения: кровотечение из зоны резекции (2 (1,6%)) и мочевой затек (12 (9,8%)). Кро вотечение из зоны резекции почечной паренхимы в обоих случаях послужило показанием к назначению гемостати ческой терапии и было остановлено консервативно. Трем (25,0%) пациентам, у которых было подтверждено поступ ление мочи по страховым дренажам, под рентгенологиче ским контролем были установлены JJ-стенты, что привело к ликвидации мочевых затеков в течение 3-12 суток после операции. В 9 (75,0%) случаях дренирование мочевых путей не потребовалось, отделение мочи из зоны резекции купировалось самостоятельно в течение 3-5 суток после опе рации. В 5 (4,1%) наблюдениях после операции диагности рован тромбоз вен нижних конечностей, у 11 (9,0%) больных, подвергнутых резекции левой почки, развился отечный неинфицированный панкреатит, у 8 (6,6%) па циентов – послеоперационная пневмония.
Осложнения позднего послеоперационного периода зарегистрированы у 2 (1,6%) пациентов и были представ лены стриктурой верхней трети мочеточника, по поводу которой одному больному выполняли баллонную дила тацию и стентирование и одному – только стентирование мочеточника JJ-стентом с положительным эффектом.
Анализ возможного влияния характеристик паци ентов, нефрометрических показателей опухоли, техни ческих особенностей резекции почки на длительность операции, объем операционной кровопотери, частоту и степень тяжести осложнений не выявил независимых факторов риска.
В раннем послеоперационном периоде медиана СКФ у больных, подвергнутых резекции почки, составила 53 (7 120) мл/мин/1,73 м2. Медиана отклонения СКФ от исход ного уровня достигла -30,5% (0 – -87%). Острое снижение почечной функции было задокументировано у 82 из 122 (67,2%) больных, в большинстве случаев относилось к ка тегории R (42,6%) и, гораздо реже, – I (15,6%) и F (6,6%) по системе RIFLE. Длительная утрата почечной функции, соответствующая категории L, имела место у 2 (1,7%) па циентов. У одного (0,8%) больного развилась терминаль ная стадия почечной недостаточности (категория E) с сохранением водовыделительной функции. Показания к острому гемодиализу имели место у 5 (4,1%) пациентов. В среднем, проводилось 2 (1-10) сеанса гемодиализа.
В логистическом регрессионном анализе единствен ным независимым фактором риска острого снижения по чечной функции являлись облигатные показания к резекции почки (отношение рисков (ОР) = 8,9 (95% дове рительные интервалы (ДИ): 3,5-21,7; p<0,0001). Для паци ентов с функционирующей второй почкой (n 57) независимыми факторами риска являлись индекс Чарль сона ≥6 (ОР=2,3 (95% ДИ: 1,4-3,9); р=0,002) и длитель ность любой ишемии почечной паренхимы > 20 мин (ОР=1,2 (95% ДИ: 1,1-1,4); р=0,004). Независимыми факто рами риска острого снижения почечной функции до кате горий F, L, E являлись время любой ишемии >20 мин (ОР =1,1 (95% ДИ: 1,0-1,2); p=0,05), удаление более одного опу холевого узла (ОР =2,7 (95% ДИ: 1,3-5,5); p=0,006) и объем кровопотери >500 мл (ОР =1,1 (95% ДИ: 1,0-1,2); p=0,008).
Медиана СКФ при медиане наблюдения 55,0±29,8 (4-142) месяца составила 55 (9-114) мл/мин/1,73 м2. Ме диана отклонения СКФ от исходных показателей до опе рации равнялась -22,0 (-13 – +87) мл/мин/1,73 м2. Уве личение СКФ >5 мл/мин/1,73 м2 по сравнению с исходными показателями отмечено у 2 (1,6%), стабилизация – у 16 (13,0%), снижение >5 мл/мин/1,73 м2 – у 104 (85,7%) паци ентов. Быстрое снижение СКФ (>5 мл/мин/1,73 м2 в год) за регистрировано у 7 (5,7%) больных. Прогрессирование ХБП отмечено в 88 (72,1%) наблюдений, при этом новые случаи ХБП 3-5 стадий зарегистрированы у 54 (44,3%) больных. Трое пациентов с сохранной водовыделительной функцией находятся на программном гемодиализе, вклю чая больного, которому проведение гемодиализа было на чато в раннем послеоперационном периоде.
В логистическом регрессионном анализе факто рами риска прогрессирования ХБП являлись: индекс Чарльсона ≥6 (ОР=1,3 (95%ДИ: 1,1-1,7); р=0,016), обли гатные показания к резекции почки (ОР=3,8 (95% ДИ: 1,7-8,4); р=0,01) и острое снижение почечной функции в раннем послеоперационном периоде (ОР=8,8 (95% ДИ: 3,1-25,1); р<0,0001). Для пациентов с функциони рующей второй почкой (n 57) независимую прогности ческую значимость продемонстрировало острое снижение почечной функции после резекции (ОР=8,8 (95% ДИ: 3,1-25,1); р<0,0001). Независимыми факторами риска развития тяжелой ХБП оказались: индекс Чарль сона ≥6 (ОР=2,1 (95%ДИ: 1,2-3,4); р=0,007) и острое сни жение почечной функции в раннем послеоперационном периоде (ОР=6,0 (95% ДИ: 1,3-27,2; р=0,021).
По данным планового гистологического исследова ния, одна (0,8%) опухоль имела строение аденомы, 121 (99,2%) – почечно-клеточного рака (ПКР) (светлоклеточ ного – 110 (90,2%), несветлоклеточного – 11 (9,0%)). Сте пень анаплазии ПКР расценена как G1 в 22 (18,0%), G2 – в 80 (65,6%), G3 – в 7 (5,7%), G4 – в 1 (0,8%) образце; степень анаплазии G не уточнена у 11 (9,0%) пациентов. Морфоло гически локализованный рак почки (pT1a-2b) имел место в 108 (88,5%) образцах; у 13 (10,7%) пациентов установлена категория рТ3а (прорастание паранефральной клетчатки – 7 (5,7%), опухолевая венозная инвазия в почечные вены, имеющие мышечную оболочку, – 8 (6,5%)). Гистологически медиана расстояния от опухоли до края резекции парен химы составила 5 (0-15) мм, хирургический отступ ≤ 1 мм был в 13 (10,6%) препаратах, а клетки опухоли по краю раз реза обнаружены в 2 (1,6%) образцах. Результаты срочного гистологического исследования оказались верны во всех 5 наблюдениях. Ни в одном из 4 образцов, полученных во время лимфодиссекции, метастазов не выявлено.
Из 43 больных двусторонними опухолями почечной паренхимы опухоль второй удаленной почки у 1 (2,3%) па циента имела строение онкоцитомы, у 42 (97,7%) боль ных – ПКР (pT1a-2b – 32 (76,2%), рТ3а – 2 (4,8%), pTx – 8 (19,0%)). Разное гистологическое строение опухолей левой и правой почек подтверждено в 3 (7,0%) наблюдениях.
Таблица 1. Характеристика больных
Table 1. Patient characterization
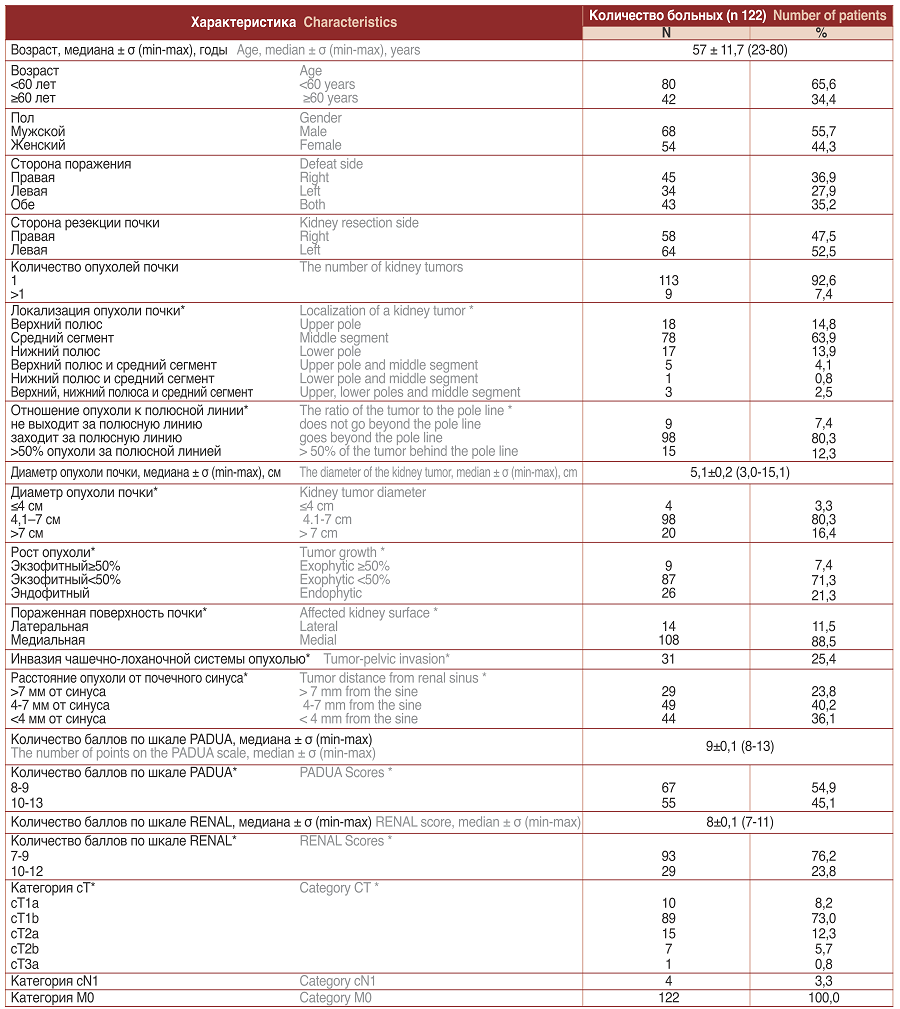
*при наличии >1 опухоли почечной паренхимы нефрометрические характеристики оценивались для новообразования, технически наиболее неудобного для резекции
* in the presence of> 1 tumor of the renal parenchyma, nephrometric characteristics were evaluated for the neoplasm, which is technically the most inconvenient for resection
Пациент, оперированный по поводу аденомы почеч ной паренхимы, жив в течение 69 месяцев после резекции почки без признаков рецидива. При медиане наблюдения 55,0±29,8 (4-142) месяца из 121 больного раком почки 106 (87,6%) живы: 103 (85,1%) – без признаков болезни, 3 (2,5%) – с метастазами; 15 (12,4%) умерли: 3 (2,5%) – от про грессирования рака почки, 12 (9,9%) – от других причин, без метастазов (7 (5,8%) – от сердечно-сосудистых заболеваний, 1 (0,8%) – от пневмонии, 1 (0,8%) – от рака предстательной железы, у 3 (2,5%) причина смерти не уточнена).
Безрецидивная и ракоспецифическая выживаемость рассчитывались для 121 больного раком почки, общая и кардиоспецифическая выживаемость – для всех 122 па циентов. Пятилетняя общая, ракоспецифическая, кардио специфическая и безрецидивная выживаемость составили 91,5%, 95,2%, 93,9% и 91,5%, соответственно. Медианы данных показателей не достигнуты.
Однофакторный анализ не выявил значимого влия ния характеристик рака почки (сторона поражения, время выявления опухоли второй почки у пациентов с двухсторонними опухолями, количество опухолевых узлов, категория pT, степень анаплазии G) и величины хи рургического отступа на безрецидивную выживаемость 121 больного ПКР, подвергнутого резекции почки (р>0,05 для всех). Недостаточное количество смертей от рака почки (3/121 (2,5%)) не позволило провести анализ фак торов риска ракоспецифичекой выживаемости.
В однофакторном анализе не отмечено значимого влияния почечной функции на кардиоспецифическую вы живаемость. Отмечается недостоверное снижение 5-летней кардиоспецифической выживаемости у пациентов с исходной ХБП ≥3 степени тяжести (с 91,9% до 93,1%), у больных, перенесших острую почечную недостаточность в раннем послеоперационном периоде (с 94,0% до 92,7%) и в случае развития клинически значимой ХБП в процессе среднесрочного наблюдения (с 96,2% до 90,5%) (р>0,05 для всех). Пол и наличие ожирения не оказывали влияния на кардиоспецифичесую выживаемость (p>0,05 для всех). От мечено достоверное снижение 5-летней кардиоспецифиче ской выживаемости у пациентов, оперированных в возрасте ≥60 лет (с 98,4% до 81,9%, р<0,0001), имеющих ин декс сопутствующих заболеваний ≥6 (с 97,1% до 81,7%, р<0,0001), а также операционный риск по шкале ASA 3-4 (с 97,2% до 87,2%, р=0,004). Независимыми факторами риска кардиоспецифической выживаемости являлись возраст на момент операции (отношение шансов (ОШ)=9,5 (95% дове рительные интервалы (ДИ): 2,6-35,4); р=0,001) и индекс Чарльсона≥6 (OШ=5,8 (95% ДИ: 1,1-31,7); р=0,041).
Однофакторный анализ не выявил зависимости общей выживаемости от пола, ожирения, стороны поражения почки опухолью и времени развития опухоли второй почки при двухстороннем раке, количества опухолевых узлов, ка тегории pT, степени анаплазии G, величины хирургического отступа, а также исходных и итоговых показателей почечной функции (р>0,05 для всех показателей). Отмечено значимое снижение 5-летней общей выживаемости у пациентов, опе рированных в возрасте ≥60 лет (с 97,1% до 84,3%, р<0,0001), имеющих индекс сопутствующих заболеваний ≥6 (с 96,0% до 84,3%, р<0,0001), а также операционный риск по шкале ASA 3-4 (с 95,0% до 87,2%, р=0,038). Независимым фактором риска общей выживаемости являлся индекс Чарльсона ≥6 (OШ=6,2 (95% ДИ: 2,1-18,4); р=0,001).
Ключевые результаты исследования приведены в таблице 2.
Таблица 2. Результаты резекции почки
Table 2. Results of kidney resection
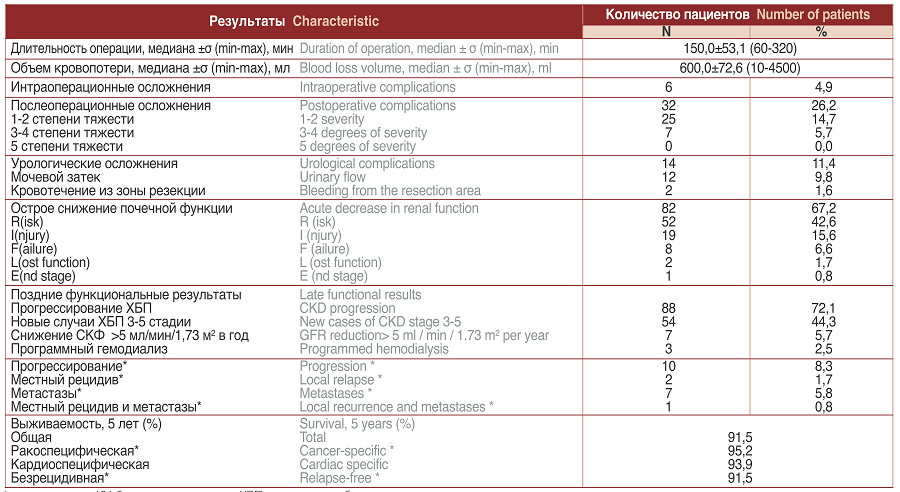
*рассчитано для 121 больного раком почки. ХБП – хроническая болезнь почек
* Designed for 121 patients with kidney cancer. CKD – chronic kidney disease
В абсолютном большинстве национальных и меж дународных клинических рекомендаций органосохра няющие операции рассматриваются как метод выбора для лечения пациентов с клинически локализованными опухолями почечной паренхимы, подходящими для ре зекции. Хирургическая и онкологическая безопасность, а также функциональный исход технически сложных ре зекций почки практически не изучались. С целью стан дартизации отбора кандидатов для технически сложной резекции почки мы выбрали наиболее широко валиди рованные нефрометрические шкалы RENAL и PADUA, отражающие анатомические особенности опухолей по чечной паренхимы. В качестве пограничных значений использовались ≥8 баллов по шкале PADUA и/или ≥7 баллов по шкале RENAL. Несомненно, выбранные шкалы не лишены недостатков, поскольку не учитывают ряда усложняющих хирургическое вмешательство осо бенностей, таких как предшествующие операции, коли чество опухолевых узлов, внутрипочечный опухолевый венозный тромбоз и аномалии развития почек. Точность систем RENAL и PADUA в отношении прогнозирования частоты осложнений резекции почки подтверждается не всеми исследователями [6], однако в настоящее время это наиболее простые в использовании универсальные шкалы, позволяющие унифицировать и сравнивать ре зультаты разных серий наблюдений [7].
Длительность технически сложной резекции почки в нашем исследовании (медиана – 150 мин) была сопо ставима с результатами открытых органосохраняющих операций у неотобранных больных, приведенных в дру гих публикациях (123-238 мин) [8,9]. Операционная кро вопотеря оказалась приемлемой (медиана – 600 мл) и послужила показанием к переливанию компонентов крови в 12,2% случаев. У неотобранных пациентов в се риях наблюдений, опубликованных другими хирургами, медиана кровопотери колебалась от 200 мл до 653 мл, ча стота гемотрансфузий составила 0-15,7% [9,10].
Несмотря на то, что некоторые исследования не подтверждают прогностическую значимость существую щих нефрометрических шкал [11], многими авторами отмечено повышение риска осложнений резекции почки при опухолях с высокими индексами RENAL и PADUA [12,13]. Единственным видом интраоперационных осложнений в нашей серии наблюдений являлось труд ноконтролируемое кровотечение из зоны резекции, раз вившееся у 4,9% больных. Эти показатели соответствуют результатам, полученным при анализе данных открытых резекций почки у неотобранных пациентов в других ле чебных учреждениях (1,5-5,1%) [8-10]. Осложнения ран него послеоперационного периода зарегистрированы у 26,2% наших пациентов и достигли 3-4 степеней тяжести в 5,7% случаев. Кровотечение из зоны резекции зареги стрировано в 1,6%, мочевой затек – в 9,8% наблюдений. Наши результаты соответствуют ранее опубликованным данным других клиник. Частота послеоперационных осложнений открытой резекции почки всех степеней сложности в разных сериях колеблется от 13% до 29,3%, осложнений 3-5 степеней тяжести – от 1,1% до 9,1%, кро вотечений – от 0% до 6%, мочевых затеков – от 2,1% до 18,5% [8-14]. Несмотря на высокие нефрометрические индексы RENAL и PADUA, частота осложнений, вклю чая нежелательные явления 3-4 степеней тяжести и уро логические осложнения, в нашем исследовании ока залась приемлемой. Все зарегистрированные нежела тельные явления удалось скорректировать без ущерба для почечной функции. Полученные результаты свиде тельствуют об относительной безопасности выполнения органосохраняющих вмешательств у больных опухо лями почки с высоким нефрометрическим индексом в центрах с большим опытом подобных вмешательств.
На основании анализа функциональных результа тов 344 резекций почки, R. Gupta и соавт. заключили, что нефрометрические индексы по шкалам RENAL и PADUA коррелируют с надиром СКФ в раннем послеопе рационном периоде (р<0,005) [15]. J.R. Bylund и соавт. от метили значимую взаимосвязь индекса PADUA и изме нений СКФ после резекции почки [16]. Эти данные поз воляют предполагать потенциальную возможность ухудшения функциональных результатов по мере повы шения технической сложности органосохраняющих вме шательств. Острое снижение почечной функции разви лось у 67,2% наших больных, достигло категорий F, L и E у 9,1% пациентов, являлось показанием к острому ге модиализу в 4,1% случаев и привело к терминальной по чечной недостаточности у 1 (0,8%) больного. В ретро спективном одноцентровом исследовании, включившем 1955 неотобранных пациентов, подвергнутых резекции почки, почечная дисфункция по критериям Acute Kidney Injury Network [17], регистрировалась реже, чем в нашей серии наблюдений (39%), и имела I степень тяжести у 33%, II степень тяжести – у 4% и III степень тяжести – у 2% пациентов [18]. Использование разных определений и шкал для оценки степени изменений почечной функ ции в исследовании, цитируемом выше, и нашей работе не позволяет сравнивать полученные результаты.
Ожидаемо, в нашей популяции с высокой долей па циентов, имевших единственную функционирующую почку, единственным независимым фактором риска ост рого снижения почечной функции являлись облигатные показания к резекции (p<0,0001); частота регистрации категорий почечной недостаточности F, L, E достоверно коррелировала с длительностью любой ишемии >20 мин (p=0,05), количеством удаленных опухолевых узлов (p=0,006) и объемом кровопотери >500 мл (p=0,008). У больных с функционирующей второй почкой значи мый вклад в снижение почечной функции в раннем послеоперационном периоде вносили индекс Чарльсона ≥6 (р=0,002) и длительность ишемии >20 мин (р=0,004). Большинство авторов также указывает на увеличение риска острого нарушения почечной функции при выполнении резекции почки по облигатным показаниям [19,20]. Ухудшение непосредственных функциональных результатов по мере увеличения времени ишемии про демонстрировано в некоторых исследованиях, в том числе – в работах, включивших пациентов, подвергну тых органосохраняющему лечению при наличии функ ционирующей второй почки [19]. Обращает на себя внимание, что в нашем исследовании наружное охлаж дение почки, направленное на снижение риска постише мических повреждений канальцев, не влияло на функ циональные результаты. Вероятнее всего, это связано с осознанным применением холодовой ишемии в случаях, требующих длительного пережатия почечных сосудов, что может нивелировать положительное влияние гипо термии на функцию почки в послеоперационном пе риоде. Влияние количества опухолей на риск острого снижения почечной функции вполне объяснимо: чем больше количество удаляемых опухолевых узлов, тем меньше остается интактной паренхимы, в том числе – за счет ушивания зон резекций; кроме того удаление муль тифокальных опухолей занимает больше времени и тре бует более длительного пережатия почечных сосудов. Негативное влияние высокого индекса Чарльсона на не посредственные функциональные результаты может объясняться неблагоприятным воздействием комплекса сопутствующих заболеваний, таких как артериальная гипертензия, сахарный диабет, атеросклероз аорты и ее ветвей, на компенсаторные возможности почечного эн дотелия, поврежденного реативацией кислородного окисления вследствие развития реперфузионного син дрома после восстановления почечного кровотока. Кор реляция риска острого снижения почечной функции с объемом кровопотери, вероятно, обусловлена неадек ватной оксигенацией почечной паренхимы после ост рого ишемического повреждения у пациентов, пере несших операционное кровотечение [21].
В нашем исследовании при медиане наблюдения 55 месяцев медиана отклонения СКФ от исходного уровня до операции равнялась -22,0 мл/мин/1,73 м2, что существенно уступает результатам резекций почки, вы полненных по элективным показаниям (-0,49 – -16,6 мл/мин/1,73м2) [10,22]. У большинства наших больных (85,7%) в позднем послеоперационном периоде СКФ снижалась, однако высокий темп редукции СКФ реги стрировался редко (5,7%). Прогрессирование ХБП от мечено у 72,1% наших пациентов, при этом новые случаи ХБП 3-5 стадий зарегистрированы в 44,3% слу чаев. Трое больных находятся на программном гемодиа лизе. Опубликовано несколько серий наблюдений за пациентами, подвергнутыми технически сложным резек циям при опухолях почки ≥7 см, в которых зарегистри ровано снижение СКФ после операции по сравнению с исходной с 92,1 мл/мин/1,73 м2 до 65 мл/мин/1,73 м2 [23]; с 81 мл/мин/1,73 м2 до 55 мл/мин/1,73 м2 [24] и повыше ние сывороточного креатинина с 1,16 мг/дл до 1,26 мг/дл соответственно [25]. В исследовании C. Long и соавт., включившем 46 больных, которым было выполнено ор ганосохраняющее вмешательство при опухолях почеч ной паренхимы ≥7 см, в том числе, – множественных, повышение стадии ХБП было зарегистрировано в 10,9% наблюдений [26]. Несмотря на несопоставимые характе ристики пациентов в выборках, результаты которых представлены выше, частота сохранения почечной функции у больных, формально являющихся кандида тами для радикальной нефрэктомии, представляется удовлетворительной во всех цитируемых работах.
Факторами риска прогрессирования ХБП в нашей серии наблюдений являлись: индекс Чарльсона ≥6 (р=0,016), облигатные показания к резекции почки (р=0,01) и ост рое снижение почечной функции в раннем послеопера ционном периоде (р<0,0001). Для пациентов с функ ционирующей второй почкой независимую прогности ческую значимость продемонстрировало острое сниже ние почечной функции после резекции (р<0,0001). Независимыми факторами риска развития тяжелой ХБП оказались индекс Чарльсона ≥6 (р=0,007) и острое сни жение почечной функции в раннем послеоперационном периоде (р=0,021). Риск ухудшения поздних функцио нальных результатов при выполнении резекции почки по облигатным показаниям, отмеченный многими авто рами [27], несомненно, обусловлен меньшим количе ством функционирующих нефронов, остающихся при наличии единственной почки. Обращает на себя внима ние, что независимым фактором риска прогрессирова ния ХБП, в том числе – до 3-5 стадий, являлось острое снижение почечной функции, а не длительность ише мии, которая, собственно, вносила наибольший вклад в ухудшение ранних функциональных результатов в нашей серии наблюдений. Это с высокой степенью веро ятности свидетельствует о том, что именно клинически значимые постишемические повреждения, проявляв шиеся повышением уровня креатинина и/или сниже нием СКФ и/или редукцией темпа диуреза, в дальней шем способны привести к нефросклерозу и перманент ному снижению клубочковой фильтрации. Индекс Чарльсона как суррогатный критерий общего здоровья оказался строгим предиктором ХБП после технически сложной резекции почки. Надо отметить, что в немно гочисленных исследованиях и метаанализах, направлен ных на выделение факторов риска развития тяжелой ХБП в общей популяции, индексу сопутствующих забо леваний уделяется большое внимание, однако пока кор реляция суммы баллов по шкале Чарльсона и частоты ХБП 3-5 стадий не выявлено [28].
Облигатные показания к резекции почки, количе ство удаляемых почечных узлов и индекс Чарльсона – некорректируемые факторы неблагоприятного про гноза почечной функции. По сути, факторами риска развития почечной дисфункции, которые могут ниве лироваться хирургической техникой, являются продолжительность ишемии и объем кровопотери. Сни зить риск кровопотери >500 мл можно путем пережатия почечных сосудов. Повышение технической сложности вмешательства на резекционном и реконструктивном этапах закономерно увеличивает длительность ишемии. Этот факт подтверждается рядом исследований, выявив ших статистически значимую корреляцию между неф рометрическим индексом и временем пережатия по чечных сосудов во время резекции [16,29]. Возможными вариантами решения проблемы снижения риска пости шемических повреждений почечных клубочков яв ляются: выполнение резекции почки, находящейся в кровотоке (при ожидаемой кровопотере <500 мл или с использованием оборудования для возврата аутокрови), селективное пережатие сегментарных артерий, раннее восстановление почечного кровотока до завершения ос новных этапов операции, наложение непрерывных швов на зону резекции и высокий темп выполнения резекции и реконструкции.
Технически сложная резекция, выполненная нами 121 больному раком почки, включая 34,7% пациентов с двухсторонними опухолями и 10,7% больных раком почки pT3a, позволила добиться удовлетворительных отдаленных результатов. Пятилетняя общая, ракоспе цифическая, кардиоспецифическая и безрецидивная выживаемость составили 91,5%, 95,2%, 93,9% и 91,5%, соответственно. Независимыми факторами риска кар диоспецифической выживаемости являлись возраст (р=0,001) и индекс Чарльсона ≥6 (р=0,041); общей вы живаемости – индекс Чарльсона ≥6 (р=0,001). Результа тов сопоставимых по характеристикам серий наблю дений не опубликовано. В исследовании, включившем 46 больных раком почки pT2, подвергнутых резекции, 5-летняя общая и специфическая выживаемость соста вила 94,5% и 70,9% соответственно [26]. Пятилетняя безрецидивная, специфическая и общая выживаемость 80 пациентов, подвергнутых органосохраняющему хи рургическому лечению по поводу рака почки pT2 R. Kopp, равнялась 79,9%, 86,7% и 83,3%, соответственно [30].
ОБСУЖДЕНИЕ
В абсолютном большинстве национальных и меж дународных клинических рекомендаций органосохра няющие операции рассматриваются как метод выбора для лечения пациентов с клинически локализованными опухолями почечной паренхимы, подходящими для ре зекции. Хирургическая и онкологическая безопасность, а также функциональный исход технически сложных ре зекций почки практически не изучались. С целью стан дартизации отбора кандидатов для технически сложной резекции почки мы выбрали наиболее широко валиди рованные нефрометрические шкалы RENAL и PADUA, отражающие анатомические особенности опухолей почечной паренхимы. В качестве пограничных значений использовались ≥8 баллов по шкале PADUA и/или ≥7 баллов по шкале RENAL. Несомненно, выбранные шкалы не лишены недостатков, поскольку не учиты вают ряда усложняющих хирургическое вмешательство особенностей, таких как предшествующие операции, количество опухолевых узлов, внутрипочечный опухо левый венозный тромбоз и аномалии развития почек. Точность систем RENAL и PADUA в отношении прогно зирования частоты осложнений резекции почки под тверждается не всеми исследователями [6], однако в настоящее время это наиболее простые в использова нии универсальные шкалы, позволяющие унифициро вать и сравнивать результаты разных серий наблюде ний [7].
Длительность технически сложной резекции почки в нашем исследовании (медиана – 150 мин) была сопоставима с результатами открытых органосохра няющих операций у неотобранных больных, приведен ных в других публикациях (123-238 мин) [8,9]. Операционная кровопотеря оказалась приемлемой (ме диана – 600 мл) и послужила показанием к переливанию компонентов крови в 12,2% случаев. У неотобранных пациентов в сериях наблюдений, опубликованных дру гими хирургами, медиана кровопотери колебалась от 200 мл до 653 мл, частота гемотрансфузий составила 0 15,7% [9,10].
Несмотря на то, что некоторые исследования не подтверждают прогностическую значимость суще ствующих нефрометрических шкал [11], многими авто рами отмечено повышение риска осложнений резекции почки при опухолях с высокими индексами RENAL и PADUA [12,13]. Единственным видом интраоперацион ных осложнений в нашей серии наблюдений являлось трудноконтролируемое кровотечение из зоны резекции, развившееся у 4,9% больных. Эти показатели соответ ствуют результатам, полученным при анализе данных открытых резекций почки у неотобранных пациентов в других лечебных учреждениях (1,5-5,1%) [8-10]. Ослож нения раннего послеоперационного периода зареги стрированы у 26,2% наших пациентов и достигли 3-4 степеней тяжести в 5,7% случаев. Кровотечение из зоны резекции зарегистрировано в 1,6%, мочевой затек – в 9,8% наблюдений. Наши результаты соответствуют ранее опубликованным данным других клиник. Частота послеоперационных осложнений открытой резекции почки всех степеней сложности в разных сериях колеб лется от 13% до 29,3%, осложнений 3-5 степеней тяже сти – от 1,1% до 9,1%, кровотечений – от 0% до 6%, мочевых затеков – от 2,1% до 18,5% [8-14]. Несмотря на высокие нефрометрические индексы RENAL и PADUA, частота осложнений, включая нежелательные явления 3-4 степеней тяжести и урологические осложнения, в нашем исследовании оказалась приемлемой. Все заре гистрированные нежелательные явления удалось скорректировать без ущерба для почечной функции. Полу ченные результаты свидетельствуют об относительной безопасности выполнения органосохраняющих вмеша тельств у больных опухолями почки с высоким нефро метрическим индексом в центрах с большим опытом подобных вмешательств.
На основании анализа функциональных результа тов 344 резекций почки, R. Gupta и соавт. заключили, что нефрометрические индексы по шкалам RENAL и PADUA коррелируют с надиром СКФ в раннем после операционном периоде (р<0,005) [15]. J. Bylund и соавт. отметили значимую взаимосвязь индекса PADUA и из менений СКФ после резекции почки [16]. Эти данные позволяют предполагать потенциальную возможность ухудшения функциональных результатов по мере повы шения технической сложности органосохраняющих вмешательств. Острое снижение почечной функции развилось у 67,2% наших больных, достигло категорий F, L и E у 9,1% пациентов, являлось показанием к ост рому гемодиализу в 4,1% случаев и привело к терми нальной почечной недостаточности у 1 (0,8%) больного. В ретроспективном одноцентровом исследовании, включившем 1955 неотобранных пациентов, подвергну тых резекции почки, почечная дисфункция по крите риям Acute Kidney Injury Network [17], регистрирова лась реже, чем в нашей серии наблюдений (39%), и имела I степень тяжести у 33%, II степень тяжести – у 4% и III степень тяжести – у 2% пациентов [18]. Исполь зование разных определений и шкал для оценки сте пени изменений почечной функции в исследовании, цитируемом выше, и нашей работе не позволяет сравнивать полученные результаты.
Ожидаемо, в нашей популяции с высокой долей пациентов, имевших единственную функционирующую почку, единственным независимым фактором риска острого снижения почечной функции являлись обли гатные показания к резекции (p<0,0001); частота ре гистрации категорий почечной недостаточности F, L, E достоверно коррелировала с длительностью любой ишемии >20 мин (p=0,05), количеством удаленных опу холевых узлов (p=0,006) и объемом кровопотери >500 мл (p=0,008). У больных с функционирующей второй почкой значимый вклад в снижение почечной функции в раннем послеоперационном периоде вносили индекс Чарльсона ≥6 (р=0,002) и длительность ишемии >20 мин (р=0,004). Большинство авторов также указывает на увеличение риска острого нарушения почечной функ ции при выполнении резекции почки по облигатным показаниям [19,20]. Ухудшение непосредственных функциональных результатов по мере увеличения вре мени ишемии продемонстрировано в некоторых иссле дованиях, в том числе – в работах, включивших па циентов, подвергнутых органосохраняющему лечению при наличии функционирующей второй почки [19]. Об ращает на себя внимание, что в нашем исследовании наружное охлаждение почки, направленное на снижение риска постишемических повреждений канальцев, не влияло на функциональные результаты. Вероятнее всего, это связано с осознанным применением холодо вой ишемии в случаях, требующих длительного пережа тия почечных сосудов, что может нивелировать поло жительное влияние гипотермии на функцию почки в послеоперационном периоде. Влияние количества опу холей на риск острого снижения почечной функции вполне объяснимо: чем больше количество удаляемых опухолевых узлов, тем меньше остается интактной па ренхимы, в том числе – за счет ушивания зон резекций; кроме того удаление мультифокальных опухолей зани мает больше времени и требует более длительного пе режатия почечных сосудов. Негативное влияние высокого индекса Чарльсона на непосредственные функциональные результаты может объясняться небла гоприятным воздействием комплекса сопутствующих заболеваний, таких как артериальная гипертензия, са харный диабет, атеросклероз аорты и ее ветвей, на ком пенсаторные возможности почечного эндотелия, по врежденного реативацией кислородного окисления вследствие развития реперфузионного синдрома после восстановления почечного кровотока. Корреляция риска острого снижения почечной функции с объемом кровопотери, вероятно, обусловлена неадекватной ок сигенацией почечной паренхимы после острого ишеми ческого повреждения у пациентов, перенесших опера ционное кровотечение [21].
В нашем исследовании при медиане наблюдения 55 месяцев медиана отклонения СКФ от исходного уровня до операции равнялась -22,0 мл/мин/1,73 м2, что существенно уступает результатам резекций почки, вы полненных по элективным показаниям (-0,49 – -16,6 мл/мин/1,73м2) [10,22]. У большинства наших больных (85,7%) в позднем послеоперационном периоде СКФ снижалась, однако высокий темп редукции СКФ ре гистрировался редко (5,7%). Прогрессирование ХБП отмечено у 72,1% наших пациентов, при этом новые случаи ХБП 3-5 стадий зарегистрированы в 44,3% слу чаев. Трое больных находятся на программном гемо диализе. Опубликовано несколько серий наблюдений за пациентами, подвергнутыми технически сложным резекциям при опухолях почки ≥7 см, в которых заре гистрировано снижение СКФ после операции по сравнению с исходной с 92,1 мл/мин/1,73 м2 до 65 мл/мин/1,73 м2 [23]; с 81 мл/мин/1,73 м2 до 55 мл/мин/1,73 м2 [24] и повышение сывороточного креатинина с 1,16 мг/дл до 1,26 мг/дл соответственно [25]. В исследовании C. Long и соавт., включившем 46 больных, которым было выполнено органосохраняю щее вмешательство при опухолях почечной паренхимы ≥7 см, в том числе, – множественных, повышение ста дии ХБП было зарегистрировано в 10,9% наблюдений [26]. Несмотря на несопоставимые характеристики пациентов в выборках, результаты которых представ лены выше, частота сохранения почечной функции у больных, формально являющихся кандидатами для ра дикальной нефрэктомии, представляется удовлетвори тельной во всех цитируемых работах.
Факторами риска прогрессирования ХБП в нашей серии наблюдений являлись: индекс Чарльсона ≥6 (р=0,016), облигатные показания к резекции почки (р=0,01) и острое снижение почечной функции в раннем послеоперационном периоде (р<0,0001). Для пациентов с функционирующей второй почкой (n 57) независимую прогностическую значимость продемонстрировало ост рое снижение почечной функции после резекции (р<0,0001). Независимыми факторами риска развития тяжелой ХБП оказались индекс Чарльсона ≥6 (р=0,007) и острое снижение почечной функции в раннем после операционном периоде (р=0,021). Риск ухудшения позд них функциональных результатов при выполнении резекции почки по облигатным показаниям, отмечен ный многими авторами [27], несомненно, обусловлен меньшим количеством функционирующих нефронов, остающихся при наличии единственной почки. Обра щает на себя внимание, что независимым фактором риска прогрессирования ХБП, в том числе – до 3-5 ста дий, являлось острое снижение почечной функции, а не длительность ишемии, которая, собственно, вносила наибольший вклад в ухудшение ранних функциональ ных результатов в нашей серии наблюдений. Это с вы сокой степенью вероятности свидетельствует о том, что именно клинически значимые постишемические по вреждения, проявлявшиеся повышением уровня креа тинина и/или снижением СКФ и/или редукцией темпа диуреза, в дальнейшем способны привести к нефро склерозу и перманентному снижению клубочковой фильтрации. Индекс Чарльсона как суррогатный крите рий общего здоровья оказался строгим предиктором ХБП после технически сложной резекции почки. Надо отметить, что в немногочисленных исследованиях и ме таанализах, направленных на выделение факторов риска развития тяжелой ХБП в общей популяции, ин дексу сопутствующих заболеваний уделяется большое внимание, однако пока корреляция суммы баллов по шкале Чарльсона и частоты ХБП 3-5 стадий не вы явлено [28].
Облигатные показания к резекции почки, количе ство удаляемых почечных узлов и индекс Чарльсона – некорректируемые факторы неблагоприятного про гноза почечной функции. По сути, факторами риска развития почечной дисфункции, которые могут ниве лироваться хирургической техникой, являются продол жительность ишемии и объем кровопотери. Снизить риск кровопотери >500 мл можно путем пережатия по чечных сосудов. Повышение технической сложности вмешательства на резекционном и реконструктивном этапах закономерно увеличивает длительность ишемии.
Этот факт подтверждается рядом исследований, вы явивших статистически значимую корреляцию между нефрометрическим индексом и временем пережатия по чечных сосудов во время резекции [16,29]. Возмож ными вариантами решения проблемы снижения риска постишемических повреждений почечных клубочков являются: выполнение резекции почки, находящейся в кровотоке (при ожидаемой кровопотере <500 мл или с использованием оборудования для возврата ауто крови), селективное пережатие сегментарных артерий, раннее восстановление почечного кровотока до завер шения основных этапов операции, наложение непре рывных швов на зону резекции и высокий темп выпол нения резекции и реконструкции.
Технически сложная резекция, выполненная нами 121 больному раком почки, включая 34,7% пациентов с двухсторонними опухолями и 10,7% больных раком почки pT3a, позволила добиться удовлетворительных отдаленных результатов. Пятилетняя общая, ракоспе цифическая, кардиоспецифическая и безрецидивная выживаемость составили 91,5%, 95,2%, 93,9% и 91,5%, соответственно. Независимыми факторами риска кар диоспецифической выживаемости являлись возраст (р=0,001) и индекс Чарльсона ≥6 (р=0,041); общей вы живаемости – индекс Чарльсона ≥6 (р=0,001). Результа тов сопоставимых по характеристикам серий наблю дений не опубликовано. В исследовании, включившем 46 больных раком почки pT2, подвергнутых резекции, 5-летняя общая и специфическая выживаемость соста вила 94,5% и 70,9% соответственно [26]. Пятилетняя безрецидивная, специфическая и общая выживае мость 80 пациентов, подвергнутых органосохраняю щему хирургическому лечению по поводу рака почки pT2 R. Kopp, равнялась 79,9%, 86,7% и 83,3%, соответ ственно [30].
ЗАКЛЮЧЕНИЕ
Резекция почки – эффективный и относительно безопасный метод лечения больных опухолями почеч ной паренхимы с нефрометрическим индексом PADUA ≥8 и/или RENAL ≥7, ассоциированный с приемлемой частотой осложнений и обеспечивающий удовлетво рительные функциональные и онкологические резуль таты. Объем кровопотери >500 мл увеличивает риск тяжелой острой почечной недостаточности. Для уменьшения объема кровопотери допустимо времен ное пережатие почечных сосудов в течение <20 мин. Возможными методами уменьшения риска постише мических повреждений почечной паренхимы яв ляются выполнение резекции почки, находящейся в кровотоке, селективное пережатие сегментарных арте рий, раннее восстановление артериальной перфузии и высокий темп выполнения резекционного и рекон структивного этапов.
ЛИТЕРАТУРА
- Kutikov A, Uzzo RG. e R.E.N.A.L. nephrometry score: a comprehensive standardized system for quantitating renal tumor size, location and depth. J Urol 2009;182(3):844–53. doi: 10.1016/j.juro.2009.05.035.
- Ficarra V, Novara G, Secco S, Macchi V, Porzionato A, De Caro R, et al. Preoperative aspects and dimensions used for an anatomical (PADUA) classification of renal tumours in patients who are candidates for nephron-sparing surgery. Eur Urol 2009;56(5):786–93. doi: 10.1016/j.eururo.2009.07.040
- Dindo D, Demartines N, Clavien PA. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg 2004; 240(2):205-213. doi: 10.1097/01.sla.0000133083.54934.ae
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Inter Suppl 2013;3(1):1–150.
- Bellomo R, Ronco C, Kellum JA, Mehta RL, Palevsky P; Acute Dialysis Quality Initiative workgroup. Acute renal failure-definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Crit Care 2004;8(4):R204–R212. doi: 10.1186/cc2872
- Lane BR, Golan S, Eggener S. Tobert CM, Kahnoski RJ, Kutikov A, et al. Differential use of partial nephrectomy for intermediate and high complexity tumors may explain variability in reported utilization rates. J Urol 2013;189(6):2047-53. doi: 10.1016/j.juro.2013.01.007
- Lieser G, Simmons MN. Developments in kidney tumor nephrometry. Postgrad Med 2011;123(3):35-42. doi: 10.3810/pgm.2011.05.2282
- Minervini A, Vittori G, Antonelli A, Celia A, Crivellaro S, Dente D, Di Santo V, et al. Open versus robotic-assisted partial nephrectomy: a multicenter comparison study of perioperative results and complications. World J Urol 2014;32(1):287–93. doi: 10.1007/s00345-013-1136-x.
- Kim KT, Choo MS, Lee HE, Park YH, Song SH, Kim HH. Comparison of robot-assisted partial nephrectomy and open partial nephrectomy: clinical outcome and complication analysis. Eur Urol Suppl 2012;11(1):E32–E32a.
- Oh JJ, Byun S, Hong SK, Jeong CW, Lee SE. Comparison of robotic and open partial nephrectomy: single-surgeon matched cohort study. Can Urol Assoc J 2014;8(7-8):E471–5. doi: 10.5489/cuaj.1679
- Desantis D, Lavallée LT, Witiuk K, Ranjeeta Mallick R, Kamal F, Fergusson D, et al. The association between renal tumour scoring system components and complications of partial nephrectomy. Can Urol Assoc J 2015;9(1-2):39–45. doi: 10.5489/cuaj.2303
- Tyritzis SI, Papadoukakis S, Katafigiotis I, Adamakis I, Anastasiou I, Stravodimos KG, et al. Implementation and external validation of Preoperative Aspects and Dimensions Used for an Anatomical (PADUA) score for predicting complications in 74 consecutive partial nephrectomies. BJU Int 2012;109(12):1813–8. doi: 10.1111/j.1464-410X.2011.10644.x.
- Mottrie A, Schatteman P, De Wil P, De Troyer B, Novara G, Ficarra V. Validation of the preoperative aspects and dimensions used for an anatomical (PADUA) score in a robot-assisted partial nephrectomy series. World J Urol 2013;31(4):799–804. doi: 10.1007/s00345-010-0639-y.
- Erlich T, Abu-Ghanem Y, Ramon J, Mor Y, Rosenzweig B, Dotan Z. Postoperative urinary leakage following partial nephrectomy for renal mass: risk factors and a proposed algorithm for the diagnosis and management. Scand J Surg 2017;106(2):139-144. doi: 10.1177/1457496916659225.
- Gupta R, Tori M, Babitz SK, Tobert CM, Anema JG, Noyes SL, Lane BR. Comparison of RENAL, PADUA, CSA, and PAVP nephrometry scores in predicting functional outcomes after partial nephrectomy. Urology 2019;124:160-167. doi:10.1016/j.urology.2018.03.055
- Bylund JR, Gayheart D, Fleming T, Venkatesh R, Preston DM, Strup SE, et al. Association of tumor size, location, R.E.N.A.L., PADUA and centrality index score with perioperative outcomes and postoperative renal function. J Urol 2012;188(5):1684-9. doi: 10.1016/j.juro.2012.07.043
- Mehta RL, Kellum JA, Shah SV, Molitoris BA, Ronco C, Warnock DG, et al. Acute Kidney Injury Network: report of an initiative to improve outcomes in acute kidney injury. Crit Care 2007;11(2):R31. doi: 10.1186/cc5713
- Rajan S, Babazade R, Govindarajan SR, Pal R, You J, Mascha EJ, et al. Perioperative factors associated with acute kidney injury after partial nephrectomy. Br J Anaesth 2016; 116(1):70–76. doi: 10.1093/bja/aev416.
- Zhang Z, Zhao J, Dong W. Acute ipsilateral renal dysfunction after partial nephrectomy in patients with a contralateral kidney: spectrum score to unmask ischemic injury. Eur Urol. 2016;70(4):692-698. doi: 10.1016/j.eururo.2016.04.015. Volpe A, Blute ML, Ficarra V. Renal ischemia and function after partial nephrectomy: a collaborative review of the literature. Eur Urol 2015;68(1):61-74. doi: 10.1016/j.eururo.2015.01.025.
- Волкова М. И., Алборов С. В., Черняев В. А., Фигурин К. М., Панахов А. Д., Ридин В. А., и др. Функциональные результаты резекции единственной функционирующей почки при опухолях почечной паренхимы. Онкоурология 2017;13(3):46-53. doi: 10.17650/1726-9776-2017-13-3-46-53 [Volkova M. I., Alborov S. V., Chernyaev V. A., Figurin K. M., Panakhov A. D., Ridin V. A., et al. Functional results of resection of the only functioning kidney in renal parenchyma tumors. Oncourology=Cancer urology 2017; 13 (3): 46-53. doi: 10.17650 / 1726-9776-2017-13-3-46-53]
- Han KS, Song GH, You D, Song C, Jeong IG, Hong JH, et al. Comparison of hand-assisted laparoscopic versus robot-assisted laparoscopic versus open partial nephrectomy in patients with T1 renal masses. J Endourol 2017;31(4):374-379. doi: 10.1089/end.2014.0517.
- Becker F, Roos FC, Janssen M, Brenner W, Hampel C, Siemer S, et al. Short term functional and oncologic outcomes of nephron‐sparing surgery for renal tumours ≥ 7 cm. Eur Urol 2011;59(6): 931–7. doi: 10.1016/j.eururo.2011.02.017.
- Karellas ME, O'Brien MF, Jang TL, Bernstein M, Russo P. Partial nephrectomy for selected renal cortical tumours of ≥ 7 cm. BJU Int 2010;106(10):1484–7. doi: 10.1111/j.1464-410X.2010.09405.x.
- Peycelon M, Hupertan V, Comperat E, Renard-Penna R, Vaessen C, Conort P, et al. Long‐term outcomes after nephron sparing surgery for renal cell carcinoma larger than 4 cm. J Urol 2009;181(1):35 41. doi: 10.1016/j.juro.2008.09.025.
- Long CJ, Canter DJ, Kutikov A, Li T, Simhan J, Smaldone M, Teper E, et al. Partial nephrectomy for renal masses ≥7 cm: technical, oncological and functional outcomes. BJU Int 2012;109(10):1450-6. doi: 10.1111/j.1464-410X.2011.10608.x.
- Simmons MN, Hillyer SP, Lee BH, Fergany AF, Kaouk J, Campbell SC. Functional recovery after partial nephrectomy: effects of volume loss and ischemic injury. J Urol 2012;187(5):1667-73. doi: 10.1016/j.juro.2011.12.068.
- Johnston MC, Marks A, Crilly MA, Prescott GJ, Robertson LM, Black C. Charlson index scores from administrative data and case-note review compared favourably in a renal disease cohort. Eur J Public Health 2015;25(3):391-6. doi: 10.1093/eurpub/cku238.
- Mottrie A, Schatteman P, De Wil P, De Troyer B, Novara G, Ficarra V. Validation of the preoperative aspects and dimensions used for an anatomical (PADUA) score in a robot-assisted partial nephrectomy series. World J Urol 2013;31(4):799-804. doi: 10.1007/s00345-010-0639-y
- Kopp RP, Mehrazin R, Palazzi KL, Liss MA, Jabaji R, Mirheydar HS, et al. Survival outcomes after radical and partial nephrectomy for clinical T2 renal tumours categorised by R.E.N.A.L. nephrometry score. BJU Int 2014 Nov;114(5):708-18. doi: 10.1111/bju.12580







