Важной проблемой современной онкологии и урологии является комплексное оказание медицинской помощи онкоурологическим больным. Целью лечения является избавление больных от онкологического процесса и обеспечение качества жизни, которое позволит пациенту вернуться к трудовой деятельности и социальной жизни. Факторами, снижающими качество жизни больных после лечения по поводу злокачественных (рак предстательной железы – РПЖ ) и доброкачественных (доброкачественная гиперплазия предстательной железы –ДГПЖ) опухолей малого таза, являются стрессовое недержание мочи (СНМ) и развитие стриктуры пузырно-уретрального анастомоза или уретры [1, 2, 3].
Недержание мочи
После радикальной простатэктомии недержание мочи у больных возникает в 12-15%. На частоту недержания влияет стадия онкологического процесса, хирургическая техника, анатомические особенности опухоли [4]. При использовании фокальных методов лечения (брахитерапия, HIFU-терапия) недержание мочи встречается несколько реже, чем после открытых операций [5].
После трансуретральной резекции предстательной железы по поводу доброкачественной гиперплазии частота недержания мочи колеблется от 3,3% до 11,4%, при этом количество осложнений возрастает при повторном вмешательстве [6].
Для коррекции недержания мочи используются различные методики. К ним относятся установка различных синтетических слинговых систем, использование васкуляризованного кожного лоскута.
Более 40 лет для лечения тотального недержания мочи у мужчин используются искусственные сфинктеры, искусственные протезы, которые представляют собой механическое и гидравлическое устройство. За последние годы были существенно доработаны конструкции манжетки, помпы, резервуара, соединительных трубок и способов их соединения. В результате имплантации современного искусственного сфинктера мочевого пузыря его успешная работа в течение 10 лет после операции наблюдается у 75% пациентов. При этом 90% пациентов, пользующихся искусственным сфинктером мочевого пузыря, полностью удовлетворены его функцией. Однако примерно в 15-25% случаев может потребоваться хирургическая ревизия сфинктера (повторная операция) для коррекции недостатков в его работе.
Начиная с 70-80-х годов прошлого века, ученые разных стран проводили активный поиск более простого и совершенного метода коррекции СНМ у мужчин. Наилучших результатов удалось добиться с разработкой и внедрением в клиническую практику современных слинговых систем [7, 8, 9, 10, 11, 12, 13, 14, 15].
Новые надежды связывались с внедрением в 2006 году трансобтураторной методики установки полипропиленовых лент, однако клинические данные, свидетельствующие в пользу этих устройств, пока недостаточно убедительны. Главные их недостатки – отсутствие уверенности во время операции в достижении достаточного для удержания мочи натяжения и отсутствие способов сохранения этого натяжения в дальнейшем [16, 17].
Стриктура пузырно-уретрального анастомоза и уретры
Одним из тяжелых осложнений после операций по поводу заболеваний предстательной железы (РПЖ, ДГПЖ) является развитие стриктур цистоуретрального анастомоза или уретры. После радикальной простатэктомии данное осложнение может достигать 13,2% [18, 19], при повреждении сфинктера мочевого пузыря частота стриктуры достигает 45% [20]. После трансуретральной резекции предстательной железы по поводу доброкачественной гиперплазии частота стриктур доходит до 14% [21]. На развитие стриктур влияет оперативная техника, анатомические и физиологические особенности больного, сроки катетеризации мочевого пузыря, характер опухоли [22].
Методом лечения стриктур уретры является внутренняя уретротомия. Однако частота рецидивов после этого вмешательства крайне высока и достигает 64% [23]. В этой ситуации одним из способов лечения является имплантация внутриуретральной спирали [24].
Наибольшие сложности для лечения возникают при сочетании стриктуры уретры и недержания мочи. В этом случае вариантом лечебной тактики является установка спирали и артифициального сфинктера [25]. Однако данная методика сложна в исполнении и имеет недостатки установки сфинктера – сложность вмешательства, риск поломки сфинктера, необходимость регулировать мочеиспускание вручную. В подобной клинической ситуации более простым методом является комбинация установки спирали и мужской слинговой системы [26].
Мы представляет наш опыт лечения больных с недержанием мочи с помощью мужской слинговой системы. В отличие от слингов, применяемых при СНМ у женщин и имплантируемых для коррекции сопротивления уретры без натяжения, мужские петли должны активно повышать уретральное сопротивление и учитывать индивидуальные анатомические и функциональные анатомические изменения, возникшие у оперированных ранее пациентов. Кроме того, в случае избыточного натяжения и развития последующей обструкции, они должны иметь возможность коррекции своего положения. Одним из видов таких систем, полностью отвечающим всем требованиям, являются петли ARGUS (Argus®, Promedon SA, Cordoba, Argentina).
МАТЕРИАЛЫ И МЕТОДЫ
В наше исследование вошло 39 пациентов, которые в 2009-2011 гг. лечились в НИИ урологии по поводу недержания мочи. Средний возраст больных составлял 64 года (51-81). Стрессовое недержание мочи развилось после следующих хирургических вмешательства по поводу рака предстательной железы и доброкачественной гиперплазии предстательной железы: радикальная простатэктомия – 11 человек, трансуретральная резекция предстательной железы – 14, открытая аденомэктомия – 8, брахитерапия – 3, лучевая терапия – 2, HIFU-терапия – 1 пациент.
Умеренная степень недержания мочи отмечалась у 35 пациентов, случаев, тяжелая – у 4-х. Ни один пациент не имел в анамнезе хирургических вмешательств по поводу недержания мочи. У 13 пациентов была так же стриктура уретры, по поводу которой у 7 была установлена внутриуретральная спираль в нашей клинике в разные сроки перед установкой мужского слинга. 6 пациентам была выполнена внутренняя уретротомия.
Всем пациентам были проведены следующие исследования: осмотр, ультразвуковое исследование органов малого таза, комплексное уродинамическое обследование, урофлоуметрия, уретрография, уретроцистоскопия, тест с прокладками. Ни у одного онкологического больного не было выявлено признаков местного рецидива опухоли или отдаленного метастазирования.
Всем больным для обезболивания использовалась спинальная анестезия. Установка мужского слинговой системы с использованием петли ARGUS выполнялась по следующей методике. На операционном столе больной находился в литотомическом положении. В полость мочевого пузыря проводился катетер Фолея 12 F. Выполнялся продольный разрез кожи промежности на протяжении 5-7 см. Далее осуществлялся доступ к задней части уретры. Последняя выделялась, мобилизовывались ножки кавернозных мышц. Бульбокавернозная мышца промежности не пересекалась. Троакары системы выводились через разрезы кожи в надлобковой области (в 5 случаях) или трансобтураторно (в 34 случаях). Подушечки слинга укладывались под луковичной частью уретры под контролем зрения и ретроградного давления утечки мочи. Разрезы ушивались. Средняя продолжительность операции составила – 63 (45-90) минуты. Общая кровопотеря составила в среднем – 43 мл. Интраоперационных осложнений не отмечалось.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В послеоперационном периоде мы получили хорошие результаты: полное удержание мочи было отмечено у 25 (64,1%) больных, 8 (20,5%) пациентов стали использовать меньшее количество прокладок, отсутствие эффекта отмечено у 6 (15,4%) пациентов. Таким образом, суммарная эффективность лечения составила 84,6 %.
Рентгенологическая картина малого таза больного после установки мужского слинга и внутриуретральной спирали представлена на рис. 1.
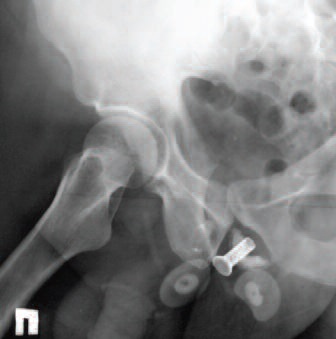
Рис. 1. Рентгенологическая картина малого таза после установки мужского слинга и внутриуретральной спирали: 1 – уретральная спираль, 2 – слинговая система
Коррекцию (подтягивание) слинговой системы из-за недостаточной эффективности потребовалось провести у 12 (30,8 %) больных. Возможность изменять степень натяжения петли в раннем или позднем послеоперационном периоде предусмотрена особенностью конструкции слинговой системы. Коррекция проводилась под местной анестезией и заключалась в подтягивании рукавов слинга. Операций по ослаблению слинговой системы не требовалось. У 4 (10,25%) пациентов произведено удаление слинговой системы вследствие нагноения послеоперационной раны.
ЗАКЛЮЧЕНИЕ
Наш опыт использования слинговой системы свидетельствует об эффективности этого метода при лечении недержания мочи у мужчин. Важной особенностью является то, что эту методику можно использовать у больных с тяжелой степенью недержания мочи, которые являются потенциальными кандидатами для установки искусственного сфинктера мочевого пузыря. Важным является возможность коррекции степени натяжения петли под местной анестезией. Слинг не требует дополнительных манипуляций для нормального мочеиспускания. Важным преимуществом является возможность комбинировать слинговую систему с имплантацией внутриуретральной спирали по поводу стриктуры уретры, что позволяет осуществлять помощь данной сложной категории больных.
Резюме:
Недержание мочи у мужчин является серьезным осложнением после хирургических вмешательств на органах малого таза. Современным методом коррекции недержания является установка мужских слинговых систем. В наше исследование вошло 39 пациентов, которые в 2009-2011 гг. лечились в НИИ урологии по поводу недержания мочи. Средний возраст больных составлял 64 года (51-81 лет). Стрессовое недержание мочи развилось после следующих хирургических вмешательства по поводу рака предстательной железы и доброкачественной гиперплазии предстательной железы: радикальная простатэктомия – 11 человек, трансуретральная резекция предстательной железы – 14, открытая аденомэктомия – 8, брахитерапия – 3, лучевая терапия – 2, HIFU-терапия – 1 пациент. Умеренная степень недержания мочи была у 35 больных, у 4-х пациентов наблюдалась тяжелая степень недержания мочи. Интраоперационных осложнений не было. Средняя продолжительность операции – 63 (45-90) мин. Полное удержание мочи отмечалось у 25 (64,1%) больных. Меньшее количество прокладок использовали 8 (20,5%) пациентов. Отсутствие эффекта было у 6 (15,4%) пациентов. Суммарная эффективность лечения составила 84,6%. Подтягивание слинговой системы из-за неэффективности потребовалось у 12 (30,8 %) больных, что не является в полной мере осложнением, а скорее конструктивной особенностью слинговой системы. У 4 (10,25%) пациентов вследствие нагноения послеоперационной раны слинговая система удалена. Слинговая система – эффективный метод лечения недержания мочи у мужчин, преимуществом которого является возможность несложной коррекции установленной системы под местной анестезией, отсутствие необходимости в дополнительных манипуляциях для проведения мочеиспускания, возможности комбинирования слинговой системы с имплантацией внутриуретральной спирали при наличии рецидивной стриктуры уретры.
ЛИТЕРАТУРА
1. Wein A.J., Kavoussi L.R., Novick A.C., Partin A.W., Peters C.A Campbell-Walsh Urology, 10th Edition. Saunders, 2012. P.4320.
2. Качмазов А.А., Серебряный С.А., Ромих В.В. Регулируемая слинговая система Argus в лечении недержания мочи у мужчин. // Экспериментальная и клиническая урология. 2012. № 12. С. 63-66.
3. Алексеев Б.Я. Лечение локализованного и местно-распространенного рака предстательной железы: Дис. … д-ра мед. наук, М., 2006. 259 с.
4. Hu JC, Gu X, Lipsitz SR, Barry MJ, D'Amico AV, Weinberg AC, Keating NL. Comparative effectiveness of minimally invasive vs open radical prostatectomy. // JAMA. 2009. Vol. 14, N 302. P. 1557-1564.
5. Arlandis Guzmán S, Bonillo García MA, Broseta Rico E. Voiding dysfunction after brachytherapy in patients with prostate cancer. // Arch Esp Urol. 2009., Vol 62, N 10. P. 826-837.
6. Zwergel U, Wullich B, Lindenmeir U, Rohde V, Zwergel T. Long-term results following transurethral resection of the prostate. //Eur Urol. 1998. Vol. 33, N 5. P. 476-480.
7. Raz S, McGuire EJ, Ehrlich RM, Zeidman EJ, Wang SC, Alarcon A, Schmidtbauer C, McLaughlin S. Fascial sling to correct male neurogenic sphincter incompetence: the McGuire/Raz approach. // J. Urol. 1988. Vol. 139. P. 528-531.
8. Mizuo T, Tanizawa A, Yamada T, Ando M, Oshima H. Sling operation for male stress incontinence by utilizing modified Stamey technique. // Urology. 1992. Vol. 39. P.211-214.
9. Palma PC, Netto NR. Al a puburetral sintetica no tratamento da incontinencia urinaria masculine. // J. Bras. Urol. 1993. P.1919.
10. Stamey T. Perineal compression of the corpum spongiosum of the bulbar urethra. An operation for post-radical prostatectomy incontinence // J. Urol.1994. Vol. 151. P. 490.
11. Shoukry MS, el-Salmy S. Urethral needle suspension for male urinary incontinence. // Scand. J. Urol. Nephrol. 1997. Vol. 31. P. 267-270.
12. Kaufman J.J. A new operation for male incontinence // Surg. Gynecol. Obstet. 1970. Vol. 131. P. 295-299.
13. Kaufman JJ. Surgical treatment of post-prostatectomy incontinence: use of the penile crura to compress the bulbous urethra // J Urol. 1972. Vol. 107. P. 293-297.
14. Kaufman JJ. Treatment of post prostatectomy urinary incontinence using a silicone gel prosthesis. //Br J Urol. 1973. Vol. 45. P. 646-653.
15. Schaeffer AJ, Clemens JQ, Ferrari M, Stamey TA. The male bulbourethral sling procedure for post-radical prostatectomy incontinence. // J. Urol. 1998. Vol. 159. P. 1510-1515.
16. Romano SV, Metrebian SE, Vaz F, Muller V, D’Ancona CA, Costa DE, Souza EA, Nakamura F. An adjustable male sling for treating urinary incontinence aer prostatectomy: a phase III multicentre trial. // BJU Int. 2006. Vol. 97. P. 533-539.
17. Hubner WA, Gallistl H, Rutkowski M, Huber ER. Adjustable bulbourethral male sling: experience after 101 cases of moderate-to-severe male stress urinary incontinence. // BJU Int. 2011. Vol. 107, No 5. P. 777-782.
18. Hisasue S, Takahashi A, Kato R, Shimizu T, Masumori N, Itoh N, Tsukamoto T. Early and late complications of radical retropubic prostatectomy: experience in a single institution. // Jpn J Clin Oncol. 2004. Vol. 34, N 5. P. 274-279.
19. Liss MA, Skarecky D, Morales B, Osann K, Eichel L, Ahlering TE. Preventing perioperative complications of robotic-assisted radical prostatectomy. // Urol. 2013. Vol. 81, N 2. P. 319-323.
20. Gerullis H, Quast S, Eimer C, Bagner JW, Otto T. Sphincter lesions after radical prostatectomyevaluation and classification. // J Endourol. 2011 Vol . 25, N 6. P. 1075-1080.
21. Kallenberg F, Hossack TA, Woo HH. Long-term followup after electrocautery transurethral resection of the prostate for benign prostatic hyperplasia. // Adv Urol 2011
22. Altinova S, Serefoglu EC, Ozdemir AT, Atmaca AF, Akbulut Z, Balbay MD. Factors affecting urethral stricture development aer radical retropubic prostatectomy. // Int Urol Nephrol. 2009. Vol. 41, N 4. P. 881-884.
23. Wong SS, Aboumarzouk OM, Narahari R, O'Riordan A, Pickard R. Simple urethral dilatation, endoscopic urethrotomy, and urethroplasty for urethral stricture disease in adult men. // Cochrane Database Syst Rev. 2012. Vol.12. P.12.
24. Isotalo T, Talja M, Välimaa T, Törmälä P, Tammela TL. A bioabsorbable self-expandable, self-reinforced poly-L-lactic acid urethral stent for recurrent urethral strictures: long-term results. // J Endourol. 2002. Vol. 16, N 10. P. 759-762.
25. Elliott DS, Boone TB. Combined stent and artificial urinary sphincter for management of severe recurrent bladder neck contracture and stress incontinence aer prostatectomy: a long-term evaluation. // J Urol. 2001. Vol. 165, N 2. P. 413-415.
26. Chernyshev I, Kachmazov A, Perepechin D. Male sling in patients with stress urinary incontinence (our first experience). // Materials of 10th International Congress of Andrology. 2013, Melbourne, Australia, – P.64.







