Впервые применение криопроцедуры описал Джеймс Арнотт, который еще в 1845-1851 гг. использовал аппликации солевых растворов, смешанных со льдом, при лечении некоторых заболеваний кожи, матки и молочной железы. Температура при этом достигала -24оС (Arnott J., 1891, Bird H., 1949). С открытием эффекта Джоуля-Томпсона, который заключается в том, что газ, выходя через небольшое отверстие и расширяясь, изменяет свою температуру, метод криоабляции получил дальнейшее развитие. Сначала для криопроцедур применяли жидкий углекислый газ, который при переходе в газообразное состояние охлаждался и образовывал так называемые «хлопья снега». Полученный «снег» из замершего СО2 спрессовывался в специальные аппликаторы и применялся при лечении заболеваний кожи. Такая методика сохранялась вплоть до 1960-х годов (Soanes W.A., 1966). В последующем в криотерапии широкое применение нашел жидкий азот, температура аппликатора которого составила -1960С.
Криоабляция в урологии
В урологии первые попытки применения криохирургии были осуществлены в 60-х годах XX века с целью лечения рака предстательной железы. Однако первые процедуры криоабляции были несовершенны – громоздкая конструкция криомашины, толстые криозонды, отсутствие контроля за проведением процедуры. Поэтому методика не получила широкого развития (Loening S.A., 1984). Сейчас аппаратура подверглась значительным усовершенствованиям – появились криомашины III поколения, которые используются в операционных ведущих клиник. С целью криоабляции используются газы аргон и гелий (аргон, расширяясь, способен охладиться до -850С, а гелий, расширяясь, наоборот, нагревается). Также используются тонкие, диаметром 17G иглы, что сравнимо с иглой для биопсии (рисунок 1).
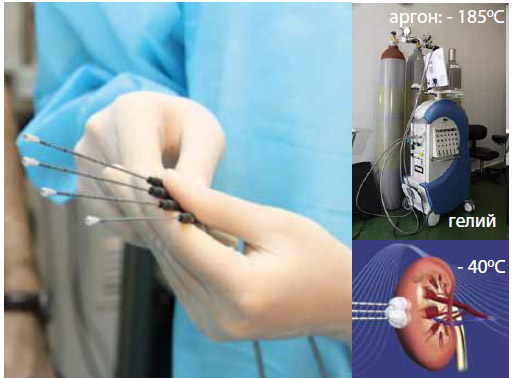
Рисунок 1. Аппаратура для проведения криоабляции – III поколение
Для того чтобы выполнить криоабляцию опухоли почки, достаточно достичь температуры -40оС. Физическое и биологическое воздействие криоабляции заключается в чередовании фаз замораживания и оттаивания, которое вызывает следующие эффекты.
1. Цитотоксический эффект – при достижении температуры -150С в межклеточном пространстве образуются кристаллы льда. Это повышает осмолярность межклеточного пространства и способствует выходу в него внутриклеточной жидкости. Во внутриклеточном пространстве, наоборот, развивается гиперосмолярность. При дальнейшем понижении температуры до -400С кристаллы льда начинают образовываться и во внутриклеточной жидкости, что ведет к разрушению мембран органелл клетки и самой клеточной мембраны. До 90% клеточных мембран необратимо разрушаются уже после первой заморозки. При последующем оттаивании, клетки с гиперосмолярным содержимым, чьи мембраны еще способны к транспорту воды, набирают жидкость, и разрушаются либо под воздействием гипергидратации, либо от формирования внутриклеточного льда в следующем цикле заморозки. Таким образом, температура -400С является летальной, причем особенно цитотоксический эффект выражен именно у опухолевых клеток, так как для них характерен более высокий обмен веществ. Такие сосудистые реакции, как повышенная отечность тканей и стаз с последующим тромбозом мелких
сосудов, приводят к дальнейшему некрозу тканей и индуцированию апоптоза (Baust J.G., 2005) .
2. Сосудистые реакции. Впервые корреляцию между замораживанием и повреждающей сосудистой реакцией выявил Cohnheim в 1877 г.
Он предположил, что некроз в замороженной, а затем оттаявшей ткани был вызван тромбозом после оттаивания. Позднее, его предположения были подтверждены Lewis (1926 г.) и другими учеными, доказавшими, что именно такие явления, как повышенная отечность тканей, стаз и дальнейший тромбоз мелких сосудов приводят к некрозу после цикла заморозки/оттаивания опытного образца ткани.
L. Marzella на экспериментах с замораживанием ушей кроликов обратил внимание на важную роль холодового повреждения эндотелия в развитии дальнейшей сосудистой реакции (Marzella L., 1989). Эндотелий разрушался при заморозке, а при оттаивании отмечалась немедленная тромбоцитарная агрегация, одновременно с которой начиналось накопление межклеточной жидкости и активация нейтрофилов. Через 6 часов начиналась экстравазация эритроцитов, а через сутки – расслоение эндотелия.
3. Активации иммунной системы (ИС) в результате криоабляции.
Первая теория активации ИС – это образование антител к опухоли в результате высвобождения внутриклеточных антигенов, которые захватываются антиген-представляющими клетками иммунной системы и запускают трансформацию В-лимфоцитов в плазматические клетки, а также хемотаксис нейтрофилов и макрофагов (Grana L., 1969).
Другая теория предполагает развитие иммунной реакции посредством индуцирования цитотоксических T-лимфоцитов. Предполагается, что замораживание тканей сенсибилизирует цитотоксические Т-лимфоциты, или усиливает презентацию антигенов (Eskandari H., 1982).
Третья теория описывает стимуляцию natural killer клеток в результате действия сверхнизкой температуры, хотя корреляция между этими процессами еще не достаточно исследована (Matsumura K., 1982).
Криоабляция уже давно не является экспериментальной методикой. Американская урологическая ассоциация (AUA) исключила криоабляцию из списка экспериментальных методов в 1996 г., а в 2009 г. к этому мнению присоединилась Европейская ассоциация урологов.
Криоабляция может проводиться различными доступами – лапароскопически, перкутанно под контролем УЗИ или КТ и открытым способом (таблица 1).
Таблица 1. Число рецидивов после криоабляции (сводные данные)
| Источник | Доступ | Число пациентов |
Среднее время наблюдения (мес.) |
% рецидивов (число пациентов) |
|---|---|---|---|---|
| Matin et al., 2006 | лапароскопический | 204 | 24 | 3,9%(8) |
| Hegarty et al., 2006 | лапароскопический | 164 | 36 | 1,8%(3) |
| Lawatsch et al., 2006 | лапароскопический | 59 | 26,8 | 3,3%(2) |
| Gill et al., 2007 | лапароскопический | 60 | 72 | 6,7%(3) |
| Turro et al., 2007 | лапароскопический | 119 | 39,7 | 0,8%(1) |
| Miki et al., 2006 | перкутанный | 13 | 35 | 15%(2) |
| Pormpongkosol et al., 2006 | перкутанный | 21 | 12,3 | 9,5% (2) |
Показанием для криоабляции опухоли почки является размер опухоли не более 4 см, отсутствие региональных и отдаленных метастазов, множественные опухоли почек, единственная почка или снижение функции почек, двустороннее поражение. Также криоабляции могут подлежать пациенты с высоким риском хирургического вмешательства, либо пациенты, которые временно воздерживаются от открытого оперативного вмешательства. Криоабляция может рассматриваться в качестве паллиативного, циторедуктивного лечения при метастатических опухолях почек.
Противопоказанием являются опухоли ворот почки или центральной зоны (близкое расположение сосудов), контактирующие с лоханкой или в/3 мочеточника, наличие метастазов, кроме случаев, когда криоабляция проводится с паллиативной целью, пациенты, получающие антикоагулянтную терапию, которую нельзя отменить (Kunkle D.A., 2008).
Если сопоставить открытую резекцию почки, парциальную нефрэктомию и остальные методы, то при достаточно большом количестве пациентов, участвующих в исследовании, несколько авторов показали относительно небольшое количество местных рецидивов, даже по сравнению с радиочастотной абляцией (РЧА) – 4,6% и 11,8% соответственно (Kunkle D.A., 2008, Stephen Jones, 2010). Необходимость повторных процедур при криоабляции составляет 1,3%, при РЧА – 8,5%, что говорит об абсолютном преимуществе криоабляции в отношении местных рецидивов и необходимости повторных лечебных процедур. Получены данные об общей выживаемости – от 88 до 98% (таблица 2). Процент безрецидивной выживаемости составляет 90,6%, при среднем наблюдении 19,5 месяцев (Stephen Jones, 2010). Процент канцерспецифической выживаемости составляет 95% при среднем периоде наблюдения 20 месяцев.
Таблица 2. Общая выживаемость после криоабляции (сводные данные)
| Год | Средний размер опухоли |
Число больных | Наблюдения (месяцы) | % | |
|---|---|---|---|---|---|
| Davol et al. | 2006 | 2,5 | 40 | 36 | 88 |
| Bandl et al. | 2007 | 2,5 | 78 | 15 | 94 |
| Cestari et al. | 2004 | 2,6 | 35 | 20 | 97 |
| Schwartz et al. | 2006 | 2,6 | 55 | 10 | 98 |
| Aron et al. | 2008 | 2,3 | 88 | > 60 | 93 |
| Silverman et al. | 2005 | 2,6 | 26 | 14 | 92 |
| Gupta et al. | 2006 | 2,4 | 16 | 6 | 94 |
Самое главное преимущество криоабляции по сравнению с другими малоинвазивными методами – это наибольшая сохранность функции почки. Процент снижения почечной функции при криоабляции опухоли почки составляет 6%, при радиочастотной абляции – 13% и открытой резекции – 26% (AUA Guidelines, 2009).
Криоабляция характеризуется невысоким количеством осложнений. Осложнения, требующие конверсии, составляют не более 3,5% случаев. Другие серьезные осложнения, но не требующие конверсии, встречаются не более чем в 2% пациентов. Осложнения в виде болей в месте оперативного вмешательства, инфекций мочевыводящих путей, инфицирования раны, наблюдаются чаще, но они не имеют существенного значения (AUA Guidelines, 2009).
Клинический случай
Пациентка 59 лет с диагнозом «Ангиомилипома нижнего сегмента левой почки» (рисунок 2).
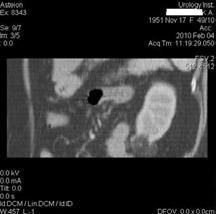
Рисунок 2. Клинический случай. Диагноз: «Ангиомиолипома нижнего сегмента левой почки»
В 2002 г. была выявлена ангиомилипома размерами 2 см, однако в течение 2010 г. был отмечен быстрый рост до 4 см. Мы выполнили лапароскопическую криоабляцию данной опухоли (рисунок 3). После окончания процедуры у пациентки отмечалось кровотечение из места вколов игл, купированное местным применением гемостатической губки «Тахокомб». Послеоперационный период протекал без особенностей. Дренаж удален на 3-и сутки. На 6-е сутки пациентка выписана. Перед выпиской сделано контрольное КТ-исследование – в области ранее расположенной ангиомиолипомы определяется участок с наличием «вакуум»-дефекта размером 3,1 × 1,8 см, с наличием тонкостенных перегородок (рисунок 4). Наружные стенки образования утолщены на отдельных участках до 0,7 см. Экскреторная функция почки сохранена. ЧЛС и мочеточник не расширены.

Рисунок 3. Выполнение лапароскопической криоабляция опухоли левой почки
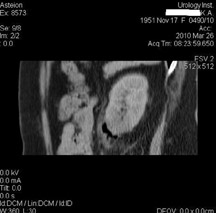
Рисунок 4. Контрольное КТ-исследование на 6-е сутки после выполнения
лапароскопической криоабляции
Спустя год после операции в области ранее расположенной ангиомиолипомы визуализируется рубцовая ткань.
Выводы
Криоабляция – это малоинвазивная процедура, имеющая достаточно высокую эффективность и низкий риск осложнений. Ее можно проводить повторно, она является методом выбора для больных с тяжелой сопутствующей патологией и оказывает, по сравнению с другими малоинвазивными методами, минимальное влияние на функцию почки.
Ключевые слова: криоабляция, рак почки.
Keywords: cryoablation, kidney cancer.






