В последнее время карт-на заболеваемости раком предстательной железы (РПЖ) очень изменилась. Сегодня РПЖ в Германии занимает первое место среди злокачественных новообразований у мужчин. Ежегодно диагностируется около 58 тыс. случаев новых случаев заболевания.
Всего несколько лет назад средний возраст пациента с впервые диагностированным РПЖ составлял 72 года, при средней продолжительности жизни в Германии 75 лет. Однако, сейчас эти показатели равны 60 и 82 годам соответственно. Среднее время жизни пациента с РПЖ составляет 7 лет.
До настоящего времени остаются актуальными вопросы диагностики РПЖ, оценки рисков, первичного радикального лечения, локального лечения рецидивов РПЖ, а также, что необходимо делать в тех случаях, когда радикальное лечение не приносит желаемых результатов (рисунок 1).
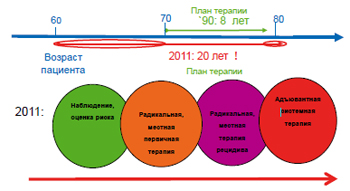
Рисунок 1. Последовательность лечебных мероприятий при РПЖ
Место HIFU в лечении РПЖ
РПЖ разрушает качество жизни мужчины уже в тот момент, когда отмечается первый подъем уровня ПСА. Психологическая подавленность у пациентов наблюдается даже в тех случаях, если отсутствуют какие-либо симптомы заболевания. Также больных очень сильно беспокоит исход и побочные эффекты самого лечения РПЖ. Тем методом, который обеспечивает радикальность лечения и малый процент осложнений, является HIFU-терапия. Для проведения HIFU-терапии используется несколько типов устройств различных производителей. Мой доклад основан на 15-летнем опыте применения HIFU-терапии РПЖ на аппарате «Аблатерм».
Действие метода HIFU основано на уничтожениизлокачественных тканей путем коагуляции, нагревания и эффекта «кавитации» (рисунок 2). Важной частью оборудования является терапевтический зонд, позволяющий фокусировать ультразвуковые излучения в одной точке в глубине тканей пациента. Другим необходимым компонентом оборудования является интегрированная система охлаждения, которая позволяет предотвратить термическое поражение стенки прямой кишки. Современные приборы позволяют проводить оценку состояния тканей предстательной железы через эндоректальный аппликатор в режиме реального времени. Все основные функции прибора интегрирован компьютерной программой, позволяющей выбирать параметры и контролировать весь процесс (рисунок 3).
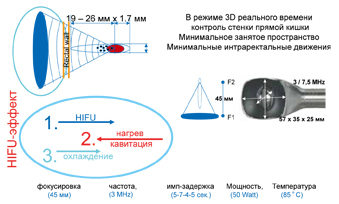
Рисунок 2. Физические характеристики и схема устройства HIFU

Рисунок 3. Аблатерм - Ablatherm®
За прошедшие годы сформировалось несколько подходов к проведению HIFU-терапии:
- монотерапия HIFU, которая активно применялась в первые 4 года существования данного метода лечения;
- одновременное выполнение трансуретральной резекции предстательной железы (ТУРПЖ) и сеанса HIFU-терапии в рамках одного вмешательства;
- последовательное выполнение HIFU-терапии через 4 недели после проведения ТУРПЖ (рисунок 4);
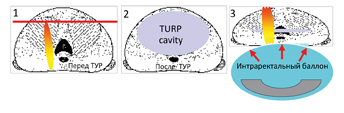
Рисунок 4. Значение выполнения ТУР перед HIFU
Последние два подхода обусловлены высокой частотой (около 35%) обструктивных осложнений HIFU-терапии из-за отторжения некротизированной ткани.
Показания для проведения HIFU-терапии должны очень строго соблюдаться, хотя на протяжении прошедших лет мы значительно расширили область применения метода.
- Локализованный РПЖ (радикальное лечение, тотальная или фокальная терапия).
- Сальважная HIFU-терапия рецидива РПЖ после других методов лечения (хирургического, лучевого, предыдущей HIFU-терапии).
- Паллиативная циторедуктивная адъювантная HIFU-терапия для локального уничтожения основного объема опухоли при местно-распространенном или метастатическом поражении.
- HIFU-терапия гормонально резистентного РПЖ.
- Случайно выявленный РПЖ после ТУРПЖ по поводу доброкачественной гиперплазии предстательной железы.
По данным французских исследователей, у больных РПЖ разных групп риска результаты лечения существенно отличаются. (Crouzet S., 2010). В группе промежуточного риска эффективность HIFU составила 80% за 5 лет наблюдения.
В центре HIFU-терапии в Мюнхене был выполнен анализ онкологических результатов пациентов в зависимости от степеней риска. Пациенты (752 человека) были разделены на III группы по степеням риска:
- низкого (T1а- T1с, ПСА менее 10 нг/мл, показатель Глисона менее 7);
- промежуточного (T1-T2a, или уровень ПСА 10-20 нг/мл, или показатель Глисона равный 7);
- высокого (T1-T2с, ПСА более 20 нг/мл, Глисон более 7).
Срок наблюдения после HIFU составил до 10 лет. Для пациентов низкой и промежуточной группы надир ПСА находился на уровне 0,06-0,07 нг/мл, что говорит о высоком проценте уничтоженных опухолевых клеток при скорости нарастания ПСА менее 05 нг/мл/год у 79 и 82% соответственно. Тогда как последний показатель в группе высокого риска составил лишь 58%. Специфическая выживаемость низкого, промежуточного и высокого риска составила 97%, 97% и 91% (таблица 1).
Таблица 1. T1-2 Надир ПСА (без гормонотерапии) и ТУР
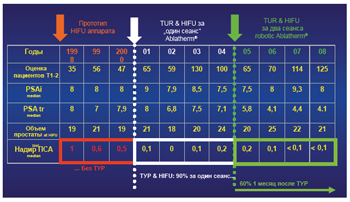
Стратегия проведения HIFU-терапии менялась на протяжении ряда лет по мере поступления новых данных об эффективности метода и его осложнениях. Применение HIFU после ТУРПЖ имеет значительные преимущества, которые проявляются в уменьшении надира ПСА после ультразвуковой абляции до 0,1-0,2 нг/мл, по сравнению с 0,5 1,0 нг/мл при монотерапии (рисунок 4).
В настоящее время существуют различные стратегии, которые помогают специалистам по HIFU перейти к фокальному лечению РПЖ. Мы можем исключить попадание сосудисто нервного пучка под ультразвуковые волны, отступая от него около 5 мм, со стороны, контралатеральной поражению, при РПЖ в стадии Т1-Т2 с унилатеральным распространением опухоли. Эта модификация лечения приводит к сохранению эректильной функции у пациентов в 75-90% (рисунок 5).
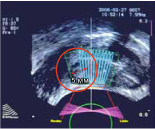
Рисунок 5. Новые стратегии HIFU-терапии (нервосберегающее лечение)
Если говорить о случайно найденном РПЖ после ТУРПЖ, мы наблюдали 52 таких пациента. Средний надир ПСА у них равнялся 0,06 нг/мл, средняя скорость нарастания ПСА – 0,05 нг/мл/год. Таким образом, можно говорить о реальной радикальности применения HIFU-терапии у пациентов со случайно обнаруженным РПЖ. Этот метод подходит таким больным из-за малого числа осложнений, по сравнению, например, с радикальной простатэктомией, выполняемой после ТУРПЖ.
До применения интегрированной охлаждающей системы, большую проблему представляли прямокишечно-уретральные свищи. Однако, после того, как подобная система была установлена, свищи стали наблюдаться только у 1-2 пациентов высокого риска после предшествующей лучевой терапии. Недержание мочи продолжительностью более 3 месяцев, которое расценивается как осложнение 3 степени тяжести, наблюдалось у 1,5% пациентов. После 2300 сеансов HIFU-терапии на протяжении 14 лет пери- или послеоперационная смертность равнялась 0%. Также никогда не возникала необходимость проведения экстренных оперативных вмешательств по причине каких-либо осложнений HIFU-терапии. Не наблюдалась и значимая гематурия, потребовавшая трансфузии препаратов крови (таблица 2).
Таблица 2. Побочные эффекты HIFU T1-2 (n = 2200)

Таким образом, ТУРПЖ должна предшествовать проведению ультразвуковой абляции, поскольку при монотерапии HIFU имеется слишком высокая вероятность обструктивных осложнений, вплоть до острой задержки мочи. Одной из отличительных черт HIFU-терапии является ее высокая радикальность (сравнимая с РПЭ), если судить по надиру ПСА, который составляет 0,1 нг/мл и является значимым параметром радикальности лечения. И, несомненно, очень важным показателем приемлемости HIFU-терапии является тот факт, что, согласно анкетированию, 93% пациентов снова выбрали бы HIFU-терапию как метод лечения РПЖ, будь у них такая возможность.
Место паллиативной HIFU-терапии
Изучая возможности расширения показаний к HIFU-терапии, мы выполняли данное вмешательство у пациентов с местнораспространенным и метастатическим РПЖ, а также пациентам с рецидивом заболевания после любого из существующих методов лечения РПЖ (радикальная простатэктомия, гормональное лечение, лучевая терапия, брахи-, криотерапия, и их различных сочетаний).
Сальважная HIFU-терапия имеет очень большое значение, поскольку известно, что в течение 10 лет после лучевой терапии у 63% пациентов наблюдается рецидив заболевания, причем у 1/3 из них рецидив имеет только местный характер. Даже у больных, перенесших РПЭ, общая частота рецидивирования составляет 23% (база данных US CaPSURE). У пациентов с рецидивом РПЖ после радикальной простатэктомии HIFU обладает наилучшим профилем безопасности. Тем не менее, после этой процедуры частота тяжелого недержания мочи достигает 19%, а риск обструкции – 24% случаев.
Если посмотреть на результаты исследований, оценивавших эффективность сальважной HIFU-терапии, то можно отметить, что 5-летняя онкоспецифическая выживаемость пациентов составила 83%, а безрецидивная выживаемость – 44% при сравнимом с другими методами уровне безопасности. В рекомендациях EAU указано, что после неудачной лучевой терапии, пациенты в большинстве своем должны либо наблюдаться, либо получать гормональную терапию. Однако, наши данные свидетельствуют об обратном. Berge et al. (2010 г) также провели исследования, которые показали, что эффективность сальважной HIFU-терапии при рецидиве РПЖ после лучевой терапии достигает 61%.
Одной из отличительных особенностей HIFU-терапии является возможность подвергнуть лечению именно ту область, в которой отмечается рецидивная опухоль, без повреждения окружающих тканей.
Возможными целями проведения паллиативной HIFU-терапии являются: предотвращение опухолевой инфильтрации стенки прямой кишки и шейки мочевого пузыря, уменьшение распространения клеток из первичной опухоли, уничтожение гормонально резистентных клеток, а также профилактика осложнений (инфра-/суправезикальной обструкции, кровотечения). Также есть мнение, что паллиативная HIFU-терапия приводит к улучшению выживаемости и повышению качества жизни.
У пациентов после паллиативной HIFU-терапии снижение ПСА наблюдается в 99% случаев (надир 0,19 нг/мл), и только 5% из них нуждаются в гормональной терапии. При гормонально-резистентном РПЖ, уровень ПСА достигает предоперационного значения в среднем через 2 года после HIFU. Показательно, что даже при метастатическом поражении при гормональнорезистентном РПЖ снижение ПСА происходит у 65% пациентов. Трудно объяснить такие результаты, однако мы полагаем, что у пациентов с метастатическим РПЖ это происходит благодаря вовлечению и активации иммунной системы. То есть, абляция опухоли является инициатором формирования иммунного ответа. Некоторые работы свидетельствуют об активации дендритных клеток и изменении экспрессии генов в раковых клетках, снижении секреции им иммуносупрессирующих цитокинов.
Фокальная, таргетная HIFU-терапия
Еще в 2008 г. в ответ на запрос «prostate cancer focal therapy» в Google, нами было получено только 46 ответов, однако в 2011 г. эта цифра составила уже 1 960 000! Это говорит о высоком интересе к проблеме фокальной терапии РПЖ среди специалистов.
Одним из основных доводов против фокального лечения является утверждение, что РПЖ – это мультифокальное заболевание, и вы никогда не знаете, сколько фокусов опухоли и где надо уничтожить, чтобы вмешательство стало радикальным. С другой стороны, известно, даже при мультифокальном поражении, уничтожение основного фокуса опухоли, позволяет увеличить время до биохимического рецидива на 3-4 года. При проведении доплеровского трансректального УЗИ, можно увидеть, что в области фокального воздействия полностью отсутствует кровоток, а при гистологическом исследовании наблюдается массивный фиброз тканей (рисунок 6). Фокальная терапия также позволяет сохранить сосудисто-нервные пучки, что приводит к сохранению эректильной функции после лечения.
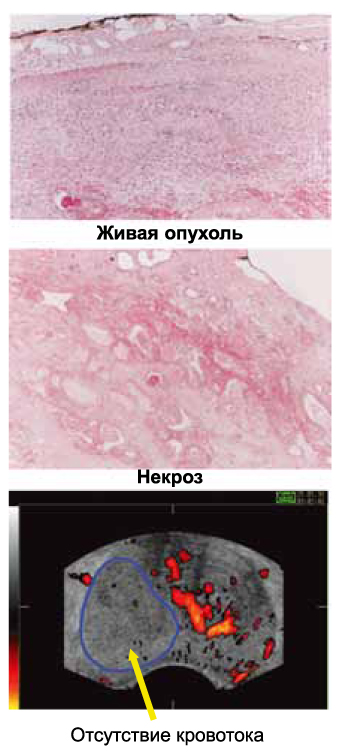
Рисунок 6. Результаты применения HIFU
Выводы
Таким образом, HIFU-терапия может рассматриваться как «идеальный» метод фокального лечения, поскольку отсутствует облучение и воздействие на ткани, и возможно сфокусировать ультразвуковые волны в очень малом объеме.
Перспективная стратегия ведения пациентов в эпоху ранней диагностики РПЖ, по нашему мнению, выглядит следующим образом. На первом этапе должна проводиться комплексная оценка рисков, связанных с заболеванием. Потом, лечение должно начинаться с фокальной терапии, и лишь при ее неэффективности необходимо переходить к радикальному лечению. В случае возникновения рецидивов заболевания после применения радикальных методов, HIFU предоставляет возможность минимальноинвазивного воздействия на них. При необходимости – в сопровождении адъювантной системной терапии. Этот мультимодальный подход может привести к более впечатляющим результатам, чем те, которые мы имеем сегодня.
Ключевые слова: рак предстательной железы, HIFU-терапия, фокальная терапия, паллиативная терапия.
Keywords: prostate cancer, HIFU-therapy, focal therapy, palliative therapy.






