Фибропластическая индурация полового члена или болезнь Пейрони в последнее десятилетие является одной из важных социальных проблем у урологических больных. Это заболевание не представляет опасности для жизни пациента, но затрудняет ведение половой жизни, приводит к сексуальной несостоятельности мужчин трудоспособного возраста, распаду семьи, выраженной депрессии [1-4].
Впервые болезнь Пейрони описана в 1743 г. F. de la Peyronie, придворным хирургом Луи XV, а по некоторым данным Фаллопиусом [5]. Однако до настоящего времени этиология и патогенез данного заболевания остаются недостаточно изученными.
Фибропластическая индурация полового члена или болезнь Пейрони в последнее десятилетие является одной из важных социальных проблем у урологических больных. Это заболевание не представляет опасности для жизни пациента, но затрудняет ведение половой жизни, приводит к сексуальной несостоятельности мужчин трудоспособного возраста, распаду семьи, выраженной депрессии [1-4].
Впервые болезнь Пейрони описана в 1743 г. F. de la Peyronie, придворным хирургом Луи XV, а по некоторым данным Фаллопиусом [5]. Однако до настоящего времени этиология и патогенез данного заболевания остаются недостаточно изученными.
В последнем пересмотре МКБ-10 (2005 г.) болезнь Пейрони и фиброз кавернозных тел полового члена объединены в одну нозологическую группу, относящуюся к пластической индурации полового члена. Отмечено много общего в патогенезе и симптоматике этих заболеваний, исходом которых бывает эректильная дисфункция [6-8].
Одни авторы под фибропластической индурацией понимают заболевание с преимущественной локализацией патологического процесса в пещеристых телах полового члена, приводящее к его деформации во время эрекции. Другие подразумевают постепенное и малоболезненное уплотнение нескольких участков пещеристых тел, появление в них плотных соединительнотканных включений, приводящих к нарушению функции полового члена. Третьи полагают, что это доброкачественное медленно прогрессирующее заболевание неясной этиологии, характеризующееся образованием фиброзных экстракавернозных бляшек на белочной оболочке полового члена, приводящих к искривлению эрегированного полового члена и нарушению эректильной функции [9, 10].
Болезнь Пейрони относится к числу редких, хотя обращаемость больных за последние годы несколько увеличилась [11-15]. Распространенность этого заболевания по данным J.A. Vale составляет 388 человек на 100 000 населения или 2-3% в мужской популяции, а ежегодный прирост составляет 25,7 человек на 100 000 населения. За последние десятилетия отмечают увеличение заболеваемости болезнью Пейрони.
По данным П.А. Щеплева и соавт. [16] болезнь Пейрони составляет 3-8% по обращаемости и до 25% по данным аутопсий. Наибольшее количество наблюдений этого заболевания приходится на возраст 50-60 лет, хотя может встречаться и у молодых людей, причем не менее 25% этих больных страдают эректильной дисфункцией [17, 18]. Частота возникновения фибропластической индурации полового члена увеличивается с возрастом.
Некоторые авторы относят болезнь Пейрони к коллагенозам и чаще рассматривают ее как полиэтиологическое заболевание. Существенную роль в развитии этой патологии играют травматический, воспалительный, генетический и иммунологические факторы. Болезнь Пейрони это очаговый фиброз белочной оболочки полового члена, приводящий к нарушению соотношения коллагеновых и эластических волокон, нарушению эластичности белочной оболочки, искривлению полового члена во время эрекции в том направлении, где белочная оболочка не нарушена.
Вовлечение в процесс фасции Букка, перфорантных сосудов и дорсальных артерий полового члена приводит к нарушению веноокклюзионного механизма и артериальной недостаточности полового члена. В рубец чаще вовлекается дорсальная часть полового члена, реже латеральная, вентральная. В связи с отложением в уплотненных участках солей кальция они приобретают хрящевую консистенцию. Соединительнотканные бляшки появляются на тыльной поверхности одного или обоих кавернозных тел, как плоское полигональное образование, растущее вниз, вглубь. Бляшек может быть одна, две и более. При болезни Пейрони мочеиспускательный канал и его пещеристые тела в патологический процесс не вовлекаются. Изъязвлений, злокачественных перерождений узлов никогда не наблюдается. При гистологическом исследовании в бляшках обнаруживали коллагеновые волокна с расположенными между ними фибробластами и небольшим количеством сосудов и эластических волокон.
Н.А. Лопаткин [2] классифицирует болезнь Пейрони по стадиям:
- 1 стадия заболевания бляшка на белочной оболочке не определяется, только присутствуют боли при эрекции;
- 2 стадия наблюдается образование фиброзно-эластической бляшки на белочной оболочке;
- 3 стадия при гистологическом исследовании бляшки обнаруживают коллагеновые волокна;
- 4 стадия кальцификация бляшки.
Оценить степень воспалительной реакции сложно, однако длительность заболевания больше года и стабильность бляшки в течение 3 мес. служат ориентиром перехода болезни в стабильную стадию.
Консервативное лечение болезни Пейрони показано в первом периоде заболевания до наступления кальцификации бляшки при угле искривления полового члена менее 30-45 градусов. Оперативное лечение выполняют при выраженном (более 45 градусов) искривлении полового члена, препятствующем коитусу. Применяют пликационные методы, иссечение бляшки с одновременным фаллоэндопротезированием полового члена, различные виды корпоропластик [1922].
Консервативное лечение включает применение противовоспалительных, противовирусных, гормональных препаратов, блокаторов кальциевых каналов (верапамил). Рекомендуется применение различных физиотерапевтических методов лечения лазеромагнитная терапия, ультразвук, чрезкожный электрофорез с верапамилом, близкофокусная рентгенотерапия, ударно-волновая терапия.
Несмотря на вышеуказанные факты, нет однозначного мнения по поводу патогенетического лечения фибропластической индурации с признаками и без признаков сосудистых нарушений полового члена.
Материалы и методы
В клинике урологии и андрологии ДПО МАПО обследовано 33 пациента с болезнью Пейрони в возрасте от 25 до 66 лет (средний возраст больных 45,5 года). Все пациенты предъявляли жалобы на незначительное искривление полового члена, снижение качества адекватных эрекций, умеренные боли при эрекции, появление уплотнений в области кожи полового члена в течение от 3 месяцев до 1,5 лет.
Обследование больных включало физикальный осмотр, определение параметров искривления полового члена на аппарате АМВЛ-01(вакуумно-лазерном), анкетирование по шкале МИЭФ5, ультразвуковую допплерографию полового члена (УЗДГ) с применением фармакопробы с альпростадилом 10-20 мг с одновременным определением максимальной систолической, средней, диастолической скорости кровотока и индексов периферического сопротивления в сосудах полового члена. Части пациентов выполняли динамическую кавернозографию. Исследовали уровень половых и гонадотропных гормонов в сыворотке крови: тестостерон, глобулин, связывающий половые гормоны (SHBG), ФСГ, ЛГ, пролактин, эстрадиол, глюкозу. У всех пациентов исключены ИППП, уровень ПСА у них был ниже 2 нг/мл. Уровень половых и гонадотропных гормонов у всех пациентов был в пределах нормы.
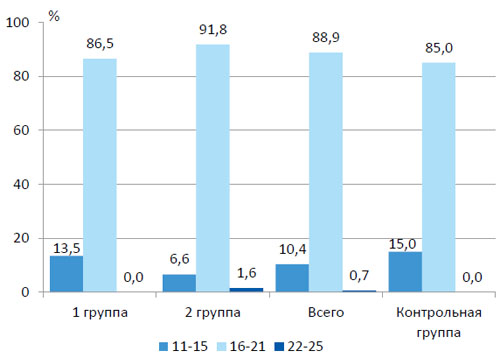
Рисунок 1. Показатели МИЭФ у больных 1,2 и контрольной групп до лечения (М ± m)
Все пациенты были разделены на 2 группы. В I группу вошли 18 больных, которым в комплексное лечение был включен препарат Лонгидаза, вводимый внутримышечно по 3000 МЕ 1 раз в течение 10 дней (на курс 10 инъекций) с одновременным введением ректально суппозиториев с Лонгидазой в той же дозе через 1 день (на курс 10 свечей). Во II группу вошли 15 пациентов, которым Лонгидазу не назначали. Пациентам обеих групп в комплексное лечение включали лазеромагнитотерапию. Контрольную группу составили 20 пациентов с эректильной дисфункцией (ЭД) без болезни Пейрони.
Таблица 1. Сосудистые нарушения у больных I, II и контрольной групп до лечения по УЗДГ полового члена
| группы с болезнью | признаки сосудистых нарушений по УЗДГ пч до лечения | |
| пейрони | Выявлены | не выявлены |
| I группа | 11 | 7 |
| II группа | 9 | 6 |
| Контрольная группа | 20 | 0 |
Таблица 2. Допплерографические показатели кровотока в сосудах полового члена у больных I,II и контрольной групп до лечения (М ± m)
| показатели в кавернозных артериях | 1 группа | II группа | контрольная группа | нормативы |
| Vmax, см/с. | 9,8 ± 0,8 | 10,5 ± 1,1 | 11,2 ± 1,6 | 25-27 |
| Vmln, см/с. | 1,0 ± 0,4 | 1,2 ± 0,5 | 1,8 ± 0,9 | 0,38 |
| Vmed, см/с. | 2,1 ± 0,2 | 2,0 ± 0,3 | 3,2 ± 0,7 | 3,5 |
| RI | 1,001 ± 0,030 | 1,040 ± 0,033 | 1,134 ± 0,046 | 0,96 |
| PI | 3,317 ± 0,322 | 3,741 ± 0,384 | 3,651 ± 0,404 | 2,45 |
Лонгидаза ковалентный конъюгат высокомолекулярного соединения полиоксидония и фермента гиалуронидаза, имеет пролонгированное действие. Гиалуронидаза препятствует образованию коллагеновых волокон и расщепляет «цементирующий» компонент соединительной ткани гиалуроновую кислоту, а полиоксидоний полимерный препарат, защищающий белковую молекулу от ингибиторов, инактивирующих фермент в организме, обладающий иммуномодулирующими, противоинфекционными, детоксикационными и антиоксидантными свойствами.
 |
 |
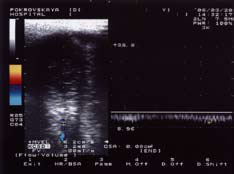 |
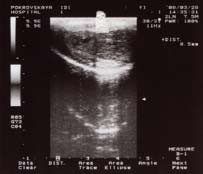
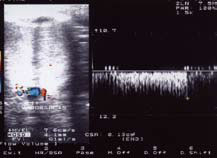
Рисунок 2. УЗДГ полового члена больного Д. 36 л. с болезнью Пейрони. Веногенная ЭД. В дистальной части полового члена выявляются бляшки размерами от 1-2 и до 8,5 мм; Vmax в кавернозных артериях в покое составляет 14,5 см/с; в фазе тумесценции -32,9 см/с.; в фазе эрекции 47,8 см/с.; в дорсальной артерии 20,9. Дорсальная вена не спадалась и кровоток по ней определялся в течении всего исследования до 30 мл/мин. Проба Вальсальвы положительная. Сахар крови 5,26 ммоль/л; SHBG 26 нмоль/л; Т 9,56; пролактин 19,26; ФСГ 4,63; ЛГ 6,62.
 |
 |
 |
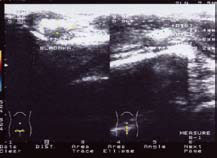 |
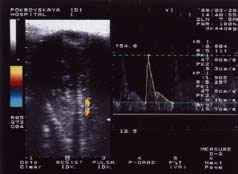
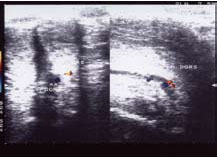
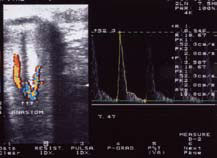
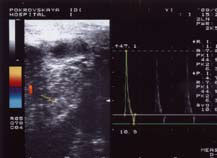
Рисунок 3. УЗДГ полового члена больного Т. 55 л. с болезнью Пейрони, веногенной ЭД.
 |
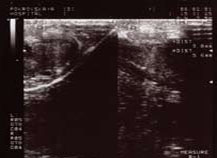 |
Рисунок 4. УЗДГ полового члена больного О. 44 лет с болезнью Пейрони без признаков ЭД. В кавернозных телах не отмечается фиброзных изменений, над белочной оболочкой левого кавернозного тела несколько бляшек до 0,6 мм, справа единичная бляшка до 0,3 мм. Асимметрия кровотока отсутствует, достигнуты оптимальные пиковые линейные скорости и индексы периферического сопротивления в обеих кавернозных артериях. Дорсальная вена не определяется.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Исходно у всех пациентов с болезнью Пейрони угол отклонения эрегированного полового члена на аппарате АМВЛ-01 был не более 30-45 градусов, пальпировались бляшки от 0,5 до 1,5 см в диаметре, чаще на дорсальной поверхности полового члена.
Результаты анкетирования МИЭФ 5 представлены на рисунке 1. При этом не отмечено статистически достоверных различий в различных группах больных.
При ультразвуковом исследовании у 17 (51,5%) из 33 пациентов размеры бляшек были от 0,5 см до 1,0 см в диаметре, у 7 (21,2%) более 1 см, у остальных 9 (27,3%) пациентов размеры бляшек менее 0,5 см в диаметре, при этом распределение больных по размерам бляшки была одинаковой и в I и во II группах (таблица 3).
Ультразвуковая допплерография полового члена выявила признаки сосудистых нарушений у 11 больных I группы, 9 больных II группы и у всех больных контрольной группы (таблица 1). У 13 пациентов 1 и 2 групп сосудистых нарушений при УЗДГ полового члена мы не выявили.
В таблице 2 представлены основные показатели гемодинамики у больных со сниженным кровотоком в артериях полового члена. Как видно из таблицы 2, у пациентов выявлено снижение максимальной систолической скорости (Vmax) кровотока в кавернозных артериях полового члена более чем в 2 раза соответственно в I, II и контрольной группах до 9,8 ± 0,8; 10,5 ± 1,1; 11,2 ± 1,6 см/с. (при норме 25-27 см/с.). Мы считаем, что снижение кровотока в артериях полового члена обусловлено механическим сдавлением фибропластической бляшкой, а патологический венозный дренаж вызван слабой эластичностью белочной оболочки.
На рисунках 2, 3, 4 представлена допплерография сосудов полового члена у различных больных.
Выявлена аномалия строения кавернозных артерий. В кавернозных телах определяются бляшки размерами 11,4 х 4,6 х 9,2 мм и деформация полового члена. В ножке полового члена кавернозные артерии имеют анастомоз. У больного имеется контрактура Дюпюитрена.
Отдаленные результаты лечения были изучены через 6 и 12 месяцев представлены в таблице 3.
Как видно из таблицы 3, исходно у 72% больных I группы размеры бляшки превышали 0,5 см, через 6 мес. 33% имели бляшки указанных размеров и через год 22%. Во II группе 73% больных исходно имели бляшки более 0,5 см, через 6 мес. 40% и через год 33%.
Таблица 3. результаты лечения больных I и II групп с болезнью Пейрони
| группы больных | размеры бляшек по данным УЗДГ | |||||||||
| с болезнью | до лечения | через 6 мес. после лечения | через 1 год после лечения | клинический эффект | ||||||
| пейрони | < 0,5 см | 0,5-1,0 см | > 1 см | < 0,5 см | 0,5-1,0 см | > 1 см | < 0,5 см | 0,5-1,0 см | > 1см | |
| I группа (n = 18) | 5 | 9 | 4 | 1 | 4 | 2 | 3 | 1 | 66,6% | |
| II группа (n = 15) | 4 | 8 | 3 | 2 | 4 | 2 | 1 | 3 | 2 | 33,3% |
| Всего (n = 33) | 9 | 17 | 7 | 2 | 7 | 4 | 1 | 6 | 3 | |
Таким образом, в результате лечения через 1 год положительный клинический эффект (увеличение МИЭФ, улучшение качества эрекции, уменьшение болевого симптома, увеличение скорости кровотока в сосудах полового члена, уменьшение размеров бляшки) нами отмечен у 66,6% больных I группы, получавших сочетанное лечение с Лонгидазой, и в 2 раза хуже получены результаты (у 33,3% пациентов) во II группе пациентов, которые не получали Лонгидазы. Трем пациентам II группы с искривлением полового члена выполнен пликационный метод без иссечения бляшки с дальнейшим приемом Лонгидазы внутрь и в виде суппозиториев.
Заключение
В ходе настоящего исследования выяснено, что у пациентов с болезнью Пейрони определяются нарушения как артериального, так и венозного кровотока в половом члене, за счет сдавления сосудов фибропластической бляшкой, слабости белочной оболочки, приводящих к эректильной дисфункции.
Таким образом, в составе комплексного лечения болезни Пейрони в качестве патогенетической терапии применение Лонгидазы оправдано и необходимо. В результате проведенного исследования отмечено, что пролонгированное действие препарата Лонгидаза эффективно и безопасно при лечении пациентов с болезнью Пейрони. При ее применении снижается выраженность клинических симптомов и воспаления в месте фибропластической индурации, повышается качество эрекции, уменьшаются болевые ощущения. Мониторинг УЗДГ полового члена помогает определить результативность или неэффективность лечебных мероприятий и выбрать патогенетически обоснованный метод лечения. Применение препарата Лонгидаза показано в любом возрасте при наличии болезни Пейрони, но особенно у пациентов, когда выполнение операций по соматическому состоянию невозможно.
Ключевые слова: Болезнь Пейрони, фибропластическая индурация полового члена, допплерография полового члена, лечение, Лонгидаза.
Keywords : Peyronie Disease, penile plastic induration, ultrasound and Doppler investigation, treatment, Longidasa.
Литература
- Мазо Е.Б., Муфагед М.Л., Иванченко Л.П. и др. Консервативное лечение болезни Пейрони в свете новых патогенетических данных // Урология. 2006. № 2. С. 31-37.
- Урология / под ред. Н. А. Лопаткина. М. ГЭОТАР-Медиа. 2007. 368 с.
- Adeniyi A. A., Goorney S.R., Pryor J.P. et al. The Lue procedure: an analysis of outcome of Peyronie, s disease // BJU Int. 2002. Vol. 89. P. 404-408.
- Austoni E., Colombo F., Mantovani F., et al. Chirurgia radicale e conservazione dell, erezione nella malattia di la Peyronie // Arch. Ital. Urol. 1995. Vol. 67. P. 359-364.
- Dunsmuir W.D., Kirby R.S. Francois de LaPeyronie (1978-1747): the man and the disease he described. Br J Urol. 1996. Oct. 78 (4): 613-22.
- Incrocci L. Wijnmmaalen A., Slob A.K. et al. Low-dose radiotherapy in 179 patients with peyronie,s disease: treatment, outcome and current sexual function // Int. J. Radiat. oncol. Biol. Phys. 2000. Vol. 47. P. 1353-1356.
- Jennifer L. Peyronie,s diasease plaque – derived fidrodlats dring cytomegalovirus (CMV) DNA // J. Urol. 2003. Vol. 170. Р. 2053-2056.
- Lebret T., Loison G., Herve J.M. et al. Extracorporeal shock wave therapy in treatment of Peyroni, s disease: experience with standard lithotripter (Simen-Multiline) // Urology. 2002. Vol. 59. P. 657-661.
- Levine L.A., Goldman K.E., greenfild J.M. Experience with itraplaque injection og verapamil for Peyronie, s disease // J. Urol. 2002. Vol. 168. P. 621-625.
- Mufti G., Aitchison M., Bramwell S.P. et al. Corporeal placation for surgical correction of Peyronie, s disease // J. Urol. 1990. Vol. 144. P. 281-282.
- Brannigan R.E., Kim E.D., Oyasu et al. Comparison of tunica fibuginea substitutes for the treatment Peyronie, s disease // J. Urol. 1998. Vol. 159. P. 1064-1068.
- Carson C.C. Penile prosthesis implantation in the treatment of Peyronie,s disease // Int. J. Impot. Res. 1998. Vol. 10. P. 125-128.
- Chilton C.P., Caste W.M., Westwood C.A. et al. Factors associated in the etiology of Peyronie,s // Br. J. Urol. 1982. Vol. 54. P. 748-750.
- El-Sacca A.I., Rashwan H.M., Lue T.F. Venosus patch graft for Peyronie,s disease. Part II. Outcome analysis // J. Urol. 1998. Vol. 160. P. 2050-2053.
- Gasior B.L., Levin F.J., Howanessian A. et al. Plaque-associated corporal veno-occlusive dysfunction in in idiopatic Peyronie,s disease: a pharmacavernosometric study // World J. Urol. 1990. Vol. 8. P 90-96.
- Щеплев П.А., Данилов И.А.. Колотинкский А.Б., Гвасалия Б.Р., Гарин Н.Н. Клинические рекомендации. Болезнь Пейрони // Андрология и генитальная хирургия. 2007. № 1. С. 55-58.
- Pryor J.P., Ralph D.J Clinical presentations of Peyronie, s disease // Int. J. Impot. Res. 2002. Vol. 14. P. 414-417.
- Кротовский Г.С. Лечение сосудистой импотенции. М. СПб. БИНОМ. 160 с.
- Сокольщик М.М. , Гагарина С.В., Петрович Р.Ю. и др. Лечение эректильной дисфункции у пациентов с пластической индурацией полового члена // Урология. 2008. № 1. С. 41-44.
- Тиктинский О.Л., Новиков И.Ф., Михайличенко В.В. Заболевания половых органов у мужчин. Л. Медицина. 1985. 293 с.
- Тиктинский О.Л., Михайличенко В.В. Андрология. СПб. Медиа Пресс. 480 с.
- Королева С.В., Ковалев В. А., Лещева Н. В. и др. Выбор метода корпоропластики при болезни Пейрони в зависимости от гемодинамического статуса полового члена // Урология 2005. № 6. С. 26-30.






