Проблема уронефрологии является одной из важнейших в системе здравоохранения. Урологические заболевания оказывают существенное влияние на состояние здоровья общества [1,2]. Если в 80-90-х гг. ХХ столетия доля урологических болезней составляла 4-5% общей заболеваемости, то к нынешнему времени она увеличилась до 7% [3]. Среди них можно выделить группу заболеваний, наиболее значимых в медико-демографическом отношении: мочекаменная болезнь (МКБ), хроническая почечная недостаточность (ХПН), заболевания предстательной железы, хронический пиелонефрит и онкоурологические заболевания. Данные нозологические единицы составляют основную долю уронефрологических заболеваний, их прогрессирование сопровождается значительным числом различных осложнений и требует серьезного специализированного лечения у специалистов-урологов [4]. Однако, как правило, наряду с урологическими заболеваниями у пациентов присутствует и ряд других, сочетанных заболеваний. Наибольшее прогностическое значение среди них имеют заболевания сердечно – сосудистой системы. Коморбидность урологических и кардиологических заболеваний необходимо учитывать при планировании тактики ведения больных.
Как известно, факторами риска развития сердечно-сосудистых заболеваний являются артериальная гипертония (АГ), гиперхолестеринемия, курение, мужской пол, ожирение и др. [5]. В исследовании Hamano S. и соавт. [6] изучалась корреляция между МКБ и такими факторами риска ишемической болезни сердца (ИБС), как индекс массы тела (ИМТ), курение, гиперхолестеринемия, АГ, сахарный диабет (СД). Было показано, что среди пациентов с развившейся МКБ по сравнению с контрольной группой, значительно чаще встречались люди с АГ, гиперхолестеринемией, высоким ИМТ и курильщики. Также было выявлено, что при ожирении и АГ повышается риск развития МКБ у людей, а гиперхолестериновая диета ведет к образованию почечных камней у крыс. Кроме того, вероятность формирования оксалатных камней увеличивается при курении и гиперлипидемии. Таким образом, показано, что факторы риска ИБС являются одновременно и факторами риска формирования МКБ [6]
Значительное количество работ показало сочетание АГ и МКБ [7, 8, 9, 10]. Так, в исследовании, проведенном шведскими учеными, была проанализирована частота встречаемости МКБ у 895 пациентов: нефролитиаз был диагностирован у 1,1% пациентов с нормальным или пониженным АД и у 13,3% – с повышенным АД [11]. В аналогичном исследовании итальянских ученых также было показано, что у людей с повышенным диастолическим АД (ДАД), по сравнению с нормальным, нефролитиаз наблюдается чаще (у 5,22% по сравнению с 3,36%, р=0,009) [7]. В результате 8летнего наблюдения за пациентами было показано, что АГ развилась у 17,4% с МКБ и только у 13,1% пациентов без нее [12]. Эти значимые различия сохранились и при введении поправки, учитывающей другие факторы риска развития АГ, такие как возраст, ИМТ, потребления алкоголя и др.
Цель настоящего исследования изучение особенностей подготовки больных с АГ к оперативному лечению МКБ.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование было включено 589 больных МКБ с сопутствующей АГ (группа I). Больные были направлены на лечение в ГКУБ № 47 ДЗ г. Москвы в период с ноября 2011 г. по февраль 2012 г. Диагностика АГ осуществлялась в соответствии с критериями, опубликованными в Рекомендациях Всероссийского Научного Общества Кардиологов (ВНОК) от 2010 г. [13]. Все больные, включенные в исследование, страдали АГ в течение нескольких лет, до выявления у них урологического заболевания. Анамнез АГ в среднем составил 7±1,5 года. В этой группе у 14 больных была выявлена АГ I стадии, у 60 II стадии и у 441больного III стадия. Преобладали больные с АГ III стадии, у которых наблюдалась ИБС и стенокардия напряжения I и II ФК. В исследование не включались больные с доказанной вторичной АГ, высокими цифрами привычного артериального давления (АД) (>200/110 мм рт.ст.), резистентного к проводимому лечению, декомпенсированным сахарным диабетом, сердечной недостаточностью III-IV ФК.
Контрольная группа (группа экстренных вмешательств – ЭВ, группа II) сформирована включением 50 сопоставимых по возрасту мужчин (от 37 до 82 лет) с анамнезом АГ 6,5±3,2 года, взятых на экстренное хирургическое вмешательство по поводу МКБ в ГКУБ №47 в тот же временной период без предшествующей консультации кардиолога. Из них у 14 больных была АГ I стадии, у 10 больных II стадии и у 26 больных III стадии. В группе экстренных вмешательств, также преобладали больные с АГ III стадии. Последняя была диагностирована после выявления ИБС и стенокардии напряжения I и II ФК. 15 больных II группы (38%) постоянно получали антигипертензивные препараты, 13 пациентов принимали ингибиторы (ИАПФ) (эналаприл, лизиноприл или фозиноприл) и 2 больных получали комбинированную терапию ИАПФ и диуретиком или бета-блокатором. Об эффективности проводимой терапии судить сложно, так как суточное мониторирование АД (СМАД) до операции больным II группы не проводилось.
У 334 больных (56,7%) группы I и у 18 лиц (36%) группы II отмечалась некардиальная сопутствующая патология. Общая клинико-демографическая характеристика больных I и II групп приведена в табл.1.
Всем больным АГ, направленным на консультацию кардиолога, проводилось СМАД до оперативного вмешательства, при необходимости после подбора терапии. Затем исследование осуществлялось на вторые сутки после операции, по результатам которого у части больных вновь проводилась коррекция терапии. Контрольное СМАД производилось на десятые сутки после урологического вмешательства.
Больным II группы СМАД до оперативного вмешательства не производилось, так как больные были госпитализированы внепланово и были направлены на экстренное хирургическое вмешательство. В послеоперационном периоде больным II группы, также как и лицам группы I, СМАД производилось на вторые и десятые сутки после хирургического вмешательства.
Коррекция антигипертензивной терапии потребовалась 448 больным (76%) I группы, из них 219 больных были с сочетанием АГ и ИБС (49,7% от общего числа больных с сочетанием АГ и ИБС). Усиление антигипертензивной терапии потребовалось 147 больным с МКБ (24,9%).
При этом больным, которые получали постоянную антигипертензивную терапию ИАПФ фозиноприлом, в случае его неэффективности, увеличивалась доза принимаемого препарата и/или в последующем присоединялся препарат другой группы (блокатор кальциевых каналов). Больным, не получавшим постоянного лечения, назначался также ИАПФ, метаболизирующийся через печень, фозиноприл по 5 мг2 раза в день, затем при необходимости увеличивалась его доза до 10 мг 2 раза в день и/или присоединялся блокатор кальциевых каналов нифедипин-ретард (в начальной дозе 10 мг 2 раза в день) или амлодипин (в начальной дозе 5 мг 1 раз в сутки). Пациенты с ИБС и нарушениями ритма сердца получали изначально комбинированную терапию ИАПФ фозиноприлом и бета-адреноблокатором (БАБ) бисопрололом в суточной дозе 2,5-5 мг. У 3 пациентов не удалось достичь целевого уровня АД на фоне приема двух антигипертензивных препаратов, поэтому им было отказано в операции и для подбора эффективного гипотензивного лечения они были направлены в многопрофильный стационар, из нашего исследования они были исключены (рис.1).
Таблица 1. Общая клинико-демографическая характеристика больных I и II групп
| Признаки | Группа I (N=589) |
Группа II (N=50) |
р | |
|---|---|---|---|---|
| Средний возраст, лет | 55±5,8 | 57±4,9 | >0,05 | |
| Среднесуточное АД, мм рт.ст. | 159,2±5,6 | – | – | |
| Анамнез АГ, лет | 5±3,1 | 4±3,5 | >0,05 | |
| Уровень креатинина мкмоль/л | 65±2,5 | 68±3,4 | >0,05 | |
| СКФ мл/мин | 137±1,1 | 139±1,3 | >0,05 | |
| Сопутствующие заболевания |
Индекс массы тела, кг/м2 |
26,5±4,3 | 25±3,9 | >0,05 |
| ИБС | 441 (74,9%) | 26 (52%) | >0,05 | |
| Хронический гастрит |
116 (19,7%) | 8 (16%) | >0,05 | |
| ХОБЛ | 102 (17,3%) | 10 (20%) | >0,05 | |
| СД 2 типа | 67 (11,4%) | 5 (10%) | >0,05 | |
| Хронический панкреатит |
37 (6,3%) | 3 (6%) | >0,05 | |
| ЖКБ | 12 (2,0%) | 2 (4%) | >0,05 | |
Остальным 586 больным I группы были проведены хирургические операции по коррекции урологической патологии. Основные виды оперативных вмешательств представлены в таблице 2.
Таблица 2. Основные оперативные вмешательства
| Вид оперативного вмешательства | Группа N=586 | % | Группа II N=50 | Группа II N=50 |
|---|---|---|---|---|
| Дистанционная литотрипсия (ДЛТ) | 500 | 85,3% | 43 | 86% |
| Контактная пиелолитотрипсия | 86 | 14,6% | 7 | 14% |
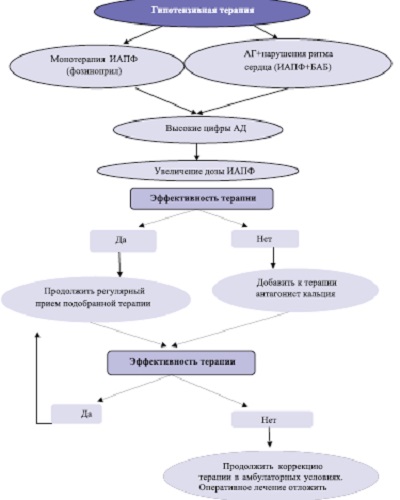
Рис. 1. Схема подбора гипотензивной терапии у больных с МКБ и АГ
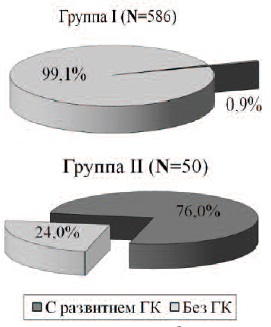
Рис. 2. Частота развития ГК у больных I и II групп в раннем послеоперационном периоде
РЕЗУЛЬТАТЫ
В раннем послеоперационном периоде у 5 больных (0,9%) I группы развился гипертонический криз (ГК). Терапия ГК заключалась в назначении фуросемида 40 мг внутривенно и 20 мг нифедипина короткого действия однократно под язык. У всех этих больных была произведена дистанционная литотрипсия (ДЛТ) по поводу МКБ. Во II группе в раннем послеоперационном периоде ГК развился у 38 больных (76,0%), причем эти больные так же подвергались ДЛТ (р< 0,0001) (рис. 2).
По результатам СМАД, проведенного на вторые сутки после операции, повышенные значения АД зарегистрированы у 81 (13,8%) больного I группы. В группе II повышенные значения АД по результатам СМАД в эти же сроки, потребовавшие коррекции антигипертензивной терапии, зарегистрированы у 39 (78%) больных (р< 0,01) (рис. 3). Все больные, у которых отмечено повышение АД по результатам СМАД, подвергались ДЛТ и повышенное АД после ДЛТ в группе I отмечено у 16,2%, в группе II – у 90,7% (39 из 43 больных) (р< 0,01).
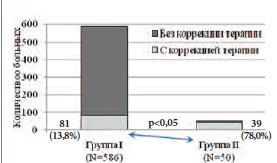
Рис. 3. Сравнение количества больных I и II групп, которые нуждались в коррекции терапии на вторые сутки послеоперационного периода
При контрольном СМАД на десятые сутки послеоперационного периода по сравнению с данными от СМАД, выполненного на вторые сутки после операции, в основной группе отмечено статистически значимое снижение уровня таких показателей, как среднесуточное систолическое АД (СССАД 24 ч, со 149,7±5,7 мм рт.ст. до 135,2±6,7 мм рт.ст., р< 0,001), среднесуточное диастолическое АД (ССДАД 24 ч, с 91,2±3,9 мм рт.ст. до 85,7±4,1 мм рт.ст., р< 0,05), процент повышенных значений ДАД за сутки (ДАД 24ч. >85 мм рт.ст., с 36,3±15,7% до 19,8±12,3%, р< 0,05), среднее систолическое АД за дневное время (ССАД день, со 148,8±16,1 мм рт.ст. до 139,8±12,2 мм рт.ст., р< 0,05), среднее диастолическое АД за дневное время (СДАД день, с 81,3±6,8 мм рт.ст. до 74,4±5,1 мм рт.ст., р< 0,05), процент повышенных значений диастолического АД за дневные часы (ДАД день >90 мм рт.ст., с 39,2±8,9% до 25,2±9,8%, р < 0,001). При этом результаты СМАД достигли уровня нормальных значений у 584 (99,7%) прооперированных больных I группы.
В группе II на десятые сутки послеоперационного периода по сравнению с результатами СМАД на вторые сутки после операции отмечено статистически значимое снижение уровня СССАД 24ч (со 158,3±5,2 мм рт.ст. до 151,2±6,1 мм рт.ст., р< 0,05), САД макс (со 181,0±14,2 мм рт.ст. до 168,6±15,2 мм рт.ст., р< 0,05), САД – день >140 мм рт.ст. (с 63,1±14,7% до 45,1±12,6%, р< 0,05). Дальнейший подбор лечения АГ потребовался у 21 больного (42,0%). То есть процент больных, потребовавших дальнейшей коррекции антигипертензивного лечения по результатам СМАД на десятые сутки послеоперационного периода, оказался статистически значимо выше в группе II по сравнению с группой I (р< 0,0001) (рис.4).
При анализе уровня суточного индекса (СИ) в I группе оказалось, что к категории dipper (с нормальной ночной динамикой АД) на вторые сутки после вмешательств можно было отнести 505 больных (86,2%). На десятые сутки послеоперационного периода количество больных категории dipper в основной группе увеличилось до 584 (99,7%) больных (р< 0,01). 80 больных (13,7%) non-dippers (с недостаточным снижением АД во время сна) на вторые сутки послеоперационного периода полностью перешли в категорию dipper к десятым суткам после вмешательств. 3 больных (0,5%) на вторые сутки и 2 больных (0,3%) на десятые сутки после коррекции урологической патологии относились к категории over-dippers (отмечалось чрезмерно сильное снижение АД в ночные часы).
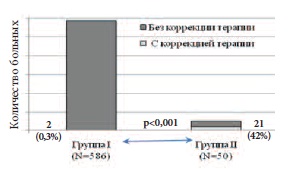
Рис. 4. Количество больных I и II групп, нуждавшихся в коррекции антигипертензивной терапии на десятые сутки послеоперационного периода
Таблица 3. Динамика показателей СМАД у больных I и II групп на вторые и десятые сутки после оперативного вмешательства
| Показатель | 2-е сутки | 10-е сутки | ||
|---|---|---|---|---|
| Группа I (N=586) |
Группа II (N=50) |
Группа I (N=586) |
Группа II (N=50) |
|
| СССАД 24 ч, мм.рт.ст. | 149,7±5,7* | 158,3±5,2** | 135,2±6,7* | 151,2±6,1** |
| ССДАД 24 ч,мм.рт.ст. | 91,2±3,9** | 96,1±3,4 | 85,7±4,1** | 93,7±3,6 |
| САД макс, мм рт.ст. | 152,3±16,2 | 181,0±14,2** | 153,7±11,6 | 168,6±15,2** |
| ДАД макс, мм рт.ст. | 100,3±12,9 | 126,7±11,3 | 97,4±9,3 | 109,8±13,2 |
| ССАД день,мм.рт.ст. | 148,8±16,1** | 159,7±14,4 | 139,8±12,2** | 157,9±11,6 |
| СДАД день, мм рт.ст. | 81,3±6,8** | 98,6±7,9 | 74,4±5,1** | 95,0±4,7 |
| СУП САД, мм рт.ст. | 14,2±4,1** | 17,8±5,2 | 8,2±1,5** | 12,9±3,6 |
| СУП ДАД, мм рт.ст. | 7,3±3,7 | 10,1±4,9 | 4,9±1,0 | 7,0±1,8 |
| САД 24 ч > 135,% | 37,4±13,5 | 52,8±13,9 | 21,5±12,4 | 45,7±11,6 |
| ДАД 24 ч > 85, % | 36,3±15,7** | 45,1±13,7 | 19,8±12,3** | 38,9±15,7 |
| ИВ % | 36,6±14,2 | 48,5±13,8 | 20,4±12,4 | 41,1±13,0 |
| САД день > 140, % | 41,1±16,8 | 63,1±14,7** | 36,6±12,7 | 45,1±12,6** |
| ДАД день > 90, % | 39,2±8,9* | 47,6±14,9 | 25,2±9,8* | 42,6±8,3 |
| СИ % | 9,8±5,6 | 13,8±6,7 | 7,9±2,2 | 10,9±5,2 |
(СУП САД скорость утреннего подъема систолического АД, СУП ДАД скорость утреннего подъема диастолического АД, ИВ индекс времени, СИ суточный индекс)
* Статистически значимое снижение уровня показателя на десятый день послеоперационного периода по
сравнению с данными на второй день после операции, * р<0,05; ** р<0,001.
Во II группе было 9 больных (18%) категории dippers на вторые сутки послеоперационного периода, на десятые сутки их количество значимо увеличилось до 28 (56%) больных (р< 0,05). Количество больных категории non-dippers, соответственно статистически значимо уменьшилось с 34 (68%) на вторые сутки до 20 (40%) на десятые сутки послеоперационного периода (p< 0,05). В группе II также были пациенты категории overdippers: 2 (4%) пациента на вторые сутки после вмешательств и 1 больной (2%) на десятые сутки (р>0,05), и категирии night-peakers (с повышением АД в ночные часы): 5 (10%) больных на вторые сутки и 1 (2%) больной на десятые сутки после лечения урологической патологии. Характеристика ночной динамики АД больных I и II групп в послеоперационном периоде представлена в таблице 4.
ОБСУЖДЕНИЕ
В данной работе нами было показано, что у больных после ДЛТ с дооперационной нормализацией АД путем усиления/начала антигипертензивной терапии (группа I), ГК в раннем послеоперационном периоде развился лишь в 0,5% случаев (у 5 из 586 больных). При отсутствии дооперационной коррекции антигипертензивной терапии (группа II) ГК развился в 76% случаев. После применения именно этой методики дробления камней в 13,8% случаев (у 81 больного из 586) отмечено повышение уровня АД по данным СМАД на вторые сутки послеоперационного периода при тщательном дооперационном подборе антигипертензивной терапии, и в 78% (39 из 50) случаев при отсутствии коррекции гипотензивного лечения.
Сравнивая наши данные с данными литературы, следует отметить, что сходные результаты были получены. Lingeman JE. et al., которые изучали результаты лечения 927 больных МКБ, 731 из которых подверглись ДЛТ (основная группа), а у 196 применялись другие методики (контрольная группа) [14]. Авторы продемонстрировали статистически значимое повышение уровня ДАД в группе ДЛТ по сравнению с данными до вмешательства, в отличие от контрольной группы. В этой работе было также показано, что при долгосрочном наблюдении частота выявления АГ в группе больных ДЛТ не превышает таковую контрольной группы. Связанное с ДЛТ острое повреждение почек, может также привести к тяжелой травме нефрона, микроциркуляторного русла и окружающего интерстиция [15]. Почечные канальцы и сосуды более уязвимы, чем почечный кровоток при воздействии волновой энергии [16]. Эти повреждения могут быть связаны с долгосрочными эффектами ДЛТ на функцию почек.
Взаимосвязь ДЛТ с развитием АГ оспаривается рядом авторов, это связано с тем, что многократно была обнаружена взаимосвязь собственно МКБ с АГ. Причем было показано как влияние наличия камней в мочевыводящих путях на повышение уровня системного АД, так и увеличение вероятности развития МКБ у больных с АГ [17]. Тем не менее, наше исследование не преследовало цель доказать связь ДЛТ с развитием АГ или влияние наличия МКБ на появление и усугубление АГ, мы стремились продемонстрировать необходимость тщательного мониторинга и коррекции АД на этапе предоперационной подготовки.
В нашей работе у больных МКБ и сопутствующей АГ после проведения лечения методом контактной литотрипсии данных за усугубление течения АГ в послеоперационном периоде не получено. Это может быть связано с более локальным дезинтегрирующим камни воздействием, использованием методик анестезии, более высокой эффективностью процедуры. Нельзя полностью исключить вклад того, что в нашем исследовании контактной литотрипсии подверглись меньшее количество пациентов (93 больных), чем ДЛТ (543 больных).
По результатам СМАД на десятые сутки после операции у большинства больных I группы уровень АД оказался нормальным (99,7%), в группе II у 42% больных потребовалась дальнейшая коррекция терапии. Данная картина может быть объяснена тем, что в I группе подбор доз и комбинаций антигипертензивных препаратов начался еще на дооперационном этапе, причем больные не допускались до оперативного вмешательства до подбора эффективного лечения, тогда как в группе II титрование дозы препаратов началось лишь после лечения основного урологического заболевания. Вероятнее всего, в последнем случае прошло недостаточно много времени для проявления эффекта гипотензивного лечения и подбора наиболее эффективных схем терапии АГ.
Таблица 4. Характеристика ночной динамики АД у больных I и II групп на вторые и десятые сутки послеоперационного периода
| Группы | СИ, % | 2е сутки |
10е сутки |
Р | |
|---|---|---|---|---|---|
| Группа (N=586) | |||||
| Нормальный СИ, % | Dippers | 10-20 | 505 (86,2%) | 584 (99,7%) | <0,01 |
| Недостаточный СИ, % | Non-dippers | < 10 | 80 (13,3%) | 0 | - |
| Избыточный СИ, % | Over-dippers | > 20 | 3 (0,5%) | 2 (0,3%) | >0,05 |
| Устойчивое повышение, % |
Night-peakers | < 0 | 0 | 0 | - |
| Нормальный СИ, % | Dippers | 10-20 | 9 (18%) | 28 (56%) | <0,05 |
| Недостаточный СИ, % | Non-dippers | < 10 | 34 (68%) | 20 (40%) | <0,05 |
| Избыточный СИ, % | Over-dippers | > 20 | 2 (4%) | 1 (2%) | <0,05 |
| Устойчивое повышение, % |
Night-peakers | < 0 | 5 (10%) | 1 (2%) | <0,001 |
ЗАКЛЮЧЕНИЕ
Таким образом, нами показано, что наиболее важным является подбор эффективной антигипертензивной терапии больным АГ, направляемым на лечение МКБ, в особенности методом ДЛТ. При адекватной коррекции лечения АГ, под контролем показателей СМАД, у больных МКБ, подвергающихся процедуре ДЛТ, значительно реже возникают гипертонические кризы в раннем послеоперационном периоде, менее значимо повышается АД в первые дни после вмешательства, меньшее количество больных нуждается в дальнейшей коррекции гипотензивной терапии.
Резюме:
Цель. Изучить течение АГ у больных МКБ. Выяснить особенности подготовки больных с АГ к оперативному лечению МКБ. Материалы и методы. Для исследования отобрано с сопутствующей АГ 589 мужчин, больных МКБ (группа I). Контрольная группа сформирована включением 50 мужчин (от 37 до 82 лет) с МКБ и АГ, взятых на экстренное хирургическое вмешательство. Группы были сопоставимы по возрасту, ИМТ, анамнезу АГ, наличию сопутствующих заболеваний. Больным I группы проводилось СМАД до оперативного вмешательства, на вторые и десятые сутки после операции. Больным II группы СМАД до оперативного вмешательства не производилось, так как больные были направлены на экстренное хирургическое вмешательство. Результаты. В раннем послеоперационном периоде у 5 больных (0,9%) I группы после ДЛТ развился ГК. Во II группе после ДЛТ ГК развился у 38 больных (76,0%), что оказалось статистически значимо больше, чем в основной группе после адекватной антигипертензивной терапии (р< 0,0001) и составил 88,4% (38 из 43). Процент пациентов с повышенными значениями АД по результатам СМАД на вторые сутки послеоперационного периода оказался статистически значимо выше у больных II группы по сравнению с группой I (р< 0,01). Причем все больные подвергались ДЛТ, доля больных МКБ с повышенным АД после ДЛТ в группе II составила 90,7% (39 из 43 больных), что оказалось статистически значимо выше, чем у больных МКБ после ДЛТ I группы (р<0,05).
Заключение. Наиболее важным является подбор эффективной антигипертензивной терапии больным АГ, направляемым на лечение МКБ, в особенности методом ДЛТ. Достижение целевых цифр АД, под контролем показателей СМАД, у больных МКБ, подвергающихся процедуре ДЛТ, позволяет снизить развитие ГК в раннем послеоперационном периоде и избежать повышения АД в первые дни после вмешательства.
ЛИТЕРАТУРА
1. Anger JT, Saigal CS, Wang M, Yano EM. Urologic disease burden in the United States: veteran users of Department of Veterans Affairs healthcare. // Urol. 2008. Vol. 72, N 1. P. 37-41.
2. Miller DC, Saigal CS, Litwin MS. The demographic burden of urologic diseases in America. // Urol Clin North Am. 2009. Vol. 36, N 1. P. 11-27.
3. Аполихин О.И., Какорина Е.П., Сивков А.В., Бешлиев Д.А., Солнцева Т.В., Комарова В.А. Состояние урологической заболеваемости в Российской Федерации по данным официальной статистики. // Урология. 2008. N 3. С. 3-9.
4. Лопатин М.Ю. Пробы с дозированной физической нагрузкой (велоэргометрия, тредмил-тест). Научно-практические рекомендации. Волгоград: ВОКЦ, 2001. 68 с.
5. LaRosa JH. National Cholesterol Education Program: report of the expert panel on the detection, evaluation, and treatment of high blood cholesterol in adults. // J Occup Med. 1988. Vol. 30, N 10. P. 826-829.
6. Hamano S, Nakatsu H, Suzuki N, . Tomioka S, Tanaka M, Murakami S. Kidney stone disease and risk factors for coronary heart disease International. // Int J Urol. 2005. Vol. 12, N 10. P. 859-863.
7. Cappuccio FP, Strazzullo P, Mancini M. Kidney stones and hypertension: роpulation based study of an independent clinical association. // BMJ. 1990. Vol. 300, N 6734. P. 1234–1236.
8. Cirillo M, Laurenzi M. Elevated blood pressure and positive history of kidney tones: results from a population-based study. // J Hypertens. 1988. Vol. 6, N 4. P. 484 486.
9. Robertson WG, Peacock M, Baker M, Marshall DH, Pearlman B, Speed R, Sergeant V, Smith A. Studies on the prevalence and epidemiology of urinary stone disease in men in Leeds. // Br J Urol. 1983. Vol. 55, N 6. P. 595–598.
10. Soucie JM, Coates RJ, McClellan W, Austin H, Thun M. Relation between geographic variability in kidney stones prevalence and risk factors for stones. //Am J Epidemiol. 1996. Vol. 143, N 5. P. 487– 495.
11. Tibblin G. High blood pressure in men aged 50 – a population study of men born in 1913. // Acta Med Scand Suppl. 1967. Vol. 470. P.1–84.
12. Madore F, Stampfer MJ, Rimm EB, Curhan GC. Nephrolithiasis and risk of hypertension. // Am J Hyperten. 1998. Vol. 11, N 1. P. 46–53.
13. Чазова И.Е., рабочая группа по разработке рекомендаций, комитет экспертов по разработке рекомендаций. Диагностика и лечение артериальной гипертензии: российские рекомендации (четвертый пересмотр). // Системные гипертензии. 2010. N 3. C. 5–26.
14. Lingeman JE, Woods JR, Toth PD. Blood pressure changes following extracorporeal shock wave lithotripsy and other forms of treatment for nephrolithiasis. // JAMA. 1990. Vol. 263, N 13. P. 1789– 1794.
15. Delvecchio F, Auge BK, Munver R, Brown SA, Brizuela R, Zhong P, Preminger GM. Shock wave lithotripsy causes ipsilateral renal injury remote from the focal point: the role of regional vasoconstriction. // J Urol. 2003. Vol. 169, N 4. P.1526–1529.
16. Connors BA, Evan AP, Willis LR, Blomgren PM, Lingeman JE, Fineberg NS. The effect of discharge voltage on renal injury and impairment caused by lithotripsy in the pig. // J Am Soc Nephrol. 2000. Vol.11. P. 310–318.
17. Madore F, Stampfer MJ, Rimm EB, Curhan GC. Nephrolithiasis and risk of hypertension. // Am J Hypertens. 1998. Vol. 11, N 1. P. 46–53.







