Метод экстракорпоральной резекции почки в условиях фармако-холодовой ишемии без пересечения мочеточника с ортотопической реплантацией сосудов при почечно-клеточном раке
 7948
7948 Злокачественные новообразования почки (ЗНП) в 2013 году составили 3,9% от всех зарегистрированных случаев злокачественных новообразований населения РФ, занимая 10 ранговое место в структуре онкологической заболеваемости обоих полов. Абсолютное число больных с впервые в жизни установленным диагнозом ЗНП в РФ в 2013 году составило 11 442 человек. Заболеваемость за 10 лет увеличилась на 41%, с ежегодным приростом 3,35 %. Стандартизированный показатель заболеваемости в 2013 году равнялся 9,39 на 100 000 человек. Смертность за 10 лет увеличилась на 8,39%. В 2013 году количество умерших составило 5 192 случаев [1, 2].
Учитывая многочисленные данные о развитии почечной недостаточности после хирургического лечения, а также возрастающее количество пациентов с ранними стадиями почечно-клеточного рака (ПКР), важность органосохраняющего лечения нельзя недооценивать. Несмотря на отсутствие рандомизированных исследований, сравнивающих эффективность органосохраняющего лечения и радикальной нефрэктомии при ПКР, многочисленные ретроспективные данные указывают на сопоставимую эффективность обоих лечебных подходов при лучших показателях функции почек в случае органосохраняющего лечения. Поэтому органосохраняющее лечение все чаще используется как приоткрытых, так и при малоинвазивных хирургических вмешательствах [3, 4, 5].
Анализируя результаты лечения более 1 миллиона пациентов в США, A.S. Go и соавт. установили, что значительное снижение функции почек ассоциируется с увеличением заболеваемости сердечно-сосудистыми болезнями и смертности от них, а также с повышением частоты госпитализаций по разным причинам. Исторически считалось, что нефрэктомия у пациентов опасности не представляет, поскольку большинство доноров почки на протяжении длительного времени после удаления органа чувствуют себя хорошо. Современные исследователи не разделяют это мнение. Данные, полученные P. Кoenig и соавт., показывают, что у больных ПКР вероятность развития почечной недостаточности больше, чем у здоровых доноров, и что эти две популяции могут существенно отличаться. Кроме того, J. МcKiernan и соавт. продемонстрировали развитие почечной недостаточности у трети больных ПКР еще до лечения. Несмотря на значительные успехи заместительной терапии почечной недостаточности (ЗТПН) с использованием таких методов как диализ или трансплантация, эта терапия становится значимой причиной появления других заболеваний и смертности от них. У пациентов, находящихся на длительном гемодиализе, смертность от сердечно-сосудистых болезней в 10-30 раз выше, чем в общей популяции. При анализе смертности от инфаркта миокарда общая выживаемость пациентов на диализе значительно меньше, чем у пациентов без почечной недостаточности даже при наличии сопутствующих болезней. Согласно базе данных США по заболеваниям почек (USRDS) смертность у больных на диализе составляет 22% в первые два года и 15% во время последующих трех лет. M. Rocco и соавт. сообщили о потребности в госпитализации более 50% больных, находящихся на хроническом диализе, около 20% из них погибли. При этом стоит отметить высокую стоимость диализа: только в США выделяется около 70 000$ в год на одного пациента. Трансплантация почки является жизненно важной для некоторых пациентов, но и она сопряжена с рисками. Согласно современным рекомендациям, трансплантацию почки в случае ПКР можно проводить через два года безрецидивного периода. Это вынуждает пациентов ждать, получая диализ, не менее двух лет. Кроме того, недостаточное количество аллогенных трансплантантов может привести к дальнейшей задержке выполнения трансплантации. И, наконец, даже при очевидных достижениях в трансплантации, от 20 до 33% трансплантатов функционируют не более 5 лет. Согласно результатам некоторых исследований, 5-летняя выживаемость после трансплантации составляет только 75% [6-14].
Основной задачей проведенного исследования является анализ непосредственных и отдаленных результатов экстракорпоральной резекции почки (ЭКРП) с применение фармакохолодовой ишемией без пересечения мочеточника с ортотопической реплантацией почечных сосудов, с целью оценки эффективности и безопасности использования данной методики у больных ПКР.
Цель исследования: разработка метода экстракорпоральной резекции почки (ЭКРП) в условиях фармако-холодовой ишемии без пересечения мочеточника с ортотопической реплантацией почечных сосудов при почечно-клеточном раке.
МАТЕРИАЛЫ И МЕТОДЫ
В урологическом отделении ФГБУ «Институт хирургии им. А.В. Вишневского» Минздрава России разработана методика ЭКРП в условиях фармако-холодовой ишемии у больных ЗНП. В исследование включено 37 больных с морфологически подтвержденным ПКР со стадией pT1aТ3вN0M0-1G1-3 с интрапаренхиматозной и центральной локализацией опухоли при наличии сопутствующей патологии, как в контрлатеральной почке, так и в почке на стороне опухолевого поражения. В это число входят 6 больных с ПКР единственной и единственно функционирующей почки. Все пациенты проходили лечение в урологическом отделении Института хирургии им. А.В. Вишневского в период с 2012 по 2015 гг. Оригинальная методика оперативного пособия заключалась в выполнении ЭКРП с применением фармако-холодовой ишемии раствором Кустодиола без пересечения мочеточника с последующей ортотопической аутотрансплантацией.
Таблица 1. Краткая характеристика больных до операции
| Критерий | Среднее значения±станд откл., частота встречаемости n(%) |
|---|---|
| Возраст, лет | 55,32±13,1 |
| Мужчины, n (%) | 27 (73) |
| Женщины, n (%) | 10 (27) |
| Сторона поражения, n (%) правая левая |
18 (48,6) 19 (51,4) |
| Размеры опухоли, мм 1x 2x 3x |
46,9±15,7 41,4±14 42±15,5 |
| Синхронный ПКР, n (%) синхронный метахронный |
3 (8,1) 2 (66,7) 1 (33,3) |
| Рак единственной почки, n (%) | 6 (16,2) |
| Локализация опухоли, n (%) центральная периферическая |
21 (56,8) 16 (43,2) |
| Категория Т распространенности, n (%) Т1а Т1в Т2 Т3 |
20 (54,1) 12 (32,4) 2 (5,4) 3 (8,1) |
| Категория N распространенности, n (%) N0 |
37 (100) |
| Категория M распространенности, n (%) M0 M1 |
36 (97,3) 1 (2,7) |
| СКФ, мл/мин | 77,78±18,4 |
Средний возраст больных составил 55,32±13,1 года (21-73 года). Мужчин было 27 (73%), женщин – 10 (27%). Соотношение мужчин и женщин – 2,7:1. Поражение правой почки выявлено у 18 (48,6%) больных, левой – у 19 (51,4%). Двусторонние опухоли почек наблюдались у трех (8,1%) больных (66,7% – синхронные, 33,3% – метахронные), единственной и единственно функционирующей почки – у 6 (16,2%) пациентов. У одного (2,7%) пациента имело место сочетание ПКР единственной почки с фактом интралюминальной инвазии (каваренальная форма). Первично-множественный рак имел место у трех (8,1%) больных. Второй локализацией являлись: рак прямой кишки, рак пищевода и рак щитовидной железы.
Размеры опухоли оценивались в в трех измерениях до оперативного пособия и по данным исследования операционного материала патоморфологом. Средние размеры опухоли до операции составили: 46,9±15,7 мм, 41,4±14 мм, 42±15,5 мм. Данные по размерам образований представлены результатами мультиспиральной компьютерной томографии (МСКТ) органов брюшной полости, подтвержденные интраоперационным УЗИ.
Определение стадии заболевания ограничивалось следующим распространением по системе ТNM: рТ1аТ3вN0M0-1G1-3. Стадия рТ1а выявлена у 20 (54,1%) больных, рТ1b – у12 (32,4%), рТ2 – у 2 (5,4%), рТ3 – у 3 (8,1%). По данным морфологического исследования ни у одного больного не были выявлены регионарные метастазы. Один больной с ПКР единственной почки и интралюминальной инвазией (каваренальная форма) имел отдаленные метастазы: мелкие гематогенные легочные местатазы в количестве 8. В таблице 1 представлена краткая характеристика больных до операции.
Опухоль локализовалась в верхнем полюсе у 11 (29,8%) больных, в нижнем – у 10 (27%), в области почечного синуса – у 16 (43,2%), в нескольких сегментах почки – у 15 (40,5%) больных. У всех больных опухоль, так или иначе, затрагивала чашечно-лоханочную систему (ЧЛС). В таблице 2 представлены нефрометрические показатели опухолей почки больных.
Таблица 2. Нефрометрические показатели опухолей почки пациентов, включенных в исследование
| Нефрометрический показатель |
Количество больных |
|
|---|---|---|
| Абс. | % | |
| Размер опухоли < 4 см > 4 см |
8 29 |
21,6 78,4 |
| Локализация опухоли: Верхний сегмент Средний сегмент Нижний сегмент |
11 16 10 |
29,7 43,3 27 |
| Заинтересованность ЧЛС: Деформация Деформация и инвазия |
10 27 |
27,2 72,8 |
| Сумма баллов по шкале RENAL 4-6 7-9 10 и более |
– 6 31 |
– 16,2 83,8 |
Всем пациентам на предоперационном этапе проводилась мультиспиральная компьютерная томография органов брюшной полости с болюсным контрастным усилением с целью адекватной оценки размера опухоли, структуры, локализации и распространенности онкологического процесса, исключения тромбоза почечной и нижней полой вены, вторичного поражения лимфатических узлов и других органов брюшной полости.
Все исследования проводились на мультидетекторных компьютерных томографах (64 и 256 срезов) Philips Brilliance 64 CT и iCT Brilliance (Philips Medical Systems, Cleveland) с применением неионных контрастных веществ (Оптирей 350, Сканлюкс 370). Для запуска сканирования использовали программный пакет «bolus tracking». Изображение оценивали во все фазы исследования в трех стандартных проекциях. В нативную фазу сканирования средний показатель плотности опухоли составил 33,6±10 ед.H. В артериальную фазу плотность составила 110,9±40,7 ед.H, в венозную фазу 84,8±20,2 ед.H и в отсроченную – 62±14,1 ед.H. Цифровые значения денситометрической плотности светлоклеточного ПКР в артериальную фазу исследования были значительно выше (131,9±29,6 ед.H), чем у папиллярного почечно-клеточного рака (59,6±17,2 ед.H).
На основании МСКТ была получена нефрометрическая оценка почечных новообразований по шкале R.E.N.A.L., разработанной сотрудниками Онкологического центра Фокс Чейз при Медицинском университете Темпл (США) в 2009 году. Шкала R.E.N.A.L. подразумевала следующие характеристики: R – радиус (размер опухоли); E – экстраили интраренальный характер роста опухоли; N – близость опухоли к синусу почки или к чашечно-лоханочной системе; A – характеристика переднего (A) или заднего (P) расположения опухоли во фронтальной плоскости; L – расположение опухоли по отношению к полярным линиям.
Подавляющее большинство больных (n=31) относилось к группе с высоким нефрометрическим индексом R.E.N.A.L. (83,8%). Средний балл составил 10,32±0,94. Таким образом, эта группа представляет сложную категорию больных для выполнения резекции почки in situ. Подробная характеристика нефрометрического индекса R.E.N.A.L. представлена в таблице 3.
Всем больным до операции выполняли ультразвуковое исследование на аппаратах Voluson 730Exp и Logiq E9 с применением стандартных методик (В-режим, цветовой, импульсно-волновой допплеграфии и спектрального анализа скоростей потока). В связи со сложной сосудистой анатомией и для уточнения вовлечения сегментарных артерий в опухолевый процесс проводили трехмерную реконструкцию изображений в В-режиме и в режиме энергетического допплера у 15 (40,5%) больных. Всем больным выполняли интраоперационное ультразвуковое исследование (ИОУЗИ) и динамическое наблюдение в послеоперационном периоде. Для получения более достоверных результатов исследование проводили по определенной методике и разработанному нами протоколу.
На дооперационном этапе в задачи УЗИ входило уточнение топографии и характеристик опухоли, описание взаимоотношения с ЧЛС и почечными сосудами, определение исходного внутрипочечного кровотока. У 34 (91,9%) больных при УЗИ почек была выявлена патология, при этом у 17 (45,9%) больных она была представлена солидными образованиями повышенной эхогенности, у 8 (21,6%) – гипоэхогенными и у 9 (24,3%) изоэхогенными образованиями. Структура опухолей в большинстве наблюдений – 33 (89,2%) была неоднородная: за счет наличия анэхогенных жидкостных кистозных включений у 26 (78,7%) больных, гипоэхогенных зон у 5 (15,2%) и у 2 – кальцинатов (6,1%). Во всех наблюдениях в режиме цветного допплеровского картирования (ЦДК) выявляли перинодулярные сосуды, которые были представлены сегментарными и междолевыми артериями. По регистрации интранодулярного кровотока опухоли разделили на аваскулярные – 10 (27%) случаев, гиповаскулярные – 14 (37,8%) и гиперваскулярные образования – 13 (35,2%). У 3 (8,1%) больных были выявлены кистозные опухоли, которые оценивались как тип 4 по шкале Bosniak.
Таблица 3. Характеристика нефрометрического индекса R.E.N.A.L. у больных до операции
| Анатомические характеристики | Медиана | Диапазон |
|---|---|---|
| Сумма нефрометрического индекса | 10,32±0,94 | 4-12 |
| Критерий R | 2,0±0,67 | 1-3 |
| Критерий E | 2,78±0,42 | 1-3 |
| Критерий N | 2,84±0,37 | 1-3 |
| Критерий L | 2,7±0,62 | 1-3 |
В В-режиме и при построении трехмерной реконструкции определяли распространение опухоли на ЧЛС. Распространение опухоли на центральные структуры проявлялось в виде регистрации опухолевых масс в проекции синуса, нарушение типичного внутрипочечного сосудистого рисунка, деформацию контуров ЧЛС. Подозрение на инвазию ЧЛС было описано у 27 (72,8%) больных. Точность в выявлении инвазии в структуры ЧЛС по данным УЗИ в В-режиме составила 87,5%, а в режиме трехмерной реконструкции – 91,7%.
Cпектральный анализ кровотока проводили на уровне междолевых артерий во всех сегментах почки с измерением пиковой систолической скорости, конечной диастолической скорости, индексов резистивности и пульсативности, а также времени акселерации.
В послеоперационном периоде проводили УЗИ на 1, 3 и 7 сутки. В первую очередь оценивали зону резекции, забрюшинное пространство, малый таз на предмет наличия свободной или отграниченной жидкости. В оперированной почке измеряли показатели кровотока во всех сегментах и сравнивали с контрлатеральной почкой (при ее наличии). В первые сутки послеоперационного периода в 14 случаях (37,8%) регистрировалась высокая резистивность в оперированной почке: индекс резистивности (РИ) составил 0,72±0,05. Во всех случаях нормализация гемодинамических показателей наблюдалась к 3-м суткам после операции. В таблице 4 приведены результаты инструментальных методов исследования больных после операции.
При патогистологическом исследовании (ПГИ) у 29 (78,4%) пациентов диагностирован светлоклеточный рак. В 51,7% случаев (n=15) были высокодифференцированные формы ПКР (G1). На долю умеренно и низкодифференцированных форм (G2-3) приходится 48,3% (n=14). Папиллярный ПКР наблюдался у 5 (13,5%) больных, и был представлен во всех случаях умеренно и низкодифференцированными формами ПКР (G2-3). У одного (2,7%) пациента был хромофобный тип рака с эозиноклеточным вариантом. В двух (5,4%) случаях имел место уротелиальный рак G1 и G3. При уротелиальном раке, выявленном на предоперационном этапе по данным КТ и МРТ, опухоль имела вид четко визуализируемых опухолевых узлов. В таблице 5 представлены морфологические типы опухолей у оперированных больных.
Таблица 4. Данные инструментальных методов исследования больных после операции
| Вид обследования | Среднее значения±станд откл., частота встречаемости n(%) |
|---|---|
| Контрастное усиление ткани опухоли на МСКТ, ед.H Нативная фаза Артериальная фаза Венозная фаза Отсроченная фаза |
33,6±10 |
| Спектральные характеристики внутрипочечного кровотока до операции ЛСК, м/с РИ |
0,31±0,09 |
| Спектральные характеристики внутрипочечного кровотока после операции ЛСК, м/с РИ |
0,27±0,09 |
Таблица 5. Гистолические типы опухолей у оперированных больных
| Гистологические типы опухолей | Частота встречаемости n(%) |
| Почечно-клеточный рак: | 35 (94,6) |
| Светлоклеточный тип G1 G2 G3 Папиллярный тип G1 G2 G3 Хромофобный тип, эозиноклеточный вариант |
29 (78,4) 15 (51,8) 11 (37,9) 3 (10,3) 5 (13,5) – 3(60) 2 (40) 1 (2,7) |
| Уротелиальный рак: G1 G2 G3 |
2 (5,4) 1 (50%) – 1 (50) |
Таким образом, подавляющее большинство случаев представлено светлоклеточным ПКР. У двух больных уротелиальный рак был выявлен по результатам ПГИ, как морфологическая находка.
Во всех случаях проводилась регионарная лимфаденэктомия. При выполнении резекции правой почки выполнялась аортокавальная лимфаденэктомия; при резекции левой почки – парааортальная лимфаденэктомия. Количество удаленных лимфоузлов варьировало от 1 до 19. Среднее количество удаленных лимфоузлов составило 5,73±4,13.
В 8 (21,6%) случаях проводилось восстановление целостности резецированных сегментарных артерий. Пересеченные во время резекционного этапа сегментарные артерии под оптическим увеличением восстанавливались путем формирования косого анастомоза «конец в конец» нитью из полипропилена 8/0.
Во всех случаях производилась резекция чашечно-лоханочной системы почки. Интраоперационное антеградное стентирование мочеточника было выполнено в 27 (72,9%) случаях.
В 9 (24,3%) случаях выполнялась ипсилатеральная адреналэктомия, что определялось онкологическими показаниями.
В 12 (32,4%) случаях потребовалось выполнение протезирования почечной артерии протезом из политетрафторэтилена. Причем, частота стороны резекции была одинакова, как слева, так и справа – по 6 случаев соответственно.
В двух случаях была выполнена симультанная операция: резекция инфраренального отдела аорты с протезированием по поводу аневризмы аорты и экстирпация пищевода с одномоментной пластикой по поводу рака пищевода.
У 8 (21,6%) больных была аномалия развития почечных артерий. Количество артерий варьировало от 1-й до 3-х. Среднее значение составило 1,29±0,62. Аномалия почечных вен наблюдалась у 3 (8,1%) больных. Среднее значение составило 1,08±0,28. Температура режим почки ex vivo варьировала от 9,1 до 11,7 0С. Среднее значение температуры почки на протяжении всего экстракорпорального этапа составило 10,58±0,66 0C.
У одного больного с раком единственной правой почки имелся опухолевый тромб, распространяющийся в просвет нижней полой вены (кава-ренальная форма). Опухолевый тромб распространялся на 48 мм антеградно от устья правой почечной вены и имел диаметр до 30 мм. Больному одномоментно была выполнена тромбэктомия с резекцией нижней полой вены и извлечение единственной правой почки из забрюшинного пространства с последующей резекцией почки, тромбэктомией из центральных сосудов почки с ортотопической реплантацией сосудов.
Характеристика интраоперационных данных представлена в таблице 6.
Таблица 6. Характеристика интраоперационных данных
| Критерий | Среднее значения±станд откл., частота встречаемости n (%) |
|---|---|
| Количество удаленных лимфоузлов, n | 5,73±4,13 |
| Многофокусные опухоли,n(%) | 2 (5,4) |
| Среднее количество удаленных опухолевых узлов, n | 3 |
| Стентирование мочеточника, n (%) | 27 (72,9) |
| Размеры опухоли в трех измерениях по данным ПГИ, мм 1x 2x 3x |
43,49±17,28 |
| Резекция и микрососудистая пластика сегментарных артерий, n (%) | 8 (21,6) |
| Адреналэктомия, n (%) | 9 (24,3) |
| Средняя температура холодой нефроплегии, 0С | 10,58±0,66 |
| Протезирование почечной артерии, n (%) | 12 (34,4) |
| Симультанная операция, n (%) | 2 (5,4) |
| Количество почечных артерий, ср. |
1,29±0,62 |
| Количество почечных вен, ср. | 1,08±0,28 |
| Единственная почка, n (%) | 6 (16,2) |
Класс предоперационного риска по классификации ASA оценен как I – II у 29 (78,4%) больных, IIIIV – у 8 (21,6%).
Методика выполнения экстракорпоральной резекции почки в условиях фармакохолодовой ишемии без пересечения мочеточника с ортотопической реплантацией почечных сосудов при почечно-клеточном раке
Доступ осуществляется путем выполнения лапаротомии. Применяется J-образная лапаротомия по общепринятой в клинике методике. Осуществляется доступ в правое (левое) забрюшинное пространство по линии Тольди. Почка мобилизуется вместе с паранефрием в пределах фасции Героты. На рис. 1 представлена МСКТ-грамма резецируемой почки.
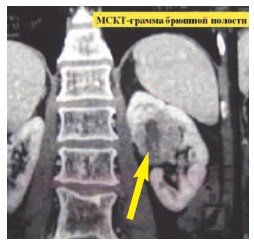
Рис. 1. МСКТ-грамма с опухолью правой почки центральной локализации
Проводится регионарная лимфаденэктомия. Справа удаляется аортокавальный лимфатический коллектор; слева – парааортальная группа лимфоузлов. Проводится мобилизация мочеточника на стороне поражения в верхней и средней трети; для хорошей визуализации, последний берется на провизорный резиновый турникет. Почка освобождается от всей паранефральной клетчатки. Клетчатка направляется на морфологическое исследование. Если опухоль имела экстраренальный тип, то прилежающая к опухоли зона клетчатки маркируется дополнительно. Выполняется тщательная диссекция элементов почечной ножки. Клетчатка с лимфоузлами области ворот почки направляется на морфологическое исследование. Почечные сосуды раздельно берутся на провизорные резиновые турникеты. Диссекция верхней трети мочеточника распространяется до лоханки для оптимальной визуализации всех элементов почечной ножки.
Интраоперационно проводится допплерографическое исследование почки, опухолевого узла с параметрической оценкой кровотока в паренхиме почки и опухоли. В случае с полностью интрапаренхиматознорасположенной опухолью производится определение границ опухолевого узла, лоцируется макимально близкий и малотравматичный нефротомический доступ к опухоли. Регистрируются показатели кровотока по магистральным почечным сосудам, аорте и нижней полой вене.
Мобилизуется аорта в супра, интраи инфраренальном отделе. Выделяется левая (правая) почечная артерия и почечная вена на всем протяжении. При выделении правой почечной артерии мобилизуется нижняя полая вена, берется на провизорный резиновый турникет ниже анатомического устья почечной артерии, формируется канал под нижней полой веной для проведения правой почечной артерии при реимплантация в аорту. Производится системная гепаринизация 5000-7500 МЕд. Почечная артерия на сосудистых зажимах пересекается у устья. Проксимальная культя перевязывается и прошивается. Почечная вена на сосудистых зажимах также пересекается у устья.
В почечную артерию через в/в катетер вводится 500-1000 мл. раствора Кустодиол с целью профилактики ишемии почки и осуществления фармакоплегии. Почка на мобилизованном мочеточнике извлекается из забрюшинного пространства и погружается в лоток с ледяной крошкой изотонического раствора ex vivo. Сразу же налаживается система перфузии почки через просвет пересеченной почечной артерии (артерий) раствором Кустодиол для осуществления классической фармако-холодовой нефроплегии. На рис. 2 представлен этап перфузии почки раствором Кустодиол.
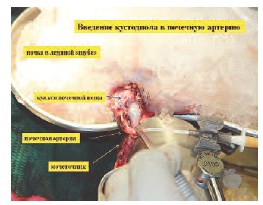
Рис. 2. Этап перфузии почки охлажденным раствором Кустодиол
Физические параметры охлаждения почки.
- температура раствора – 5-8°С; скорость перфузии – 1,5 мл/мин/г оценочной массы почки (в среднем 150 г у взрослого человека);
- давление перфузии, измеряемое в месте ввода канюли в проствет почечной артерии, – 90-110 мм рт. ст. (емкость с раствором расположена на высоте 120-140 см над уровнем почки);
- время перфузии – не менее 8-10 мин (чтобы обеспечить гомогенное распределение раствора во внеклеточном пространстве, включая промежуточную ткань и систему почечных канальцев);
- дополнительные мероприятия: до начала перфузии рекомендуется обеспечить усиленный диурез с помощью мочегонных средств и/или гидратацией; методические указания: необходим контроль времени перфузии и высоты расположения емкости с раствором над уровнем почки либо, если раствор подается с помощью насоса, и контроль времени перфузии и давление на конце почечной канюли.
Охлажденная почка находится в препарате Кустодиол, охлажденном до 2-4°С весь период резекции оперативного пособия. Каждые 30 минут проводится определение температуры почки. При полном соблюдении правил охлаждения почки продолжительность защиты органа от ишемических повреждений достигает 24 – 48 часов.
После интраоперационной эхографии выполняется резекция опухоли острым путем. Опухолевый узел резецируется в пределах здоровых тканей. Отступ от края резекции должен составлять 2-3 мм. На рис. 3 представлена обширная пострезекционная рана почки.
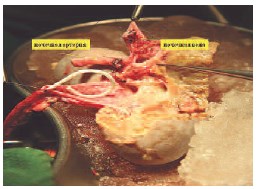
Рис. 3. Почка после удаления опухоли
Если при удалении опухоли было отмечено повреждение интрапаренхиматозных артерий и/или вен (диаметром 1-2 мм), они, по возможности, анастомозируются косым анастомозом «конец в конец» нитью из полипропилена 8/0, или ушиваются наглухо той же нитью. Герметичность швов контролируется дополнительными инсуфляциями Кустодиола в почечную артерию. На рисунках 4-6 представлена пересеченная сегментарная артерия.
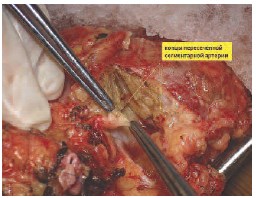
Рис. 4. Проксимальный и дистальный сегмент пересеченной сегментарной артерии
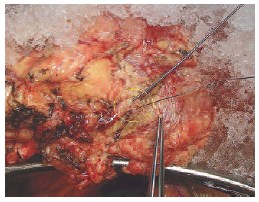
Рис 5. Этап формирования артериального анастомоза «конец в конец» полипропиленовым швом 8/0
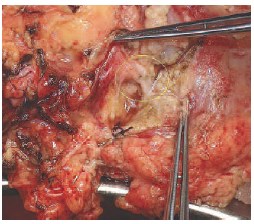
Рис 6. Конечный вид артериального микрососудистого анастомоза «конец в конец»
Макропрепарат отправляется на морфологическое исследование при помощи увеличения проводится тщательная ревизия дна резекции. По показаниям (при обширном нарушении целостности ЧЛС) выполняется антеградное стентирование мочеточника. Используется стент внутреннего дренирования Ch № 6-8. Дефект в ЧЛС ликвидируется непрерывным викриловым швом 4/0. Зияющие сосуды под увеличением тщательно прошиваются Z-образными викриловыми швами 4-5/0. Герметичность швов контролируется дополнительными инсуфляциями Кустодиола в почечную артерию. Целостность паренхимы почки восстанавливается 2-3 этажными одиночными викриловыми швами 12/0. Если герметичность удовлетворительная почка перемещается в забрюшинное пространство.
В почечную артерию вводится дополнительная доза Кустодиола (100-300 мл.) и приступают к реконструкции почечных сосудов и реваскуляризации почки. Почка ортотопически укладывается в забрюшюнное пространство. При реимплантации левой почечной артерии в инфраренальном отделе аорты по левой боковой стенке с помощью аортального «панча» выкраивается окно диаметром 5 мм, в которое имплантируется по типу конец в бок почечная артерия нитью из полипропилена 6-7/0 непрерывным обвивным швом. При реимплантации правой почечной артерии оценивается диастаз между культей почечной артерии и аортой.
На рис. 7 представлен этап реконструкции почечных сосудов.
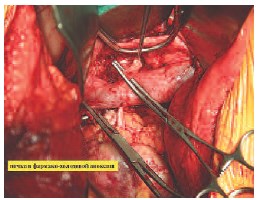
Рис. 7. Краевое отжатие аорты и проведение почечной артерии за нижней полой веной
Определяется необходимость протезирования почечной артерии. Если такой необходимости нет, то почечная артерия проводится в ранее сформированное окно под нижней полой веной к аорте. Далее в инфернальном отделе аорты по правой боковой стенке с помощью аортального «панча» выкраивается окно диаметром 8-10 мм, в которое имплантируется по типу конец в бок почечная артерия нитью из полипропилена 6/0 непрерывным обвивным швом. Затем формируется анастомоз по типу конец в конец между проксимальной и дистальной культей почечной вены нитью из полипропилена 5/0 непрерывным обвивным швом (с применением методики «расширения анастомоза» для профилактики стенозирования анастомоза). При наложении последних швов целесообразно ослабить зажим на сосудах для проверки герметичности сосудистого анастомоза и вымывания раствора Кустодиола из паренхимы почки током крови (v=200-300 мл).
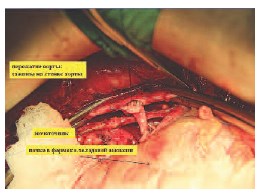
Рис. 8. Этап формирования аорто-артериального анастомоза
На рис. 8 представлен этап формирования аорто-артериального анастомоза.
После окончания реваскуляризации проводится макроскопическая оценка почки и интраоперационный эхографический контроль показателей кровотока на уровне междолевых и дуговых артерий во всех сегментах почки, почечных артериях и вены. Нейтрализация оставшейся дозы гепарина как правило не требуется. На рис. 9 представлен вид операционного поля после пуска кровотока.
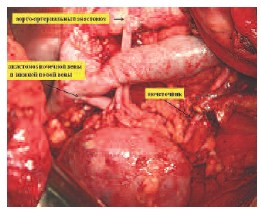
Рис. 9. Операционное поле после пуска кровотока
Иногда при благоприятных топографо-анатомических условиях основная почечная артерия реимлантируется в старое устье (очень редко).
При дефиците длины почечной артерии выполняется протезирование. В качестве протеза во всех случаях использовался протез диаметром 8 мм из политетрафторэтилена производства «Gore-Tex». Первым накладывается анастомоз ex vivo между почечной артерией и протезом, и уже в ортотопической позиции почки между протезом и аортой. На рис. 10 представлен этап протезирования почечной артерии.
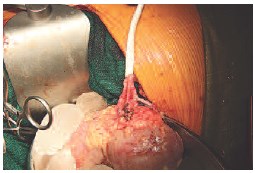
Рис. 10. Протезирование почечной артерии
При наличии дополнительной почечной артерии, которая, как правило, кровоснабжает один из полюсов почки, она в подавляющем большинстве случаев имлантируется в основной ствол по типу конец в бок нитью из полипропилена 7-8/0 ex vivo или нитью из полипропилена 6-7/0 непрерывным обвивным швом. Очень редко дополнительная артерия самостоятельно имплантируется в аорту.
В случае артериального тромбоза почечной артерии проводится артериотомия с эвакуацией сгустков крови, отмывания просвета артерии и дополнительной гепаринизацией. Артериотомный дефект ликвидируется непрерывным швом полипропилена 8/0. Дополнительно проводится эхографическая оценка показателей кровотока по системе почечной артерии.
РЕЗУЛЬТАТЫ
Продолжительность оперативного вмешательства варьировала от 280 до 730 мин. Средняя длительности операции составила 413,97± 89,14 мин. Следует отметить, что продолжительность первых 5 операций была более 500 мин, что связано с освоением методики. Средняя продолжительность последующих 32 операций составила 388,8±58,2 мин, что сопоставимо с литературными данными при ЭКРП с аутотрансплантацией в подвздошную область [15]. Общее время наркоза составило 485,95±98,8 минут. Тепловая ишемия определялась периодом от момента пересечения почечной артерии до момента погружения почки в ледяную крошку с одномоментным началом перфузии охлажденным раствором Кустодиол. Среднее время тепловой ишемии составило 8,39± 4,75 мин. Продолжительность холодовой ишемии варьировала от 70 до 240 мин, в среднем 151,41±41,29 мин. Объем кровопотери равнялся 729,03± 481,4 мл и колебался от 200 мл до 2300 мл. В таблице 7 представлены данные, характеризующие операционный период.
Интраоперационные осложнения выявлены у трех (8,1%) больных. В двух случаях после пуска кровотока почка была признана нежизнеспособной. При нормально функционирующих магистральных сосудов в обоих случаях отсутствовал внутрипочечный кровоток. После безуспешных консервативных мероприятий по восстановлению внутрипочечного кровотока в обоих случаях было выполнено доудаление почки по типу радикальной нефрэктомии.
Таблица 7. Данные продолжительности операции, наркоза, ишемии
| Критерий оперативного пособия |
Среднее значения± станд откл. |
|---|---|
| Продолжительность операции, мин. | 413,97±89,14 |
| Продолжительность наркоза, мин. | 485,95±98,8 |
| Период тепловой ишемии, мин. | 8,39±4,75 |
| Период холодовой ишемии, мин. | 151,41±41,29 |
| Кровопотеря, мл. | 729,03±481,4 |
Еще в одном случае после пуска кровотока произошел тромбоз протезированной почечной артерии. После артериотомии и удаления сгустков вновь отмечен рецидив тромбоза. Однако на этом фоне имелся удовлетворительный внутрипочечный кровоток. Было принято решение не выполнять нефрэктомию. В послеоперационном периоде гладкое течение. Однако через 3 месяца по данным КТ зафиксировано сморщивание почки с отсутствием функции, что было обусловлено артериальным тромбозом протеза.
Для оценки тяжести послеоперационных осложнений использована общепринятая классификация Clavien-Dindo. При возникновении у пациента более одного осложнения, в анализ включалось осложнение, имевшее наиболее высокую степень [16].
Послеоперационные осложнения выявлены у 18 (48,6%) больных. У 15 (40,5%) больных в послеоперационном периоде по данным УЗИ, МСКТ и МРТ определялись гематомы в зоне резекции. В 5 случаях потребовалось пункционное дренирование гематом под УЗИ контролем. Остальные 10 больных велись консервативно с эхографическим контролем. Мы связываем столь частое осложнение с повышенной технической сложностью операций (множественные зоны резекций, их глубина и объем), травмой почки при резекциях в условиях ex vivo, интраоперационной гепаринизацией. Гематомы во всех случаях разрешились благополучно, без открытых повторных вмешательств.
В одном (2,7%) случае проводилось длительное консервативное лечение атаки острого необтурационного пиелонефрита оперированной почки.
Был один (2,7%) случай эвентерации на 6-е сутки после операции.
При резекции единственной почки (2,7%) с одномоментной тромбэктомией и резекцией нижней полой вены в течение трех суток наблюдалась острая почечная недостаточность. Было проведено три сеанса гемодиализа. Следует отметить отсутствие необходимости в гемодиализе в послеоперационном периоде у остальных 5 (13,5%) больных с единственной оперированной почкой. В этих случаях наблюдалось транзиторное повышение уровня азотистых шлаков, не требующее проведения гемодиализа.
У одного (2,7%) больного в первые сутки произошло внутрибрюшное кровотечение из зоны резекции почки. Была выполнена релапаротомия с дополнительным прошиванием шва резецированной почки. У этого же пациента на 8-е сутки отмечена массивная макрогематурия. По данным МСКТ с внутривенным усилением обнаружена артерио-венозно-чашечно-лоханочная фистула, которая была ликвидирована эндоваскулярной установкой окклюдера в сегментарную почечную артерию.
У одного (2,7%) больного послеоперационный период осложнился острым деструктивным панкреатитом.
Один (2,7%) летальный исход был обусловлен мезентериальным тромбозом, произошедшим на 4-е сутки послеоперационного периода с развитием последующей полиорганной недостаточности.
В структуре осложнений I степени все случаи представлены наличием гематомы в зоне резекции, не требующей хирургического вмешательства. Структура осложнений указана в таблице 8.
Таблица 8. Распределение послеоперационых осложнений по группам в соответствии со степенью тяжести по Clavien-Dindo
| Степень тяжести осложнения по Clavien-Dindo | Частота встречаемости |
|
|---|---|---|
| Абс. | % | |
| I степень | 7 | 38,8 |
| II степень | 1 | 5,6 |
| III a степень | 4 | 22,2 |
| III b степень | 4 | 22,2 |
| IV a степень | 1 | 5,6 |
| IV b степень | - | - |
| V степень | 1 | 5,6 |
Не выявлено влияния на частоту послеоперационных кровотечений, гематом стороны поражения, размеров, локализации опухоли, категории Т, длительности холодовой ишемии. Сравнивая с личным опытом резекций почек in situ в урологической клинике Института хирургии, отмечается значительное увеличение этих осложнений при выполнении ex vivo (2,3% и 43% соответственно).
Пол, возраст, сторона поражения, локализация, размеры опухоли и категория Т влияния на риск снижения почечной функции в раннем и позднем послеоперационном периоде не оказывали. Наличие второй функционирующей почки значительно снижало риски транзиторного повышения уровня азотистых шлаков. Частота и вид осложнений зависел от нефрометрических показателей по шкале R.E.N.A.L. Определялась связь с частотой гематом в области резекции и высоким индексом резистентности.
При плановом гистологическом исследовании по краю резекции опухолевые клетки не выявлены ни в одном случае. Сроки наблюдения после операции составили от 3 до 41 месяца (21,4±7,3). Данных за рецидив опухоли и прогрессирование опухолевого процесса не выявлено ни у одного больного. Скорость клубочковой фильтрации (СКФ) до операции составляла 77,78± 18,4 мл/мин, а после 63±26,06 мл/мин. При выписке ни один больной не был переведен в ренопривном состоянии.
ОБСУЖДЕНИЕ
Первая успешная трансплантация почки была выполнена 23 декабря 1954 г. M.E. Murray. В 1990 г. хирург-пионер был награжден Нобелевской премией. Первыми пациентами были однояйцевые близнецы, что позволило избежать иммунологических проблем и обеспечило успех хирургического вмешательства. Выживаемость трансплантата составила 11 мес. В настоящее время 5-летняя выживаемость аллогенного трансплантата в Европе колеблется от 60 до 80%. В 1960-е годы велись активные эксперименты со все возрастающим числом различных ЭКРП, которые, как правило, выполнялись при хронических доброкачественных заболеваниях (хроническая почечная недостаточность) и редко — при ПКР. В 1970 г. наблюдался пик частоты выполнения подобных комплексных оперативных вмешательств, и ПКР стал принятым показанием к такому хирургическому лечению. 1980-е годы характеризовались снижением доли операций ex vivo параллельно с увеличением возможностей гемодиализа. В 1990-е годы сообщалось лишь о нескольких случаях использования экстракорпоральных хирургических вмешательств. Несмотря на это, в течение последних лет отмечается заметное оживление интереса к операциям на почке ex vivo с последующей аутотрансплантацией. Это может быть обусловлено несколькими причинами. Первой и, возможно, наиболее важной из них является резкое сокращение активности доноров почек, а также отсутствие приоритета больных ПКР в центрах трансплантологии. В связи с этим альтернативная стратегия, заключающаяся в нефрэктомии с последующей пересадкой донорской почки, ассоциирована с серьезными сложностями, связанными с необходимостью длительного наблюдения, проведения программного диализа и наличием листа ожидания трансплантации. Во-вторых, программный гемодиализ достоверно снижает качество жизни, приводит к развитию соответствующих осложнений и летальности, а также является дорогостоящей процедурой [17-20].
При критической оценке нашего собственного опыта, представленного 37 наблюдениями, можно заключить, что ЭКРП с последующей аутотрансплантацией по поводу ПКР технически осуществима и оправдана. Следует подчеркнуть необходимость тщательного отбора больных, у которых есть абсолютные показания к органосохраняющему лечению при опухолях, ограниченных почкой, соблюдения мультидисциплинарного подхода и выполнения подобных операций в крупных центрах, где есть соответствующие технические возможности и опыт сложных оперативных вмешательств. При соблюдении этих условий ЭКРП с последующей аутотрансплантацией будет одним из относительно безопасных вариантов лечения этой сложной группы пациентов и будет находить все более широкое применение. В одном случае нами была благополучно выполнена одномоментная резекция единственной почки с тромбэктомией из нижней полой вены при ПКР с интралюминальной инвазией (рено-кавальная форма). По данным морфологического исследования местного статуса операция была радикально выполненной. Хирургическое лечение больных с ПКР в объеме ЭКРП является сложным и высокотехнологичным процессом. Ключевыми в терапии таких больных должны быть использование мультидисциплинарного подхода, а также индивидуализации алгоритмов лечения. Несмотря на актуальность представленной проблемы, анализ литературных данных свидетельствует о дефиците доказательной базы, в особенности рандомизированных исследований посвященных хирургическому лечению этой патологии. Основным критерием успешного лечения является возможность одновременного онкологического излечения и реализации ораносохранного лечения. Это в большей степени касается резекций единственной почки.
ЗАКЛЮЧЕНИЕ
Актуальность органосохранного лечения при ПКР определяется несколькими важными причинами. Первой является незначительное количество больных ПКР в центрах трансплантологии в связи с длительной сопутствующей иммуносупрессией. В связи с этим альтернативная стратегия, заключающаяся в нефрэктомии с последующей пересадкой донорской почки, ассоциирована с серьезными сложностями, связанными с необходимостью длительного наблюдения, проведения программного диализа и наличием листа ожидания трансплантации. Вовторых, программный гемодиализ достоверно снижает качество жизни, приводит к развитию соответствующих осложнений и летальности, а также является дорогостоящей процедурой. При правильно соблюдаемых условиях данной методики ЭКРП становится относительно безопасным вариантом органосохранного лечения этой сложной группы больных. Она позволяет на длительное время отключать почку из магистрального кровотока, использовать максимально допустимое время холодовой ишемии для выполнения полноценной резекции с тщательным восстановлением сосудистых и собирательных структур почки. Несмотря на всю сложность операции, она обладает рядом несомненных достоинств: практически неограниченный запас времени для работы на почке, идеальная визуализация, максимальная защита почечной паренхимы в условиях холодовой консервации, возможность выполнения срочного морфологического исследования границ резекции почки. Данный метод позволяет выполнять радикальные резекции опухолей, значительно превышающих размер 40 мм. В связи с этим при данной операции необходимо выполнение парааортальной лимфаденэктомии, которая выполняется в расширенном варианте за счет мобилизации супраи инфраренального отделов аорты и нижней полой вены до ворот печени. При данном варианте консервации почки возможно безопасно выполнять расширенные резекции почки, вплоть до одномоментной резекции единственной почки с тромбэктомией из нижней полой вены, резекцией нижней полой вены. Разработанный авторами метод позволяет произвести возврат почки на прежнее место с ортотопической реплантаций почечных сосудов, исключает выполнение дополнительного доступа с последующей потерей времени для диссекции и аутотрансплантации почки в подвздошную область, и также отсутствует необходимость пересечения мочеточника с последующим наложением уретеро-уретероанастомоза или уретероцистоанастомоза.
ВЫВОДЫ
1. Разработанный метод экстракорпоральной резекции почки в условиях фармако-холодовой ишемии без пересечения мочеточника с ортотопической реплантацией почечных сосудов является эффективной и безопасной методикой органосохраняющего лечения.
2. Холодовая ишемия почки поддерживается контролируемой фармакоплегией, что позволяет выполнять резекционный этап с реконструкцией внутрипочечных сосудов и собирательной системы почки любой сложности и длительности, с привлечением микрохирургической техники.
3. Данный метод позволяет выполнять резекции почки при внутрипаренхиматозной и центральной локализации опухоли, вовлечении в опухолевый процесс артерий и вен почки, при размерах опухоли более 40 мм.
4. Ортотопическая реплантация сосудов почки позволяет исключить выполнение дополнительного доступа к подвздошной области и сосудам таза, значительно сокращая длительность и уменьшая травматичность операции.
5. Отсутствие необходимости пересечения мочеточника позволяет исключить вмешательства на мочеточнике и мочевом пузыре, что сокращает время операции, уменьшает риски развития послеоперационных осложнений со стороны мочевой системы.
6. Соблюдение всех онкологических принципов при данном оперативном вмешательстве (радикальное удаление опухоли, морфологический контроль по границам резекции почки, как паренхимы, так и собирательной системы почки, выполнение адекватной расширенной парааортальной лимфаденэктомии, удаление паранефральной клетчатки) позволяет добиться хороших ближайших и отдаленных онкологических результатов.
ЛИТЕРАТУРА
1. Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2013 году. М., 2015. С. 9-15.
2. Широкорад В.И., Махсон А.Н., Ядыкова О.А. Состояние онкоурологической помощи в Москве. // Онкоурология. 2013. N 4. С.11-15.
3. Bratslavsky G, Boris RS. Emerging strategies of nephron sparing surgery in patients with localized and recurrent renal cell carcinoma. // Malign Tumours. 2010. N 1. P. 5-14.
4. Gill I. Laparoscopic radical nephrectomy for cancer. // Orol Clin North Am. 2000. Vol. 27, N 4. P. 707-719.
5. Клиническая онкоурология. [Под ред. Б.П. Матвеева]. М.: ООО «Издательский дом «АБВ-пресс». 2011. С.76-77.
6. Go AS, Chertow GM, Fan D, McCulloch C. E, Hsu CY. Chronic kidney disease and the risks of death, cardiovascular events, and hospitalization. // N Engl J Med. 2004. Vol. 351, N 13. P. 1296-1305.
7. Koenig P, Gill IS, Kamoi K, Aron M, Haber G, Singh AB, Weight CJ, Desai MM, Kaouk JH, Goldfarb DA, Poggio E.D. Kidney cancer and the risk for chronic kidney disease: matchedpaired comparison with living donors. // J Urol. 2008. Vol. 179, Issue 4, Suppl. P. 170.
8. McKiernan J, Simmons R, Katz J, Russo P. Natural history of chronic renal insufficiency after partial and radical nephrectomy. // Urology. 2002. Vol. 59, N 6. Р. 816-820.
9. System USRD.: Annual Data Report. National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK), National Institutes of Health (NIH), and US Department of Health and Human Services (DHHS). 2007.// URL: http://www.niddk.nih.gov/health-information/health-topics/kidney-disease...
10. Foley RN, Parfrey PS, Sarnak MJ. Clinical epidemiology of cardiovascular disease in chronic renal disease. // Am J Kidney Dis. 1998. Vol. 32, 5, Suppl.3. Р. 112-119.
11. Rocco M, Frankenfield DL, Hopson SK, McClellan WM. Relationship between clinical performance measures and outcomes among patients receiving long-term hemodialysis. // Ann Intern Med. 2006. Vol. 145, N 7. P. 512-519.
12. Neil N, Guest S, Wong L, Inglese G, Bhattacharyya S K, Gehr T, Walker DR, Golper T.The financial implications for Medicare of greater use of peritoneal dialysis. // Clin ther. 2009. Vol. 31, N 4. P. 880-888.
13. Kasiske BL, Cangro CB, Hariharan S, Hricik DE, Kerman RH, Roth D, Rush DN, Vazquez MA, Weir MR; The evaluation of renal transplantation candidates: clinical practice guidelines. // Am J Transplant. 2001. Vol. 1, Supp.2. p. 3-95
14. Lin SJ, Koford JK, Baird BC, Habib AN, Reznik I, Chelamcharla M, Shihab FS, Goldfarb-Rumyantzev AS. The association between length of post-kidney transplant hospitalization and long-term graft and recipient survival. // Clin Transplant. 2006. Vol. 20, N 3. Р. 245-250.
15. Джеральд Г.Д. Микич. Почечно-клеточный рак: экстракорпоральная резекция почки с последующей аутотрансплантацией при локализованной форме заболевания. // Онкоурология. 2007. N 3. С. 16-20.
16. Clavien P, Sanabria J, Strasberg S. Proposed classification of complication of surgery with examples of utility in cholecystectomy. // Surgery. 1992. Vol. 111, N 5. P. 518 -526.
17. Bellinger MF, Koontz WW. Jr Smith MJ. Renal cell carcinoma: twenty years of experience. // Va Med. 1979. Vol. 106, N 11. Р. 819-824.
18. Montie JE. «Bench surgery» for renal cell carcinoma: a proper niche. // Mayo Clin Proc. 1992. Vol. 67, N 7. Р. 701-702.
19. Petritsch PH, Gruber H, Colombo T, Rauchenwald M, Breinl E, Ratschek M, Vilits P. Indications and results of ex vivo surgery of the kidney. // Wien Klin Wochenschr. 1995. Vol. 107, N 23. P. 731-735.
20. Stormont TJ, Bilhartz DL, Zincke H. Pitfalls of «bench surgery » and autotransplantation for renal cell carcinoma. // Mayo Clin Proc. 1992. Vol. 67, N 7. Р.621-628.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 1.16 Мб |















































































