Номографический метод оценки индекса ионной активности мочи при кальций-оксалатном уролитиазе DOI: Doi 10.29188/2222-8543-2018-9-1-79-83
- Батько А.Б. – д.м.н., доцент, врач-уролог ООО «Ава-Петер» Клиника Скандинавия, e-mail: abb69@mail.ru
- Забоин В.Н.– д.т.н., профессор кафедры теоретической электротехники и электромеханики федерального государственного автономного образовательного учреждения высшего образования «Санкт-Петербургский политехнический университет Петра Великого», e-mail: zaboin@yandex.ru
 4524
4524 Мочекаменная болезнь (МКБ) является распространенным урологическим заболеванием [1]. В Российской Федерации на долю МКБ в структуре урологической заболеваемости приходиться от 28,3 до 38,2% и эта доля продолжает увеличиваться [2]. В 2010 году показатель числа зарегистрированных больных на 100 000 всего населения равнялся 535,7. В период с 2005 по 2012 год, прирост абсолютного числа пациентов с мочекаменной болезнью, составил 15,7% [3]. Уролитиаз имеет выраженную склонность к рецидивированию из-за отсутствия эффективных патогенетических методов лечения. Суммарный показатель рецидива образования мочевого камня находится на уровне 14% на первом году наблюдений, 35% – на пятом году, а к 10 годам достигает 52% [4]. В клиническом течении уролитиаза выделяют самостоятельные нозологические единицы (нефролитиаз, уретеролитиаз и др.), что отражено в МКБ-Х и оправдано с точки зрения лечебной тактики. Cубклинические формы, предшествующие развитию заболевания, расширяют понятие до гиперкальцийурии, гипероксалурии,гипоцитратурии,гипомагнийурии и др., что имеет важное значение для выявления причин камнеобразования, специфического лечения и создания адекватных мер профилактики иметафилактики МКБ [5-7]. Работами, проведенными в последние годы, показана взаимосвязь изменений, характерных для метаболического синдрома (МС) и его составляющих и повышении риска развития уролитиаза [8]. Так, например, результаты исследования NHAS-III, проведенного вСШАс 1988 по 1994 гг. и включавшее в себя 8814 человек, продемонстрировали тесную корреляцию между симптомами МС и повышением случаев уролитиаза примерно в 2 раза [9]. Избыточная масса тела, артериальная гипертензия также независимо коррелируют с высоким риском МКБ, при этом риск развития уролитиаза не снижается при приеме антигипертензивных препаратов [10]. Это, в свою очередь, значительно увеличивает контингент потенциальных «латентных» больных МКБ.
Для оценки степени риска заболевания и эффективности проводимого лечения существует необходимость использования инструментов оценки камнеобразования.
История изучения физико-химических свойств мочи и маркеров риска камнеобразования мочи имеет давнюю историю и число публикаций по данной проблеме постоянно увеличивается, и не только в специализированной литературе (рис. 1,2).
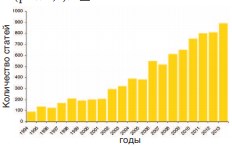
Рис. 1. Количество публикаций, посвященных исследованиям мочи (по данным издательства «Elsevier» за 1994-2013 гг.)
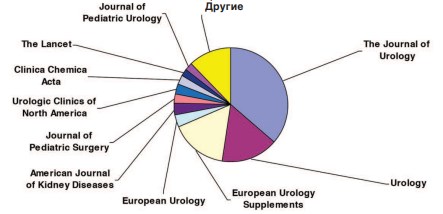
Рис. 2. Основные журналы, в которых опубликованы статьи посвященные исследованиям мочи (по данным издательства «Elsevier» за 1994-2013 гг.)
Исследователями было предложено большое количество диагностических индексов и коэффициентов ионной активности мочи (ИИАМ), отражающих соотношение промоторов и ингибиторов камнеобразования.
Для оценки активности камнеобразования при кальций-оксалатном типе уролитиаза H.G. Tiselius предложен ИИАМ, обозначенный как АP[CaOx] index [11,12]. В 2010 году этот ИИАМ был рекомендован EAU к применению в клинических условиях. При расчёте АP[CaOx] в оригинальной расчетной методике используется следующая формула:
АP[CaOx]=1,9⋅Са 0,84 ⋅Ox1.0 ⋅Cit-0,22 ⋅Mg-0,12 ⋅Vмочи-1,03(1) в которой значения экскреции кальция (Ca), оксалата (Ox), цитратов (Cit) и магния (Mg) представлены в ммоль/сут, а суточный объем мочи Vмочи − в литрах.
Результат ИИАМ следует оценивать следующим образом: при коэффициенте 1,6 и менее – риск камнеобразования низкий, а при и индексе 2,8 и выше риск становится высоким [13].
Предложены и другие типы расчета ИИАМ, которые основаны на моделях классического термодинамического равновесия и применяют в анализе огромное количество (до 23) исходных химических компонентов мочи. Для расчета ИИАМ используют компьютерные программы EQULL и близкую с ней систему Joint Expert Speciation System (JESS) [14,15], которые не нашли широкого распространения из-за очень большого количества исходных переменных, связанных с этим трудозатрат и необходимости использовать вычислительную технику. Поиск различных упрощенных способов расчета ИИАМ привел к появлению ряда специфических показателей: Боннского индекса кристаллизации (BRI) [16,17], относительной перенасыщенности мочи (ОПМ), начальной скорости кристаллообразования (НСК) [18], упрощенного индекса H.G. Tiselius [19,20]. Все эти показатели применяются для прогноза рецидивирования МКБ или коррекции проводимой терапии, однако их клиническая значимость до конца еще не определена [21].
Во всех формулах для оценки ИИАМ используются значения параметров сдвоенных ионных комбинаций для выбранной пары ионов кальция и оксалата (промоутеров камнеобразования) и магния и цитрата (ингибиторов литогенеза). Анализ всех возможных комбинаций промоутеров и ингибиторов камнеобразования показали, что для образования кальций-оксалатного камня достаточно нормального суточного количества экскретируемого кальция, что является наиболее значимым фактором литогенеза [22].
Большое количество методических подходов к оценке степени риска камнеобразования диктует необходимость создания простого способа расчета ИААМ не только для врачей урологов поликлинического звена, но и семейных врачей, врачей общей практики и других специалистов, осуществляющих амбулаторное наблюдение за пациентами группы риска развития или рецидива уролитиаза. С этой целью нами проведен математический анализ параметров ИИАМ при помощи современных компьютерных технологий, определены наиболее значимые из них и предложен простой и наглядный способ расчета риска камнеобразования в виде номограммы.
Цель работы: Выполнить математический анализ переменных составляющих индекс ионной активности мочи при кальций-оксалатном уролитиазе с помощью современных компьютерных технологий, определить значимые параметры и создть простой способ расчета риска камнеобразования в виде номограммы.
МАТЕРИАЛЫ И МЕТОДЫ
Для расчета ИИАМ по методу H.G. Tiselius, как апробированного способа оценки риска камнеобразования, мы использовали компьютерную программу Mathcad V.15, ориентированную на подготовку интерактивных документов с вычислениями и последующим визуальным графическим сопровождением, которое можно переработать в номограмму. Согласно теории построения номограмм произведение двух переменных величин можно определить по Z-номограмме с двумя параллельными равномерными шкалами и одной наклонной неравномерной шкалой, что непосредственно следует из свойств проективной шкалы (шкалы результата произведения), параллельной исходной равномерной шкале. В соответствии с исследуемой формулой (1), в качестве исходной равномерной шкалы с модулем (масштабом) мы приняли значения оксалата, а для равномерной проективной шкалы результата выбрали табличные значения Са0,84 *Ох. Разметку неравномерной наклонной шкалы кальция осуществляли, соединяя две любые точки на параллельных шкалах прямой линией, пересечение которой с этой шкалой отмечали пометкой (штрихом) и обозначали соответствующим значением Са из таблицы.
РЕЗУЛЬТАТЫ
Непосредственное применение формулы H.G. Tiselius (1) в клинической практике встречает затруднение не только из-за математической сложности, но и из-за неоднозначности трактовки получаемых результатов, поскольку предложенная формула, как любая математическая модель (в нашем случае мультипликативная модель степенных функций показателей) справедлива лишь в определенном диапазоне изменений, входящих в нее переменных.
При расширении диапазона изучаемых показателей концентраций электролитов, данное уравнение неизбежно порождает конфликт математического содержания исследуемой модели с физиологической сутью описываемого ею процесса. Несомненно, любой из изучаемых показателей, не может полностью отсутствовать в биологических жидкостях (в моче), однако установленные калибровки приборов могут не выявить минимальное количество изучаемого вещества, что приводит к его нулевому значению. Например, это часто встречается при изучении концентраций цитрата мочи, что и подтверждает выдвинутый нами тезис о математическом конфликте – деление на ноль, так как Cit -0,22 = 1/Cit 0,22 .
На рисунке 3 представлены зависимости Са0,84, Cit -0,22 и Mg -0,12 от их суточной экскреции. Из рассмотрения этих зависимостей следует, что снижение концентрации антилитогенных факторов ниже 1,0 ммоль/сут может увеличивать АP[CaOx] вплоть до бесконечности (левая верхняя часть зависимостей). Важно отметить, что любые увеличения концентрации магния и цитрата в моче больше 1,0 ммоль/сут, особенно в области их референтных значений (от 2,5 до 5,7 ммоль/сут) и выше, не влияют на АP[CaOx], так как значения соответствующих степенных зависимостей Mg -0,12= f(Mg) и Cit -0,22= f (Cit) остаются по сути неизменными, в отличие от кальция, для которого характерна практически прямо пропорциональная зависимость Са 0,84= f (Ca).
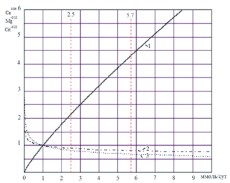
Рис. 3. Зависимости: Са 0,84 (1), Mg-0,12 (2) и Cit-0,22 (3) от их суточной экскреции
В соответствии с заявленной целью нашей работы расчет предложенной сложной функциональной зависимости АP[CaOx] = f (Ca, Ox, Cit, Mg, Vмочи) можно заменить простыми геометрическими построениями (прикладывания линейки) с использованием соответствующих номограмм как это часто делается в практической медицине, в том числе и в урологии [25]. Для создания этих, как правило, Z-номограмм используются таблично заданные значения произведения исходных переменных. Причем, сами таблицы служат не только для проверки точности геометрических построений, но и имеют самостоятельное значение. Поэтому было принято решение сначала преобразовать формулу (1) в удобную для расчета таблиц форму
После несложных замен и вычислений формула (1) приобретает следующий вид:
АP[CaOx]= (2⋅kl⋅kal)/ V, (2) где kl = Са 0,84⋅Ох – произведение литогенных факторов, kal=0.94⋅Cit-0,22⋅ Mg-0,12 – произведение антилитогенных факторов, а V – суточный объем мочи. В широком диапазоне изменения переменных Ca, Ox, Cit и Mg с помощью прикладного математического пакета Mathcad V.15 были рассчитаны матрицы1) (таблицы) значений kl и kal, которые и были использованы для построения номограмм.
На рис. 4 представлена полная номограмма для оценки АP[CaOx] с учетом всех переменных, входящих в формулу (2). Она представляет собой последовательность (слева направо) четырех Zномограмм, важнейшими и определяющими из которых являются, конечно, первая – для расчета kl = Са0,84⋅Ох и вторая – для учета V согласно формуле (2).
В каждой из четырех Z-номограмм исходная шкала и параллельная ей проективная шкала результата умножения принимались равномерными с требуемым модулем (масштабом), а масштаб наклонной неравномерной шкалы зависел от расстояния между ними, как принято в теории построения номограмм [23,24]. В частности, для первой номограммы в качестве исходной была принята равномерная шкала Ох с учетом возможного малого диапазона его изменения, а масштаб равномерной проективной шкалы результата kl = Са0,84⋅Ох был обусловлен его табличными значениями. Расстояние между этими шкалами определяло угол наклона (характер нелинейности) неравномерной шкалы Са, а пометки (штрихи) на ней находили, соединяя прямой две точки на параллельных шкалах согласно матрице значений kl= f (Ca, Ox).
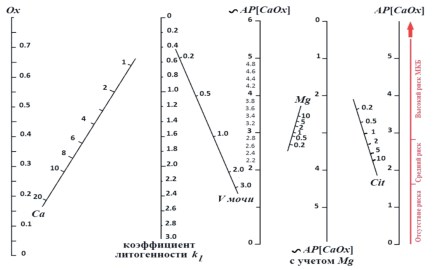
Рис. 4. Полная номограмма для определения АP[CaOx]
Разработанная полная номограмма позволяет уже на стадии амбулаторного приема конкретного пациента, зная лабораторные значения всех рассмотренных выше показателей мочи, без проведения каких-либо вычислений лишь в результате простых геометрических действий оценить риск наличия у него МКБ.
Соответствующий диагностический алгоритм можно проиллюстрировать на конкретном примере:
По данным лабораторных исследований у пациента суточная экскреция (в ммоль/сут): Са = 6,0, Ох =0,55, Mg = 0,5, Cit =2,0 и V =2,0 л. На первом наиболее важном диагностическом этапе, проводя прямую линию через точку 0,55 на шкале Ох и точку на шкале Са = 6 до пересечения со шкалой литогенности kl, получаем пометку (значение kl), равную 2,5, а проводя через нее и точку 2 на шкале V до пересечения с третьей параллельной шкалой 1,88kl/V, находим, как следует из формулы (2), предварительное значение ИИАМ (≈АP[CaOx]) = 2,2.
Это значение на втором диагностическом этапе аналогично уточняется по двум последним номограммам, используя значения Mg и Сit. В конечном итоге получим значение АP[CaOx] = 2,1. Точный расчет по модели H.G. Tiselius (1) дает величину АP[CaOx]index, равную 2,15, что свидетельствует, с одной стороны, о практической значимости предлагаемой номограммы, а с другой стороны, указывает на возможность предварительной оценки АP[CaOx] лишь по первым двум номограммам.
ВЫВОДЫ
1. Переводформулы H.G. Tiselius и его последующая переработка в графическое изображение позволяет в клинической практике упростить оценку риска камнеобразования на амбулаторном приеме, что позволяет индивидуально подходить к лечению конкретного пациента. Разработанную номограмму можно представить на бумажном носителе (в том числе и в упрощенном виде);
2. При значении антилитогенных факторов (магния и цитрата) – экскреция 1,0 ммоль/сут и выше не оказывает значимого влияния на величину АP[CaOx];
3. Быстрая оценка риска развития, прогрессирования или рецидивирования кальций-оксалатного уролитиаза позволяет дать конкретные рекомендации пациенту сразу на амбулаторном приеме (низкая степень риска – отсутствие терапии, средняя степень риска – проведение монотерапии растительными средствами, высокая степень риска – фармакологическая коррекция выявленных нарушений лекарственными препаратами);
4. Оценка ИИАМ может проводится пациентом самостоятельно после получения данных лабораторного обследования и отчетливо показывает зависимость коэффициента литогенности мочи от суточного объема потребляемой жидкости, что повышает комплаентность в лечении.
ЛИТЕРАТУРА
1. Константинова О.В., Шадеркина В.А. Эпидемиологическая оценка мочекаменной болезни в амбулаторной урологической практике. Экспериментальная и клиническая урология 2015;(1):11-14.
2.Аполихин О.И.,СивковА.В., БешлиевД.А.,Солнцева Т.В.,Комарова В.А., Зайцевская Е.В. Анализ урологической заболеваемости в Российской Федерации в 2002-2009 годах по данным официальной статистики. Экспериментальная и клиническая урология 2011;(1):4-10.
3. Аполихин О.И., Сивков А.В., Солнцева Т.В., Комарова В.А. Анализ урологической заболеваемости в Российской Федерации в 2005-2010 годах. Экспериментальная и клиническая урология 2012;(2):4-9.
4. Вощула В.И. Мочекаменная болезнь. Этиотропное и патогенетическое лечение, профилактика. Минск; 2007, 268 с.
5. Колпаков И.С. Консервативное лечение мочекаменной болезни. М: МИА; 2009, 148 с.
6. Батько А.Б., Колмакова Е.В. Оптимизация лечебной тактики у больных с различными формами метаболических нарушений при мочекаменной болезни. Профилактическая и клиническая медицина 2011;40(3):456-457.
7. Назаров Т.Х., Тагиров Н.С., Васильев А.Г., Батько А.Б. Диагностика и коррекция метаболических нарушений при уролитиазе. Фарматека 2014;(4):28-31
8. Гусакова Д.А., Калинченко С.Ю., Камалов А.А., Тишова Ю.А. Факторы риска мочекаменной болезни у больных с метаболическим синдромом. Экспериментальная и клиническая урология 2013;(2):61-64.
9. West B, Luke A, Durazo-Arvizu RA, Cao G, Shoham D, Kramer H. Metabolic syndrome and self-reported history of kidney stones: the National Health and Nutrition Examination Survey (NHANES-III) 1988-1994. Am J Kidney Dis 2008;51(5):741-747. doi: 10.1053/j.ajkd.2007.12.030
10. Батько А.Б. Артериальная гипертензия и мочекаменная болезнь: патогенетические параллели. Terra Medica 2013;(1):44-48.
11. Tiselius HG. Solution chemistry of supersaturation. In: Coe F.L., Favus M.J., Pak C.Y.C., Parks H.G., Preminger G.M. Kidney Stones: Medical and Surgical Management. Philadelphia: Lippincott-Raven, 1996, P. 33-54.
12. Tiselius HG. Risk formulasin calcium oxalate urolithiasis. World J Urol 1997;(15):176–185.
13. Tatati JJ, Tiselius HG, Albala DM, Urolithiasis. Basic Stianse and Clinical Practice. Springer London, 2012.
14. Brown CM, Ackermann DK, Purich DL. EQUIL93: a tool for experimental and clinical urolithiasis. Urol Res 1994;(22):119–126.
15. Werness PG, Brown CM, Smith LH, Finlayson B. EQUIL 2: a basic computer program for the calculation of urinary supersaturation. J Urol 1985;(134):1242–1244.
16. Laube N, Schneider A, Hesse A. A new approach to calculate the risk of calcium oxalate crystallization from unprepared native urine. Urol Res 2000;(28):274–280.
17. Laube N, Hergarten S, Hoppe B, Schmidt M, HesseA. Determination of the calcium oxalate crystallization risk from urine samples: the BONN Risk Index in comparison to other risk formulas. J Urol 2004;(172):355–359. doi:10.1097/01.ju.0000123822.20291.4d
18. Голованов С.А., Сивков А.В., Анохин Н.В., Дрожжева В.В. Подходы к оценке литогенности мочи у пациентов с оксалатным уролитиазом. Экспериментальная и клиническая урология 2015;(2):72-78.
19. Tiselius HG.Aproposed method for approximate estimates of the ion-activity products of calcium oxalate and calcium phosphate in spot-urine samples or in urine samples collected during less well defined periods of time. Urolithiasis 2013;41(2):105-109. doi: 10.1007/s00240-012-0524-9
20. Tiselius HG, Ferraz RR, Heilberg IP. Simplified estimates of ion-activity products of calcium oxalate and calcium phosphate in mouse urine. Urol Res 2012;40(4):285291. doi: 10.1007/s00240-011-0443-1
21. Лисовая Н.А. Лабораторные подходы к выявлению мочекаменной болезни. Terra Medica 2006;1(9):6-11.
22. Жариков А.Ю., Брюханов В.М., Зверев Я.Ф., Лампатов В.В. Современные методы моделирования оксалатного нефролитиаза. Нефрология 2008;12(4):28-35.
23. Глаголев Н.А. Курс номографии. М: Высш. школа 1961:270.
24. Лысенко А.В. Построение номограмм: методические указания. Курск 2016:18.
25. Черняев В.А., Иванова Е.О. Номограммы для урологов: как и для чего они создаются. Урология сегодня 2010;4(8):1-2
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 761.93 кб |















































































