Состояние сексуальной функции у пациентов с нейрогенной гиперактивностью мочевого пузыря до и после лечения ботулиническим токсином типа А
 6039
6039 Нейрогенная дисфункция мочевого пузыря (НДМП) – одна из наиболее частых дисфункций нижних мочевых путей у пациентов с заболеваниями нервной системы различного генеза, клинически проявляющаяся императивными позывами к мочеиспусканию, учащенным мочеиспусканием, недержанием мочи, задержкой мочеиспускания, нарушением сократимости и чувствительности мочевого пузыря.
В ряде случаев при НДМП развивается спазм мышц тазового дна или рефлекторное сокращение сфинктерных зон, приводящих к хронической задержке мочи – функциональная инфравезикальная обструкция (фИВО).
Нарушения мочеиспускания значительно снижают качество жизни больных, так как оказывают существенное влияние на все стороны жизни пациента – социальную, семейную, профессиональную и сексуальную [1]. Сексуальная функция является одной из основополагающих составляющих качества жизни, включающая в себя эмоциональное спокойствие, социальное взаимодействие, самооценку, уверенность. По литературным данным около 70% людей из общей популяции считают крайне важной нормальную и стабильную половую жизнь [2].
Развитие сексуальной дисфункции на фоне гиперактивного мочевого пузыря (ГМП) позволяет предположить, что нормализация мочеиспускания приводит к снижению или устранению выраженности сексуальных расстройств [3].
В настоящее время медикаментозное лечение ГМП получило наибольшее распространение в связи с его доступностью, возможностью длительного применения и достаточно высокой эффективностью. М-холиноблокаторы являются эффективными и доступными препаратами для лечения ГМП [4, 5]. Однако возникновение побочных эффектов, неудовлетворенность результатами лечения и низкая комплаентность пациентов к приему препаратов при большой длительности курсового лечения заставляют искать новые терапевтические подходы к коррекции симптомов нарушенного мочеиспускания [6].
Перспективным методом лечения ГМП является ботулинический токсин типа А (БТА), который эффективен не только при идиопатическом ГМП, но и при нейрогенной гиперактивности детрузора (НГД) [7, 8]. В литературе имеются многочисленные сообщения об успешном применении БТА при ГМП с резистентностью к консервативной терапии. При использовании данного метода лечения отмечается низкий риск побочных реакций, высокая эффективность, выражающаяся в купировании/снижении выраженности императивных симптомов, нормализации уродинамических параметров: снижение детрузорного давления при наполнении, повышение максимальной цистометрической емкости и комплаэнтности мочевого пузыря [9-12]. Необходимо учитывать, что достоверная оценка метода лечения должна основываться как на объективных данных (показателях уродинамики), так и на уровне качества жизни пациентов, неотъемлемой составляющей которого является сексуальное здоровье.
Цель исследования: оценить уровень и динамику сексуальной функции у пациентов, страдающих нейрогенной детрузорной гиперактивностью на фоне лечения БТА.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включено 119 пациентов с нейрогенной дисфункцией мочевого пузыря и НГД, наблюдавшихся в НИИ урологии им. Н.А. Лопаткина в 2012 – 2014 гг. У всех пациентов наличие НГД подтверждено уродинамически. Обследовано 52 мужчины и 67 женщин в возрасте от 18 до 70 лет. В среднем, возраст больных составил 38,0 [25,0; 51,0] лет.
Критерии включения:
- информированное согласие пациентов на участие в исследовании;
- наличие уродинамически подтвержденной НГД с императивными позывами к мочеиспусканию и/или императивным недержанием мочи.
Критерии исключения:
- отказ пациента от обследования;
- острые воспалительные процессы мочевыделительной системы;
- пролапс органов таза 3-4 степени;
- психические расстройства, требующие наблюдения врача-психиатра;
- онкологические заболевания;
- органическая эректильная дисфункция;
- беременность.
Всем пациентам проводили стандартизированное обследование, включавшее: комплексное уродинамическое исследование (КУДИ) в объеме урофлоуметрии (УФМ), цистометрии наполнения/опорожнения, профилометрии уретры; анализ дневников мочеиспускания. В зависимости от пола пациентам выполняли: тестирование с применением опросника «Индекс женской сексуальной функции» (FSFI) или «Шкала количественной оценки мужской копулятивной функции» (МКФ).
На основании общеклинического обследования больные разделены на три группы:
I группа – 29 человек (24,4%): пациенты с НГД без императивного недержания мочи; II группа – 40 человек (33,6%): пациенты с НГД и императивным недержанием мочи; III группа – 50 человек (42,0%): пациенты с НГД на фоне фИВО.
Изменение частоты микций и количества эпизодов недержания мочи оценивали по дневникам регистрации мочеиспусканий. Критерии результатов КУДИ: максимальная цистометрическая емкость в мл (Мaximal Cystometric Capacity – MCC) и максимальная амплитуда сокращений детрузора при наполнении – pdetmax (смН2О), у больных с фИВО учитывали максимальную объемную скорость мочеиспускания – Qmax (мл/сек) и объем остаточной мочи – PVR (мл).
На основании комплексной оценки исследований нами предложена интергативная оценка эффективности терапии: 1 балл – низкая эффективность, 2 балла – средняя и 3 балла – высокая.
Обследование пациентов проводили на 1-м визите – непосредственно перед введением БТА; на 2-м визите – через месяц после введения БТА, на 3-м визите – при возобновлении симптомов ГМП.
Всем пациентам под внутривенной анестезией выполнена уретроцистоскопия, с введением 200 ЕД БТА, разведенных в 20 мл 0,9% физиологического раствора через цистоскоп гибкой иглой в 20 точек мышечного слоя мочевого пузыря, за исключением верхушки и зоны треугольника Льето. В один участок вводили не более 10 ЕД токсина. После инъекции БТА устанавливали уретральный катетер на 4-24 часа.
У больных с НГД на фоне фИВО после введения БТА в детрузор мочевого пузыря, дополнительно вводили 100 ЕД БТА в поперечно-полосатый сфинктер мочевого пузыря.
Статистическую обработку полученных в ходе исследования результатов проводили с помощью программы Statistica for Windows 6.1 (StatSoft Inc.). Качественные признаки были описаны с использованием абсолютных и относительных (%) показателей, количественные – медианы (Ме) и квартиля (Ме [25%; 75%]). Для оценки статистической достоверности различий между группами применены методы: Манна-Уитни; Вилкоксона; Краскела-Уоллиса; хи-квадрат, при необходимости точный критерий Фишера. Уровень достоверности был принят как достаточный при p< 0,05; в случае множественных сравнений использовали поправку Бонферрони.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Сексуальная дисфункция, динамика клинических показателей и уродинамических наблюдений при нейрогенной детрузорной гиперактивности у мужчин.
У пациентов I группы ко второму визиту частота дневных мочеиспусканий снизилась с 18,0 [17,0; 19,0] в начале исследования до 7,5 [5,0; 10,0]. Во II группе частота дневных мочеиспусканий уменьшилась с 26,0 [18,0; 53,0] до 13,0 [9,0; 14,0], ночных мочеиспусканий – с 6,0 [3,0; 12,0] до 0,0 [0,0; 2,0]. В III группе частота дневных мочеиспусканий снизилась с 20,0 [19,0; 27,5] до 12,5 [9,0; 14,5], а ночных мочеиспусканий с 7,0 [5,0; 10,0] до 0,5 [0,0; 4,0]. Во II группе после введения БТА остаточные жалобы на императивное недержание мочи предъявлял только 1 пациент, частота эпизодов ургентного недержания у которого снизилась до 1-2 раз в день.
По данным КУДИ после введения БТА у всех пациентов выявлено повышение максимальной цистометрической емкости и снижение максимального давления детрузора при наполнении. У пациентов III группы также отмечено повышение максимальной скорости мочеиспускания и снижение объема остаточной мочи. Все различия достигли статистически значимого уровня (табл. 1).
Таблица 1. Динамика показателей комплексного уродинамического исследования и урофлоуметрии у мужчин
| Параметры | Группа | 1 визит | 2 визит | р |
|---|---|---|---|---|
| Максимальная цистометрическая емкость (мл) | I | 184,5 [168,0; 201,0] | 358,5 [350,0; 367,0] | 0,015* |
| II | 141,0 [94,0; 148,0] | 216,0 [194,0; 386,0] | 0,008* | |
| III | 192,5 [186,0; 248,0] | 327,5 [287,0; 367,0] | <0,001* | |
| Максимальное давление детрузора при наполнении (см H2O) (pdetmax) | I | 17,0 [11,0; 23,0] | 7,0 [5,0; 8,0] | 0,015* |
| II | 97,0 [28,0; 119,0] | 10,5 [9,0; 12,0] | 0,015* | |
| III | 40,5 [28,0; 70,0] | 18,0 [10,0; 22,0] | 0,043* | |
| Максимальная скорость (мл/сек) | I | 24,0 [20,0; 29,0] | 18,5 [16,0; 21,0] | 0,015* |
| II | 29,0 [17,0; 46,0] | 17,0 [15,0; 19,0] | 0,155 | |
| III | 4,1 [3,0; 6,0] | 11,5 [9,0; 14,1] | 0,002* | |
| Объем остаточной мочи (мл) | I | 6,5 [0,0; 14,0] | 29,0 [0,0; 59,0] | 0,109 |
| II | 17,0 [12,0; 31,0] | 54,0 [41,0; 75,0] | 0,102 | |
| III | 171,0 [100,0; 209,0] | 105,5 [90,0; 125,0] | 0,638 |
Средний интегративный показатель эффективности терапии у больных III группы оказался достоверно ниже, чем в I и II группе: 2,0 [1,0; 2,0]; 3,0 [2,0; 3,0] и 3,0 [2,0; 3,0] балла, соответственно (p1-2=0,735, p1-3=0,01, p2-3=0,024).
Средний показатель копулятивной функции у мужчин по шкале МКФ до начала лечения был выражено снижен относительно средневозрастной нормы. Наиболее низкие показатели по группам можно наблюдать в пунктах: «нейрогуморальная составляющая», «психическая составляющая» и «эрекционная составляющая». В III группе выявлены самые низкие показатели в графе: «эякуляторная составляющая» и «функционирование копулятивной системы в целом».
По параграфу «мнение пациента о его сексуальной потенции в целом» выявлено самое большое значение в I группе (рис. 1).
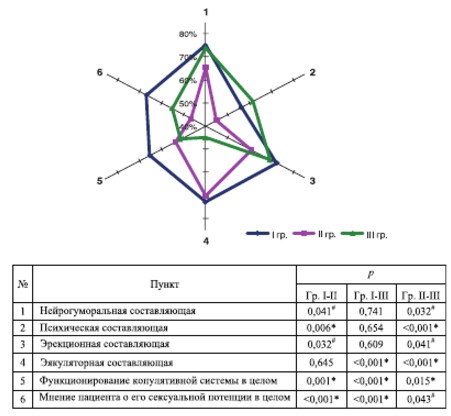
* различия достигли статистически значимого уровня
# различия на уровне статистической тенденции (pкрит=0,017)
Рис. 1. Оценка мужской копулятивной функции по шкале МКФ до введения БТА (относительно средневозрастной нормы)
Через месяц после введения БТА в I и II группах отмечено улучшение мужской копулятивной функции по всем пунктам шкалы МКФ. В III группе заметное улучшение отмечено лишь по пунктам «психическая составляющая», «эякуляторная составляющая» и «мнение пациента о его сексуальной потенции в целом» (рис. 2).
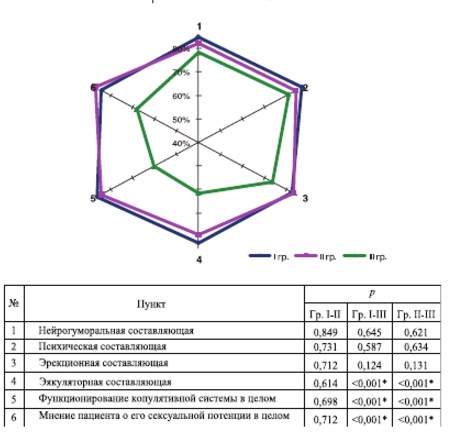
* различия достигли статистически значимого уровня
# различия на уровне статистической тенденции (pкрит=0,017)
Рис. 2. Оценка мужской копулятивной функции по шкале МКФ через месяц после введения БТА (относительно средневозрастной нормы)
При межгрупповом сравнительном анализе можно отметить более выраженную сексуальную дисфункцию у пациентов III группы. Таким образом, наблюдается прямая корреляционная зависимость мужской копулятивной функции и состояния нижних мочевых путей (рис. 3).
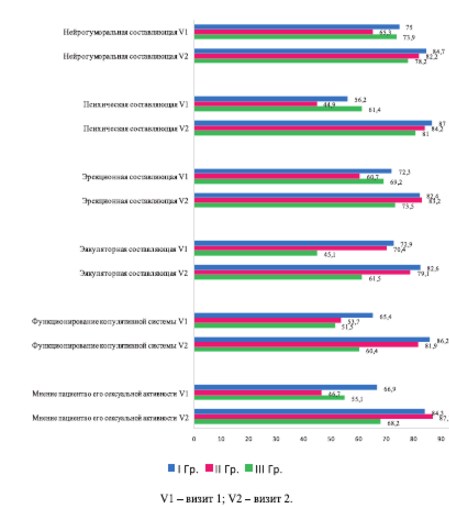
Рис. 3. Динамика показателей шкалы МКФ в %
Сексуальная дисфункция, динамика клинических показателей и уродинамических наблюдений при нейрогенной детрузорной гиперактивности у женщин.
У женщин I группы ко времени второго визита частота дневных мочеиспусканий снизилась с 18,0 [17,0; 20,0] до 6,0 [5,0; 7,0]. Во II группе отмечено снижение частоты дневных мочеиспусканий с 21,0 [17,0; 33,0] до 8,0 [6,0; 12,0], ночных мочеиспусканий – с 8,0 [4,0; 11,0] до 0,0 [0,0; 2,0]. В III группе частота ночных мочеиспусканий уменьшилась с 21,0 [19,0; 25,5] до 9,5 [8,0; 14,5], а ночных мочеиспусканий с 6,5 [4,5; 8,0] до 2,0 [1,0; 3,0]. Во II группе после введения БТА остаточные жалобы на недержание мочи при позыве предъявляли 3 пациентки, но максимальная частота эпизодов недержания у них не превышала 3 раз.
По данным КУДИ через месяц после введения БТА у всех пациенток отмечено повышение максимальной цистометрической емкости и снижение максимального давления детрузора при наполнении. У пациенток III группы выявлено повышение максимальной скорости мочеиспускания, и снижение объема остаточной мочи. Все различия достигли статистически значимого уровня (табл. 2).
Таблица 2. Динамика показателей комплексного уродинамического исследования и урофлоуметрии у женщин
| Параметры | Группа | 1 визит | 2 визит | р |
|---|---|---|---|---|
| Максимальная цистометрическая емкость (мл) | I | 163,0 [139,0; 174,0] | 349,0 [326,0; 351,0] | <0,001* |
| II | 130,0 [121,0; 189,0] | 315,0 [269,0; 351,0] | <0,001* | |
| III | 156,0 [130,5; 223,5] | 326,5 [247,5; 402,5] | <0,001* | |
| Максимальное давление детрузора при наполнении (см H2O) (pdetmax) | I | 21,0 [20,0; 23,0] | 0 | <0,001* |
| II | 55,0 [29,0; 80,0] | 23,0 [14,5; 33,5] | 0,002* | |
| III | 47,0 [18,5; 64,6] | 12,5 [3,5; 25,5] | 0,068 | |
| Максимальная скорость (мл/сек) | I | 22,0 [20,0; 26,0] | 17,0 [16,0; 19,0] | <0,001* |
| II | 29,0 [27,0; 31,0] | 18,0 [17,0; 19,0] | <0,001* | |
| III | 8,2 [5,0; 10,0] | 14,0 [6,5; 19,0] | 0,004* | |
| Объем остаточной мочи (мл) | I | 0,0 [0,0; 0,0] | 44,0 [37,0; 47,0] | <0,001* |
| II | 0,0 [0,0; 0,0] | 41,0 [22,0; 48,0] | <0,001* | |
| III | 147,5 [108,0; 195,0] | 73,0 [50,0; 169,5] | 0,004* |
Средний интегративный показатель эффективности терапии у больных III группы оказался достоверно ниже, чем в I и II группе: 2,0 [1,0; 2,0]; 3,0 [2,0; 3,0] и 3,0 [2,0; 3,0] балла, соответственно (p1-2=0,629, p1-3=0,028, p2-3=0,032).
Анализ результатов индекса женской сексуальности на первом визите выявил снижение сексуальной функции по всем пунктам шкалы и общему баллу, наиболее выраженное у больных II группы (рис. 4).
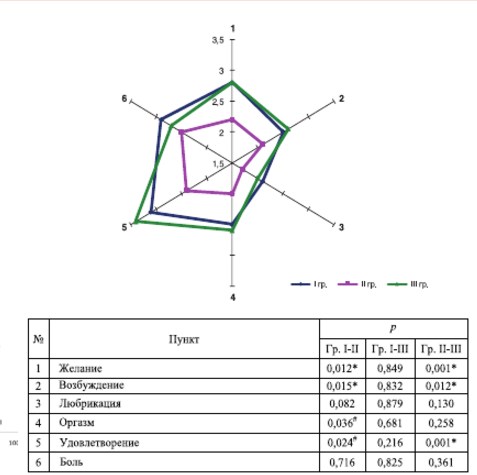
* различия достигли статистически значимого уровня
# различия на уровне статистической тенденции (pкрит=0,017)
Рис. 4. Оценка женской сексуальной функции по шкале FSFI до введения БТА
Через месяц после введения БТА у пациенток всех групп отмечено увеличение общего балла по шкале FSFI: в I группе – с 15,9 [13,6; 16,6] до 18,2 [16,4; 19,8] (p=0,031); во II группе – с 12,9 [11,1; 13,5] до 15,1 [13,4; 16,2] (p=0,028), за счет достоверно значимого увеличения в пунктах «возбуждение» и «оргазм».
Показатели III группы имели общую тенденцию к улучшению, но статистически достоверных различий не выявлено (рис. 5).
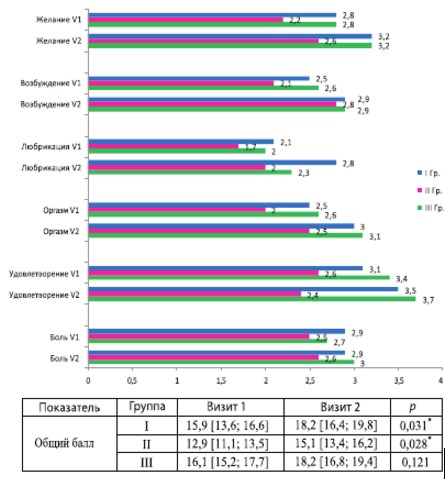
* различия достигли статистически значимого уровня
Рис. 5. Динамика показателей шкалы FSFI
Через месяц после лечения показатели в исследуемых группах имели тенденцию к улучшению, однако, сохранялись межгрупповые различия, выявленные изначально (рис. 6).
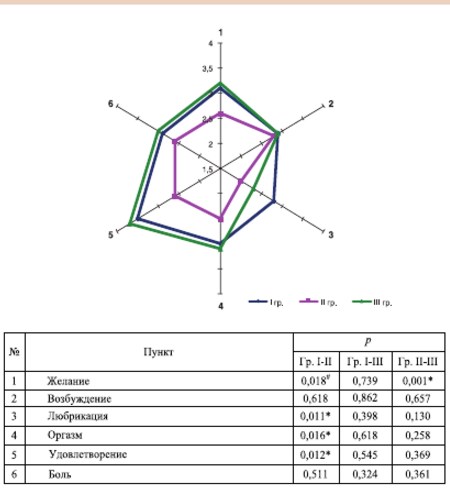
* различия достигли статистически значимого уровня
# различия на уровне статистической тенденции (pкрит=0,017)
Рис. 6. Оценка женской сексуальной функции по шкале FSFI через месяц после введения БТА
Таким образом, нейрогенная дисфункция мочевого пузыря, независимо от тяжести заболевания, сопровождается снижением качества жизни у пациентов обоих полов затрагивающим, в том числе, и сексуальную функцию.
Наиболее выраженные изменения в сексуальной сфере отмечены у пациентов с ГМП при наличии императивного недержания мочи.
В нашем исследовании достоверно подтверждено улучшение всех показателей половой сферы на фоне улучшения уродинамических показателей у мужчин, независимо от тяжести исходного состояния. У женщин, после лечения, также выявлено значительное улучшение уродинамических показателей во всех группах, однако, несмотря на положительные тенденции в показателях сексуальной функции после введения БТА достоверно значимых изменений не выявлено. Следовательно, можно сказать, что качество жизни, в том числе и сексуальной функции, несмотря на улучшение клинической картины НГД у женщин остается на более низком уровне, чем у мужчин.
ЛИТЕРАТУРА
1. Pellat GC. Neurogenic continence. Part 1: Pathophysiology and quality of ilfe. Br J Nurs 2008;17(13):836–841.
2. Арбузова Л.И., Кривонос А.В. Сексуальные расстройства при депрессиях и их терапия. Здоровье мужчины 2014;(1):62-64
3. Кузьмин И.В. Оценка качества жизни у больных с гиперактивностью мочевого пузыря. Нефрология 2006; 10(4):89-92.
4. Goepel M, Kirschner-Hermanns R, WelzBarth A, Steinwachs KC, Rübben H. Urinary incontinence in the elderly. Dtsch Arztebl Int 2010;107(30):531–536.
5. Cerruto MA, Asimakopoulos AD, Artibani W, Del Popolo G, La Martina M, Carone R. et al. Insight into new potential targets for the treatment of overactive bladder and detrusor overactivity. Urol Int 2012;89(1):1-8.
6. Smith CP, Chancellor MB. Emerging role of botulinum toxin in the management of voiding dysfunction. J Urol 2004;171:2128-2137.
7. Grosse J, Kramer G, Stohrer M. Success of repeat detrusor injections of botulinum A toxin in patient with severe neurogenic detrusor overactivity and incontinence. Eur. Urol 2005;47(5):653–659.
8. Smith CP, Somogyi GT, Chancellor MB, Appell RA. A case for botulinum toxin-A in idiopathic bladder overactivit. Curr Urol Rep 2004;5(6):432–436.
9. Мазо Е.Б. Проблемы нейроурологии: настоящее и будущее. Вестник РГМУ 2006; (4):68-74
10. Cruz F, Herschorn S, Aliotta P, Brin M, Thompson C, Lam W, et al. Efficacy and safety of onabotulinumtoxinA in patients with urinary incontinence due to neurogenic detrusor overactivity: a randomised, double-blind, placebo-controlled trial. Eur Urol 2011;60(4):742-750.
11. Rovner E, Dmochowski R, Chapple C, Thompson C, Lam W, Haag-Molkenteller C. OnabotulinumtoxinA improves urodynamic outcomes in patients with neurogenic detrusor overactivity. Neurourol Urodyn 2013;32(8):109–1115.
12. Сивков А.В., Ромих В.В. Фармакотерапия гиперактивного мочевого пузыря. Consilium medicum 2002;(7):348-356
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 1.14 Мб |















































































