Сравнительная морфологическая оценка сперматогенеза крыс после курсового воздействия ингибиторами фосфодиэстеразы 5-го типа
 12590
12590 В настоящее время препаратами первой линии терапии эректильной дисфункции (ЭД) являются ингибиторы фосфодиэстеразы 5-го типа (иФДЭ-5) [1, 2]. Данные лекарственные препараты имеют относительно высокую селективность к ФДЭ-5, но, несмотря на это, все иФДЭ-5 воздействуют также и на другие изоферменты фосфодиэстеразы, расположенные в различных тканях организма человека. Относительно влияния препаратов иФДЭ-5 на фертильность спермы в мировой литературе приведены достаточно противоречивые данные [3-7].
Известно, что именно ФДЭ-11 принимает участие в регуляции процессов сперматогенеза. В ряде исследований проведен анализ роли ФДЭ-11 в сперматогенезе и рассмотрены возможные механизмы ее воздействия. Сперматогенез включает в себя дифференциацию сперматогоний в сперматиды в течение первого и второго мейотического деления. Существуют доказательства того, что этот процесс регулируется по ЦАМФ-зависимому механизму. Во-первых, в сперматогониях была выявлена экспрессия аденилил-циклазы, ее пик приходится на ранний мейоз [8]. Во-вторых, CREM-ген (ЦАМФ-ответственный элемент) это фактор транскрипции, который связывается с ЦАМФ и индуцирует транскрипцию нескольких генов, вовлеченных в сперматогенез. Нокаутированные по CREM-гену мыши бесплодны по причине полного блокирования сперматогенеза [9]. Это может быть предотвращено имплантацией сперматогоний дикого типа, и этот факт свидетельствует о том, что проблема специфична для сперматогоний и не является системной гормональной проблемой [9]. Предположение о том, что ФДЭ-11 контролирует уровни ЦАМФ посредством его разрушения, объясняет важную роль этого изоэнзима в регулировании сперматогенеза [10]. Это доказывают экспериментальные и клинические исследования тадалафила [11, 12], а также опыты на мышах, нокаутированных по ФДЭ-11 [9]. Экспериментальная работа на мышах с моделированным подавлением ФДЭ-11 показала достоверное уменьшение концентрации сперматозоидов, количества активно подвижных и жизнеспособных форм [13]. Также в хроническом эксперименте на животных было продемонстрировано, что ежедневное назначение высоких доз тадалафила (>10 мг/кг/сутки) собакам вызывает атрофию герминогенного эпителия у 20-100% животных с последующей олигоспермией в 40-75% [12]. Этот эффект был необратимым после отмены препарата, что дает основание предполагать повреждение популяции герминогенных стволовых клеток. Является ли этот эффект следствием ингибирования ФДЭ-11 или другим неспецифическим эффектом тадалафила, до сих пор остается неясным. Интересно, что это негативное влияние на сперматогенез не наблюдалось при назначении сходных высоких доз тадалафила мышам [12, 14]. К сожалению, интерпретация всех экспериментальных исследований представляет некоторые трудности, так как существуют различия в видовой принадлежности изучаемого объекта (люди, крысы, мыши, собаки) и специфических изоформах фермента (ФДЭ-11A1, ФДЭ-11A2, ФДЭ11A3 и ФДЭ-11A4).
Несмотря на то, что экспрессия ФДЭ-11 в тканях яичка до сих пор остается дискутабельным вопросом, есть все основания полагать, что именно этот изоэнзим и его подтипы играют важную роль в регуляции сперматогенеза.
Целью нашего исследования была оценка состояния сперматогенеза у крыс с помощью проведения сравнительного морфологического анализа после длительного воздействия иФДЭ5.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Экспериментальная работа проведена на 45 белых беспородных крысах-самцах. Все животные выращены в виварии ФГБУ «НИИ урологии» Минздрава России и получали до начала экспериментальной работы стандартный пищевой/питьевой рацион, в который входил комбикорм и вода в неограниченном количестве. Средний вес животных составил 290-350 гр. Все крысы были в возрасте 8-12 месяцев, что соответствует активному половозрелому состоянию. Животные содержались в клетках объемом 6 литров по 5 крыс в каждой клетке.
Все крысы были разделены на 5 групп. В контрольной группе находились 5 крыс, содержащихся на стандартной диете. В четырех экспериментальных группах было по 10 крыс, которые находились на стандартной диете, но с добавлением в течение 1 месяца раствора соответствующего иФДЭ5 (силденафила, тадалафила, варденафила и уденафила).
Всем 45 крысам в начале эксперимента под эфирным наркозом была произведена срединная лапаротомия с последующей односторонней орхэктомией. Все крысы маркировались так, чтобы при повторной орхэктомии оба яичка, подвергнутые гистологическому исследованию, были от одной и той же особи. Гистологическое исследование яичек осуществляли по стандартной методике с окрашиванием парафиновых срезов гематоксилином и эозином. При морфологическом исследовании микропрепарата индекс сперматогенеза оценивался как соотношение сустентоциты/ клетки сперматогенной ткани.
Через 71 сутки после начала приема лекарственного препарата крысам всех групп была проведена повторная орхэктомия. Именно такой срок был выбран не случайно. Необходимо было получить яичко при повторной орхэктомии, в котором гарантированно завершился хотя бы один цикл сперматогенеза. Известно, что полный цикл развития сперматозоида крысы происходит за 34-35 суток [15]. К 70 суткам заканчивается второй полный цикл развития сперматозоидов.
Таким образом, по истечении почти 2 месяцев после первичной проведенной операции все экспериментальные животные были подвергнуты повторной орхэктомии с последующим гистологическим исследованием тканей яичка.
Расчет дозы препарата, получаемого экспериментальными животными, исходил из того, что крысы принимали иФДЭ5 ежедневно. Это соответствовало курсовому режиму приема лекарственных препаратов у людей. Как следует из инструкций данных лекарственных препаратов, максимальная рекомендуемая кратность применения – 1 раз/сутки для всех иФДЭ5. При этом максимальная суточная дозировка силденафила составляет 100 мг, тадалафила20 мг, варденафила-20 мг, уденафила100 мг.
По нашим расчетам, для того, чтобы на одну крысу (весом в среднем 330 г) приходилась ежедневная эквипатентная людям доза, необходимо разбавить в 5-6 л воды 25 мг силденафила, 5 мг тадалафила, 5 мг варденафила, 25 мг уденафила на 1 неделю. Для того чтобы не происходило возможного распада действующего вещества в воде за неделю, было принято решение разбить дозы и, соответственно, количество воды для разведения на две части. Были использованы максимально допустимые терапевтические дозы препаратов для получения выраженных изменений в ткани яичка, обусловленных воздействием иФДЭ-5 на сперматогенез.
РЕЗУЛЬТАТЫ
При проведении эксперимента во время эфирного наркоза в ходе оперативного вмешательства и в последующем послеоперационном периоде погибло 9 крыс, из которых одна крыса в контрольной группе, две – в группе варденафила, одна в группе силденафила, три в группе тадалафила, две в группе уденафила. Причинами смерти животных явились передозировка эфира во время наркоза и гнойные осложнения после операции.
При гистологическом исследовании в группе силденафила индекс сперматогенеза у каждой крысы до операции составил 3,2. После 2-х месяцев эксперимента этот индекс был таким же (3,2), и морфологическая картина ткани яичек у крыс осталась без изменения после курса приема препарата (рис. 1). В группе тадалафила индекс сперматогенеза у крыс до и после приема препарата составил 3,3. В группе варденафила индекс сперматогенеза снизился с 3,3 до 3,1.
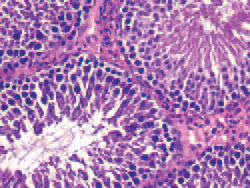
Рис. 1. Нормальная гистологическая картина ткани яичек крыс
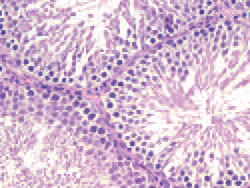
Рис. 2. Гистологическая картина ткани яичек крыс после приема варденафила
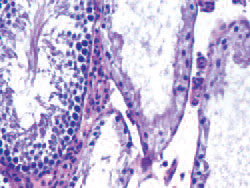
Рис. 3. Гистологическая картина ткани яичек крысы после приема варденафила. Атрофии сперматогенного эпителия
Гистологическая картина ткани яичек после приема варденафила представлена на рис. 2 и 3. В одном из препаратов наблюдалась атрофия сперматогенного эпителия – стенка части канальцев состояла только из клеток Сертоли, клетки сперматоге-неза отсутствовали (рис. 3). В группе уденафила произошло значительное снижение индекса сперматогенеза у крыс с 3,2 до 2,3. При этом отмечена различная гистологическая картина ткани яичек. В одном из препаратов наблюдалась гипотрофия сперматогенного эпителия – уменьшение количества его слоев (рис. 4А), в другом препарате наблюдалась гипотрофия сперматогенного эпителия и дегенеративные формы сперматогенных клеток крупные клетки с полиморфными гиперхромными ядрами, часть клеток с двумя и более ядрами (рис. 4Б). В третьем препарате произошла остановка сперматогенеза на уровне сперматогоний – стенка канальцев состояла только из сперматогоний, другие более зрелые формы сперматогенных клеток отсутствовали.
При гипотрофии ткани яичек присутствуют все формы сперматогенных клеток, но в меньшем количестве, а при атрофии все формы сперматогенных клеток отсутствуют, есть только клетки Сертоли.
У крыс контрольной группы индекс сперматогенеза остался неизменным: был 3,3 до и через 71 день эксперимента. Данные об изменении индекса сперматогенеза у крыс при приеме различных иФДЭ представлены на рис. 5.

Рис. 4. Гистологические картины ткани яичек крыс после приема уденафила
А – отмечается угнетение спертатогенеза
Б – отмечается наличие Дегенеративных форм сперматогенных клеток (отмечено стрелкой) на
фоне гипотрофии сперматогенного эпителия
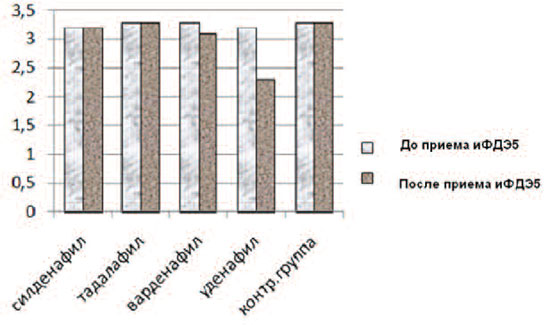
Рис. 5. Индекс сперматогенеза у крыс до и после приема иФДЭ
ОБСУЖДЕНИЯ И ВЫВОДЫ
В данном исследовании изучалось влияние на сперматогенез всех иФДЭ5, реализуемых на территории России. Как показала наша экспериментальная работа, индекс сперматогенеза значимо снизился только у крыс в группе уденафила, там же происходили выраженные дегенеративные изменения форм сперматогенных клеток. И только в данной группе произошла полная остановка сперматогенеза на уровне сперматогоний. Необходимо отметить, что изменения сперматогенеза у крыс в группе уденафила носили не столько угнетающий характер, сколько искажающий («извращенный» сперматогенез). Незначительное снижение индекса сперматогенеза произошло в группе варденафила. Таким образом, можно однозначно утверждать, что иФДЭ5 по-разному воздействуют на сперматогенез крысы: от полного отсутствия какого-либо влияния (силденафил, тадалафил) до выраженных атрофических и дегенеративных изменений (уденафил).
ЗАКЛЮЧЕНИЕ
Несомненно, нельзя ставить знак равенства между сперматогенезом крысы и человека, и, соответственно, полной аналогии воздействия на него различных иФДЭ5 (как и любых других лекарственных средств) добиться невозможно. Однако следует отметить, что именно лабораторные крысы и мыши являются животными, наиболее часто используемыми в качестве экс-периментальной модели для изучения сперматогенеза.
На данный момент однозначного ответа, насколько клинически значимо полученные нами данные коррелируют с фертильностью спермы человека, дать довольно сложно. Только после сравнительного анализа результатов экспериментов, как in vitro, так и in vivo, на животных, а также клинического наблюдения на большой выборке людей может быть составлена комплексная картина, дающая понимание не только влияния того или иного иФДЭ5 на сперматогенез (включая механизм действия), но и дальнейшего совершенствования экспериментальных моделей, используемых для изучения профиля безопасности. Интегральная оценка полученных данных позволит рекомендовать тот или иной иФДЭ5 мужчинам с ЭД, планирующим зачатие ребенка.
ЛИТЕРАТУРА
- Montorsi F, Salonia A, Deho F, Cestari A, Guazzoni G, Rigatti P, Stief C Pharmacological management of erectile dysfunction. // BJU Int. 2003.Vol.91, №5. P. 446-454.
- Ковалев В.А. Диагностика и лечение эректильной дисфункции: Автореф. дис. … д-ра мед.наук. М., 2001. 37 с.
- Ali ST, Rakkah NI. Neurophysiological role of sildenafil citrate (Viagra) on seminal parameters in diabetic males with and without neuropathy. // Pak J Pharm Sci. 2007. Vol.20, №1. P. 36-42.
- Hellstrom WJ, Overstreet JW, Yu A, Saikali K, Shen W, Beasley CM, Watkins VS. Tadalafil has no detrimental effect on human spermatogenesis or reproductive hormones. // J Urol. 2003. Vol.170, №3. P. 887-891.
- Bauer RJ, Rohde G. A single dose of Vardenafil had no acute effect on sperm motility in healthy males. // 27th annual meeting of the American Society of Andrology. 2002 Seattle. Washington, USA. J Andr. Vol. 23, Suppl.1. P. 26
- Boolell M, Allen MJ, Ballard SA, Gepi-Attee S, Muirhead GJ, Naylor AM, Osterloh IH, Gingell C. Int Sildenafil: an orally active type 5 cyclic GMP-specific phosphodiesterase inhibitor for the treatment of penile erectile dysfunction. // J Impot Res. Vol.8, №2. P. 47-52.
- Saenz de Tejada I, Angulo J, Cuevas P, Fernández A, Moncada I, Allona A, Lledó E, Körschen HG, Niewöhner U, Haning H, Pages E, Bischoff E. The phosphodiesterase inhibitory selectivity and the in vitro and in vivo potency of the new PDE5 inhibitor vardenafil. // Int J Impot Res. 2001. Vol.13, №5. P. 282-290.
- Sinclair ML, Wang XY, Mattia M, Conti M, Buck J, Wolgemuth DJ, Levin LR. Specific expression of soluble adenylyl cyclase in male germ cells. // Mol Reprod Dev. 2000. Vol.56, №1. P. 6-11.
- Nantel F, Monaco L, Foulkes NS, Masquilier D, LeMeur M, Henriksen K, Dierich A, Parvinen M, Sassone-Corsi P. Spermiogenesis deficiency and germ-cell apoptosis in CREM-mutant mice. // Nature. 1996. Vol.380, №6570. P. 159-162.
- Baxendale RW, Fraser LR. Mammalian sperm phosphodiesterases and their involvement in receptor-mediated cell signaling important for capacitation. // Mol Reprod Dev. 2005.Vol.71, №4. P. 495-508.
- Pomara G, Morelli G, Canale D, Turchi P, Caglieresi C, Moschini C, Liguori G, Selli C, Macchia E, Martino E, Francesca F. Alterations in sperm motility after acute oral administration of sildenafil or tadalafil in young, infertile men. // Fertil Steril. 2007. Vol.88, №4. P. 860-865.
- Cialis® (Tadalafil) label insert. Australia. 2011
- Wayman C, Philips S, Lunny C, Webb T, Fawcett L, Baxendale RW, Burgess G. Phosphodiesterase 11 (PDE11) regulation of spermatozoa physiology. // Int J Impot Res. 2005.Vol.17, №3. P. 216-223.
- Sausen PJ, Reams RY, Morford LL, Dietsch GN. Tadalafil has no effect on testes in rodents. // Int J Impot Res, 2002. Vol.14, №4. P.82.
- Ковалевский К.Л., Метелкин А.И. Лабораторное животноводство. Практическое руководство по разведению, содержанию и применению лабораторных животных. Изд. АМН СССР, М., 1951. 309 с.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 385.76 кб |















































































