Взаимосвязь компонентов метаболического синдрома и гормональных нарушений в патогенезе заболеваний предстательной железы
 20347
20347 Определение размеров и структуры предстательной железы является одним из кардинальных моментов урологического обследования любого пациента. Как на заре развития урологии, так и до сих пор, в клинической практике это происходит посредством пальцевого ректального исследования данного органа, которое не потеряло своей актуальности и диагностической значимости и в настоящее время прежде всего как метод первичной диагностики (скрининга) заболеваний предстательной железы. После открытия X-лучей в клинической урологии начала-середины XX века были внедрены современные по тем меркам методы рентгенологической диагностики заболеваний простаты. Многие из них, например контрастная простатография, в силу своей инвазивности уже давно имеют исключительно исторический интерес. Причина тому - появление в диагностическом арсенале урологов безопасных и неинвазивных лучевых методов, прежде всего ультразвуковой диагностики, которая в истории урологии совершила вторую по значимости (после рентгенологических методов) диагностическую революцию. Современные методы радиологической диагностики (УЗИ, трансректальное УЗИ, допплерографическая сонография, КТ, МСКТ, МРТ и целый ряд других) позволяют решать практически все тактикостратегические вопросы точной и объективной оценки морфометрических характеристик предстательной железы, что позволило достичь существенного прогресса как в выявлении ранних (доклинических) стадий заболеваний предстательной железы, так и объективной оценке стадии уже имеющейся патологии, это помогает осуществлять объективный мониторинг заболевания и оценивать эффективность его лечения. Таким образом, мы сегодня очень быстро и достаточно объективно можем ответить на вопрос, увеличена ли предстательная железа у пациента или нет. На второй закономерный вопрос, почему предстательная железа увеличена, ответить еще несколько лет назад тоже можно было достаточно быстро и просто: она увеличена вследствие аденомы (рака) предстательной железы. Действительно, в нашем сознании
ее увеличение традиционно ассоциируется в первую очередь с ее опухолевыми заболеваниями (аденомой или раком). Ни для кого не секрет, что предстательная железа является андроген-зависимым органом, а общепризнанная точка зрения трактует ДГПЖ как возраст-ассоциированное прогрессирующее заболевание [1-3]. Однако с возрастом у мужчин увеличивается распространенность не только ДГПЖ, рака предстательной железы или простатита, но и целого ряда возраст-ассоциированных гормонально-метаболических нарушений, таких как ожирение, метаболический синдром (МС), сахарный диабет 2-го типа (СД-2), возрастной андрогенный дефицит, между которыми сегодня установлены достоверные патогенетические связи [4 - 10]. Показана существенная обратная корреляция между уровнем тестостерона и детрузорным давлением, а также детрузорным давлением и максимальной объемной скоростью мочеиспускания Qmax [7]. Уровень сывороточного С-реактивного белка как маркера МС (предиктор артериальной гипертонии) ассоциирован с интрапростатическим воспалением
и, по мнению ряда авторов, может служить предиктором ожидаемого увеличения объема предстательной железы [11 - 13]. Частота выявления симптоматического или бессимптомного увеличения предстательной железы у мужчин старше 50 лет превышает 50 %. Этот показатель увеличивается с возрастом и мало отличается в разных индустриализованных странах [6, 14], как, впрочем, и частота андрогенного дефицита, что является уже, пожалуй, аксиомой медицины [15 - 18]. Эти факты позволяют предположить, что патофизиологические механизмы, лежащие в основе формирования разных типов нарушения гормональнометаболического гомеостаза у мужчин, могут играть существенную роль в процессах индукции роста предстательной железы и прогрессирования нарушений всех ее функций, а коррекция гормональных нарушений может рассматриваться как перспективная патогенетическая терапия ДГПЖ [19].
Подобное заключение приводит к мысли о том, что группа пациентов с выявленными пальпаторными и/или лучевыми методами увеличенной или болезненной предстательной железой, имеющими определенный известный набор клинических симптомов какого-либо ее заболевания (или без них), становится патогенетически неоднородной, а именно: различные системные факторы способны привести к практически одинаковому клиническому и морфометрическому результату - к симптоматическому или бессимптомному увеличению всего объема или определенных зон предстательной железы, изменению ее чувствительности и т. д.
Очевидно, что только междисциплинарное понимание мультифакторного патогенеза увеличения предстательной железы (речь идет не только о ДГПЖ, но и о любом другом ее заболевании, при котором увеличивается ее объем) позволит в будущем разработать патогенетические методы ее профилактики и консервативного лечения многих ее заболеваний. Именно поэтому мы считаем важным познакомить урологов с системными гормональнометаболическими механизмами, ведущими к увеличению предстательной железы, которые изучены относительно недавно.
КЛИНИЧЕСКИЕ АСПЕКТЫ АНАТОМИИ, ЭНДОКРИНОЛОГИИ И НЕЙРОФИЗИОЛОГИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Простата состоит из двух основных структурных компонентов - эпителиального (гландулярного, или железистого) и стромального (фибромускулярного). В норме соотношение этих компонентов выглядит как 1:1 [3]. Короткоживущие эпителиальные клетки непрерывно обновляются за счет деления плюрипотентных базальных, в то время как клетки диффузной нейроэндокринной системы (APUD-системы) образуют псевдослойный (многорядный) эпителий. В противоположность ему строма состоит из долгоживущих гладкомышечных клеток и фибробластов, окружающих секреторный эпителий. В ней находятся основные сосудистонервные структуры простаты [3]. Согласно концепции зонального строения простаты, предложенной в классических работах Gil-Vernet S. (1953) и MсNeal J.E. (1968), в простате различают три зоны: центральную, переходную (транзиторную) и периферическую [20]. Центральная зона простаты по величине составляет около 25 % от общего объема органа и непосредственно прилегает к уретре. Эта зона содержит рецепторы к андрогенам и в большей степени к эстрогенам, за счет изменения баланса которых с течением возраста в ней начинаются процессы железистой и стромальной гиперплазии, ведущие впоследствии к ДГП [3]. Переходная (транзиторная) зона простаты достаточно мала по объему (не более 5 % от общего объема железы), отличается от центральной зоны по своему строению и гормональной регуляции (двойной контроль: андрогены и эстрогены). Небольшой процент раков простаты формируется в этой зоне, однако наиболее актуальной с онкологической точки зрения является периферическая зона простаты (до 70 % объема железы), которая содержит преимущественно андрогеновые рецепторы [3]. В ней развивается большинство карцином [3]. Простата почти не увеличивается в размере у мальчиков до периода полового созревания. После, под действием тестостерона происходит быстрое увеличение железы, а в дальнейшем она удваивается каждые три года и достигает взрослых размеров (около 20 см3) примерно к 20 годам [21]. После этого отмечается ее постоянное, но незначительное увеличение. Факторами риска дальнейшего роста простаты являются возраст и ассоциированный с ним гормональный дисбаланс между половыми гормонами. При этом риск прогрессирования заболевания выше у мужчин в возрасте до 50 лет, с размерами простаты более 40 см3 и уровнем ПСА крови > 1,5 нг/мл [2, 3].
Ткань предстательной железы имеет мощную иннервацию. Адренергические рецепторы (a1A-/B-/D-, и в-1/2) имеют наибольшую плотность в строме, сосудах, мышцах и меньше в эпителии предстательной железы. Преимущественно в эпителии и мышечных элементах железы расположены β-адренорецепторы, плотность которых находится под андрогенным контролем [22]. Железистый эпителий простаты человека - первая описанная ткань (после мозга), где преобладают М-1- холинорецепторы. Столько же их и в семявыносящем протоке кролика [23]. Функция М-холинорецепторов простаты в целом не уточнена (секреция / рост простаты?) [23]. В ткани предстательной железы описаны также нейрокининовые рецепторы к субстанции тахикинина Р к нейрокинину А, а также к нейропептидам (ВИП, нейропептид Y, ген-связанный кальцитонин, соматостатин, энкефалины), роль которых в настоящее время уточняется (нейромодуляция, трофические эффекты, релаксация, синаптическая трансмиссия, регуляция тонуса мышц простаты и т. д.) [24].
Наиболее важным практическим моментом эндокринологии предстательной железы является наличие в ее ткани эндотелиновых рецепторов и рецепторов к оксиду азота (NO), которые экспрессируются геном NO- синтаз - основных ферментов синтеза оксида азота (NO) [25, 26]. Эндотелин-1 (ET-1) - самый мощный вазоконстриктор, продуцируемый эндотелием простаты (он состоит из 21 аминокислоты), который является физиологическим антагонистом оксида азота NO. В настоящее время идентифицировано три гена: ET-1, ET-2, ET-3 [26]. Экспрессия этих генов описана в клетках строме и эпителии предстательной железы и в периферической и центральной ее зонах (транзиторная зона не исследована) [26, 27]. Оксид азота NO, который находится в физиологическом антагонизме с эндотелином-1, продуцируется эндотелием простаты, а также в ее интраорганных нейрональных окончаниях [27]. Оксид азота NO участвует в обеспечении гладкомышечного тонуса простаты и регуляции ее кровообращения, поскольку является мощным вазодилататором [25-27].
Как известно, синтез оксида азота у мужчин является андрогенозависимым процессом, поэтому любой дефицит тестостерона сопровождается системной вазоконстрикцией, в том числе в органах малого таза, приводя к хронической ишемии предстательной железы, склерозированию и нарушению ее структуры и функции [28 - 30]. Очевидно, что именно этот механизм лежит в основе современного патогенетического объяснения феномена простатотестикулярного взаимоотношения, известного в урологии с 1913 года под названием «феномен Белова» [15]. Таким образом, предстательная железа в присутствии достаточного уровня тестостерона обладает физиологическими механизмами регуляции органного кровотока и обеспечения определенного уровня функционального состояния своего нервно-мышечного аппарата, что является важным теоретическим базисом для нового понимания сущности, в частности урологического синдрома хронической тазовой боли и хронического простатита, при стандартной диагностике и лечении которых состояние гормонально-метаболического статуса больного вообще не учитывается. Это, по нашему мнению, является одной из причин неудовлетворительных результатов их терапии, носящей сегодня в большинстве случаев симптоматический характер.
Половые гормоны и предстательная железа
Предстательная железа является ярким примером андроген-зависимого органа, поэтому большинство современных теорий патогенеза простатической гиперплазии прямо или косвенно являются гормональными:
- теория стволовой клетки;
- дигидротестостероновая теория;
- теория андрогенно эстрогенного дисбаланса;
- теория стромально эпителиальных взаимоотношений;
- теория ингибирования клеточного апоптоза (программированной смерти клетки) [2, 3].
Предрасположенность к увеличению предстательной железы может быть связана с генетическими особенностями андрогеновых рецепторов. У мужчин с меньшим числом триплетов CAG в гене андрогенного рецептора вероятность развития аденомы предстательной железы выше, чем у тех, ген которых содержит большее число этих триплетов [31, 32]. Известно, что 5-а-дигидротестостерон (5-а-ДГТ) - основной регулятор роста и индуктор гиперплазии простаты за счет прямой и косвенной модуляции пролиферации, клеточной дифференцировки и апоптоза (железистая гиперплазия), в отличие от действия эстрогенов, стимулирующих стромальную гиперплазию простаты [3, 33, 34]. Как полагают, в большинстве случаев повышение активности 5-α-редуктазы - компенсаторная реакция простаты поддержать нормальный уровень 5-α-ДГТ при снижении в притекающей крови к простате уровня основного субстрата - тестостерона [33]. При нормальном уровне тестостерона в крови в пределах 5 - 10 нг/мл стимуляции роста простаты, очевидно, не происходит [33]. Ввиду того, что активность ферментов зависит от уровня тестостерона (исходного субстрата), который остается низким, образование 5-α-ДГТ и эстрадиола из него оказывается значительно превосходящим норму [33]. Это способствует развитию железистой и стромальной гиперплазии железы [3, 33].
Очевидно, что низкий уровень плазменного тестостерона является для простаты существенным триггером, запускающим механизмы 5-α-редуктазной активности и эпителиальной (меньше стромальной) пролиферации. В связи с избыточным расходованием основного субстрата - тестостерона - по механизму 5-α-редуктазной трансформации уменьшается образование других побочных продуктов метаболизма тестостерона в простате (в частности, образование андростендиола) [34]. Возникающий дефицит андростендиола в предстательной железе сопровождается активацией α-адренорецепторов шейки мочевого пузыря и простатического отдела уретры, так как андростендиол является природным блокатором этого типа α-рецепторов [34]. Это клинически манифестирует различными симптомами нижних мочевых путей (СНМП) даже в отсутствие какого-либо заболевания предстательной железы [34, 35]. При восполнении уровня тестостерона крови (например, при лечении андрогенного дефицита) до нормальных физиологических показателей происходит нормализация активности 5-α-редуктазы и ароматазы предстательной железы [36, 37]. Показано, что при увеличении предстательной железы на фоне ДГПЖ или простатостаза могут наблюдаться различные гормональные диссоциации - как более низкий уровень андрогенов, так и повышение его у эстрогенов у мужчин [38, 39]. Анализируя 260 мужчин старше 60 лет в ходе исследования NHANES III, Rohrmann et al. (2005) отметили, что высокий уровень эстрогенов, высокое соотношение «эстрадиол/ тестостерон» и низкий уровень андростендиола глюкоронида (метаболит 5-α-ДГТ) связаны с большим риском СНМП на фоне увеличения простаты [12]. Экзогенное введение эстрадиола ведет к угнетению 5-α-редуктазной активности и резкому угнетению секреции в эпителии простаты, однако в нем сохраняется синтез андростендиона [38, 39]. Согласно проведенным на данный момент исследованиям, роль эстрогенов в патогенезе гиперплазии простаты двоякая: они выступают как активаторы синтеза 5-α-ДГТ в эпителии (за счет повышения чувствительности к андрогенам), что ведет к железистой гиперплазии, а также являются самостоятельными факторами регуляции клеточной пролиферации / апоптоза, приводящими к стромальной гиперплазии простаты [38, 39].
Предстательная железа является андрогено-зависимым органом, а критическую роль для ее метаболизма играет сывороточный уровень тестостерона, дефицит которого является доказанным патогенетическим фактором развития и прогрессирования эндотелиальной дисфункции (в том числе в тазовых и простатических сосудах), проявляющейся в урогенитальном тракте в виде тазового и / или простатического атеросклероза [40]. В его основе лежит недостаток оксида азота NO, для синтеза которого нужен тестостерон и L-аргинин [40, 41]. Считается, что дефицит оксида азота является предиктором нарушения простатической гемодинамики, гипоксии органа с активацией системы фибробластов, что может приводить к усилению склеротических процессов в паренхиме предстательной железы [28]. Поэтому андрогенный дефицит - плохой прогностический маркер течения заболеваний данного органа, так как его роль в инициации системы 5-α-редуктазы - основного изученного механизма железистой пролиферации, ведущей к прогрессивному увеличению размеров железы, считается доказанной [33 - 39].
Метаболический синдром и предстательная железа
Метаболический синдром (МС) - актуальная междисциплинарная проблема современной медицины, привлекающая все большее число специалистов - не только эндокринологов, терапевтов, кардиологов и врачей общей практики, но также гинекологов, неврологов и урологов. МС - это сочетание абдоминального ожирения, инсулинорезистентности, гипергликемии, дислипидемии, артериальной гипертонии, нарушений системы гемостаза и хронического субклинического воспаления (IDF, 2005) [4]. Эта классификация наиболее широко используется в России. Известный в прошлом как синдром X, «смертельный квартет», и синдром инсулинорезистентности (ИР), MС вообще рассматривается как совокупность находящихся во взаимосвязи факторов риска сердечнососудистых заболеваний, состоящих из ожирения, инсулинорезистентности / гиперинсулинемии, атерогенной дислипидемии, эндотелиальной дисфункции и системного хронического воспаления [4, 16].
В настоящее время МС привлекает все большее внимание урологов в виду выявленных патогенетических связей его компонентов с урологическими заболеваниями. Так, Hammarsten et al. (1998) установили, что мужчины с СД-2, леченной артериальной гипертонией и дислипидемией имели более высокую медиану роста предстательной железы [40]. Авторы отметили, что ежегодная шкала роста аденомы была непосредственно связана с диастолическим артериальным давлением и ожирением и обратно пропорционально связана с уровнем ЛПВП [40]. Мультивариационный анализ показал, что уровень инсулина сыворотки крови непосредственно коррелирует с общим объемом предстательной железы [40]. По данным Ozden et al. (2007), у мужчин с МС общий объем предстательной железы оказался достоверно больше, чем у мужчин без МС [41]. Кроме того, наличие МС у пациента ассоциировалось с достоверно более высокой медианой ежегодного прироста объема переходной зоны предстательной железы [41]. При этом больные с МС имели достоверно более высокий уровень ПСА в сыворотке крови, который авторы предлагают использовать в качестве индекса простатического объема и степени выраженности СНМП [41].
Используя данные из Boston Area Community Health Survey, Kupelian et al. (2009) продемонстрировали, что присутствие MС было достоверно связано с более выраженными СНМП, оцененными по шкале Symptom Index Score, используемой Американским обществом урологов (AUA) [42]. Demir et al. (2009) в обобщенном моновариационном анализе показали, что MС и его компоненты (особенно артериальная гипертония и леченная артериальная гипертония, повышенный уровень сахара крови или медикаментозно компенсированный СД 2-го типа, а также увеличение окружности талии) были ассоциированы с большим объемом предстательной железы [43].
Инсулинорезистентность и предстательная железа
Одним из ведущих механизмов патогенетического единства МС и индуцированного роста предстательной железы является инсулинорезистентность / гиперинсулинемия как ключевой компонент МС [44-46]. Инсулинорезистентность как ключевой патогенетический фактор развития МС есть комплекс компенсаторноприспособительных реакций, развивающихся на фоне ожирения и / или андрогенного дефицита [18]. При снижении уровня андрогенов, в том числе на фоне ожирения, помимо всего, резко снижается, в частности, экспрессия гена рецептора инсулина, что ведет к уменьшению плотности рецепторов на поверхности клеток и возникновению резистентности к инсулину. Как следствие развивается гиперинсулинемия, которая обеспечивает поддержание эффективности углеводного обмена и адекватную митогенную активность в условиях недостатка эндокринного активатора деления клеток (тестостерона) [44, 45]. При этом отмечается нарушение дифференцировки андроген-зависимых клеток, морфологически проявляющееся их атрофией и компенсаторным повышением образования клеточных ростовых факторов. Как известно, инсулин имеет выраженный промитогенный и антиапоптотический эффекты, и его повышенный уровень связан с усилением роста в клетках линии рака простаты [47]. Инсулинорезистентность ведет к увеличению симпатической активности через нарушение метаболизма глюкозы в вентромедиальных гипоталамических нейронах, что приводит к повышенной системной активности α-адренорецепторов (автономной симпатической гиперактивности или нейропатии), в том числе гладких мышц простатической капсулы и шейки мочевого пузыря, а также индукции роста предстательной железы [44, 45]. Эта концепция получила свое подтверждение как у животных, так и у человека [41]. Так, у лабораторной модели крысы повышенная автономная активность вела к стимулированному росту предстательной железы, что заканчивалось формированием аденомы (очевидно, посредством активизации инсулиноподобных факторов роста 1 и 3, обнаруженных в ткани предстательной железы) [40, 41].
McVary et al. (2006) обследовали мужчин на фоне индуцированной повышенной автономной симпатической активности после «tilt-table testing» («тест наклоняемого стола») и показали, что маркеры автономной гиперактивности (повышение артериального давления и частоты сердечных сокращений, а также повышение в сыворотке крови или моче уровня катехоламинов) положительно коррелировали с субъективными маркерами СНМП (суммарным баллом по шкале AUA и качеством жизни) [45].
Дополнительный мультивариационный анализ выявил достоверную положительную корреляцию между плазменным уровнем норэпинефрина (маркер симпатической гиперактивности) и объемом транзиторной зоны предстательной железы [41]. McVary (2005) выдвинул гипотезу, что повышенная автономная активность может воздействовать на α-адренорецепторы, что вызывает сокращения мышц во всех отделах мужского урогенитального тракта, включая шейку мочевого пузыря, предстательную железу и уретру (нейропатия), таким образом способствуя появлению СНМП даже при отсутствии роста предстательной железы [44].
Дефицит оксида азота и предстательная железа. В основе еще одной теории индукции нарушений метаболизма простаты на фоне МС лежит уменьшение экспрессии гена NOS (NO-синтазы) и снижение синтеза NO в простате, что ведет к нарушению мочепузырного и простатического кровообращения [44, 45]. Сообщается о снижении NO-зависимой иннервации предстательной железы на фоне более низких уровней оксида азота (NO) и NOS-активности в ее транзиторной зоне [44]. Это может приводить к усилению пролиферации гладких мышц и увеличению железы в размерах [44]. Кроме того, по распределению типов эндотелиальных NO-синтаз и нейрональных NO-синтаз в предстательной железе можно заключить, что оксид азота NO является важнейшим регулятором региональной простатической гемодинамики [44].
Тазовый атеросклероз и предстательная железа
Нарушения функционирования NO-синтаз и вызванный этим дефицит оксида азота (NO) могут играть важнейшую роль в другом возможном этиологическом механизме простатической пролиферации - развитии тазового и простатического атеросклероза [28].
Многочисленные исследования на животных показали связь атеросклероза и хронической ишемии мочевого пузыря и предстательной железы [28, 48]. У кроликов с лабораторной моделью тазового атеросклероза развивались фиброз мочевого пузыря, гладкомышечная атрофия, уменьшалась эластичность детрузора [48]. Хроническая простатическая ишемия приводила к стромальному и капсулярному фиброзу железы, ее железистой кистозной атрофии [48]. В ишемизированных моделях предстательной железы отмечалось уменьшение расслабления гладких мышц, регулируемых через NO- зависимый механизм подобно аналогичному механизму в кавернозных телах [28, 48].
Система внутриклеточных ферментов - RHO-киназ и предстательная железа. Система RHO-киназ (ROK) может вносить определенный вклад в активацию механизмов простатической пролиферации при МС [49-51]. ROK-киназа вызывает гладкомышечное сокращение за счет изменения чувствительности к кальцию элементов контрактильно го механизма клетки без изменения концентрации кальция в ней [50]. Воздействие на деятельность гладких мышц ROK-киназа, очевидно, оказывает через ингибирование фосфатазы легких миозиновых цепей, что приводит к их фосфорилированию и сокращению в результате взаимодействия актина и миозина [51]. Оксид азота NO противодействует этому, косвенно влияя на активную форму контрактильных белков [51]. Напротив, α-адренергическая деятельность стимулирует путь метаболизма ROK-киназ, обеспечивая связь между ними и автономной гиперактивностью [50].
Таким образом, в данный механизм может быть вовлечен оксид азота NO, дефицит которого является неблагоприятным метаболическим нарушением для функции андроген-зависимых органов мочеполовой системы, включая предстательную железу.
Системное хроническое воспаление и предстательная железа. Системное хроническое воспаление - важный компонент МС, который самостоятельно способен индуцировать СНМП [52, 53]. Инфильтраты из макрофагов и Т-лимфоцитов часто обнаруживаются в ткани предстательной железы, удаленной в ходе открытой или эндоскопической операции на железе [52]. При этом выраженность воспаления непосредственно коррелирует с объемом данного органа [53]. Предполагается наличие нескольких классов провоспалительных цитокинов, приводящих к развитию аутоиммунного воспаления в предстательной железе [53]. Интерлейкины 6-го и 8-го типов вносят наиболее существенный вклад в развитие гиперплазии простаты и воспаления в ней, так как секретируются непосредственно простатической стромой под влиянием цитокинов [54]. Таким образом, эти механизмы могут лежать в основе патогенеза воспалительных заболеваний предстательной железы.
Липотоксичность жировой ткани и предстательная железа. В условиях выраженного ожирения развивается системный эффект жировой ткани, известный под названием «липотоксичность» [55]. Она реализуется как через негативное местное воздействие адипоцитов, расположенных внутри паренхиматозных органов (цитокиновые реакции, нарушение термообмена в органе и т. д.), так и за счет системного негативного влияния свободных радикалов и продуктов перекисного окисления липидов и свободных жирных кислот (мембрано-дестабилизирующие процессы в клетках) [55].
Таким образом, в настоящее время получено достаточное количество достоверных подтверждений тому, что компоненты МС и андрогенный дефицит принимают активное патофизиологическое участие в механизмах заболеваний предстательной железы (Рис. 1.).
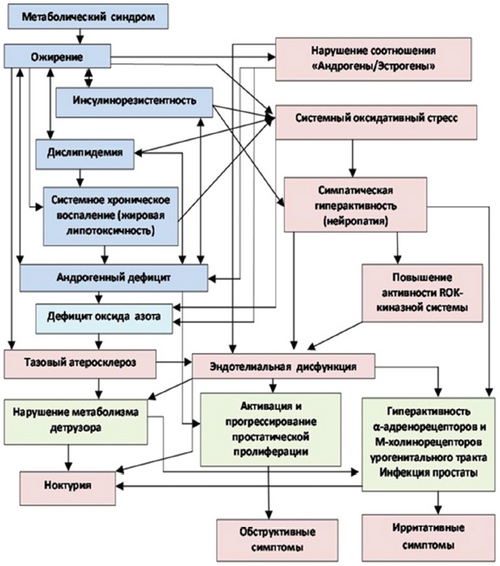
Рисунок 1. Взаимосвязь компонентов метаболического синдрома и андрогенного дефицита в патогенезе заболеваний предстательной железы (обобщенные литературные данные) [33 - 54].
Пролактин, гормон роста и предстательная железа
Менее изученными гормонами, определяющими метаболизм и рост предстательной железы, являются пролактин и близкий к нему гормон роста (соматотропин, или СТГ). В семью рецепторов СТГ/пролактин включают также рецепторы с различными цитокинами (ИЛ-2; ИЛ-3; ИЛ-4; ИЛ-5; ИЛ-6; ИЛ-7; гранулоцитарный колониестимулирующий фактор; гранулоцитарный макрофагальный колониестимулирующий фактор) [56, 57]. Гены, ответственные за синтез рецепторов к пролактину и СТГ, локализуются на 5-й хромосоме (5p13-14) [57, 58]. Экспрессия рецепторов к пролактину и СТГ в органах регулируется через концентрацию соответствующих гормонов: если низкие концентрации в крови СТГ вызывают повышение количества рецепторов на периферии как к СТГ, так и к пролактину, то пролактин стимулирует увеличение только своих собственных рецепторов в органах и тканях [58]. И, наоборот, высокие концентрации этих гормонов вызывают снижение количества рецепторов через уменьшение экспрессии соответствующего гена [58].
Пролактин обладает богатым спектром физиологических эффектов у мужчин, многие из которых недостаточно ясны [58, 59]. Однако в настоящее время доказана роль гиперпролактинемии в патогенезе ожирения и инсулинорезистентности у мужчин, что делает это состояние и МС во многом патогенетически однотипными заболеваниями и применительно к теме обзора - весьма актуальными [59]. У обоих полов пролактин является важным гормоном репродукции, а у 10 - 15 % бесплодных мужчин при гормональном обследовании выявляется гиперпролактинемия [59]. Кроме того, пролактин активно участвует в механизмах простатической трансформации тестостерона в 5-α-ДГТ [15, 59]. За счет нарушения обмена андрогенов при гиперпролактинемии может развиваться гиперпролактинемический гипогонадизм, который является не редкой, но плохо выявляемой урологами причиной снижения либидо у пациентов [15, 59].
За счет нарушения внутрипростатического метаболизма андрогенов при гиперпролактинемии могут формироваться условия для развития относительной гиперэстрогенемии - еще одного механизма снижения полового влечения у мужчин с любыми заболеваниями предстательной железы [15, 59]. Есть данные, что при хронических заболеваниях предстательной железы, протекающих с необратимой потерей массы функционирующей паренхимы органа (длительные простатиты с исходом в кальциноз, склероз или фиброцирроз предстательной железы) и, как следствие, нарушением внутриорганного метаболизма тестостерона, возникающая гиперэстрогенемия, в свою очередь, может индуцировать гиперпролактинемию [15]. Таким образом, клиническая практика показывает, что между пролактином и предстательной железой имеются двойственные связи, однако точные механизмы такого взаимовлияния пока не установлены. Согласно одной из теорий, пролактин регулирует рост простаты через эффекты СТГ посредством его фактора роста - инсулиноподобного фактора роста-1 (ИФР-1) [59, 60]. Экспрессия рецепторов к пролактину выявлена как в здоровой, так и в опухолевой тканях предстательной железы [60]. Уровень экспрессии повышен при дисплазии эпителия, поэтому предполагается участие пролактина в ранних пренеопластических стадиях, хотя нет доказательств тому, что при раке простаты наблюдается гиперэкспрессия рецепторов к пролактину [60]. В целом же влияние пролактина и гормона роста на предстательную железу требует дальнейших исследований.
ЗАКЛЮЧЕНИЕ
Проведенный анализ литературных данных последних лет заставляет задуматься над диагностическим и прогностическим значением выявления у пациента увеличенной предстательной железы. С одной стороны, урологу понятно, что увеличение предстательной железы является морфометрическим признаком ее заболевания, в частности ДГПЖ, застойного (конгестивного) простатита, простатостаза или рака железы. Выставленный урологический диагноз на основании имеющихся рекомендаций по уточняющей диагностике позволяет проводить соответствующее лечение, направленное на ликвидацию клинических симптомов заболевания предстательной железы и улучшение качества жизни пациента. Но, с другой стороны, увеличение предстательной железы - это маркер гормональнометаболического нездоровья пациента. Мы уверены, что это так, потому что в клинической практике нередко выявляется бессимптомное увеличение предстательной железы у мужчин среднего возраста, подходящее под критерии ДГПЖ, однако все мы испытывали определенное смущение при постановке клинического диагноза аденомы предстательной железы, например, мужчине в возрасте 35 лет. Ведь имеющиеся эпидемиологические данные свидетельствуют, что ДГПЖ - заболевание мужчин старших возрастных групп. Учитывая, что механизм формирования аденомы является многофакторным, можно предположить, что действительно это заболевание, первые симптомы которого проявляются у мужчин 40 - 50 лет, но до этого простатическая пролиферация проходит длительный путь бессимптомного (оккультного) течения, который может начаться и в 25, и в 30 лет. Как поступать с этими пациентами? Лечить их или нет? В подавляющем большинстве случаев мы их не лечим, так как при суммарном балле по шкале IPSS-QL 0-7, согласно всем руководствам, мы можем ограничиться динамическим наблюдением за пациентом с увеличенной предстательной железой [2, 3]. Есть ли в наших стандартах диагностики заболеваний предстательной железы лабораторные методы оценки гормонально-метаболического статуса пациентов? Нет. Поэтому, отказывая себе и пациенту в поиске возможных системных гормональнометаболических факторов индукции и прогрессирования роста простаты, коррекция которых, как показывает проведенный литературный обзор, способна затормозить эти процессы, влияя на них патогенетически, мы попрежнему так и останемся в рамках симптоматической терапии как ДГПЖ (кроме ингибиторов 5-α-редуктазы), так и СХТБ/ХП, для которого сегодня урология практически не имеет методов патогенетического лечения, кроме антибиотиков при доказанной инфекции в простате [1, 2].
Совершенно очевидно, что дальнейшее изучение системных и, самое главное, корректируемых факторов риска заболеваний предстательной железы позволит наконец посмотреть на них как серьезную междисциплинарную проблему мужского здоровья, начинать решать которую надо уже у мужчины в возрасте 30 лет - во время возможного начала андрогенного дефицита в популяции современных мужчин, маркерами которого являются возникновение и прогрессирование ожирения, доклинические симптомы нарушений углеводного обмена (инсулинорезистентность), урогенитальная нейропатия, ведущие к нарушению половой функции или ранним нарушениям мочеиспускания (прежде всего ноктурии) при отсутствии органических урологических причин, и случайно выявленное и пока бессимптомное увеличение предстательной железы. Наблюдать таких больных или лечить? Если лечить, то когда начинать и чем лечить? Очень хочется надеяться, что в скором будущем мы получим исчерпывающие ответы на эти и еще массу других вопросов, на которые пока в рамках традиционной монотеории урологии ответить трудно.
Ключевые слова: метаболический синдром, ожирение, инсулинорезистентность, андрогенный дефицит, пролактин, предстательная железа, заболевания предстательной железы, патогенетические связи.
Keywords: metabolic syndrome, obesity, insulin resistance, androgen deficiency, prolactin, prostate, prostate diseases, pathogenetic relations.
ЛИТЕРАТУРА
- Урология. Клинические рекомендации. / Под ред. Лопаткина Н.А. - М.: «ГЭОТАР- Медиа», 2007. 368 с.
- Урология. Национальное руководство. / Под ред. Лопаткина Н.А. - М.: «ГЭОТАР-Медиа», 2009. 1024 с.
- Oelke M., Bachmann A., Descazeaud A. et al. Guideline on the Management of Male Urinary Tract Symptoms (LUTS), incl. Benign Prostatic Obsruction (BPO). European Association of Urology, 2012. 74 р.
- Alberti G. Introduction to the metabolic syndrome. // Eur. Heart J., 2005. N 7. Suppl D. Р. 3 - 5.
- Kalinchenko S.Y., Tishova Y.A., Mskhalaya G.J., Gooren L.J., Giltay E.J., Saad F. Effects of testosterone supplementation on markers of the metabolic syndrome and inflammation in hypogonadal men with the metabolic syndrome: the double-blinded placebo-controlled Moscow study. // Clin. Endocrinol., 2010. Vol. 73, N 5. Р. 602 - 612.
- Karazindiyanoglu S., Cayan S. The effect of testosterone therapy on lower urinary tract symptoms/ bladder and sexual functions in men with symptomatic late-onset hypogonadism. // Aging Male, 2008. Vol. 11, N 3. Р. 146 - 149.
- Koritsiadis G., Stravodimos K., Mitropoulos D. Androgens and bladder outlet obstruction: a correlation with pressure-flow variables in a preliminary study. // BJU Int., 2008. Vol. 101, N 12. Р. 1542 - 1546.
- Traish A.M., Saad F., Guay A. The dark side of testosterone deficiency: II. Type 2 diabetes and insulin resistance. // J. Androl., 2009. Vol. 30, N 1. Р. 23 - 32.
- Чупрына П.С., Деревянченко В.И., Щелков С.В. Доброкачественная гиперплазия простаты, осложненная ОЗМ, и уровень тестостерона крови. // Материалы IV Всероссийского конгресса «Мужское здоровье». М., 2008. С. 66 - 67.
- Корнеев И.А., Глазнева С.Ю. Уровень тестостерона и расстройства мочеиспускания у больных с доброкачественной гиперплазией предстательной железы. // Материалы IV Всероссийского конгресса «Мужское здоровье». М., 2008. С. 49 - 50.
- Robert G., Descazeaud A., Nicolaiew N., Terry S., Sirab N., Vacherot F., Maille P., Allory Y., de la Taille A. Inflammation in benign prostatic hyperplasia: a 282 patients’ immunohistochemical analysis. // Prostate, 2009. Vol. 69, N 16. Р. 1774 - 1780.
- Rohrmann S., De Marzo A.M., Smit E., Giovannucci E., Platz E.A. Serum C-reactive protein concentration and lower urinary tract symptoms in older men in the Third National Health and Nutrition Examination Survey (NHANES III). // Prostate, 2005. Vol. 62, N 1. Р. 27 - 33.
- Devaraj S., Singh U., Jialal I. Human C-reactive protein and the metabolic syndrome. // Curr Opin Lipidol., 2009. № 20. Р. 182 - 189.
- Rhoden E.L., Fornari A., Fuchs S.C., Ribeiro E.P. Evaluation of the association between lower urinary tract symptoms and erectile dysfunction, considering its multiple risk factors. // J Sex Med., 2008. Vol. 5, N 11. Р. 2662 - 2668.
- Калинченко С.Ю., Тюзиков И.А. Практическая андрология. М.: «Практическая медицина», 2009. 400 с.
- Gorbachinsky I., Akpinar H., Assimos D.G. Metabolic syndrome and urological diseases. // Rev Urol., Vol. 12, N 4. Р. 157 - 180.
- Jockenhovel F. Male hypogonadism. Auflage-Bremen: Uni-Med., 2004. - 185 р.
- Srikanthan P., Karlamangla A.S. Relative muscle mass is inversely associated with insulin resistance and prediabetes. Findings from the third National Health and Nutrition Examination Survey. // J Clin Endocrin Metab., 2011. Vol. 96, N 9. Р.2898 - 2909.
- Rohrmann S., Nelson WG., Rifai N., Kanarek N., Basaria S., Tsilidis K.K., Smit E., Giovannucci E., Platz E.A. Serum sex steroid hormones and lower urinary tract symptoms in Third National Health and Nutrition Examination Survey (NHANES III). // Urology, 2007. Vol. 69, N 4. Р. 708 - 713.
- McNeal J.E. Regional morphology and pathology ofthe prostate. // Am. J Clin Pathol., 1968. Vol. 49, N 3. Р. 347 - 357.
- Chawnshang C. Androgens and androgen receptor: mechanisms, functions, and clinical applications. USA: Kluwer Academic Publishers, 2002. 503 p.
- Burnett A.L., Calvin D.C., Chamness S.L., Liu J.X., Nelson R.J., Klein S.L., Dawson V.L., Dawson T.M., Snyder S.H. Urinary bladder-urethral sphincter dysfunction in mice with targeted disruption of neuronal nitric oxide synthase models idiopathic voiding disorders in humans.// Nat Med., 1997. Vol. 3, N 5. Р. 571 - 574.
- James S., Chapple C.R., Phillips M.I., Greengrass P.M., Davey M.J., Turner-Warwick R.T., Milroy E.J., Burnstock G. Autoradiographic analysis of а-adrenoreceptors and muscarinic cholinergic receptors in the hyperplasic human prostate. // J. Urol., 1989. Vol. 142, N 2, Pt. 1. Р. 438 - 444.
- Простатит. /Под ред. Щеплева П.А. - М.: «МЕДпресс-информ», 2007. 224 с.
- Ito S., Juncos L.A., Nushiro N., Johnson C.S., Carretero O.A. Endothelium-derived relaxing factor modulates endothelin action in aggerent arterioles. // Hypertension, 1991. Vol. 17, N 6, Pt. 2. Р. 1052 - 1056.
- Le Brun G., Moldovan F., Aubin P., Ropiquet F., Cussenot O., Fiet J. Identification of endothelin receptors in normal and hyperplasic human prostate tissues. // Prostate. 1996. Vol. 28, N 6. Р. 379 - 384.
- Burnett A.L., Maguire M.P., Chamness S.L., Ricker D.D., Takeda M., Lepor H., Chang T.S. Characterization and localization of nitric oxide synthase in the human prostate. // Urology, 1995. Vol. N 3. Р. 435 - 439.
- Azadzoi K.M., Babayan R.K., Kozlowski R., Siroky M.B. Chronic ischemia increases prostatic smooth muscle contraction in the rabbits. // J. Urol., 2003. Vol. 170, N 2, Pt 1 . Р. 659 - 663.
- Barry M.J., Cockett A.T., Holtgrewe H.L., McConnell J.D., Sihelnik S.A., Winfield H.N. Relationship of symptoms of prostatism to commonly used physiological and anatomical measures of the severity of benign prostatic hyperplasia. // J Urol., 1993. Vol. 150, N 2, Pt 1. Р. 351 - 358.
- Barton M., Cosentino F., Brandes R.P., Moreau P., Shaw S., Luscher T.F. Anatomic heterogeneity of vascular aging: role of nitric oxide and endothelin. // Hypertension, 1997. Vol. 30, N 4. Р. 817 - 824.
- Коган М.И., Киреев А.Ю. Различия уровней тестостерона и полиморфизма гена андрогенового рецептора у пациентов с симптомной ДГП в зависимости от сексуальной активности. // Материалы Международного Конгресса по андрологии. Сочи, Дагомыс, 2009. С.118.
- Giovannucci E., Stampfer M.J., Chan A., Krithivas K., Gann P.H., Hennekens C.H., Kantoff P.W. CAG- repeat within the androgen receptor gene and incidence of surgery for benign prostatic hyperplasia in U.S. physicians. // Prostate, 1999. Vol. 39, N 2. Р. 130 - 134.
- El-Alfy M., Luu-The V., Huang X.F., Berger L., Labrie F., Pelletier G. Localization of type 5 17beta- hydroxysteroid dehydrogenase, 3beta-hydroxysteroid dehydrogenase, and androgen receptor in the human prostate by in situ hybridization and immunocytochemistry. // Endocrinology, 1999. Vol. 140, N 3. Р. 1481 - 1491.
- Medina J.J., Parra R.O., Moore R.G. Benign prostatic hyperplasia (the aging prostate). // Med Clin North Am., 1999. Vol.83, N 5. Р. 1213 - 1229.
- Park I.I., Zhang Q., Liu V, Kozlowski J.M., Zhang J., Lee C. 17-Beta-estradiol at low concentrations acts through distinct pathways in normal versus BPH-derived prostate stromal cells. // Endocrinology, 2009. Vol. 150, N 10. Р. 4594 - 4605.
- Kester R.R., Mooppan U.M., Gousse A.E., Alver J.E., Gintautas J., Gulmi F.A., Abadir A.R., Kim H. Pharmacological characterization of isolated human prostate. // J. Urol., 2003. Vol. 170, N 3. Р. 1032 - 1038.
- Li M-K., Garcia L.A., Rosen R. Lower urinary tract symptoms and male sexual dysfunction in Asia: a survey of ageing men from five Asian countries // BJU, 2005. Vol. 96, N 9. Р.1339 - 1354.
- Rosenzweig B.A., Bolina P.S., Birch L., Moran C., Marcovici I., Prins G.S. Location and concentration of estrogen, progesterone and androgen receptors in the bladder and urethra of the rabbits. // Neurourol Urodyn., 1995. Vol. 14, N 1. Р. 87 - 96.
- Schatzl G., Brossner C., Schmid S., Kugler W, Roehrich M., Treu T., Szalay A., Djavan B., Schmidbauer C.P., Soregi S., Madersbacher S. Endocrine status in elderly men with lower urinary tract symptoms: correlation of age, hormonal status, and lower urinary tract function. The Prostate Study Group of the Austrian Society of Urology. // Urology, 2000. Vol. 55, N 3. Р. 397 - 402.
- Hammarsten J., Hogstedt B., Holthuis N., Mellstrom D. Components of the metabolic syndrome-risk factors for the development of benign prostatic hyperplasia // Prostate Cancer Prostatic Dis., 1998. Vol. 1, N 3. Р. 157 - 162.
- Ozden C., Ozdal O.L., Urgancioglu G., Koyuncu H., Gokkaya S., Memis A. The correlation between metabolic syndrome and prostatic growth in patients with benign prostatic hyperplasia. // Eur Urol., 2007. Vol. 51, N 1. Р.199 - 203.
- Kupelian V., McVary K.T., Kaplan S.A., Hall S.A., Link C.L., Aiyer L.P., Mollon P., Tamimi N, Rosen RC, McKinlay JB. Association of lower urinary tract symptoms and the metabolic syndrome: results from the Boston Area Community Health Survey. // J Urol., 2009. Vol. 182, N 2. Р. 616 - 624.
- Demir O., Akgul K., Akar Z., Cakmak O., Ozdemir I., Bolukbasi A., Can E., Gumus B.H. Association between severity of lower urinary tract symptoms, erectile dysfunction and metabolic syndrome. // Aging Male, 2009. Vol. 12, N 1. Р. 29 - 34.
- McVary K.T., Rademaker A., Lloyd G.L., Gann P. Autonomic nervous system overactivity in men with lower urinary tract symptoms secondary to benign prostatic hyperplasia. // J Urol., 2005. Vol. 174, N 4, Pt. 1. Р. 1327 - 1433.
- McVary K. Lower urinary tract symptoms and sexual dysfunction: epidemiology and pathophysiology. // BJU Int., 2006. Vol. 97, Suppl. 2. Р. 23 - 28.
- Leibson C.L., O'Brien P.C., Atkinson E., Palumbo P.J., Melton L.J. 3rd. Relative contributions of incidence and survival to increasing prevalence of adult-onset diabetes mellitus: a population-based study. // Am J Epidemiol., 1997. Vol. 146, N 1. Р. 12 - 22.
- Rustenbeck I. Desensitization of insulin secretion. // Biochem. Pharmacol., 2002. Vol.63, N 11. Р. 1921 - 1935.
- Azadzoi K.M., Tarcan T, Siroky M.B., Krane R.J. Atherosclerosis-induced chronic ischemia causes bladder fibrosis and non-compliance in the rabbits. // J. Urol., 1999. Vol. 161, N 5. Р. 1626 - 1635.
- Penna G., Fibbi B., Amuchastegui S., Corsiero E., Laverny G., Silvestrini E., Chavalmane A., Morelli A., Sarchielli E., Vannelli G.B., Gacci M., Colli E., Maggi M., Adorini L. The vitamin D receptor agonist elocalcitol inhibits IL-8-dependent benign prostatic hyperplasia stromal cell proliferation and inflammatory response by targeting the RhoA/Rho kinase and NF-kappaB pathways. // Prostate, 2009. Vol. 69, N 5. Р.480 - 493.
- Peters S.L., Schmidt M., Michel M.C. Rho kinase: a target for treating urinary bladder dysfunction? // Trends Pharmacol Sci., 2006. Vol. 27, 9. Р. 492 - 497.
- Rees R.W., Foxwell N.A., Ralph D.J., Kell P.D., Moncada S., Cellek S. Y-27632, a Rho-kinase inhibitor, inhibits proliferation and adrenergic contraction of prostatic smooth muscle cells. // J Urol., 2003. Vol. 170, N 6, Pt. 1. Р. 2517 - 2522.
- Alexandraki K., Piperi C., Kalofoutis C., Singh J., Alaveras A., Kalofoutis A. Inflammatory process in type 2 diabetes: the role of cytokines. // Ann N Y Acad Sci., 2006. Vol. 1084. Р. 89 - 117.
- Ansari M.A., Begum D., Islam F. Serum sex steroids, gonadotrophins and sex hormonebinding globulin in prostatic hyperplasia. // Ann. Saudi Med., 2008. Vol. 28, N 3. Р.174 - 178.
- Fibbi B., Penna G., Morelli A., Adorini L., Maggi M. Chronic inflammation in the pathogenesis of benign prostatic hyperplasia. // Int J Androl., 2010. Vol. 33, N 3. Р. 475 - 488.
- Schaffer J.E. Lipotoxicity: when tissues overeat. // Curr Opin Lipidol., 2003. Vol. 14, N 3. Р. 281 - 287.
- Schlechte J.A. Clinical Practice. Prolactinoma. // N Engl J Med., 2003. Vol. 349, N 21. Р. 2035 - 2041.
- Laron Z. The growth-hormone -prolactin relationship: a neglected issue. // Ped Endocrinol Rev., 2011. Vol. 9, N 2. Р. 546 - 548.
- Шамбах Х., Кнаппе Г., Карол В. Гормонотерапия. М.: «Медицина», 1988. 416 с.
- Калинченко С.Ю. Шаг вперед в лечении гиперпролактинемии. М.: «Практическая медицина», 2010. 96 с.
- Abdulghani J., Gu L., Dagvadorj A., Lutz J., Leiby B., Bonuccelli G., Lisanti M.P., Zellweger T., Alanen K., Mirtti T., Visakorpi T., Bubendorf L., Nevalainen M.T. Stat-3 promotes metastatic progression of prostate cancer. // Am J Pathol., 2008. Vol. 172, N 6. Р. 1717 - 1728.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 1.31 Мб |















































































