Частота бесплодного брака в Европе составляет 15%, при этом около 5% семейных пар так и остаются бесплодными [1]. В последнее годы доля мужского фактора в бесплодии семейной пары превышает женский – его частота достигает, по данным Европейской Ассоциации Урологов (EUA) и Американского общества по репродуктивной медицине (ASRM), 50-60% [2, 3].
Несмотря на значительные успехи, достигнутые клиницистами в лечении женского бесплодия, коррекция нарушений сперматогенеза зачастую остается малоэффективной. Внедрение в практику репродуктивных технологий процедуры интрацитоплазматической инъекции сперматозоида (Intracytoplasmic sperm injection – ICSI, ИКСИ) позволило достигнуть значительного прогресса в наступлении беременности в семьях с мужским фактором бесплодия [4]. Оплодотворения яйцеклеток и достижения беременности на данный момент можно достигнуть не только с использованием сперматозоидов, выделенных из эякулята, но и полученных из семенных канальцев у пациентов с азооспермией. Именно пациенты с азооспермией являются одними из самых сложных в клинической практике врача, занимающегося мужским бесплодием. По данным мировой литературы азооспермия встречается с частотой 1% в общей популяции и у 10-15% у мужчин с бесплодием [5-8]. И если в случае обструктивного характера азооспермии (ОА) никаких сложностей с получением сперматозоидов не возникает, то в случае необструктивной или секреторной азооспермии (НОА) частота получения сперматозоидов до недавних пор оставалась крайне низкой. Однако именно НОА является превалирующей и составляет 80-90% всех случаев азооспермии [1].
Получение сперматозоидов при азооспермии в большинстве случаев производится при помощи биопсии придатка яичка или яичка. Методики TESE (testicular sperm extraction или получение тестикулярных сперматозоидов) и PESA (percutaneous epididymal sperm aspiration или транскутанная аспирация эпидидимальных сперматозоидов) получили широкое распространение еще в начале 90-х годов прошлого столетия.
Однако применение данных методик у пациентов с НОА малоэффективно: так, в случае традиционной TESE вероятность получения сперматозоидов составляет лишь 17% [9].
Интраоперационное использование микроскопа позволяет визуализировать расширенные семенные канальцы, которые могут содержать сперматозоиды, и выполнить микродиссекцию этих участков. Преимуществами данной технологии являются малая инвазивность и высокая результативность в получении сперматозоидов – при секреторной азооспермии она составляет до 63% в отличие от открытой биопсии, а также более демонстративна при тестикулярном объеме менее 10 см3 [11-13].
На первый взгляд, менее травматичным является применение аспирационной биопсии, перкутанного получения биоптата с помощью биопсийного пистолета, либо биопсийной иглой – PESA. Однако, применение данного метода дает статистически значительно меньше шансов получить достаточное количество сперматозоидов для вспомогательных репродуктивных технологий (ВРТ), а также нередко имеет осложнения [14].
В настоящее время метод MDTESE является наиболее безопасной технологией в отношении послеоперационных осложнений и развития дистрофических изменений в гонаде.
Целью данного исследования явилась оценка эффективности метода микрохирургической экстракции сперматозоидов у пациентов с НОА.
МАТЕРИАЛЫ И МЕТОДЫ
Работа выполнена на основании совместных исследований ФГБУ «НИИ Урологии» Минздрава России и Медицинской Клиники Репродукции «МАМА», Москва.
Было отобрано 30 пациентов с НОА в возрасте от 27 до 35 лет (средний возраст 31 год), обратившихся с жалобами на отсутствие беременностей в паре.
Азооспермия была подтверждена минимум двумя исследованиями эякулята с 3-х недельным интервалом и соблюдением последних рекомендаций ВОЗ от 2010 г. [15].
Всем пациентам проводился анализ крови на гормоны : лютеинизирующий и фолликулостимулирующий гормоны (ЛГ, ФСГ), общий тестостерон. Анализ крови забирался строго натощак между 8:00 и 10:00 часами. Объем тестикул оценивался при помощи орхидометра. Всем пациентам проводилось медико-генетическое обследование (исследование кариотипа, анализ крови на наличие микроделеций AZF локуса Y-хромосомы), ультразвуковое исследование органов мошонки.
В исследование были включены пациенты с крипторхизмом в анамнезе, ранее перенесенным орхитом, проведенной химиотерапией, варикоцеле, частичными и полными делециями AZFc локуса Y-хромосомы, патологическими изменениями кариотипа (робертсоновской транслокацией –45,ХY,der(13;14) (q10;q10)). Критериями исключения были эндокринные заболевания, ведущие к снижению секреции тестостерона, за исключением гипергонадотропного гипогонадизма: гипотиреоз, тиреотоксикоз, гиперпролактинемия (определяется на основании уровней тиреотропного гормона (ТТГ), свободного тироксина (Т4), пролактина), декомпенсация сахарного диабета, гиперкортицизм, а так же почечная или печеночная недостаточность, воспалительные заболевания урогенитального тракта в стадии обострения.
Все пациенты подписали протокол стандартного информированного согласия.
Всем пациентам микрохирургическая биопсия яичка проводилась одновременно с проведением стимуляции суперовуляции и экстракции ооцитов у супруги в рамках программы экстракорпорального оплодотворения (ЭКО).
29 пациентам выполнялась проводниковая и местная инфильтративная анестезия. Один пациент с паховой формой крипторхизма нуждался в спинномозговой анестезии.
Сторона вмешательства выбиралась в пользу яичка большего объема (пальпаторно и по данным ультразвуковой диагностики). Интраоперационно при отсутствии очагов сперматогенеза и сперматозоидов с удовлетворительными морфофункциональными качествами решался вопрос о контрлатеральной биопсии.
Интраоперационная спермиоскопия выполнялась эмбриологом при увеличении х256 с помощью бинокулярного инвертированного микроскопа БИОЛАМ-П 2-1, Россия.
Статистический анализ полученных данных проводился с использованием пакета прикладных программ STATISTICA (StatSoft Inc. США, версия 6.0). Количественные данные представлены в виде медиан и интерквартильных интервалов.
ТЕХНИКА ОПЕРАЦИИ
Производилась обработка операционного поля раствором йодопирона. Затем выполнялась проводниковая анестезия яичка и его придатка посредством введения в семенной канатик раствора анестетика (10 мл раствора ронивакаина 0,5%). Далее с помощью 20 мл раствора новокаина 0,5% выполнялась поверхностная инфильтрационная анестезия кожи мошонки (создание «лимонной корочки») в месте предполагаемого разреза. Поперечным разрезом мошонки осуществлялся доступ к белочной оболочке яичка. Яичко с придатком вывихивалось в рану. Интраоперационный гемостаз. Продольным разрезом в области хвоста или тела придатка яичка осуществлялся доступ к канальцам последнего. С помощью операционного микроскопа OPMI VARIO 700 Carl Zeiss Meditec, Германия под 18-ти кратным увеличением выполнялась ревизия канальцев придатка яичка. Ткань придатка резецировалась с помощью микроножниц. Материал интраоперационно передавался эмбриологу. Выполнялась экстракция сперматозоидов из полученного материала в среде для отмывки гамет человека FertiCult IVF Medium (FertiPro). Производилась интраоперационная спермиоскопия. В случае отсутствия сперматозоидов в обработанном материале, после предварительного ушивания дефекта придатка яичка отдельными узловыми швами (Vikril 5/0) осуществлялся последовательный доступ к телу и головке с последующей ревизией. Если сперматозоиды не были обнаружены выполнялся тестикулярный доступ. Скальпелем проводилось поперечное или продольное рассечение белочной оболочки яичка (до 40% длины окружности). Гемостаз тестикулярных сосудов осуществлялся с помощью биполярного коагулятора, далее выполнялась ревизия канальцев яичка вплоть до его средостения. Выявленные наиболее перспективные канальцы яичка резецировались. Фрагмент ткани передавался на патогистологическую экспертизу. Дефект белочной оболочки ушивался отдельными узловыми швами (Vikril 5/0). Производился окончательный гемостаз, послойное ушивание раны (Vikril 3/0). Края раны обрабатывались раствором йодопирона. Асептическая повязка. В случае отсутствия пригодных по своим морфо-функциональным качествам сперматозоидов выполнялась повторная операция с контрлатеральной стороны.
В послеоперационном периоде назначался левофлоксацин 750 мг 5 дней, свечи с диклофенаком 100 мг ректально 5 дней, анальгетики по показаниям, перевязки, ограничение средней и тяжелой физической нагрузки в течение 14 дней.
Снятие швов проводилось на 14 сутки.
РЕЗУЛЬТАТЫ
У всех пациентов был нормальный объем тестикул, уровень лютеинизирующего гормона и общего тестостерона. Средние значения этих показателей представлены в таблице 1.
Основные результаты произведенной экстракции сперматозоидов представлены в таблице 2.
По результатам проведенной микрохирургической биопсии яичка у 12(40 %) пациентов были обнаружены и выделены сперматозоиды, пригодные для выполнения ИКСИ. У 23 (69%) пациентов выполнено билатеральное вмешательство.
Выделенные из биоптатов сперматозоиды у всех пациентов были использованы для оплодотворения ооцитов супруги, также у 8 пациентов была проведена криоконсервация части сперматозоидов для их дальнейшего использования с целью достижения беременности у супруги.
При патологогистологическом исследовании ткань яичка у всех пациеньтов была представлена склерозированными семенными канальцами с участками атрофии или гипотрофии сперматогенного эпителия, блоком сперматогенеза на различных уровнях.
У 60% пациентов выявлена остановка сперматогенеза на уровне сперматогоний, в оставшейся части исследованных биоптатов блок обнаружен на уровне сперматоцитов (рис. 1).
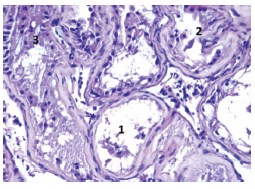
Рис. 1. Биоптат ткани яичка. 1. Семенной каналец. Атрофия сперматогенного эпителия. 2. Гипотрофия сперматогенного эпителия с малым количеством сперматогоний в просвете семенного канальца. 3. Гиперплазированные клетки Лейдига в интерстиции
При проведении анестезии ни одного случая индивидуальной непереносимости или побочных реакций отмечено не было.
В послеоперационном периоде у одного пациента развился орхит вследствие нарушения последним предписанного лечения, что потребовало назначения активной антибактериальной терапии с хорошим эффектом.
ОБСУЖДЕНИЕ
Микрохирургическая экстракция сперматозоидов давно зарекомендовала себя как высокорезультативный метод получения сперматозоидов в случае необструктивной азооспермии различной этиологии (гипергонадотропный гипогонадизм, генетические нарушения).
Помимо этого, малая инвазивность вмешательства позволяет практически полностью избежать таких частых осложнений биопсии, как гематомы и инфекционные осложнения. Микроскопически интраоперационная картина позволяет отчетливо визуализировать мелкие сосуды и выполнить их тщательный гемостаз, а микрохирургический инструмент обеспечивает максимально аккуратную экстракцию фрагментов канальцев.
Основной жалобой после вмешательства являются боли в области послеоперационной раны. Исходя из нашего опыта, боли хорошо купируются ненаркотическими анальгетиками (вольтарен, анальгин) и полностью исчезают к 10-14 суткам.
Большое клиническое и экономическое значение имеет сокращение времени пребывания пациента в стационаре – до нескольких часов наблюдения после вмешательства. Большинство пациентов не нуждаются в листке нетрудоспособности вследствие незначительной физической нагрузки на рабочем месте: офисная работа, вождение автомобиля.
Таблица 1. Средние значения некоторых параметров при обследовании пациентов
| Показатель | Медиана и интерквартильный размах |
|---|---|
| Суммарный объем яичек, см3 |
28,5 [17; 32] |
| ЛГ, мЕд/мл |
5,48 [3,75; 8,5] |
| Общий тестостерон, нмоль/л |
13,4 [10,9; 19,0] |
| ФСГ, мЕд/мл | 10,2 [5,3; 21,6] |
Таблица 2. Результаты экстракции сперматозоидов
| Показатель |
Кол-во больных (чел., %) |
|---|---|
| Успешные экстракции сперматозоидов |
12 (40%) |
| Билатеральное вмешательство |
23 (69%) |
| Обнаружено сперматозоидов в придатке (MESE): |
|
| Хвост |
6 (20%) |
| Тело |
5 (16,6%) |
| Головка |
10 (33,3%) |
| Обнаружено сперматозоидов в яичке (MD-TESE) |
12 (40%) |
| Выявлено гистологически: Сперматогонии Сперматоциты |
1 (3,3%) |
| Всего | 30 (100%) |
Кроме того, хорошие результаты при использовании криоконсервированных сперматозоидов, позволяют проводить вмешательство однократно с последующим успешным использованием сохраненных гамет.
Исходя из данных, представленных в таблице 1, медиана фолликулостимулирующего гормона находится на верхней границе нормы, что в совокупности с НОА свидетельствует о необратимом нарушении сперматогенеза. У ряда пациентов с секреторной азооспермией при нормальном уровне ФСГ можно говорить о блоке сперматогенеза, как о причине азооспермии
Несмотря на более высокую долю (33,3%) обнаружения тестикулярных сперматозоидов при MD-TESE, мы считаем более целесообразным в первую очередь выполнять MESE (Microsurgical Epididymal Sperm Extraction) для выявления более зрелых и морфологически правильных форм, поскольку именно в придатке под влиянием андрогенов происходит морфологическое, биохимическое и физиологическое дозревание сперматозоидов.
Оценка качества и достаточного количества полученного материала должна проводиться эмбриологом интраоперационно, поскольку это позволяет более эффективно выявить очаги сперматогенеза, обеспечивает более экономную экстракцию, ограничивает объем вмешательства. Однако нами были отмечены случаи выявления сперматозоидов в полученном материале только в лаборатории ЭКО при применении специализированной аппаратуры и достаточного количества времени для выделения половых клеток.
Согласно последним рекомендациям Европейской урологической ассоциации проведение диагностической биопсии яичка в случае мужского бесплодия без возможности криоконсервации полученных сперматозоидов не рекомендовано [1]. К сожалению, в подавляющем большинстве случаев проведения операций TESE или PESA в России криоконсервация даже не рассматривается как необходимая манипуляция. В случае же проведения MDTESE возможно одновременное использование полученных сперматозоидов для оплодотворения ооцитов супруги и проведение криоконсервации.
ВЫВОДЫ
Высокая эффективность метода микрохирургической экстракции сперматозоидов у пациентов с НОА при отсутствии осложнений позволяет считать данный метод перспективным в лечении мужского фактора бесплодия.
ЛИТЕРАТУРА
1. Jungwirth A, Diemer T, Dohle GR, Giwercman A., Kopa Z., Tournaye H, Krausz C. The updated EAU guidelines on Male Infertility. EAU Guidelines Office, Arnhem, The Netherlands. 2013
2. The Practice Committee of the American Society for Reproductive Medicine Diagnostic evaluation of the infertile male: a committee opinion. //Fertility and Sterility. 2012.Vol. 98, N 2 , P. 294-301.
3. Mascarenhas MN, Flaxman SR, Boerma T, Vanderpoel S, Stevens GA. National, regional, and global trends in infertility prevalence since 1990: a systematic analysis of 277 health surveys. // PLoS Med. 2012. Vol. 9, N12. P. 1-12
4. Palermo G, Joris H, Devroey P, Van Steirteghem AC. Pregnancies after intracytoplasmic injection of single spermatozoon into an oocyte. // Lancet. 1992. Vol. 340. P. 17-18.
5. Nieschlag E., Behre H., Nieschlag S. Andrology. 3rd Edition, Springer 2010, P. 643
6. Jarow JP, Espeland MA, Lipshultz LI. Evaluation of the azoospermic patients. // J Urol. 1989. Vol. 142. P. 62-65.
7. Irvine D. S. Epidemiology and etiology of male infertility // Hum Reprod. 1998. Vol. 13, Suppl. 1. P. 33–44.
8. Hernandez U. L., Cervera-Aguilar R. Frequency and etiology of azoospermia in the study of infertile couples // Gynecol. Obstet. 2005. Vol. 69. P. 322–326.
9. Okada H, Dobashi M, Yamazaki T, Hara I, Fujisawa M, Arakawa S, Kamidono S. Conventional versus microdissection testicular sperm extraction for nonobstructive azoospermia. // J Urol. 2002. Vol. 168, N 3. P. 1063-1067.
10. Schlegel PN. Testicular sperm extraction: microdissection improves sperm yield with minimal tissue excision. // Hum Reprod. 1999. Vol. 14. P. 131-135.
11. Mulhall JP, Ghaly SW, Aviv N, Ahmed A. The utility of optical loupe magnification for testis sperm extraction in men with nonobstructive azoospermia. // J Androl. 2005. Vol. 26 P. 178-181.
12. Ramasamy R, Lin K, Gosden L, Rosenwaks Z, Palermo GD, Schlegel PN. High serum FSH levels in men with nonobstructive azoospermia does not affect success of microdissection testicular sperm extraction. // Fertil Steril. 2009. Vol. 92, N2 P. 590-593.
13. Ishikawa T, Nose R, Yamaguchi K, Chiba K, Fujisawa M. Learning curves of microdissection testicular sperm extraction for non-obstructive azoospermia. // Fertil Steril. 2010. Vol. 94. P. 1008-1011. 14. Houwen J, Lundin K, Söderlund B, Bergh C, Kremer JA, Ekerhovd E. Efficacy of percutaneous needle aspiration and open biopsy for sperm retrieval in men with non-obstructive azoospermia. // Acta Obstet Gynecol Scand. 2008. Vol. 87, N 10. P. 1033-1038.
15. WHO laboratory manual for the examination and processing of human semen. 5th ed.Geneva. World Health Organization. 286 p.







