В настоящее время перкутанная нефролитотрипсия (ПНЛ) является общепризнанным стандартом оперативного лечения нефролитиаза [1-3]. В последнее время в экспертном сообществе активно обсуждается вопрос о расширении показаний к бездренажному проведению перкутанных вмешательств. Определяющими факторами выбора данной методики являются степень выраженности бактериурии, объем камня, наличие резидуальных конкрементов, диаметр перкутанного тракта, количество доступов, повреждение чашечно-лоханочной системы (ЧЛС) и выраженность кровотечения в конце операции [4]. На заре внедрения в клиническую практику ПНЛ установка нефростомы большого диаметра была общепринятым стандартом, что обеспечивало хорошую дренажную и гемостатическую функцию, позволяло выполнять уретеропиелографию с контрастированием и при необходимости осуществление повторного доступа в полостную систему почки.
Однако используемые в то время нефростомы за счет своих физических свойств и конструкций нередко являлись причиной возникновения болевых симптомов, что послужило предпосылкой для совершенствования их форм и конфигураций, а также заставило задуматься о необходимости и целесообразности в ряде случаев дренирования чрескожного хода [5]. Впервые о бездренажной технике выполнения ПНЛ, так называемой «tubeless» методике, сообщили G.C. Bellman и соавт. в 1997 г. [6]. Однако следует отметить, что первое рандомизированное клиническое исследование, посвященное применению «tubeless» методики, было проведено M.O. Istanbulluoglu и соавт. и опубликовано в 2009 г. [7]. Авторами были проанализированы результаты лечения 90 пациентов.
Сравнивались две группы больных: пациенты, подвергнутые бездренажной методике ПНЛ и группа больных, оперативное вмешательство у которых завершалось дренированием ЧЛС посредством установки нефростомы типа Малекот 14 Fr. Критериями включения являлись отсутствие выраженного кровотечения из перкутанного тракта и/или перфорации ЧЛС, а также полная санация ЧЛС от клинически значимых резидуальных фрагментов (более 3мм) при выполнении операции из одного доступа. Проведенные рядом авторов исследования позволили выявить преимущества данной методики, включавшие в себя снижение интенсивности болевого симптома и степени экстравазации мочи из перкутанного тракта в послеоперационном периоде, сокращение сроков пребывания пациента в стационаре, а также уменьшение потребности в анальгетиках, особенно наркотических [8, 9]. Важным аспектом проводимой в этом направлении работы, стало изучение технологии закрытия чрескожного хода с использованием различных гемостатических агентов: фибриновых гелей и гемостатических желатиновых матриксов [10]. В литературе даже описаны случаи применения криоаблации нефростомического тракта с целью создания гемостаза [11]. Используемые в настоящее время в хирургии фибриновые гели имеют жидкую субстанцию и обладают всеми необходимыми компонентами (тромбин и фибриноген) для тромбообразования при контакте с раневой поверхностью. Важно отметить, что фибриновые гели эффективны независимо от состояния факторов свертывания крови самого пациента, а препаратам, содержащим желатин и тромбин, при контакте с раневой поверхностью требуется собственный фибриноген пациента для запуска процесса свертывания. Желатиновые частицы в этом случае играют роль матрицы для последующего формирования сгустка [10].
Применение гемостатических субстанций при неосложненных ПНЛ впервые было продемонстрировано A.A. Mikhail и соавт. [12]. Авторы провели рандомизированное исследование, в ходе которого сравнивались результаты лечения двух групп пациентов (основная и контрольная группа). Основная группа была представлена пациентами, у которых оперативное вмешательство завершалось введением фибринового геля в перкутанный тракт. Последующий анализ полученных данных не выявил статистически достоверной разницы по изменению уровня гемоглобина до и после операции и по интенсивности болевого симптома в двух сравниваемых группах больных. Результаты проведенного исследования позволили авторам заключить, что применение бездренажной методики ПНЛ с использованием фибринового геля оправдано в случаях отсутствия выраженного кровотечения из перкутанного тракта.
В настоящее время эффективность применения гемостатических материалов в перкутанной хирургии дискутируется и находится на этапе активного изучения. В свою очередь продолжается поиск и внедрение в клиническую практику новых оптимальных гемостатических материалов для применения, в том числе, и в перкутанной хирургии [13-16].
МАТЕРИАЛЫ И МЕТОДЫ
За период с 2009 по 2015 гг. в НИИ урологии методика бездренажной техники ПНЛ была применена у 59 пациентов. Критерии включения и исключения в исследование базировались на результатах собственного опыта выполнения бездренажной ПНЛ и на подходах, принятых в мировой практике. Таким образом, критериями включения являлись: отсутствие выраженного кровотечения в процессе оперативного вмешательства, отсутствие клинически значимых резидуальных фрагментов (не более 4 мм), одиночный доступ, отсутствие бактериурии в бактериологическом анализе мочи, отсутствие в анамнезе атак пиелонефрита, отсутствие перфорации лоханки, продолжительность операции менее двух часов. В свою очередь к критериям исключения мы отнесли: наличие заболеваний обусловленных нарушением свертывающей системы крови и наличие стриктур верхних мочевыводящих путей (ВМП). Следует отметить, что с целью повышения объективности оценки результатов мы также исключали из исследования пациентов, которым выполнялась миниперкутанная нефролитотрипсия. Все больные, подвергнутые бездренажной технике ПНЛ, были рандомизированы на две группы. Основную группу в количестве 29 человек составили больные, которым в конце операции вводили гемостатический матрикс в область перкутанного тракта. Контрольная группа была представлена 30 пациентами. Возраст пациентов варьировал от 28 до 60 лет. Средней размер камня в максимальном поперечнике составил 21 и 23 мм в основной и контрольной группе, соответственно (табл. 1). Различия между основной и контрольно группой относительно возраста, пола, размера и локализации камней была статистически недостоверна.
Таблица 1. Основные характеристики больных, включенных в исследование (n=59)
| Показатели | Основная группа (n=29) | Контрольная группа(n=30) |
|---|---|---|
| Возраст (лет) | 49 (min 28; max 56) | 53 (min 31; max 60) |
| Наличие сопутствующих заболеваний (%) | 41,3 | 48,9 |
| Размер камня (мм) | 21 (min-17; max-24) | 23 (min-19; max-26) |
| Мужчин (абс. число, %) | 13 (44,8) | 14 (46,7) |
| Женщин (абс. число, %) | 16 (55,2) | 16 (53,3) |
| Рецидивные камни (абс. число, %) | 12 (41,4) | 14 (46,7) |
| Наличие бактериурии (абс. число, %) | 17 (58,6) | 19 (63,3) |
| Наличие расширения ЧЛС (абс. число, %) | 17 (58,6) | 18(60,0) |
| Дефицит функции почки (%) | 27 (min-23; max-38) | 23 (min-19; max-34) |
Предоперационное обследование пациентов производилось по стандартной методике, выполняемой у пациентов с мочекаменной болезнью. Основное внимание уделяли размеру, количеству форме конкрементов, их конфигурации и расположению в полостной системе почки, выраженности воспалительного процесса, наличию и степени пиелокаликоэктазии, а также функциональному состоянию почечной паренхимы, поскольку именно эти факторы являются ведущими при выборе метода лечения. Все процедуры ПНЛ выполнены посредством установки тубуса нефроскопа №24-26 Ch после предварительного бужирования пункционного хода телескопическими бужами Алкена. Следует отметить, что всем пациентам до начала вмешательства выполнялась установка наружнего мочеточникового стента 6 Fr, который оставляли на сутки после операции. Для дезинтергации конкрементов нами использовался ультразвуковой литотриптер. Все оперативные вмешательства в основной группе пациентов завершали введением предварительно приготовленного гемостатического матрикса в просвет перкутанного тракта (рисунок 1 а-д).
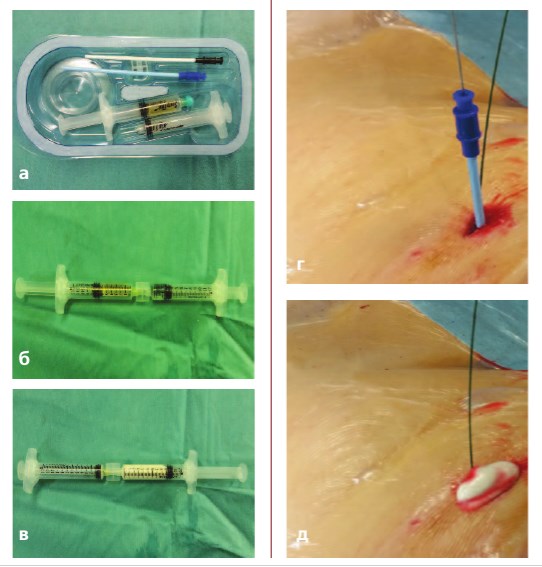
Рис. 1. Введение предварительно приготовленного гемостатического матрикса в просвет перкутанного тракта. а) Набор для приготовления гемостатического матрикса б) Разведение сухого гемостатического матрикса на 3 мл раствора тромбина в) Разведеный гемостатический матрикс г) Установка полихлорвиниловой канюли по проводнику в перкутанный тракт с целью последующего введения гемостатического матрикса д) Окончательный вид послеоперационной раны после введения в перкутанный тракт гемостатического матрикса
Были определены следующие прогностические критерии эффективности, по которым проводился сравнительный анализ групп пациентов: кровопотеря, интенсивность подтекания мочи из чрескожного хода и степень экстравазации в паранефральную клетчатку. Объем кровопотери оценивался по уровню снижения гемоглобина. Интенсивность подтекания по нефростомическому ходу оценивалась по степени промокания раневой повязки. На основании данных УЗИ определяли наличие либо отсутствие экстравазации в паранефральном пространстве. Всем пациентам через две недели после выписки производилось контрольное обследование по стандартной методике.
Статистическую обработку полученных данных производили на персональном компьютере посредством программы statistica 10.
РЕЗУЛЬТАТЫ
Данные по основным параметрам, посредством которых сравнивались результаты лечения, представлены в таблице 2. Длительность оперативного вмешательства в среднем составила 49±5,3 минут применительно ко всей группе пациентов. И как видно из таблицы разница между группами по данному критерию была статистически недостоверной (p=0,15). Как уже было отмечено выше, бездренажная методика ПНЛ применялась только у пациентов с минимальным интраоперационным объемом кровопотери и отсутствием интенсивного кровотечения из перкутанного тракта после удаления тубуса нефроскопа, и связи с этим данный показатель в таблице не отражался. Среднее значение уровня гемоглобина до и после операции также применительно ко всей группе пациентов составило 142,25±4,3% и 134,7±4,4%, соответственно (p=0,001). В основной группе эти показатели равнялись 141,8 ± 3,5% и 133,9 ± 4,9% (p=0,017) до и после вмешательства, соответственно, а в контрольной группе – 143,2 ± 5% и 135,1 ± 4,2% (p=0,003). По уровню снижения гемоглобина после выполнения ПНЛ между группами больных, включенных в исследование, не было отмечено статистически достоверной разницы (p=0,23). У 5 пациентов в основной и у 6 – в контрольной группах в ближайшем послеоперационном периоде по данным ультразвукового исследования определялось жидкостное образование в паранефральном пространстве (не превышающее по объему 50 мл), свидетельствующее об экстравазации мочи и/или крови из полостной системы и паренхимы почки в окружающую клетчатку. Следует отметить, что ни в одном случае не потребовалось выполнения каких либо интервенций по данному факту. Промокание более одной повязки в день было отмечено у 7 (24,1%) и 8 (26,7%) пациентов в основной и контрольной группах, соответственно (p>0,05). Ни у одного из пациентов не было зафиксировано значимого кровотечения из перкутанного доступа с последующей тампонадой ЧЛС. Соответственно ни в одном случае не потребовалось переливания компонентов крови или кровезаменителей. Инфекционно-воспалительные осложнения в послеоперационном периоде наблюдались у 5 (17,2%) и 6 (20%) пациентов в основной и контрольной группе, соответственно (p>0,05), и во всех случаях были купированы консервативно. Все пациенты были выписаны на вторые сутки после вмешательства в удовлетворительном состоянии.
Таблица 2. Послеоперационные параметры в основной и контрольной группах
| Показатели | Основная группа (n=29) | Контрольная группа(n=30) |
|---|---|---|
| Длительность операции (мин) | 48,8±3,9 | 51,1±4,1 |
| Гемоглобин до операции (г/л) | 141,8 ± 3,5 | 143,2 ± 5 |
| Гемоглобин после операции (г/л) | 133,9 ± 4,9 | 135,1 ± 4,2 |
| Экстравазация в паранефральное пространство (абс. число, %) |
5 (17,2) | 6 (20) |
| Истечение мочи из перкутанного тракта (абс. число, %) |
7 (24,1) | 8 (26,7) |
| Инфекционно-воспалительные осложнения (абс. число, %) |
5 (17,2) | 6 (20) |
ОБСУЖДЕНИЕ
В настоящее время ПНЛ широко применяется как стандартный метод лечения при крупных и коралловидных камнях почек. По причине того, что нефростомические дренажи могут являться причиной болевого синдрома и причиняют неудобства пациентам, в качестве альтернативного подхода рассматривается применение бездренажной методики ПНЛ. Для окклюзии нефростомического тракта было предложено применение в клинической практике фибриновых гелей и гемостатических матриксов. В нашем исследовании мы провели оценку эффективности и безопасности применения гемостатического матрикса у пациентов после ПНЛ по бездренажной методике. Собственный опыт применения бездренажной техники выполнения ПНЛ позволил сделать ряд выводов: отсутствие различий в эффективности и уровне осложнений со стандартной ПНЛ, значительное сокращение времени пребывания (больше, чем в 2 раза) в стационаре, снижение выраженности болей, снижение потребности в анальгетиках в послеоперационном периоде.
Результаты исследования оценивались по трем основным параметрам: по уровню снижения гемоглобина, объему экстравазации в паранефральное пространство и степени истечения мочи по перкутанному тракту. Несмотря на то, что в обеих группах исследуемых больных отмечалось снижение уровня гемоглобина после вмешательства, разница по данному параметру была статистически недостоверной. В изучаемых группах больных герметизация перкутанного тракта осуществлялась достаточно надежно и не было отмечено клинически значимой экстравазации в паранефральное пространство. Осложнения в послеоперационном периоде носили типовой для данных вмешательств характер и во всех случаях были купированы консервативно. Следует отметить, что такие грозные осложнения как развитие выраженного кровотечения с необходимостью гемотрансфузии, перфорация плевральной полости и близлежащих органов не были отмечены ни в одном из случаев.
ЗАКЛЮЧЕНИЕ
Применение бездренажной техники выполнения ПНЛ позволяет избавить пациента от болевого симптома в послеоперационном периоде и, соответственно, значительно снизить потребность в применении анальгетиков, сокращает время пребывания пациентов в стационаре, способствуя таким образом ранней реабилитации больных и снижению экономических затрат лечебного учреждения. Естественно, что бездренажная методика могла быть применена нами лишь у пациентов с отсутствием выраженного интраоперационного кровотечения, что может вызвать дискуссию относительно целесообразности введения у этой категории пациентов кровоостанавливающих агентов. Однако, несмотря на то, что нами не было получено статистически достоверных преимуществ применения гемостатического матрикса у пациентов после ПНЛ по бездренажной методике, мы отмечаем безопасность использования данных агентов, и считаем дополнительной важной мерой профилактики активного кровотечения из чрескожного хода в раннем послеоперационном периоде. Кроме того введение гемостатических агентов является дополнительным фактором, способствующим герметизации тракта и снижающим вероятность экстравазации в паранефральное пространство. В настоящее время требуется проведение дальнейших исследований, направленных на определение оптимальных гемостатических агентов с целью последующей рекомендации их внедрения в клиническую практику.
ЛИТЕРАТУРА
1. Меринов Д.С., Павлов Д.А., Гурбанов Ш.Ш., Фатихов Р.Р., Епишов В.А., Артемов А.В., Швангирадзе И.А. Наш 5-летний опыт выполнения перкутанной нефролитотомии у пациентов с крупными и коралловидными камнями почек. Экспериментальная и клиническая урология 2014;(2): 54-59
2. Wein AJ, Kavoussi LR, Novick AC, Partin AW, Peters CA. Campbell-Walsh Urology. 10th ed. Philadelphia: Saunders. 2012. P. 1325–1356.
3. European Association of Urology Guidelines, Arnhem, The Netherlands. 2015. P. 19-20 4. Karadag MA, Cecen K, Demir A, Kocaaslan R, Taken K, Altunrende F. Tubeless percutaneous nephrolithotomy: can be a choice, why not? Open Urol Nephrol J 2014;(7):4-7.
5. Paul EM, Marcovich R, Lee BR, Smith AD. Choosing the ideal nephrostomy tube. BJU Int 2003;92(7):672–677.
6. Bellman GC, Davidoff R, Candela J, Gerspach J, Kurtz, S, Stout, L. Tubeless percutaneous renal surgery. J Urol 1997;157(5):1578–1582.
7. Istanbulluoglu MO, Ozturk B, Gonen M, Cıcek T, Ozkardes H. Effectiveness of totally tubeless percutaneous nephrolithotomy in selected patients: a prospective randomized study. Int Urol Nephrol 2009;41(3):541–545
8. Yoon GH, Bellman GC. Tubeless percutaneous nephrolithotomy: A new standard in percutaneous renal surgery. J EndoUrol 2008;22(9):1865–1867
9. Sofer M, Lidawi G, Keren-Paz G, Yehiely R, Beri A, Matzkin H. Tubeless percutaneous nephrolithotomy: first 200 cases in Israel. Isr Med Assoc J 2010;12(3):164-167.
10. Arun K. Srinivasan, Zeph Okeke & Arthur D. Smith: Exit strategy after percutaneous renal surgery: drainage and hemostasis. In Smith's Textbook of Endourology 3rd Ed. 2012. P 326-333.
11. Okeke Z, Andonian S, Srinivasan A, Shapiro E, Vanderbrink BA, Kavoussi LR, et al. Cryotherapy of the nephrostomy tract: A novel technique to decrease the risk of hemorrhage after tubeless percutaneous renal surgery. J Endourol 2009;23(3):417–420.
12. Mikhail AA, Kaptein JS, Bellman GC. Use of fibrin glue in percutaneous nephrolithotomy. Urology 2003;61(5):910–914.
13. Aghamir SM, Khazaeli MH, Meisami A. Use of Surgicel for sealing nephrostomy tract after totally tubeless percutaneous nephrolithotomy. J Endourol 2006;20(5):293-295.
14. Ziaee SA, Sarhangnejad R, Abolghasemi H, Eshghi P, Radfar MH, Ahanian A, et al. Autologous fibrin sealant in tubeless percutaneous nephrolithotomy; a prospective study. Urol J 2013;10(3):999-1003.
15. Koo KC, Park SU, Jang HS, Hong CH. Tubeless percutaneous nephrolithotomy with non-absorbable hemostatic sealant (Quikclot®) versus nephrostomy tube placement: a propensity score-matched analysis. Urolithiasis 2015;43(6):527-533.
16. Abbott JE, Cicic A, Jump RW 3rd, Davalos JG. Hemostatic plug: novel technique for closure of percutaneous nephrostomy tract. J Endourol 2015;29(3):263-269







