Роль робот-ассистированной хирургии растет во всем мире, в том числе и в России. Области применения роботов неуклонно расширяются – в урологии робот-асисстированные операции наиболее часто выполняются при раке предстательной железы и раке почки.
Рак почки в мире составляет 2-3% всех онкологических заболеваний у взрослых. В США ежегодный прирост заболеваемости составляет те же 2-3%, но урологи задаются вопросом – является ли это реальным приростом или результатом улучшения диагностики. По данным Американского онкологического общества в 2010 г. подобная тенденция наблюдается практически повсеместно. Примерно 2/3 всех наблюдений составляют опухоли малого размера, выявленные случайно у пациентов, проходивших обследование по каким-либо другим причинам.
Классическая триада симптомов рака почки – боль в боку, макрогематурия и пальпируемое образование – встречаются в наше время редко. Если подобная триада всетаки наблюдается, то это уже говорит о распространенности заболевания и такая находка может быть слишком запоздалой для радикального лечения.
Для стадирования рака почки применяется система TNM, известная всем урологам. Раньше в нашей клинике резекцию почки выполняли только при стадии T1а, теперь же резекция выполняется во всех случаях стадии T1. Это – эволюция хирургического мышления. Изначально мы выполняли радикальную нефрэктомию, потом – нефрэктомию с сохранением надпочечников, затем перешли к органосберегающим операциям, потом – к аблятивным технологиям и, наконец, – к активному наблюдению. Все начиналось с максимально агрессивного удаления органа с окружающими тканями и закончилось тем, что в определенных случаях допустимо простое наблюдение пациента. Хирургические методы, применяемые при раке почки, также эволюционировали. Когда-то все начиналось с открытых вмешательств (радикальной нефрэктомии или резекции почки), затем доступ для этих операций стал выполняться лапароскопически или робот-ассистированно. В дальнейшем появились аблятивные методики с различными доступами (открыто, лапароскопически, перкутанно) при помощи различных физических факторов: криоабляция, радиочастотная абляция. В последние годы появилась новая нехирургическая опция – активное наблюдение.
Почему же мы стараемся выполнять именно органосохраняющие вмешательства, например, резекцию почки? Есть две причины, которые заставляют стремиться сохранить орган: онкологическая и функциональная. С онкологической точки зрения, согласно последним данным канцер-специфическая выживаемость после радикальной нефрэктомии и резекции почки с опухолями от 4 до 7 см примерно одинакова. То есть, удалена вся почка или же только часть ее с опухолью, специфическая выживаемость будет одинаковой. Это подтверждают несколько публикаций пионера в этой области доктора Novak с результатами долгосрочных наблюдений сначала пациентов с опухолями меньше 4 см, затем – с опухолями до 7 см. В чем же состоит смысл функциональной причины? В последние годы опубликовано несколько статей относительно развития почечной недостаточности после нефрэктомии и резекции почки. Основной вывод, сделанный в данных статьях, заключается в том, что пациенты после радикальная нефрэктомия более подвержены риску почечной недостаточности, чем пациенты после резекции почки, т.е. у пациентов с сохраненным органом реже развивается почечная недостаточность, что, в свою очередь, снижает риск осложнений и увеличивает выживаемость.
Какие же малоинвазивные методы доступны сегодня для лечения рака почки? Это: лапароскопия, робот-ассистированная хирургия, аблятивные методы и активное наблюдение. Преимущества малоинвазивных методов известны всем: пациент подвергается меньшей травматизации, испытывает меньше болевых ощущений, быстрее восстанавливается. Преимущества для хирурга: улучшение визуализации, уменьшение кровопотери. К недостаткам малоинвазивных методов можно отнести длительное время обучения, увеличение себестоимости лечения и увеличение времени операции, особенно на этапе становления методики.
Вернувшись к истории метода, можно упомянуть, что первая лапароскопическая процедура была выполнена в начале XX века с использованием цистоскопа. В 1987 г. была выполнена первая лапароскопическая холецистэктомия. А теперь настало время роботической революции. Первым роботом был AESOP, который, по моему мнению, был «истинным» роботом, одобренным FDA (рисунок 1). Его функция состояла в управлении камерой на основании голосовых команд. Современный робот Da Vinci, на самом деле не «истинный» робот, так как его работа пассивна. Если обратиться к происхождению слова «робот», то на самом деле это означает рабский труд. Первым человеком, сконструировавшим робота, был Леонардо да Винчи. Поэтому первый прототип для робот-ассистированной хирургии назвали Моной, в честь Моны Лизы. Система FDA 2000 в дальнейшем была названа Da Vinci. Есть интересное высказывание о роботах: «Роботы помнят все, но не придумывают ничего нового. Они могли бы быть хорошими университетскими профессорами». Что представляет собой система Da Vinci? Это компьютер-опосредованная система по типу «хозяин-раб». Это «истинный» робот, поскольку на самом деле инструменты следуют движениям хирурга, у которого есть удобная консоль управления с 3D изображением, и манипуляторы, которые в отличие от прямых лапароскопических инструментов, подвижны более чем кисть человека и обладают 7-ю степенями свободы движения, могут снижать тремор пальцев, увеличивая точность манипуляций. Другим новшеством в робот-ассистированной хирургии является система TILE PRO, когда можно накладывать диагностические изображения в реальном времени на изображения хирургического поля. Первым роботом 1999 г. был Da Vinci, потом появился Da Vinci S, последней версией является Da Vinci SI. Последняя модель более компактна, построена на цифровых технологиях и имеет ряд преимуществ – возможность подключения двух консолей управления, которые используются во время подготовки специалистов (рисунок 2).

Рисунок 1. AESOP
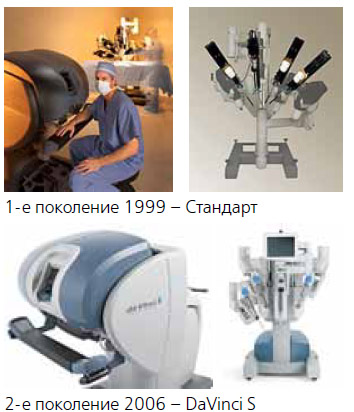

Рисунок 2. Хирургическая система DaVinci
Каковы же основные преимущества робота перед лапароскопией для хирурга? Это меньшая физическая нагрузка, меньшее время на обучение, большая эргономичность,улучшенное 3D изображение, легкость манипуляций, уменьшение времени операции за счет упрощения наложения швов, возможность оперирования в более сложных случаях. Поэтому почти все публикации говорят о преимуществах робот-ассистированной резекции почки перед лапароскопической.
Показания к органосберегающей операции:
- опухоли меньше 7 см при нормально функционирующей контрлатеральной почке;
- единственная функционирующая почка;
- почечная недостаточность;
- системные заболевания, которые в дальнейшем могут вызвать снижение функции почек (сахарный диабет, мочекаменная болезнь).
Робот-ассистированную резекцию почки можно выполнять трансперитонеально или ретроперитонеально. В нашей клинике такие операции выполняются трансперитонеально, так как при этом создается большее рабочее пространство, а исследования показывают отсутствие разницы в сроках восстановления после таких операций.Большинство пациентов выписываются в течение следующих 24-48 часов.
Технические особенности: четвертый манипулятор, которым можно фиксировать почку при операции (рисунки 3, 4).
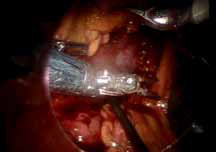
Рисунок 3. Роботическая резекция опухоли почки: эффективное применение 4-й руки
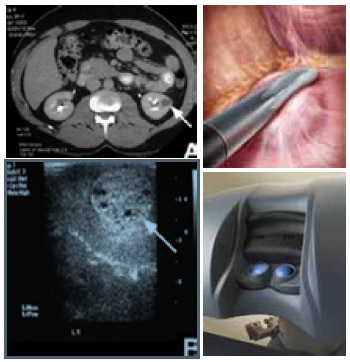
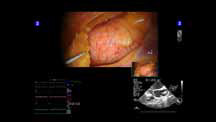
| Интраоперационная ультразвуковая визуализация опухоли |
TILE PRO image guidance |
Рисунок 4. Роботическая резекция Рисунок 6. Ушивание ложа опухоли почки – техника
Доступ к почечным сосудам осуществляется манипуляторами. С целью экономии времени я использую зажим Сатинского для пережатия всей почечной ножки. После выделения ножки производится маркировка опухоли под ультразвуковым контролем. При этом ультразвуковое изображение выводится на окуляры пульта (TILE PRO). Можно одномоментно наблюдать манипуляции ассистента и УЗ-изображение. После маркировки границ опухоли на сосуды накладывается зажим Сатинского или «бульдоги» (рисунок 5).
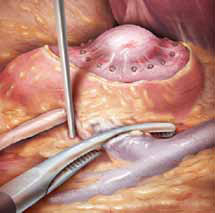
Рисунок 5. Роботическая резекция почки
При иссечении опухоли трехмерное изображение улучшает визуализацию. После иссечения опухоли производится ушивание ложа в два слоя (рисунок 6). При ушивании нижнего слоя, прежде всего, обращают внимание на сосуды, питавшие опухоль. Здесь можно использовать SurgiCell. Потом ушивается капсула почки, т.е. соблюдаются те же хирургические принципы, как и при открытой операции. С целью экономии времени в нашей клинике мы используем реабсорбируемые клипсы и клей SurgiFlo для дополнительного гемостаза перед ушиванием капсулы. Также применяем нить V loc, которая фиксирует сама себя, шов не распускается, благодаря специальным насечкам на нити, и скользящую клипсу Hem-O-Lok, которая также накладывается на нить V lok с двух сторон и не дает шву распускаться. Самым главным преимуществом данной техники является то, что можно затягивать шов,
сдвигая клипсу.
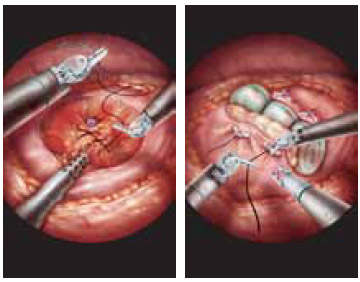
Рисунок 6. Ушивание ложа опухоли
Возможные осложнения операции:
- кровотечение, раннее и отсроченное;
- положительный хирургический край (вопрос о тактике при обнаружении положительного хирургического края вызывает больше всего дискуссий);
- длительная тепловая ишемия;
- подтекание мочи при повреждении собирательной системы;
- конверсия;
- нефрэктомия.
Много вопросов вызывает время ишемии. При малых опухолях можно не перекрывать кровоток совсем или открыть кровоток после ушивания первого слоя ложа опухоли. В любом случае следует стараться придерживаться 30-минутных рамок ишемии. Можно использовать различные агенты для гемостаза, а также микроволновой инструмент, который срезает ткани без существенной кровопотери. Еще одним преимуществом робота является возможность манипулирования под разными углами. При этом время ушивания ложа удаленной опухоли снижается при робот-ассистированной операции за счет подвижности манипуляторов и лучшего угла обзора, что опять же уменьшает время ишемии.
Что же касается стоимости робот-ассистированных операций, то в США Da Vinci стоит 1,5 млн долларов, инструменты на одну операцию – 1000 долларов. Конечно, это немало, но в плане стоимости улучшения результатов – бесценно.
Каков же основной посыл данного сообщения? Выполнять органосберегающие операции при стадии Т1, в любых возможных ситуациях, вне зависимости от методики (открыто, лапароскопически, при помощи робота). В США только 20% опухолей почки удаляются с помощью резекции, что же касается нашей клиники, то в 70% случаев мы выполняем органосберегающие операции. Резекция почки в настоящее время недооценена, поскольку легче выполнить нефрэктомию, чем резекцию. Как говорится в одном изречении: «…не будь первым, кто испытывает новое, но и не последним, кто откажется от старого». Мы должны расти в ногу со временем и развивающимися технологиями.
Ключевые слова: рак почки, робот-ассистированная хирургия, радикальная нефрэктомия, резекция почки.
Keywords: kidney cancer, robotic surgery, radical nephrectomy, partial nephrectomy.






