ВВЕДЕНИЕ
В настоящее время доступны различные техники выполнения радикальной простатэктомии (РПЭ). Лидирующую позицию занимает робот-ассистированная радикальная простатэктомия (РРПЭ), что обусловлено относительной низкой морбидностью данного вмешательства и коротким реабилитационным периодом. Важно не только излечить пациента от злокачественного заболевания, но и сохранить его привычный образ жизни. РПЭ относится к разряду тех операций, техника исполнения которых существенно определяет функциональные исходы – удержание мочи и эректильную функцию, в связи с чем хирургическая техника непрерывно совершенствуется.
При оценке функциональных результатов радикальной простатэктомии все шире используется понятие «пентафекты» (отсутствие периоперативных осложнений, отрицательный хирургический край, отсутствие биохимического рецидива, сохраненная эректильная функция и полное удержание мочи) [1].
Роботическая хирургия обеспечивает прецизионную технику операции и демонстрирует преимущество в отношении онкологических исходов и функциональных результатов [2, 3]. Однако, среди перенесших РРПЭ, имеет место значительная вариабельность показателей восстановления удержания мочи. По данным публикаций интерес хирургов смещаются в сторону поиска методик, обеспечивающих раннюю континенцию. В этом свете интерес представляет РРПЭ с сохранением Ретциева пространства.
МАТЕРИАЛЫ И МЕТОДЫ
В период с 2017 по 2018 гг. в клинике урологии и хирургической андрологии РМАНПО на базе 14 урологического отделения ГКБ им. С.П. Боткина 54 пациентам с клинически локализованной формой РПЖ выполнена нервосберегающая робот-ассистированная радикальную простатэктомия (НС-РРПЭ). В зависимости от примененной оперативной техники пациенты были разделены на две группы. Характеристика пациентов представлена в таблице 1.
Таблица 1. Характеристика пациентов по группам
Table 1. Patients features
| Показатель / Features | Группа I / Group I | Группа II / Group II |
|---|---|---|
| Количество пациентов Number of patients |
29 | 25 |
| Средний возраст, лет (M+SD)* Mean age, years (M+SD)* |
62,2+5,7 | 63,3+6,8 |
| Индекс массы тела (M+SD)* Body mass index (M+SD)* |
26,6+ 3,8 | 28,5+ 4,9 |
| МИЭФ-15, домен эректильной функции (M+SD) * IIEF-15, domain of erectile function (M+SD)* |
27,74+6,12 | 27,28+ 6,02 |
| Предоперационный уровень общего ПСА, нг/мл (Mo, 25% - 75% перцентиль)* Preoperative level of total PSA, ng/ml (Me, 25% - 75% percentile)* |
6,69 (5,1-8,8) | 6,54 (5,2-11,8) |
| Клиническая стадия Т, % Clinical stage T, % |
сТ1с -39,20 сТ2а - 31,05 сТ2в - 23,12 сТ2с - 6,63 |
сТ1с - 41,2 сТ2а - 33,83 сТ2в - 22,14 сТ2с - 2,83 |
Примечание, notes: *p> 0,05
Пациентам первой группы была выполнена НСРРПЭ с тотальным нервосбережением и сохранением Ретциева пространства. Во второй группе данная операция выполнялась по стандартной методике. Нервосберегающая техника применялась при условии сохранной эректильной функции (ЭФ). Все мужчины перед операцией были полностью континентными.
Функция удержания мочи оценивалась у пациентов перед операцией, далее через неделю после удаления уретрального катетера, а также спустя 1, 3, 6 и 12 месяцев после НС-РРПЭ. Полное удержание мочи определялось как отсутствие непроизвольного ее выделения в покое или при физической нагрузке с возможным использованием одной прокладки в сутки в качестве страховочной. Легкая степень стрессового недержания мочи (НМ) допускала использование 1-2 прокладок в сутки, средняя – трех, тяжелая – более трех прокладок в сутки.
Статистическая обработка данных проводилась с помощью компьютерных программ Microsoft Office Excel (2019, USA) и Graph Pad PrismVersion 8,0 (USA, 2018). Различия считали статистически достоверными при р<0,05.
Операционный материал для морфологического исследования фиксировали в 10% забуференном растворе формалина, далее заливали в парафин. Обработанные срезы окрашивались гематоксилином и эозином. Для визуализации нервных волокон и оценки их плотности выполнялось иммуногистохимическое исследование с использованием поликлональных антител к белку S100 (VENTANA, DAB), маркера клеток нейроэктодермального происхождения. Микропрепараты сканировали на гистоскане Ponoramic 3DHistotex.
РЕЗУЛЬТАТЫ
При гистологическом исследовании после НСРРПЭ с сохранением Ретциева пространства нервные волокна в псевдокапсуле предстательной железы(ПЖ) практически не определяются (рис. 1). При стандартной НС-РПЭ визуализируется минимальное количество нервных волокон, расположенных в псевдокапсуле (рис. 2).
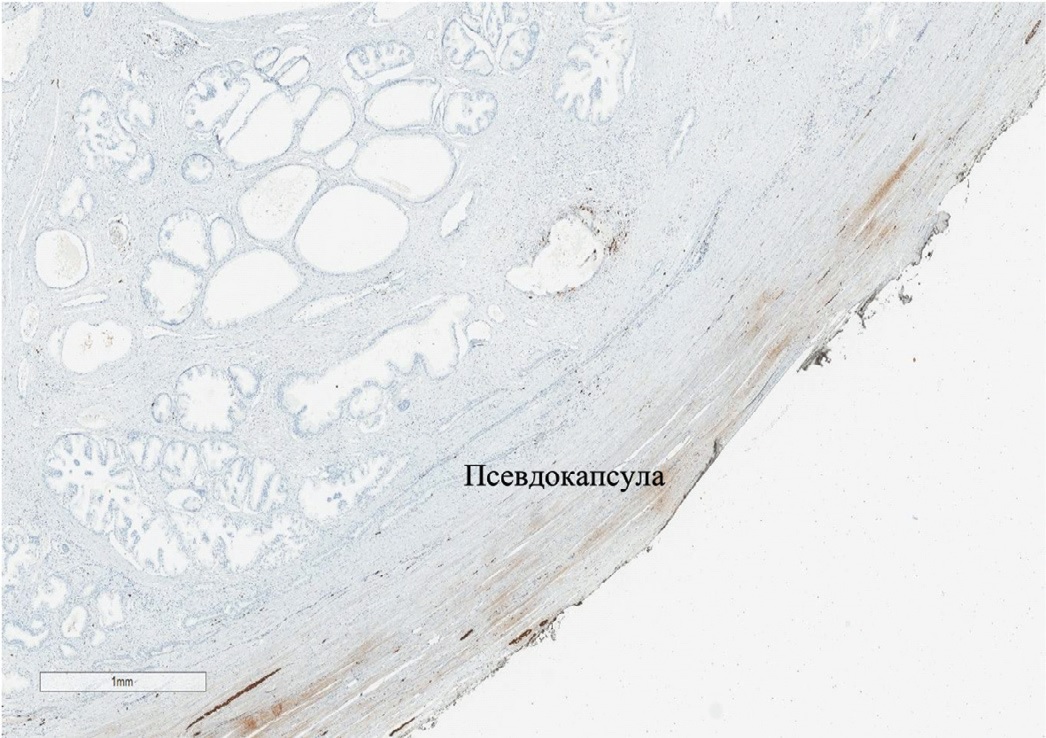
Рис. 1. Радикальная простатэктомия с сохранением Ретциева пространства. ИГХ, S100. Нервные волокна в псевдокапсуле практически не определяются
Fig. 1. Radical prostatectomy with preservation of the Retinal space, immunohystochemical study, S100. Nerve fibers in the pseudocapsule are almost undetectable

Рис. 2. Радикальная простатэктомия со стандартной техникой нервосохранения, ИГХ, S100. Плотность нервных волокон минимальная, составляет 1-2 на см длины окружности капсулы
Fig. 2. Radical nerve sparing prostatectomy with standard technique, immunohystochemical study, S100. The density of nerve fibers is minimal; it is 1-2 per cm of the capsule circumference
Через неделю после удаления уретрального катетера континентными были 54,13% и 41,81% прооперированных в первой и второй группе соответственно. Спустя месяц уровень континенции составил 68,12% и 59,21%, через 3 месяца этот показатель вышел на плато – 94,15% и 90,63% соответственно. Через 6 месяцев частота удержания мочи составила 98,54% и 97,12% больных, а спустя 9 месяцев – 98,62% и 97,31% соответственно. По окончании 12 месяцев наблюдения в первой группе удержание мочи отмечено у 98,83%, во второй – у 97,82%.
Таким образом, через 12 месяцев наблюдения у пациентов двух групп отмечено стрессовое НМ легкой степени (1,17%, vs 2,18 %, р<0,05). Стрессового НМ средней и тяжелой степени выраженности не зафиксировано.
ОБСУЖДЕНИЕ
Удержание мочи после операции является одним из основных функциональных результатов РПЭ, существенно влияющим на социальную реабилитацию.
Частота инконтиненции в первые месяцы после перенесенной операции варьирует в диапазоне 8-87%. В последующем этот показатель существенно снижается, достигая 3 – 10% [4]. Фокусируясь на анатомофункциональных взаимосвязях структур малого таза, становится возможным непрерывное совершенствование хирургической техники и, как следствие, улучшение функциональных результатов [5, 6].
В процессе хирургического вмешательства происходит разрушение анатомических структур, ответственных за удержание мочи. Условно их можно разделить на три группы:
- фиброзные (пубопростатические связки, волокна Ретциева пространства, фасция Денонвилье, уретропельвикальные связки, эндопельвикальная фасция, сухожильная дуга);
- мышечные (внутренний сфинктер уретры, шейка мочевого пузыря, наружный рабдосфинктер уретры, мембранозная уретра, мышцы тазового дна);
- сосудисто-нервные (половые нервы, тазовые соматические и автономные нижнего гипогастрального сплетения, включающие симпатические и парасимпатические волокна).
По результатам исследования фиброзных структур малого таза Z. Xu и соавт. описали несколько слоев. Передний представлен фиброзными волокнами, фиксированными к лонным костям. Средний – в дистальном направлении соединяется с фасцией дорсального венозного комплекса. Задний – формирует фиброзно-мышечный слой ПЖ, который заканчивается на уровне наружного рабдосфинктера [7].
Сфинктерный аппарат состоит из поперечнополосатых мышечных волокон наружного рабдосфинктера, гладкомышечных циркулярных и продольных элементов внутреннего сфинктера и поддерживающих мышечно-фасциальных компонентов. Прецизионная апикальная диссекция и лигирование дорсального венозного комплекса (ДВК) позволяет минимизировать повреждение сфинктерного аппарата и ассоциированных с ним фиброзно-мышечных структур.
Мембранозная уретра начинается от апекса ПЖ и проходит через диафрагму таза до уровня бульбозного отдела. Значимость длины мембранозной уретры подтверждена результатами многочисленных исследований [8-11].
К. Kitamura и соавт. проанализировали восстановление функции удержания мочи у 320 пациентов после РРПЭ и сообщили, что континенция была достигнута у 44%, 71%, 83% и 93% пациентов через 1, 3, 6 и 12 месяцев после удаления уретрального катетера соответственно. При этом, возраст, индекс массы тела и размер простаты не являлись статистически значимыми факторами восстановления удержания мочи. Напротив, длина мембранозной уретры была значимым фактором прогноза достижения континенции в ранние сроки после РРПЭ [11].
Понимание нейроанатомии ПЖ необходимо для оптимизации функциональных исходов РПЭ. Ряд клинико-морфологических работ продемонстрировал значимость сохранения фиброзных, мышечных и сосудисто-нервных структур, прилежащих к ПЖ, в том числе в области ДВК, для восстановления удержания мочи [12, 13].
С развитием хирургии органов малого таза и совершенствованием роботической хирургии, становится возможным сочетание стратегий сохранения и реконструкции анатомических структур, обеспечивающих континенцию (табл. 2).
Таблица 2. Возможности сохранения и реконструкции анатомических структур, обеспечивающих континенцию
Table 2. Possibilities of preservation and reconstruction of anatomical structures providing continuity
| Сохранение анатомических структур Preservation of anatomical structures |
Реконструкция Reconstruction |
|---|---|
|
Реконструкция передней полуокружности уретровезикального анастомоза,
Реконструкция задней полуокружности, Posterior semicircle reconstruction:
|
Сохранение анатомических структур перекликается с идеей реконструкции передней полуокружности уретровезикального анастомоза (УВА). Шейка и треугольник мочевого пузыря, внутренний уретральный сфинктер иннервируются норадренергическими симпатическими нервными волокнами гипогастрального и тазового сплетений, повышающих тонус гладкомышечных волокон, способствую удержанию мочи в фазу накопления [14].
Предложены различные техники сохранения шейки мочевого пузыря. М. Smolski и соавт. провели систематический обзор 33 исследований и показали, что сбережение шейки мочевого пузыря было связано как с более быстрым восстановлением континенции во все сроки наблюдения, так и с более низкой частотой стриктур УВА. При этом не отмечено статистически значимого увеличения частоты позитивного хирургического края [15].
E. Gazel и соавт. проанализировали частоту ранней континенции после РРПЭ с применением реконструктивных техник. В первой группе (n=60) пациентам была выполнена РРПЭ с сохранением шейки мочевого пузыря, во второй (n=60) – сочетание передней фиксации уретры и сбережения шейки мочевого пузыря. Восстановление континенции оценивалось на 7 день, а также через один, три и шесть месяцев после оперативного вмешательства. Через неделю и месяц после оперативного вмешательства частота восстановления удержания мочи была выше во второй группе. В первой группе в ранние сроки чаще отмечены постмикционные симптомы расстройства мочеиспускания. Однако при сравнительной оценке через 3 и 6 месяцев статистически значимой разницы между группами не отмечено. Таким образом, сочетание передней фиксации уретры и сохранения шейки мочевого пузыря увеличивает скорость восстановления удержания мочи и снижает выраженность постмикционных симптомов в ранние сроки после операции [16].
Нервы, имеющие отношение к механизмам удержания мочи, представлены тремя основными группами: половые, нервные волокна в составе сосудистонервных пучков (СНП), автономные ветви гипогастрального и тазового сплетений [17].
A. Takenaka и соавт. в своих работах показали присутствие сфинктерных ветвей половых нервов в дистальных отделах эндопельвикальной фасции интимно прилежащей к апексу ПЖ. Это обстоятельство подчеркивает важность прецизионной хирургической техники при апекальной диссекции и лигировании ДВК. Необходима минимизация повреждений нервных волокон и сохранение кровоснабжения мембранозной уретры [18].
Целесообразность сохранения СНП в восстановлении удержания мочи, особенно в ранние сроки после операции, доказана многочисленными исследованиями [19].
Y. Park и соавт. провели анализ восстановления континенции у мужчин с эректильной дисфункцией до операции. Сохранение СНП способствовало более быстрому возврату к континенции [20].
В соответствии со степенями нервосохранения, описанных A. Tewari и соавт., сбережение максимального количества нервов, в том числе в проксимальном направлении в области семенных пузырьков, связано со скоростью и качеством восстановления удержания мочи [21]. Возможно, это связано с сохранением симпатических волокон тазового сплетения, иннервирующих шейку мочевого пузыря и внутренний уретральный сфинктер [22].
Очевидно, что сохранение пубопростатических связок способствует стабилизации сфинктерного аппарата, то есть улучшает восстановление удержание мочи. Техника сбережения пубопростатических связок также сопряжена с селективным лигированием ДВК.
Y.Lei и соавт. опубликовали результаты исследования, которые показали, что через 5 месяцев после РПЭ у 303 пациентов, оперированных с применением методики селективного лигирования ДВК, частота континенции была выше в сравнении с группой 240 пациентов без применения таковой [23].
С развитием роботической хирургии и накоплением опыта, появляются различные методики реконструкции зоны УВА, что является продолжением идеи сохранения естественной анатомии малого таза. Реконструкция фасции Денонвилье и задней стенки мочевого пузыря является первоначальным шагом. Таким образом достигается поддержка и фиксация задней уретры [24].
Шов Rocco способствует большей стабилизации задней полуокружности УВА [25]. Тотальная анатомическая реконструкция предполагает сочетание методик. Фиксация сухожильного центра к шейке мочевого пузыря укрепляет переднюю полуокружность УВА [26].
В нашем исследовании совместно с клиническими морфологами был обнаружено, что при гистологическом исследовании после стандартной НС-РРПЭ отмечается минимальное количество нервных волокон на единицу поверхности в капсуле железы. После РРПЭ с сохранением Ретциева пространства нервные волокна в капсуле ПЖ практически не визуализируются. По результатам проспективного анализа через неделю после удаления уретрального катетера в первой группе мочу удерживали 54,13% больных, во второй - 41,81%, спустя месяц – 68,12% и 59,21% соответственно. Таким образом, статистически значимые различия в частоте удержания мочи отмечены в ранние сроки после НС-РРПЭ. Через 3 месяца уровень континенции вышел на плато и составил 94,15% и 90,63%, в первой и второй группе соответственно.
По данным литературы НС-РРПЭ с сохранением Ретциева пространства превосходит стандартную операцию по функциональным результатам, не компрометируя онкологические исходы. Частота удержания мочи составляет 70-92% по итогам первого месяца наблюдения [26, 27].
Преимущества РРПЭ с сохранением Ретциева пространства заключаются в укорочении времени операции посредством пропуска нескольких этапов (мобилизация мочевого пузыря, удаление поверхностного жира по передней поверхности ПЖ, вскрытие эндопельвикальной фасции, выделение и перевязка ДВК, реконструктивные приемы). Сохранение артерий в ДВК, как и добавочных половых артерий (встречающихся у 30% мужчин), возможно, приводит к лучшим функциональным результатами после операции. Сохранение СНП по задней поверхности ПЖ до их разветвления в латеральных направлениях уменьшает риск травматизации мелких ветвей, особенно в проксимальных отделах СНП [28].
ВЫВОДЫ
Углубление наших знаний анатомии малого таза и понимания функциональных механизмов удержания мочи после радикальной простатэктомии в сочетании техническими преимуществами роботической хирургией, позволяют совершенствовать методику ее исполнения. Комбинация оперативной техники с максимально возможным сохранением анатомических структур малого таза и их реконструкции при повреждении, позволяют минимизировать частоту недержания мочи после операции. В свете такого подхода НС-РРПЭ с применением техники сохранения Ретциева пространства может считаться обоснованной альтернативой стандартной технике, поскольку она демонстрирует преимущества в отношении частоты и скорости восстановления континенции.
ЛИТЕРАТУРА
1. Соколов Е.А, Велиев Е.И., Богданов А.Б., Велиев Р.А., Гончарук Д.А. Онкологическая безопасность нервосберегающей техники радикальной простатэктомии: оценка патоморфологических результатов и безрецидивной выживаемости. Урология 2020(2):60-64 [Sokolov E.A., Veliev E.I., Bogdanov A.B., Veliev R.A., Goncharuk D.A. Oncological safety of nerve-sparing radical prostatectomy: evaluation of histopathologicaloutcomes and recurrence-free survival. Urologiya = Urology 2020(2):60–64 (In Russian)]. https://dx.doi.org/10.18565/ urology.2020.2.60-64.
2. Велиев Е.И., Соколов Е.А., Лоран О.Б. Сравнительный анализ частоты позитивных хирургических краев у пациентов, перенесших роботассистированную или позадилонную радикальную простатэктомию по поводу рака предстательной железы. Урология 2015(4):44-47. [Veliev E. I., Sokolov E. A., Loran O. B. Comparative analysis of positive surgical margin rates in patients undergoing robotassisted or retropubic radical prostatectomy for prostate cancer. Urologiya = Urology 2015(4):44-47 (In Russian)].
3. Соколов Е.А., Велиев Е.И., Паклина О.В., Кнышинский Г.В. Интраоперационное гистологическое исследование замороженных срезов участков предстательной железы, прилегающих к сосудисто-нервному пучку: первичный опыт применения при робот-ассистированной радикальной простатэктомии. Вестник современной клинической медицины 2019;12(6):66–71. [Sokolov E.A., Veliev E.I., Paklina O.V., Knyshinsky G.V. Intraoperative histological frozen-section examination of prostate regions adjacent to neurovascular bundle: initial implementation experience during roboticassisted radical prostatectomy. Vestnik sovremennoj klinicheskoj mediciny = The Bulletin of Contemporary Clinical Medicine 2019;12(6):66-71 (In Russian)]. http://doi.org/10.20969/ VSKM.2019.12(6).66-71.
4. Xu AJ, Taksler GB, Llukani E, Lepor H. Long-term continence outcomes in men undergoing radical prostatectomy: a prospective 15-year longitudinal study. J Urol 2018;200(3):626-632. https://doi.org/10.1016/ j.juro2018.05.005.
5. Autorino R, Porpiglia F, Dasgupta P, Rassweiler J, Catto JW, Hampton LJ, et al. Precision surgery and genitourinary cancers. Eur J Surg Oncol 2017;43(5):893-908. http://doi.org/10.1016/j.ejso.2017.02.005.
6. Соколов Е.А., Велиев Е.И., Велиев Р.А. Современный взгляд на нервосберегающую технику радикальной простатэктомии. Онкоурология 2019;15(3):17-27. [Sokolov E.A., Veliev E.I., Veliev R.A. Current view on nerve-sparing radical prostatectomy. Oncourologiya = Cancer Urology 2019;15(3):17–27. (In Russian)]. http://doi.org/10.17650/1726-9776-2019-15-3-17-27
7. Xu Z, Chapuis PH, Bokey L, Zhang M. Nature and architecture of the puboprostatic ligament: a macro- and microscopic cadaveric study using epoxy sheet plastination. Urology 2017;110:263.e1-8. https://doi.org/10.1016/ j.urology.2017.08.018.
8. Mungovan SF, Sandhu JS, Akin O, Smart NA, Graham PL, Patel MI. Preoperative membranous urethral length measurement and continence recovery following radical prostatectomy: a systematic review and meta-analysis. EurUrol 2017(71):368-78. https//doi.org/10.1016/ j.eururo.2016.06.023.
9. Song W, Kim CK, Park BK, Jeon HG, Jeong BC, Seo SI, et al. Impact of preoperative and postoperative membranous urethral length measured by 3 Tesla magnetic resonance imaging on urinary continence recovery after robotic-assisted radical prostatectomy. Can Urol Assoc J 2017;11(3-4):E93- E99. https://doi.org/10.5489/cuaj.4035.
10. Ko YH, Huynh LM, See K, Lall C, Skarecky D, Ahlering TE. Impact of surgically maximized versus native membranous urethral length on 30-day and long-term pad-free continence after robot assisted radical prostatectomy. Prostate Int 2020;8(2):55–61. https://doi.org/10.1016/ j.prnil.2019.12.005
11. Kitamura K, China T, Kanayama M, Nagata M, Isotani S, Wakumoto Y, et al. Significant association between urethral length measured by magnetic resonance imaging and urinary continence recovery after robot assisted radical prostatectomy. Prostate Int 2019;7(2):54–59. https://doi.org/10.1016/ j.prnil.2018.06.003.
12. Arroyo C, Martini A, Wang J, Tewari AK. Anatomical, surgical and technical factors influencing continence after radical prostatectomy. Ther Adv Urol 2019;8(11):1756287218813787. https://doi.org/10.1177/1756287218813787.
13. Sridhar AN, Abozaid M, Rajan P, Sooriakumaran P, Shaw G, Nathan S, et al. Surgical techniques to optimize early urinary continence recovery post robot assisted radical prostatectomy for prostate cancer. Curr Urol Rep 2017;18(9):71-79. http://doi.org/10.1007/s11934-017-0717-4.
14. Zattoni F, Artibani W, Patel V, Montorsi F, Porpiglia F, Hampton LJ, et al. Technical innovations to optimize continence recovery after robotic assisted radical prostatectomy. Minerva Urol Nefrol 2019(71):324-38. https://doi.org/10.23736/S0393-2249.19.03395-2.
15. Smolski M, Esler RC, Turo R, Collins GN, Oakley N, Brough R. Bladder neck sparing in radical prostatectomy. Indian J Urol 2013;29(4):338- 44. http://doi.org/10.4103/0970-1591.120118.
16. Gazel E, Kaya E, Acikgoz O, Yalcin S, Yilmaz S, Aybal C, Tunc L. The effects of bladder neck sparing with an additional anterior urethral fixation on postoperative continence after robot-assisted radical prostatectomy. North Clin Istanb 2020 24;8(1):57-62. http://doi.org/10.14744/ nci.2020.00533.
17. Sridhar AN, Abozaid M, Rajan P, Sooriakumaran P, Shaw G, Nathan S, et al. Surgical techniques to optimize early urinary continence recovery post robot assisted radical prostatectomy for prostate cancer. Curr Urol Rep 2017;18(9):71-8. http://doi.org/10.1007/s11934-017-0717-4.
18. Takenaka A, Hara R, Soga H, Murakami G, Fujisawa M. A novel technique for approaching the endopelvic fascia in retropubic radical prostatectomy, based on an anatomical study of fixed and fresh cadavers. BJU Int 2005(95):766-71. http://doi.org/10.1111/j.1464-410X.2005.05397.x.
19. Reeves F, Preece P, Kapoor J, Everaerts W, Murphy DG, Corcoran NM, Costello AJ. Preservation of the neurovascular bundles is associated with improved time to continence after radical prostatectomy but not longterm continence rates: results of a systematic review and meta-analysis. Eur Urol 2015;68(4):692-704. htts://doi.org/10.1016/j.eururo.2014.10.020.
20. Park YH, Kwon OS, Hong SH, Kim SW, Hwang TK, Lee JY. Effect of nerve-sparing radical prostatectomy on urinary continence in patients with preoperative erectile dysfunction. Int Neurourol J 2006(20):69-74. http://doi.org/10.5213/inj.1630428.214.
21. Tewari AK, Srivastava A, Huang MW, Robinson BD, Shevchuk MM, Durand M, et al. Anatomical grades of nerve sparing: a risk-stratified approach to neural-hammock sparing during robot-assisted radical prostatectomy (RARP). BJU Int 2011;108(6 Pt 2):984-92. http://doi.org/10.1111/ j.1464-410X.2011.10565.x.
22. Srivastava A, Chopra S, Pham A, Sooriakumaran P, Durand M, Chughtai B, et al. Effect of a risk-stratified grade of nerve-sparing technique on early return of continence after robot-assisted laparoscopic radical prostatectomy. Eur Urol 2013;63(3):438-44. https://doi.org/10.1016/ j.eururo.2012.07.009.
23. Lei Y, Alemozaffar M, Williams SB, Hevelone N, Lipsitz SR, Plaster BA, et al. Athermal division and selective suture ligation of the dorsal vein complex during robot-assisted laparoscopic radical prostatectomy: description of technique and outcomes. Eur Urol 2011(59):235-43. https://doi.org/10.1016/j.eururo.2010.08.043.
24. Martini A, Tewari AK. Anatomic robotic prostatectomy: current best practice. Ther Adv Urol 2019(11):1756287218813789. http://doi.org/10.1177/1756287218813789.
25. Rocco B, Gregori A, Stener S, Santoro L, Bozzola A, Galli S, et al. Posterior reconstruction of the rhabdosphincter allows a rapid recovery of continence after transperitoneal video laparoscopic radical prostatectomy. Eur Urol 2007;51(4):996-1003. https://doi.org/10.1016/ j.eururo.2006.10.014.
26. Lim SK, Kim KH, Shin TY, Han WK, Chung BH, Hong SJ, et al. Retzius-sparing robot-assisted laparoscopic radical prostatectomy: combining the best of retropubic and perineal approaches. BJU Int 2014(114):236–244. http://doi.org/10.1111/bju.12705.
27. Sayyid RK, Simpson WG, Lu C, Terris MK, Klaassen Z, Madi R. Retzius-sparing robotic-assisted laparoscopic radical prostatectomy: a safe surgical technique with superior continence outcomes. J Endourol 2017;31(12):1244–1250. http://doi.org/10.1089/end.2017.0490.
28. Eden CG. Retzius-sparing robotic radical prostatectomy. Asian Journal of Andrology 2020;22(2):149-151. http://doi.org/10.4103/aja.aja_82_19.







