Несмотря на большое количество исследований многие аспекты этиологии, патогенеза, диагностики и терапии бактериального простатита (БП) окончательно не установлены. Длительное время бактериальные патогены семейства Enterobacteriaceae рассматривались в качестве основных возбудителей БП. В актуальных публикациях, посвященных микробиологической оценке секрета предстательной железы (СПЖ) с использованием расширенного набора питательных сред и специальных условий культивирования, а также методов молекулярно-биологической диагностики (ПЦР), приводятся данные свидетельствующие о значительном увеличении удельного веса бактериальных патогенов из дебатируемого кластера, идентифицированных в эксприматах предстательной железы (ПЖ), а именно неклостридиальных анаэробных бактерий и коагулазоотрицательных стафилококков. Помимо этого, в нескольких крупных работах приводятся данные об этиологической принадлежности внутриклеточных патогенов к формированию синдрома хронической тазовой боли/хроническому простатиту (СХТБ/ХП IIIa, NIH NIDDK 1995), что позволяет рассматривать эту нозологию в плоскости бактериального простатита II категории (NIH NIDDK 1995) [1-4]. Ко всему прочему, бактериальная колонизация ПЖ и индуцируемый ею острый/хронический воспалительный процесс в настоящее время рассматривается не только как этиологическая причина развития бактериального простатита, дебатируется вопрос о предиктивной или триггерной роли бактерий в формировании доброкачественной простатической обструкции/доброкачественной гиперплазии предстательной железы и рака ПЖ [5-7].
«Золотым стандартом» диагностики хронического бактериального простатита (ХБП) остается проба MearesStamey (ПМС), хотя в качестве альтернативы предлагается выполнение препостмассажного теста Nickel (ППМТ). Однако эти методы диагностики не применимы при остром бактериальном простатите (ОБП) и необходимо производить анализ 1 и 2 порций мочи (ПМ) [8]. В дополнение к этому, отсутствие консенсуса о валидном титре идентифицированных в биоматериале от пациентов уропатогенов, на основании которых производится дифференциальная диагностика ХБП и других нозологических форм (в частности, уретрита, СХТБ/ХП, цистита и т.д.), а также определяется терапевтическая тактика, затрудняет адекватную интерпретацию лабораторных данных. Согласно различным литературным источникам диагностический уровень бактерий в ПМ-1, ПМ-2, СП или ПМ-3 (в зависимости от выбранного метода диагностики – ПМС/ППМТ), определяющий формулировку диагноза (БП I или II категорий, NIH NIDDK 1995), окончательно не установлен и варьируется в публикациях от 104 – 105 КОЕ/мл, либо основывается на 10-ти кратных различиях показателей между ПМ2 и СП/ПМ3. С другой стороны, известно, что практикующими врачами экспоненты ≤103 КОЕ/мл, особенно в отношении представителей дебатируемых штаммов микроорганизмов, для диагностики ОБП и ХБП вообще не учитываются [9-11].
Цель исследования. Сравнить бактериологические и морфологические особенности развития и течения патологического процесса в ПЖ при ее трансуретральном инфицировании низкими титрами каузативных и дебатируемых штаммов микроорганизмов при экспериментальном моделировании бактериального простатита.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Дизайн исследования разработан в соответствии с рекомендациями ARRIVE; описание экспериментальной части основано на чек-листе проверки качества экспериментальных исследований [12-13].
Этическое заявление. Экспериментальное исследование с использованием лабораторных животных одобрено Локальным независимым этическим комитетом (ЛНЭК) ФГБОУ ВО РостГМУ Минздрава России (протокол № 16/17 от 05.10.2017г.) после ознакомления с предоставленными материалами дизайна и плана эксперимента.
Разработка и проведение клинической части эксперимента основано на положениях, статьях и требованиях, отраженных в международных и отечественных документах и руководствах (согласно рекомендациям Rus-LASA) [14-16].
Лабораторные животные (ЛЖ): 20 половозрелых кроликов-самцов породы «New Zealand рода Oryctolagus cuniculus» массой 3,7±0,4 кг и возрастом 28±2 нед. Содержание ЛЖ в условиях вивария отвечало санитарно-эпидемиологическим и гигиеническим нормам, в соответствии с ГОСТ 33215-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур» и ГОСТ 33216 – 2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами» [17-18]. Срок адаптации ЛЖ перед началом исследования – 7 дней.
Экспериментальные штаммы: E. сoli (штамм №32), S. haemolyticus (штамм № 28), Peptococcus niger (штамм № 7) идентифицированные в СП, полученного путем проведения пробы Meares-Stamey, у пациентов с диагнозом – хронический бактериальный простатит II категории (NIH-NIDDK, 1995). В соответствии с разработанной методикой проводили посев материала на расширенный набор питательных сред (патент RU 2452774 C1 № 2011103414/10 от 31.01.2011) [19]. Условия культивирования идентифицированных штаммов: 1) Е. coli, S. haemolyticus – в Tryptic-soy Вroth при (t-37оС) в течение 12 часов перед проведением инокуляции; 2) Peptococcus niger – в Tryptic-soy Вroth при (t-37оС) в анаэробных условиях в течение 24-36 часов проведением инокуляции. Накануне эксперимента производили титрование культур в фосфатно-буферном растворе методом серийных разведений до достижения концентраций 1x103 КОЕ/мл, преаналитический период проведен в соответствии с описанной методикой [20].
Рандомизация. С целью редуцирования ошибок отбора (selection bias), которые бы ухудшали качество проведения эксперимента, ЛЖ по истечении адаптационного срока были рандомно разделены на 5 групп по 4 особи в зависимости от используемого титра микроорганизмов: группа 1 – Е.сoli 1 x 103 КОЕ/мл, группа 2 – S. haemolyticus 1 x 103 КОЕ/мл, группа 3 – Peptococcus niger 1 х 103 КОЕ/мл, группа 4 (контрольная) – Sol. NaCl 0,9%.
Экспериментальное моделирование бактериального простатита. Трансуретральная методика воспроизведения БП разработана и апробирована в серии пилотных экспериментов. Техника инфицирования: в фиксированном положении ЛЖ на спине под общим обезболиванием посредством модифицированного уретрального катетера Foley осуществляли топическую инокуляцию 0,5 мл в простатический отдел уретры. Для снижения степени диссеминации инфектанта в ретроградном направлении симультантно баллончиком катетера производилась изоляция нижних мочевых путей на уровне шейки мочевого пузыря. Время экспозиции инокулята в простатической уретре – 30 минут; после удаления катетера производили повторное обезболивание. В течение 2 часов каждые 15 минут после оперативного вмешательства производилась регистрация витальных показателей ЛЖ, после чего его перемещали в виварий.
С целью предотвращения систематических ошибок при уходе и наблюдении за ЛЖ разных групп (performance bias) путем присвоения индивидуального идентификационного кода для каждой особи производилось ослепление обслуживающего персонала и основных участников эксперимента.
Вивисекцию ЛЖ в каждой группе выполняли на 1, 3, 7, 14 контрольные сутки наблюдения. Эвтаназию ЛЖ осуществляли путем интракардиальной инъекции Sol. Lidocaini 2% под предварительным общим обезболиванием. Послойный доступ в брюшную полость и органам таза осуществляли посредством срединной лапаротомии. Кишечник перевязывали и удаляли единым блоком, все крупные магистральные сосуды, семявыносящие протоки и мочеточники лигировали, после чего выполняли переднюю тазовую эвисцерацию органокомплекса, представленного мочевым пузырем, простатическим комплексом и мембранозной уретрой.
Формирование биоптатов. Из компаративных участков органокомплекса по разработанным схемам осуществляли формирование 6 блок-биоптатов для бактериологического исследования и 3 продольных срезовых биоптата для морфологического оценки. Каждый биоптат маркировался и получал индивидуальную кодировку с целью ангажированности и исключения ошибок детекции (detection bias) у персонала, выполняющего бактериологическое и морфологическое исследования.
Бактериологическое исследование. Биоптаты подвергали гомогенизации в аппарате механической дезагрегации BDTM Medimachine System («Becton, Dickinson and Company, BD Biosciences», США) в течение 15 мин с 10 мл фосфат-буферного раствора. Далее методом серийных разведений выполняли 10-кратную дилюцию гомогената. Посев полученных образцов производили на плотную питательную среду MacConkey Agar («HiMedia», Индия) с последующей инкубацией в термостате ТС-1/80 СПУ («Смоленское СКТБ СПУ», РФ) при 37оС в течение суток.
Морфологическое исследование.Фиксацию биоптатов осуществляли путем экспозиции в 10% розовом нейтральном забуференном формалине («БликМедиклПродакшн», РФ) в течение 2 суток. Впоследствии препараты обезвоживали, уплотняли, микротомировали по стандартным методикам. Окраска осуществляли Hematoxylineosin («БликМедиклПродакшн», РФ). Оценку и регистрацию морфологических изменений проводили с помощью прямого светового микроскопа Leica DM1000 («Leica Microsystems », Германия) и цифровой камеры Leica ICC50 E 5.0 Mpx («Leica Microsystems», Германия) в увеличении 10х, 40х и 100х.
Статический анализ. Обработку данных проводили с помощью пакетов прикладных программ Microso Excel Office 365 («Microso», США) и Statistica 10.2 («StatSo Inc.», США). Описательная статистика количественных признаков представлена в виде центральной тенденции медианы (Me) и интерквартильного размаха (25 и 75 процентили), верхних и нижних пределов (min-max), а также среднего (M) и стандартного отклонения среднего (m). В тексте представлено как Ме [LQ; UQ]; min-max и M ± m.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При выполнении экспериментальной работы отмечена летальность у 1 ЛЖ на этапе вводного наркоза. Согласно результатам эксплоративных вивисекций составлена схема анатомического взаимоотношения нижних мочевых путей и внутренних половых органов ЛЖ (рис. 1).
Бактериологическое исследование. Посредством трансуретральной методики воспроизведения рефлюксогенного БП удалось достичь контаминации тканей внутренних половых органов ЛЖ во всех случаях наблюдения (табл. 1)
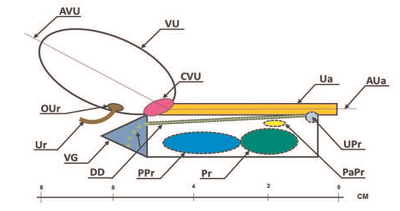
Рис. 1. Схематическое отображение макропрепарата нижних мочевых и внутренних половых органов ЛЖ: латеральный вид. Простатический комплекс: Pr – простата + PPr – пропростата +; PaPr парапростата; DD – семявыносящий проток; OUr – устье мочеточника; UPr – простатическая маточка; Ur – мочеточник; Ua – уретра; AUa – ось уретры; VU – мочевой пузырь; AVU – ось мочевого пузыря; СVU – шейка мочевого пузыря. Представленные данные соотносятся с литературными [19]
Fig. 1. Schematic representation of the lower urinary and internal genital organs macrospecimen of laboratory animals: lateral view. Prostatic complex: Pr prostate + PPr proprostate +; PaPr paraprostate; DD vas deferens; OUr – ureter`s ostium; UPr prostatic uterus; Ur ureter; Ua urethra; AUa – the axis of the urethra; VU bladder; AVU the axis of the bladder; CVU bladder neck. The data presented are correlated with publication` s materials [19]
Таблица 1. Результаты бактериологического исследования биоптатов тканей экспериментальных групп (1-3) лабораторных животных (интегративные показатели)
Table 1. The prostate and lower urinary tract biopsy samples` microbial load of experimental groups (1-3) of laboratory animals (integrative indicators)
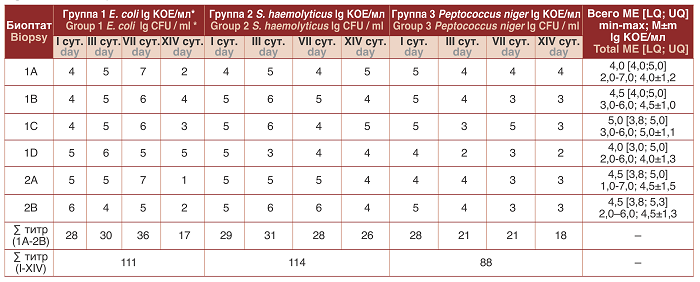
Примечания: 1) Биоптаты: 1А – дистальная ПЖ с семенным бугорком; 1В - проксимальная ПЖ + дистальная проПЖ; 1С – проксимальная проПЖ; 1D – параПЖ; 2А – мембранозная уретра; 2В – шейка мочевого пузыря. 2) I, III, VII, XIV – 1, 3, 7, 14 сутки эксперимента соответственно. * - lg КОЕ/мл – десятичный логарифм КОЕ/мл
Notes: 1) Biopsy specimens: 1A - distal prostate with seminal tubercle; 1B - proximal prostate + distal proprostate; 1C - proximal proprostate; 1D - paraprostate; 2A - membranous urethra; 2B –bladder neck. 2) I, III, VII, XIV - Experiment days 1, 3, 7, 14, respectively. * - log CFU / ml - decimal logarithm CFU / ml
Наивысший интегральный показатель бактериальной обсемененности отмечен в группе 2, соизмеримые результаты бактериологического исследования получены в группе 1. В группе 3 экспонент микробной нагрузки был в ~1,3 меньше, чем группах 1 и 2. Интерпретировать данные показатели можно путем сопоставления факторов патогенности использованных в эксперименте таксонов микроорганизмов с результатами бактериологического исследования [7].
Установлено, что максимальная микробная нагрузка имеет место в группе 1 на 7 сутки, в группе 2 – на 3 сутки и в группе 3 – на 1 сутки. При этом в группе 1 отмечен номинальный прогредиентный тренд нарастания титров от 1 к 7 суткам, в группе 2 – колебания суммапных титров с 1 по 7 сутки незначительны, в группе 3, напротив, определено снижение от 1 к 3 суткам, сохраняющееся с 3 по 7 сутки на одном совокупном показателе, однако, при детальном анализе результатов в группе 3 установлено, что на 3 сутки экспонента контаминации определена на уровне 4,0 [3,3; 4,0]; 2,0 – 4,0 КОЕ/мл, а к 7 суткам, в свою очередь, эти показатели снизились до градации 3,0 [3,0; 3,8]; 3,0 – 5,0 КОЕ/мл. Тем не менее, во всех группах к 14 суткам зарегистрировано общее снижение показателей обсемененности ткани до минимальных групповых значений, что свидетельствует о наличии общей тенденции течения инфекционно-воспалительного процесса в рамках данного эксперимента (рис. 2).
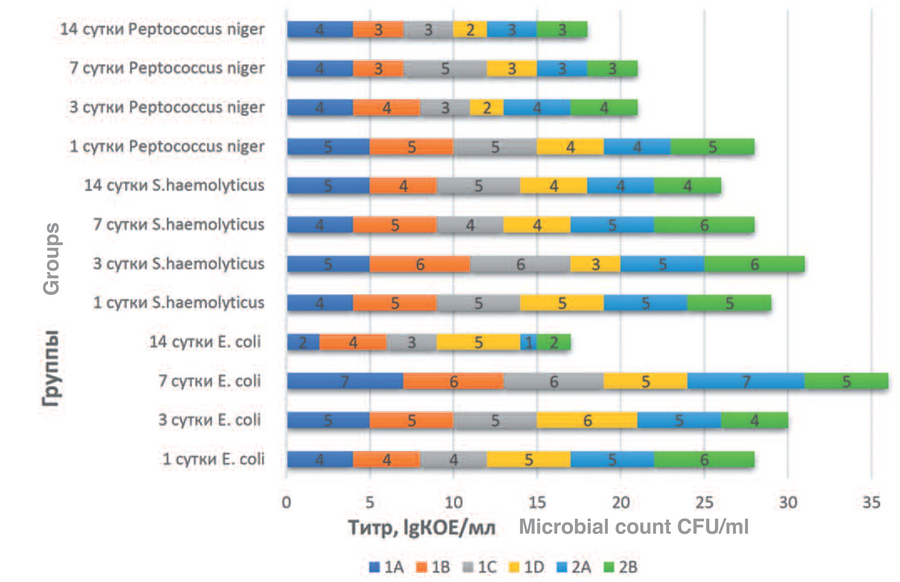
Рис. 2. Посуточные показатели обсеменённости биоптатов тканей органокомплекса
Fig. 2. Microbial load of biopsies from organ complex tissues, daily indicators
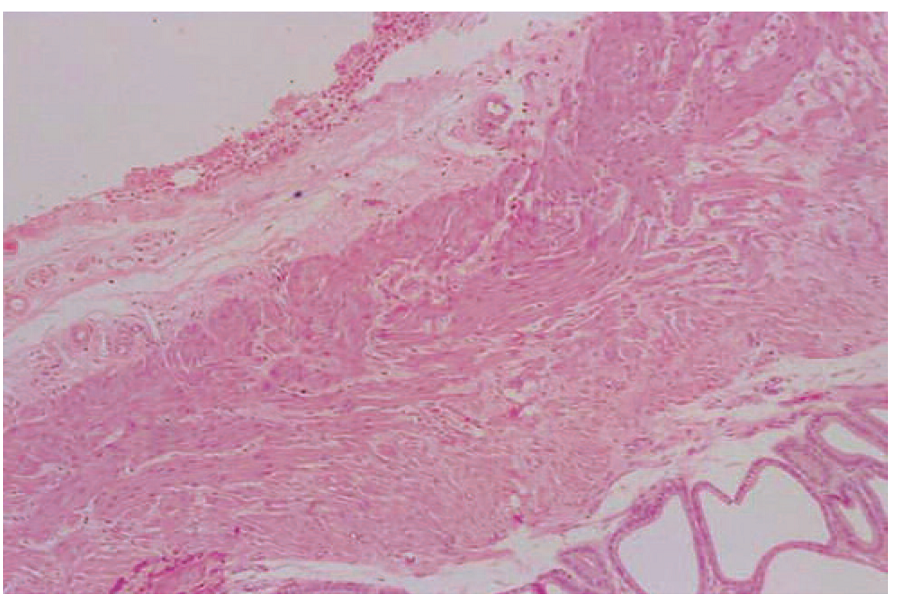
Рис. 2.1. Группа 1, 1 сутки. Участок ткани ПЖ в непосредственной близости от семенного бугорка. Умеренно выраженное гнойное воспаление с очагами некроза клеток, неравномерная умеренная эктазия желёз ПЖ и параПЖ, отек их стромы, реактивная гиперемия сосудов. Окраска: гематоксилин-эозин. Ув. 40х
Fig. 2.1. Group 1, day 1. Prostate area in the near of the seminal tubercle. Moderately expressed purulent inflammation with foci of cell necrosis, uneven moderate ectasia of the prostate and paraprostate glands, edema of their stroma, reactive hyperemia of the vessels. Strain: Hematoxylin-eosin. Magn. 40x
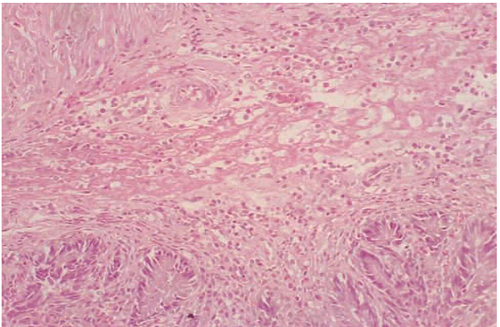
Рис. 2.2. Группа 1, 7 сутки. Диффузные фокусы дистрофии в интерстиции, некротические изменения эпителия желёз простатического комплекса и реактивный отек стромы желез, полнокровие микроциркуляторного русла, дезинтеграция стромальной ткани. Окраска: гематоксилин-эозин. Ув. 100х
Fig. 2.2. Group 1, day 7. Diffuse dystrophy foci in the interstitial tissue, necrotic changes in the epithelium of the glands of the prostatic complex and reactive edema of the glands` stroma, hyperaemia of the microcirculatory channels, disintegration of stromal tissue. Strain: Hematoxylin-eosin. Magn. 100x
При оценке экспонентов микробной обсемененности биоптатов наивысший титр отмечен в локусе ткани, соответствующем топической дислокации проксимальной части пропростаты (1С) и составил 5,0±1,1 lgКОЕ/мл (ДИ 4,1 – 5,9, α=0,05). Необходимо подчеркнуть, что бактериальная нагрузка всех биоптатов тканей зафиксирована на уровне 4,5±0,4 lgКОЕ/мл (ДИ 4,2 – 4,8, α=0,05).
Таким образом, посредством топической инокуляции инфектанта в простатический отдел уретры достигнута относительно равномерная обсемененность тканей простатического комплекса. Парадоксальным является тот факт, что локус с наибольшими интегральными показателями бактериального роста, проксимальная проПЖ (1С), располагается на значительном удалении от «точки входа» инокулята в ткани простатического комплекса на месте слияния выводных протоков желез – семенного бугорка и простатической маточки, а с наименьшим – в локусах, соответствующих биоптатам дистальной ПЖ и параПЖ (1А и 1D) – участкам, прилегающим к вышеперечисленным конклюзивным экскреторным структурам. Компрессивный рефлюкс бактериальной взвеси через вышепредставленные анатомические структуры в простатический комплекс имитирует один из основных патогенетических механизмов формирования бактериального простатита. Однако, вызывает определенный интерес тот факт, что распространение патогена per continuitatem от дистальной части ПЖ к проксимальной части проПЖ не вызывает выраженной тканевой иммунной реакции в ответ на внедрение бактериального флогогена, препятствующей развитию инфекционного процесса. В противоположность этому, в серии предшествующих экспериментов по трансуретральной селективной инокуляции каузативного уропатогена E.coli с применением вышеуказанной методики была определена обратная тенденция – наиболее релевантные интегративные показатели обсемененности тканей определены в зоне дистальной части ПЖ и параПЖ (1A и 1D) – анатомических структурах, располагающихся в непосредственной близости от семенного бугорка и простатической маточки.
Опираясь на эти данные проведен сепаратный анализ каждой из групп, который показал, что в группе 1 максимальный уровень бактериальной обсемененности определен в биоптате 1D (5,3±0,5 lgКОЕ/мл), в группе 2 – в биоптатах 1В и 1С (5,0±0,8 lgКОЕ/мл) и в группе 3 – в биоптате 1А (4,3±0,5 lgКОЕ/мл). В свою очередь, в группах 2 и 3 минимальные показатели бактериальной контаминации определены в биоптатах 1D (4,0±0,8 lgКОЕ/мл и 2,8±1,0 lgКОЕ/мл соответственно), тогда как в группе 1 – в биоптате 1А (4,0±2,0 lgКОЕ/мл) (табл. 2).
Таким образом, закономерность распределения показателей бактериальной контаминации может быть связана с особенностями клеточной и гуморальной тканевой иммунной реакции в ответ на внедрение бактериальных флогогенов, имеющих различный компартмент факторов патогенности и вирулентный потенциал. Ко всему прочему, железы простатического комплекса и, в особенности, железистые структуры в области семенного бугорка и простатической маточки, также вырабатывают секрет, который (по аналогии с СП у мужчин) должен обладать антимикробной активностью и подавлять деление бактерий в данной области. С другой стороны, можно предположить, что все-таки, существуют выводные протоки проПЖ в области, расположенной дистальнее шейки мочевого пузыря, соединяющие ее непосредственно с просветом простатического отдела уретры, посредством которых происходит колонизация бактериями ткани органа.
Таблица 2. Результаты бактериологического исследования биоптатов тканей (погрупповые показатели)
Table 2. The results of bacteriological study of tissues` biopsy samples (group indicators).
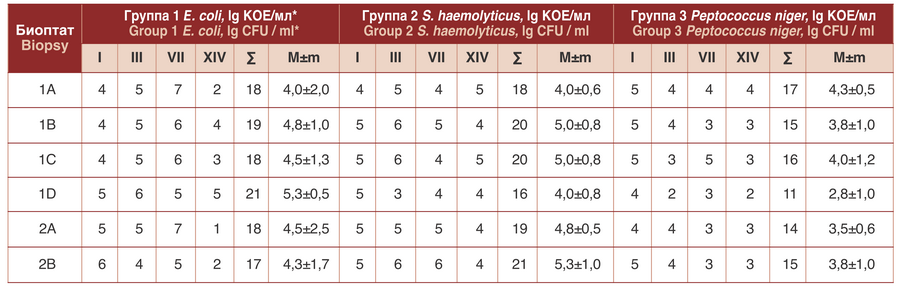
Примечания: 1) Биоптаты: 1А – дистальная ПЖ с семенным бугорком; 1В - проксимальная ПЖ + дистальная проПЖ; 1С – проксимальная проПЖ; 1D – параПЖ; 2А – мембранозная уретра; 2В – шейка мочевого пузыря. 2) I, III, VII, XIV – 1, 3, 7, 14 сутки эксперимента соответственно. * - lgКОЕ/мл – десятичный логарифм КОЕ/мл
Notes: 1) Biopsy specimens: 1A - distal pancreas with seed tubercle; 1B - proximal pancreas + distal proPZh; 1C - proximal proPJ; 1D - parasite 2A - membranous urethra;2B - the neck of the bladder. 2) I, III, VII, XIV - 1, 3, 7, 14 days of the experiment, respectively. * - log CFU / ml - decimal logarithm CFU / ml
В группе 4 (группа контроля) идентифицирован рост резидентной, преимущественно неклостридиальной анаэробной микрофлоры (Propionibacterium spp., Eubacterium spp., Bacteroides spp., Peptostreptococcus spp. и т.д.), представленной как в моноварианте, так и в виде микробных поликомпонентных ассоциаций в титрах от 101 – 104 КОЕ/мл.
Патоморфологическое исследование. Результаты гистологического исследования показали наличие релевантных воспалительных изменений в биоптатах во всех случаях.
Так, на 1 сутки после инфицирования E.coli 103КОЕ/мл в стенке семенного бугорка и окружающей его ткани ПЖ и параПЖ идентифицировано умеренно выраженное гнойное воспаление с очагами некроза клеток, неравномерная умеренная эктазия желез ПЖ и параПЖ, отек их стромы с отложением в ней фибрина, а также полнокровие сосудов с набуханием клеток эндотелия; в клеточном инфильтрате преобладают нейтрофилы с участками скоплений эозинофилов (рис. 2.1). К 3 сутками в ткани ПЖ и параПЖ определено выраженное гнойное воспаление с развитием мелких диффузных фокусов дистрофии, сопровождающееся некротическими изменениями эпителия желез ПЖ и параПЖ, а также значительным полнокровием микроциркуляторного русла с участками десквамации эндотелия сосудов. В динамике на 7 сутки отмечены симилярные гистологические изменения с увеличением количества гнойно-деструктивных очагов в поле зрения, максимально выраженным отеком стромы желез ПЖ и параПЖ и резкой плеторой окружающих питающих сосудов; при этом в некоторых участках нейтрофильно-эозинофильный состав инфильтрата сменяется на лимфо-гистиоцитарный (рис. 2.2). На 14 сутки в препаратах визуализированы изменения, характерные для перехода экссудативной в пролиферативную фазу воспаления, а именно извитость желез ПЖ, в просветах которых определено наличие амилоидных телец, а в строме, окружающей железы ПЖ, отмечено формирование мелких фокусов колликвационного некроза и появление участков ремоделирования тканей, сопровождающее пролиферацией рыхлой волокнистой соединительной ткани; клеточный состав имеет смешанную структуру с наличием участков умеренной лимфо-гистиоцитарной инфильтрации с плазматическими клетками, преобладающими, в первую очередь, в эпителиальных структурах, а также диффузных очагах нейтрофильно-макрофагальной инфильтрации; при этом во всех участках препарата сохранялось умеренное полнокровие сосудов и отек интерстиция.
В группе 2 после инфицирования S. haemolyticus 103 КОЕ/мл определены симилярные по отношению к группе 1 гнойно-некротические изменения тканей простатического комплекса. На 1 сутки в ткани простатического комплекса определены выраженная гиперемия сосудов микроциркуляторного русла, отек стромальной ткани, в просвете желез семенного бугорка – лизис эпителиальных клеточных элементов, в стенке желез – клеточная инфильтрация представленная эозинофильными гранулоцитами с признаками дегрануляции; в интерстиции и прилежащих простатических железах – фокусы коагуляционного некроза, в просвете желез простатического комплекса визуализированы скопления гранулоцитов с эозинофильно-нейтрофильным клеточным составом, белковые массы и единичные палочковидные структуры (бактерии) (рис 3.1). В динамике на 3 сутки сохраняется отек интерстиция ПЖ с формированием очагов гнойно-деструктивных изменений, полнокровие капилляров сосудистой сети, в строме структур простатического комплекса вокруг желез идентифицированы смешанные фокальные нейтрофильно-лимфоцитарные инфильтраты, в просвете этих желез – белковые массы с выраженной эозинофилией (рис. 3.2). К 7 суткам отмечено персистирование отека интерстициальной ткани, и гиперемия сосудов микроциркуляторного русла, фокусы колликвационного некроза в межуточном веществе, окружающем железы простатического комплекса; в этих железах определены дистрофические изменения клеток железистого эпителия, в их просвете – амилоидные корпускулы различного размера с выраженной эозинофилией; определена инициальная смена клеточного инфильтрата с появлением диффузных участков лимфо-плазмацитарных скоплений. На 14 сутки сохраняется выраженный отек стромы и реактивная дилятация сосудов микроциркуляторного русла, в подслизистой оболочке, прилежащей к железам простатического комплекса и отделяющей их от эпителиальной выстилки семявыносящего протока, визуализированы фокусы разрастания рыхлой волокнистой соединительной ткани; на значительном протяжении микропрепарата просветы альвеолярных структур простатического комплекса эктазированы, заполнены конгломератами, состоящими из белковых эозинофильных масс, лизированных клеток и очаговых скоплений бактерий, клеточный состав инфильтрата имеет смешанный характер и представлен, в основном макрофагальными элементами, а также локусными скоплениями нейтрофилов и фокусами лимфо-плазмацитарной инфильтрации.
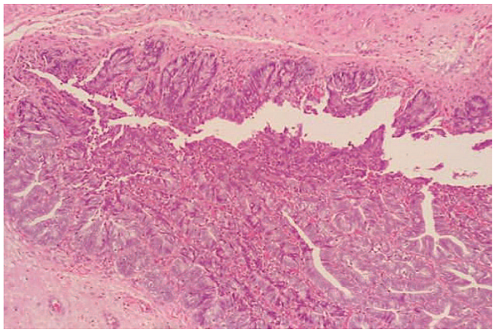
Рис. 3.1. Группа 2, 1 сутки. Отек и дезинтеграция интерстиция, выраженная гранулоцитраная инфильтрация перигляандулярных пространств простатического коплекса, инициальные деструктивные изменения альвеолярных структур. Окраска:гематоксилин-эозин. Ув. 40х
Fig. 3.1. Group 2, day 1. Edema and disintegration of interstitial tissue, severe granulocyte infiltration of the periglangular spaces of the prostatic complex, initial destructive changes in the alveolar structures. Strain: Hematoxylin-eosin. Magn. 40x
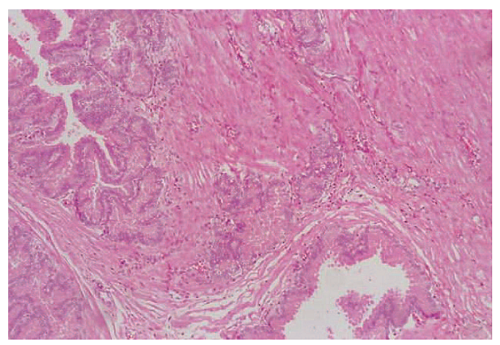
Рис. 3.2. Группа 2, 3 сутки. В железах простатического комплекса определены инициальные дистрофические изменения эпителия. В межуточном веществе, окружающем простатические железы – очаг деструкции и дезинтеграции интерстиция. Окраска: гематоксилин-эозин. Ув. 100х
Fig. 3.2. Group 2, day 3. Initial dystrophic changes in the epithelium were determined in the glands of the prostatic complex. Focus of destruction and disintegration is defined in the interstitial tissue surrounding the prostatic glands. Strain: Hematoxylineosin. Magn. 100x
В группе 3 после инокуляции Peptococcus niger 103 КОЕ/мл также определены альтеративные изменения, однако, несколько меньшей эксплицитности по сравнению с аналогичной воспалительной трансформацией тканей в группах 1 и 2 на сопоставимых сроках. На 1 сутки идентифицирован умеренно выраженный отек интерстициальной стромы с резким полнокровием питающих сосудов микроциркуляторного русла, альвеолярные структуры простатического комплекса заполнены белковым секретом/гранулами, в межуточном веществе небольшие диффузные скопления нейтрофильных гранулоцитов и выраженная эозинофильная инфильтрация, особенно в участках ткани между железами простатического комплекса и прилегающих железах уретры (рис. 4.1). К 3 суткам в прилегающих к простатической маточке участках стенки уретры и ткани ПЖ определены единичные фокусы коагуляционного некроза, поверхностные эрозии и десквамация уротелия, отек подслизистой оболочки; железы простатического комплекса значительно эктазированы, заполнены белковым секретом, интерстиций между альвеолярными структурами резко отечен, также идентифицированы выраженная дилятация сосудов микроциркуляторного русла и равномерная диффузная умеренно выраженная клеточная гистиоцитарная инфильтрация тканей. На 7 контрольные сутки определено развитие фокусов рыхлой волокнистой соединительной ткани в слизистой оболочке семенного бугорка и интерстициальной ткани вокруг простатических желез, сохраняется отек стромы и полнокровие капилляров и мелких артериол, в железах простатического комплекса идентифицированы участки десквамации железистого эпителия, строма желез эдематозно изменена, в окружающей их ткани – визуализированы диффузные лимфоцитарно-макрофагальные инфильтраты и нейтрофильные скопления (рис. 4.2). К 14 суткам сохраняется умеренных отек стромы и гиперемия сосудов, в расширенных альвеолярных структурах простатического комплекса – десквамация железистого эпителия и скопления белковых масс, в строме окружающей железы визуализированы скопления нейтрофилов; в прилегающих участках уретры и идентифицированных уретральных железах – очаговый поверхностный некроз уротелия, апоптоз отдельных клеточных пластов, фокусы лимфо-плазмацитарной инфильтрации подслизистого слоя.
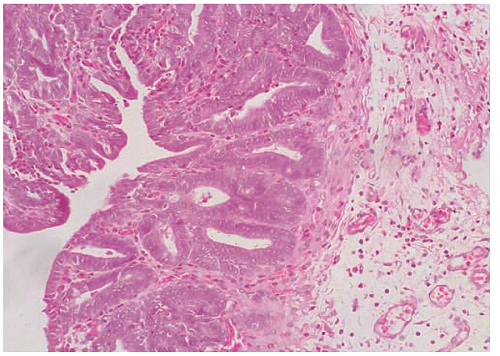
Рис. 4.1. Группа 3, 1 сутки. Эктазия желез простатического комплекса. Реактивный отек и дезинтеграция стромы. Плетора сосудов микроциркуляторного русла.Окраска: гематоксилин-эозин Ув. 100х
Fig. 4.1. Group 3, day 1. Ectasion of the prostatic complex glands. Reactive edema and stroma disintegration. Hyperemia of the microvasculature. Strain: Hematoxylineosin. Magn. 100x
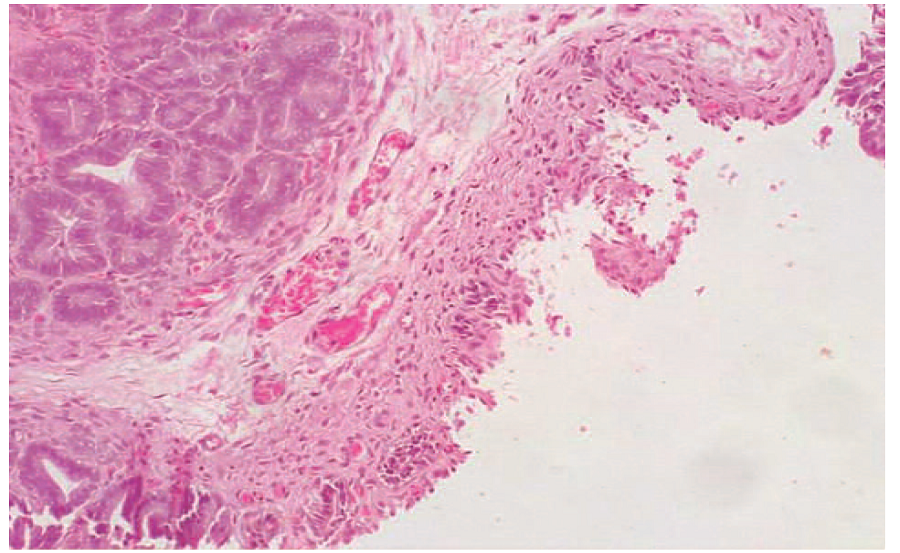
Рис. 4.2. Группа 3, 7 сутки. В прилегающих к простатической маточке участках стенки уретры и ткани ПЖ определены единичные фокусы коагуляционного некроза, поверхностные эрозии и десквамация уротелия, отек подслизистой оболочки. Окраска: гематоксилин-эозин. Ув. 100х
Fig. 4.2. Group 3, day 7. In the areas of the urethral wall and prostate tissue adjacent to the prostatic uterus, single foci of coagulation necrosis, superficial erosions and desquamation of urothelium, and submucosal edema were identified. Strain: Hematoxylineosin. Magn. 100x
В группе 4 (группа контроля) исследование биоптатов тканей органокомплекса не выявило инфекционно-воспалительных изменений в исследуемых анатомических структурах в каждом из контрольных сроков наблюдения.
Таким образом, в группе 1 (выступающей в роли группы сравнения) при инфицировании низким тиром каузативного уропатогена определено стадийное развитие инфламационных изменений с максимальной степенью их выраженности на 7 сутки в виде пурулентных экссудативных участков деструкции тканевых структур простатического комплекса. В группе 2 идентифицировано симилярное по отношению к группе 1 течение воспалительного процесса, и аналогичные воспалительные трансформации в ткани простатического комплекса с наивысшей степенью эксплицитности уже на 3 сутки (и сохранением к 7 суткам), что может свидетельствовать о более рапидном течении инфекционного процесса. Проведя анализ результатов патоморфологического исследования и сопоставив с данными бактериологического посева можно придти к заключению, что тканевые воспалительные изменения в анатомических структурах в полной мере соотносятся со степенью их обсемененности: представленный выше анализ бактериологического исследования показал, что максимальные показатели обсемененности тканей в группах 1 и 2 определены на 7 и 3 сутки соответственно. J.E. Elkahwaji и соавт. описывают подобные изменения в ткани ПЖ у мышей C3H/HeOuJ на 5 сутки после инокуляции, полученные в результате выполнения собственного экспериментального исследования c использованием E. coli 1677 Strain в титре 2 x 106 КОЕ/мл [21]. В группе 3 выявленные морфологические изменения носят умеренный диффузный инфильтративно-отечный характер и менее деструктивны, а субстанциальных очагов гнойного расплавления тканей не обнаружено. Также обращает на себя внимание диссеминированная эозинофильная инфильтрация тканей и формирование крупных лимфомакрофагальных скоплений на 3-7 сутки после инфицирования в тканях простатического комплекса, прилежащих к альвеолярным структурам, что можно расценивать как визуальное проявлений реакции гиперчувствительности II/IV типов (по Gell-Coombs) [22]. Сходные данные приводят H. Kiyokawa и соавт. в своем обзоре клинического случая, посвященного оценке морфологических особенностей эозинофильного простатита у пациента с синдромом Churg-Strauss [23]. Принимая во внимание данные микробиологического исследования в группе 4, показавшие доминирование в биоптатах тканей резидентной неклостридиальной анаэробной флоры (Propionibacterium spp., Eubacterium spp., Bacteroides spp., Peptostreptococcus spp. и т.д) можно предположить, что обнаруженная клеточная реакция направлена на противодействие распространению и размножению Peptococcus niger за счет перекрестных иммунных реакций на схожие антигены используемого в эксперименте бактериального патогена и резидентной микробиоты. В таком случае, в качестве отражения данной теории выступают более низкие показатели обсемененности ткани биоптатов по результатам бактериологического посева в группе 3, по сравнению с группами 1 и 2.
Следует подчеркнуть, что к 14 суткам в группах 1 и 2 определено комплементарное снижение контаминации тканей бактериальными патогенами с уменьшением эксплицитности морфологических тканевых воспалительный изменений и инициацией конверсии экссудативной фазы воспаления в пролиферативную, сопровождающейся появлением диффузных фокусов разрастания рыхлой волокнистой соединительной ткани в структурах простатического комплекса. Подобные изменения в группе 3 отмечены уже с 7 суток и также свидетельствуют в пользу предположения о максимальной реактивности иммунной системы в отношении представителя кластера неклостридиальной анаэробной флоры в рамках эксперимента.
ЗАКЛЮЧЕНИЕ
При экспериментальном моделировании бактериального простатита определено, что микроорганизмы из дебатируемого кластера, а именно S. haemolyticus и Peptococcus niger способны вызывать в низком титре (103 КОЕ/мл) развитие симилярных инфекционно-воспалительных процессов в ПЖ, сопоставимых по эксплицитности и релевантности с изменениями, вызываемыми при инфицировании каузативным уропатогеном E. coli. В свою очередь, исходом этих инфильтративно-деструктивных воспалительных изменений во всех случаях является торпидное развитие пролиферативного продуктивного процесса в структурах простатического комплекса, свидетельствующего об трансформации ОБП в ХБП.
Учитывая вышесказанное, во-первых, необходимо инициировать пересмотр представлений об этиологическом спектре микроорганизмов, способных вызывать развитие бактериального простатита, как I, так и II категорий, и сместить акценты «исследовательского поиска» с таксонов семейства Enterobacteriaceae на представителей иных семейств. Во-вторых, не игнорировать низкие титры (103 КОЕ/мл) уропатогенов в условиях отсутствия/стертой клинической симптоматики у пациентов, и в соответствии с этим включать в схему терапии антибактериальные препараты, с сопоставимыми показателями бактериальной обсемененности биоматериала (СП/моча) при интерпретации результатов пробы Meares-Stamey и препостмассажного теста Nickel.
ЛИТЕРАТУРА
- Коган М.И., Ибишев Х.С., Набока Ю.Л., Ферзаули А.Х. Mикробные патогены при хроническом бактериальном простатите. Медицинский вестник Башкортостана 2011;6(2): 104-106 [Kogan M.I., Ibishev H.S., Naboka U.L., Ferzauly A.H. Pathogens in microbial chronic bacterial prostatitis. Medicinskij vestnik Bashkortostana=Medical Bulletin of Bashkortostan 2011;6(2): 104-106. (In Russian)].
- Набока Ю.Л., Коган М.И., Черницкая М.Л., Гудима И. А., Ибишев Х.С., Ферзаули А.Х. Mикробный спектр секрета предстательной железы и факторы персистенции бактерий, обнаруженных при хроническом бактериальном простатите. Бюллетень Оренбургского научного центра УрО РАН 2012;3: 1-6. [Naboka Y.L., Kogan M.I., Chernitskaya M.L., Gudima I.N., Ibishev K.S., Ferzauli A.H. Microbial spectrum of prostate fluid and predictors of persistence of the bacteria detected in chronic bacterial prostatitis. Byulleten' Orenburgskogo nauchnogo centra UrO RAN=Bulletin of the Orenburg Scientific Center of the Ural Branch of the Russian Academy of Sciences 2012;3: 1-6. (In Russian.)].
- Mazzoli S. Conventional bacteriology in prostatitis patients: microbiological bias, problems and epidemiology on 1686 microbial isolates. Arch Ital Urol Androl 2007;79(2): 71–75.
- Cai T, Mazzoli S, Meacci F, Boddi V, Mondaini N, Malossini G. et ai/Epidemiological features and resistance pattern in uropathogens isolated from chronic bacterial prostatitis.e J of Microbiol 2011;49(3): 448-454. doi:10.1007/s12275-011-0391-z
- Delongchamps NB, de la Roza G, Chandan V, Jones R, Sunheimer R, Threatte G. et al., Evaluation of prostatitis in autopsied prostates—is chronic inflammation more associated with benign prostatic hyperplasia or cancer? J Urol 2008;179(5): 1736–1740. doi: 10.1016/j.juro.2008.01.034.
- Sutcliffe S, Platz EA. Inflammation and prostate cancer: a focus on infections. Curr Urol Rep 2008;9: 243–249. doi: 10.1007/s11934-008-0042-z
- Brooks GF, Carroll KC, Butel JS, Morse SA, Meitzner TA Jawetz, Melnick & Adelberg`s Medical microbiology. 26th Edition. A LANGE medical book, The McGraw-Hill Companies, Inc, New York, USA. 2010; 877p.
- Bonkat G, Bartoletti RR, Bruyère F, Cai T, Geerlings SE, Köves B. et al. Guidelines on Urological Infections. European Association of Urology. Edn. Presented at the EAU Annual Congress Barcelona 2019.
- Coker TJ, Dierfeldt DM. Acute bacterial prostatitis. Diagnosis and management: a systematic review. Am Fam Physician 2016;93(2): 114-120.
- Schaeffer AJ, Weidner W, Barbalias GA, Bottod H, Bjerklund Johansen T E, Hochreiter WW. et al. Summary consensus statement: diagnosis and management of chronic prostatitis/Chronic Pelvic Pain Syndrom. European Urology Supplements 2003;2(2): 1-4. doi: 10.1016/S1569-9056(02)00191-4.
- Набер К.Г., Сухорукова М.В. Микробиологические аспекты диагностики хронического простатита. Клиническая микробиология и антимикробная химиотерапия 2006; 8(1): 4-17. [Naber K.G., Sukhorukova M.V. Microbiological aspects of Chronic Prostatitis. Klinicheskaya mikrobiologiya i antimikrobnaya khimioterapiya=Clinical Microbiology and Antimicrobial Chemotherapy 2006; 8(1): 4-17. (In Russian.)].
- Hooijmans CR, Leenaars M, Ritskes-Hoitinga M. A gold standard publication checklist to improve the quality of animal studies, to fully integrate the Three Rs, and to make systematic reviews more feasible. Altern Lab Anim 2010;38(2): 167-182. doi: 10.1177/026119291003800208
- Kilkenny C, Browne WJ, Cuthill IC, Emerson M, Altman DG. Improving bioscience research reporting: the ARRIVE guidelines for reporting animal research. PLoS Biol 2010;8(6): e1000412. doi: 10.1371/journal.pbio.1000412.
- Directive 2010/63/EU of the European Parliament and of the Council of 22 September 2010 on the protection of Animals used for Scientific purposes. OJ L 2010;276: 33–79.
- European Convention for the Protection of Vertebrate Animals used for Experimental and Other Scientific Purposes (ETS No.123). Appendix A «Guidelines for the maintenance and care of animals». Adopted: Strasbourg, 18.03.1986, entry in force: 01.01.1991. URL: https://rm.coe.int/CoERMPublicCommonSearchServices/DisplayDCTMContent?documentId= 090000168007a67b
- Mahler M, Berard M, Feinstein R, Gallagher A, Illgen-Wilcke B, Pritchett-Corning K. et al. FELASA recommendations for the health monitoring of mouse, rat, hamster, guinea pig and rabbit colonies in breeding and experimental units. Lab Anim 2014;48(3); 178–192. doi: 10.1177/0023677213516312
- ГОСТ 33215-2014. Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур. Введ. 2017-01-06. М.: Стандартинформ, 2016. 20 с. [Guidelines for accommodation and care of animals. Environment, housing and management. Adopted: 2017-01-06. Vved. 2017-01-06. M.: Standartinform, 2016. 20 s. (In Russian)].
- ГОСТ 33216 – 2014. Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами. Введ. 2016-07-01. М.: Стандартинформ, 2016. 22 с. [Guidelines for accommodation and care of animals. Species-specific provisions for laboratory rodents and rabbits. Adopted 201607-01. Vved. 2016-07-01. M.: Standartinform, 2016. 22 s. (In Russian)].
- Набока Ю.Л., Коган М.И., Гудима И.А., Мирошниченко Е.А., Ибишев Х.С., Брагина Л.Е., Ферзаули А.Х., Джалагония О.Т. Способ определения бактериологической обсемененности мочи, секрета предстательной железы и эякулята. Патент РФ RU 2452774 C1 № 2011103414/10 от 31.01.2011. Заявитель и патентообладатель: Набока Ю.Л., Коган М.И. Опубл. 10.06.2012. Бюл. №16. 12 с. [Russian Federation patent RU 2452774 C1 No. 2011103414/10. Method of evaluating bacterial load of urine, prostatic secretion, and ejaculate. Naboka Yu.L., Kogan M.I., Gudima I.A., Miroshnichenko E.A., Ibishev Kh.S., Bragina L.E., Ferzauli A.Kh., Dzhalagoniya O.T. Applicant and patent holder: Naboka Yu.L., Kogan M.I. Dated January 31, 2011. Published 10.06.2012. Bul. №16. 12 p. (In Russian)].
- Vykhovanets E.V., Resnick M.I., MacLennan G.T., Gupta S.ьExperimental rodent models of prostatitis: limitations and potential. Prostate Cancer Prostatic Dis 2007;10(1): 15-29. doi: 10.1038/sj.pcan.4500930
- Harcourt-Brown F, Nigel H. Textbook of Rabbit Medicine. Butterworth–Heinemann`s Reed Educ. and Prof. Publ. Ltd. Alden Press, Oxford, United Kingdom. 2002; 426 p.
- Elkahwaji JE, Haukel RJ, Brawner CM. Chronic bacterial inflammation induces prostatic intraepithelial neoplasia in mouse prostate. Brit J Can 2009;101(10): 1740-1748. doi: 10.1038/sj.bjc.6605370
- Rajan TV. The Gell–Coombs classification of hypersensitivity reactions: a re-interpretation. Trends Immunol 2003;24(7): 376-379.
- Kiyokawa H, Koyama M, Kato H. Churg-Strauss syndrome presenting with eosinophilic prostatitis. Int J Urol 2006;13(6):838-840. doi: 10.1111/j.1442-2042.2006.01419.x







