ВВЕДЕНИЕ
В настоящее время перкутанная нефролитотрипсия (ПНЛ) является основным методом лечения конкрементов более 2 см и коралловидных камней у детей [1-5]. В процессе анализа данных отечественной, зарубежной литературы и клинических рекомендаций для внедрения терминов «крупный», «средний» и «мелкий» камень нами предложена Формула оценки размера камня (ФОРК) почки у детей разных возрастных групп, где учитывается соотношение размера камня почки к продольному размеру почки [6]. В результате выполнения работы, был сделан вывод, что ПНЛ следует выполнять детям разных возрастных групп с крупными конкрементами почки при ФОРК >20%. Общепринятым завершающим этапом ПНЛ является установка нефростомического дренажа, который обеспечивает хорошую дренажную и гемостатическую функцию, позволяет осуществить контроль за почкой в раннем послеоперационном периоде, выполнить антеградную пиелоуретерографию и при необходимости осуществить повторный доступ в полостную систему почки [7-9].
Целью исследования было изучение эффективности «безнефростомной» ПНЛ при лечении мочекаменной болезни у детей разных возрастных групп.
МАТЕРИАЛЫ И МЕТОДЫ
В детском урологическом отделении НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиале ФГБУ «НМИЦ радиологии» Минздрава России с 2013 по 2019 год ПНЛ по «безнефростомной» методике выполнена 66 детям. Обследование всех пациентов проводилось по общепринятому плану: сбор анамнеза, осмотр и физикальное обследование, клинические и лабораторные исследования, ультразвуковое исследование мочеполовой системы, обзорная и экскреторная урография, динамическая нефросцинтиграфия. В ряде сложных клинический случаев пациентам дополнительно проводилась мультиспиральная компьютерная томография (МСКТ) органов забрюшинного пространства. На дооперационном периоде обследования так же выполнялся общий и биохимический анализы крови, общий анализ мочи, бактериологический анализ мочи, электрокардиография, определялось состояние свертывающей системы крови.
В наше исследование включены дети, дооперационные и операционные данные которых соответствующие следующим критериям:
- отсутствие бактериурии в посеве мочи;
- отсутствие аномалии количества и расположения почек;
- размеры камня почек от 1,5 до 3 см;
- один перкутанный доступ;
- полное удаление конкремента;
- отсутствие повреждений чашечно-лоханочной системы (ЧЛС) интраоперационно;
- отсутствие выраженных явлений кровотечения по доступу в конце операции.
Пациенты были разделены на три исследуемые группы, в зависимости от размера используемого инструментария и способа окончания оперативного вмешательства. Основные клинические и демографические характеристики групп пациентов представлены в таблице 1. В младшую возрастную группу входили дети в возрасте 1-3 лет, в среднюю – в возрасте 4-10 лет и в старшую – 11-17 лет.
Таблица 1. Демографические и клинические данные пациентов
Table 1. Patient demographics and clinical data
| Параметр Parameter |
Группы пациентов Patient groups |
|||
|---|---|---|---|---|
| I группа, (n-28) Group I, (n-28) |
II группа, (n-21) Group II, (n-21) |
III группа, (n-17) Group III, (n-17) |
||
| Средний возраст, лет Age, years |
5,7±1,1 (2-16) | 6,3±1,2 (1-17) | 11,2±1,0 (8-17)* | |
| Число детей в группе Number of children in a group |
младшая возрастная группа, n younger age group, n |
9 | 7 | 3 |
| средняя возрастная группа, n average age group, n |
7 | 5 | 6 | |
| старшая возрастная группа, n senior age group, 11-17 y/о, n |
12 | 9 | 8 | |
| Соотношение полов, м/д, n Sex ratio, b/g, n |
16/12 | 12/9 | 10/7 | |
| Размер конкремента, мм (ФОРК, %) Stone size, mm (KSS-CDA, %) |
общая группа general group |
21,5±6,5 (26,8) | 22,5±7,5 (27,4) | 25,5±4,5* (27,1) |
| младшая возрастная группа younger age group |
16,0±1,0 (24,6) | 15,5±5,0 (23,8) | 22,0±1,0 (33,8) | |
| средняя возрастная группа average age group |
21,5±1,5 ( 25,0) | 20,0±1,0 (23,5) | 23,5±0,5 (27,7) | |
| старшая возрастная группа senior age group |
24,5±2,5 (23,3) | 27,0±3 (25,7) | 27,5±2,5 (26,2) | |
| Сторона операции: правая/левая, % Operation side: right/left, % |
57,1/42,9 | 52,4/47,6 | 58,8/41,2 | |
| Размеры ЧЛС, мм PCS size, mm |
20±2,5 (0-31) | 21±2,7 (0-30) | 20,5±2,8 (0-32) | |
| Дефицит функции почки со стороны вмешательства, % Renal function deficiency on the part of the intervention, % |
16±4,2 (0-52) | 18±4,0 (0-48) | 15±4,5 (0-51) | |
Примечание: * различия между группой 3 и группами 1 и 2 достоверны при р<0,05
Note: * differences between group 3 and groups 1 and 2 are significant at p<0,05
В I группу вошли дети (n=28), операция которым выполнялась по методике мини-ПНЛ с последующим глухим ушиванием нефростомического доступа. Дренирование верхних мочевых путей в послеоперационном периоде осуществлялось за счет установки «JJ»-внутренних и «J» -наружных мочеточниковых стентов, которые держали до 14 дней. В эту группу вошли дети, у которых отсутствовало активное кровотечение после извлечения нефроскопа в конце операции в сочетании с полным удалением камня, подтвержденным визуально и рентгеноскопически.
II группу составили дети (n=21), оперированные по аналогичной методике мини-ПНЛ, у которых в финальной части оперативного вмешательства выявлена умеренная геморрагия по перкутанному тракту, которая потребовала введения гемостатического матрикса с тромбином с целью ее купирования. Дренирование верхних мочевых путей выполнялось так же с помощью наружных и внутренних мочеточниковых стентов.
Пациенты, сформировавшие III группу (n=17), были прооперированы по стандартной методике ПНЛ, также, как и во второй группе, в конце операции имели умеренное кровотечение, и, с целью его «безнефростомного» завершения, была произведена аппликация гемостатического матрикса с тромбином.
Малая выборка наблюдений в каждой группе (в среднем n =22) обусловлена строгим отбором пациентов для завершения ПНЛ по «безнефростомной» методике. Использование ФОРК для оценки размера камня почки и в последующем характеристики каждой группы, не выявило больших различий между группами, что также подтвердил проведенный статистический анализ. Сравнение расчетных показателей ФОРК, согласно возрастным подгруппам, не продемонстрировало значимых различий и характеризовалось небольшим числом наблюдений. Таким образом, проведение статистического анализа в подгруппах, разделенных по возрастам не выполнялось.
В 2021 г в НИИ урологии им Н.А. Лопаткина был получен патент по безнефростомному малоинвазивному лечению нефролитиаза у детей [10]. Главным положением в патенте является применение гемостатического матрикса на завершающем этапе ПНЛ, техника выполнения которого представлена на рисунке 1. По рабочему каналу в полость собирательной системы устанавливалась струна-проводник. Используемым веществом, заполняющим нефростомический доступ в целях остановки кровотечения и попадания мочи в забрюшинное пространство, была гемостатическая матрица SurgifloTM с тромбином 2000 МЕ (производитель «Ферросан Медикал Девайсез А/С», Дания, регистрационное удостоверение № ФСЗ 2012/12021 от 10.04.2017).
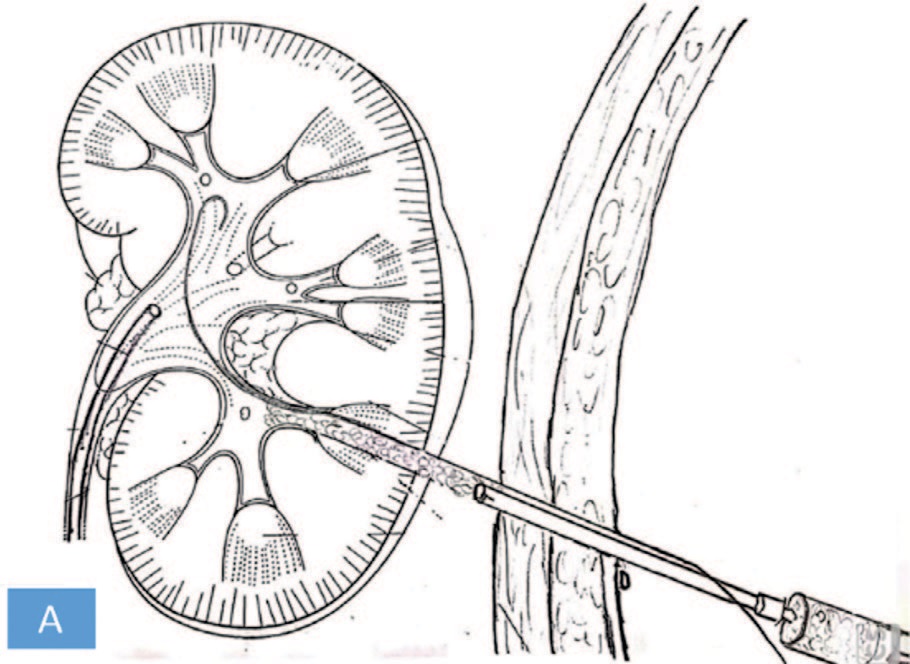
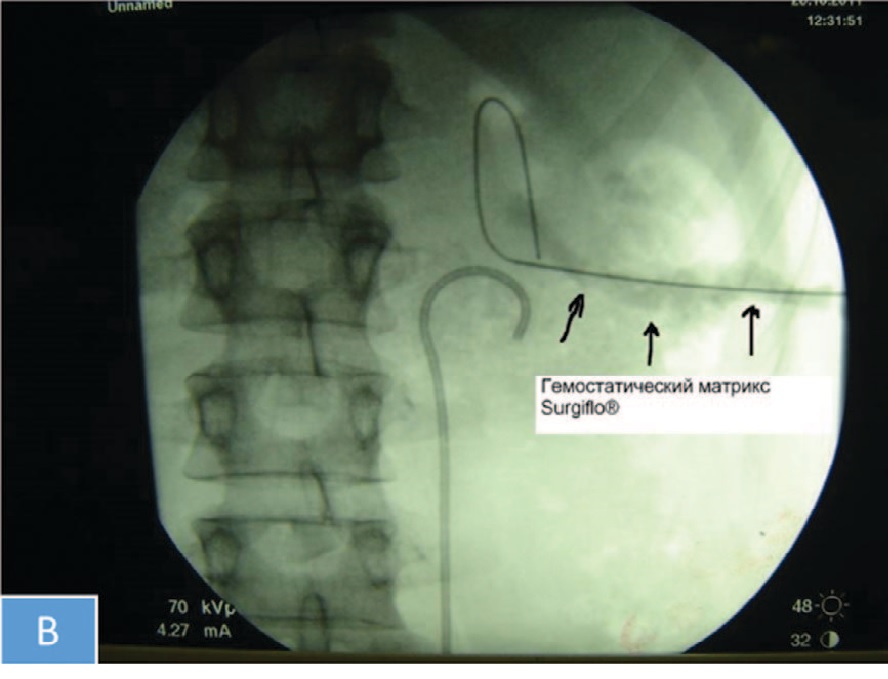
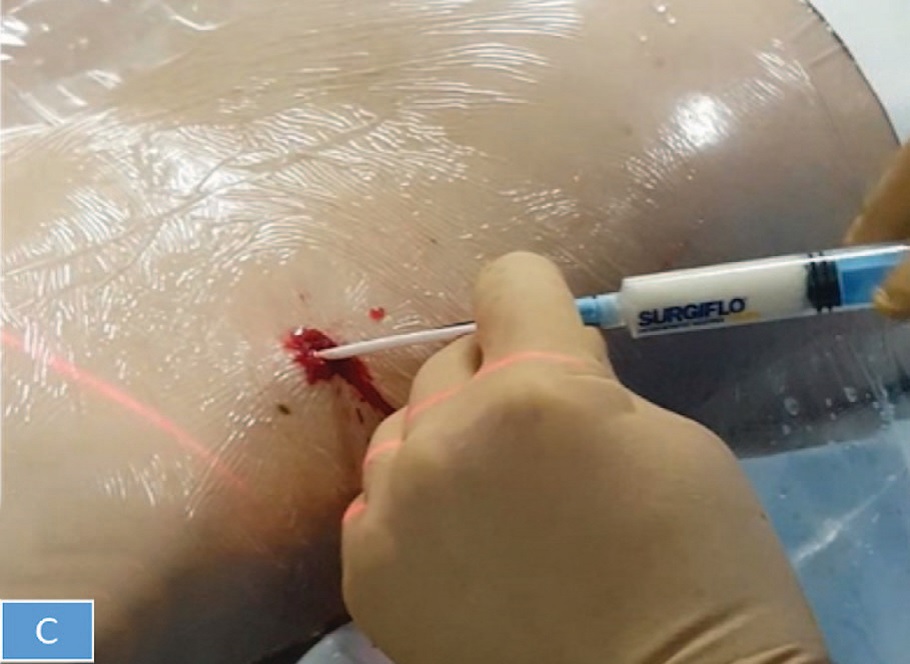
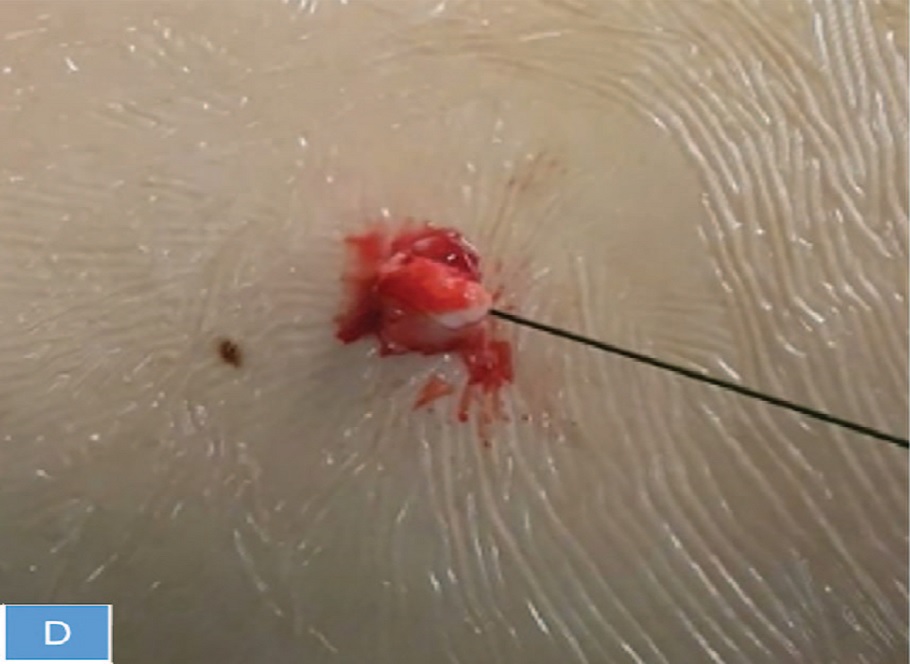
Рис. 1. Этапы введение гемостатического матрикса в перкутанный канал. А- Схема введения гемостатического матрикса в перкутанный канал. В- Рентгеноскопическая картина этапа введения гемостатического матрикса по апликатору. С- Введение гемостатического матрикса в перкутанный канал (интраоперационный вид). D - Наружный вид раны, спустя 5 минут наблюдения после введения в перкутанный тракт гемостатического матрикса.
Fig. 1. Steps of introducing a hemostatic matrix into the renal-access tract. А- The scheme of introducing a hemostatic matrix into the renal-access tract. В- X-ray of introduction of the hemostatic matrix through the applicator. С - intraoperative view. D - View of the wound, 5 minutes after the introduction of the hemostatic matrix into the renal-access tract
В конце операции выполнялся нефроскопический осмотр доступа на предмет наличия и степени интенсивности кровотечения. По нефроскопу в полостную систему почки и мочеточник под визуальным и ренгеноскопическим контролем проводилась жесткая струна-проводник длиной 75 см с мягким кончиком длиной 3 см. Причем страховая струна локализовалась в доступе во время всего вмешательства. По жесткой струне в лоханку почки проводился гемостатический аппликатор. Ориентируясь на ретроградную уретеропиелографию, выполнялась установка аппликатора на 3 мм поверхностнее чашечно-лоханочной системы по нефростомическому доступу. Затем шприц с гемостатическим матриксом соединялся с аппликатором, и производилось плавное, постепенное введение препарата с одновременным извлечением аппликатора по доступу. В результате осуществлялось полное заполнение гемостатическим матриксом нефростомического канала. Нефростомический канал заполнялся матриксом до уровня подкожно-жировой клетчатки, не контактируя с краем раны: последняя ушивалась отдельными швами. Затем осуществлялся рентгеноскопический контроль, путем выполнения ретроградной уретеропиелографии, на предмет отсутствия затеков контрастного препарата. Также возможно добавление 2 мл контрастного вещества в матрикс для визуализации последнего при рентгеноскопическом контроле. Выполнялось наблюдение за ушитой раной в течение 5-7 минут с целью контроля выраженного кровотечения. Страховая струна находилась в чашечно-лоханочной системе ребенка на период наблюдения явлений возможного кровотечения.
В случае отсутствия кровотечения страховая струна удалялась, на рану накладывалась асептическая повязка.
При возникновении кровотечения по нефростомического каналу при выраженной гематурии по мочеточниковому катетеру-стенту выполнялось дренирование почки путем установки нефростомы с раздувным баллоном. По страховой струне-проводнику нефростомический дренаж проводился в собирательную систему почки, баллон раздувался до 2-3 мл, и осуществлялось поджатие области доступа со стороны ЧЛС ребенка.
РЕЗУЛЬТАТЫ
Оперативное лечение выполнялось по стандартной методике. Операцию детям выполняли под эндотрахеальным наркозом, и она состояла из 4 этапов: цистоскопия, ретроградная катетеризации почки, формирование доступа в чашечно-лоханочную систему, литотрипсия и литоэкстракция. Вмешательство завершалось эндоскопическим осмотром чашечно-лоханочной системы и рентгеноскопическим контролем на предмет полного удаления фрагментов конкремента. В таблице 2 представлены результаты лечения пациентов.
Таблица 2. Сравнительная оценка показателей оперативных вмешательств у детей, прооперированных по «безнефростомной» методике
Table 2. Comparative evaluation of the indicators of surgical interventions in children operated on by the «non-nephrostomy» method
| Показатель Index |
Группы пациентов Patient groups |
P | ||
|---|---|---|---|---|
| I группа, (n-28) Group I, (n-28) |
II группа, (n-21) Group II, (n-21) |
III группа, (n-17) Group III, (n-17) |
||
| Продолжительность операции, мин, Surgery duration, min M±m [min-max] |
50±5,4 [25-95] |
55±8,6 [30-115] |
40±7,8 [20-90] |
р1-2=0,877 р1-3=0,458 р2-3=0,326 |
| Полное удаление конкремента за один сеанс, n (%) Complete removal of the calculus in one session, n (%) |
26 (92,8) | 19 (90,4) | 16 (94,1) | p-2=0,764 p1-3=0,870 p2-3=0,679 |
| Использование внутреннего стента, n,(%) Use of an external stent n, (%) |
22 (78,6) | 16 (76,1) | 11 (64,7) | p1-2=0,844 p1-3=0,308 p2-3=0,438 |
| Использование наружного стента, n, (%) Use of an external stent n, (%) |
6 (21,4) | 5 (23,9) | 6 (35,3) | p1-2=0,843 p1-3=0,502 p2-3=0,238 |
| Длительность макрогематурии в послеоперационном периоде, час. Duration of gross hematuria in the postoperative period, h., M±m [min-max] |
35±10,0 [2-115] |
17±5,9 [0-68] |
26±9,7 [0-84] |
p-2=0,245 p1-3=0,577 p2-3=0,632 |
| Койко-день после операции, дней Bed-day after surgery, days, M±m [min-max] |
3,5±2,3 [1-7] |
3,5±2,5 [1-9] |
4±2,9 [1-10] |
p1-2=0,943 p1-3=0,712 p2-3=0,663 |
| Окончательная эффективность, n (%) Final efficiency, n (%) |
27 (96,4) | 20 (95,2) | 17 (100) | p1-2=0,835 p1-3=0,431 p2-3=0,362 |
Полное удаление конкремента за один оперативный сеанс во всех трех группах сходное. В I группе этот показатель составил 92,8% (26 детей). Дренирование чашечно-лоханочной системы у 22 (78,6%) детей было осуществлено с помощью установки внутреннего стента мочеточника размерами 4,8 и 6 Ch длиной 14, 16 и 24 см, в зависимости от возраста ребенка. У 6 (21,4%) детей дренирование почки выполнялось с помощью наружного стента размером 5 Ch длиной 70 см, фиксирующегося пластырем к уретральному катетеру. Срок дренирования составил до 2-х дней. Во II исследуемой группе детей первичная эффективность была достигнута у 19 (90,4%) пациентов. В 76,1% случаев почка дренировалась за счет установки внутреннего стента, тогда как наружный интубатор использовался в 23,9% клинических случаев. В III группе детей процент полного удаления конкремента за один сеанс составил 94,1% (16 пациентов). Как и в предшествующих двух группах, дренирование преимущественно выполнялось с использованием внутреннего стента у 11 (64,7%) детей и наружного стента у 6 (35,3%). Наибольшая длительность макрогематурии в послеоперационном периоде была отмечена в I группе и составила в среднем 35 (2-115) часов, тогда как, во II и III группах этот показатель был 17 (0-68) и 26 (0-84) часов соответственно. Во всех трех группах показатель нахождения в стационаре после оперативного вмешательства был практически одинаковым и в среднем составил 3,5 дня.
Потребность в дополнительных вмешательствах после проведенного оперативного лечения детям составила 21,4% в I группе, 23,7% – во II и 17,5% – в III исследуемой группе.
У 3 (10,7%) детей в I группе в связи с дилатацией чашечно-лоханочной системы после удаления наружного стента потребовалось повторное дренирование с использованием внутреннего стента. Необходимость установки внутреннего стента во II и III группах составила 9,5% (2 ребенка) и 11,7% (2 ребенка) соответственно.
Сеансы дистанционной пиелолитотрипсии с целью удаления резидуальных конкрементов после оперативного вмешательства были выполнены нескольким пациентам. Во всех трех группах показатели были примерно схожи и составляли 3,6%, 9,5% и 5,8% для I, II и III групп соответственно. Также у 2 (7,1%) детей I группы и у 1 (4,7%) ребенка II группы конкременты мочеточника разрушались контактно с помощью ригидного уретероскопа. В группе детей, прооперированных с помощью инструмента стандартного размера, данное вмешательство не потребовалась. Во всех трех группах потребности выполнения повторного перкутанного доступа для окончательного удаления конкрементов или дренирования почки не отмечалось. Понятно, что больший размер инструмента позволяет удалить конкременты легче и более надежно, но размер повреждения ткани почки при создании доступа большего диаметра также больше травмирует почки, и у детей младшего возраста нежелателен.
Виды и частота осложнений в послеоперационном периоде у детей, прооперированных по «безнефростомной» методике, представлены в таблице 3.
Таблица 3. Сравнительная оценка осложнений в трех группах детей после ПНЛ с использованием «безнефростомной» методики
Table 3. Comparative assessment of complications in 3 groups of children after PNL using a «non-nephrostomy» method
| Осложнения Complications |
I группа, (n-28) Group I, (n-28) |
II группа, (n-21) Group II, (n-21) |
III группа, (n-17) Group III, (n-17) |
|---|---|---|---|
| Стойкая гипертермия (38 0С), n (%) Persistent hyperthermia (38 0C), n (%) |
3 (10,7) | 1 (4,7) | 1 (5,8) |
| Синдром системной воспалительной реакции, n (%) Systemic inflammatory response syndrome, n (%) |
2 (7,1) | 1 (4,7) | 0 (0) |
| Смена антибактериального препарата, n (%) Changing an antibacterial drug, n (%) |
3 (10,7) | 1 (4,7) | 0 (0) |
| Кровотечение (гематурия более 3-х дней), гемотрансфузия, n (%) Bleeding (hematuria for more than 3 days), blood transfusion, n (%) |
2 (7,1) | 0 (0) | 0 (0) |
| Паранефральная гематома, n (%) Perinephric hematoma, n (%) |
5 (17,8)* | 0 (0) | 0(0) |
| Потребность в анальгетиках более 3-х суток, n (%) The need for analgesics for more than 3 days, n (%) |
6 (21,4) | 5 (23,8) | 5 (29,4) |
| Дилатация ЧЛС после удаления стента, n (%) Dilatation of the PCS after stent removal, n (%) |
4 (14,2) | 2 (9,5) | 3 (17,6) |
| Всего Total |
25 (89,3%)** | 10 (47,6%) | 9 (52,9%) |
| Всего I+II степень по Clavien | 18 (64,3%) | 10 (47,6%) | 9 (52,9%) |
| Всего III+IV grades Clavien | 7 (25,0%)*** | 0 | 0 |
* различия статистически значимы при сравнении 1-й группы с 2-й и 3-й группами при р<0,05, **различия значимы при р<0,01, *** различия значимы при р<0,001
*differences are statistically significant when comparing group 1 with groups 2 and 3 at p<0.05, **differences are significant at p<0.01, *** differences are significant at p< 0.001
Фебрильная лихорадка (стойкая температура 380С) чаще всего встречалась у детей I группы – в 10,7% случаев, тогда как во II и III группах данное осложнение выявлено в 4,7% и 5,8% наблюдений соответственно. Таких грозных осложнений, как перфорация чашечнолоханочной системы, плевральной полости, потеря перкутанного хода, отмечено не было.
Отсутствие нефростомического дренажа в послеоперационном периоде снижало болевые ощущения у детей, и уменьшалась потребность в приеме ненаркотических анальгетиков. Характеристики данного показателя были схожи во всех трех группах. Необходимость в обезболивающих более 3-х суток была выявлена у 6 (21,4%) детей в I группе, 5 (23,8%) – во II и у 5 (29,4%) детей в III группе.
Интраоперационная травма почки после перкутанного доступа в нескольких случаях сопровождалась формированием паранефральной гематомы, которую выявляли при ультразвуковом исследовании почек в послеоперационном периоде. Околопочечные гематомы в области перкутанного доступа почки были отмечены только у детей из I группы – 5 (17,8%). Во II и III группах детей, где вмешательство проводилось с введением гемостатического матрикса с тромбином, данное осложнение не наблюдали, что свидетельствует об эффективности данного метода. Различия по частоте развития этого осложнения оказались статистически значимыми при р<0,05.
По другим видам осложнений статистически значимых различий не выявлено, однако при суммировании всех осложнений оказалось, что они достоверно чаще развивались у детей, входящих в I группу, по сравнению II и III группами (р<0,001), причем это различие было связано в основном с более тяжелыми осложнениями (группы III+IV по Clavien) (р<0,01), тогда как частота развития легких осложнений, хоть и была выше у детей I группы, но эти различия не достигали статистической значимости.
ОБСУЖДЕНИЕ
Наличие нефростомического дренажа влечет за собой ряд негативных последствий, таких как дискомфорт и болевой симптом у ребенка в первую очередь, увеличение сроков пребывания в стационаре, возможная экстравазация мочи [11-13]. В связи с вышеуказанным, появилась тенденция к совершенствованию форм и конфигураций нефростомических дренажей, а также возник вопрос целесообразности в ряде случаев дренирования чрескожного хода [14-16]. Далее в практике детского уролога начала активно внедряться так называемая «безнефростомная» (tubeless) методика ПНЛ у детей. Данная методика сопровождалась установкой внутренних либо наружных мочеточниковых стентов при завершении ПНЛ, как альтернатива дренирования чашечно-лоханочной системы нефростомой [17-22]. Развитию «безнефростомной» методики ПНЛ у пациентов детского возраста также способствовало уменьшение диаметра эндоскопического оборудования [23-26]. Впервые о «безнефростомной» технике выполнения ПНЛ у взрослых сообщили G.C. Bellman и соавт. в 1997 г. [27]. О выполнении «безнефростомной» ПНЛ у 23 детей сообщили S.M. Aghamir и соавт. в 2012 г. [28]. Первое рандомизированное клиническое исследование с применением «безнефростомной» методики было проведено G. Song и соавт. и опубликовано в 2015 г. [29]. В данное исследование вошли результаты лечения 70 детей. Сравнивались две группы пациентов детского возраста, подвергнуты «безнефростомной» методике ПНЛ, и группа детей, эндоскопическое вмешательство у которых завершалось дренированием ЧЛС посредством установки баллонной нефростомы 12 Ch. Выполнение ПНЛ с использованием «безнефростомной» методики позволяет снизить риск указанных состояний. Данный вид лечения идеально подходит в случае достижения полного удаления конкремента размером 1,5-3 см при отсутствии бактериуриии и без явлений интенсивного кровотечения в финальной стадии ПНЛ [30-35]. Предпочтительно дренирование верхних мочевых путей в послеоперационном периоде за счет установки внутренних и наружных мочеточниковых стентов. Явления макрогематурии в послеоперационном периоде были продолжительнее в группе без использования гемостатического матрикса и с среднем продолжались 35 (2-115) часов. Использование «безнефростомной» ПНЛ с аппликацией перкутанного доступа гемостатическим матриксом позволяет исключить возникновение паранефральной гематомы [36-38]. Тогда как в группе без введения матрикса данное осложнение отмечено в 17,8% случаев.
ВЫВОДЫ
Предложенная «безнефростомная» ПНЛ с применением гемостатического матрикса показана детям без бактериурии при полном удалении конкремента при отсутствии травмы ЧЛС и явлений интенсивного кровотечения. Продолжительность макрогематурии уменьшилась в сравнении с обычной «безнефростомной» ПНЛ на 51,4% при мини-ПНЛ и на 25,8% – при стандартном доступе.
Таким образом, выполнение ПНЛ с использованием «безнефростомной» методики, с учетом строгих показаний, позволяет снизить частоту инфекционно-воспалительных и геморрагических осложнений у детей.







