ВВЕДЕНИЕ
Нейрогенный мочевой пузырь представляет собой нарушение функции нижних мочевых путей (НМП), обусловленное поражением нервной системы как на центральном, так и периферическом уровне [1].
Выбор оптимального подхода к лечению каждого конкретного пациента с нейрогенной дисфункцией мочевого пузыря является сложной задачей для уролога. Тактика лечения требует индивидуального подхода с учетом причины заболевания, выраженности как урологических, так и неврологических симптомов и риска осложнений. В ряде стран мира разработаны клинические рекомендации, направленные на стандартизацию и оптимизацию методов лечения данного состояния. В 2020 году подобное руководство утверждено и Минздравом России [2].
Опыт Великобритании и Ирландии [3], Франции [4] и Голландии [5] показал, что реальная клиническая практика расходится с утвержденными в этих странах рекомендациями по ведению больных с нейрогенным мочевым пузырем. Подобных исследований в России не проводилось.
Цель данной работы – оценить клиническую практику урологов Российской Федерации в лечении больных с нейрогенным мочевым пузырем.
МАТЕРИАЛЫ И МЕТОДЫ
Опрос врачей проводился на специализированном профессиональном интернет-ресурсе для урологов Uroweb.ru. Приглашение к участию в опросе было размещено в виде баннера, проводились рассылки по электронной почте и в мессенджерах. Всего в исследовании, продлившемся с 07.07.23 по 30.12.23 г., приняли участие 250 российских врачей, которым после идентификации на перечисленных выше ресурсах были предложены вопросы с несколькими вариантами ответов.
Опросник разрабатывался по действующим Российским клиническим рекомендациям [2]. В части вопросов участникам можно было выбрать только 1 вариант ответа, а в некоторых была возможность выбрать несколько ответов. Также в конце каждого вопроса можно было оставить свое мнение или замечание, которое отразилось в результатах как «другое». Каждый отвечающий должен был ответить на все вопросы без исключения, возможности пропустить ответ на какой-либо вопрос не было.
Дополнительно была собрана информация о регионе работы, возрасте, стаже и наличии категории/ученой степени респондента.
После окончания опроса была сделана выгрузка всех данных, произведен подсчет вариантов ответов.
РЕЗУЛЬТАТЫ
В нашем опросе участвовало 250 врачей со всей территории России. Бо́льшая часть опрошенных коллег представляла Центральный федеральный округ –26,1%, Южный федеральный округ – 25,7% и Сибирский федеральный округ – 20,9%. Оставшиеся 27,3% поделили между собой Северо-Западный (8,8%), Дальневосточный (8%), Уральский (6,8%), Северо-Кавказский (2,4) и Приволжский (1,2%) федеральные округа (рис. 1).
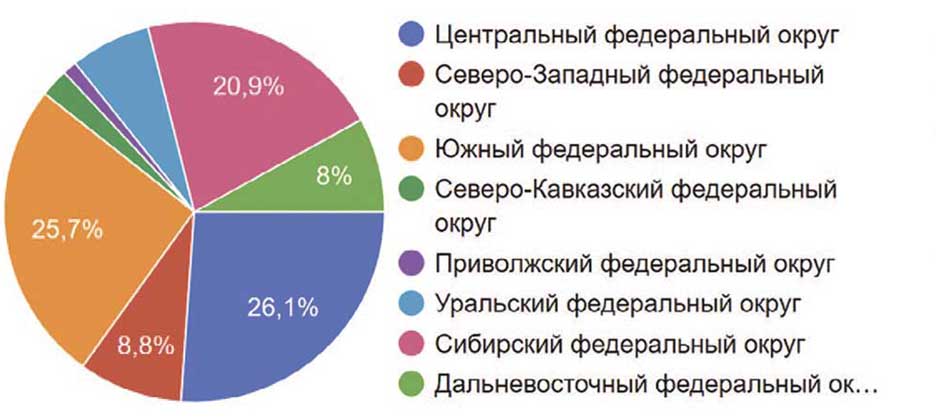
Рис. 1. Регион работы респондента (Федеральный округ)
Fig. 1. Respondent's region of work (Federal District)
Среди областей лидировали не Москва (9,6%) и Московская область (5,2%), а Омская область, доля которой в опросе составляла 14,1%, на втором месте по количеству принявших участие в опросе – Республика Крым – 12,9%. Другие 87 областей России разделили между собой оставшуюся долю 58,2%. Самое меньшее количество опрошенных отмечено в Республике Хакасия, Еврейской автономной области, Владивостоке, Хабаровске, Белгородской области, Башкортостане и Нижегородской области. Там прошли опрос по 1 человеку (pис. 2).
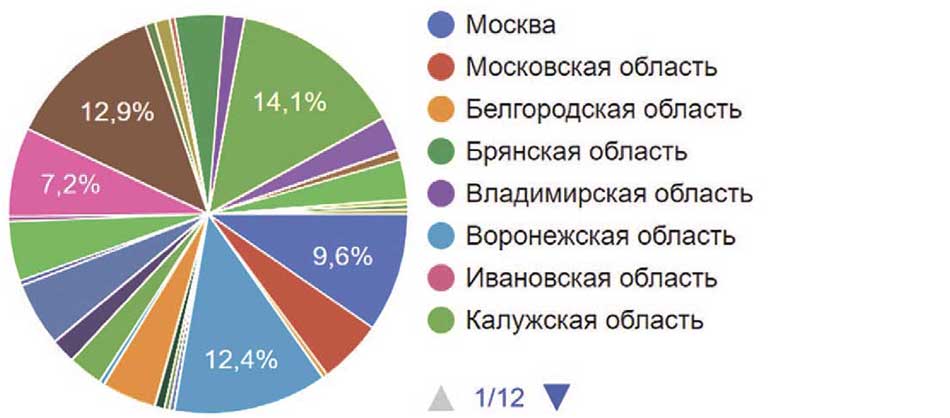
Рис. 2. Регион работы респондента (Область/Край)
Fig. 2. Region of work of the respondent (Region)
Судя по результатам исследования, наибольший интерес опрос вызвал у коллег в возрасте 30-40 лет (38,6%), на втором месте коллеги в возрасте 40-50 лет (24,9%). Практически такую же долю опрошенных составляли коллеги старше 50 лет (25,3%). Доля молодых коллег 20-30 лет составляла 10,4% (рис. 3), при этом 77,5% были коллеги мужского пола и 22,5% женского (рис. 4).
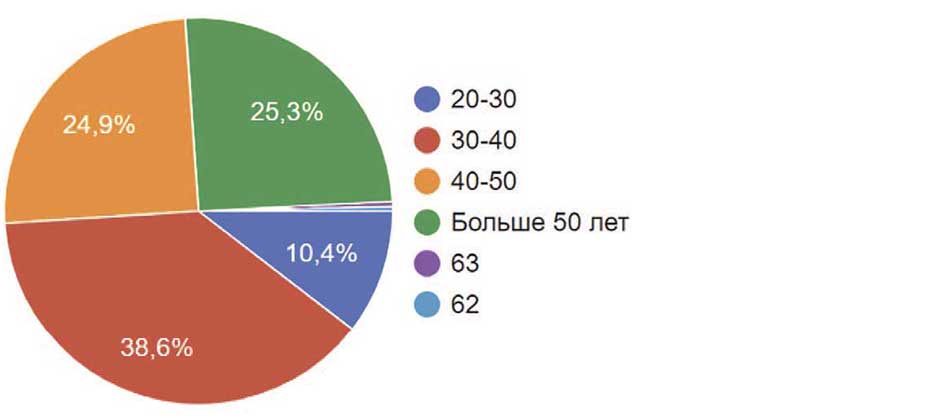
Рис. 3. Возраст респондентов
Fig. 3. Age of respondents
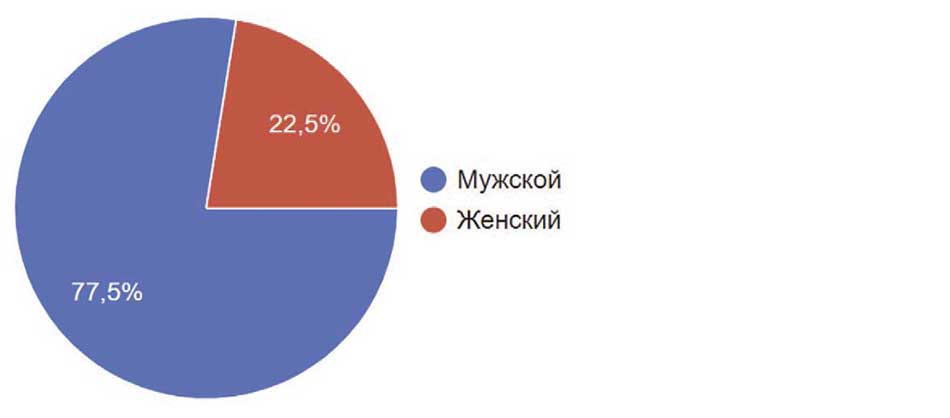
Рис. 4. Пол респондентов
Fig. 4. Gender of respondents
Среди участников исследования бо́льшая часть имели стаж работы от 11 до 25 лет (41,8%). Оставшиеся 58,2 % поделили между собой молодые коллеги со стажем работы до 5 лет и от 6 до 10 лет (14,5% и 19,3% соответственно), а также более опытные доктора со стажем более 25 лет (23,7%) (рис. 5). При этом у большинства (43,4%) участников опроса не было категории. Коллеги с высшей категорией составляли долю в 37,3%. Первая и вторая категории были у 14,5% и 4,8% соответственно (рис. 6). Так же нужно отметить, что в опросе участвовало 27 кандидатов наук (10,8%) и даже 10 докторов наук (4%). Остальные участники ученой степени не имели (рис. 7).
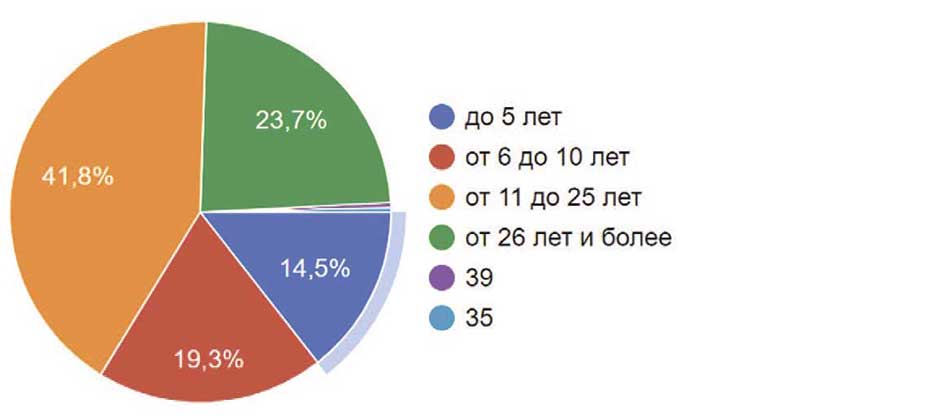
Рис.5.Стаж работы респондентов
Fig. 5. Work experience of respondents
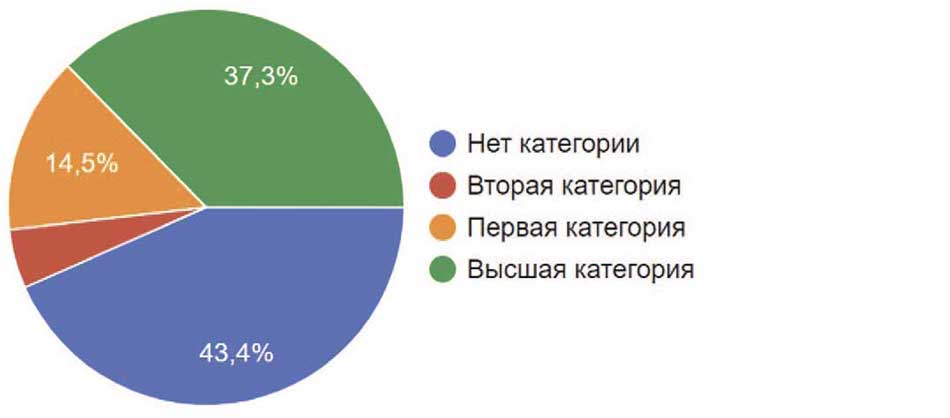
Рис. 6. Наличие категории у респондентов
Fig. 6. Availability of category among respondents
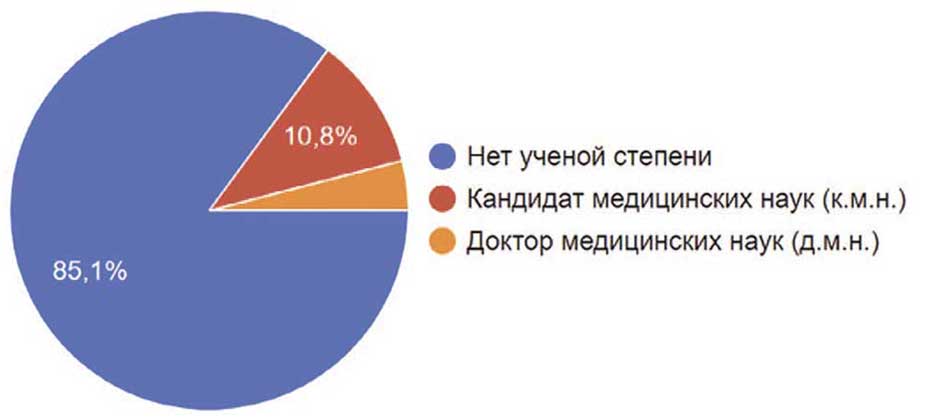
Рис. 7. Наличие ученой степени у респондентов
Fig. 7. The respondents have an academic degree
Подавляющее большинство (67%) опрошенных врачей являлись работниками государственных учреждений. Частные медицинские центры занимают второе место. На их долю приходится 26,9% врачей. 5,2% составляют врачи, работающие в ведомственных клиниках и 0,8% – в клиниках Министерства обороны РФ (рис. 8).
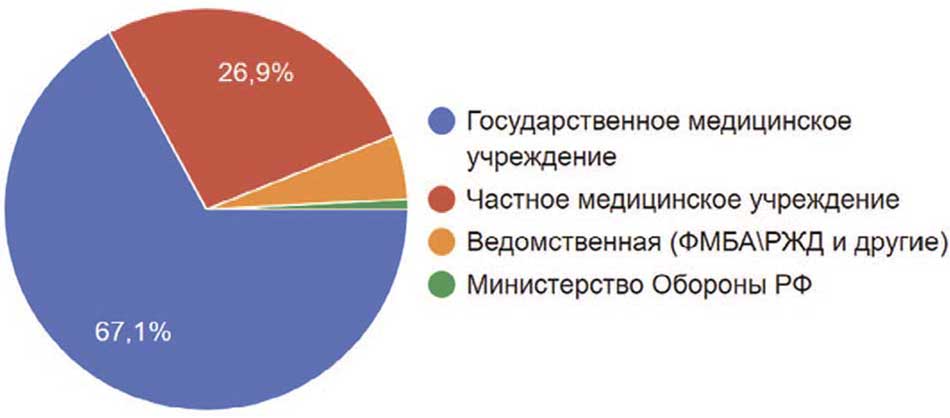
Рис. 8. Система здравоохранения, в которой работают респонденты
Fig.8. Health care system where respondents work
Среди опрошенных 50,2% докторов работали в стационаре, 49,4% – в амбулаторном звене. Один доктор работал в клинике (0,4%), а вот сотрудников реабилитационных центров, к сожалению, среди прошедших опрос, не было (рис. 9).
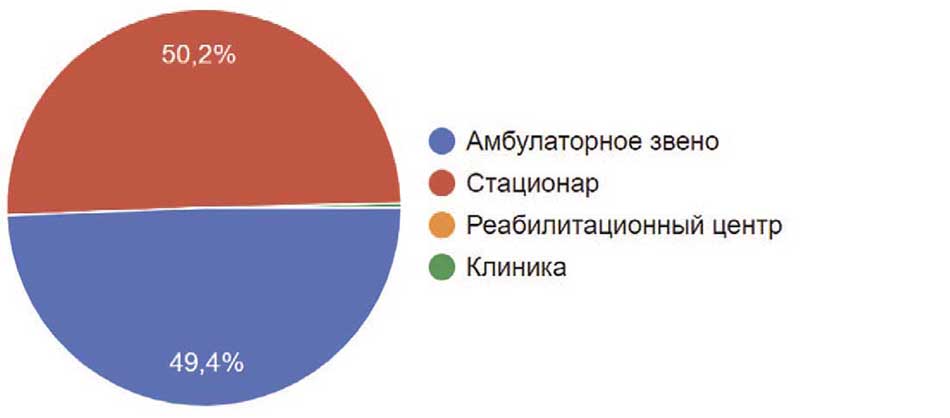
Рис. 9. Основное место работы респондентов
Fig. 9. Main place of work of the respondents
У подавляющего большинства опрошенных урологов (59,4%) количество пациентов с нейрогенными нарушениями мочеиспускания небольшое – не более 10%. У 31,7% урологов количество таких пациентов колебалось от 11% до 20%. Меньшее количество врачей (6,8%) работало с такими пациентами в 21-30% случаев. У 4 урологов (1,6%) доля пациентов с нейрогенной дисфункцией мочеиспускания составляет 31-40%, и только у 1 уролога (0,4%) доля таких пациентов составляла более 40%. Возможно, что это уролог, работающий в специализированной неврологической или нейрохирургической клинике (рис. 10).
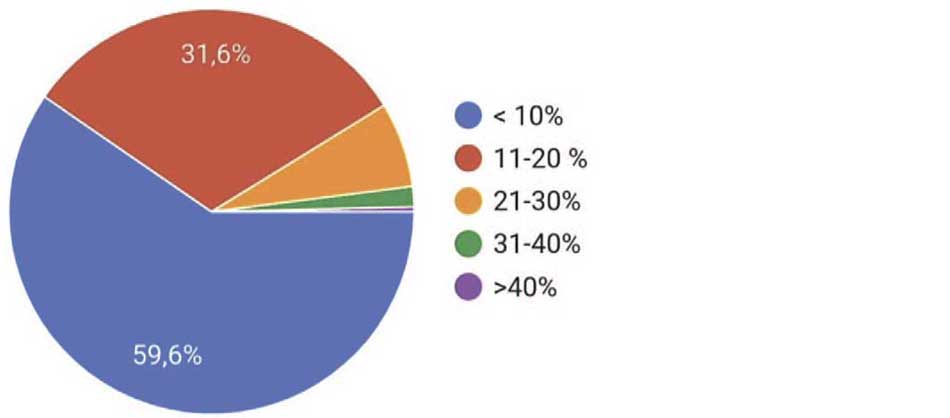
Рис. 10. Процент пациентов с нейрогенной дисфункцией мочеиспускания в практике респондентов
Fig. 10. Percentage of patients with neurogenic urinary dysfunction in the practice of respondents
Среди пациентов в большинстве случаев (46,2%) преобладали нарушения мочеиспускания в фазу опорожнения мочевого пузыря, у 20,5% больных отмечено нарушение в фазу наполнения мочевого пузыря и у 33,3% имелась смешанная симптоматика (рис. 11).
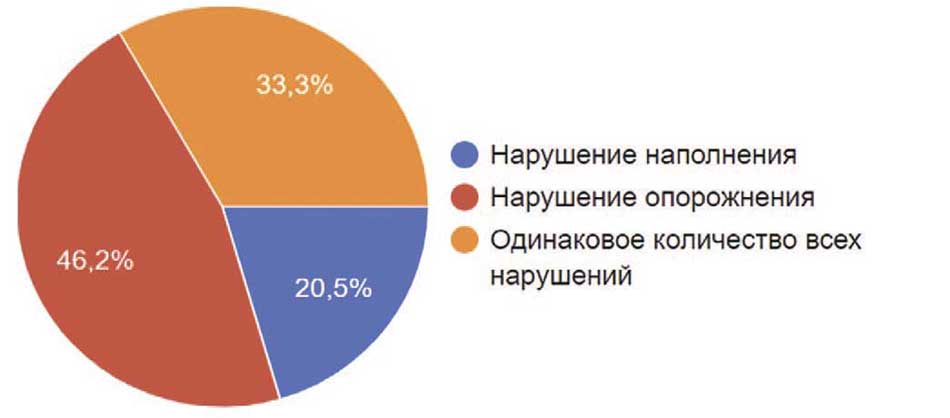
Рис. 11. Виды нарушения мочеиспускания, встречающиеся в практике респондентов
Fig. 11. Types of urinary disorders occurring in the practice of respondents
При наблюдении и ведении пациентов с нейрогенными нарушениями мочеиспускания в качестве контроля за состоянием верхних мочевых путей большинство урологов предпочитали использовать ультразвуковое исследование (УЗИ) и определение уровня почечных показателей биохимии крови: 245 (98,4%) и 231 (92%) опрошенных соответственно. 210 (84,3%) опрошенных в качестве контроля за состоянием верхних мочевых путей использовали общий анализ мочи. 129 (51,8%) урологов выполняли своим пациентам компьютерную томографию, а 69 (27,7%) предпочитали экскреторную урографию (рис. 12).
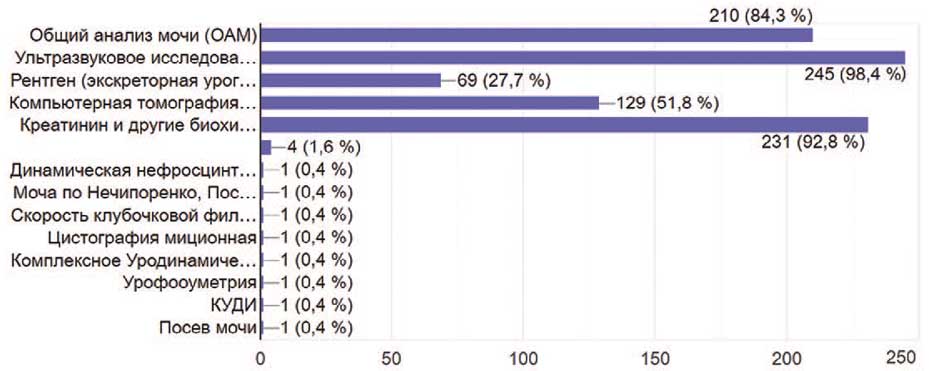
Рис. 12. Контроль за состоянием верхних мочевых путей респондентами (можно выбрать несколько ответов)
Fig. 12. Monitoring the condition of the upper urinary tract by respondents. (It is
possible to select multiple answers)
С целью контроля за состоянием нижних мочевых путей большинство (96,4%) опрошенных использовали УЗИ. Почти 72% выполняли урофлоуметрию, а около 40% проводили цистоскопию. Всего лишь 28,1% выполняли пациентам уродинамическое исследование и почти 13% – микционную цистографию (рис. 13). При этом частота контроля за состоянием нижних мочевых путей у 43,8% урологов осуществлялась не реже 1 раза в 3 месяца, 38,2% предпочитали контроль 1 раз в 6 месяцев, 10% коллег – 1 раз в год. Однако есть и те (7,2%), кто контролировал 1 раз в месяц, а 2 врача (0,8%) контроль не проводили (рис. 14).
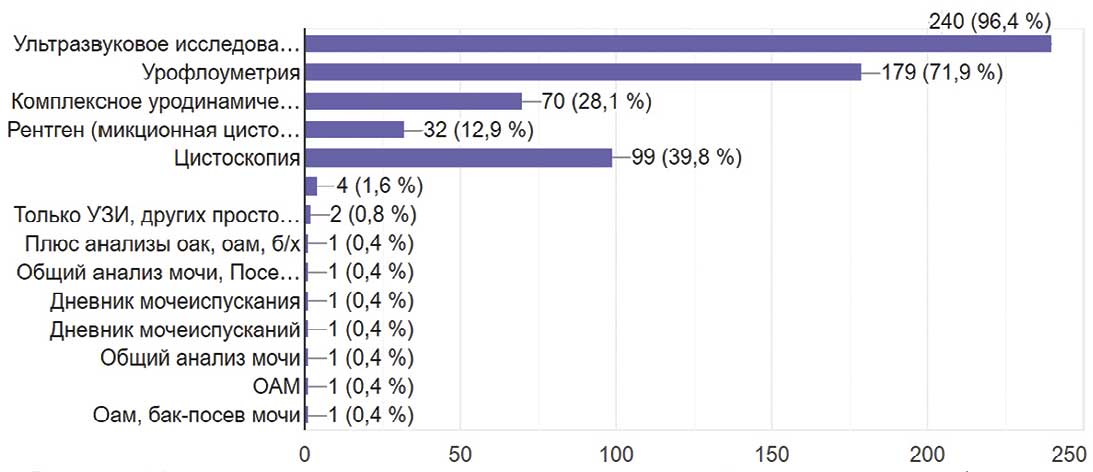
Рис. 13. Контроль состояния нижних мочевых путей респондентами (можно выбрать несколько ответов)
Fig. 13. Monitoring the condition of the lower urinary tract by respondents. (It is
possible to select multiple answers)
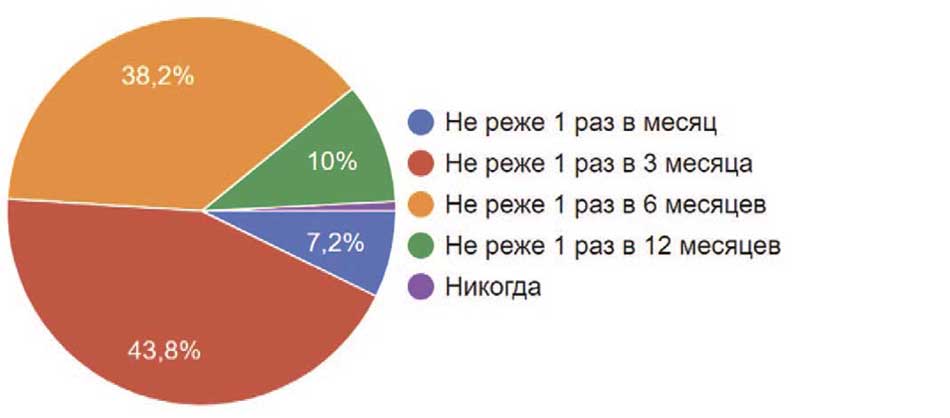
Рис. 14. Частота контроля состояния нижних мочевых путей при длительном наблюдении респондентами
Fig. 14. Frequency of monitoring the condition of the lower urinary tract during long-term observation by respondents
Если говорить о конкретных методах обследований, то цистоскопию у пациентов с нейрогенными нарушениями мочеиспускания выполняли всем своим пациентам 17,3% опрошенных. 41% врачей выполняли цистоскопию только тем пациентам, у которых выявлена гематурия, 21,7% – пациентам с длительным нарушением мочеиспускания, 59,4% – только тем пациентам, у которых обнаружена патология при УЗИ, а 29% опрошенных не выполняют цистоскопию своим пациентам (рис. 15).
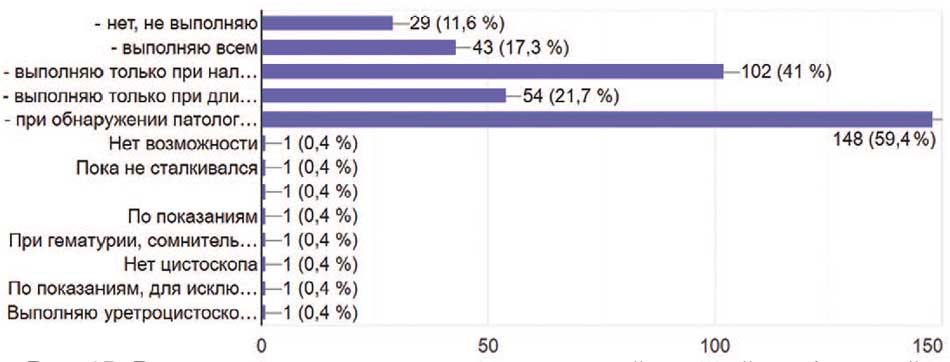
Рис. 15. Выполнение цистоскопии пациентам с нейрогенной дисфункцией нижних мочевых путей респондентами
Fig. 15. Cystoscopy performed in patients with neurogenic dysfunction of the
lower urinary tract by respondents
Дневник мочеиспускания – самый простой и доступный метод контроля функции мочевого пузыря, рекомендуют 61,8% урологов, 27,7% рекомендуют дневник мочеиспускания только однократно на первичном приеме, а 5,2% вообще никогда не используют дневник мочеиспускания как метод диагностики у своих пациентов (рис. 16).
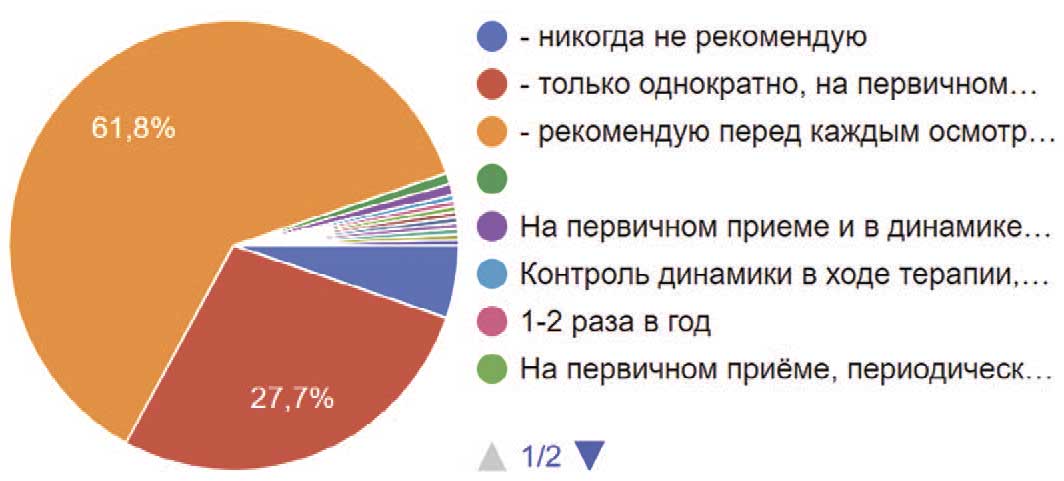
Рис. 16. Частота рекомендации пациентам заполнение дневника мочеиспускания респондентами
Fig. 16. Frequency of recommendations for patients to complete a voiding diary by respondents
Оценка рефлексов мочеиспускания – важный раздел обследования неврологического пациента с нарушениями процесса опорожнения мочевого пузыря. В своей практике его использует 41% врачей, но однократно и на первичном осмотре, 18,5% оценивают рефлексы на каждом приеме, а 37,8% никогда не оценивают рефлексы и чувствительность в урогенитальной зоне (рис. 17).
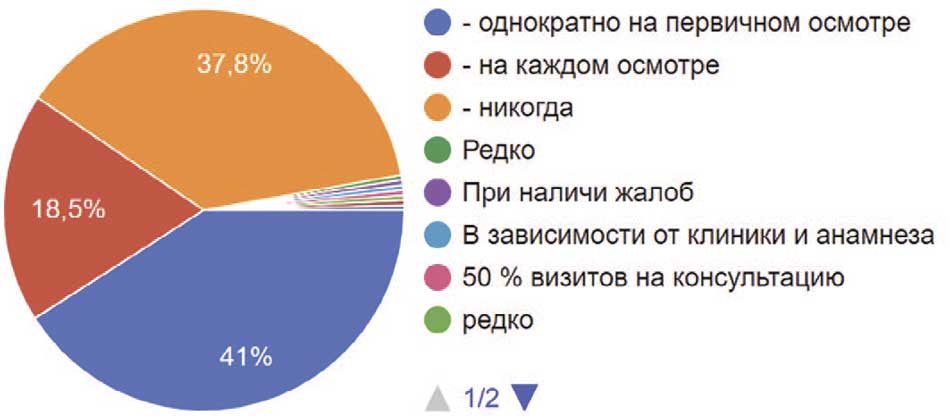
Рис. 17. Частота оценки рефлексов и чувствительности в урогенитальной зоне у пациентов респондентами
Fig. 17. Frequency of assessment of reflexes and sensitivity in the urogenital area in patients by respondents
Нарушение функции кишечника может быть взаимосвязано с нарушением функции мочевого пузыря, так как оба иннервируются из одного сегмента спинного мозга. Среди опрошенных 47,4% оценивали функцию кишечника только на первичном приема, в то время как 35,3% оценивают на каждом приеме. При этом 16,1% не оценивают функцию кишечника у своих пациентов (рис. 18).
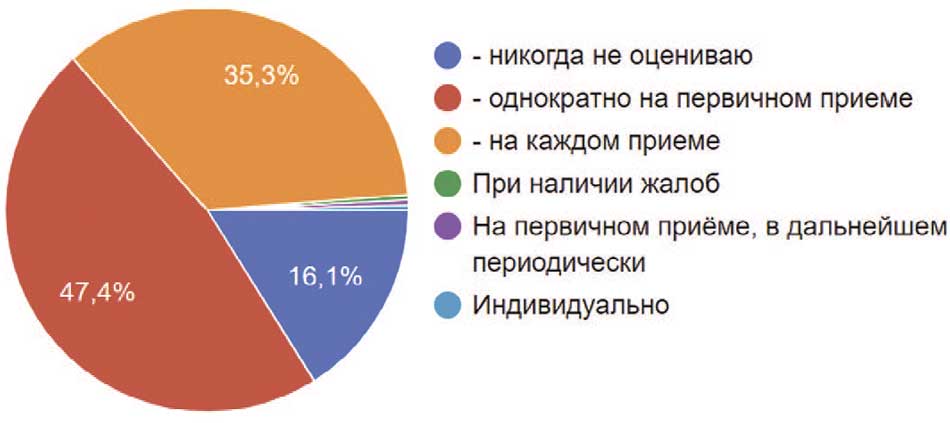
Рис. 18. Оценка функции кишечника у пациентов респондентами
Fig. 18. Assessing bowel function in patients by respondents
Объем остаточной мочи – важный показатель для любого урологического пациента, но для пациентов с нейрогенной дисфункцией мочевого пузыря он имеет особое значение, поэтому необходимо осуществлять контроль за объемом остаточной мочи у этой категории пациентов. Так почти половина опрошенных (46,6%) выполняли контроль остаточной мочи каждые 3 месяца, 33,7% урологов предпочитают это делать 1 раз в 6 месяцев, в то время как 4,8% выполняли контроль только 1 раз в год. Однако есть и те, кто выполнял контроль 1 раз в месяц – их 10,8%. Некоторые урологи считают, что это надо делать в зависимости от клинической картины и получаемых данных; когда возникает вопрос о решении установки цистостомы; при нахождении в стационаре. Врачей, не выполняющих контроль объема остаточной мочи, не было (рис. 19).
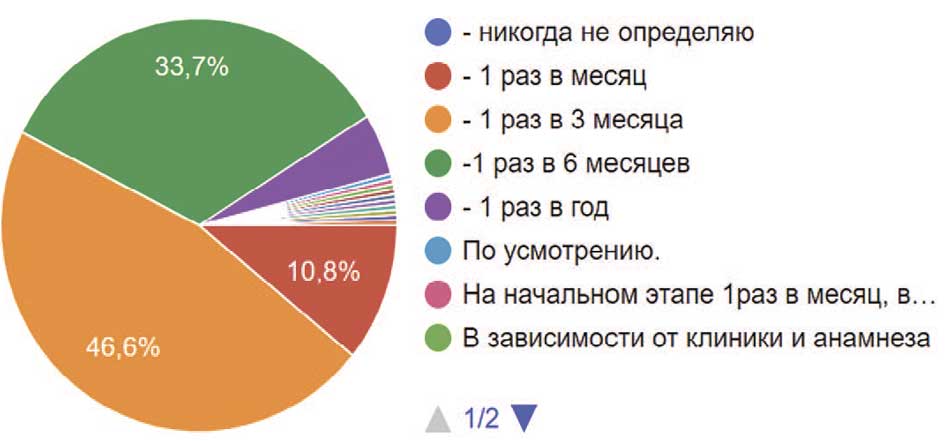
Рис. 19. Частота определения объем остаточной мочи у пациентов респондентами
Fig. 19. Frequency of determining the volume of residual urine in patients by respondents
В отношении показаний для назначения посева мочи на микрофлору мнения разделились: 37,3% опрошенных выполняли это исследование только пациентам с бактериурией в общем анализе мочи, 26,9% – при лейкоцитурии и без бактериурии, 14,5% пациентам – с бактериурией в любом титре, 12,4% – при любом повышении температуры, 2% – выполняли посев всем пациентам. Единичные участники ответили, что выполняют посев пациентам с риском развития инфекции; пациентам, попадающим под критерии первых трех вариантов ответа; при первом посещении; при бактериурии с увеличением лейкоцитов; после проведенной антибактериальной терапии; беременным, при обострении хронических заболеваний, для контроля излеченности при отсутствии стомы и катетера; практически всем; при дизурии, обострении хронического цистита, признаках пиелонефрита и мочекаменной болезни (МКБ); при часто рецидивирующей острой инфекции верхних мочевых путей (ИВМП); чаще при лейкоцитурии и бактериурии, для назначения эффективной лекарственной терапии; всегда при первичном обращении (рис. 20).
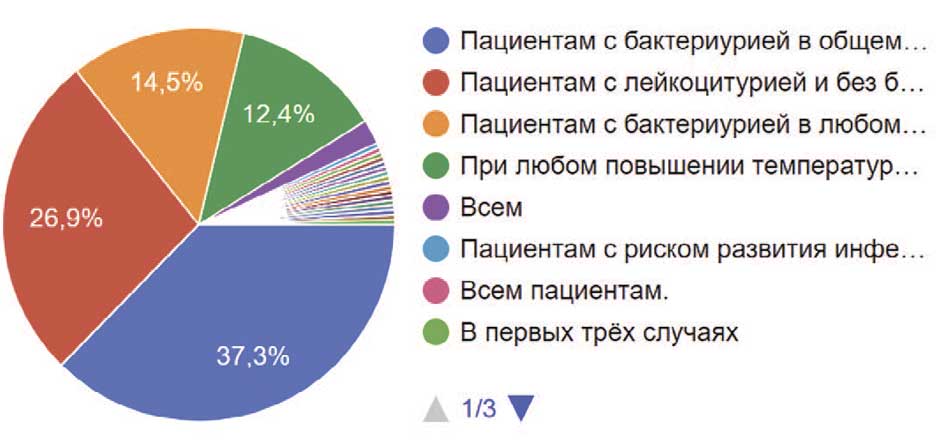
Рис. 20. Причина назначения бактериального посева мочи респондентами
Fig. 20. Reason for prescribing bacterial urine culture by respondents
Нарушение работы почек на фоне нейрогенных нарушений мочевого пузыря – самое опасное состояние, которое может стать фатальным, в связи с чем контроль является очень важным критерием сохранной функции почек. Почти половина урологов (48,6%) определяют уровень креатинина 1 раз в 3 месяца, 32,5% определяют его 1 раз в 6 месяцев, 9,2% – только 1 раз в год. Есть коллеги, которые будут определять уровень креатинина ежемесячно (4,4% опрошенных), в то время как 3,6% не будут определять его вообще у пациентов с нейрогенными расстройствами мочеиспускания. 0,8% будут контролировать только при обращении пациента и 1 уролог (0,4%) будет определять уровень креатинина только при нахождении пациента в стационаре (рис. 21).
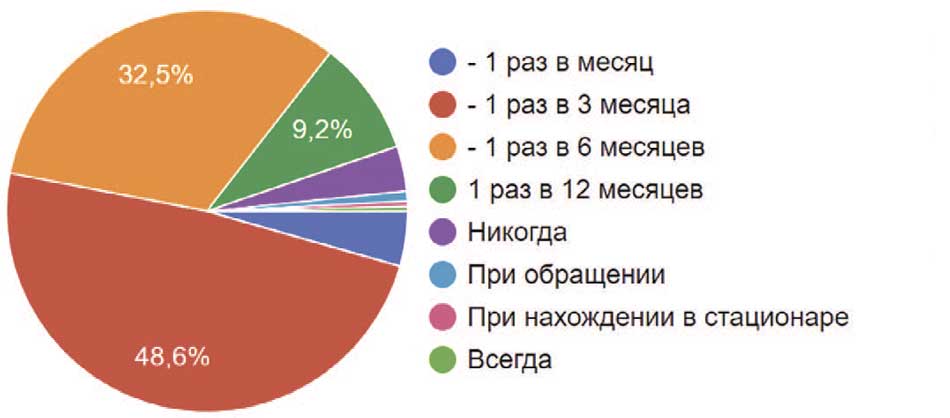
Рис. 21. Частота оценки уровня креатинина в сыворотке крови у пациентов с нейрогенными расстройствами мочеиспускания респондентами
Fig. 21. Frequency of assessing serum creatinine levels in patients with neurogenic voiding disorders by respondents
Проведение урофлоуметрии – важный этап обследования пациентов с нарушением процесса мочеиспускания, а определение объема остаточной мочи сразу после исследования дает возможность расширить понимание процесса мочеиспускания. Более того, определение остаточной мочи после урофлоуметрии является золотым стандартом этого исследования, при этом способы определения остаточной мочи у каждого специалиста могут быть разные.
Среди 250 опрошенных 202 специалиста (81,5%) выполняли определение объема остаточной мочи методом УЗИ. 3,6% выполняли контроль остаточной мочи путем катетеризации мочевого пузыря после урофлоуметрии. 2,4% опрошенных выполняли урофлоуметрию пациентам, но без определения объема остаточной мочи. По 1 человеку ответили, что урофлоуметрию в стационаре не делали, отметили отсутствие урофлоуметра, не отлажена логистика, отсутствие сертификата УЗИ или аппарата УЗИ в кабинете. Один человек отметил, что владеет «оригинальной методикой» (рис. 22).
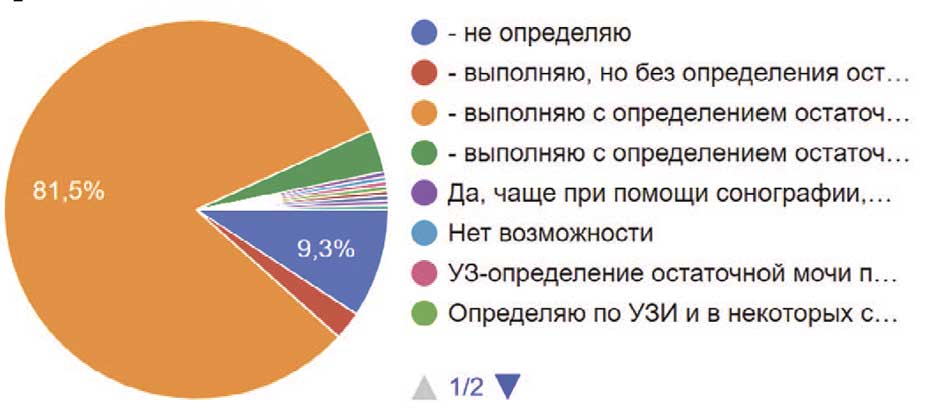
Рис. 22. Определение объема остаточной мочи у пациентов после проведения урофлоуметрии у пациентов с нейрогенной дисфункцией мочеиспускания респондентами
Fig. 22. Determination of the volume of residual urine in patients after uroflowmetry in patients with neurogenic dysfunction of urination by respondents
Пациенты с постоянными уретральными дренажами находятся в группе высокого риска по инфекциям мочевыводящих путей. Ведение, наблюдение и лечение инфекций у таких пациентов всегда вызывало массу дискуссий и разногласий. В нашем исследовании также мнения разделились. Большинство респондентов (40,2%) назначали посев мочи, но только при появлении клиники острого цистита или пиелонефрита. 22,5% назначали 1 раз в 3 месяца, 9,6% – 1 раз в 6 месяцев, а 2% рекомендовали выполнять посев 1 раз в год, при том, что 14,9% вообще не назначали посев мочи таким пациентам (рис. 23).
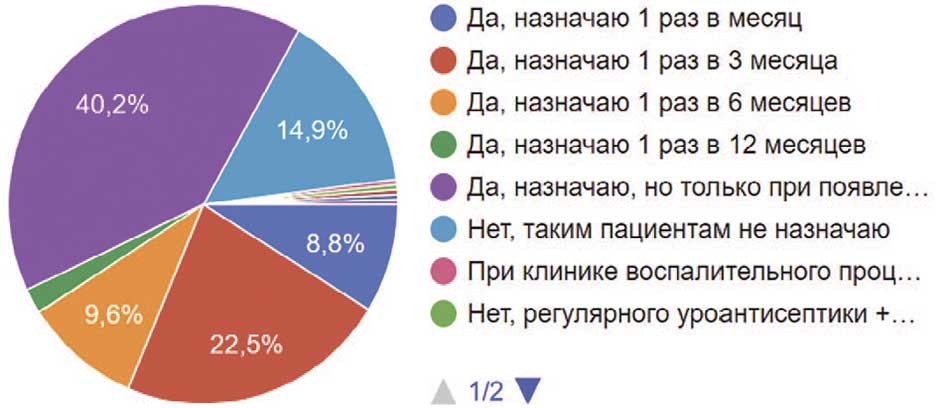
Рис. 23. Частота назначения бактериального посева мочи пациентам с постоянными уретральными катетерами/цистостомами респондентами
Fig. 23. Frequency of urine bacterial culture in patients with indwelling urethral catheters/cystostomies by respondents
Комплексное уродинамическое исследование (КУДИ) – способ понять «механизм» нарушения мочеиспускания, является основным методом обследования для пациентов с нейрогенными нарушениями мочеиспускания, необходимым как для постановки диагноза, так и для определения тактики ведения. Данное исследование требует от специалиста определенных знаний и навыков работы с непростым оборудованием. К сожалению, только у 64% опрошенных урологов есть возможность проведения уродинамического исследования пациентам. Среди них – 7 урологов (2,8%), которые имеют возможность выполнить КУДИ своим пациентам, но направляют к другим специалистам своей же клиники, 10,8% выполняет исследование самостоятельно, 32% вынуждены направлять в другую клинику города, а 18,1% – в другую клинику региона или области (рис. 24).
КУДИ является дорогостоящим, в связи с высокой стоимостью расходных материалов, поэтому актуален вопрос о финансовой возможности выполнения данного исследования у пациентов, особенно с инвалидностью, так как не во всех регионах и клиниках есть возможность выполнения данного исследования в рамках обязательного медицинского страхования (ОМС) по медицинскому полису.
По данным опроса 34,2% медицинских учреждений России могут выполнять КУДИ в рамках обязательного медицинского страхования. Из них в 19,7% лечебно-профилактических учреждениях (ЛПУ) есть возможность выполнить КУДИ по медицинскому полису, но только для жителей региона, и лишь 14,5% клиник выполняет это исследование по полису для любого гражданина России. Больше половины клиник (52,2%) могут выполнять КУДИ только платно.
В 13,6% ЛПУ России нет возможности выполнить исследование для своих пациентов по разным причинам, но самая распространенная – это отсутствие уродинамической лаборатории (рис. 25).
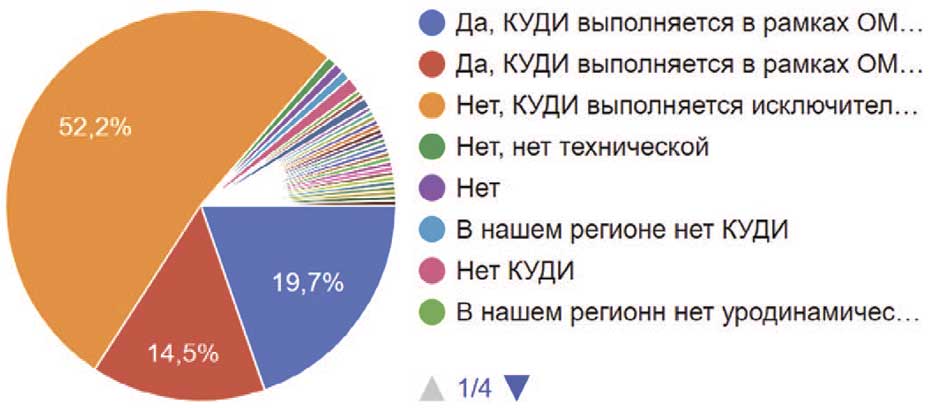
Рис. 25. Возможность выполнения КУДИ в вашем городе/районе/области пациентам в рамках обязательного медицинского страхования (ОМС)
Fig. 25. The ability to perform a complex urodynamic study in your city/district/region for patients under of compulsory health insurance
Невзирая на все сложности выполнения КУДИ и его высокую стоимость, каждый уролог в своей практике сталкивался с необходимостью рекомендовать своим пациентам уродинамическое исследование. У 74,7% врачей таких пациентов в месяц было не более 10, от 10 до 20 таких пациентов принимал 15,3% урологов, у 8 врачей (3,2%) таких пациентов было от 20 до 30 в месяц и у 7 врачей – более 30 пациентов в месяц, которым необходимо рекомендовать КУДИ. У остальных ответивших либо нет необходимости назначить КУДИ, либо пациенты не выполняют рекомендации лечащего уролога (рис. 26).
Учитывая, что у пациентов с неврологическими нарушениями мочеиспускания клиническая и уродинамическая картина могут изменяться и требовать корректировки лечения, таким пациентам необходимо выполнять периодический контроль уродинамических исследований. В данном вопросе так же нет единого мнения – 31,3% респондентов рекомендовали контрольное КУДИ 1 раз в год, чуть менее четверти опрошенных (24,1%) проводили контроль 1 раз в 6 месяцев, а 6,4% проводили повторные КУДИ 1 раз в 3 месяца, в то время как 4,8% проводили контроль уродинамики только 1 раз в 2 года, при этом не рекомендовали контрольное КУДИ четверть респондентов (25,3%). У оставшихся почти 11% либо не было возможности выполнить КУДИ, либо они полагались на мнение коллеги, который непосредственно занимался проведением этого исследования (рис. 27).
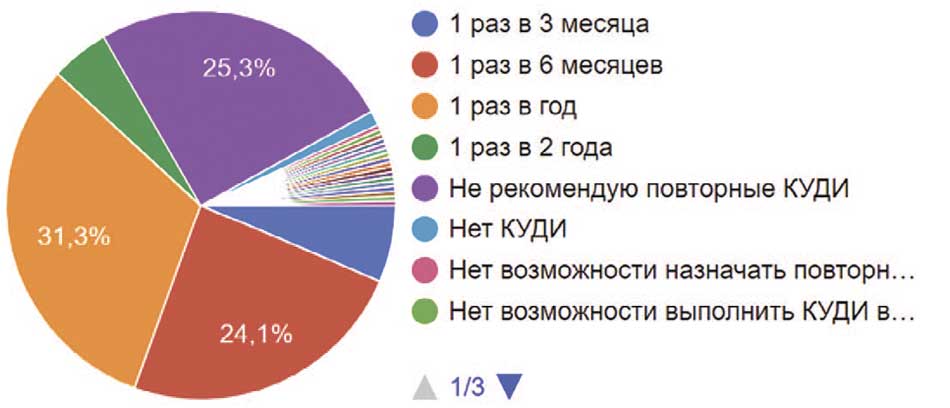
Рис. 27. Нуждаемость респондентов в повторном КУДИ при длительном наблюдении. Если да, то через какой интервал времени?
Fig. 27. The need of respondents for repeated complex urodynamic study during long-term follow-up. If yes, then after what time interval?
Вопросы о тактике терапии пациентов с нейрогенными нарушениями мочевого пузыря так же, как и вопросы диагностики порождают большое количество дискуссий. Так, при нарушении функции накопления мочевого пузыря почти 70% порекомендуют М-холиноблокаторы своим пациентам, в то время как 14,1% порекомендуют β-адреномиметики, 9,2% предпочтут αадреноблокаторы для купирования симптомов накопления. Были и те, кто порекомендовал своим пациентам фитопрепараты – их 6 человек (2,4%) среди опрошенных. Но также были и другие специалисты, которые порекомендовали периодическую катетеризацию (1,6%) или постоянный мочевой дренаж (постоянный уретральный катетер (0,4%) или цистостому (0,4%), 3 человека (1,2%) предпочли пептиды, остальные выбрали комбинированную терапию (рис. 28).
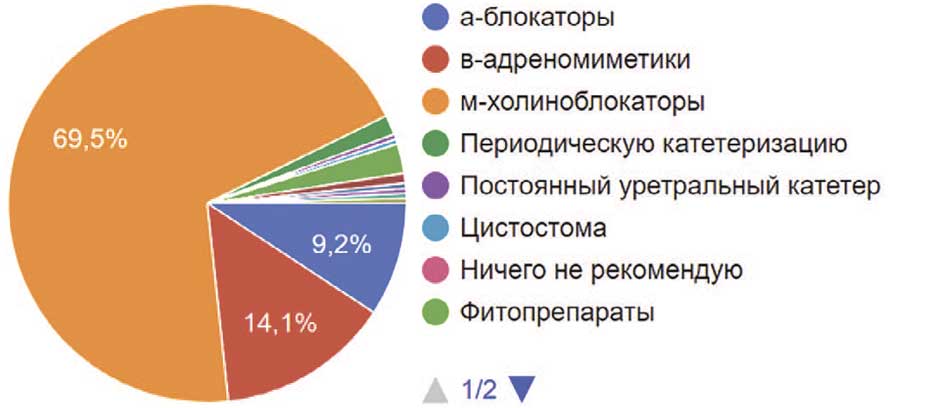
Рис. 28. Рекомендуемая респондентами терапия пациентам с нарушением функции накопления мочевого пузыря
Fig. 28. Therapy recommended of respondents for patients with bladder storage dysfunction
В отношении пациентов с симптомами опорожнения ситуация тоже непростая. Подавляющее большинство – 89,2%, предпочли α-адреноблокаторы, 7,25 порекомендовали β-адреномиметики, а 10,4% вообще – М-холиноблокаторы. При этом 14,1% лечили пациентов фитопрепаратами, 10 человек (4%) – назначали но-шпу, а 12 человек (4,8%) – пептиды. Один доктор (0,4%) вообще ничего не назначал таким пациентам. Оставшиеся 3,6% порекомендовали либо М-холиномиметики, либо периодическую катетеризацию (рис. 29).
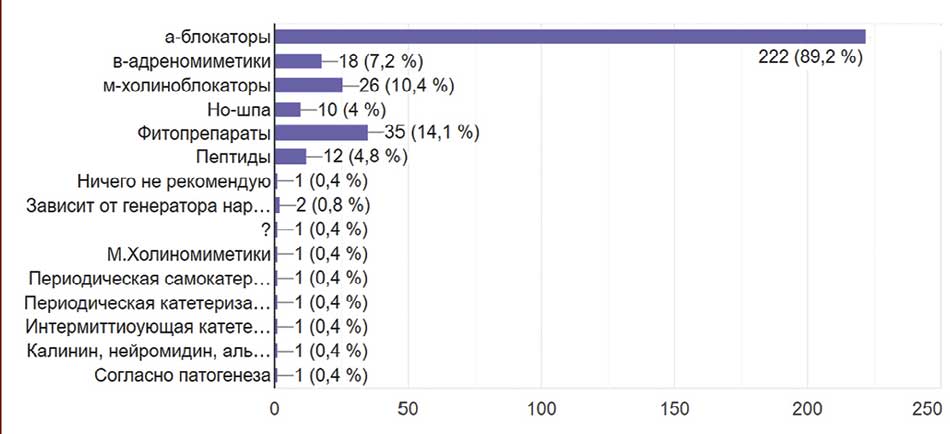
Рис. 29. Рекомендуемая респондентами терапия пациентам с нарушением опорожнения мочевого пузыря
Fig. 29. Therapy recommended of respondents for patients with bladder emptying disorders
Причины нарушения опорожнения мочевого пузыря могут быть различны. В случае, когда консервативными медикаментозными средствами улучшить процесс опорожнения мочевого пузыря не удается, 72,7% рекомендовали периодическую катетеризацию пациентам, почти 29% предложили использование постоянного мочевого дренажа, из них 17,9% наложат цистостому, а 11% установят уретральный катетер. Так же есть и те (4%), кто предложит использовать памперс (рис. 30).
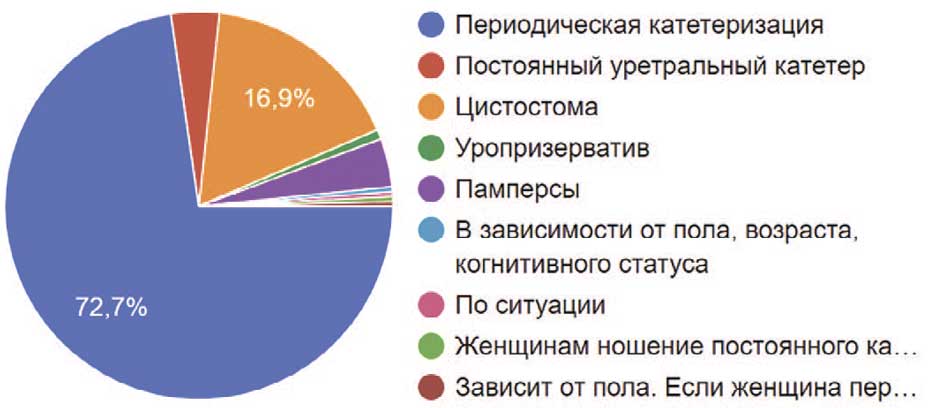
Рис. 30. Методы отведения мочи у пациентов с нарушением опорожнения мочевого пузыря нейрогенной природы, рекомендованные респондентами
Fig. 30. Methods of urine diversion in patients with bladder emptying disorders of a neurogenic nature recommended by respondents
В случае, если причиной нарушения опорожнения мочевого пузыря будет гипоактивность (арефлексия или атония) мочевого пузыря на фоне поражения спинного мозга, то большинство (45,8%) респондентов чаще всего рекомендовали периодическую катетеризацию. Почти четверть (23,7%) чаще предлагали наложение цистостомы, а 18,1% просто направили пациентов к нейроурологу, вероятно для того, чтобы нейроуролог принимал решение о наиболее подходящем способе опорожнения мочевого пузыря у данных пациентов, исходя из его неврологического статуса, а 3,2% направляют пациента к неврологу, 3,6% так же чаще устанавливают постоянный уретральный катетер (рис. 31).

Рис. 31. Рекомендации респондентов пациентам при гипоактивности (арефлексии/атонии) мочевого пузыря (детрузора) на фоне поражения спинного мозга
Fig. 31. Recommendations by respondents for patients with hypoactivity (areflexia/atony) of the bladder (detrusor) due to spinal cord damage
Пациенты с нейрогенными нарушениями мочеиспускания подвержены частым обострениям инфекций мочевыводящих путей, что требует правильного подбора терапии. Подавляющее большинство опрошенных нами специалистов (83,9%) назначали антибактериальную терапию только при наличии клинически значимой инфекции мочевыводящих путей, 10% респондентов ответили, что назначают антибиотики только при наличии повышенного содержания лейкоцитов в общем анализе мочи. При наличии только бактерий в общем анализе мочи антибиотик рекомендовали 2,4% опрошенных, в то время как 2,8% рекомендовали антибиотик только при обнаружении бактерий в посеве мочи в любом титре. Один (0,4%) уролог рекомендовал антибактериальную терапию при клинических признаках воспаления, подтвержденных анализами (рис. 32).
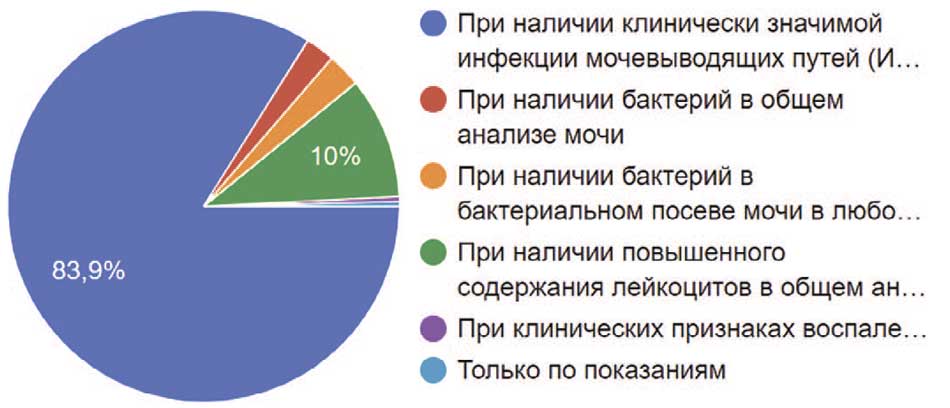
Рис. 32. Причины назначения антибактериальной терапии респондентами
Fig. 32. Reasons for prescribing antibacterial therapy by respondents
Пациентов, для которых установка постоянного мочевого дренажа (цистостома или постоянный уретральный катетер) была единственным способом отведения мочи, постоянно сопровождает бактериурия. Антибактериальная терапия у таких пациентов всегда была предметом жарких дискуссий среди урологов. Половина опрошенных нами урологов (50,2%) не проводила антибактериальную терапию таким пациентам. Четверть (24,9%) проводили антибактериальную терапию пациентам при обнаружении одного и того же штамма бактерий в двух посевах мочи. 15,7% респондентов назначали антибиотики только при наличии повышенного количества лейкоцитов в общем анализе мочи, и 8,4% проводили терапию антибиотиками всегда (рис. 33).
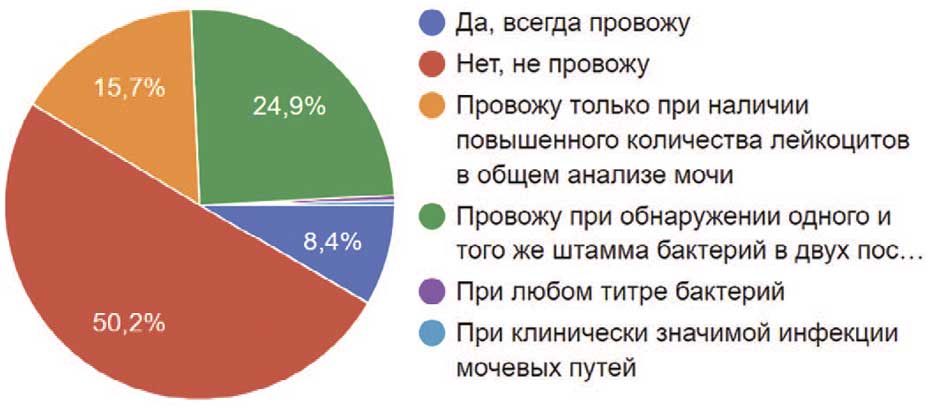
Рис. 33. Проведение респондентами антибактериальной терапии ИМП пациентам с постоянным катетером/цистостомой и бактериурией при отсутствии симптомов (бессимптомная бактериурия)
Fig. 33. Conducting antibacterial therapy for UTI by respondents in patients with an indwelling catheter/cystostomy and bacteriuria in the absence of symptoms (asymptomatic bacteriuria)
Профилактика мочевой инфекции – дискутабельный вопрос среди урологов, клинических фармакологов, терапевтов. Назначать антибактериальную профилактику или нет? Почти 70% опрошенных считали, что антибактериальную профилактику мочевой инфекции на фоне постоянных мочевых дренажей проводить не требуется, около 20% считали, что назначение возможно в ежемесячном режиме, но в стандартных дозах на рекомендованный курс 3-5-7-10 дней. 4,8% назначали на длительный срок (до 30 дней), но в малых дозах препарата, а 4% – в малых дозах и на постоянной основе. Профилактику уросептиками проводили 0,8% опрошенных. По 1 урологу (по 0,4%) назначали антибиотик только первые 7-10 дней после установки дренажа и фитопрепараты (рис. 34).
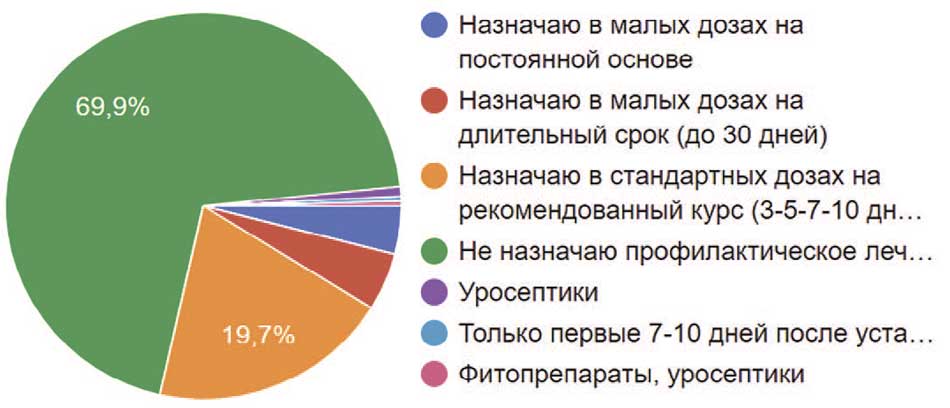
Рис. 34. Назначение респондентами профилактического антибактериального лечения пациентам с постоянными мочевыми дренажами (уретральный катетер/цистостома)
Fig. 34. Prescription by respondents of prophylactic antibacterial treatment for patients with permanent urinary drainage (urethral catheter/cystostomy)
Такая же ситуация отмечена и у пациентов, находящихся на интермитирующей катетеризации. Подавляющее большинство урологов (75,1%) не назначали профилактическую антибактериальную терапию. В стандартных дозах рекомендовали почти 13%, что меньше на 3%, чем у пациентов с постоянными мочевыми дренажами. Меньше и количество врачей, рекомендующих назначение антибиотиков в малых дозах до 30 дней – 2,4%, однако количество врачей, назначающих антибиотик в малых дозах, но на постоянной основе колеблется от 4% до 6,4% (рис. 35).
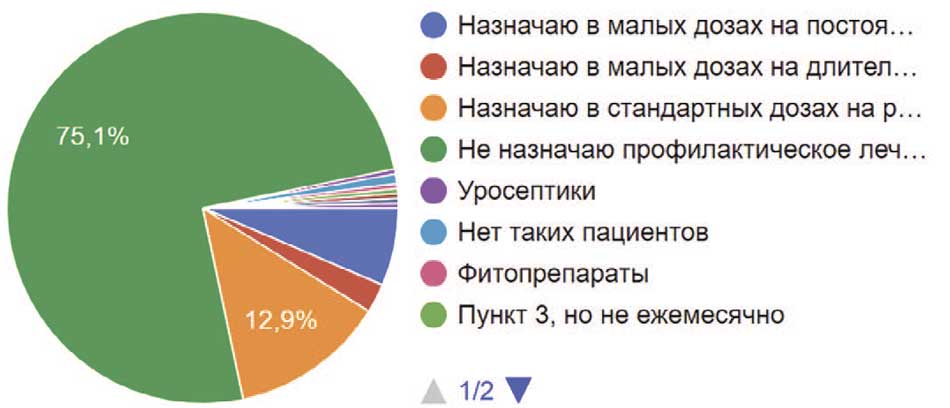
Рис. 35. Назначение респондентами профилактического антибактериального лечение пациентам, находящимся на периодической катетеризации
Fig. 35. Prescription by respondents of prophylactic antibacterial treatment for patients undergoing intermittent catheterization
У пациентов с нейрогенными расстройствами мочеиспускания клиника этих нарушений может быть различна в зависимости от уровня поражения нервной системы. Это могут быть симптомы как накопления, так и опорожнения, но существует категория пациентов, у которых имеется комбинация симптомов. Такие пациенты вынуждены принимать М-холиноблокаторы для устранения гиперактивности и, прежде всего, снижения повышенного детрузорного давления, которое опасно для почек, а также выполнять периодическую катетеризацию мочевого пузыря в связи с наличием большого количества остаточной мочи. Данная категория пациентов является одной из сложных, и подбор терапии так же вызывает определенные сложности у таких пациентов.
Исходя из нашего опроса, видно, что в случае повышения детрузорного давления и недержания мочи у пациента, находящегося на катетеризации, 37,8% коллег предпочли комбинировать М-холиноблокаторы и β-адреномиметики, 21% предпочли перевод пациента на монотерапию β-адреномиметиками. Одинаковое количество (по 11,6%) коллег увеличивали дозы М-холиноблокатора, а другие искали замену М-холиноблокатора. Ботулинотерапию предложили таким пациентам 12,9% коллег, а 2,8% порекомендовали уропрезерватив или гигиеническое белье. Аугментацию мочевого пузыря предложил 1 уролог (0,4%), остальные затруднялись ответить на этот вопрос (рис. 36). При этом в своей практике пациентам с постоянными мочевыми дренажами подавляющее большинство (81,5%) урологов не назначали антимускариновые препараты, 5,2% рекомендовали данную группу препаратов только пациентам с поражением шейного отдела спинного мозга, а 7,6% – только тем, у кого имелось супрасакральное поражение спинного мозга. 4,7% – назначали всем пациентам с постоянными катетерами антимускариновые препараты (рис. 37).
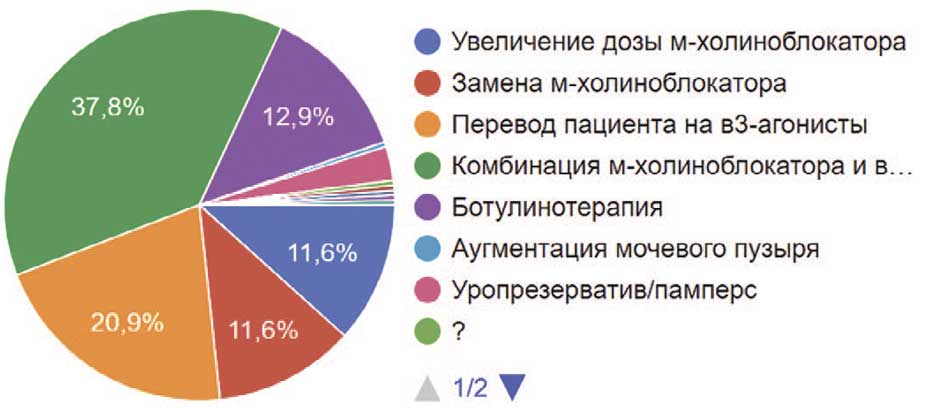
Рис. 36. Дальнейшие действия респондентов, если у пациента, находящегося на периодической катетеризации и принимающего м-холиноблокаторы, зафиксировано повышенное детрузорное давление и отмечается недержание мочи
Fig. 36. Further actions of respondents if a patient undergoing periodic catheterization and taking m-anticholinergic drugs has increased detrusor pressure and urinary incontinence
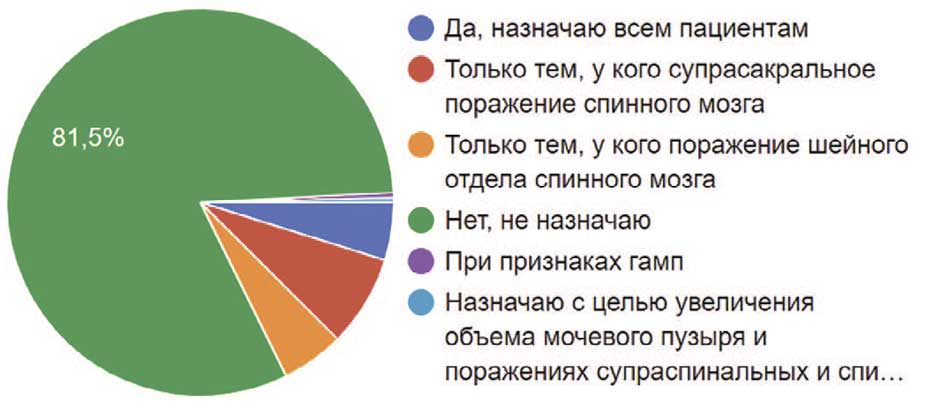
Рис. 37. Назначение респондентами пациентам с постоянным катетером антимускариновых препаратов
Fig. 37. Prescribing by respondents antimuscarinic drugs to patients with an indwelling catheter
Как изложено выше, пациенты, вынужденные использовать постоянные мочевые дренажи (цистостому или постоянный уретральный катетер), подвержены частым обострениям ИМП и находятся в группе повышенного риска, поэтому регулярность замены мочевого дренажа оказывает большое влияние на частоту возникновения инфекционных и других осложнений. Вопросы частоты замены постоянных мочевых дренажей часто являются поводом для активных дискуссий среди урологов, и нет однозначного мнения по этому вопросу. Что же касается цистостомического дренажа, подавляющее большинство (75,5%) выполняли его замену 1 раз в месяц, а 4,8% – 1 раз в 2 месяца, один раз в 2 недели рекомендовали замену цистостомы 9,2% и только 2,8% меняли цистостому 1 раз в 7 дней. Остальные урологи меняли цистостому в зависимости от складывающейся ситуации (рис. 38).

Рис. 38. Рекомендации респондентов по частоте замены цистостомического дренажа
Fig. 38. Respondents' recommendations on the frequency of cystostomy drainage
replacement
С заменой постоянного уретрального катетера ситуация выглядит немного иначе. 25,7% меняли катетер 1 раз в 3 месяца, количество рекомендующих замену катетера 1 раз в 2 месяца составило лишь 0,8%, значимо велико количество урологов, которые выполняли замену катетера каждые 7 дней с 2,8% до 36,5%. 5,6% опро5,6% опрошенных меняет катетер по мере нарушения его функционирования (рис. 39).
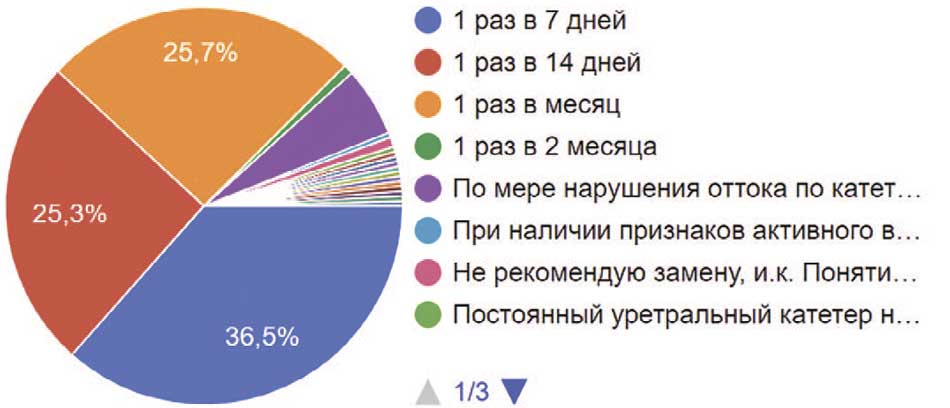
Рис. 39. Рекомендации респондентов по частоте замены постоянного уретрального катетера
Fig. 39. Respondents' recommendations on the frequency of indwelling urethral catheter replacement
При наличии у пациента постоянного мочевого дренажа многие врачи рекомендовали его промывание, что также вызывает споры среди специалистов о целесообразности данного мероприятия, хотя этот вопрос давно отражен в клинических рекомендациях, в том числе Федеральных [6]. Как показывает наше исследование, меньше половины опрошенных (41,4%) не рекомендовали промывание дренажей, при этом остальные рекомендовли промывание мочевого пузыря в ежедневном режиме (20,5%), другие – один раз в 3 дня (8%), при этом большинство сторонников промывания дренажа (28,9%) рекомендовали делать это только при нарушении признаков оттока (рис. 40).
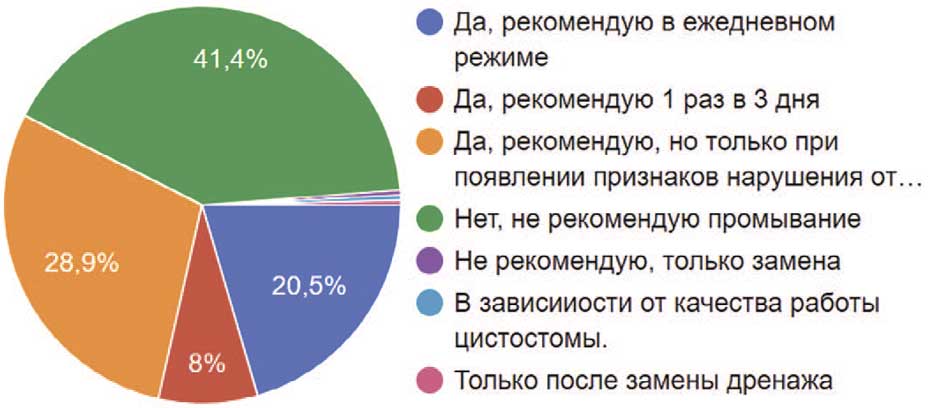
Рис. 40. Рекомендации респондентов по промыванию мочевого пузыря у пациентов с постоянным дренированием мочевого пузыря (уретральный катетер или цистостома)
Fig. 40. Respondents' recommendations on bladder lavage in patients with permanent bladder drainage (urethral catheter or cystostomy)
Пациенты, являющиеся постоянными носителями цистостомы или уретрального катетера, так же, как и пациенты, находящиеся на периодической катетеризации, нуждаются в регулярном наблюдении уролога. Так 51,4% урологов рекомендовали контрольную явку 1 раз в квартал обеим группам пациентов. Практически одинаковое количество (почти четверть опрошенных) приглашали пациентов с катетерами (24,1%) и на периодической катетеризации (24,5%) на контрольный осмотр 1 раз в 6 месяцев. Один раз в год на контроль приглашали пациентов с цистостомой 2,4% опрошенных, а пациентов на периодической катетеризации – 2,8%. Только при возникновении жалоб у пациентов с цистостомой – 7,2% и на катетеризации – 10,4% коллег проводили контрольную явку и обследование. В любой экстренной ситуации готовы принять и обследовать пациента с цистостомой 11,2% врачей и на периодической катетеризации – 8%. Остальные действовали исходя из конкретной ситуации (рис. 41, 42).
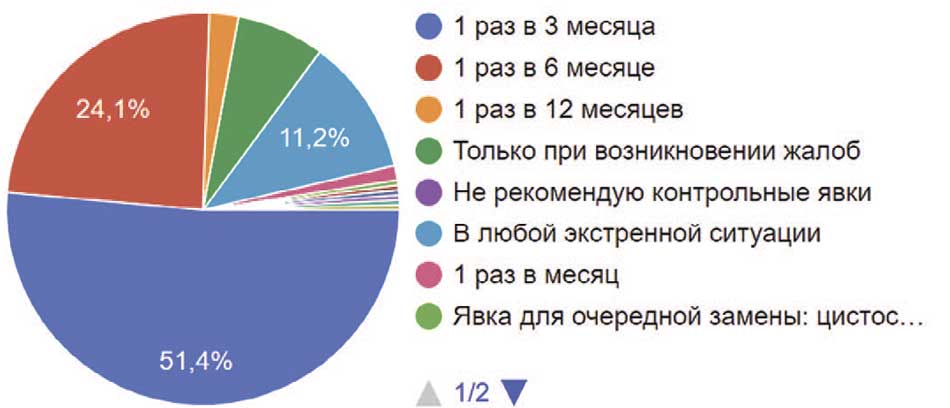
Рис. 41. Рекомендации респондентов по контрольной явке и контрольном плановом обследовании пациентов с постоянными мочевыми дренажами (цистостома/постоянный уретральный катетер)
Fig. 41. Respondents' recommendations for control attendance and routine control examination of patients with permanent urinary drainage (cystostomy/permanent urethral catheter)
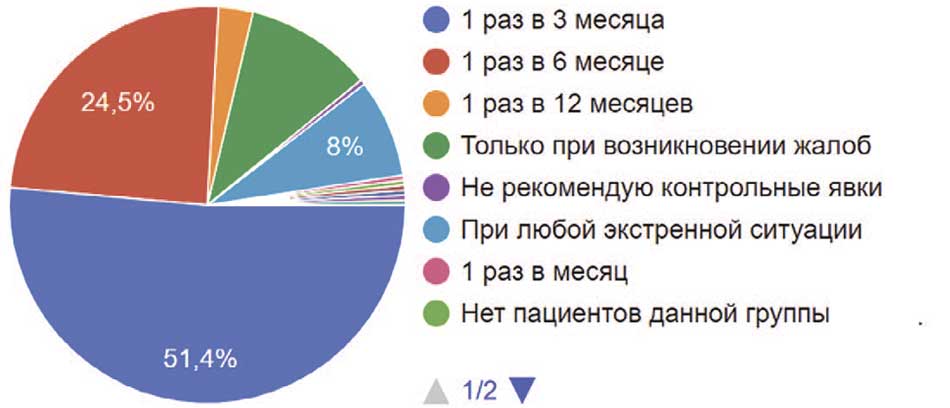
Рис. 42. Рекомендации респондентов по контрольной явке и контрольном плановом обследовании пациентов, находящимся на периодической катетеризации
Fig. 42. Respondents' recommendations for сontrol attendance and routine control examination of patients undergoing periodic catheterization
Нейроурологическая помощь – достаточно узконаправленная отрасль медицины, которая требует знаний не только в урологии, но и в неврологии, а также нейрохирургии. В связи с этим есть достаточно высокая потребность такого рода медицинской помощи в регионах. Из 250 опрошенных урологов 45,4% считают, что нейроурологическая помощь в их регионе организована удовлетворительно, а 20,5% отметили, что хорошо. 3,6% урологов поставили оценку «отлично», в то же время 27,7% отметили, что нет условий для организации медицинской помощи таким пациентам. Также были коллеги, которые отметили неудовлетворительную организацию, но их меньшинство (рис. 43).
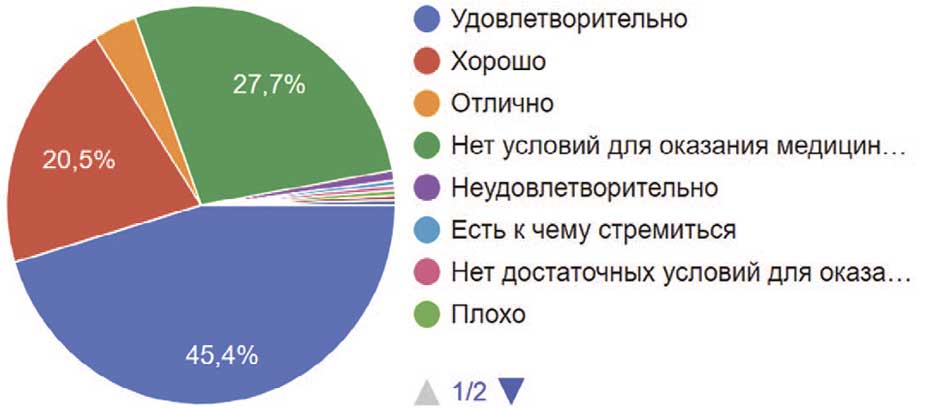
Рис. 43. Оценка респондентами нейроурологической помощи в регионе
Fig. 43. Evaluation by respondents of neurourological care in the region
ОБСУЖДЕНИЕ
Благодаря организации опроса на Всероссийском урологическом информационном портале Uroweb.ru, удалось проанализировать практику 250 урологов в отношении пациентов с нейрогенным мочевым пузырем. В опросе приняли участие урологи 8 Федеральных округов и 12 из 89 регионов России, это может указывать на сниженный интерес врачей к пациентам с нейрогенной дисфункцией мочевого пузыря, отсутствие опыта и знаний в этой предметной области, нежелание публично высказывать свое мнение.
По результатам опроса ведением пациентов неврологического профиля чаще всего занимаются специалисты амбулаторного звена и стационаров со стажем более 10 лет (66,2% опрошенных). Надо отметить, что ни один уролог из многочисленных реабилитационных центров Российской Федерации не изъявил желания участвовать в анкетировании, что, возможно, могло повлиять на результаты опроса. Однако мы считаем, что полученные данные хорошо отражают картину ведения таких пациентов рядовыми врачами в регионах.
В целом диагностическая тактика российских урологов приближена к национальным рекомендациям.
Мониторинг пациентов
Неврологические и нейрохирургические заболевания могут вызывать нарушение процесса мочеиспускания, вид которого будет зависить от уровня поражения нервной системы. Патология головного мозга тесно связана с нарушением функции накопления мочевого пузыря, в то время как поражение нижних отделов спинного – сопряжено с изменением его опорожнения. Регулярное наблюдение за пациентами с нейрогенными расстройствами мочеиспускания традиционно сосредоточено на предотвращении ухудшения состояния верхних мочевых путей и поддержании качества жизни.
Немаловажную роль играют осложнения, возникающие при нарушении опорожнения мочевого пузыря, такие как ИМП, мочекаменная болезнь, пузырномочеточниковый рефлюкс, гидронефроз и другие. Нужно заметить, что между всеми перечисленными осложнениями есть взаимосвязь, которая формирует своеобразный порочный круг. Таким образом, возникает необходимость в регулярном и обязательном наблюдении, а также периодическом обследовании пациентов с нарушениями опорожнения мочевого пузыря на фоне нейрогенной дисфункции.
Ряд авторов считает, что динамическое наблюдение и своевременное дообследование пациентов с дисфункцией опорожнения приводит к увеличению продолжительности и улучшению качества жизни этих пациентов, но не все урологические проблемы остаются решенными до конца [7].
В российских клинических рекомендациях, одобренных Минздравом России, указана периодичность обследования (общий анализ мочи, мочевина и креатинин крови, УЗИ почек и мочевого пузыря и уродинамические исследования) – один раз в год [3]. Результаты нашего опроса показали, что только 10% врачей следуют этому постулату, тогда как 43,8% рекомендуют контроль не реже 1 раза в 3 месяца, а 38,2% – в 6 месяцев. Подобная ситуация отмечена в голландском исследовании B. Rikken, B. Blok. 94% урологов Голландии занимались лечением пациентов с нейрогенным мочевым пузырем и в 86% случаев проводили диспансерное наблюдение либо каждые 6, либо 12 месяцев. В спектр обследования входили: анализ мочи в 85% обращений; УЗИ верхних мочевых путей – в 60%; и только 12% врачей регулярно повторяли уродинамические исследования. Авторы пришли к интересным выводам: значимость специализированных центров по лечению нейрогенного мочевого пузыря невелика, так как большинство голландских урологов ведет таких пациентов самостоятельно; уродинамические исследования рутинно не проводятся; реальная практика противоречит имеющимся руководствам [5].
Подобные данные по периоду диспансерного наблюдения больных с нейрогенной дисфункцией мочевого пузыря зафиксированы и во французском исследовании [4]. Интересен опыт Англии и Ирландии – в опросе приняли участие сотрудники 12 отделений, занимающихся ведением пациентов после спинальной травмы. Частота урологического осмотра была следующей: в двух клиниках принимали пациентов только в случае особой необходимости; в одном – раз в полгода; в шести – ежегодно; в трех – применялся индивидуальный протокол наблюдения [3].
В Саудовской Аравии коллеги рекомендуют контроль за нейроурологическими больными 1 раз в год, но, при отсутствии жалоб у пациента промежуток увеличивается до 2 лет [8].
Опросы врачей Италии, Канады и Турции показали, что большинство специалистов придерживаются рекомендаций обследования больных с нейрогенной дисфункцией мочевого пузыря ежегодно [9-11].
Американские коллеги четкого и окончательного ответа не дали, так как считают, что у лиц, которые имеют высокий риск аномалий нижних мочевыводящих путей, таких как рецидивирующие ИМП или впервые возникший гидронефроз, либо у которых наблюдалось изменение характера мочеиспускания, должны проходить обследование чаще, при этом на сколько – не указано.
Согласно рекомендациям Европейской ассоциации урологов, в зависимости от типа неврологической патологии и стабильности симптомов нейрогенной дисфункции нижних мочевых путей интервал между первичным и контрольным обследованием может варьировать и во многих случаях не превышать 1–2 лет [12]. В группе неврологических пациентов высокого риска этот период может быть намного короче. Общий анализ мочи рекомендовано выполнять только при наличии симптомов.
Ультразвуковое исследование верхних мочевых путей – проводить 1 раз в 6 месяцев пациентам из группы высокого риска. Уродинамическое исследование рекомендовано выполнять при первичном обследовании и наблюдении на регулярной основе, однако частота не описана. Также указывается на необходимость чаще проводить уродинамическое исследование пациентам из группы высокого риска, но частота временных интервалов не отмечена. Рекомендации в отношении нефросцинтиграфии неоднозначны, так как нет исследований высокого качества по этому вопросу. Ситуация с выполнением цистоскопии обстоит несколько иначе. Так как пациенты находятся в группе повышенного риска выявления рака мочевого пузыря, им требуется длительное наблюдение и проведение цистоскопии, однако какова должна быть регулярность выполнения манипуляции у таких больных – не указано. Согласно Российским клиническим рекомендациям, нейрогенная дисфункция нижних мочевых путей является не основным заболеванием, а следствием неврологической патологии (повреждений центральной или периферической нервной системы), и профилактики развития нейрогенных нарушений мочеиспускания не существует [2]. В связи с выше изложенным предлагается ежегодный осмотр пациентов с нейрогенной дисфункцией нижних мочевых путей у врачем-урологом с проведением исследований: лабораторных (общий анализ мочи, мочевина и креатинин крови) и инструментальных (УЗИ почек и мочевого пузыря, уродинамические исследования) для оценки состояния пациента в динамике [2]. Целесообразно выполнение лабораторных и инструментальных обследований 1 раз в год.
Можно заметить, что хорошим инструментом в наблюдении пациентов с нейрогенными нарушениями мочеиспускания является дистанционный урологический домашний мониторинг, который позволяет пациенту и его родственникам выполнять обследования без посещения лечебного учреждения. В настоящее время для выполнения в домашних условиях доступны общий анализ мочи, урофлоуметрия, измерение объема остаточной мочи носимыми устройствами [13-15].
В современное время всеобщей цифровизации больные могут использовать специальные приложения в смартфонах, а уролог – в режиме реального времени следить за изменениями состояния человека [16]. Перспективным видится в ближайшем будущем получение, систематизация, анализ медицинской информации врачами, обучение пациентов с помощью больших языковых моделей (LLM – large language model) и других систем искусственного интеллекта [17]. Мы считаем, что тема дистанционного урологического домашнего мониторинга требует дальнейшего как методологического, так и организационного развития с последующим активным внедрением в клиническую практику и внесением в клинические рекомендации. Отдельно надо отметить, что необоснованно частое проведение диагностических исследований утяжеляет финансовое бремя на систему здравоохранения страны.
Дренирование мочевых путей
Периодическая катетеризация является наиболее предпочтительным методом опорожнения мочевого пузыря при его арефлексии у 82% опрошенных турецких врачей. Длительный постоянный дренаж предпочли 6% специалистов, а 12% предложили использовать маневры Вальсальвы или Креде [10]. В Канаде периодическая катетеризация была выбрана 93% урологов для лечения пациентов с проблемами опорожнения из-за нейрогенной дисфункции мочевого пузыря, а постоянный катетер использовали 5% урологов [11]. 90% респондентов в США указывают на периодическую катетеризацию в качестве распространенного метода лечения, и только 4% опрошенных высказались за длительное постоянное катетерное дренирование [18]. Следует отметить, что в исследовании приняли участие урологи, проявляющие интерес и обладающие знаниями в области уродинамических исследований, что внесло очевидную предвзятость в полученные результаты.
Среди способов опорожнения мочевого пузыря при нейрогенных нарушениях нижних мочевых путей ассистируемые опорожнения, такие как прием Креде, Вальсальвы, мочеиспускание за счет триггерного рефлекса, не рекомендованы в связи с очень высоким риском отдаленных осложнений, а чистая периодическая катетеризация 4-6 раз в сутки признана «золотым стандартом». При этом риск инфекции нижних мочевых путей снижается при использовании лубрицированных катетеров.
Использование постоянных дренажей (цистостома) допускается в случае тетраплегии, нарушении проходимости уретры или при сформировавшемся микроцистисе.
Российские клинические рекомендации во всех случаях неполного опорожнения мочевого пузыря нейрогенной природы советуют использовать интермиттирующую катетеризацию, избегать приема Креде, постоянного уретрального дренажа и цистостомии [2]. По данным нашего опроса, 72,7% урологов назначают периодическую катетеризацию пациентам с «нарушением опорожнения мочевого пузыря». Но при детализации вопроса оказалось, что только 45,8% врачей порекомендуют ее при гипоактивном мочевом пузыре 23,7% – предложат цистостому, 9% – постоянный уретральный катетер и лишь 18,1% обратятся за советом к нейроурологу. Подобный опыт был получен японскими коллегами при анкетировании членов Японского общества нейрогенного мочевого пузыря. Так, 73,7% урологов предпочли периодическую катетеризацию. Надо отметить, что 19,8% специалистов выбрали прием Креде или постукивание [7].
Инфекции мочевых путей
Инфекции мочевых путей широко распространены у пациентов с нейрогенными нарушениями опорожнения мочевого пузыря [19]. В данной группе больных часто симптоматика неклассическая и может проявляться усилением спастичности, болью в животе или спине, появлением недержания мочи. С одной стороны, нераспознанная инфекция может привести к жизнеугрожающей автономной дисрефлексии или уросепсису, с другой – бесконтрольное использование антибиотиков способствует развитию устойчивости к ним, снижая варианты лечения в перспективе.
Национальные российские руководства рекомендуют не проводить рутинный скрининг на бессимптомную бактериурию. Культуральное исследование на уропатогены необходимо назначать при наличии у нейрогенных пациентов таких симптомов, как боль, гипертермия и гематурия [2].
По данным нашего исследования, 83,9% опрошенных назначают антибактериальную терапию только при клинически значимой инфекции мочевых путей, 10% проводит антибактериальную терапию при наличии повышенного содержания лейкоцитов, 7% – при выявлении бактерий в посеве мочи в любом титре, а 6% – в общем анализе мочи. Но распределение голосов изменилось при конкретизации вопросов в отношении дренажной методики. Вероятно, отсутствует четкое понимание стратегий профилактики и лечения инфекционных осложнений в нейрогенной группе пациентов.
Интересные данные описаны в уже упомянутой выше работе B. Rikken, B. Blok – 18% специалистов «часто» использовали рекомендации Европейской ассоциации урологов по нейроурологии, 35% — «время от времени», а 47% — не использовали их вообще. Урологи, которые часто обращались к руководствам, лечили бессимптомные инфекции мочевых путей у пациентов на периодической катетеризацию значительно реже, чем те, кто полагался на собственный опыт [5].
Согласно Российским рекомендациям, клинически значимой бактериурией принято считать >102 КОЕ/мл у пациентов, проводящих периодическую катетеризацию, >104 КОЕ /мл в чистых образцах мочи, выпущенной самостоятельно, а при надлобковой аспирации мочи значимой считается любая определяемая концентрация бактерий.
Клинически значимой лейкоцитурией считается наличие 10 и более лейкоцитов в поле зрения (400х) в осадке мочи после центрифугирования. При этом не рекомендован рутинный скрининг на бессимптомную бактериурию у пациентов с нейрогенными нарушениями опорожнения мочевого пузыря, а «золотым стандартом» диагностики является посев и общий анализ мочи [2].
В терапии ИМП у пациентов с нейрогенными нарушениями мочеиспускания следует выбирать антибактериальные препараты согласно данным посева мочи, при этом длительность терапии составляет от 5-7 дней и может быть продлена до 14 дней. Не рекомендовано назначение антибиотиков при бессимптомной бактериурии (в том числе у пациентов, находящихся на интермитирующей катетеризации), длительное лечение низкими дозами антибактериального препарата при рецидивах, так как это не приводит к улучшению результатов и способствует формированию бактериальной резистентности. Указано, что применение гидрофильных катетеров позволяет снизить риски ИМП, а промывание мочевого пузыря неэффективно [12].
Анализ зарубежного опыта показал, что только в 5 из 12 отделений урологии в Англии и Ирландии существует единая стратегия лечения пациентов. При этом только одно из 12 отделений проводило терапию пациентов, находящихся на периодической катетеризации, антибиотикопрофилактика проводилась в 4-х центрах. [3]. В Италии врачи предпочитали курсы антибактериальной терапии менее 7 дней, и ни один из центров не назначал лечение >10 дней [9]. В Нидерландах редко лечат бессимптомные инфекции мочевых путей у пациентов на периодической катетеризации. А при наличии клинической картины курс составляет в среднем 7-9 дней. В Саудовской Аравии 40% опрошенных врачей лечат бессимптомную бактериурию антибиотиками от 7 до 14 дней [8]. Турецкие коллеги при отсутствии симптомов, но при наличии пиурии у пациентов на интермиттирующей катетеризации назначат терапию в 48% случаев, а при персистирующей бактериурии в трех последних посевах мочи – только в 15%. ИМП, сопровождающуюся симптомами, лечат в течение 5, 7, 10 и 14 дней 4%, 11%, 45% и 39% респондентов соответственно. [10]. В Канаде предпочитали не проводить терапию бессимптомной инфекции, а при клинической картине – антибиотики на 7– 10 дней назначают 75% ответивших урологов. [11].
Инструментальные обследования
Ультразвуковое исследование в качестве метода контроля за верхними мочевыми путями в Англии и Ирландии предпочитают выполнять 1 раз в год, но одно из опрошенных отделений проводило его только 1 раз в 3 года [3]. В Италии более широкий диапазон контроля – 1 раз в 6-36 месяцев (в среднем 1 раз в год). Однако в 4-х центрах УЗИ выполняется в зависимости от клинического состояния пациента [9]. Среди опрошенных 105 урологов Саудовской Аравии, 60% выполняют УЗИ каждые 6 месяцев [8]. 85% врачей в США ежегодно проводят УЗИ органов мочеполовой системы [18].
В Японии 71,8% врачей используют ультразвук в качестве метода первого выбора, однако о частоте проведения данного обследования в работе упомянуто не было [7]. 93% опрошенных турецких специалистов выбирают УЗИ в качестве основной диагностики верхних мочевых путей, при этом 36% предпочитают выполнять контроль каждые 6 месяцев, 59% – 1 раз в год и 5% – 1 раз в 2 года. В канадском исследовании 93% респондентов считают, что УЗИ является предпочтительным диагностическим исследованием для рутинного наблюдения за верхними путями, однако, как и в японском исследовании, данных о периодичности не опубликовано [11].
В нашем опросе среди российских коллег 98% предпочтут выполнить УЗИ, при этом 92% комбинируют обследование с определением уровня креатинина в сыворотке крови.
Контроль за состоянием нижних мочевых путей при помощи уродинамического оборудования в Саудовской Аравии проводят 61% врачей каждые 1-2 года или при ухудшении состояния пациента [8]. В Англии и Ирландии были отмечены различия в предпочтениях по выполнению уродинамических исследований. В половине отделений не проводилось рутинных измерений, два центра делали их ежегодно, один – раз в два года после того, как с момента травмы прошло 10 лет, а другое отделение проводило рутинные исследования только один раз (во время реабилитации) [3].
В Турции 62% предпочитают КУДИ как метод контроля над функцией нижних мочевых путей, при этом 29% предпочитают проводить контроль каждые 6 месяцев, 51% – каждый год и 9% – каждые 2 года, а 10% предпочитают видеоуродинамику [10]. В канадском исследовании уродинамическое исследование проводилось ежегодно или раз в два года [11]. Коллеги из США предпочитают видеоуродинамическое обследование (65% респондентов), в Японии его проводят только 9,9% врачей. Более половины японских респондентов (52,3%) используют только цистометрию.
В России контроль за нижними мочевыми путями почти 44% врачей проводят 1 раз в 3 месяца, 38% – 1 раз в 6 месяцев и только 10% – не реже 1 раза в 12 месяцев. При этом в качестве метода диагностики 96% предпочитает УЗИ, а КУДИ пациентам используют всего 28% врачей.
Цистоскопию в Саудовской Аравии врачи выполняют ежегодно у пациентов с постоянным катетером [7]. В США 25% респондентов периодически проводили цистоскопию [18]. В Японии процент врачей, проводящих данную манипуляцию, составил 6,6 [7].
Российские урологи выполняют цистоскопию в 59% случаев при обнаружении патологии в мочевом пузыре при УЗИ, в 41% – при гематурии, 21,7% – только при длительном нарушении мочеиспускания, а 17% – всем пациентам с дисфункцией мочевых путей. При этом 39,8% используют цистоскопию как метод контроля за нижними мочевыми путями.
Фармакотерапия
Согласно современным руководствам, для купирования симптомов накопления при нейрогенном мочевом пузыре применяются М-холиноблокаторы [2, 20]. 69,5% российских урологов следуют данному совету, тогда как 14,1% выбирают β-адреномиметики, а 9,2% – α-блокаторы. В исследованиях-опросах зарубежных авторов мы не нашли упоминаний об использовании α-адренергических средств при нейрогенной детрузорной гиперактивности.
В завершение опроса урологи оценили оказание и доступность нейроурологической помощи в своем регионе – 69,6% врачей оценили ее как «хорошо», «удовлетворительно» и «отлично».
Наша работа — это первое исследование по изучению тактики ведения больных при нейрогенных расстройствах мочевого пузыря, которое проведено в России среди урологов, работающих в разных звеньях медицинской помощи (амбулаторное, стационарное, реабилитационные центры). Нужно заметить, что не только в Российской Федерации, но и в других странах нет единого мнения о том, как часто проводить обследование пациентов с нейрогенными нарушениями мочеиспускания или о спектре анализов, которые следует включать в диагностику. Как видно из проведенного нами опроса, в настоящее время существует широкий разброс в стратегиях ведения среди урологов, занимающихся как амбулаторной практикой, так и работающих в стационаре.
ЗАКЛЮЧЕНИЕ
- Большинство российских урологов частично следуют национальным рекомендациям по принципам диагностики и лечения нейрогенного мочевого пузыря. Тем не менее, нет единого мнения о лечении гипери гипоактивных форм дисфункции мочевых путей. До сих пор остаются случаи необоснованного применения антибактериальной терапии, а также устаревших методов ведения дренированных пациентов.
- Результаты исследования подчеркивают актуальность проведения образовательных программ и междисциплинарных конференций по нейроурологии во всех регионах.
- Обеспечение оборудованием для проведения урофлоуметрии, в том числе домашней, для УЗ-диагностики остаточной мочи, систем уродинамического наблюдения могли бы улучшить ситуацию с нейроурологическими пациентами.
- Необходимо проведение Школ для пациентов и их родственников, обучению их уходу за нейроурологическими, в том числе стомированными пациентами.
ЛИТЕРАТУРА
- Panicker JN. Neurogenic Bladder: Epidemiology, Diagnosis, and Management. Semin Neurol 2020;40(5):569-79. https://doi.org/10.1055/s-0040-1713876.
- Касян Г.Р., Кривобородов Г.Г., Гаджиева З.К., Салюков Р.В., Аль-Шукри С.Х., Тищенко Г.Е. и д.р. Клинические рекомендации «Нейрогенная дисфункция нижних мочевыводящих путей». [Электронный ресурс]. [Kasyan G.R., Krivoborodov G.G., Gadzhieva Z.K., Salyukov R.V., Al-Shukri S.H., Tishchenko G.E. et al. Clinical guidelines «Neurogenic dysfunction of the lower urinary tract». [Electronic resource]. (In Russian)]. URL: https://cr.minzdrav.gov.ru/schema/588_2.
- Bycroft J, Hamid R, Bywater H, Patki P, Craggs M, Shah J. Variation in urological practice amongst spinal injuries units in the UK and Eire. Neurourol Urodyn 2004;23(3):252-6. https://doi.org/10.1002/nau.20005.
- Denys P, Soler J-M, Fatton B, Rischmann P, Yelnik A, Aegerter P, et al. Prise en charge des patients ayant une vessie neurologique en France : une enquête du groupe d’études de neurourologie de langue française (GENULF). Progrès En Urologie 2012;22(9):540–8. https://doi.org/10.1016/j.purol.2012.02.004.
- Rikken B, Blok BFM. Management of neurogenic bladder patients in The Netherlands: do urologists follow guidelines? Neurourol Urodyn 2008;27:758-62. https://doi.org/10.1002/nau.20582.
- Аляев Ю.Г., Аполихин О.И., Пушкарь Д.Ю., Перепанова Т.С. и соавт. Федеральные клинические рекомендации. Антимикробная терапия и профилактика инфекций почек, мочевыводящих путей и мужских половых органов 2022. [Alyaev Yu.G., Apolikhin O.I., Pushkar D.Yu., Perepanova T.S. et al. Federal clinical guidelines. Antimicrobial therapy and prevention of infections of the kidneys, urinary tract and male genital organs 2022. (In Russian)].
- Kitahara S, Iwatsubo E, Yasuda K, Ushiyama T, Nakai H, Suzuki T, et al. Practice patterns of Japanese physicians in urologic surveillance and management of spinal cord injury patients. Spinal Cord 2006;44:362–8. https://doi.org/10.1038/sj.sc.3101854.
- Al Taweel W, Alkhayal A. Neurogenic bladder evaluation and management after spinal cord injury: Current practice among urologists working in Saudi Arabia. Urol Ann 2011;3(1):24-8. https://doi.org/10.4103/0974-7796.75872.
- Andretta E, Pagliacci MC, Zuliani C, Filocamo MT, Losavio E, Krassioukov A. A survey of clinical practice concerning long-term follow-up of neurogenic lower urinary tract dysfunction due to spinal cord injury in Italy. J Spinal Cord Med 2022;45(6):907-15. https://doi.org/10.1080/10790268.2020.1863899.
- Akkoç Y, Ersöz M, Çınar E, Gök H. Evaluation and management of neurogenic bladder after spinal cord injury: Current practice among physical medicine and rehabilitation specialists in Turkey. Turk J Phys Med Rehab 2021;67(2):225-32. https://doi.org/10.5606/tftrd.2021.5817.
- Blok BFM, Karsenty G, Corcos J. Urological surveillance and management of patients with neurogenic bladder: results of a survey among practicing urologists in Canada. Can J Urol 2006;13:3239-43.
- European Association of Urology 2023. [Electronic resource]. URL: https://uroweb.org/
- Шадеркин И.А., Владзимирский А.В., Цой А.А., Войтко Д.А., Просянников М.Ю., Зеленский М.М. Диагностическая ценность портативного анализатора мочи «ЭТТА АМП-01», как инструмента самостоятельного мониторинга в mHealth и при скрининге в первичном звене медицинской помощи. Экспериментальная и клиническая урология 2015;4:22-6. [Shaderkin I.A., Vladzimirsky A.V., Tsoi A.A., Voitko D.A., Prosyannikov M.Yu., Zelensky M.M. The diagnostic value of the portable urine analyzer «ETTA AMP-01» as a self-monitoring tool in mHealth and for screening in primary care. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2015;4:22-6. (In Russian)].
- Лебедев Г.С., Владзимирский А.В., Шадеркин И.А., Дударева В.П. Комплекс дистанционного мониторинга при хронических неинфекционных заболеваниях. Российский журнал телемедицины и электронного здравоохранения 2022;8(1):7-14. [Lebedev G.S., Vladzimirsky A.V., Shaderkin I.A., Dudareva V.P. Complex of remote monitoring for chronic non-infectious diseases. Rossiyskiy zhurnal telemeditsiny i elektronnogo zdravookhraneniya = Russian Journal of Telemedicine and Electronic Health 2022;8(1):7-14 (In Russian)]. https://doi.org/10.29188/2712-9217-2022-8-1-7-14.
- Монаков Д.М., Шадеркина А.И., Шадеркин И.А. Мониторинг наполнения мочевого пузыря у пациентов с нейрогенными нарушениями мочеиспускания: роль носимых аппаратно-программных комплексов. Экспериментальная и клиническая урология 2021;14(2):124-31. [Monakov D.M., Shaderkina A.I., Shaderkin I.A. Monitoring bladder filling in patients with neurogenic urination disorders: the role of wearable hardware and software systems. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2021;14(2):124-31. (In Russian)]. https://doi.org/10.29188/2222-8543-2021-14-2-124-131.
- Филиппова Е.С., Баженов И.В., Зырянов А.В., Журавлев В.Н., Борзунов И.В. Информационный ресурс для больных нейрогенной дисфункцией нижних мочевыводящих путей. Экспериментальная и клиническая урология 2019;(3):20-5. [Filippova E.S., Bazhenov I.V., Zyryanov A.V., Zhuravlev V.N., Borzunov I.V. Information resource for patients with neurogenic dysfunction of the lower urinary tract. Eksperimental'naya i klinicheskaya urologiya = Experimental and Clinical Urology 2019;(3):20-5. (In Russian)]. https://doi.org/110.29188/2222-8543-2019-11-3-20-25.
- Шадеркина В.А. ChatGPT в медицине: возможности и ограничения. Российский журнал телемедицины и электронного здравоохранения 2024;10(1):33-43. [Shaderkina V.A. ChatGPT in medicine: opportunities and limitations. Rossiyskiy zhurnal telemeditsiny i elektronnogo zdravookhraneniya = Russian Journal of Telemedicine and Electronic Health 2024;10(1):33-43. (In Russian)]. https://doi.org/10.29188/2712-9217-2024-10-1-33-43.
- Razdan S, Leboeuf L, Meinbach DS, Weinstein D, Gousse AE. Current practice patterns in the urologic surveillance and management of patients with spinal cord injury. Urology 2003;61(5):893-6. https://doi.org/10.1016/s0090-4295(02)02518-9.
- Neuro-urology. Guideline. EAU 2024. [Electronic recourse]. URL: https://uroweb.org/guideline/neuro-urology/.
- Cardozo, L, Rovner, E, Wagg, A, Wein, A, Abrams, P. (Eds) Incontinence 7th Edition. ICI-ICS. International Continence Society, Bristol UK 2023.







