Новые концепции и патофизиология симптомов нижних мочевых путей у мужчин
 11780
11780 В соответствии с классической теорией, увеличение объема предстательной железы при ДГПЖ ведет к нарушению оттока мочи, вызывая симптомы нарушения функции нижних мочевых путей (СНМП). Простатэктомия устраняет обструкцию и способствует разрешению СНМП.
Данная концепция не до конца отражает действительность. В исследовании, проведенном Neal и соавт., в ходе 11-месячного контрольного наблюдения 217 пациентов, которые перенесли простатэктомию, было показано, что оперативное вмешательство в большинстве случаев устраняет симптомы обструкции, но не способствует разрешению симптомов накопления: неотложные позывы на мочеиспускание оставались у 50% пациентов, неотложные позывы и недержание - у 33% пациентов [1].
В исследовании, где 217 мужчин в возрасте 45 лет или старше с СНМП в анамнезе наблюдали в течение 13 лет после трансуретральной резекции предстательной железы, у 66% пациентов отмечалось возобновление симптомов [2]. После уродинамических исследований было установлено, что отсроченный рецидив симптомов был обусловлен нарушением функции детрузора, особенно за счет его гиперактивности (гиперактивность детрузора - ГД), которую наблюдали у 64% пациентов (рисунок 1).
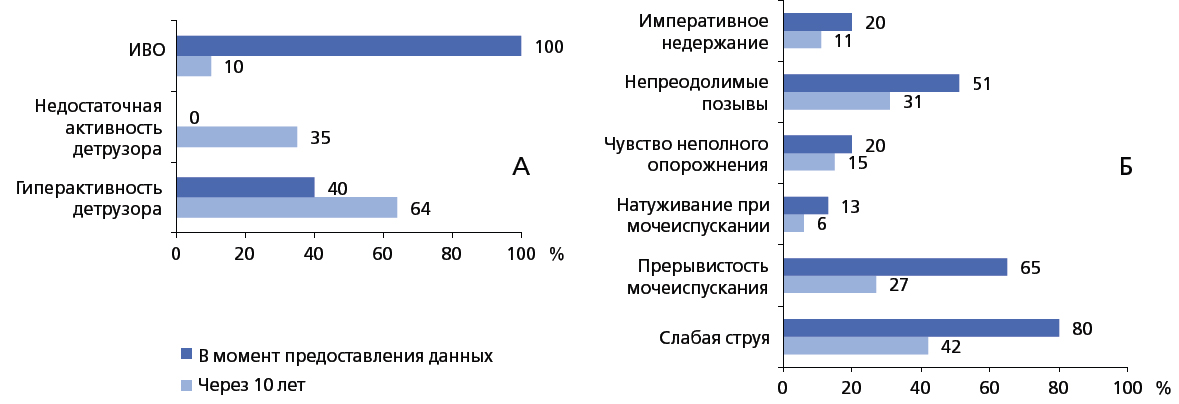
Рисунок 1. История наблюдений (на протяжении не менее 10 лет) нарушений функции мочевого тракта после ТУР предстательной железы [2]
РОЛЬ МОЧЕВОГО ПУЗЫРЯ
Частота нарушений функции детрузора предполагает, что мочевой пузырь наряду с предстательной железой вносит сопоставимый вклад в развитие СНМП. Следует отметить, что СНМП, связанные с накоплением мочи, и симптомы при гиперактивном мочевом пузыре (ГАМП) практически одинаковы, единственное отличие - в их значимости. При СНМП, связанных с накоплением, чаще отмечают учащенное мочеиспускание и ноктурию, затем неотложные позывы на мочеиспускание, потом следует недержание мочи. При ГАМП наиболее часто наблюдают неотложные позывы и учащенное мочеиспускание, затем - ноктурию и неотложное недержание мочи. Кроме этих общих данных, есть дополнительные данные о вовлечении мочевого пузыря в развитие СНМП. Было продемонстрировано, что выраженность инфравезикальной обструкции (ИВО) и ГД тесно связаны [2]. Действительно, до 80% пациентов с выраженной ИВО, подтвержденной исследованиями скорости потока мочи, имеют ГД, которая отмечается в два раза чаще, чем случайное обнаружение ГД у людей без признаков ИВО.
ЧТО ЯВЛЯЕТСЯ ПРИЧИНОЙ РАЗВИТИЯ ГИПЕРАКТИВНОСТИ ДЕТРУЗОРА?
Эти наблюдения позволяют выяснить причины, приводящие к ГД. Предложено несколько объяснений.
Усиление симпатической стимуляции
При ИВО усиливается влияние симпатической нервной системы за счет увеличения экспрессии определенного подтипа альфа-адренорецепторов. У крыс ИВО вызывала шестикратное увеличение веса мочевого пузыря и переключение экспрессии адренорецепторов с 70% а1А и 25% a1D на 23% a1A и 75% a1D. Возросшая аффинность подтипа a1D к эндогенному норадреналину в 10-100 раз может объяснить увеличение сократимости мочевого пузыря [4]. Однако, при исследовании у пациентов с нормальным мочевым пузырем и с наличием обструкции было выяснено, что изменение экспрессии этих рецепторов в мочевом пузыре человека не существенно [5].
В клинических условиях силодозин, являющийся высокоселективным антагонистом а1А-адренорецепторов, демонстрирует не меньшую эффективность в отношении облегчения СНМП при ДГПЖ по сравнению с тамсулозином, который является блокатором а1А и аШ-адренорецепторов [6]. Эти данные подтверждают существенную роль подтипа а1А адренорецепторов в патогенезе СНМП, связанных с накоплением, но эта роль остается не до конца выясненной. Она может заключаться в активности а1А-рецепторов в С-сенсорных волокнах и спинном мозге [7].
Кроме этого, симпатическая система может вызывать ГД за счет активации Rho-киназного пути. ИВО стимулирует RhoA/Rho-киназный путь [8], что ведет к фосфорилированию миофиламентов и увеличению сократительного тонуса гладкомышечных клеток детрузора. В опытах на крысах со спонтанной гипертензией была показана стимуляция этого пути и развитие повышенной активности мочевого пузыря, которая может быть купирована ингибиторами Rho-киназы [9].
Повышенная чувствительность к ацетилхолину
Ранее было предложено объяснение развития ГД вследствие ИВО, которая вызывает гиперчувствительность к ацетилхолину за счет парасимпатической денервации, что обуславливает более стойкие и интенсивные сокращения [10]. При наличии частичной обструкции в нижних отделах мочевого пузыря у кроликов и человека наблюдают снижение холинацетилтрансферазы в мышечных клетках детрузора [11].
 |
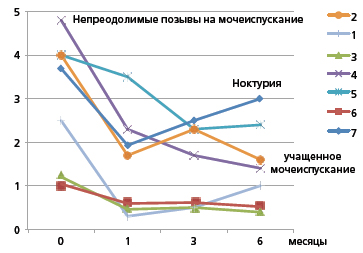 |
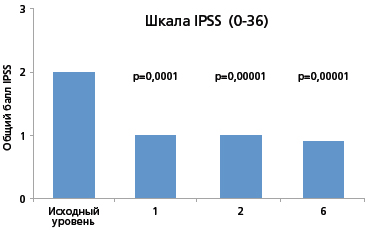
Рисунок 2. Эффект влияния потери афферентной чувствительности (резинифератоксин) на СНП, связанные с ДГПЖ [18]
Причиной денервации может быть ишемия, т к ИВО обычно сопровождается снижением кровотока в нарушенном мочевом пузыре [12]. Эти данные предполагают, что снижение кровотока в детрузоре ведет к его контрактильной дисфункции, а не наоборот.
Местная сегментарная сократимость
Другим объяснением развития ГД является то, что ИВО способствует изменению межклеточных контактов в гладкой мускулатуре детрузора. В исследовании ультраструктуры гладкомышечных клеток детрузора и проводящих нервных волокон у 51 пациента обоих полов с нейрогенной дисфункцией мочевого пузыря было установлено наличие протрузий межклеточных соединений и тесное прилегание клеточных опор [13]. Наличие таких патологических контактов наблюдали и между гладкомышечными клетками детрузора у пациентов с ИВО [14]. Патологическое поступление сигналов из клетки в клетку может вызывать сегментарные сокращения. Такие сокращения или микросокращения детрузора были отмечены с частотой существенно большей у пациентов с неотложными позывами на мочеиспускание, нежели у здоровых добровольцев (85% из 14 пациентов по сравнению с 30% из 6 добровольцев; p = 0,02) [15]. У них также выше афферентная нервная активность [16], что приводит (за счет афферентной стимуляции) к раздражению дуги рефлекса мочеиспускания. Эта гипотеза подтверждена исследованиями, в которых при ингибировании сенсорных волокон исчезала ГД. При внутрипузырном введении лидокаина, блокирующего С-сенсорную передачу, наблюдали увеличение емкости мочевого пузыря [17].
В испытании для обоснования концепции, выключение чувствительности С-волокон мочвого пузыря внутрипузырным введением резинифератоксина вызывало длительное облегчение СНМП. У пациентов наблюдали значительное улучшение симптомов по Международной шкале IPSS (International Prostate Symptom Score) и выраженности симптомов накопления (неотложность, ноктурия, учащенное мочеиспускание). Улучшение состояния наблюдалось на протяжении 3 мес . (рисунок 2) [18].
Селективный а1А-адреноблокатор силодозин продемонстрировал способность улучшать функцию накопления мочевого пузыря за счет подавления афферентной активности С-волокон в модели инсульта у крыс [7].
Нейротрансмиттеры, выделяемые уротелием, также могут стимулировать сенсорные волокна. Было экспериментально продемонстрировано, что растяжение мочевого пузыря вызывает выброс уротелием аденозинтрифосфата (АТФ). АТФ избыточно связывает пуринергические рецепторы P2X3 в сенсорных волокнах мочевого пузыря, что играет большую роль в контролировании рефлексов, связанных с объемом мочевого пузыря [19, 20]. В настоящее время проводят исследования P2X3- антагонистов в связи с их терапевтическим потенциалом в отношении лечения пациентов с СНМП и ГАМП.
Увеличение содержания фактора роста нервной ткани
Было показано, что ИВО ведет к увеличению синтеза фактора роста нервной ткани (NGF - nerve growth factor) в мочевых пузырях крыс и человека. Это увеличение нельзя полностью купировать устранением обструкции [21]. Введение NGF грызунам приводит к активации рефлекса мочеиспускания и появлению ГД на цистограм- мах. NGF оказывает существенный тропный эффект на сенсорные С-волокна мочевого пузыря путем стимуляции их прорастания в центральную нервную систему за счет изменения экспрессии рецепторов в чувствительных волокнах и снижения их порога чувствительности к природной стимуляции [22, 23].
УРОЛОГИЧЕСКИЕ НАРУШЕНИЯ И МЕТАБОЛИЧЕСКИЙ СИНДРОМ
Недавно было обнаружено, что метаболический синдром имеет связь с урологическими нарушениями.
Метаболический синдром является сложным и не до конца изученным синдромом, который связан с абдоминальным отложением жира, вызывающим инсулинорезистентность. Есть несколько международных определений этого синдрома. Наиболее широко распространенными являются определения Всемирной организации здравоохранения (ВОЗ) [24], Национальной образовательной программы по холестерину (NCEP - National Cholesterol Education Program) - разработанный кардиологами [25] и Международной диабетической федерацией (IDF - International Diabetes Federation) [26]. Критерии немного различны. Например, в определениях ВОЗ и IDF в качестве одного из критериев используют окружность талии > 94 см по сравнению с определением NCEP, где окружность талии должна быть > 102 см. Но везде метаболический синдром определяют как наличие центрального ожирения и гиперинсулинемии, в основе которой лежит инсулинорезистентность, плюс любые два из следующих факторов риска сердечно-сосудистой системы: нарушение толерантности к глюкозе, повышение уровней триглицеридов, снижение уровня липопротеидов высокой плотности и повышенное артериальное давление [27]. Этот синдром не является заболеванием сам по себе, но выступает патогенетическим фактором развития заболеваний. При его наличии в 2 раза возрастает риск смерти из-за сердечно-сосудистых осложнений. По другим данным он связан с 25-кратным возрастанием вероятности развития сахарного диабета 2 типа [28]. С возрастом частота возникновения метаболического синдрома возрастает - в опросе, проведенном в Германии, половина пожилых мужчин имеет метаболический синдром [29].
Гипотестостеронемия
Метаболический синдром связан со снижением уровня тестостерона. Этот эффект был документально подтвержден более чем у 500 пожилых мужчин, репрезентативных в отношении общей популяции (13,8% имели метаболический синдром) в Тоскане (Италия) в исследовании InCHIANTI [30].
Кроме того, в исследовании в Аргентине была обнаружена негативная корреляция между окружностью талии и общим тестостероном у 95 эугонадных субъектов, из которых у 78 наблюдали эректильную дисфункцию (ЭД). У 17 пациентов эректильная функция была в норме (r = 22) [31].
Этот феномен опосредован за счет 3 механизмов: увеличение активности ароматаз в адипоцитах, которые способствуют превращению тестостерона в эстрадиол, увеличение уровня лептина и увеличение содержания инсулина, в ответ на что клетки Лейдига вырабатывают меньше тестостерона.
Эректильная дисфункция
В исследовании в Аргентине было установлено, что окружность талии негативно коррелирует с Международным индексом эректильной дисфунции (r = 0,23) [30]. В Турции было обнаружено, что метаболический синдром был тесно связан с ЭД (р < 0,001). Из 393 пациентов в возрасте 40-70 лет, которые поступили в клинику урологии 39,9% имели метаболический синдром [32].
Причиной, вызывающей ЭД, скорее всего, является инсулинорезистентность, ведущая к нарушению функции эндотелия и которую сопровождают недостаточное образование и выброс оксида азота.
Доброкачественная гиперплазия предстательной железы и симптомы нижних мочевых путей
Есть большое количество данных, которые свидетельствуют о том, что метаболический синдром связан с ДГПЖ и СНМП. В исследовании 307 пациентов с СНМП в Швеции была выявлена корреляция между срединным ежегодным увеличением объема простаты и уровнем инсулина в плазме натощак (р = 0,009) [33]. Сходные результаты были отмечены в исследовании 78 пациентов с ДГЖП в Турции, из которых общий объем предстательной железы увеличивался в среднем на 1,0 мл/год у мужчин с метаболическим синдромом по сравнению с 0,6 мл/год у пациентов без метаболического синдрома (p < 0,05) [34].
Kaplan и соавт. [35] обнаружили тесную положительную корреляцию между окружностью талии/метаболическим синдромом, объемом простаты и значениями IPSS и отрицательную корреляцию с максимальной скоростью потока мочи. Kristal и соавт. [36] в контексте исследования профилактики развития рака предстательной железы на 5667 субъектах обнаружили корреляцию между ДГПЖ и абдоминальным ожирением (р < 0,003). Desgrandchamps установил связь между наличием большой окружности талии и СНМП (IPSS > 8) [37].
Несколько исследований не выявили наличие связи между метаболическим синдромом и СНМП. В данных из реестра 1206 ветеранов Вьетнамской войны за период 15,6 лет не было выявлено связи между ДГПЖ и метаболическим синдромом [38]. При анализе результатов медицинского осмотра 2371 мужчины в Австрии (средний возраст 46,1 лет), 33,8% имели метаболический синдром и IPSS > 7 [39]. Эти отрицательные результаты объясняются слабостью набора данных: в первом случае проводили ретроспективное исследование, во втором-клинически важные СНМП отмечали лишь у небольшого числа субъектов.
Обнаруженная связь между метаболическим синдромом и ДГПЖ предполагает возможное облегчение состояния урологических пациентов при изменении образа жизни. В рандомизированном одностороннем слепом исследовании 110 мужчин, страдающих ожирением, меры, направленные на снижение веса (снижение калорийности пищи и увеличение двигательной активности) на протяжении 2 лет, привели к улучшению сексуальной функции у трети пациентов с ЭД по сравнению с исходным уровнем [40]. Среди 30 634 мужчин в возрасте 40-75 лет в США, которых наблюдали на протяжении 8 лет, нагрузка ходьбой пешком была обратно пропорциональна риску возможного хирургического вмешательства по поводу ДГЖП [41].
ВЫВОДЫ
Дисфункция мочевого пузыря вследствие длительной ИВО является важной причиной СНМП у пациентов с ДГЖП. Она включает как моторные (детрузор), так и сенсорные нарушения ДГЖП и СНМП могут быть связаны с метаболическим синдромом, положительного эффекта можно добиться изменением образа жизни. Эти новые сведения должны быть использованы для разработки современного подхода к лечению пациентов с ДГЖП/ СНМП.
КОНФЛИКТ ИНТЕРЕСОВ
В последние годы, Cruz получал исследовательскую поддержку, гонорары за консультации и лекции по темам, связанным с а1- адренорецепторами от компании Recordati. Desgrandchamps является консультантом компаний Recordati и GlaxoSmithKline.
Ключевые слова: СНМП, мочевой пузырь, предстательная железа, гиперактивность детрузора, ИВО, метаболический синдром, силадозин.
Keywords: LUTS, bladder, prostate, overactive detrusor, IVO, the metabolic syndrome, siladosin.
ЛИТЕРАТУРА
- Neal D .E ., Ramsden P. D ., Sharples L . et al . Outcome of elective prostatectomy. BMJ. 1989; 299: 762-7.
- Thomas A .W. , Cannon A ., Bartlett E ., Ellis-Jones J ., Abrams P. The natural history of lower urinary tract dysfunction in men: minimum 10-year urodynamic follow-up of transurethral resection of prostate for bladder outlet obstruction . J Urol 2005; 174: 1887-91.
- Oelke M . , Baard J . , Wijkstra H . , de la Rosette J. J . , Jonas U. , Hofner K. Age and bladder outlet obstruction are independently associated with detrusor overactivity in patients with benign prostatic hyperplasia Eur Urol 2008; 54: 419-26
- Hampel C , Dolber P C , Smith M P et al Modulation of bladder alpha1adrenergic receptor subtype expression by bladder outlet obstruction J Urol. 2002; 167: 1513-21.
- NomiyaM ., Yamaguchi O . Aquantitative analysis of mRNA expression of alpha 1 and beta-adrenoceptor subtypes and their functional roles in human normal and obstructed bladders J Urol 2003; 170: 649-53
- Kawabe K , Yoshida M , Homma Y , Silodosin Clinical Study Group Silodosin, a new alpha1A-adrenoceptor-selective antagonist for treating benign prostatic hyperplasia: results of a phase III randomized, placebo- controlled, double-blind study in Japanese men BJU Int 2006; 98: 1019-24
- Yokoyama O , Ito H , Aoki Y , Oyama N , Miwa Y , Akino H Selective alpha(1A)-blocker improves bladder storage function in rats via suppression of C-fi ber afferent activity. World J Urol . In press . doi: 10.1007/ s00345-009-0481-2
- Bing W , Chang S , Hypolite J A et al Obstruction-induced changes in urinary bladder smooth muscle contractility: a role for Rho kinase Am J Physiol Renal Physiol 2003; 285: F990-7
- Rajasekaran M ., Wilkes N ., Kuntz S ., E Albo M . Rho-kinase inhibition suppresses bladder hyperactivity in spontaneously hypertensive rats Neurourol Urodyn 2005; 24: 295-300
- Brading A F A myogenic basis for the overactive bladder Urology 1997; 50(6A Suppl): 57-67
- Levin R .M ., Haugaard N ., O’Connor L . et al . Obstructive response of human bladder to BPH vs rabbit bladder response to partial outlet obstruction: a direct comparison Neurourol Urodyn 2000; 19: 609-29
- Schroder A ., Chichester P. , Kogan B .A . et al . Effect of chronic bladder outlet obstruction on blood fl ow of the rabbit bladder. J Urol 2001; 165: 640-6
- Elbadawi A ., Resnick N .M ., Dorsam J. , Yalla S .V., Haferkamp A . Structural basis of neurogenic bladder dysfunction I Methods of prospective ultra- structural study and overview of the findings J Urol 2003; 169: 540-6
- Tse V , Wills E , Szonyi G , Khadra M H The application of ultrastructural studies in the diagnosis of bladder dysfunction in a clinical setting J Urol 2000; 163: 535-9
- Drake M J , Harvey I J , Gillespie J I , Van Duyl W A Localized contractions in the normal human bladder and in urinary urgency BJU Int 2005; 95: 1002-5
- McCarthy C . J. , Zabbarova I . V. , Brumovsky P. R . , Roppolo J . R . , Gebhart G . F. , Kanai A J Spontaneous contractions evoke afferent nerve firing in mouse bladders with detrusor over activity J Urol 2009; 181: 1459-66
- Yokoyama O , Komatsu K , Kodama K , Yotsuyanagi S , Niikura S , Namiki M Diagnostic value of intravesical lidocaine for overactive bladder J Urol 2000; 164: 340-3.
- Dinis P , Silva J , Ribeiro M J , Avelino A , Reis M , Cruz F Bladder C-fi ber desensitization induces a long-lasting improvement of BPH-associated storage LUTS: a pilot study Eur Urol 2004; 46: 88-94
- Vlaskovska M , Kasakov L , Rong W et al P2X3 knock-out mice reveal a major sensory role for urothelially released ATP. J Neurosci 2001; 21: 5670-7
- Cockayne D .A ., Hamilton S .G ., Zhu Q. M . et al . Urinary bladder hyporefl exia and reduced pain-related behaviour in P2X3-defi cient mice Nature 2000; 407: 1011-5
- Steers W D , Kolbeck S , Creedon D , Tuttle J B Nerve growth factor in the urinary bladder of the adult regulates neuronal form and function J Clin Invest 1991; 88: 1709-15.
- Charrua A , Pinto R , Frias B , Cruz C D , Cruz F TRPV1 expression in the bladder is essential for NGF-induced detrusor overactivity Neurourol Urodynam 2009; 28: 99, abstract
- Steers W D Rat: overview and innervation Neurourol Urodyn 1994; 13: 97-118 .
- Balkau B ., Charles M .A . Comment on the provisional report from the WHO consultation European Group for the Study of Insulin Resistance (EGIR). Diabetes Med 1999; 16: 442-3.
- Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults Executive summary of the third report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) . JAMA 2001; 285: 2486-97.
- Makhsida N , Shah J , Yan G , Fisch H , Shabsigh R Hypogonadism and metabolic syndrome: implications for testosterone therapy J Urol 2005; 174: 827-34
- Meigs J B Epidemiology of the metabolic syndrome Am J Manag Care 2002; 8(Suppl): S283-92
- Hu G , Qiao Q , Tuomilehto J , Balkau B , Borch-Johnsen K , Pyorala K , DECODE Study Group Prevalence of the metabolic syndrome and its relation to all-cause and cardiovascular mortality in nondiabetic European men and women Arch Intern Med 2004; 164: 1066-76
- Moebus S , Hanisch J U , Aidelsburger P , Bramlage P , Wasem J , Jockel K H Impact of 4 different defi nitions used for the assessment of the prevalence of the metabolic syndrome in primary healthcare: the German Metabolic and Cardiovascular Risk Project (GEMCAS) Cardiovasc Diabetol 2007; 6: 22
- Maggio M ., Lauretani F., Ceda G . et al. Estradiol and metabolic syndrome in older Italian men: the InCHIANTI study J Androl 2010; 31: 155-62
- Knoblovits P , Pablo R , Costanzo P R et al Erectile dysfunction, obesity, insulin resistance, and their relationship with testosterone levels in eugonadal patients in an andrology clinic setting . J Androl . In press . doi: .2164/jandrol.109.007757.
- Bal K , Oder M , Sahin A S et al Prevalence of metabolic syndrome and its association with erectile dysfunction among urologic patients: metabolic backgrounds of erectile dysfunction Urology 2007; 69: 356-60
- Hammarsten J , Hogstedt B Hyperinsulinaemia as a risk factor for developing benign prostatic hyperplasia . Eur Urol 2001; 39: 151-8.
- Ozden C , Ozdal O L , Urgancioglu G , Koyuncu H , Gokkaya S , Memis A The correlation between metabolic syndrome and prostatic growth in patients with benign prostatic hyperplasia Eur Urol 2007; 51: 199-206
- Kaplan S , Fisch H , Berriman S J Central obesity as measured by waist circumference is predictive of severity of lower urinary tract symptoms, sexual dysfunction, and components of the metabolic syndrome J Urol 2007; 177(Suppl): 497-8, Abstract 1508.
- Kristal A R , Arnold K B , Schenk J M et al Race/ethnicity, obesity, health related behaviors and the risk of symptomatic benign prostatic hyperplasia: results from the prostate cancer prevention trial J Urol 2007; 177: 1395400
- Desgrandchamps F. , Haab F. , Coloby P. , Slama A . , Gaudin A . F. Instant 2006: cardiometabolic markers in subjects with lower urinary tract symptoms in the French general population Eur Urol Suppl 2008; 7: 130, Abstract 237
- Gupta A , Gupta S , Pavuk M , Roehrborn C G Anthropometric and metabolic factors and risk of benign prostatic hyperplasia: a prospective cohort study of Air Force veterans . Urology 2006; 68: 1198-205.
- Temml C , Obermayr R , Marszalek M , Rauchenwald M , Madersbacher S , Ponholzer A Are lower urinary tract symptoms infl uenced by metabolic syndrome? Urology 2009; 73: 544-8.
- Esposito K , Giugliano F , Di Palo C et al Effect of lifestyle changes on erectile dysfunction in obese men: a randomized controlled trial JAMA 2004; 291: 2978-84.
- Platz E A , Kawachi I , Rimm E B et al Physical activity and benign prostatic hyperplasia Arch Intern Med 1998; 158: 2349-56
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 9 Мб |















































































