Оптимизация диагностики воспалительных заболеваний предстательной железы на основе междисциплинарного подхода
 10670
10670 Учение о воспалительных заболеваниях предстательной железы имеет давнюю историю, и ее эволюция наглядно демонстрирует борьбу теорий и взглядов на саму сущность заболевания, называемого «простатит». Предстательная железа впервые описана в исследованиях Герофила в 350 году до н.э., а ее точное морфологическое описание представил Вердес в 1838 году. Учение о простатите получило новое развитие после введения Янгом в клиническую практику методики исследования ее секрета [1]. В 1926 году на основе исследований Никеля была признана роль бактерий в этиологии воспаления предстательной железы, а в 1957 году получила распространение неинфекционная теория патогенеза хронического простатита, предложенная Campbell MF [2, 3]. Таким образом, в течение XX века были сформулированы практически две противоположные концепции заболевания, которые до сих пор имеют как сторонников, так и противников, что свидетельствует об отсутствии единого понимания патогенеза заболевания [2-6].
Среди современных теорий развития заболевания описаны инфекционная теория, теория химического ожога простаты, теория интрапростатического рефлюкса мочи, теория асептического воспаления, мионейрогенная теория дисфункции тазового дна, теория аутоиммунного воспаления и т.д., которые явились основой для применения соответствующих методов лечения хронического простатита [4-6]. Однако никто не будет спорить с тем, что «революция» в нашем понимании патогенеза и подходов к терапии воспалительных заболеваний предстательной железы связана с такими событиями в истории учения о простатите, как:
- разработка в 1968 году техники топической диагностики инфекции (4-стаканная проба Meares-Stamey), которая до сих пор является «золотым стандартом» диагностики инфекции уретроростатического сегмента [7];
- появление в 1978 году классификации простатитов Drach GW, которая сыграла ключевую роль в понимании сущности заболевания, так как впервые две противоположные теории патогенеза простатита (инфекционная и неинфекционная) нашли логическое таксонометрическое положение в рамках единой классификации [8]. По нашему мнению, именно эта классификация, долгое время оставаясь общепризнанной, способствовала преодолению методологических проблем диагностики заболевания;
- открытие и широкое внедрение в клиническую практику антибиотиков, которые позволили осуществлять качественное управление инфекционным воспалительным процессом в предстательной железе [4].
Тем не менее, несмотря на более чем 200-летнюю историю научных исследований, хронический простатит, по-прежнему, остается «темной лошадкой» современной урологии и, по образному выражению Stamey (1982), является «мусорной корзиной для клинического невежества, в которую традиционно сливается вся патология предстательной железы, выявляемая урологами при помощи пальца…» [5].
Успехи концепции «междисциплинарной доказательной медицины», получившей свое становление и бурное развитие в 90 годах XX века, позволили уже сегодня поиному посмотреть на патогенез целого ряда заболеваний человека, включая урологические. Таким образом, междисциплинарный подход доказал свое неоспоримое преимущество перед узкопрофильным решением диагностических и лечебных задач. Мы уверены, что прогресс в понимании сущности воспалительных заболеваний предстательной железы, как комплексной междисциплинарной медико-социальной проблемы, способен помочь преодолеть существующие проблемы их лечения, результаты которого по-прежнему мало кого удовлетворяют. Однако для этого нужно проанализировать, обсудить и оптимизировать существующие методы диагностики заболеваний предстательной железы.
ВЗГЛЯД НА ЭПИДЕМИОЛОГИЮ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Согласно существующему мнению, простатит – одно из частых урологических заболеваний у мужчин всех возрастных групп [4-6]. Его частота составляет 13,2-35%, а пик заболеваемости (65,2%) традиционно приходится на лиц моложе 50 лет [9,10,11]. В старшем возрасте частота простатита составляет 21,6%, при этом у мужчин с доброкачественной гиперплазией предстательной железы (ДГПЖ) инфекционный агент в предстательной железе с помощью бактериологических методов исследования может быть выявлен практически в 100% случаев [6]. Но на практике его выявление в этом возрасте и у этой категории пациентов происходит недостаточно активно, так как существует «общепринятое мнение», что простатит – болезнь мужчин молодого и среднего возраста. Это приводит к тому, что до 62% больных ДГПЖ оперируются с нераспознанным до операции хроническим инфекционным простатитом, обуславливающим немалую частоту послеоперационных гнойно-воспалительных осложнений аденомэктомии или трансуретральной резекции предстательной железы (ТУРПЖ) [12].
В связи со становлением и развитием в XX веке доказательной медицины были разработаны и внедрены в практику стандарты качественной диагностики и лечения многих заболеваний, а развитие Интернета в XXI веке значительно облегчило доступ к международным базам данных [13,14].
В настоящее время наиболее известной и авторитетной базой данных систематических обзоров медицинской литературы в мире является Кокрановская библиотека. В ней найдено лишь два крупных систематических обзора, посвященных хроническому простатиту [15]. Для такой распространенной проблемы как простатит - это крайне недостаточно. Очевидно, что по-настоящему достоверных сведений о данном заболевании не так уж много. С учетом этого, современное состояние проблемы хронических воспалительных заболеваний предстательной железы выглядит крайне неоднозначно. Существуют проблемы эпидемиологического, патогенетического, классификационного, диагностического и терапевтического плана, которые признаются большинством современных исследователей и клиницистов. Наличие этих проблем на этапе классификации и диагностики закономерно приводит к назначению неадекватной терапии, которая сегодня применительно к простатиту не может быть названа патогенетической.
Типичный пример: хронический простатит относится к числу широко распространенных заболеваний, а его проявления отличаются разнообразием клинических симптомов. Встречаются публикации, указывающие на чрезвычайно высокую заболеваемость. По данным статистических исследований Американского общества урологов (АUA, 2005), заболеваемость хроническим простатитом мужчин репродуктивного возраста варьирует от 35 до 98%, однако доказанная встречаемость составляет лишь 11% [16]. Более того, убедительных эпидемиологических данных о распространенности простатита в России просто не существует [4,13]. Такие эпидемиологические «диссонансы», по нашему мнению, являются отражением явного недопонимания патогенетической сущности заболевания под названием «простатит», что на фоне отсутствия его четких клинико-лабораторных критериев (описано около 100 симптомов простатита, и ни один из них не является патогномоничным!) не позволяет правильно ставить патогенетический диагноз в большинстве случаев. Возможно, поэтому мы называем простатитом любую боль в области предстательной железы или внизу живота у мужчины. Еще страшнее, если диагноз простатита ставится только на основании данных УЗИ, когда неквалифицированный врач-диагност уже в заключении «штампует» готовый клинический диагноз (!), хотя его роль состоит в изучении и описании морфометрических параметров железы, и он, по нашему мнению, не вправе ставить клинический диагноз, так как это является прерогативой КЛИНИЦИСТА! Такая гипердиагностика «хронического простатита» является, к сожалению, рутинной практикой урологов страны.
ТЕРМИНОЛОГИЯ И КЛАССИФИКАЦИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ КАК ВОЗМОЖНЫЕ ПРИЧИНЫ ПАРАДОКСОВ И ТРАГЕДИЙ ДИАГНОСТИКИ
В настоящее время описано более 50 различных классификаций воспалительных заболеваний предстательной железы, многие из которых очень громоздки и сложны и имеют сегодня исключительно исторический интерес. Такое обилие классификаций одного и того же заболевания является лишним подтверждением сложностей понимания его патогенеза. С точки зрения практической ценности и существенного влияния на развитие учения о простатите можно выделить классификации простатитов, предложенные Drach GW (1978), а в нашей стране - Тиктинским О.Л. (1990) [8, 17]. Именно они сыграли важную роль в нашем понимании сущности заболевания. Мы считаем, что термин «простатодиния», который ввел Drach GW в свою классификацию, явился первой в истории учения о простатите методологической попыткой отразить в термине мультфакторный патогенез заболевания, и отойти, наконец, от ведущей роли инфекции в его патогенезе [8].
Таким образом, клинически – простатический болевой синдром, а патогенетически – различные неинфекционные механизмы, лечить которые надо не антибиотиками – вот основной лозунг классификации Drach GW, которая сегодня незаслуженно забыта [8]. Эту же мысль можно понять и из классификации Тиктинского О.Л., которая, несмотря на определенную критику, наиболее точно отражала на тот период времени этиопатогенетические особенности инфекционного простатита и простатодинии [17]. Она тоже, к сожалению, была оставлена, так как в 1995 году Национальный институт здоровья (NIH) (США) предложил свою классификацию [18].
Для разграничения инфекционного и неинфекционного воспаления предстательной железы Европейской ассоциацией урологов (EAU) в 2003 году был рекомендован термин «синдром хронической тазовой боли» (СХТБ) [19]. Этот термин появился благодаря осознанию экспертами того факта, что СХТБ распространен не только в урологической практике и может иметь множество «внетазовых», «неурологических» и неинфекционных причин [19]. Согласно пересмотренным рекомендациям, СХТБ у мужчин, связанный с неинфекционными механизмами, выделен в отдельный подраздел «Урологический СХТБ», а воспалительные заболевания предстательной железы инфекционной этиологии включены в подраздел «Другие точно определенные состояния, вызывающие боль» под графой «Инфекционный простатит» [20].
По нашему мнению, этот методологический прорыв позволил начать пересмотр традиционных подходов к лечению хронического простатита и СХТБ и стал началом пути от симптоматической терапии болевого синдрома к патогенетическому лечению, поскольку признан полиэтиологический механизм болевого синдрома при данном патологическом состоянии. В настоящее время на фоне существенного повышения коморбидного фона мужской части населения можно с большой долей вероятности утверждать, что и СХТБ, и хронические инфекционные простатиты достаточно редко диагностируются у абсолютно здоровых мужчин, как, впрочем, и любое другое заболевание. Кроме того, нередко наши пациенты с урологическим СХТБ получают медикаментозное лечение по поводу других неурологических заболеваний. Все это необходимо учитывать при осуществлении диагностического поиска.
Как уже было упомянуто ранее, с 1995 года все мировое урологическое сообщество пользуется известной классификацией простатита, предложенной Национальным институтом здоровья (NIH) (США) [18]. Согласно ей, все клинические формы заболевания следует интерпретировать в рамках четырех категорий, при этом только две из них – острый инфекционный простатит (категория I) и хронический инфекционный простатит (категория II) достоверно связаны с клинически значимым бактериальным обсеменением ткани предстательной железы,которое может быть подтверждено объективными методами цитологические и (лучше) бактериологические исследования секрета предстательной железы) [18].
По нашему мнению, истинным «простатитом» воспалением предстательной железы с точки зрения классической патоморфологии можно назвать только инфекционные формы заболевания (категории I и II). Существование остальных двух других категорий заболевания (III и IV), при которых выявление инфекционного агента в предстательной железе затруднено или он не выявляется стандартными методами (неинфекционный простатит категории III), как и бессимптомная персистенция микроорганизмов в предстательной железе (латентный простатит категории IV), можно долго обсуждать. Очевидна определенная «однобокость» данной международной классификации с точки зрения критериев заболевания и тактики, которые нацеливают уролога, прежде всего, на поиск инфекционного фактора. Как можно классифицировать в рамках одной классификации «разные» заболевания, отличающиеся только результатами лабораторной диагностики? Очевидно, это не самостоятельные заболевания, а стадии одного и того же патологического процесса в предстательной железе. Более того, следствием такой «диагностики» становится назначение антибактериальных препаратов практически каждому больному с выявленной, «невыявленной» или «подозреваемой» инфекцией в предстательной железе. Это уводит клиническое мышление врача от выявления других патогенетических механизмов заболевания, которые выполняют роль триггера или поддерживают простатический болевой синдром за счет неинфекционных (невоспалительных), нейропатических и целого ряда других механизмов боли.
Таким образом, пришло время переосмыслить наше понимание простатита и разработать на основе новых междисциплинарных исследований последних лет документ, который позволит на данном этапе современной науки получить шанс хоть какого-то управления воспалительными заболеваниями предстательной железы. Существующая классификация NIH (1995) морально, патогенетически и тактически устарела, а принятие новой патогенетической классификации имело бы не только академическое или методологическое значение, но позволило бы соотнести новые известные данные о мультифакторном патогенезе заболеваний предстательной железы с насущными потребностями урологической практики. К слову, в 2011 году Европейское общество урологов (EAU) приняло существенные революционные изменения в классификации инфекций мочевых путей (ИМП) (классификация ORENUC), в которой немалое место отводится сопутствующим нарушениям системного метаболизма как фактора осложнения или повышенного риска ИМП. В отличие от ранее использовавшейся классификации ИМП, новая редакция, хоть и является очень громоздкой, но позволяет реализовать одну из важнейших тенденций и потребностей современной медицинской науки и практики – междисциплинарный подход, ведущий к патогенетическим методам лечения.
Мы твердо уверены, что нечто аналогичное необходимо предпринять и в отношении разработки новой патогенетической классификации СХТБ и инфекционного простатита, если мы хотим рационально и надежно управлять ими для обеспечения высокого качества жизни пациентов.
РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ СХТБ И ХРОНИЧЕСКОГО ПРОСТАТИТА EAU (2012): ЧТО НОВОГО?
В 2011 году Европейское общество урологов (EAU) опубликовало предварительные рекомендации, а в 2012 году выпустило полную версию уточненных рекомендаций по терминологии, диагностике и лечению урологического СХТБ и простатита [21]. К сожалению, на русский язык они пока не переведены, поэтому мы предлагаем ее анализ на основе собственного перевода англоязычной версии с сайта EAU, находящегося в свободном доступе в Интернете [21].
Во введении к рекомендациям, в частности, сказано, что в прошлом болевой синдром в области предстательной железы назывался «простатит», хотя доказанную бактериальную природу заболевания имеют не более 10% всех его случаев, в отношении которых и рекомендуется использовать термин «простатит» (острый или хронический). Остальные 90% заболевания при наличии болевого синдрома в области предстательной железы должны быть классифицированы как «простатический болевой синдром» (ПБС). Если болевой синдром не локализуется четко в предстательной железе, но локализуется в области малого таза у мужчин, данное состояние следует классифицировать как «синдром хронической тазовой боли» (СХТБ). При этом этиология его связана не столько с урологическими, сколько с неврологическими, сосудистыми, проктологическими и т.д. причинами [21]. Поэтому не следует любой болевой синдром в области малого таза у мужчин до проведения обследования трактовать как исключительно урологический.
Согласно новому определению, простатический болевой синдром (ПБС) – это постоянный или рецидивирующий болевой синдром в области предстательной железы длительностью не менее 3 месяцев в течение последних 6 месяцев [21]. ПБС, в отличие от инфекционного простатита, имеет неинфекционную природу и в такой интерпретации соответствует существующей трактовке понятия СХТБ/ХП III (абактериальный СХТБ) по классификации NIH (1995) [18,21]. Ключевым моментом в новом понимании патогенеза тазового и простатического болевых синдромов, по нашему мнению, является указание в рекомендациях EAU (2012) на то, что на сегодняшний день отсутствуют клинически релевантные диагностические исследования или терапевтические результаты, которые бы позволили отличить воспалительный СХТБ/ХП (категория IIIA по классификации NIH, 1995) от невоспалительного СХТБ/ХП (категория IIIB по той же классификации). Поэтому в клинической практике в настоящее время не рекомендуется различать воспалительный и невоспалительный варианты СХТБ/ХП-III [21].
Таким образом, боль в области предстательной железы и/или малого таза остается ведущим клиническим симптомом воспалительных заболеваний предстательной железы независимо от ее этиопатогенеза [21]. И проблема диагностики заключается в точном и объективном выявлении всех возможных причин болевого синдрома, а не только в поиске инфекционного агента в предстательной железе [21].
МУЛЬТИФАКТОРНАЯ ОЦЕНКА БОЛЕВОГО СИНДРОМА ПРИ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЯХ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ КАК ПУТЬ К ИХ ПАТОГЕНЕТИЧЕСКОЙ ДИАГНОСТИКЕ И ТЕРАПИИ
Боль - неприятное сенсорное ощущение или эмоциональное переживание, которому сопутствует существующее или потенциальное повреждение тканей, либо нечто, описываемое понятиями подобного повреждения (Международная ассоциация по изучению боли, 1994). Боль является универсальным проявлением повреждения или поражения органа или ткани и имеет жизненно важное защитное значение, сформировавшееся в ходе эволюции. Это сложная реакция, имеющая физиологические, сенсорные, эмоциональные, познавательные и поведенческие компоненты. Существует три основных вида болевых синдромов:
- Ноцицептивная (соматогенная) боль возникает в связи с прямым действием вредного раздражителя на кожу или ткани организма как результат раздражения болевых рецепторов. Это ключевой механизм защиты организма при повреждении или инфекционном воспалении, поэтому она еще называется воспалительная боль (острый или хронический бактериальный простатит) [21].
- Нейропатическая (неврогенная) боль исходит из места поражения центральной или периферической нервной системы. Она может сохраняться и после действия раздражителя, плохо локализована, сопровождается различными нарушениями чувствительности (одна из ведущих причин урологического СХТБ и ПБС) [21].
- Психогенная боль возникает при отсутствии органической патологии – эмоциональные боли, боли как бред или галлюцинации, боли при истерии, ипохондрии, депрессии. Чаще всего она хроническая. Вопрос о ее первичности продолжает дискутироваться. К психогенной боли примыкает так называемое соматоформное болевое расстройство – тяжелая изнуряющая боль без какой-либо известной соматической причины длительностью не менее 6 месяцев. Эта боль не соответствует анатомии органа или нервных структур, поражение которых могло бы быть причиной этого болевого синдрома.
По нашему мнению, при воспалительных заболеваниях предстательной железы мы имеем дело как с изолированным болевым синдромом различной этиологии, так и с сочетанным болевым синдромом, что наблюдается гораздо чаще (рис. 1.)
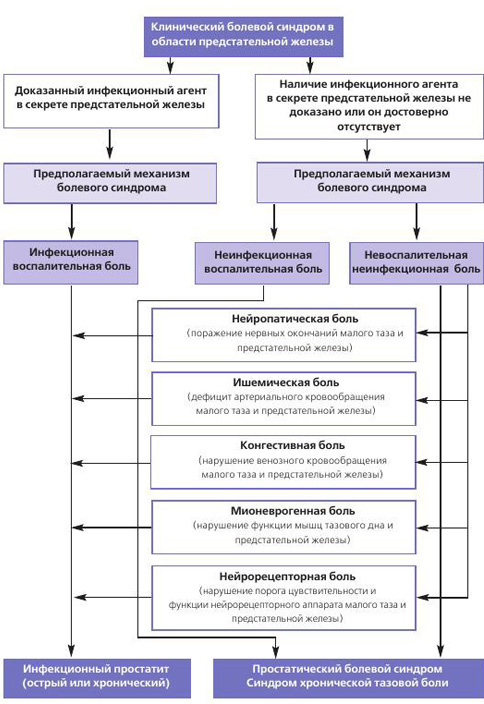
Рис 1. Основные патогенетические механизмы болевого синдрома при воспалительных заболеваниях предстательной железы.
Провести дифференциальную диагностику в клинической практике этих причин болевого синдрома достаточно сложно, но можно. Изолированная инфекционная воспалительная боль («моноболь») в предтательной железе у больного инфекционным простатитом адекватно купируется длительным (не менее 4-6 недель) курсом правильно подобранного антибиотика [21]. При полной лабораторной санации секрета простаты после курса целенаправленной антибактерильной терапии сохранение болевого синдрома может указывать на наличие нейропатического, сосудистого или любого другого неинфекционного (воспалительного или невоспалительного) компонента боли.
Мы полагаем, что резидуальные (остаточные) боли в области малого таза/предстательной железы после рационального курса противомикробной химиотерапии доказанного инфекционного простатита практически всегда будут связаны с нейропатическим компонентом, воздействия на который мы никогда не оказываем, надеясь лишь на силу антибиотиков. В соответствии с имеющимися рекомендациями по антибактериальной терапии инфекционного простатита препаратами выбора для его эмпирической терапии долгие годы являются пероральные фторхинолоны [19, 20, 21]. Однако, с одной стороны, антибиотик для эмпирической терапии должен обладать не более чем 10-20%-ным уровнем резистентности к наиболее частым патогенам, ассоциированным с хроническим инфекционным простатитом, чтобы обеспечить адекватную эрадикацию возбудителя у большинства пациентов. Мы живем в «век антибиотикорезистентности», при этом наиболее существенная проблема антимикробной химиотерапии – угрожающий рост числа патогенов, резистентных к фторхинолонам [22, 23]. Точное разграничение инфекционного и неинфекционного факторов патогенеза простатического болевого синдрома крайне важно с практической точки зрения. Если мы будет отождествлять любую боль в области предстательной железы только с инфекционной (воспалительной) болью, то мы так и останемся на пути упорного исключительного применения одних антибиотиков для ее лечения, что в условиях растущей антибиотикорезистентности непременно приведет нас в «тупик терапии», так как мы можем вскоре реально потерять единственную группу антибиотиков – фторхинолонов, которые пока остаются препаратами выбора при лечении инфекционных простатитов [22, 23]. Мы показали, что этот процесс уже, к сожалению, начался. При исследовании чувствительности простатопатогенов, выделенных из секрета предстательной железы 70 мужчин с сахарным диабетом 2 типа различной степени компенсации, диабетической урогенитальной нейропатией и андрогенным дефицитом, оказалось, что чувствительность выделенных микроорганизмов не позволяла использовать режим эмпирической антибактериальной терапии фторхинолонами, так как эти препараты продемонстрировали превышающий 10%-ный допустимый порог резистентности, являющийся основным условием эффективной эмпирической антибактериальной терапии [24].
ДИАГНОСТИКА ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ: РЕАЛИИ СЕГОДНЯШНЕГО ДНЯ И БУДУЩЕЕ ПАТОГЕНЕТИЧЕСКОЙ ДИАГНОСТИКИ
Согласно имеющимся рекомендациям, при выявлении инфекции в диагностически значимом титре из секрета предстательной железы диагноз больного с клиникой простатического болевого синдрома трактуется как «инфекционный простатит». В противоположность этому диагноз СХТБ или ПБС, согласно определению EAU (2012), является по сути симптоматическим диагнозом «исключения», так как инфекционный фактор не выявляется, а для назначения терапии требуется тщательный поиск неинфекционных причин болевого синдрома [21]. В настоящее время «золотого» стандарта диагностики СХТБ или ПБС не существует [21] (табл.1.).
Таблица 1. Рекомендованный диагностический минимум при воспалительных заболеваниях предстательной железы (EAU, 2012)
| Клиническая оценка |
| Общий анализ мочи и культуральное исследование мочи |
| Исключение ЗППП |
| Суточный ритм мочеиспусканий, урофлоуметрия и определение остаточной мочи |
| 4-стаканная проба Meares-Stamey |
| Микроскопия секрета предстательной железы |
| Культуральное исследование секрета предстательной железы |
| «Пробное» лечение антибиотиками при наличии признаков воспаления |
Однако понимание методологических проблем СХТБ и ПБС позволило европейским экспертам в новых рекомендациях 2012 года констатировать, что предлагаемый алгоритм обследования не должен включать минимальное количество диагностических тестов, так как опытный уролог сам должен определить объем обследования у конкретного больного[21]. По нашему мнению, это позволяет расширить спектр традиционной диагностики СХТБ и ПБС у каждого конкретного пациента и подтверждает правильность выбранного нами пути мультифакторной патогенетической диагностики. Мы считаем, что с учетом того, что мы проводим диагностику и лечение заболеваний андрогензависимого органа – предстательной железы, то обойтись без оценки основного условия ее нормального метаболизма – уровня тестостерона просто нельзя. Его определение позволит оценить до статочность уровня эндокринной обеспеченности организма и предстательной железы и разработать с учетом этого индивидуальные программы патогенетического лечения для каждого больного. Мы считаем, что при диагностике СХТБ, ПБС и инфекционных простатитов не может быть стандартов, универсальных для всех больных, так как все пациенты разные! В то же время мы согласны с тем, что должен быть перечень неких рекомендуемых минимальных обследований, однако каждый уролог должен сам на основе клинического мышления творчески осуществлять индивидуальную диагностику причин боли у каждого конкретного пациента.
Оценка системных гормональноетаболических условий, в которых происходит развитие и клиническая манифестация любых болевых урологических синдромов (тазовый, простатический, мошоночный и т.д.), должна проводиться, по нашему мнению, в обязательном порядке перед проведением стандартного урологического обследования у каждого больного. Это позволит «не пропустить» системные факторы болевого синдрома, так как синдром хронической тазовой или простатической боли является, по нашему мнению, одной из самых ярких клинических «болезней-масок» [24-30] (рис.2.).
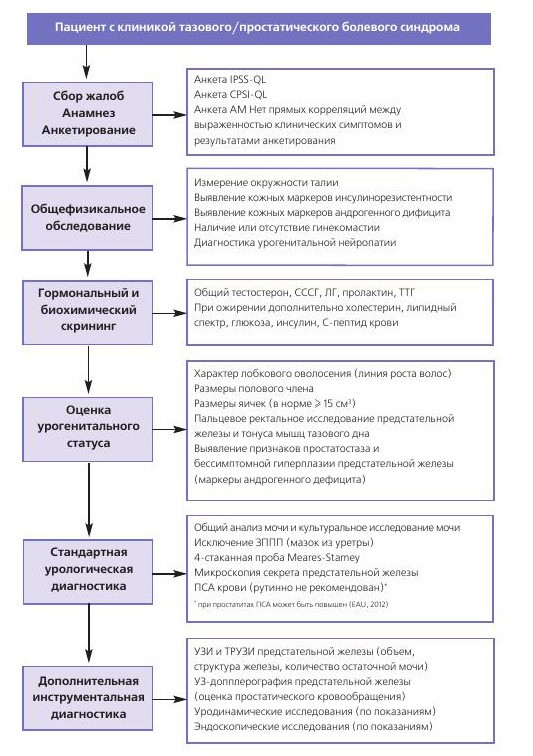
Рис 2. Оптимизация патогенетической диагностики воспалительных заболеваний предстательной железы
Почему важны для урологической практики предлагаемые нами оптимизированные схемы комплексной междисциплинарной диагностики воспалительных заболеваний предстательной железы?
Во-первых, важным и новым, на наш взгляд, положением, которое существенно обогатило современную методологическую базу воспалительных заболеваний предстательной железы, является указание в рекомендациях EAU (2012) на то, что риск развития простатита увеличивается с возрастом. Но с возрастом мужчина накапливает потенциал и других серьезных заболеваний (ожирение, сердечноосудистые заболевания, сахарный диабет 2 типа, возрастной андрогенный дефицит и т.д.). Таким образом, можно говорить о том, что простатит является своеобразным возраст-ассоциированным заболеванием [21, 24, 27-30]. Диагностика и лечение заболеваний предстательной железы существенно отличаются от лечебно-диагностических мероприятий при заболеваниях других органов, и этим ключевым отличием является андрогенозависимость предстательной железы, о которой мы в погоне за инфекцией совершенно забыли [24-31].
Во-вторых, современная наука получила достаточно доказательств патогенетической связи андрогенного дефицита, метаболического синдрома, сахарного диабета 2 типа с сосудистыми, неврологическими и другими метаболическими нарушениями на уровне систем органов и органов, включая предстательную железу [32-36]. Именно этот факт и требует сегодня своей практической реализации, что, по нашему глубокому убеждению, позволит перейти от симптоматического лечения воспалительных заболеваний предстательной железы к их патогенетической терапии и профилактике.
ЗАКЛЮЧЕНИЕ
В истории урологии не было и, пожалуй, нет и сейчас, заболеваний, более дискуссионных и сложных в понимании, чем воспалительные заболевания предстательной железы. Многовековая история их изучения не привнесла революционных перемен в эффективность современной терапии, которая, по мнению многих исследователей и клиницистов, до сих пор остается неудовлетворительной. Клиническое коварство этих заболеваний состоит в общей клинической картине наличии стойкого постоянного или рецидивирующего болевого синдрома в области малого таза и /или предстательной железы, причины которого крайне разнообразны и не всегда выявляются даже с помощью современных методов диагностики. Проблема современной методологии этих заболеваний состоит в сохраняющихся долгие годы неизменных подходах к диагностике и лечению, в алгоритмах которых попрежнему ведущее место занимают методы идентификации инфекционного агента в предстательной железе и борьба с ним. Многочисленные теории СХТБ, ПБС и хронического инфекционного простатита говорят сегодня об их однозначно мультфакторном патогенезе. Поэтому в алгоритм современной диагностики необходимо активно включать методы обследования из смежных медицинских дисциплин (неврология, эндокринология, ангиология и т.д.), а также проводить оценку гормонального и метаболического статуса каждого пациента с тазово-простатической болью. Игнорировать роль половых гормонов как основных регуляторов простатического кровообращения, иннервации, метаболизма и иммунитета уже невозможно.
«Готовы ли мы сейчас для публикации рекомендаций по лечению хронического простатита? Мы думаем, что нет. Однако нам это надо сделать для того, чтобы перейти через трясину под названием «хронический простатит», - так в свое время высказался Д.К.Никель, один из основоположников современного учения о хроническом простатите.
Нам кажется, что новое понимание патогенеза воспалительных заболеваний предстательной железы на основе междисциплинарных взаимодействий поможет нам перейти эту диагностическую «трясину». Другого пути просто нет, так как только такой лечебноиагностический сценарий соответствует высоким требованиям медицины XXI века – века патогенетической профилактики и патогенетического лечения всех заболеваний мужчин и их высокого качества жизни.
ЛИТЕРАТУРА
1. Young HH, Gereghty JC, Stevens AR. Chronic Prostatitis. // Johns Hopkins Hospital Rep. 1906. № 3. Р. 271-384.
2. Nickel AC. The localization in animals of bacteria isolated from foci of infection. // JAMA. 1926. № 87. Р. 1117-1122.
3. Campbell MF. Principals of urology: an introductory text to the diseases of the urogenital tract. Philadelphia: W.B. Saunders, 1957. – Р. 311-314.
4. Руководство по урологии. / Под ред. Лопаткина Н.А. М.: Медицина, 1998. Том 2. – С. 393-440.
5. Простатит. / Под ред. Щеплева П.А. М.: МЕД-Пресс-Информ, 2007. 224 с.
6. Урология. Национальное руководство. / Под ред. Лопаткина Н.А. М.: ГЭОТАР-Медиа, 2009. 1024 с.
7. Meares EM, Stamey TA. Bacteriologic localization patterns in bacterial prostatitis and urethritis. // Invest Urol. 1968.Vol. 5, № 5. Р. 492-518.
8. Drach GW, Mears EM, Fair WR, Stamey TA. Classification of benigh disease associated with prostatic pain: Prostatitis or Prostatodynia? // J. Urol. 1978. Vol. 120, № 2. Р. 266.
9. Ильин И.И. Негонококковые уретриты у мужчин. М.: Медицина, 1991. 288 с.
10. Lummus WF, Thompson I. Prostatitis // Emerg Med Clin North. Am. 2001. Vol. 19, № 3. Р. 691-707.
11. Mearеs EM. Prostatitis // In: Scientific foundation of Urology. / Eds. Chisholm GT, Fair WR, 3rd ed. - London: Hememann, 1990. – Р. 373- 378.
12. Nickel JC. The Pre and Post massage test (PPMT): a simple screening for prostatitis. // Tech. Urol. 1997. Vol. 3, № 1. Р. 38-43.
13. Аполихин О.И., Сивков А.В., Лямин Б.А. Стандартизация оценки результатов лечения хронического простатита. // Материалы Пленума Правления Всеросс. общ-ва урологов. Саратов, 2004. – С. 30-31.
14. Извозчиков С.Б., Каприн А.Д. Синдром хронической тазовой боли: современные подходы к проблеме. // Материалы VI Российского конгресса «Мужское здоровье». - Москва, 2010. – С. 70-71.
15. McNaughton Colins M, Fowler FJ Jr, Elliot DB, Albertsen PC, Barry MJ. Diagnosing and treating chronic prostatitis: do urologist use fourglass test? // Urol. 2000. Vol. 55, № 3. Р. 403-407.
16. Hellstrom WJ, Schmidt RA, Lue TF, Tanagho EA. Neuromuscular dysfunction in non-bacterial proststitis. // Urol. 1987. Vol. 30, № 2. Р. 183-187.
17. Руководство по андрологии. / Под ред. Тиктинского О.Л. Л.: Медицина, 1990. 416 с.
18. NIH Summary Statement. NIH/NIDDK workshop on Chronic Prostatitis Executive Summary, Bethesda MD, December, 1995.
19. Guideline on Chronic Pelvic Pain Syndrome/Chronic Prostatitis. EAU, 2003. 94 р.
20. Guideline on Chronic Pelvic Pain Syndrome/Chronic Prostatitis. EAU, 2008. 101 р.
21. Guideline on Chronic Pelvic Pain Syndrome. EAU, 2012. 132 р.
22. Рафальский В.В., Страчунский Л.С., Бабкин П.А. Валенская В.С., Габбасова Л.А., Дмитриева О.Б., Емельянова И.В., Крупин В.Н., Малев И.В., Петров С.Б., Рохликов И.М., Фурлетова Н.М., Хайруллов А.С. Резистентность возбудителей неосложненных инфекций мочевых путей в России. // Урология. 2006. № 5. С. 34-37.
23. Научный отчет о результатах многоцентрового исследования динамики антибиотикорезистентности возбудителей инфекций мочевых путей в различных субпопуляциях пациентов («ДАР- МИС»). Смоленск, 2011. - 118 с.
24. Тюзиков И.А. Новые патогенетические подходы к диагностике заболеваний предстательной железы у мужчин с ожирением, андрогенным дефицитом и диабетической нейропатией. // Андрология и генитальная хирургия. 2011. № 4. С. 34-39.
25. Калинченко С.Ю., Тюзиков И.А. Практическая андрология. М.: Практическая медицина, 2009. 400 с.
26. Kalinchenko S, Vishnevsky EL, Koval AN, Mskhalaya GJ, Saad F. Beneficial effects of testosterone administration on symptoms of the lower urinary tract in men with late-onset hypogonadism: a pilot study. // Aging Male. 2008. Vol. 11, № 2. Р. 57–61.
27. Тюзиков И.А., Иванов А.П. Абактериальный синдром хронической тазовой боли у мужчин как мультидисциплинарная проблема. // Фундаментальные исследования. 2012. № 1. С. 121-124.
28. Тюзиков И.А., Мартов А.Г., Калинченко С.Ю. Влияние ожирения и андрогенного дефицита на кровообращение предстательной железы. // Бюллетень Сибирской медицины. 2012. № 2. С. 80-83.
29. Тюзиков И.А. Клинико-экспериментальные параллели в патогенезе заболеваний предстательной железы. // Современные проблемы науки и образования (электронный журнал). 2012. № 1; URL: www.science-education.ru/101-5476 (дата обращения: 08.02.2012).
30. Тюзиков И.А., Мартов А.Г., Калинченко С.Ю. Новые системные механизмы патогенеза симптомов нижних мочевых путей у мужчин (литературный обзор). // Бюллетень Сибирской медицины. 2012. № 2. С. 93-100.
31. Gorbachinsky I, Akpinar H, Assimos DG. Metabolic syndrome and urological diseases. // Rev Urol. 2010. Vol. 12, № 4. Р. 157-180.
32. Kalinchenko SY, Tishova YA, Mskhalaya GJ, Gooren LJ, Giltay EJ, Saad F. Effects of testosterone supplementation on markers of the metabolic syndrome and inflammation in hypogonadal men with the metabolic syndrome: the double-blinded placebo-controlled Moscow study.// Clin Endocrinol. (Oxf). 2010. Vol. 73, № 5. Р. 602-612.
33. McVary K. Lower urinary tract symptoms and sexual dysfunction: epidemiology and pathophysiology. // BJU Int. 2006. Vol. 97, Suppl. 2. Р. 23–28.
34. Ozden C, Ozdal OL, Urgancioglu G. The correlation between metabolic syndrome and prostatic growth in patients with benign prostatic hyperplasia. // Eur Urol. 2007. Vol. 51, № 1. Р. 199–203.
35. Srikanthan P, Karlamangla AS. Relative Muscle Mass Is Inversely Associated with Insulin Resistance and Prediabetes. Findings from the third National Health and Nutrition Examination Survey. // JCEM. 2011. Vol 96. P. 2898-2903
36. Yassin AA, Saad F, Gooren LJ. Metabolic syndrome, testosterone deficiency and erectile dysfunction never come alone. // Andrologia. 2008. Vol. 40, № 4. Р. 259–264.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 246.32 кб |















































































