Применение ингибиторов фосфодиэстеразы 5 типа у пациентов с гиперактивным мочевым пузырем
 10734
10734 А.В. Сивков, В.В. Ромих, Е.С. Коршунова, М.Н. Коршунов
НИИ урологии Минздравсоцразвития, Москва
В настоящее время известно 11 изоформ фосфодиэстеразы (ФДЭ). Распределение их в тканях организма происходит следующим образом: сердце ФДЭ 1, 2 и 3 типов, почки ФДЭ 4 и 9 типов, гладкие мышцы ФДЭ 5 типа, фоторецепторы ФДЭ 6 типа, скелетная мускулатура ФДЭ 7 типа, тестикулы ФДЭ 8 и 10 типов, головной мозг ФДЭ 10 типа, предстательная железа ФДЭ 11 типа [1]. Появление селективных ингибиторов ФДЭ 5 типа (иФДЭ-5) стало основой проведения большого числа исследований, направленных на изучение функции и клинического значения фармакологического воздействия на эти ферменты в разных тканях организма. Эффективность ингибиторов ФДЭ 5 типа при лечении эректильной дисфункции известна давно. В последнее время появились сообщения об использовании данных препаратов при гиперактивном мочевом пузыре (ГМП) [2, 3].
Существует все больше доказательств, что уротелий, детрузор и простата обладают способностью высвобождать химические молекулы аденозинтрифосфат, ацетилхолин и оксид азота (NO) [4-9]. В ткани детрузора NO, выделяемый из нервных окончаний, инициирует биохимический каскад: NO диффундирует в гладкомышечные клетки и соединяется с ферментом гуанилатциклазой (ГЦ), в результате чего его активность значительно возрастает [10, 11, 12]. Это приводит к повышению продукции цГМФ, который, в свою очередь, активирует протеинкиназу, фосфорилирующую несколько различных белков, что ведет к снижению внутриклеточной концентрации ионов Ca2 [13, 14]. Итогом описанного процесса является расслабление гладкомышечных клеток детрузора. Концентрация цГМФ во всех клетках определяется соотношением между уровнем его продукции ГЦ и скоростью его распада, происходящего в результате воздействия ферментов группы фосфодиэстераз [15]. Нарушение баланса между двумя этими процессами, приводит к снижению внутриклеточной концентрации цГМФ. В этой связи, воздействие на активность ФДЭ 5 типа, являющейся доминирующей формой данного фермента в гладких миоцитах, можно считать логически обоснованным методом коррекции детрузорной гиперактивности. Следует отметить, что в условиях ингибирования ФДЭ даже незначительное усиление активности ГЦ может приводить к резкому повышению внутриклеточной концентрации цГМФ и, соответственно, к снижению тонуса гладкомышечных клеток. По мнению ряда авторов, ингибиторы ФДЭ 5 типа способны уменьшить гиперактивность детрузора, хотя бы частично [10, 12, 16-20].
В исследовании Porst H., Sandner P., Ulbrich E. (2008) было изучено влияние варденафила на симптомы нижних мочевых путей при доброкачественной гиперплазии предстательной железы (ДГПЖ). Авторы сделали вывод, что основной эффект варденафила снижение ирритативной симптоматики связан именно с детрузором, а не с предстательной железой [18].
Варденафил является селективным ингибитором цГМФспецифической ФДЭ 5 типа. Варденафил быстро абсорбируется при приеме внутрь. Абсолютная биодоступность 15%. При приеме внутрь здоровыми добровольцами однократной дозы 20 мг Ттах составляет 30-120 мин. (в среднем 60 мин.). Общий клиренс варденафила 56 л/час., терминальный Т1/2 варденафила примерно 4-5 час. Препарат применяется внутрь, независимо от приема пищи, начальная доза составляет 10 мг за 25-60 мин. до полового акта; можно принимать также за 4-5 часов до сексуального контакта. С учетом эффективности и переносимости доза может быть увеличена до 20 мг или уменьшена до 5 мг. Максимальная рекомендуемая частота приема 1 раз в сутки. Для достижения эффективности необходим достаточный уровень сексуальной стимуляции. Максимальная суточная доза 20 мг [21].
В современной литературе встречается ряд статей, посвященных изучению действия варденафила при ГМП как в эксперименте, так и в практике. Одним из фундаментальных исследований можно считать работу Matsumoto S. et al. (2009), в которой изучалось влияние варденафила на симптомы нижних мочевых путей (СНМП), вызванные искусственно созданной инфравезикальной обструкцией у самок крыс. Была доказана эффективность высоких доз варденафила [22].
В рандомизированном плацебо-контролируемом исследовании Stief C.G. et al. (2008) мужчинам с СНМП вследствие ДГПЖ назначали варденафил по 10 мг два раза в сутки. Через 8 недель лечения авторы отметили статистически значимое снижение суммарного балла по шкале IPSS, улучшение эректильной функции и повышение качества жизни больных. Исследователи сделали вывод, что варденафил является многообещающим методом лечения СНМП при ДГПЖ [23].
Цель работы сравнительная оценка эффективности М-холинолитиков (солифенацина) и ингибиторов фосфодиэстеразы 5 типа (варденафила) у больных ГМП.
Материалы и методы
В исследовании приняли участие 26 мужчин (средний возраст 45,7 лет) с подтвержденным уродинамически ГМП и жалобами на снижение эрекции. Ни у одного больного не было данных за неврологические заболевания головного и спинного мозга и инфравезикальную обструкцию. Из исследования исключены больные с урологическими заболеваниями, в клинической картине которых были симптомы накопления нижних мочевых путей, но характер которых не соответствовал теме исследования. В частности мы исключили больных с хроническим простатитом, ДГПЖ и раком предстательной железы. Также в исследуемую группу не вошли больные сахарным диабетом. Таким образом, 26 больным данной группы был назначен варденафил по 10 мг 2 раза в сутки на протяжении 8 недель.
В качестве контрольной группы, по данным архивной документации, были отобраны 26 мужчин с ГМП и сходными клиническими показателями, которые принимали солифенацин по 5 мг в сутки в течение 8 недель. Отметим, что у 9 больных первой и 10 больных второй группы, помимо учащенного мочеиспускания и ургентных позывов, было выявлено императивное недержание мочи. Эффективность проводимой терапии оценивали по данным визуальной аналоговой шкалы, опросника IPSS, шкалы Homma, дневника мочеиспусканий, а в первой группе, кроме того, были выполнены уродинамические исследования.
Результаты
Субъективно все больные первой группы по окончании курса лечения отметили улучшение своего состояния. Через 8 недель приема варденафила зарегестрировано: снижение числа мочеиспусканий в сутки с 11,5 ± 3,0 (8-15) до 10,0 ± 2,6 (6-12); числа императивных позывов с 2,3 ± 1,1 (1-5) до 1,8 ± 0,9 (0-4) и эпизодов ургентного недержания мочи с 2,0 ± 1,1 (1-4) до 1,3 ± 0,8 (0-4). Отметим, что снижение числа мочеиспусканий, ургентных позывов и эпизодов ургентного недержания мочи, в целом по группе, не достигли статистической достоверности. В то же время, у 4 из 26 больных, симптомы ГМП полностью исчезли. Констатировано снижение среднего суммарного балла IPSS с 13,5 ± 1,7 до 10,8 ± 0,9, а по шкале Homma с 9,4 ± 2,3 (4-14) до 8,1 ± 3,5 (2-11). Анализ визуальных аналоговых шкал свидетель
Таблица 1. Динамика средних значений основных клинических показателей до и после применения варденафила у больных первой группы (n = 26)
| Показатель | До лечения | Через 8 недель лечения |
| Суммарный балл по шкале IPSS | 13,5 ± 1,7 | 10,8 ± 0,9** |
| Суммарный балл по шкале Homma | 9,4 ± 2,3 | 8,1 ± 3,5* |
| Число мочеиспусканий | 11,5 ± 3,0 | 10,0 ± 2,6 |
| Число ургентных позывов к акту мочеиспускания | 2,3 ± 1,1 | 1,8 ± 0,9 |
| Число эпизодов ургентного недержания мочи | 2,0 ± 1,1 | 1,5 ± 0,8 |
| Средний цистометрический объем мочевого пузыря | 150,2 ± 31,5 | 224,7 ± 40,1** |
| * различие достоверно по сравнению с соответствующим показателем до лечения (р < 0,05); **различие достоверно по сравнению с соответствующим показателем до лечения (р < 0,01). | ||
При цистометрии у 26 больных первой группы до лечения были выявлены непроизвольные сокращения детрузора. После приема варденафила объем наполнения, при котором они возникали, в среднем, увеличился с 93,9 ± 14,5 до 146,4 ± 13,0 см вод. ст. Число непроизвольных сокращений детрузора снизилось с 2,5 ± 1,1 до 1,9 ± 0,9, амплитуда максимального непроизвольного сокращения детрузора с 21,1 ± 10,0 до 15,3 ± 9,4 см вод. ст. Только у 2 из 9 больных по-прежнему отмечалось императивное недержание мочи. Среднее значение цистометрической емкости увеличилось со 150,2 ± 31,5 до 224,7 ± 40,1 см вод. ст. (таблица 1).
У трех (11,5%) из 26 больных на фоне лечения отмечены головные боли, у двух (7,7%) тошнота, один (3,9%) пациент отметил гиперемию лица, один (3,9%) боли в спине. Отметим, что эти побочные явления были легкой и средней степени выраженности и не потребовали снижения дозы/отмены препарата (рисунок 1).
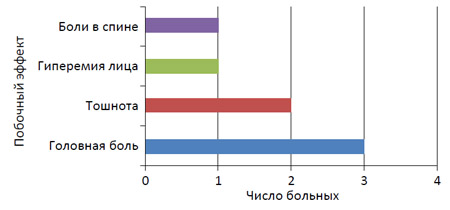
Рисунок 1. Распространенность побочных эффектов при применении варденафила для лечения больных ГМП
Согласно ретроспективным данным, через 8 недель приема солифенацина субъективно все больные контрольной группы отметили улучшение общего состояния. Суммарный балл по шкале IPSS у них уменьшился с 11,3 ± 1,6 (8-15) до 8,5 ± 1,8 (5-11), а показатель шкалы Homma с 10,9 ± 2,1 (4-16) до 7,9 ± 3,9 (2-11). Число мочеиспусканий в сутки уменьшилось с 11,0 ±3,4 (8-19) до 8,8 ±2,4 (6-13). Количество ургентных позывов, в среднем, снизилось с 2,9 ± 1,4 (1-5) до 1,9 ± 0,9 (0-4), а эпизодов ургентного недержания мочи с 2,6 ± 1,2 (1-5) до 1,7 ± 0,8 (0-4). Эпизоды ургентного недержания мочи исчезли у 12 из 26 больных (46%). Среднеэффективный объем мочевого пузыря увеличился с 154,3 ± 19,6 (130-185) до 205,0 ± 31,7 (150 -250) мл (таблица 2).
Таблица 2. Изменение средних значений основных клинических показателей до и после применения солифенацина у больных второй группы (n = 26)
| Показатель | До лечения | Через 8 недель лечения |
| Суммарный балл по шкале IPSS | 11,3 ± 1,6 | 8,5 ± 1,8** |
| Суммарный балл по шкале Homma | 10,9 ± 2,1 | 7,9 ± 3,9** |
| Число мочеиспусканий | 11,0 ± 3,4 | 8,8 ± 2,4** |
| Число ургентных позывов к акту мочеиспускания | 2,9 ± 1,4 | 1,9 ± 0,9** |
| Число эпизодов ургентного недержания мочи | 2,6 ± 1,2 | 1,8 ± 0,8** |
| Средний цистометрический объем мочевого пузыря | 154,3 ± 19,6 | 237,0 ± 31,7** |
| * различие достоверно по сравнению с соответствующим показателем до лечения (р < 0,05); **различие достоверно по сравнению с соответствующим показателем до лечения (р < 0,01). | ||
Побочные эффекты в виде сухости во рту (4) и нарушения опорожнения кишечника (3) констатированы у 7 больных (27%). Данные осложнения были расценены как незначительные и не потребовали снижения дозы или отмены препарата. Ни у одного больного не было выявлено головной боли и нарушения аккомодации (рисунок 2).
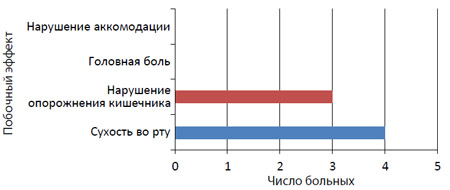
Рисунок 2. Распространенность побочных эффектов при лечении солифенацином больных ГМП
Клиническое наблюдение. Больной Б., 49 лет, водитель, женат, двое детей, в течение года страдает симптомами ГМП. Предъявляет жалобы на учащенное мочеиспускание до 14 раз в сутки, ургентные позывы, ноктурию до 3 раз, нарушение сна, нарушение эректильной функции. Последние два месяца стал отмечать утечку мочи при императивном позыве. Изменений со стороны нижних мочевых путей не выявлено.
При обследовании суммарный балл симптоматики IPSS составил 14 (11 за счет наличия ирритативных симптомов и 3 за счет обструктивных). Уровень качества жизни по QOL 5 баллов.
В общем анализе и посеве мочи признаков воспаления и инфекции мочевых путей выявлено не было. При УЗИ почек и мочевого пузыря отклонений не выявлено, предстательная железа объемом 22 см3, изоэхогенна, остаточной мочи нет, среднеэффективный объем мочевого пузыря 180 мл. При проведении комплексного уродинамического исследования выявлена детрузорная гиперактивность. Отмечены непроизвольные сокращения детрузора, сопровождающиеся повышением детрузорного давления (P det.) до 24 см вод. ст. в фазе наполнения мочевого пузыря. Первое непроизвольное сокращение детрузора при объеме 79 мл, повышение детрузорного давления до 21 см вод. ст. Максимальная цистометрическая емкость 236 мл (рисунок 3).
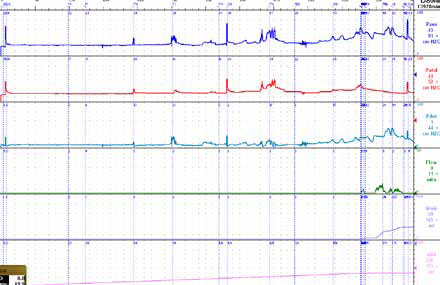
Рисунок 3. Больной Б: уродинамическая картина детрузорной гиперактивности
Для определения причины детрузорной гиперактивности больному была проведена компьютерная томограмма головы и позвоночника, а так же консультация невролога патологических изменений со стороны нервной системы не было выявлено. Пациенту поставлен диагноз: гиперактивный мочевой пузырь, идиопатическая детрузорная гиперактивность. Эректильная дисфункция. Назначен варденафил по 10 мг два раза в сутки. Курс лечения составил 8 недель.
На фоне лечения отмечена существенная позитивная динамика. Выраженность симптомов по шкале IPSS сократилась до 8 или на 43%. Частота дневных мочеиспусканий снизилась до 8, а ночных до 1 раза. Отмечено улучшение эректильной функции с 17 до 25 баллов (на 47%) (МИЭФ-5). Показатель качества жизни составил 1 (QoL).
Уродинамически результаты лечения проявились снижением количества непроизвольных сокращений детрузора и их амплитуды в ходе цистометрии. Первое непроизвольное сокращение детрузора наблюдали при объеме 212 мл, повышение детрузорного давления до 15 см вод. ст. Максимальная цистометрическая емкость составила 254 мл. При мочеиспускании на графике ЭМГ непроизвольных сокращений мышц тазового дна не выявлено. Максимальная скорость потока мочи не изменилась (рисунок 4).
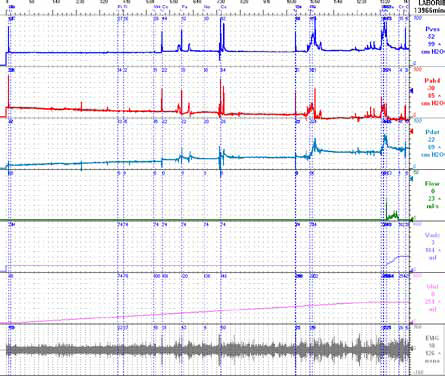
Рисунок 4. Больной Б: позитивные уродинамические изменения после лечения варденафилом
Обсуждение
В рандомизированном двойном слепом плацебо-контролируемом исследовании Stief C.G. et al. (2008) изучалось влияние варденафила на функцию нижних мочевых путей и качество жизни у мужчин с доброкачественной гиперплазией простаты в сочетании или без эректильной дисфункции [23]. Участвовали мужчины в возрасте 45-64 лет с симптомами нижних мочевых путей, ассоциированными с ДГПЖ. Суммарный балл по шкале IPSS был больше или равен 12. После рандомизации больные получали либо по 10 мг варденафила, либо плацебо дважды в день. Функция нижних мочевых путей оценивалась с использованием основных параметров эффективности: суммарный балл по шкале IPSS, максимальная скорость потока мочи (Q ), а также объем остаточной мочи. Эректильная функция определялась с помощью анкеты «Международный индекс эректильной функции» (МИЭФ). Качество жизни оценивали по вопроснику Urolifetrade-9.
После 8 недель лечения, произошло значительное снижение общего балла IPSS в группе варденафила по сравнению с плацебо (-5,9 и -3,6 соответственно, р = 0,0013). Номинально значительные улучшения произошли в отношении ирритативной и обструктивной симптоматики (по шкале IPSS) (р = 0,0017 и р = 0,0081 соответственно), эректильной функции (р = 0,0001), а также качества жизни по Urolifetrade-9 (р < 0,0001) в группе принимавшей варденафил. Q и объем остаточной мочи существенно не изменились. Варденафил, как правило, хорошо переносился. Побочные эффекты, наблюдаемые при приеме варденафила, имели легкую или умеренную степень тяжести. Авторы пришли к выводу, что варденафил значительно улучшает симптоматику нижних мочевых путей, эректильную функцию и качество жизни у мужчин с ДГПЖ.
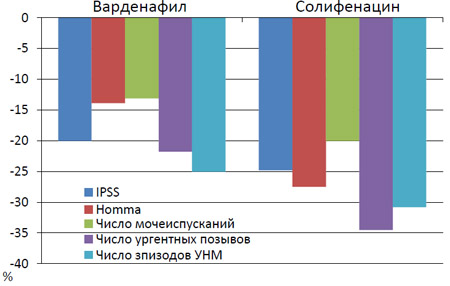
Рисунок 5. Динамика основных клинических показателей в обеих группах (%)
В своей работе мы представили сравнение разных видов лечения в двух группах больных сопоставимых по тяжести клинических симптомов, возрасту, полу и при отсутствии сведений о наличии доброкачественной гиперплазии предстательной железы.
Нами установлено, что суммарный балл по шкале IPSS при приеме варденафила уменьшился на 20%, а при приеме солифенацина на 24,8%. Суммарный балл по шкале Homma при приеме ФДЭ5 ингибитора снизился на 13,9%, при приеме солифенацина на 27,5%. Частота мочеиспусканий в сутки уменьшилась на 13,1% на фоне приема варденафила и на 20,0% при лечении солифенацином. Число ургентных позывов снизилось на 21,8% и 34,5% при приеме варденафила и солифенацина соответственно. Число эпизодов ургентного недержания мочи при назначении варденафила снизилось на 25,0%, а солифенацина на 30,8% (рисунок 5).
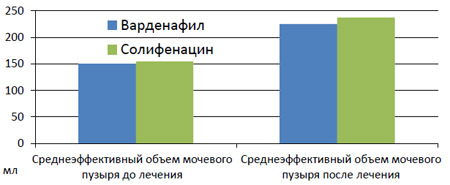
Рисунок 5. Динамика основных клинических показателей в обеих группах (%)
Средний эффективный объем мочевого пузыря по данным КУДИ в I группе, принимавшей варденафил, увеличился на 49,6%. Во II группе, использовавшей солифенацин, объем мочевого пузыря по данным УЗИ увеличился на 53,6% (рисунок 6).
Анализ объективных результатов лечения свидетельствует о достоверном снижении средних значений IPSS, шкалы Homma и увеличении среднеэффективного объема мочевого пузыря после назначения варденафила. В то же время, такой объективный показатель, как снижение числа ургентных позывов и эпизодов ургентного недержания за сутки статистически достоверно уменьшился только у больных, получавших солифенацин. Важным фактором является улучшение эректильной функции у больных группы варденафила.
Заключение
Несмотря на то, что применение варденафила по влиянию на функцию нижних мочевых путей у больных ГМП несколько уступает по своей эффективности солифенацину, мы считаем целесообразным использование ингибиторов ФДЭ 5 типа у мужчин с ГМП в сочетании с эректильной дисфункцией или в составе комбинированной терапии ДГПЖ. Метод является патогенетически обоснованным. Варденафил при ежедневном приеме достоверно снижает выраженность симптомов ГМП, способствует улучшению эректильной функции и, как результат, ведет к улучшению качества жизни пациентов.
Ключевые слова: гиперактивный мочевой пузырь, лечение, качество жизни, варденафил, солифенацин. Keywords: hyperactive bladder, treatment, quality of life, vardenafil, solifenacin.
Литература
- Верткин А.Л.. Выбор ингибитора фосфодиэстеразы типа 5: взгляд клинического фармаколога // Consilium-medicum. 2004. Т. 6. № 7. С. 502-505
- Speakman M.J. PDE5 inhibitors in the treatment of LUTS // Curr. Pharm. Des. 2009. Vol. 15. № 30. P. 3502-3205.
- Mouli S., McVary K.T. PDE5 inhibitors for LUTS. // Prostate Cancer Prostatic Dis. 2009. Vol.12. № 4. P. 316-324.
- Yoshida M., Masunaga K., Nagata T., Yono M., Homma Y. The forefront for novel therapeutic agents based on the pathophysiology of lower urinary tract dysfunction: pathophysiology and pharmacotherapy of overactive bladder // J. Pharmacol. Sci. 2010. Vol. 112. № 2. P. 128-134.
- Kedia G.T., Uckert S., Jonas U., Kuczyk M.A., Burchardt M. The nitric oxide pathway in the human prostate: clinical implications in men with lower urinary tract symptoms // World J. Urol. 2008. Vol. 26. № 6. P. 603-609.
- Guh J.H., Hwang T.L., Ko F.N., Chueh S.C., Lai M.K., Teng C.M. Antiproliferative effect in human prostatic smooth muscle cells by nitric oxide donor. Mol. Pharmacol. 1998. Mar. 53 (3): 467-74.
- Montorsi F., Corbin J., Phillips S. Review of phosphodiesterases in the urogenital system: new directions for therapeutic intervention. J. Sex Med. 2004. Nov. 1 (3): 322-36.
- Tinel H., Stelte-Ludwig B., HUtter J., Sandner P. Pre-clinical evidence for the use of phosphodiesterase-5 inhibitors for treating benign prostatic hyperplasia and lower urinary tract symptoms. BJU Int. 2006. Dec. 98 (6): 1259-63.
- Fibbi B., Morelli A., Vignozzi L., Filippi S., Chavalmane A., De Vita G., Marini M., Gacci M., Vannelli G.B., Sandner P., Maggi M. Characterization of phosphodiesterase type 5 expression and functional activity in the human male lower urinary tract. J. Sex Med. 2010. Jan. 7 (1 Pt 1): 59-69.
- Yoshimura N., Kaiho Y., Miyazato M., Yunoki T., Tai C., Chancellor M.B., Tyagi P. Therapeutic receptor targets for lower urinary tract dysfunction // Naunyn Schmiedebergs Arch Pharmacol. 2008. Vol. 377. № 4-6. P. 437-448.
- Andersson K.E, Persson K. Nitric oxide synthase and nitric oxide-mediated effects in lower urinary tract smooth muscles. // World J. Urol. 1994. Vol. 12. P. 274-280.
- Andersson K.E., Wein A.J. Pharmacology of the lower urinary tract: basis for current and future treatments of urinary incontinence. // Pharmacol Rev. 2004. Vol. 56. P. 581-631.
- Waldkirch E.S., Uckert S., Langnase K., Richter K., Jonas U., Wolf G., Andersson K.E., Stief C.G., Hedlund P. Immunohistochemical distribution of cyclic GMP-dependent protein kinase-1 in human prostate tissue //Eur. Urol. 2007. Vol. 52. № 2. P. 495-501.
- Uckert S., Oelke M., Stief C.G., Andersson K.E., Jonas U., Hedlund P. Immunohistochemical distribution of cAMPand cGMP-phosphodiesterase (PDE) isoenzymes in the human prostate // Eur. Urol. 2006. Vol. 49. № 4. P. 740-745.
- Мазо Е.Б., Гамидов С.И., Овчинников Р.И. Пероральная монои комбинированная терапия эректильной дисфункции ингибиторами фосфодиэстеразы-5 и Импазой новым отечественным индуктором NO-синтазы // Русский медицинский журнал. 2004. Т. 12. № 8. С. 552559.
- Roehrborn C.G. Lower urinary tract symptoms, benign prostatic hyperplasia, erectile dysfunction, and phosphodiesterase-5 inhibitors. // Rev. Urol. 2004. Vol. 6. № 3. P. 121-127.
- Uckert S., Kuthe A., Jonas U., Stief C.G. Characterization and functional relevance of cyclic nucleotide phosphodiesterase isoenzymes of the human prostate // J. Urol. 2001. Vol. 166. P. 2484-2490.
- Porst H., Sandner P., Ulbrich E. Vardenafil in the treatment of lower urinary tract symptoms secondary to benign prostatic hyperplasia // Curr. Urol. Rep. 2008. Vol. 9. № 4. P. 295-301.
- Filippi S., Morelli A., Sandner P., Fibbi B., Mancina R., Marini M., Gacci M., Vignozzi L., Vannelli G.B., Carini M., Forti G., Maggi M. Characterization and functional role of androgen-dependent PDE5 activity in the bladder. Endocrinology. 2007. Mar. 148 (3): 1019-29.
- Morelli A., Filippi S., Sandner P., Fibbi B., Chavalmane A.K., Silvestrini E., Sarchielli E., Vignozzi L., Gacci M., Carini M., Vannelli G.B., Maggi M. Vardenafil modulates bladder contractility through cGMP-mediated inhibition of RhoA/Rho kinase signaling pathway in spontaneously hypertensive rats. J. Sex Med. 2009. Jun. 6 (6): 1594-608.
- Справочник лекарств РЛС.
- Matsumoto S., Hanai T., Uemura H., Levin R.M. Effects of chronic treatment with vardenafil, a phosphodiesterase 5 inhibitor, on female rat bladder in a partial bladder outlet obstruction model. BJU Int. 2009. Apr. 103 (7): 987-90. Epub 2008 .Nov. 13.
- Stief C.G., Porst H., Neuser D., Beneke M., Ulbrich E. A randomised, placebo-controlled study to assess the efficacy of twice-daily vardenafil in the treatment of lower urinary tract symptoms secondary to benign prostatic hyperplasia. Eur. Urol. 2008. Jun. 53 (6): 1236-44.
| Прикрепленный файл | Размер |
|---|---|
| Статья в формате PDF | 457.39 кб |















































































