Протезирующая реконструкция тазового дна влагалищным доступом: современный взгляд на проблему
 7912
7912 Пролапс тазовых органов (ПТО) и стрессовое недержание мочи (СНМ) относятся к наиболее часто встречающимся заболеваниям у женщин средней и старшей возрастной группы. По данным Л.В. Адамян и В.И. Кулакова в России проявления ПТО наблюдаются у 15-40 % женского населения [1, 2]. Симптомы СНМ в нашей стране встречаются у 38,6% женщин [3]. Согласно данным масштабного популяционного исследования J.M. Wu с соавт., каждая пятая женщина к 80 годам переносит операцию по поводу СНМ или ПТО, причем при СНМ пик хирургической активности приходится на возраст 46 и 70-71 год (3,8-3,9 на 1000 женщин), при ПТО на 71-73 года (4,3 на 1000 женщин) [4].
Конец ХХ – начало ХХI века ознаменовались бурным развитием протезирующей тазовой хирургии. В 1996 г. Ethicon (США) представил синтетическую петлю для лечения СНМ (TVT™), а в 2004 г. AMS (США) первые наборы для тазовой реконструкции (Apogee™, Perigee™). К 2010 году было создано уже около 100 различных модификаций сетчатых протезов. За этот же год только в США выполнено 300 000 операций по поводу ПТО, при этом треть проводилась с использованием сетчатых имплантатов, три четверти из которых были установлены трансвагинально [5]. В августе-сентябре 2011 года FDA опубликовало официальное предостережение, сделанное на основе анализа проблем, связанных с применением «влагалищных сеток» в хирургии ПТО и СНМ. Было принято решение о запрещении вывода на рынок новых протезов без предварительных многоцентровых клинических исследований, как это было ранее. Врачей же обязали проходить специальное обучение методикам имплантации протезов и возможным рискам, а также ставить пациентов в известность о возможных осложнениях.
Цель настоящего обзора – определить место протезирующей пластики в лечении СНМ и ПТО на современном этапе, а также представить преимущества, недостатки основных методик и показания для их использования.
СИНТЕТИЧЕСКИЕ СЛИНГИ В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ СНМ
На сегодняшний день известно более 200 хирургических способов лечения стрессового недержания мочи у женщин [6]. Традиционными являются позадилонные методики, включающие кольпосуспензию по Burch и пубовагинальные слинги. Благодаря своей высокой эффективности эти вмешательства долгое время были золотым стандартом лечения СНМ. В отличие от традиционных методик U. Ulmsten и P. Petros предложили операцию с использованием синтетической петли, основанную на «интегральной теории» удержания мочи и направленную, прежде всего на реконструкцию пубоуретральных связок [7]. Главное отличие состояло в локализации петли, которая теперь располагалась под средней уретрой и без натяжения (tension-free vaginal tape). Легкость освоения, малая травматичность и высокая эффективность открыли новую страницу в хирургии СНМ. Операция может выполняться по восходящему (снизу-вверх) или нисходящему (сверху-вниз) типу. Использование восходящей методики по сравнению с нисходящей позволяет снизить количество перфораций мочевого пузыря (4,7% против 8,5%; ОР 0,55 (от 0,31 до 0,98), 95% ДИ), эрозий влагалища (0,7% против 3,5%; ОР 0,27 (от 0,08 до 0,95), 95% ДИ) и повысить субъективную (85% против 77%; ОР 1,1 (от 1,01 до 1,2), 95% ДИ) и объективную (92% против 87%; ОР 1,06, 95% ДИ 1,01– 1,11) эффективность [8].
Очередным шагом к повышению результативности и безопасности среднеуретрального слинга стала предложенная в 2001 г. трансобтураторная методика [9]. Она основывается на теории «вагинального гамака» De lancey, а проведение троакаров через обтураторные мембраны и обтураторные мышцы значительно снижает вероятность повреждения мочевого пузыря, кишечника и сосудов. Эффективность подхода составляет от 77,5-92,3% при этом количество осложнений стало минимальным [10]. Собственный опыт использования среднеуретральных слингов показал, что общая результативность методики может доходить до 97,798,3% [11]. Исполнение операции возможно в двух вариантах: изнутри наружу и в обратном порядке. Сравнение двух этих подходов показало их одинаковую эффективность, в тоже время опасность повреждения мочевого пузыря и развитие острой задержки мочи выше при продвижении троакара снаружи внутрь (ОР 0,17 (от 0,005 до 0,05), 95% ДИ и OР 0,49 (от 0,24 до 1,04), 95% ДИ) [12, 13].
При сравнении трансобтураторной и позадилонной методики среднеуретрального слинга их эффективность сопоставима, однако уровень развития осложнений у них различный (0,8–6,4% против 12,2– 13,8% соответственно, р< 0,03): перфорация мочевого пузыря (0,3% против 5,5%; ОР 0,14 (от 0,07 до 0,26), 95% ДИ), острая задержка мочи (0– 4% против 2,7–7%; ОР 0,63 (от 0,44 до 0,89), 95% ДИ), болевой синдром (9,4–12% против 1,7–4%, р = 0,01), перфорация влагалища (4,3% против 2,0%), повреждение уретры (0–2,5% против 0,1–5,5%), эрозий (4,7% против 3,5%, р < 0,05). В тоже время не выявлено статистически значимых различий в развитии ургентности de novo и качества жизни между двумя этими методиками [14, 15].
Стремление сохранить высокую эффективность среднеуретрального слинга и одновременно с этим снизить его травматичность привели к созданию вмешательств из одного разреза, так называемых «минислингов». Данные о результативности такого подхода очень разнятся. Так, эффективность применения TVT SECUR™ колеблется от 58% через 30 мес. [16] до 100% после 12– 18 мес. [17], а MiniArc® от 23,7% через 18,6±11,5 мес. [18], до 94% [19]. Что же касается сравнения различных систем «мини-слингов» то значимой разницы нет, их эффективность при двухлетнем наблюдении не превышает 65%, а риск быть вновь прооперированными достигал 32,5% [20]. M. Abdel-Fattah и соавт. опубликовали мета-анализ, оценивающий эффективность и безопасность стандартных среднеуретральных слингов и «мини-слингов» [21]. Объективная и субъективная эффективность последних оказалась значительно ниже, чем при стандартных методиках (ОР 0,83 (от 0,70 до 0,99), 95% ДИ и ОР 0,85 (от 0,74 до 0,97), 95% ДИ, ретроспективно), а уровень повторных вмешательств (ОР 6,72 (от 2,39 до 18,89), 95% ДИ) и развития ургентности de novo (ОР 2,08 (от 1,01 до 4,28), 95% ДИ) выше. Несмотря на низкий уровень осложнений, FDA запросил постмаркетинговые данные наблюдений от изготовителей, чтобы определиться с безопасностью и проблемами эффективности данного метода.
Все вышеописанное касалось классического стрессового недержания мочи. Однако существует микст тип, который включает в себя ургентность и стрессовое недержание. Проведённый P. Jain и соавт. метаанализ показал большую эффективность трансобтураторной методики по сравнению с позадилонной (ОР 0,9, 95% ДИ 0,63–1,27) в течение 6– 33 мес. Так же СНМ может быть связано с недостаточностью внутреннего сфинктера в дополнение к гипермобильности уретры, что является фактором риска неудачи среднеуретрального слинга [22]. C.W. Nager и соавт. оценили результаты применения пубовагинальных слингов, TVT™ и TOTs у пациентов с недостаточностью внутреннего сфинктера. Эффективность в течение двух лет составила 87,25%, 86,94% и 34,89% соответственно [23]. Данные результаты подтвердили и другие исследования [24, 25]. Еще одной сложной проблемой является рецидивное СНМ. Недавний мета-анализ, включающий в себя 11 проспективных когортных исследований, показал первичную эффективность среднеуретрального слинга 78,5% (95% ДИ 69– 88) в течение 30 мес., вторичную 73,3% (95% ДИ 55–97) в течение 16 мес. Гораздо менее результативным в таких случаях был трансобтураторный тип (33–67%), по сравнению с позадилонным (61–100%) [26].
Обобщение современных данных о результатах хирургического лечения СНМ отражено в мета-анализе библиотек Медлайн и Кохрейн с 1990г. по апрель 2013г., представленном на 39 Ежегодном научном съезде Ассоциации гинекологов США (Society of gynecologic surgeons – SGS) [27]. Сравнение кольпосуспензии по Burch и среднеуретральных слингов (10 рандомизированных исследований (РИ), включающих 1028 пациента со сроками наблюдения от 12 мес. до 5 лет) не выявило значимой разницы в их объективной (OР 1,18 (от 0,73 до 1,89), 95% ДИ) и субъективной (OР 1,12 (от 0,79 до 1,60), 95% ДИ) эффективности. Если говорить о риске развития гиперактивности мочевого пузыря, эрозий и подвергнуться повторному вмешательству, то он также был равным для обоих подходов. Анализ объективной и субъективной эффективности минии полноразмерных слингов (15 РИ, 1716 больных, медиана наблюдения 12-24 мес.) показал значимое превосходство последних (OР 4,16 (от 2,15 до 8,05), 95% ДИ и OР 2,65 (от 1,36 до 5,17), 95% ДИ соответственно). Что касается частоты осложнений, то для обеих методик она примерно одинакова.
ПРОТЕЗИРУЮЩАЯ РЕКОНСТРУКЦИЯ ТАЗОВОГО ДНА ПО ПОВОДУ ПТО
Передний компартмент. При центральном дефекте лобково-шеечной фасции (цистоцеле) стандартной операцией является передняя кольпорафия, при латеральном – реапроксимация влагалища к стенкам таза – паравагинальная реконструкция. При этом частота рецидивов у методик, использующих собственные ткани, доходит до 3060% [28]. Основываясь на опыте использования синтетических сеток в абдоминальной хирургии и успехах слинговых операций, в 2002 г. группа французских урогинекологов предложила трансвагинальную сетчатую реконструкцию (ТСР) при ПТО ≥3 ст. Так, эффективность использования наиболее популярной системы Prolift достигает 80,5 % в течение 3-х лет и 77 % в течение 5 лет, полная анатомическая коррекция наступает в 69 и 67% соответственно, серьезные осложнения возникли в 18% случаев, повторные операции потребовались 13,3% пациенткам [29, 30]. Применение облегченных сеток (Prolift+M) дает положительный результат в 85 – 87 % случаев, а анатомическая эффективность колеблется между 76 и 96%, эрозии возникали у 5,6-14,8% пациенток [31, 32]. Однако «mesh-хирургия» даже при применении легких протезов сопровождается повышением риска осложнений, количество которых зависит от опыта хирурга: развитие эрозий (4– 19%), перфораций мочевого пузыря (0,5-3,5%), хронической тазовой боли и пролапса/ургентности de novo [33, 34]. Наш опыт применения сетчатых имплантатов при пролапсе органов малого таза показал, что при соблюдении показаний к операции и методики ее исполнения, количество осложнений минимально, а эффективность находится на очень высоком уровне [35]. Представленные выше данные подтверждает и опубликованный в 2013 году анализ базы библиотеки Кохрейн [36]. Так, сравнение традиционной передней кольпорафии при цистоцеле с ТСР (10 РИ, 1056 больных) показало, что риск развития рецидива в несколько раз выше при пластике собственными тканями (ОР 3,83 (от 2,34 до 6,26) 95% ДИ). В тоже время частота развития таких осложнений как СНМ de novo (ОР 0,58 (от 0,36 до 0,94) 95% ДИ) и, естественно, эрозий слизистой влагалища (ОР 0,07 (от 0,03 до 0,18) 95% ДИ) была выше при использовании протезов (рис. 1).
Патология срединного или верхнего компартмента (утеровагинальный или постгистерэктомический пролапс).
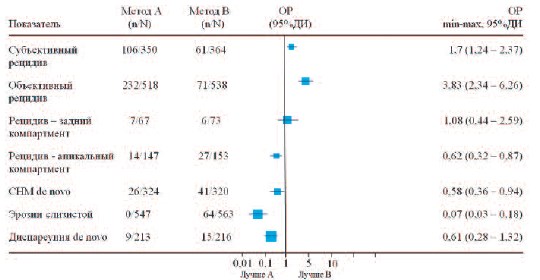
Рис.1. Сравнение передней кольпорафии (А) и трансвагинальной сетчатой реконструкции (В)
n – пациенты с наличием показателя, Nобщее число пациентов
Золотым стандартом лечения апикального пролапса является трансабдоминальная сакрокольпопексия (ТСК) с использованием сетчатого имплантата, фиксируемого к продольным связкам крестца. Согласно исследованиям результативность метода достигает 78-100%, при этом вероятность рецидива не превышает 6%, а частота имплантатассоциированных эрозий колеблется от 0 до 12% [37, 38]. Главными недостатками такого подхода является большая длительность операции (265 минут для роботизированной и 199 минут для лапароскопической ТСР), длительный период послеоперационной реабилитации (3-4 недели) и высокая стоимость (3205 – 16278 долл. США) [39]. Кроме того, в долгосрочной перспективе по разным данным около 8-15% прооперированных пациенток возвращались к хирургическому лечению [40, 41]. Особое место занимает постгистерэктомический пролапс. Традиционным методом его лечения является трансвагинальный подход: сакроспинальная фиксация и McCall/Mayo кульдопластика. Уровень рецидива после пластики собственными тканями составляет 3–10 % [42]. В 1997 году P. Petros предложил оригинальный подход в лечении пролапса свода влагалища – заднюю интравагинальную слингпластику, обеспечивающую анатомическое восстановление первого уровня вагинальной поддержки (крестцово-маточных связок). В дальнейшем этот метод нашел свое применение и в случае сохранения матки. Результативность данной методики с медианой наблюдения более 9 лет достигает 93,8 – 96,6%, а частота эрозий не превышает 2,27 – 8,5% [43, 44]. Приведенные выше данные нашли свое отражение и в анализе библиотеки Кохрейн от 2013г. Сравнение стандартной сакроспинальной кольпопексии с задней интравагинальной слингпластикой (2 РИ, 111 пациенток) не выявило значимых различий ни по эффективности (ОР 0,31 (от 0,3 до 2,91) 95% ДИ), ни по частоте развития побочных эффектов (ОР 0,73 (от 0,29 до 1,82) 95% ДИ). В тоже время необходимо отметить, что риск развития пролапса в непрооперированном компартменте несколько выше в случае выполнения сакрокольпопексии (ОР 1,65 (от 0,83 до 3,27) 95% ДИ) (рис. 2).
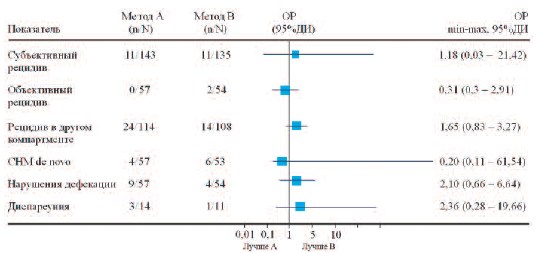
Рис.2. Сравнение сакрокольпопексии (в том числе лапароскопической и роботизированной) (А) и
трансвагинальной сетчатой реконструкции (В)
n – пациенты с наличием показателя, N общее число пациентов
Задний компартмент. Наиболее популярная операция при дефекте задней стенки влагалища – трансвагинальная задняя кольпорафия, которая дает хорошие анатомические результаты (85-95%) и значительно улучшает качество жизни пациентов [45]. Использование имплантатов не улучшает анатомические результаты, но увеличивает риск осложнений и целесообразно лишь при одновременном выполнении и апикальной поддержки [46]. В случае такого подхода эффективность доходит до 92%, с хорошими функциональными результатами, при этом эрозии возникли в 6,5 % случаев [47]. Анализ базы библиотеки Кохрейн, основанный на 3 РИ, включавших 323 пациенток, так же не выявил значимых преимуществ протезирующей хирургии перед классической кольпорафией (ОР 1,11 (от 0,4 до 3,19) 95% ДИ) (рис. 3).
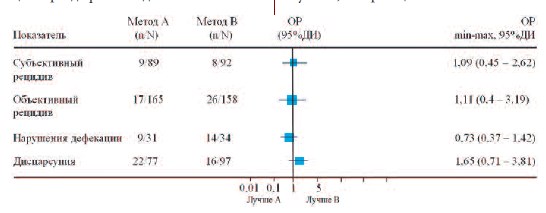
Рис.3. Сравнение задней кольпорафии (А) и протезирующей реконструкции заднего компартмента (В)
n – пациенты с наличием показателя, Nобщее число пациентов
Современная протезирующая хирургия не стоит на месте – очередным шагом стало появление имплантатов для установки из одного разреза – SIMS (single-incision mesh system). Принципиальным отличием этих систем является крепление сетки с помощью специальных фиксирующих элементов – «якорей» к наиболее прочным сакроспинальным связкам и отсутствие необходимости проводить троакары через ткани таза. Так, объективная эффективность применения системы Elevate™ в течение года при пластике переднего компартмента составляет от 88 % до 92 %, апикального – от 89% до 96%, заднего до 93% [47, 48]. При сравнении использования систем SIMS с традиционной пластикой (210 пациентов, срок наблюдения 1 год) анатомическая эффективность для переднего компартмента составила 98% против 87% (p=0,006), для апикального – 99% против 96% (p=0,317), а для заднего – 100% против 97% (p=0,367) [49]. При данном подходе удается минимизировать уровень серьезных осложнений (перфорация органов, кровотечение), в приведенном выше исследовании лишь в 3% наблюдений возникли эрозии слизистой, в 4% – боли в ягодичной области (оба осложнения были разрешены консервативно).
Открытым остается вопрос о надежности и точности установки самофиксирующих элементов. Так, недавнее исследование показало, что лишь 10 из 20 «якорей» системы Elevate были проведены сквозь сакроспинальные связки, что привело к их миграции в каудальном и краниальном направлении более чем на 4 мм. Однако, что интересно, это не сказалось на эффективности лечения [50].
Исходя из всего выше сказанного, возникает законный вопрос: что же является показанием к использованию в реконструктивной хирургии синтетических материалов? Консенсус был достигнут на 2-ом Круглом столе по оптимизации протезирующей хирургии тазового пролапса под эгидой Международной ассоциации урогинекологов (International Urogynecological Association – IUGA) [51]. Итогом проведенных консультаций стала выработка рекомендаций по использованию сеток. Значимая польза имеется при сочетании следующих факторов риска: цистоцеле > второй стадии или рецидива ПТО (кроме заднего компартмента) в дополнении с наличием высокого интраабдоминального давления или слабости соединительной ткани или же при вовлечении в процесс апекса/ шейки/купола влагалища. Вероятная польза от протезирующей хирургии возможна при возрасте пациентки более 50 лет, рецидиве ПТО (в том же отделе), цистоцеле > второй стадии, при задействовании апекса/шейки/купола влагалища, хроническом высоком внутрибрюшном давлении, слабости соединительной ткани, рецидиве ПТО в сочетании с ректоцеле. Польза сомнительна – при возрасте пациентки менее 50 лет, пролапсе задней стенки влагалища. Использовать сетчатые имплантаты нежелательно при цистоцеле < второй стадии, наличии болевого синдрома (локальный/системный), планируемой беременности.
ВЫВОДЫ
Таким образом, при неосложненном стрессовом недержании мочи большинство авторов на сегодняшний день рекомендуют использовать полноразмерные среднеуретральные слинги, указывая на недостаточную эффективность минислингов. При наличии ургентности лучше применять трансобтураторный, а при недостаточности внутреннего сфинктера уретры – позадилонный среднеуретральный слинг.
Современные данные, полученные в результате анализа многоцентровых исследований, указывают на очевидную целесообразность применения синтетических эндопротезов в хирургическом лечении пролапса в переднем компартменте тазового дна (выраженные формы цистоцеле), т.к. это снижает риск рецидива более, чем в 3 раза по сравнению с традиционными методиками. Имеющиеся данные указывают также на умеренные преимущества протезирующей пластики тазового дна в среднем компартменте (апикальный пролапс в следствие дефекта крестцово-маточных связок). В то же время, на сегодняшний день нельзя рекомендовать применение сетчатых имплантатов в реконструкции заднего компартмента (ректоцеле), так как эффективность этого подхода не обеспечивает преимуществ по сравнению с традиционными методиками. Необходимо также учитывать, что применение сетчатых материалов требует специальных знаний и навыков от хирургов для минимизации риска «имплант-ассоциированных» осложнений. Наибольшие преимущества протезирующая реконструкция тазового дна обеспечивает у пациенток с выраженными формами пролапса и высоким риском рецидива.
ЛИТЕРАТУРА
- Адамян Л.В., Блинова М.А., Сашин Б.Е. Современные концепции хирургического лечения опущения и выпадения женских половых органов. // Материалы международного Конгресса «Эндоскопия в диагностике, лечении и мониторинге женских болезней». М. 2000. С. 622 – 635.
- Кулаков В.И., Адамян Л.В., Мынбаев О.А. Хирургическое лечение опущения и выпадения влагалища и матки. // Оперативная гинекология – хирургичеcкие энергии. М. 2000. С. 741 – 760.
- Пушкарь Д.Ю. Диагностика и лечение сложных и комбинированных форм недержания мочи у женщин: Автореф. дисс. ... д-ра мед. наук. М., 1996. 53 с.
- Wu JM, Matthews CA, Conover MM, Pate V, Jonsson FM. Lifetime risk of stress uri-nary incontinence or pelvic organ prolapse surgery. // Obstet Gynecol. 2014. Vol. 123. N. 6. P. 1201 – 1206.
- Jonsson FM, Edenfield AL, Pate V, Visco AG, Weidner AC, Wu JM, Jonsson FM. Trends in use of surgical mesh for pelvic organ prolapse. // Am J Obstet Gynecol. 2013. Vol. 208. N. 1. P. 79. e1–7.
- Farrell SC. Thr Sub-committee on Urogynaecology of the Society of Obstetricians and Gynaecologists of Canada. Tension-free vaginal tape (TVT) Procedure. SOGC Technical Update No. 132, August 2003. // J Obstet Gynaecol Can. 2003. Vol. 25. N. 8. P. 692 – 694.
- Ulmsten U, Petros P. Intravaginal slingplasty (IVS): an ambulatory surgical procedure for treatment of female urinary incontinence. // Scand. J. Urol. Nephrol. 1995. Vol. 29. P. 75 – 82.
- Ogah J, Cody JD, Rogerson L. Minimally invasive synthetic suburethral sling operations for stress urinary incontinence in women. // Cochrane Database Syst Rev. 2009. Vol. 7. N. 4. CD006375.
- Delorme E. Transobturator urethral suspension: mini-invasive procedure in the treatment of stress urinary incontinence in women. // Prog. Urol. 2001. Vol. 11. P. 1306 – 1313.
- Waltregny D, de Leval J. The TVT-obturator surgical procedure for the treatment of female stress urinary incontinence: a clinical update. // Int. Urogynecol. J. Pelvic Floor Dysfunct. 2009. Vol. 20. P. 337 – 348.
- Шкарупа Д.Д., Кубин Н.Д. Малоинвазивная хирургия стрессового недержания мочи у женщин: 5-ти летний опыт использования протеза Урослинг. // Вестник Санкт-Петербургского университета Серия 11. Медицина. 2014. Вып. 1. С. 186 – 192.
- Novara G, Artibani W, Barber MD, Chapple CR, Costantini E, Ficarra V, Hilton P, Nilsson CG, Waltregny D. Updated systematic review and meta-analysis of the com-parative data on colposuspensions, pubovaginal slings, and midurethral tapes in the surgical treatment of female stress urinary incontinence. // Eur. Urol. 2010. Vol. 58. P. 218 – 238.
- Latthe PM, Singh P., Foon R, Toozs-Hobson P. Two routes of transobturator tape procedures in stress urinary incontinence: a meta-analysis with direct and indirect com-parison of randomized trials. // BJU Int. 2010. Vol. 106. P. 68 – 76.
- Long CY, Hsu CS, Wu MP, Liu CM, Wang TN, Tsai EM. Comparison of tension-free vaginal tape and transobturator tape procedure for the treatment of stress urinary in-continence. // Curr. Opin. Obstet. Gynecol. 2009. Vol. 21. P. 342 – 347.
- Laurikainen E, Valpas A, Aukee P, Kivelä A, Rinne K, Takala T, Nilsson GG. Five-year Results of a Randomized Trial Comparing Retropubic and Transobturator Midurethral Slings for Stress Incontinence. // Eur Urol. 2014. Vol. 65. N. 6. P. 1109 – 1114.
- Cornu JN, Sèbe P, Peyrat L, Ciofu C, Cussenot O, Haab F. Midterm prospective evaluation of TVT-Secur reveals high failure rate. // Eur. Urol. 2010. Vol. 58. P. 157 – 161.
- Tartaglia E, Delicato G, Baffigo G, Signore S, Corvese F, Perla A, Ferdinandi V. Theirdgeneration tension-free tape for female stress urinary incontinence. // J. Urol. 2009. Vol. 182. P. 612 – 615.
- Madsen AM, El-Nashar SA, Woelk JL, Klingele CJ, Gebhart JB, Trabuco EC. A co-hort study comparing a single-incision sling with a retropubic midurethral sling. // Int Urogynecol J. 2014. Vol. 25. N. 3. P. 351-358.
- Oliveira R, Resende A, Silva C, Dinis P, Cruz F. Mini-arc for the treatment of female stress urinary incontinence: long-term prospective evaluation by patient reported outcomes. // ISRN Urol. 2014. doi: 10.1155/2014/659383.
- Palomba S, Falbo A, Oppedisano R, Torella M, Materazzo C, Maiorana A, Tolino A, Mastrantonio P, La Sala GB, Alio L, Colacurci N, Zullo F. The SIMS Italian Group.A randomized controlled trial comparing three single-incision minislings for stress uri-nary incontinence. // Int Urogynecol J. 2014. Vol. 25. N. 10. P. 1333-1341.
- Abdel-Fattah M, Ford JA, Lim CP, Madhuvrata P. Single-incision mini-slings versus standard midurethral slings in surgical management of female stress urinary inconti-nence: a meta-analysis of effectiveness and complications. // Eur. Urol. 2011. Vol. 60. P. 468 – 480.
- Jain P, Jirschele K, Botros SM, Latthe PM. Effectiveness of midurethral slings in mixed urinary incontinence: a systematic review and meta-analysis. // Int. Urogynecol. J. 2011. Vol. 22. P. 923 – 932.
- Nager CW, Sirls L, Litman HJ, Richter H, Nygaard I, Chai T, Kraus S, Zyczynski H, Kenton K, Huang L, Kusek J. Baseline urodynamic predictors of treatment failure 1 year after mid urethral sling surgery. // J. Urol. 2011. Vol. 186. P. 597 – 603.
- Schierlitz L, Dwyer PL, Rosamilia A, Murray C, Thomas E, De Souza A, Lim YN, Hiscock R. Effectiveness of tension-free vaginal tape compared with transobturator tape in women with stress urinary incontinence and intrinsic sphincter deficiency: a randomized controlled trial. // Obstet. Gynecol. 2008. Vol. 112. P. 1253 – 1261.
- Rechberger T, Futyma K, Jankiewicz K, Adamiak A, Skorupski P. The clinical effec-tiveness of retropubic (IVS02) and transobturator (IVS04) midurethral slings: random-ized trial. // Eur. Urol. 2009. Vol. 56. P. 24 – 30.
- Pradhan A, Jain P, Latthe PM. Effectiveness of midurethral slings in recurrent stress urinary incontinence: a systematic review and meta-analysis. // Int. Urogynecol. J. 2012. Vol. 23. P. 831 – 841.
- Schimpf MO, Rahn DD, Wheeler TL, Patel M, White AB, Orejuela FJ, El-Nashar SA, Margulies RU, Gleason JL, Aschkenazi SO, Mamik MM, Ward RM, Balk EM, Sung VW. Society of Gynecologic Surgeons Systematic Review Group. Sling surgery for stress urinary incontinence in women: a systematic review and metaanalysis. // Am J Obstet Gynecol. 2014. – doi: 10.1016/j.ajog.2014.01.030.
- Maher CF, Baessler K. Surgical management of anterior vaginal wall prolapse: an ev-idence based literature review. // Int Urogynecol J Pelvic Floor Dysfunct. 2006. Vol. 17. P. 195 – 201.
- Jacquetin B, Fatton B, Rosenthal C, Clavé H, Debodinance P, Hinoul P, Gauld J, Garbin O, Berrocal J, Villet R, Salet Lizée D, Cosson M. Total transvaginal mesh (TVM) technique for treatment of pelvic organ prolapse: a 3 year prospective fol-lowup study. // Int Urogynecol J. 2010. Vol. 21. N. 12. P. 1455 – 1462.
- Miller D, Lucente V, Babin E, Beach P, Jones P, Robinson D. Prospective clinical as-sessment of the transvaginal mesh technique for treatment of pelvic organ prolapse 5-year results. // Female Pelvic Med Reconstr Surg. 2011. Vol. 17. P. 139 – 143.
- Milani AL, Hinoul P, Gauld J. Medium term clinical outcomes following trocar guided mesh repair of vaginal prolapse using partially absorbable mesh. // 37th IUGA An-nual Meeting. 2012. Abstract 81.
- Stanford EJ, Moore RD, Roovers JP. A prospective multi-center clinical trial evaluating Elevate Anterior and Apical in the treatment of pelvic organ prolapse: two year followup. // 37th IUGA Annual Meeting. 2012. Abstracts 42, 83.
- Mourtialon P, Letouzey V, Eglin G, de Tayrac R, French Ugytex Study Group. Cystocele repair by vaginal route: comparison of three different surgical techniques of mesh placement. // Int Urogynecol J. 2012. Vol. 23. P. 699 – 706.
- Sokol AI, Iglesia CB, Kudish BI, Gutman RE, Shveiky D, Bercik R, Sokol ER. One-year objective and functional outcomes of a randomized clinical trial of vaginal mesh for prolapse. // Am J Obstet Gynecol. 2012. Vol. 206. N. 1. P. 86.e1– 86.e9.
- Кубин Н.Д., Шкарупа Д.Д. Хирургическое лечение тазового пролапса – 2-х летний опыт применения синтетических сетчатых эндопротезов сверхлегкой конструкции. // Вестник Санкт-Петербургского университета Серия 11. Медицина. 2014. Вып. 1. С. 201 – 206.
- Maher CC, Feiner B, Baessler K, Schmid C. Surgical management of pelvic organ prolapse in women (Review). // Cochrane Database Syst Rev. 2013 Apr 30;4:CD004014. doi: 10.1002/14651858.CD004014.pub5.
- Jia X, Glazener C, Mowat G, Jenkinson D, Fraser C, Bain C, Burr J. Systematic re-view of the efficacy and safety of using mesh in surgery for uterine or vaginal vault prolapse. // Int Urogynecol J. 2010. Vol. 21. P. 1413 – 1431.
- Nygaard I, Brubaker L, Zyczynski HM, Cundiff G, Richter H, Gantz M, Fine P, Menefee S, Ridgeway B, Visco A, Warren LK, Zhang M, Meikle S. Long-term outcomes following abdominal sacrocolpopexy for pelvic organ prolapse. // JAMA. 2013. Vol. 309. N. 19. P. 2016–2024.
- Siddiqui NY, Edenfield AL. Clinical challenges in the management of vaginal pro-lapse. // Int J Womens Health. 2014. Vol. 6. P. 83 – 94.
- Salvatore S, Athanasiou S, Digesu GA, Soligo M, Sotiropoulou M, Serati M, Antsak-lis A, Milani R. Identification of risk factors for genital prolapse recurrence. // Neu-rourol Urodyn. 2009. Vol. 28. N. 4. P. 301 – 304.
- Dällenbach P, Jungo Nancoz C, Eperon I, Dubuisson JB, Boulvain M. Incidence and risk factors for reoperation of surgically treated pelvic organ prolapse. // Int Uro-gynecol J. 2012. Vol. 23. N. 1. P. 35 – 41.
- Klauschie JL, Cornella JL. Surgical treatment of vaginal vault prolapse: a historic summary and review of outcomes. // Female Pelvic Med Reconstr Surg. 2012. Vol. 18. N. 1. P. 10 – 17.
- Cosma, S. Preti M, Mitidieri M, Petruzzelli P, Possavino F, Menato G. Posterior in-travaginal slingplasty: efficacy and complications in a continuous series of 118 cases. // Int Urogynecol J. 2011. Vol. 22. N. 5. P. 611 – 619.
- Capobianco G, Donolo E, Wenger JM, Madonia M, Cosmi E, Antimi L, Dessole M, Cherchi PL. Efficacy and 9 years' follow-up of posterior intravaginal slingplasty for genital prolapse. // J Obstet Gynaecol Res. 2014. Vol. 40. N. 1. P. 219–223.
- Grimes CL, Tan-Kim J, Whitcomb EL, Lukacz ES, Menefee SA. Long-term outcomes after native tissue vs. biological graft augmented repair in the posterior compartment. // Int Urogynecol J. 2012. Vol. 23. P. 597 – 604.
- Kudish BI, Iglesia CB. Posterior wall prolapse and repair. // Clin Obstet Gynecol. 2010. Vol. 53. P. 59 – 71.
- Lukban JC, Roovers JP, VanDrie DM, Erickson T, Zylstra S, Patel MP, Moore RD. Singleincision apical and posterior mesh repair: 1-year prospective outcomes. // Int Urogynecol J. 2012. Vol. 23. P. 1413 – 1419.
- Stanford EJ, Moore RD, Roovers JP, Courtieu C, Lukban JC, Bataller E, Liedl B, Sutherland SE. Elevate anterior/apical: 12-month data showing safety and efficacy in surgical treatment of pelvic organ prolapse. // Female Pelvic Med Reconstr Surg. 2013. Vol. 19. N. 2. P. 79–83.
- Su TH, Lau HH, Huang WC, Hsieh CH, Chang RC, Su CH. Single-incision mesh repair versus traditional native tissue repair for pelvic organ prolapse: results of a cohort study. // Int Urogynecol J. 2014. DOI. 10.1007/s00192-013-2294-5.
- Brennand EA, Bhayana D, Tang S, Birch C, Murphy M, Cenaiko D, Ross S, Robert M. Anchor placement and subsequent movement in a mesh kit with self-fixating tips: 6-month follow-up of a prospective cohort. // BJOG. 2014. Vol. 121. N. 5. P. 634 – 640.
- Davila GW, Baessler K, Cosson M, Cardozo L. Selection of patients in whom vaginal graft use may be appropriate. Consensus of the 2nd IUGA Grafts Roundtable: opti-mizing safety and appropriateness of graft use in transvaginal pelvic reconstructive surgery. // International Urogynecology Journal. 2012. Vol.23. s.1. S7–S14.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 382.85 кб |















































































