Лечение сочетанного стеноза лоханочно-мочеточникового сегмента (ЛМС) и протяженной гипоплазии мочеточника не является повседневной задачей детского уролога, но имеет большое значение и чрезвычайно востребовано в детской урологии. Немногочисленные литературные публикации, в частности Allen TD. с соавт. [1, 2] подтверждают большое количество осложнений и необходимость выполнения нефрэктомий при неадекватном лечении этого сочетанного порока развития мочевыделительной системы.
Аномалии ЛМС развиваются в результате эмбриопатогенетических нарушений в эпителиальной мембране и в процессе реканализации мочеточника. Также к причинам их возникновения относят фиброз фетальной уретральной складки, ишемию мочеточника, нейромышечную дисплазию мочеточника, обструктивные эмбриональные уретральные пороки [3].
Пороки мочеполовой системы, возникающие на ранних стадиях развития эмбриона, приводят к выраженной почечной дисплазии и полному гломерулосклерозу, что изначально ограничивает все возможности лечения. Обструктивные уропатии, возникшие в более поздние сроки, преимущественно приводят к развитию гидронефротической трансформации с сегментарным нарушением функции почечных клубочков. В этом случае существуют определенные возможности оперативной коррекции порока.
Большое значение для выбора метода лечения указанной аномалии ЛМС имеют результаты гистологического исследования, в особенности, с точки зрения потенциальной способности созревания гипоплазированных сегментов мочеточника. При гистологическом исследовании пораженного мочеточника отмечается узость его просвета с частичной тонкостенностью, дефекты эпителия, уменьшенное межклеточное пространство с коллагеновой диссоциацией мышечных клеток, а также выраженное уменьшение количества внутриклеточных энергоносителей, в особенности в пиноцитарных пузырьках и гликогеновых гранулах. Как известно из ранее проведенных исследований относительно повторной резекции мочеточника после уретерокутеонестомии, функциональное восстановление мочеточника обусловлено способностью к стабилизации имеющегося синтиция. Подобные компенсаторные механизмы могут обеспечить успешность оперативной реконструкции гипоплазированного мочеточника без необходимости его замены [4-6].
РОЛЬ СТЕНТА С DD-ЗАМКОМ У ПАЦИЕНТОВ С КОМБИНИРОВАННЫМИ АНОМАЛИЯМИ ЛМС
Одним из методов лечения комбинированных аномалий ЛМС, в ряде случаев приводящих к улучшению функционального состояния мочеточника, является его продолжительное стентирование, обеспечивающее разгрузку почки на длительное время. На сегодняшний день доказано, что применение традиционных (внешних) стентов [2] сопровождается большим количеством осложнений инфекционного характера, низкой эффективностью в отношении восстановления функции мочеточника, высоким риском инкрустации стента, а также возможностью развития пузырномочеточникового рефлюкса. Вышеуказанных осложнений можно избежать при применении JJ-стента с DD-замком (рис.1) [7-9]. Этот полиуретановый мочеточниковый катетер - стент имеет на пузырном конце мембранный клапан из мягкого вирутана, который автоматически закрывается при повышении давления в пузыре. После установки он предотвращает обратный заброс мочи из мочеточника в почечную лоханку. Дополнительный широкий клапан предотвращает миграцию пузырного конца стента и обеспечивает надежность местоположения катетера в мочеточнике. Благодаря простоте применения этого стента он уже использовался в клинической практике для решения проблем, связанных с суправезикальным нарушением оттока мочи. Экспериментальные и клинические результаты показали, что антирефлюксный мочеточниковый JJ-стент с DD-замком позволяет обеспечить адекватный отток мочи из почечной лоханки. Клапан не нарушает тока мочи, поскольку отток обеспечивается не только через отверстия стента, но и паралюминально [5, 10]. В работах Hanna MK с соавт. [6] и Mortensen J. [11], а также в собственных исследованиях [2, 5, 9, 12, 13] было показано, что длительное стентирование мочеточника усиливает его перистальтическую активность при снижении давления в лоханке.
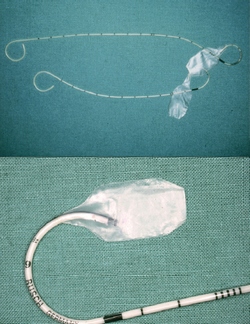
Рис. 1. JJ-стент с DD-замком.
РЕЗУЛЬТАТЫ ОПЕРАТИВНОГО ЛЕЧЕНИЯ
С 1994 по 1998 гг. наблюдалось 146 детей с обструкцией ЛМС, 130 из которых были прооперированы по методу Хайнс-Андерсона. У 57 (38%) пациентов наряду с комбинированной стриктурой ЛМС и гипоплазией мочеточника выявлены другие аномалии мочевыводящих путей, при этом у 7 детей (4,3%) в возрасте от 3 недель до 13 лет, имела место сегментарная гипоплазия мочеточника большой протяжности с нормальной или частично сохраненной функцией почки (табл. 1). Всем больным до операции первым этапом была выполнена нефростомия для восстановления оттока мочи.
Таблица 1. Сочетанные пороки развития мочевыводящих путей у детей с обструкцией ЛМС
| Вид порока | Число больных |
| Уретральный клапан YOUNG 1 | 15 |
| Стеноз устья мочеточника | 13 |
| Пузырно-мочеточниковый рефлюкс | 7 (1 двусторонний) |
| Сегментарная гипоплазия мочеточника большой протяжности | 7 |
| Подковообразная почка | 5 |
| Аномалии взаиморасположения почек | 3 |
| Уретроцеле | 2 |
| Единственная почка | 1 |
| Почечная дисплазия | 1 |
| Всего: | 57 |
После этого проводилось полное обследование, включающее антероградную и ретроградную пиелоуретерографию, микционную цистографию, радиоизотопную ренографию и эндоскопическое исследование.
Ниже приведены клинические случаи применения JJ-стента с DD- замком.
Клинический случай 1
Девочка трех месяцев с двусторонней обструкцией ЛМС и установленными перкутанными нефростомами с обеих сторон поступила для выполнения оперативного лечения в объеме пластики ЛМС по Хайнс-Андерсену с двух сторон. Интраоперационно справа выявлена гипоплазия дистального отдела мочеточника и рубцовое изменение почечной лоханки, в связи с чем наложение пиелоуретерального анастомоза оказалось невозможным (рис. 2). Установлен мочеточниковый стент справа. Слева выполнен пиелоуретеральный анастомоз. Через 10 дней выполнено повторное оперативное вмешательство справа - резекция измененного дистального отдела мочеточника с установкой стента 4Ch с DD-замком. Через 6 месяцев стент удален. По данным статической нефросцинтиграфии функция справа через 6 месяцев составила 63%, слева 37%. В течение 3 лет состояние ребенка без отрицательной динамики.
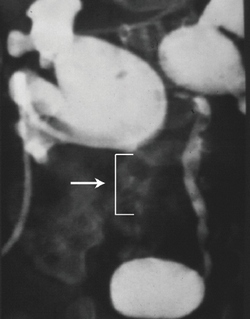
Рис. 2. Антеградная пиелоуретерография с двух сторон: стрелкой указан участок гипоплазированного мочеточника справа (клинический случай 1).
Клинический случай 2
Девочка 13 лет поступила с жалобами на боли в поясничной области слева. При обследовании выявлен нарушение оттока мочи из левой почки, в связи с чем была выполнена нефростомия и назначена антибактериальная терапия. При антеградной пиелоуретерографии выявлена обструкция ЛМС, стеноз устья мочеточника и сегментарная гипоплазия дистального отдела мочеточника на большом протяжении (рис.3). Выполнена пластика ЛМС по Хайнс-Андерсену с установкой мочеточникового стента 3Ch с DD- замком. Затем при стабильных уродинамических показателях произведена замена стента на больший по диаметру (4,8 Ch). После 8-недельного стационарного лечения нефростома удалена, стент заменен на 6Ch, который еще через 3 месяца заменили на 7Ch. При установке стента выполнена его фиксация в мочевом пузыре для предотвращения миграции. Стент был оставлен на 12 месяцев. По данным реносцинтиграфии функция слева составляла 47%, справа 53%. После удаления стента ребенок находится под постоянным наблюдением, жалоб нет
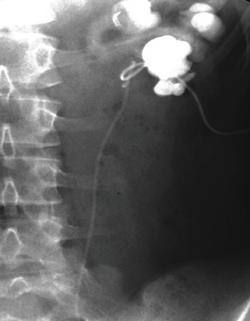
Рис. 3. Антеградная пиелоуретерография слева: обструкция ЛМС, мочеточниковый стент с DD-замком (клинический случай 2).
Клинический случай 3
Девочка 7 лет после падения с горки была госпитализирована для стационарного лечения с ушибом поясничного отдела позвоночника. Во время проведения УЗИ брюшной полости был выявлена гидронефротическая трансформация справа. По данным ретроградной уретеропиелографии справа выявлена стриктура ЛМС справа и сужение н/3 правого мочеточника (рис. 4). Исходно функция правой почки составляла 27% от суммарной функции обеих почек. Пациентке выполнена пластика ЛМС по Хайнс-Андерсону. Учитывая выраженное сужение дистального отдела мочеточника произведена установка мочеточникового стента 3Ch с DD-замком, который через 5 месяцев был заменен на стент 4Ch. Через 6 месяцев функция почки справа составляла 43% без нарушения оттока мочи. Через 5 лет после операции, состояние ребенка удовлетворительное, жалоб нет.
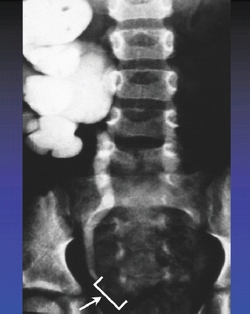
Рис. 4. Ретроградная уретеропиелография справа – стриктура ЛМС справа, сужение нижней трети правого мочеточника (клинический случай 3).
Клинический случай 4
Мальчик 11 лет поступил с диагнозом: подковообразная почка, гидронефртическая трансформация слева. При УЗ-исследовании органов брюшной полости выявлен пиеловазальный конфликт слева. Данных за инфекцию мочевых путей не выявлено. Пациенту была выполнена пластика ЛМС с установкой нефростомы. Интраоперационно выявлена гипоплазия дистального отдела мочеточника на протяжении 10 см. Выполнено длительное стентирование с помощью мочеточникового стента 3Ch с DD-замком в течение 21 месяца. Функция почки через 21 месяц составляет 21%. В отдаленном периоде пациент жалоб не предъявляет.
ОБСУЖДЕНИЕ
Сочетание обструкции ЛМС и сегментарной гипоплазии мочеточника представляет собой наиболее сложную проблему как в отношении лечения, так и в отношении отдаленных результатов [14-16]. Очень часто больным данной категории выполняется нефрэктомия [1, 2]. У всех детей с данной сочетанной аномалией развития мочевыводящих путей отмечается выраженное нарушение оттока мочи из почки, что требует выполнения нефростомии. В план обследования должна включаться не только антеградная пиелоуретрография, но и ретроградная уретерография для исключения гипоплазии дистального отдела мочеточника. Наряду с пластикой ЛМС по Хайнс-Андерсену [17] данной группе пациентов показано выполнение антирефлюкского стентирования мочеточника на длительный срок с помощью мочеточниковых стентов разных типов. В настоящее время неудачи лечения данной аномалии развития связаны с отсутствием у ряда стентов антирефлюксной защиты. Использование стента с DD-замком, предотвращающего возникновение ПМР, позволяет понизить давление в почечной лоханке, постепенно восстановить пейсмекерную функцию пиелоуретрального сегмента и дренировать мочевые пути сроком до двух лет. Для пациентов младенческого возраста можно применять стенты 3- или 4-Ch, до 6-ти лет - 4,8-Ch стент и после 6-лет - 6-Ch и 7-Ch стенты. Первым этапом пациентам выполняется нефростомия для нормализации давления в почечной лоханке. В последующем оценивается функция почек и состояние мочеточника.
Сроки удаления стента определяются восстановлением функции почек и мочеточника [18, 19]. В сложных случаях необходимо выполнение эндоскопических контрольных исследований. Для предотвращения инкрустации стента и возникновения инфекционно-воспалительных осложнений необходимо адекватное санирование верхних мочевых путей, профилактика повторных инфекции и прием большого количество жидкости. Если не наблюдается улучшения функции почки и мочеточника у пациентов данной группы, необходимо выполнить аутотрансплантацию почки [20-23] не позднее чем через 2 года от момента диагностирования заболевания.
В целом, представленные результаты лечения этого тяжелого комбинированного порока развития мочеполовой системы позволяют говорить о высокой эффективности применения антирефлюксного стентирования мочеточника в течение длительного срока.
Ключевые слова: стеноз лоханочно-мочеточникового сегмента, сегментарная гпоплазия мочеточника, пластика лоханочно-мочеточникового сегммента, антирефлюксное пиелоуретеральное стентирование, JJ-стент с DD-замком.
Keywords: ureteropelvic junction obstruction, segmental ureteral hypoplasia, plastic ureteropelvic junction, antireflux ureteropelvic stenting, JJ-stent with DD-lock.
ЛИТЕРАТУРА
- Allen TD. Congenital ureteral stricture. // J Urol. 1970. Vol. 104, N 1. P. 196-204
- Allen TD. Husmann DA. Ureteropelvic junction obstruction associated with ureteral hypoplasia. // J Urol. 1989. Vol. 142, N 2, Pt. 1. P. 353-355
- Alcaraz A, Vinaixa F, Tejedo-Mateau A, Fores MM, Gotzens V, Mestres CA, Oliveira J, Carretero P. Obstruction and recanalization of the ureter during embryonic development. // J Urol. 1991. Vol. 145, N 2. P. 410-416
- Friedrich U, Schreiber D, Gottschalk E, Dietz W. Ultrastruktur des distalen ureters bei kongenitalen Malformationen im Kindesalter. // Z Kinderchir. 1987. Vol. 42, N 2. P. 94-102
- Friedrich U, Vetter R, Jorgensen TM, Muhr M. Experimental and clinical experience with new pyeloureteral stents in pediatric urology. // J Endourol. 1997. Vol. 11, N 6. P. 431-439
- Hanna MK, Jeffs RD, Sturgess JM, Barkin M. Ureteral structure and ultrastructure. Part II. Congenital ureteropelvic junction obstruction and primary obstructive megaureter. // J Urol. 1976. Vol. 116, N 6. P. 725-730
- Ahmadzadeh M. Flap valve ureteral sent with an antireflux function: a review of 46 cases. // Urol Int. 1992. Vol. 48, N 4. P. 466-468
- Finney RP. Double-J and diversion stents.// Urol Clin North Am. 1982. Vol. 9, N 1. P. 89-94
- Friedrich U, Vetter R. Der antirefluxive Ventil-DD-Ureterstent im Kindesalter. // Sonderheft Rusch-Direkt. 1999. P. 1-15
- Yamaguchi O, Yoshimura Y, Irisawa C, Shiraiwa Y. Prototype of a reflux-preventing ureteral sent and its clinical use.// Urology. 1992. Vol. 40, N 4. P. 326-329
- Mortensen J. Hydrodynamics of the pyeloureter of the pig. // Neurourol Urodyn. 1986. Vol. 5. P. 87-117
- Friedrich U, Vetter R. Use of pyeloureteral DD stents in children. / In: Yachia D (Ed). Stenting the urinary system. Isis Medical Media Ltd, Oxford 1998; 141-149
- Ransley PG. Dhillon HK, Gordon I, Duffy PG, Dillon MB, Baratt TM. The postnatal management of hydronephrosis diagnosed by prenatal ultrasound. // J Urol. 1990. Vol. 144, N 2, Pt.2. P. 584-587
- Djurhuus JC, Nerstrom B, Hansen RI, Gyrd-Hansen N, Rask-Andersen H. Dynamics of the upper urinary tract. I. An electrophysiologic in vivo study of renal pelvis in pigs: method and normal pattern. // Invest Urol. 1977. Vol. 14, N 6. P. 465-468, 475477
- Gosling JA, Dixon JS. Funcional obstruction of the ureter and renal pelvis.// Brit J Urol. 1978. Vol. 50, N 3. P. 145-152
- Gosling JA, Dixon JS. The structure of the normal and hydronephrotic upper urinary tract. / In: O’Reilly PH, Gosling JA (Eds). Idiopathic Hydronephrosis. Springer, Berlin, Heidelberg, New York 1982; 1-15
- Anderson JC, Hynes W. Retrocaval ureter. // Brit J Urol. 1949. Vol. 21, N 3. P. 209-214
- Friedrich U, Reifi-Zimmermann GU, Endert G, Ritter EP. Die Urokinetographie in der Diagnostik und Verlaufsbeobachtung obstuktiver Uropathien im Kindesalter. // Z Kinderchir. 1990. Vol. 45, N 2. P. 100-108
- Woolfson RG, Hilson AJW, Lewis CA, Hill PD, Shah PJ, Neild GH. Scintigraphie evidence of abnormal ureteric peristalsis following urological surgery. // Brit J Urol. 1994. Vol. 73, N 3. P. 142-146
- Hendren WH, McLorie GA. Late stricture of intestinal ureter. // J Urol. 1983. Vol. 129, N 3. P. 584-590
- Hendren WH. Tapered bowel segment for ureteral replacement.// Urol Clin North Am. 1978. Vol. 5, N 3. P. 607-616
- Juma S, Nickel JC. Apendix interposition of the ureter. // J Urol. 1990. Vol. 144, N 2. P. 130-131
- Melchior H, Spehr C. Ureterersatz-Operationen. // Urologe A. 1987. Vol. 26, N 4. P. 181-188






