ВВЕДЕНИЕ
Коррекция нарушений мочеиспускания, которые могут наблюдаться у 10-90% неврологических больных, несмотря на достижения современной медицины, остается неразрешенной проблемой [1].
Клинические проявления этих нарушений разнообразны. Они включают гиперактивность или сниженную активность детрузора, детрузорно-сфинктерную диссинергию, нарушение произвольного расслабления наружного сфинктера уретры (псевдодиссенергия), гиперсенсорную форму детрузорной гиперактивности и стрессовое недержание мочи. Тип нарушения мочеиспускания определяются характером и степенью выраженности лежащей в его основе неврологической патологии [2].
При поражении супрапонтинных центров регуляции мочеиспускания у пациентов преобладают симптомы накопления. При локализации патологического процесса в супраскакральных отделах спинного мозга отмечаются гиперактивность мочевого пузыря и сфинктерного аппарата, что клинически может проявляется как симптомами накопления, так и опорожнения. При повреждении сакрального центра мочеиспускания у пациентов диагностируется гипоактивность мочевого пузыря при сниженной или нормальной активности сфинктера [3].
Следует отметить, что симптомы накопления в большей степени влияют на качество жизни пациента, а их возникновение побуждает пациента и его лечащего врача к проведению диагностических процедур и медицинских вмешательств, направленных на их коррекцию. В тоже время, симптомы опорожнения, в силу нарушения у этих пациентов ощущения наполнения мочевого пузыря, часто диагностируются после присоединения инфекционно-воспалительных осложнений или нарушения функции почек.
Это приводит к острой необходимости ультразвукового мониторинга опорожнения мочевого пузыря у пациентов нейрогенными нарушениями мочеиспускания, что затруднительно в амбулаторных условиях при учете низкой мобильности таких пациентов.
Один из способов разрешения этой проблемы – использование носимых аппаратно-программных комплексов для мониторинга наполнения мочевого пузыря. Однако настоящее время количество исследований, посвященных их роли в медицинской реабилитации пациентов с нейрогенными нарушениями мочеиспускания, недостаточно, что побудило нас к подготовке настоящего литературного обзора.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен поиск, анализ и систематизация литературы по базам PubMed, e-library и Google Scholar по ключевым словам «нейрогенные нарушения мочеиспускания», «neurogenic bladder», «ультразвуковая диагностика», «ultrasound examination», «мониторинг», «monitoring» – всего 211 источников, из которых для написания статьи были отобраны 46. Из анализа были исключены диссертации и их авторефераты, а также тезисы конференций.
РЕЗУЛЬТАТЫ
На первом этапе исследования нами определены группы пациентов, у которых могут развиваться нейрогенные нарушения мочеиспускания, в том числе, оценена частота симптомов опорожнения, то есть тех их них, кому целесообразно проведение ультразвукового мониторинга наполнения мочевого пузыря.
Позвоночно-спинальная травма Последствия позвоночно-спинальной травмы относится к наиболее частым патологическим состояниям, которые приводят к развитию нейрогенных нарушений мочеиспускания.
По данным M. Fitzharris и соавт. в 2007 г. частота травматических повреждений спинного мозга в мире составила 23 на 1 000 000 (179,312 случаев в год) [4], а в 2015 году, по данным S.B. Jazayeri и соавт., этот показатель варьировал от 3,6 до 195, 4 на 1 000 000 [4-5].
Клинические проявления нейрогенных нарушений мочеиспускания у пациентов, перенесших травму позвоночника и спинного мозга, вариабельны, а их диагностика и лечение требует индивидуального и мультидисциплинарного подхода [6].
Дегенеративно-дистрофические и воспалительные заболевания позвоночника
Другая группа патологических состояний, приводящих к развитию нейрогенных нарушений мочеиспускания, – заболевания позвоночника. Их характер и степень выраженности определяются уровнем поражения.
В.Б. Бердичевский и соавт. при обследовании 157 пациентов (72 мужчин и 85 женщин) с дегенеративнодистрофическими заболеваниями позвоночника выявил гиперактивность мочевого пузыря у 21,4%, а гипоактивность детрузора – у 8,5% из них [7].
А.И. Горбунов и соавт. обнаружил гипоактивность детрузора у 50% пациентов со спондилитом, у 13,1% – детрузорно-сфинктерную диссинергию [8].
А.Н. Муравьев и соавт. обследовав 78 пациентов с туберкулезным спондилитом, диагностировал нарушения мочеиспускания у каждого второго пациента [9].
ОНМК, болезнь Паркинсона
Урологические осложнения встречаются у 24-87% пациентов с ОНМК. При этом у 44% их них отмечаются симптомы накопления, у 23% – опорожнения, а 14% наблюдается смешанная симптоматика. Наличие более 150 мл остаточной мочи в 1-е сутки после ОНМК выявляется у 36% больных, на 90-й день – у 19%. Наличие остаточной мочи относится к неблагоприятным прогностическим факторам, которые повышают риск смерти пациентов в течение 90 суток после ОНМК на 16-22%. ИМП составляют до 40% госпитальных инфекций. 80% из них – катетер-ассоциированные. ДЭП – изменение ощущения позывов на микцию (пациент не может четко дифференцировать позыв на микцию), что сопровождается прогрессированием СНМП. Рассеянный склероз – нарушения мочеиспускания до 24-96%. [10].
Возникновение гиперактивности мочевого пузыря после ОНМК обусловлено ишемическим повреждение корковых, подкорковых и стволовых центров мочеиспускания, в том числе ядра Баррингтона, которое участвует в различных адаптационных процессах. Нарушение ассоциативных связей головного мозга, их функциональное разобщение вследствие демиелинизации афферентных и эфферентных путей приводит к снижению церебрального влияния на спинальные рефлексы мочеиспускания. При повреждении околоводопроводного серого вещества варолиева моста острая задержка мочи, требующая катетеризации мочевого пузыря, развивается у 64% пациентов, а при повреждении М-зоны ядра Баррингтона – у 22% [11].
У этих пациентов значительно повышается риск развития катетер-ассоциированной инфекции мочевыводящих путей, что значительно осложняет течение заболевания и удлиняет сроки реабилитации после острого нарушения мозгового кровообращения [12].
При болезни Паркинсона различные нарушения мочеиспускания встречаются у 40-80% пациентов. Наиболее часто диагностируются сфинктерные нарушения – у 30-90% их них. У 10% пациентов выявляются нарушения сократительной способности детрузора. Эти изменения могут приводить к развитию у этих пациентов острой и хронической задержки мочи [10].
Рассеянный склероз
Рассеянный склероз часто сопровождается возникновением у пациента нарушений мочеиспускания. Так А.В. Зыряновым и соавт., при обследовании 160 пациентов с рассеянным склерозом нейрогенная дисфункция мочеиспускания выявлена у 65% из них. При этом симптомы опорожнения составили встречались у 76%, а накопления – у 98% из них [13].
Сахарный диабет
Урологические осложнения сахарного диабета относят к наиболее значимым для пациента. До появления уродинамических исследований все эти осложнения считались инфекционно-воспалительными. У больных сахарным диабетом на первый план выступает симптоматика ГМП [14].
В 1976 г. датский уролог C. Frimodt-Moller описал три уродинамических признака диабетических нарушений мочеиспускания – уменьшение чувствительности мочевого пузыря, увеличение его емкости и уменьшение сократимости с увеличением количества остаточной мочи. Им же предложен термин «диабетическая цистопатия» [15].
На основании экспериментальных исследований предложена гипотеза развития диабетической цистопатии. На первой стадии, вследствие полиурии, развивается гипертрофия детрузора. В дальнейшем, по мере прогрессирования микроангиопатии, происходит его декомпенсация с развитием гипо- или аконтрактильности детрузора и нарушением опорожнения мочевого пузыря [16].
Повреждение интрамуральных нервных окончаний в стенке мочевого пузыря вследствие ее ишемии, обусловленной диабетической микроангиопатией, а также изменения нейромышечной трансмиссии при диабетической цистопатии приводит к снижению сократимости детрузора, диабетической нейропатии и увеличению количества остаточной мочи [17-20].
К другим патогенетическим механизмам развития нейрогенных нарушений мочеиспускания относят дисфункцию уротелия, среди которых выделяют барьерную и сенсорную. Последняя заключается в выработке медиаторов, которые воздействуют на афферентные нервные окончания. При диабетической цистопатии отмечается повышенный синтез АТФ клетками уротелия, что приводит к гиперактивности детрузора. При его гипоактивности отмечается повышение выработки уротелием NO при нормальном уровне синтеза АТФ [21].
Осложнения оперативных вмешательств на органах малого таза
В силу анатомической близости, особенностям кровоснабжения и иннервации органов малого таза оперативные вмешательства в данной зоне могут приводить к развитию нарушений мочеиспускания. Чаще всего данные осложнения развиваются после хирургического лечения колоректального рака и рака шейки матки [22].
У 33% этих больных могут развиваться недержание мочи, детрузорная арефлексия, гиперактивность мочевого пузыря [23].
Таким образом, нейрогенные нарушения мочеиспускания возможны у пациентов с последствиями позвоночно-спинальной травмы и оперативных вмешательств на органах малого таза, а также дегенеративнодистрофическими и воспалительными заболеваниями позвоночника, ОНМК, болезнью Паркинсона, рассеянным склерозом, сахарным диабетом.
В процессе оказания помощи этим пациентам необходимо проведение мониторинга функционального состояния нижних мочевыводящих путей [24]. У пациентов с наличием симптомов опорожнения крайне важно осуществление контроля количества остаточной мочи.
С этой целью наиболее часто используется портативные ультразвуковые сканеры, которые позволяют осуществить исследование непосредственно у постели пациента [25-27].
Применение таких сканеров позволяет c достаточно высокой точностью оценивать количество мочи в мочевом пузыре, избежать ненужных катетеризаций и облегчает ведение пациентов с нарушениями мочеиспускания [28-30].
При этом следует отметить, что несмотря на свои преимущества ультразвуковое исследование остается оператор-зависимым методом, а его результаты достаточно вариабельны, что требует повторных сканирований для повышения его информативности [31-33].
Кроме того, наличие у пациентов некоторых заболеваний органов малого таза может затруднять оценку наполнения мочевого пузыря. Так, например, Cooperberg M.R. с соавт. описано три клинических наблюдения, в которых при проведении ультразвукового сканирования кисты яичников были расценены как мочевой пузырь, содержащий мочу [34].
Эти недостатки затрудняют использование портативных ультразвуковых аппаратов в домашних условиях, когда сканирование выполняется непосредственно пациентом или его родственниками, осуществляющими уход за ним.
Одним из возможных решений было использование импедансной томографии [35, 36].
В основе метода лежит изменение электрического сопротивления биологических тканей. Поскольку среди биологических тканей жидкость имеет наименьшее сопротивление, то по мере наполнении мочевого пузыря оно будет снижаться [37].
В качестве примеров оборудования, которое может быть использовано для амбулаторного мониторинга наполнения мочевого пузыря, нами приведено два устройства, в одном из которых используется принцип измерения биоимпеданса, а во втором – проводится ультразвуковое сканирование в автоматическом режиме [38].
Компанией «Lir Scientiific» разработан прибор «Brightly» (рис. 1). Он изготовлен в виде пояса, содержащего биосенсоры, который укрепляется на пояс пациента. При наполнении мочевого пузыря прибор через Bluetooth посылает на смартфон пациента предупреждение о необходимости его опорожнения (рис. 2).
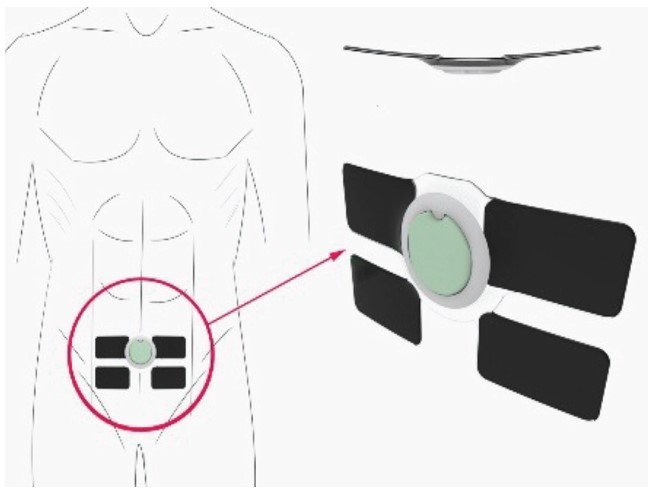
Рис. 1. Прибор «Brightly»
Fig. 1. Device «Brightly»

Рис. 2. Сообщение от прибора на смартфон пациента
Fig. 2. A message from the device to the patient's smartphone
Компанией «Triple W» разработано устройство «DFree» (рис. 3). Он состоит из хаба весом 73 г и подключенного сенсора, которые способны функционировать в непрерывном режиме в течение 24 часов. В системе используется неинвазивный ультразвуковой сенсор, который отслеживает степень наполнения мочевого пузыря (рис. 4). Сенсор фиксируется на передней брюшной стенке. При правильном его расположении светодиод на устройстве изменит свой цвет. Данные, получаемые с помощью ультразвукового датчика, обрабатываются и анализируются прибором, а результаты посредством беспроводной связи направляются в приложение на смартфоне пациента [39].
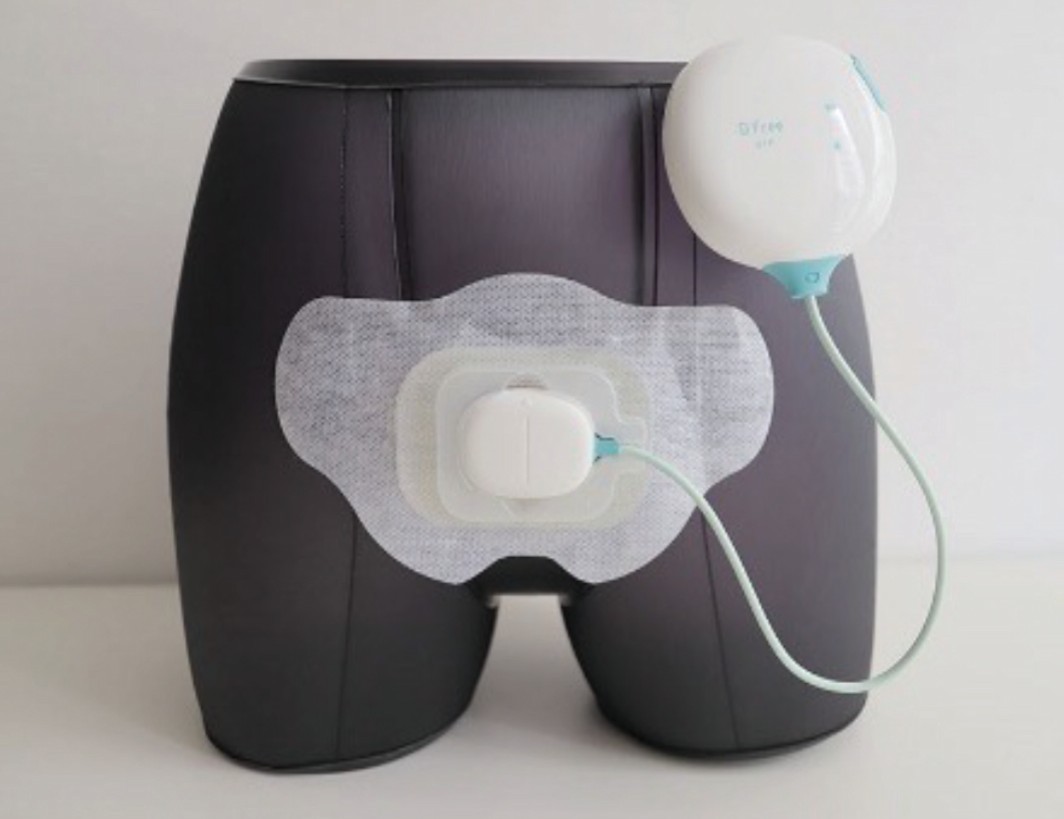
Рис. 3. Прибор «DFee»
Fig. 3. Device «DFee»
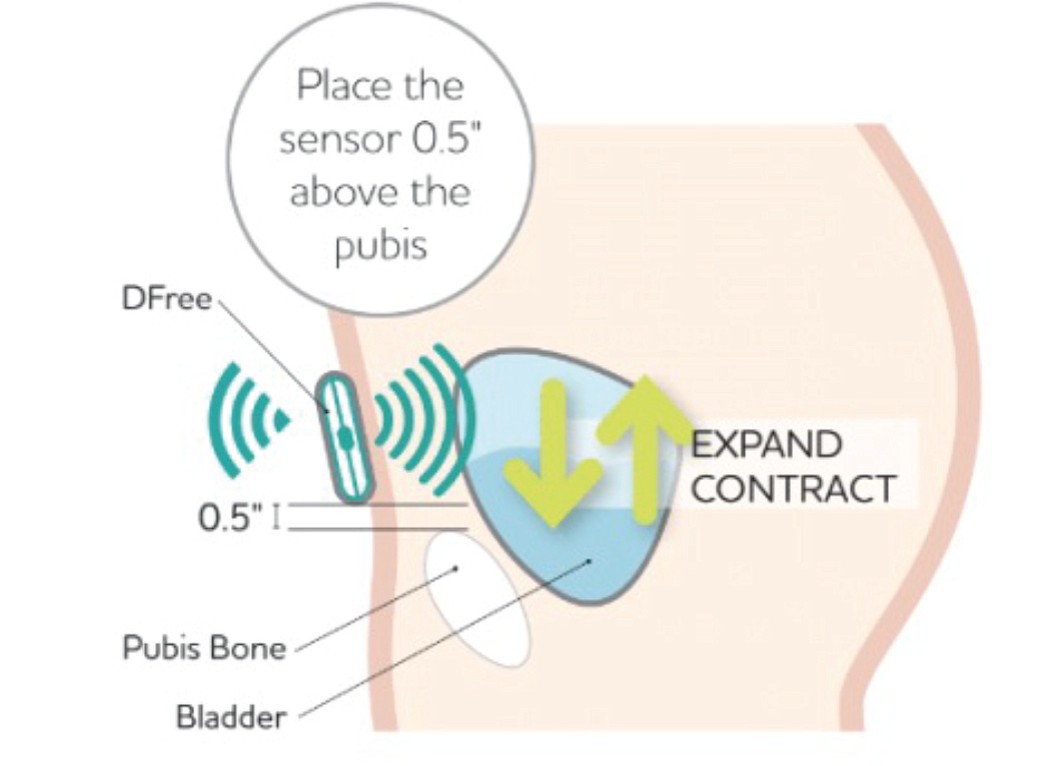
Рис. 4. Принцип работы прибора «Dfee»
Fig. 4. The principle of operation of the device «Dfee»
Мониторинг наполнения мочевого пузыря у детей В настоящее время ночной энурез у детей является наиболее часто встречающейся урологической проблемой [40]. Исследования показывают, вероятность снижения качества жизни у детей, страдающих данным заболеванием, в 2,87 раз выше, чем у их сверстников [41]. Лечение может быть как медикаментозным, так и с помощью различных устройств, действие которых заключается в обучении своевременному пробуждению при первых позывах к мочеиспусканию. Такими устройствами являются энурезные будильники, состоящие из датчика, который воспринимает появление первых капель мочи, и самого будильника [42]. Данный метод позволяет сформировать рефлекс и таким образом вылечить ночной энурез. Существенным недостатком является пробуждение во время мочеиспускания, а не до его начала, что делает необходимым поиск методов для определения объема мочевого пузыря и его наполнения.
Одним из решений стало использование ультразвука. W.M.J. Kwinten и соавт. предлагают использование неинвазивного носимого ультразвукового датчика, который позволяет мониторировать объем мочевого пузыря [43]. Прибор SENS-U устанавливается на 1 см выше лобковой кости, на одной линии с пупком, измеряет наполнение мочевого пузыря в течение ночи и, при достижении критической отметки, начинает вибрировать, пробуждая ребенка. Четыре ультразвуковых датчика с «полем зрения» 30° определяют расстояние от передней до задней стенки мочевого пузыря в саггитальной плоскости по разнице амплитуд отраженных от стенок волн. По полученному результату определяется высота мочевого пузыря и далее – его объем [44]. Расчет максимального объема мочевого пузыря позволяет установить порог его наполнения, при выявлении которого устройство уведомит ребенка о необходимости мочеиспускания. Помимо датчика, авторы предлагают использование приложения, которое получает и хранит информацию с прибора, что позволяет импортировать данные на другие устройства и в дальнейшем анализировать их. Преимущества устройства заключаются в его неинвазивности, определении объема мочевого пузыря, уведомлении пациента о позыве до начала мочеиспускания, а также возможности дальнейшей работы с получаемыми данными. К недостаткам относят сложности самостоятельной постановки датчика на правильную позицию, определение порога наполнения мочевого пузыря и использование устройства у детей с ожирением
Другим решением стала разрабатываемая K. Kuru и соавт. умная система, состоящая из неинвазивных ультразвуковых датчиков, необходимых для измерения объема мочевого пузыря, прикроватного будильника и приложения для смартфона [45-46]. Определение объема мочевого пузыря происходит не только по расстоянию между стенками, расчету ширины и высоты органа, но и по изменению толщины его стенки. Для минимизирования ошибок при постановке датчика в домашних условиях он прикрепляется к специальному нижнему белью, что делает возможным использование прибора детьми самостоятельно. Прикроватный будильник представляет собой компьютер с собственными источником питания и Wi-Fi-роутером. Все это позволяет анализировать данные с устройства без подключения к телефону. Частота измерений выбрана на основе исследования скорости наполнения мочевого пузыря у детей и составляет 3 последовательных ультразвуковых импульса один раз в 2 минуты. Приложение для смартфона позволяет корректировать и уточнять параметры мочевого пузыря, необходимые для правильной работы прибора. Достоинствами данного устройства является возможность его адаптации под каждого пациента и неинвазивность. К ограничениям относится небольшое количество участников исследования и сравнение результатов с конвексным датчиком УЗИ, а не определением объема мочевого пузыря с помощью катетеризации.
ОБСУЖДЕНИЕ
Существует достаточно большая группа пациентов, у которых развиваются нейрогенные нарушения мочеиспускания. Наибольшую опасность представляет нарушение функции опорожнения мочевого пузыря, которое длительное время протекает бессимптомно, что приводит к прогрессирующему и часто необратимому нарушению функции почек [47, 48, 49].
На сегодняшний день возможности лечения таких пациентов весьма ограничены и представляют собой мероприятия, направленные на периодическое опорожнение мочевого пузыря, что необходимо осуществлять несколько раз в день.
Катетеризация мочевого пузыря, которая выполняется с целью опорожнения мочевого пузыря, является инвазивной процедурой. Ее необходимо выполнять только по показаниям, то есть при наличии в мочевом пузыре значительного количества мочи и риске развития инфекционно-воспалительных процессов.
Следует отметить, что темп диуреза индивидуален. Он также зависит от диеты, питьевого режима, функционального состояния пациента и температуры окружающей среды. Ультразвуковой мониторинг и биоимпедансометрия или их сочетание, позволяет проводить неинвазивную оценку объема мочевого пузыря, а использование современных технологий, таких как беспроводная связи и приложения на смартфонах, позволяет пациенту максимально индивидуализировать ритм опорожнения мочевого пузыря. Осложняющими моментами в использовании данных технологий являются консерватизм врачей, комплаентность пациентов, отсутствие методических разработок и рекомендаций по использованию данных технологий мониторинга.
ВЫВОДЫ
Использование носимых аппаратно-программных комплексов для мониторинга наполнения мочевого пузыря и специальных приложений в смартфонах у пациентов с нейрогенными нарушениями мочеиспускания – важный шаг в реализации стратегии развития «Медицины 5П»: предиктивной и превентивной (их применение позволяет предсказать и, следовательно, предотвратить, возможное развитие осложнений вследствие переполнения мочевого пузыря), персонализированной (частота и ритм периодических катетеризаций мочевого пузыря максимально соответствует текущему физиологическому состоянию пациента), пациент-ориентированной (пациент непосредственно вовлечен в лечебный процесс) и прецизионной (катетеризация мочевого пузыря выполняется строго по показаниями и при достижении порогового объема мочи). Необходимо проведение клинических исследований мониторинга в рутинной урологической практике.
ЛИТЕРАТУРА
- Шварц П.Г. Диагностика нейрогенных нарушений мочеиспускания. РМЖ 2011;19(32):2063-7. [Shvarts P. G. Diagnostics of neurogenic disorders of urination RMZh = RMJ 2011;19(32):2063-7. (In Russian)].
- Шварц П.Г. Феноменология нейрогенных нарушений мочеиспускания. РМЖ 2012;20(18):912-6. [Shvarts P. G.Phenomenology of neurogenic urination disorders RMZh = RMJ 2012;20(18):912-6. (In Russian)].
- Blok B, Castro-Diaz D, Popolo G, Groen J, Hamid R, Karsenty G, et al. Neuro-urology EAU Guidelines. [Electronic resource]. URL: https://uroweb.org/guideline/neuro-urology/.
- Fitzharris M, Cripps RA, Lee BB. Estimating the global incidence of traumatic spinal cord injury. Spinal Cord 2014;52(2):117-22. https://doi.org/10.1038/sc.2013.135.
- Jazayeri SB, Beygi S, Shokraneh F, Hagen EM, Rahimi-Movaghar V. Incidence of traumatic spinal cord injury worldwide: a systematic review. Eur Spine J 2015;24(5):905-18. https://doi.org/10.1007/s00586-014-3424-6.
- Тищенко Г.Е., Бородулина И.В., Салюков Р.В., Рачин А.П. Нейрогенные расстройства мочеиспускания при травме позвоночника и спинного мозга: взгляд невролога и уролога. РМЖ 2017;25(9):653-6. [Tishchenko G.E., Borodulina I.V., Saliukov R.V., Rachin A.P. Neurogenic urination disorders in spinal cord and spinal cord injury: a neurologist's and urologist's view. RMZh = RMJ 2017;25(9):653-6. (In Russian)].
- Бердичевский В.Б., Бердичевский Б. А., Казенко Н.И., Чибулаева Е.В., Барашин А.Д., Романова А.В. Влияние хронического нейрогенного болевого синдрома на особенности ритма мочеиспускания. Университетская медицина Урала 2017;3(4,11):9-10. [Berdichevskii V.B., Berdichevskii B.A., Kazenko N.I., Chibulaeva E.V., Barashin A.D., Romanova A.V. The influence of chronic neurogenic pain syndrome on the peculiarities of urination rhythm. Universitetskaia meditsina Urala = University Medicine of the Urals 2017;3(4,11):9-10. (In Russian)].
- Горбунов А. И., Лебедев А. А., Муравьев А. Н., Яблонский П. К. Нейрогенные нарушения мочеиспускания у больных спондилитом. Туберкулез и социально-значимые заболевания 2017;(4):45-8. [Gorbunov A.I., Lebedev A.A., Muravev A.N., Iablonskii P.K. Neurogenic disorders of urination in patients with spondylitis. Tuberkulez i sotsialno-znachimye zabolevaniia = Tuberculosis and socially significant diseases 2017(4):45-8. (In Russian)].
- Муравьев А.Н., Лебедев А.А., Горбунов А.И., Орлова Н.И., Семченко А.Ф. Нарушения уродинамики нижних мочевых путей у больных туберкулезным спондилита. Туберкулез и болезни легких 2015(1):24-30. [Muravev A.N., Lebedev A.A., Gorbunov A.I., Orlova N.I., Semchenko A.F. Disorders of the urodynamics of the lower urinary tract in patients with tuberculous spondylitis. Tuberkulez i bolezni legkikh = Tuberculosis and lung diseases 2015(1):24-30. (In Russian)].
- Акшулаков С.К., Такенов Ж.Т., Карибай С.Д., Кисамеденов Н.Г. Нарушения мочеиспускания при сосудистых и воспалительных заболеваниях головного мозга. Нейрохирургия и неврология Казахстана 2015;39(2):34-40. [Akshulakov S.K., Takenov Zh.T., Karibai S.D., Kisamedenov N.G. Disorders of urination in vascular and inflammatory diseases of the brain. Neirokhirurgiia i nevrologiia Kazakhstana = Neurosurgery and neurology of Kazakhstan 2015;39(2):34-40. (In Russian)].
- Шварц П.Г., Попов С.В., Бершадский А.В. Патофизиология и принципы терапии нейрогенного гиперактивного мочевого пузыря у пациентов, перенесших нарушение мозгового кровообращения. Исследования и практика в медицине 2017;4(2):43-53. [Shvarts P.G., Popov S.V., Bershadskii A.V. Issledovaniia i praktika v meditsine = Research and Practical Medicine Journal 2017;4(2):43-53. (In Russian)].
- Кулов Б.Б., Каскеев Д.М., Сулайманов А.Э. Нарушения мочеиспускания у больных с сосудистыми заболеваниями головного мозга (обзор литературы). Наука, новые технологии и инновации Кыргызстана 2018(2):96-8. [Kulov B. B., Kaskeev D. M., Sulaimanov A. E. Disorders of urination in patients with vascular diseases of the brain (literature review). Nauka, novye tekhnologii i innovatsii Kyrgyzstana = Science, new technologies and innovations of Kyrgyzstan 2018(2):96-8. (In Russian)].
- Зырянов А.В., Баженов И.В., Филиппова Е.С., Устинов Г.С., Турова Е.Л., Тореев И.О., Леушин Е.К. Эпидемиология и характер расстройств мочеиспускания у больных с рассеянным склерозом. Вестник урологии 2020;8(2):29-36 [Zyrianov A.V., Bazhenov I.V., Filippova E.S., Ustinov G.S., Turova E.L., Toreev I.O., Leushin E.K. Epidemiology and nature of urination disorders in patients with multiple sclerosis. Vestnik urologii = Bulletin of Urology 2020;8(2):29-36 (In Russian)].
- Кузмин И.В., Шабудина Н.О. Патогенетические основы развития диабетической цистопатии. Экспериментальная и клиническая урология 2014(4):92-99. [Kuzmin I.V., Shabudina N.O. Pathogenetic bases of diabetic cystopathy development. Eksperimentalnaia i klinicheskaia urologiia=Experimental and clinical urology 2014;(4):92-99. (In Russian)].
- Frimodt-Moller C. Diabetic cystopathy I: a clinical study of the frequency of bladder dysfunction in diabetics. Dan Med Bull 1976(23):267-78.
- Daneshgari F, Liu G, Birder L, Hanna-Mitchell AT, Chacko S. Diabetic bladder dysfunction: current translational knowledge. J Urol 2009(182):18-26.
- Yoshimura N, Chancellor MB, Andersson KE. Recent advances in understanding the biology of diabetic-associated bladder complications and novel therapy. BJU Int 2006(95):733-8.
- Yamaguchi O, Nomiya M, Andersson KE. Functional consequences of chronic bladder ischemia. Neurourol Urodyn 2014;33(1):54-8.
- Burnstock G. Purinergic signalling in lower urinary tract: handbook of experimental pharmacology I: purinergic and pyrimidinergic signalling I. In: Molecular, nervous and urinogenitary system function: Springer-Verlag. Berlin 2001(151):423-515.
- Yi C, Wei Z, Wang H, Song T, Ding L. The effects of peptidergic nerve (calcitonin gene-20. related peptide, cgrp) and calcium-related contraction on the voiding dysfunction and histopathological alteration in the diabetic cystopathy rats. 40th Annual Meeting of International Incontinence Society, Toronto, Canada 2010:516.
- Munoz A, Smith C, Boone T, Somogyi G. Overactive and underactive bladder dysfunction is reflected by alterations in urothelial ATP and NO release. Neurochem Int 2011;58(3):295–300.
- Онопко В.Ф., Загайнова Е.А., Кириленко Е.А. Нейрогенная дисфункция мочевого пузыря у онкобольных, оперированных на органах малого таза. Acta Biomedica Scientifica (East Siberian Biomedical Journal) 2019;4(3):89-95. [Onopko V. F., Zagainova E. A., Kirilenko E. A. Neurogenic dysfunction of the bladder in cancer patients operated on the pelvic organs. Acta Biomedica Scientifica (East Siberian Biomedical Journal) 2019;4(3):89-95. (In Russian)].
- Франк М.А., Демидов С.М., Мурзин М.О. Нейрогеная дисфункция детрузора и половые расстройства у больных колоректальным раком, после хирургического лечения. Уральский медицинский журнал 2017;146(2):118-121. [Frank M. A., Demidov S. M., Murzin M. O. Neurogenic detrusor dysfunction and sexual disorders in patients with colorectal cancer, after surgical treatment. Uralskii meditsinskii zhurnal = Ural Medical Journal 2017;146(2):118-121 (In Russian)].
- Филиппова Е.С., Баженов И.В., Зырянов А.В., Журавлев В.Н. Эпидемиология нейрогенных нарушений мочеиспускания. Экспериментальная и клиническая урология 2020(3):25-33. [Filippova E.S., Bazhenov I.V., Zy`ryanov A.V., Zhuravlev V.N. Epidemiology of neurogenic urinary disorders. E`ksperimental`naya i klinicheskaya urologiya = Experimental and clinical urology 2020(3):25-33. (In Russian)]. https://doi.org/10.29188/2222-8543-2020-12-3-25-33.
- Byun SS, Kim HH, Lee E, JS Paick, Kamg W, Oh SJ. Accuracy of bladder volume determinations by ultrasonography: are they accurate over entire bladder volume range? Urology 2003;62(4):656-60. https://doi.org/10.1016/s0090- 4295(03)00559-4.
- Ghani KR, Pilcher J, Rowland D, Patel U, Nassiri D, Anson K. Portable ultrasonography and bladder volume accuracy--a comparative study using three-dimensional ultrasonography. Urology 2008;72(1):24-8. https://doi.org/10.1016/j.urology.2008.02.033.
- Oh-Oka H, Nose R. Efficacy and problems of bladder volume measurement using portable three dimensional ultrasound scanning device – in particular, on measuring bladder volume lower than 100 ml. Nihon Hinyokika Gakkai Zasshi 2005;96(6):601-9. https://doi.org/10.5980/jpnjurol1989.96.601.
- Al-Shaikh G, Larochelle A, Campbell CE, Schachter J, Baker K, Pascali D. Accuracy of bladder scanning in the assessment of postvoid residual volume. J Obstet Gynaecol Can 2009;31(6):526-32. https://doi.org/10.1016/ S1701-2163(16)34215-3.
- D'Silva KA, Dahm P, Wong CL. Does this man with lower urinary tract symptoms have bladder outlet obstruction?: The rational clinical examination: a systematic review. JAMA 2014;312(5):535-42. https://doi.org/10.1001/ jama.2014.5555.
- Cho MK, Noh EJ, Kim CH. Accuracy and precision of a new portable ultrasound scanner, the Biocon-700, in residual urine volume measurement. Int Urogynecol J 2017;28(7):1057-61. https://doi.org/10.1007/s00192-016-3224-0.
- Daurat A, Choquet O, Bringuier S, Charbit J, Egan M, Capdevila X. Diagnosis of postoperative urinary retention using a simplified ultrasound bladder measurement. Anesth Analg 2015;120(5):1033-8. https://doi.org/10.1213/ANE.0000000000000595.
- Thanagumtorn K. Accuracy of post-void residual urine volume measurement using an ultrasound bladder scanner among postoperative radical hysterectomy patients. J Med Assoc Thai 2016;99(10):1061-6.
- Park YH, Ku JH, Oh SJ. Accuracy of post-void residual urine volume measurement using a portable ultrasound bladder scanner with real-time pre-scan imaging. Neurourol Urodyn 2011;30(3):335-8. https://doi.org/10.1002/ nau.20977.
- Cooperberg MR, Chambers SK, Rutherford TJ, Foster HE Jr. Cystic pelvic pathology presenting as falsely elevated post-void residual urine measured by portable ultrasound bladder scanning: report of 3 cases and review of the literature. Urology 2000;55(4):590. https://doi.org/10.1016/ s0090-4295(99)00565-8.
- Schlebusch T, Nienke S, Santos SA, Leonhardt S. Bladder volume estimation from electrical impedance tomography. Annu Int Conf IEEE Eng Med Biol Soc 2013;2013:6441-4. https://doi.org/10.1109/EMBC.2013.6611029.
- Leonhäuser D, Castelar C, Schlebusch T, Rohm M, Rupp R, Leonhardt S, Walter M, Grosse JO. Evaluation of electrical impedance tomography for determination of urinary bladder volume: comparison with standard ultrasound methods in healthy volunteers. Biomed Eng Online 2018;17(1):95. https://doi.org/10.1186/s12938-018-0526-0.
- Николаев Д. В., Щелыкалина С. П. Лекции по биоимпедансному анализу состава тела человека. М., РИО ЦНИИОИЗ МЗ РФ, 2016;152 с. [Nikolaev D. V., Shchelykalina S. P. Lectures on bioimpedance analysis of human body composition. Мoscow, Russian Central Research Institute of Healthcare Organization and Informatization, 2016;152 p. (In Russian)].
- Устройство, помогающее контролировать мочеиспускание [Электронный ресурс]. URL: https://mhealthrussian.wordpress.com/2015/06/30/ brightly/. [Ustroystvo, pomogayuschee kontrolirovat mocheispuskanie [Elektronnyiy resurs]. URL: https://mhealthrussian.wordpress.com/2015/06/30/ brightly//. (In Russian)].
- Triple W launches DFee, first wearable device for incontinence. [Electronic resource]. URL: https://www.prweb.com/releases/triple_w_launches_ dfree_first_wearable_device_for_incontinence/prweb15841075.htm.
- Gomez RM, Leslie SW, Lotfollahzadeh S. Nocturnal Enuresis. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing, 2021.
- Rangel RA, Seabra CR, Ferrarez CE, Soares JL, Choi M, Cotta RG. Quality of life in enuretic children. Int Braz J Urol 2021;3(47):535–41. https://doi.org/10.1590/S1677-5538.IBJU.2020.0308.
- Arda E, Cakiroglu B, Thomas DT. Primary nocturnal enuresis: a review. Nephrourol Mon 2016;4(8): e35809. https://doi.org/10.5812/numonthly.35809.
- Kwinten WMJ, Leuteren PG, Iersel M.D., Dik P., Jira P.E. SENS-U: continuous home monitoring of natural nocturnal bladder filling in children with nocturnal enuresis – a feasibility study. J Pediatr Urol 2020;2(16):196.e1-196.e6. https://doi.org/10.1016/j.jpurol.2020.01.012.
- Leuteren PG, Klijn AJ, M de Jong TPV, Dik P. SENS-U: validation of a wearable ultrasonic bladder monitor in children during urodynamic studies. J Pediatr Urol 2018;6(14):569.e1-569.e6. https://doi.org/0.1016/ j.jpurol.2018.07.018.
- Kuru K, Ansell D, Jones M, Goede CD, Leather P. Feasibility study of intelligent autonomous determination of the bladder voiding need to treat bedwetting using ultrasound and smartphone ML techniques: Intelligent autonomous treatment of bedwetting. Med Biol Eng Comput 2019;5(57):1079–97. https://doi.org/ 10.1007/s11517-018-1942-9.
- Kuru K, Ansell D, Jones M, Watkinson BJ, Caswell N, Leather P. Intelligent autonomous treatment of bedwetting using non-invasive wearable advanced mechatronics systems and MEMS sensors: Intelligent autonomous bladder monitoring to treat NE. Med Biol Eng Comput 2020;5(58):943–65. https://doi.org/10.1007/s11517-019-02091-x.
- Коршунова Е.С., Коршунов М.Н., Даренков С.П. Нейрогенный и идиопатический гиперактивный мочевой пузырь: камни преткновения. Consilium Medicum 2019;21(7):53-57. [Korshunova E.S., Korshunov M.N., Darenkov S.P. Neyrogennyiy i idiopaticheskiy giperaktivnyiy mochevoy puzyir: kamni pretknoveniya. Consilium Medicum 2019;21(7):53-57. (In Russian)].
- Коршунова Е.С., Коршунов М.Н., Даренков С.П. На стыке дисциплин: нейрогенный мочевой пузырь у пациентов с травматической болезнью спинного мозга. Нейрохирургия 2018;20(4)87-94. [Korshunova E.S., Korshunov M.N., Darenkov S.P. Na styike distsiplin: neyrogennyiy mochevoy puzyir u patsientov s travmaticheskoy boleznyu spinnogo mozga. Neyrohirurgiya = The Russian Journal of Neurosurgery 2018;20(4)87-94. (In Russian)].
- Коршунова Е.С., Мазуренко Д.А., Коршунов М.Н., Даренков С.П. Опыт применения ботулинического нейротоксина типа а у больных с нейрогенной детрузорной гиперактивностью вследствие болезни Паркинсона. Кремлевская медицина. Клинический вестник 2017(2)53-57. [Korshunova E.S., Mazurenko D.A., Korshunov M.N., Darenkov S.P. Opyit primeneniya botulinicheskogo neyrotoksina tipa a u bolnyih s neyrogennoy detruzornoy giperaktivnostyu vsledstvie bolezni Parkinsona. Kremlevskaya meditsina. Klinicheskiy vestnik = Kremlin Medicine Journal 2017(2)53-57. (In Russian)].







