ВВЕДЕНИЕ
Мегауретер занимает второе место по частоте встречаемости среди пороков развития уретеровезикального сегмента (УВС) после пузырно-мочеточникового рефлюкса (ПМР). Данный термин является собирательным и обозначает мочеточник увеличенного диаметра (более 5–7 мм), дилатация обычно затрагивает почечную лоханку, следовательно, у больных развивается уретерогидронефроз [1–5]. На сегодняшний день пациентам с мегауретером можно предложить различные способы коррекции данного порока. С высокой эффективностью (до 80%) применяются следующие операции: баллонная дилатация УВС при стриктурах протяженностью менее 10 мм [6–8]; реимплантация мочеточника (РМ) открытым способом [9], лапароскопическим (экстравезикальная) [10–12], роботизированным [13, 14] и пневмовезикоскопическим [12, 15–17]. В качестве меры подготовки к операции по коррекции мегауретера используют установку внутреннего стента [18], наложение разгрузочной уретерокутанеостомы (односторонней, двухсторонней) или терминальной уретерокутанеостомы [19–22]. Ряд авторов предлагают этапный хирургический подход в лечении мегауретера [23, 24]. Однако следует помнить, что первичный не рефлюксирующий мегауретер и, частично, первичный обструктивный мегауретер имеют склонность к спонтанному разрешению. Согласно исследованию 2016 г., к первому году жизни происходит разрешение мегауретера у 33% пациентов, к 3 году – у 72%, к 5 году – у 85% пациентов. В среднем спонтанное разрешение порока развития наблюдается в течение 19 месяцев наблюдения. Тем не менее, прогрессирование степени мегауретера, рецидивирующие инфекции мочевых путей, которые провоцируют ухудшение почечной функции до риска ее полной потери, являются решающим доводом к переходу от наблюдения к оперативному лечению [2, 25–27].
На данный момент необходима оптимизация подхода выполнения различных видов хирургических вмешательств у детей с мегауретером. Остается открытым вопрос о сроках и показаниях к операции, их количестве и последовательности этапов лечения. В данном исследовании мы уделили внимание анализу причин повторных хирургических вмешательств при коррекции мегауретера.
МАТЕРИАЛЫ И МЕТОДЫ
В детском уроандрологическом отделении НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиале ФГБУ «НМИЦ радиологии» Минздрава России с 2014 по 2023 гг. была выполнена пневмовезикоскопическая РМ по Коэну 26 ранее оперированным пациентам. Виды хирургических вмешательств, которые ранее получили пациенты представлены в таблице 1. Всего в этой группе было зарегистрировано 52 вмешательства до пневмовезикоскопической РМ (рис. 1). Распределение по полу было следующим: 10 девочек (38,5%) и 16 мальчиков (61,5%), соотношение девочек к мальчикам – 1:1,6. Средний возраст пациентов составил 2,54 года, средний возраст в месяцах 34,5. Из анамнеза пациентов, включенных в исследование, известно, что 4 (15,4%) пациента ранее были оперированы в НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина, 4 (15,4%) – по месту жительства и затем получали этапное лечение в НИИ урологии, 18 (69,2%) пациентов – по месту жительства.
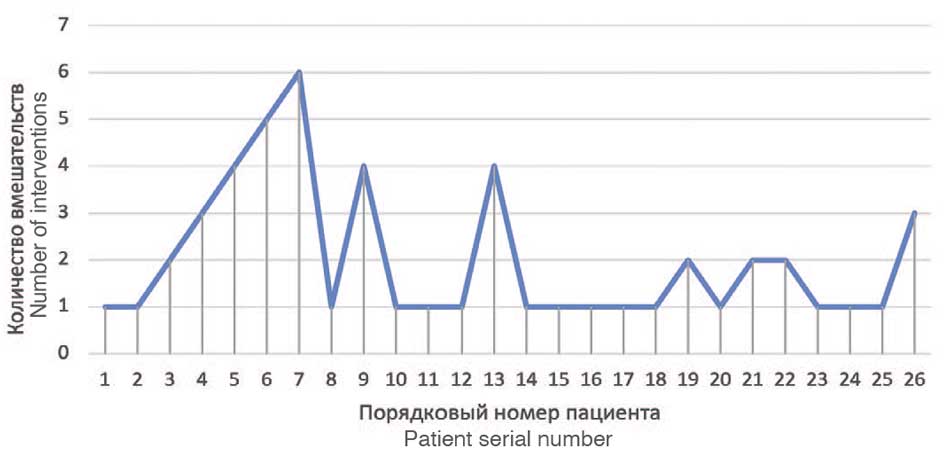
Рис. 1. Количество хирургических вмешательств у пациентов включенных в исследование
Fig. 1. Number of surgical interventions in patients included in the study
Таким образом, пациенты, перенесли от 1 до 6 хирургических вмешательств, среднее значение составило 2 вмешательства на одного пациента до РМ пневмовезикоскопическим доступом (табл. 1). Представленные данные демонстрирует клиническую сложность пациентов, включенных в данное исследование. Проведение хирургического вмешательства у ранее не оперированных пациентов предполагает более высокую эффективность, так как тканевые структуры, подвергаемые коррекции ранее не подвергалась хирургическим манипуляциям. Все вмешательства выполнялись одним оперирующим хирургом.
Основным показанием к повторной или этапной операции пневмовезикоскопической РМ служило наличие обструктивного мегауретера у 12 (46,1%) больных, существование ПМР 3-5-й ст. после неэффективной его коррекции объемобразующим веществом или приобретенный мегауретер у 10 (38,5%) и мегауретер, классифицируемый как рефлюкс-стеноз у 4 (15,4%) пациентов. Клинические особенности данной группы пациентов представлены в таблице 2.
Таблица 1. Вид и частота встречаемости (абсолютные и относительные значения) хирургических вмешательств у пациентов, включенных в исследование
Table 1. Type and frequency of occurrence (absolute and relative values) of surgical interventions in patients included in the study
| Группировка ранее выполненных хирургических вмешательств по их частоте встречаемости Grouping of previously performed surgical interventions according to their frequency of occurrence | ||
|---|---|---|
| ≥ 8 случаев ≥ 8 cases | 4-7 случаев 4-7 cases | 1-3 случая 1-3 cases |
| 19 (36,5%): инъекция объемобразующего вещества 19 (36.5%): injection of a bulk-forming agents | 6 (11,5%): бужирование уретероцистоанастомоза 6 (11.5%): bougienage of ureterocystoanastomosis | 2 (3,8%): рассечение клапана уретры 2 (3.8%): urethral valve dissection; 2 (3,8%): чрезкожная пункционная нефростомия (ЧПНС) 2 (3.8%): percutaneous puncture nephrostomy (PPNS); 2 (3,8%): пиелоуретеропластика 2 (3,8%): pyelourethroplasty 2 (3,8%): Рассечение уретероцеле 2 (3.8%): Dissection of ureterocele |
| 9 (17,3%): установка внутреннего мочеточникового стента 9 (17.3%): installation internal ureteral stent | ||
| 8 (15,4%): уретероцистоанастомоз: односторонний или двухсторонний 8 (15,4%): ureterocysto-anastomosis on 1 side or 2 sides | 1 (1,9%): первичное закрытие мочевого пузыря с пластикой шейки и уретероцистоанастомоза с 2-х сторон 1 (1.9%): primary closure of the bladder with neck plastic surgery and ureterocysto-anastomosis on 2 sides 1 (1,9%): лапароскопическая нефруретероэктомия 1 (1.9%): laparoscopic nephroureterectomy | |
Таблица 2. Клинические особенности пациентов, включенных в исследование
Table 2. Clinical characteristics of patients included in the study
| Особенности состояния почек Features of the kidney condition | Количество наблюдений Number of observations |
Особенности РМ Features of ureteral reimplantation (UR) | Количество наблюдений Number of observations |
|---|---|---|---|
| Сращение почек Kidney fusion | 2 | РМ после коррекции экстрофии мочевого пузыря UR after correction of bladder exstrophy | 1 |
| Двухсторонний мегауретер Bilateral megaureter | 1 | ||
| Дистопированная почка Dystopic kidney | 1 | РМ единым блоком UR as a single block | 2 |
| РМ и иссечение уретероцеле UR and excision of ureterocele | 2 | ||
| Единственно функционирующая почка The only functioning kidney | 3 | РМ и удаление болюса объемобразующего вещества UR and bolus removal of bulking agent | 19 |
У 6 (23,1%) пациентов были признаки нейрогенной дисфункции мочевого пузыря (НДМП). При оценке бактериального посева мочи рост фиксировался в 9 (34,6%) случаях. Мы использовали оригинальную методику фиксации троакаров (5 мм оптический порт и два 3 мм рабочих порта) при выполнении пневмовезикоскопического доступа [28, 29]. На этапе освоения методики постановки троакаров 2 пациентам была выполнена конверсия в связи с потерей визуализирующего порта.
Отличительной чертой наших пациентов было подтвержденное интраоперационное расширение реимплантируемого мочеточника более 2 см.
Внутрипузырная продольная пликация мочеточника по модифицированной нами методике A. Starr [30] требовалась в 7 случаях и выполнялась внутрипузырно, по оригинальной запатентованной технике фиксации мобилизованного расширенного мочеточника с помощью лигатурной петли на игле Туохи к стенке мочевого пузыря в области шейки [31], а оригинальный способ увеличения подслизистого туннеля при реимплантации мочеточника по Коэну за счет фиксации мочеточника в натяжении к детрузору в 2 точках выполнялся в 26 случаях [32]. В завершении операции всем пациентам устанавливался транскутанно по струне проводнику наружный мочеточниковый стент и уретральный катетер [16].
РЕЗУЛЬТАТЫ
Среднее время, затраченное на РМ пневмовезикоскопическим доступом в группе повторных пациентов составило 149 минут. Средний койко-день до операции составил 4 дня, после операции – 6 дней. В ходе РМ было проведено 2 конверсии.
Ранними послеоперационными осложнениями являлись: мочевой затек в паравезикальную область -1, необходимость коррекции положения стента – 3 (в одном случае коррекция проходила под наркозом в связи с его потерей). Поздние осложнения: рецидив мегауретера наблюдался в 1 случае; ПМР, требующий эндоскопической коррекции, был в 3 наблюдениях; геминефрэктомия на стороне поражения была выполнена в 1 случае в связи с рецидивирующими инфекциями верхних мочевых путей (ВМП) после стабилизации показателей мочеточника и чашелоханочной системы.
Ретроспективно для улучшения качества выполнения РМ пневмовезикоскопическим доступом был проведен анализ 26 карт стационарных больных для определения причин повторных операций при мегауретере у детей и мер их профилактики. Период наблюдения составил от 6 мес. до 10 лет. Контрольное обследование проводилось на 3, 6 и 12 мес. после операции и оценивалось по результатам ультразвукового исследования (УЗИ), мы отмечали постепенное уменьшение размеров чашечно-лоханочной системы и мочеточника. Признаков обструкции выявлено не было. При устойчивых изменениях в общем анализе мочи выполнялась микционная цистограмма. Рефлюкс был обнаружен у шести из 26 пациентов (23%). Эндоскопическая коррекция рефлюкса потребовалась 4 детям (15,4%). В нашей практике, причинами возникновения ПМР после реимплантнации мегауретера были: ряд осложняющих факторов, влияющих на качество формирования уретероцистоанастомоза в связи с ранее перенесеными вмешательствами, нейрогенная дисфункция мочевого пузыря; технические погрешности реимплантации на этапах формировании авторской методики.
ОБСУЖДЕНИЕ
Анализ причин повторных хирургических вмешательств при коррекции мегауретера позволил их объединить в два блока:
- Общие нарушения дренирования мочеточника, требующие повторных манипуляций (в том числе под наркозом);
- Ряд осложняющих факторов, влияющих на качество формирования уретероцистоанастомоза, хирургические погрешности методики реимплантации и тактические ошибки, которые могут приводить к возникновению ПМР или обструкции, требующие повторной операции.
Из нашей практики, к первому блоку причин повторных вмешательств можно отнести: смещение или потерю/выпадение дренажа (профилактика смещения интубаторов: двойная фиксация дренажа узловым швом к коже и широкой пластырной наклейкой, послеоперационный рентгенологический и ультразвуковой контроль положения). Нарушение адекватного оттока из мочевых путей после операции является главной причиной воспалительных осложнений в послеоперационном периоде. Для иллюстрации данной группы осложнений и метода их коррекции мы представляем два клинических наблюдения.
Девочка А. 10 лет, после пневмовезикоскопической реимплантации мочеточника слева в связи с обструктивным мегауретером была выполнена контрольная рентгенограмма для оценки положения наружного стента мочеточника (рис. 2А).
Пациентка была выписана в удовлетворительном состоянии, однако повторно обратилась через 3 дня с жалобами на дискомфорт в уретре в связи с выпадением петли интубирующего дренажа через мочеиспускательный канал (рис. 2Б). Были выполнены подтягивание дренажа для удаления петли образованной в мочевом пузыре и повторная его фиксация узловым швом к коже для предотвращения его выпадения и смещения.
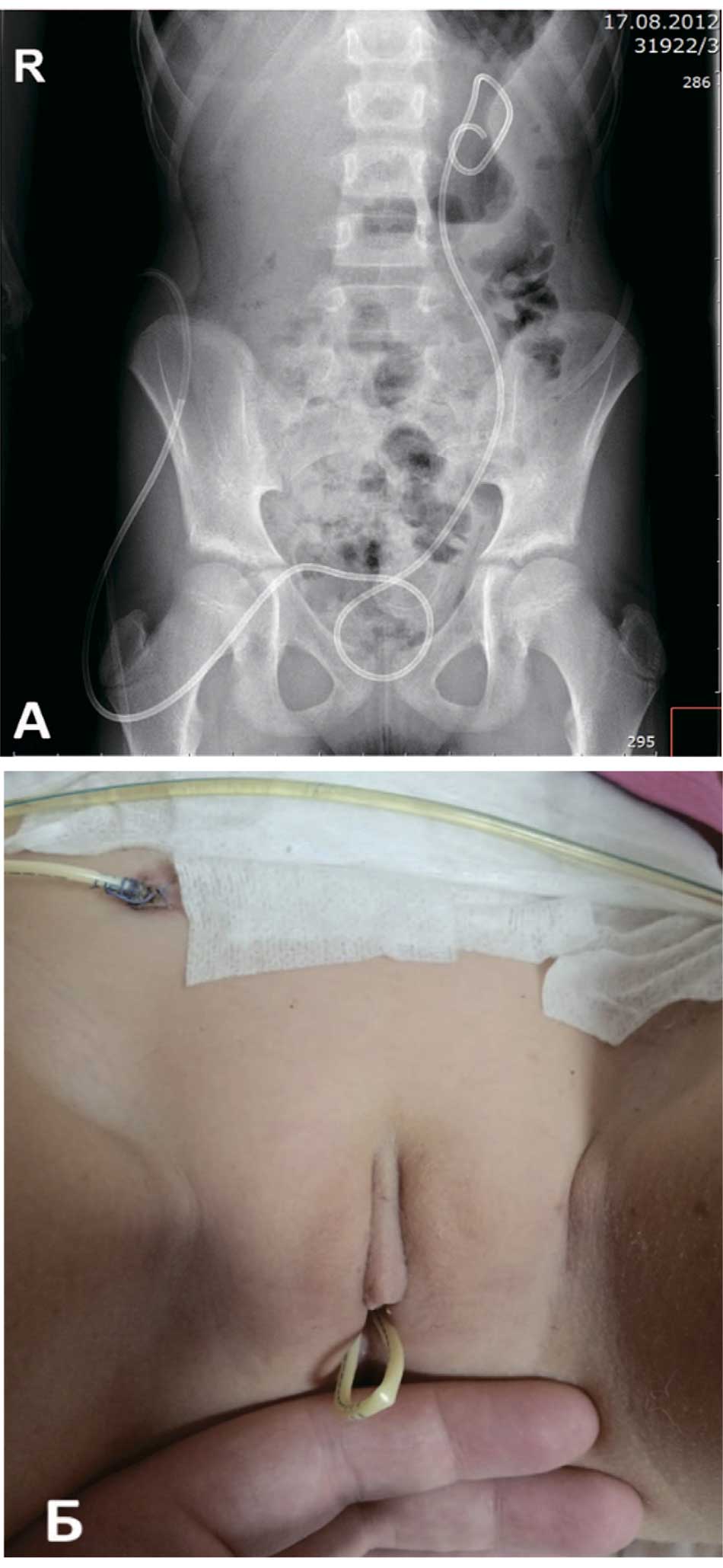
Рис. 2. Клиническое наблюдение. Девочка А 10 л. – Контрольная рентгенограмма после операции. Б – внешний вид выпадения мочеточникового дренажа через уретру
Fig. 2. Clinical data of a 10-year-old girl. A – Control radiograph after surgery. Б – appearance of prolapse of ureteral drainage through the urethra
Мальчик Б. 2 лет на 2-е сутки после пневмовезикоскопической реимплантации мочеточника по Коэну слева выдернул наружный мочеточниковый стент. Пациента экстренно направили в операционную. При цистоскопии повторная установка мочеточникового стента в неоустье левого мочеточника была затруднена. Нами был применен метод пункционного стентирования под цистоскопическим контролем (рис. 3) [33]. Учитывая атипичное расположение неоустья, которое не позволяет проводить стандартную уретероскопию и ретроградную установку мочеточникового стента, мы применили транскутанно-трансвезикоскопическую установку мочеточникового стента под цистоскопическим контролем.
Ко второму блоку причин повторных хирургических вмешательств мы отнесли ряд осложняющих факторов, влияющих на качество формирования уретероцистоанастомоза. Анатомические особенности осложняющие РМ:
- неоднократные коррекции ПМР объемобразующим веществом, которые привели к обструктивному мегауретеру;
- короткий мочеточник после его протяженной мобилизации и/или формирования Т-образной уретерокутанеостомы;
- микроцистис вследствие двусторонней уретерокутанеостомы или терминальной уретерокутанеостомы;
- реимплантация огромного по диаметру мочеточника в дистальном отделе (РМ без обуживания мочеточника);
- РМ у пациентов с НДМП;
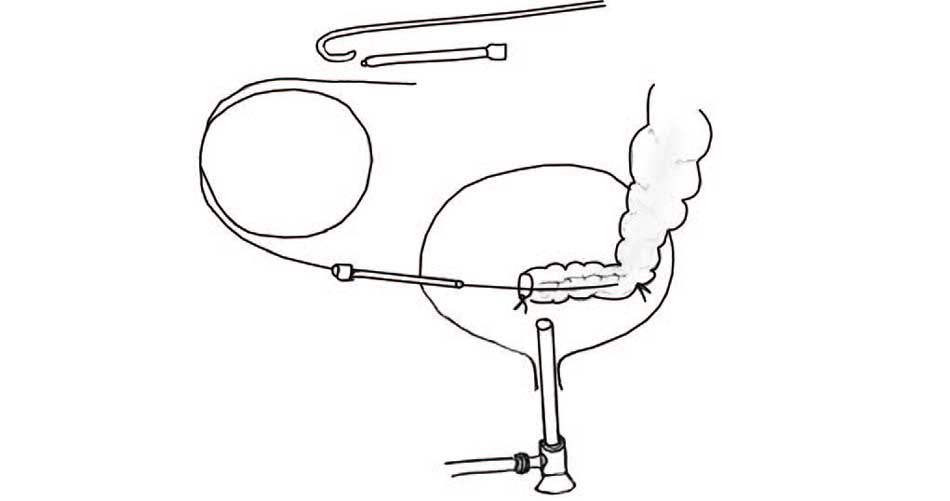
Рис. 3. Схема пункционного стентирования мочеточника под цистоскопическим контролем после операции Коэна
Figure 3. Scheme of puncture stenting of the ureter after Cohen's operation
Для иллюстрации данной группы осложнений и метода их коррекции мы представляем два клинических наблюдения. Пациент В. 5 лет, изначально наблюдался с ПМР 2-3 ст. слева, неоднократно проводились эндоскопические инъекции объемобразующего вещества, последняя коррекция сопровождалась стойкой обструкцией уретеровезикального сегмента. Через полгода пациент обратился в нашу клинику, по данным экскреторной урограммы определяется стаз рентгенконтрастного вещества в нижней-средней трети мочеточника слева. Левый мочеточник расширен более 3 см (рис. 4А).
Пациенту выполнили пневмовезикоскопическую реимплантацию мочеточника по Коэну. Этап выделения дистального отдела мочеточника был затруднен в связи с наличием выраженных рубцовых межфасциальных сращений (рис. 4Б), обусловленных асептическим воспалением в области депозита объемобразующего вещества (рис. 4 В, Г).
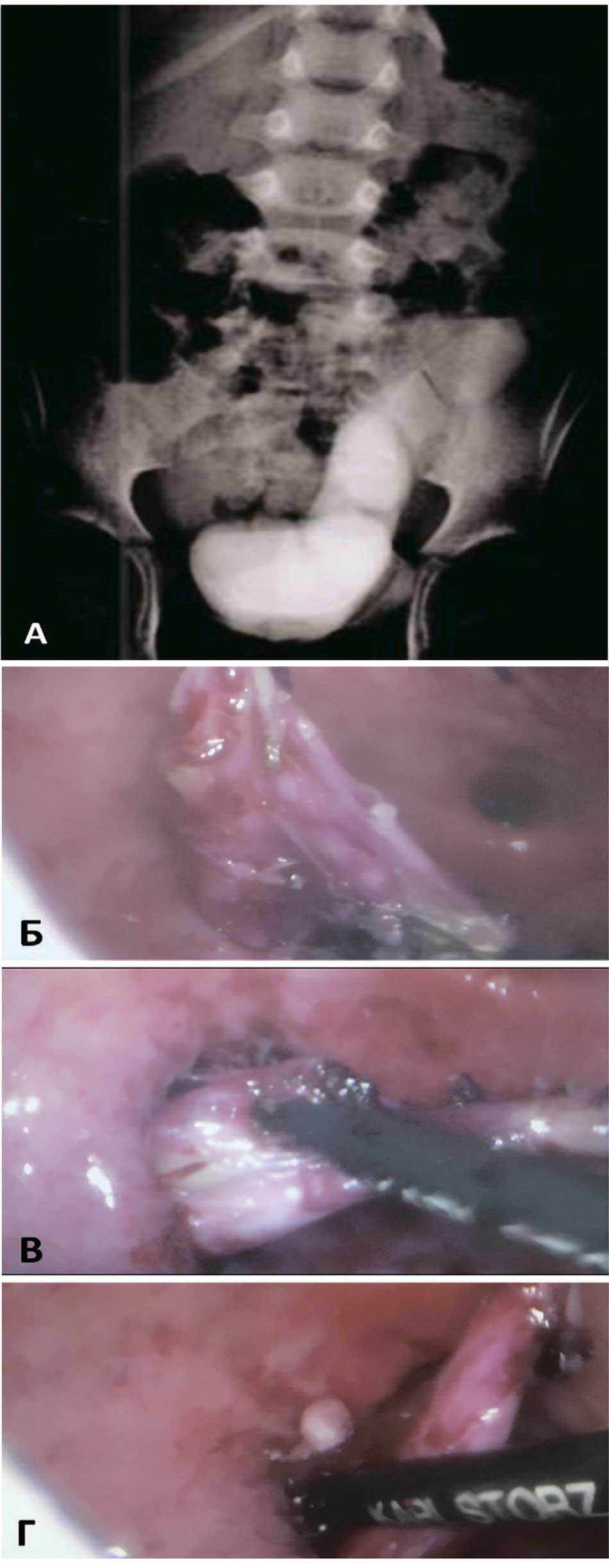
Рис. 4 Инструментальное обследование и интраоперационная картина Пациента В 5 л. А – экскреторная урограмма через полгода после коррекции ПМР 2-3 ст слева. Б – интраоперационый вид рубцовых спаек между мочеточником и детрузором. В – интраоперационый вид – инкапсулированный депозит объемобразующего вещества, спаенный с дисплазированным дистальным отделом мочеточника. Г – вскрытие и эвакуация депозита объемобразующего вещества.
Fig. 4. Clinical data of Patient В 5 years old. A – excretory urogram six months after correction of grade 2-3 VUR on the left. Б – intraoperative view of adhesions between the ureter and detrusor. B – intraoperative view – encapsulated deposit of a bulking agent fused to the dysplastic distal part of the ureter. Г – opening and evacuation of the deposit of bulking agent.
Девочка Г. 4 года: после наложения разгрузочной Т-образной уретерокутанеостомы с коротким мочеточником пневмовезикоскопическая РМ была невозможно. Была выбрана лапароскопическая РМ с использованием лоскута мочевого пузыря по Боари для удлинения подслизистого туннеля и формирования уретероцистоанастомоза без натяжения мочеточника (рис. 5).
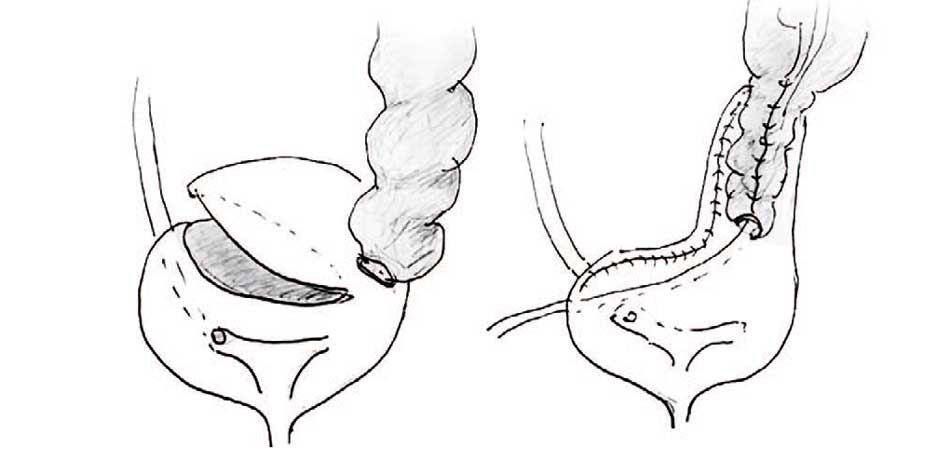
Рис. 5. Схема использования лапароскопической методики Боари в сочетании с обуживанием мочеточника и его имплантации в мобилизованный лоскут мочевого пузыря
Fig. 5. Scheme of the laparoscopic Boari technique in combination with reimplantation of a plicated ureter into a mobilized bladder flap
Второй блок объединяет причины повторных операций, связанных с хирургическими погрешностями выполнения РМ (возникновение ПМР или рецидива обструктивного мегауретера). Осуществление РМ при широком мочеточнике более 2 см без его плицирования, может провоцировать развитие ПМР. Фиксация мочеточника только к слизистой мочевого пузыря в области устья, без дополнительного крепления мочеточника к детрузору (особенно при коротком мочеточнике), может приводить к сползанию устья в подслизистый туннель и формированию рецидива мегауретера. Несоблюдения правила формирования антирефлюксного механизма 1:5 или 1:3 (1 – это ширина мочеточника, 5 или 3 – длина подслизистого туннеля), приводит к созданию короткого подслизистого туннеля и, как следствие, забросу мочи из мочевого пузыря в мочеточник.
Нами предложен оригинальный способ для увеличения подслизистого туннеля при реимплантации мочеточника по Коэну у пациентов с мегауретером с или без плицирования мочеточника (рис. 6). Способ основывается на фиксации в натяжении реимпланти руемого мочеточника двумя швами к детрузору: в области ранее расположенного устья и неоустья. Таким образом, создается подслизистый туннель, состоящий из следующих частей: стандартной (в области треугольника Льетто) и дополнительных (в проксимальном и дистальном отделе мочеточника, за счет фиксации и последующего укрытия слизистой оболочкой мочевого пузыря) [32].
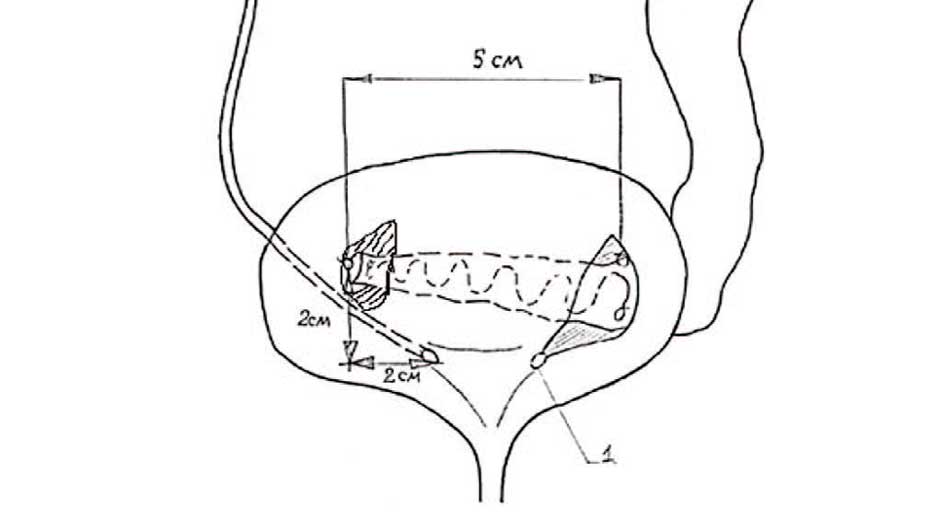
Рис. 6. Оригинальный способ увеличения подслизистого туннеля при реимплантации мочеточника по Коэну: фиксация мочеточника в натяжении к детрузору в 2 точках
Fig. 6. An original method of increasing the submucosal tunnel during reimplantation of the ureter according to Cohen: fixation of the ureter in tension to the detrusor at 2 points
Использование нерассасывающегося шовного материала при формировании устья, может приводить к образованию лигатурных камней, требующих их эндоскопического удаления вместе с лигатурами (рис. 7).
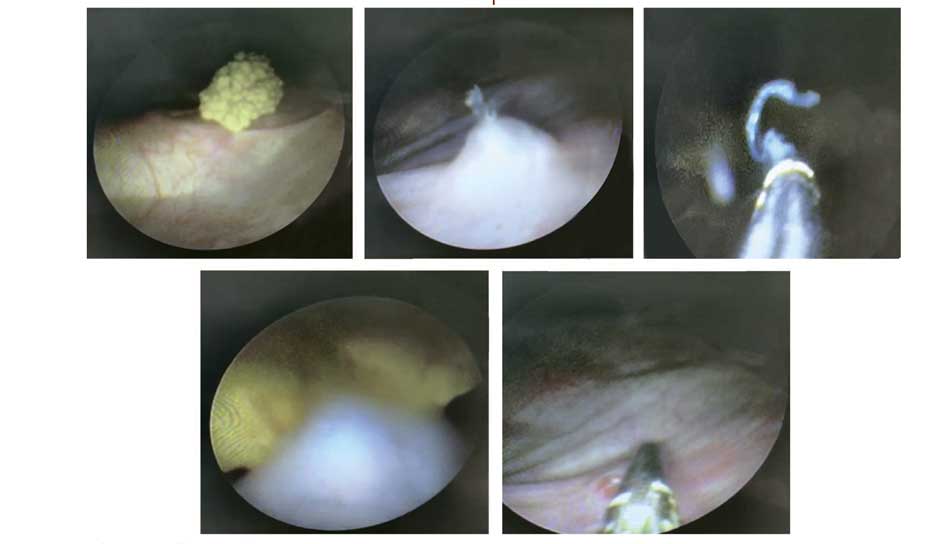
Рис. 7. Клиническое наблюдение. Пациент К. 10 л., интраоперационная картина эндоскопического удаления лигатурного камня и лигатуры в области реимплантируемого устья мочеточника
Fig. 7. Clinical observation. Patient K, 10 years old, intraoperative picture of endoscopic removal of a ligature stone and ligature in the area of the reimplanted ureteric orifice
Мальчик Д., 10 лет: через 5 лет после двухсторонней реимплантации мочеточника по методике Коэна впервые отмечено образование мочевых камней и самостоятельное их отхождение, до 4 эпизодов за 2,5 года. При инструментальном обследовании ни разу не был обнаружен камень почек или мочеточников. В среднем величина отходивших камней варьировалась от 0,5 до 1,5 см. В одном эпизоде при прохождении мочевого камня по уретре потребовалось вмешательство под наркозом в связи с обструкцией уретры и выраженным болевым синдромом. Продолжительное консервативное лечение, модификация питания и увеличение потребления воды не повлияли на количество рецидивов образования камней. При поступлении пациента в НИИ урологии и интервенционной радиологии с камнем, локализующимся у устья мочеточника, с подозрением на камень интрамурального отдела была визуализирована лигатура – источник рецидивирующего образования камней. При цистоскопии: камень был фиксирован к лигатуре, раздроблен, фрагмента отмыты из мочевого пузыря, а остатки лигатура с помощью эндоскопических щипчиков была удалена.
Во второй блок были отнесены и тактические ошибки, которые стали причинами повторных операций: выбор органосохраняющих операций у детей со значительном снижением функции почки по данным статической нефросцинтиграфии (функция менее 15-20% – гипоплазия почки) и с рецидивирующими инфекциями мочевых путей, ПМР. В группе данных пациентов проведенная хирургическая коррекция приводит к дальнейшему прогрессированию нефросклероза и отсроченным нефрэктомиям (рис. 8).
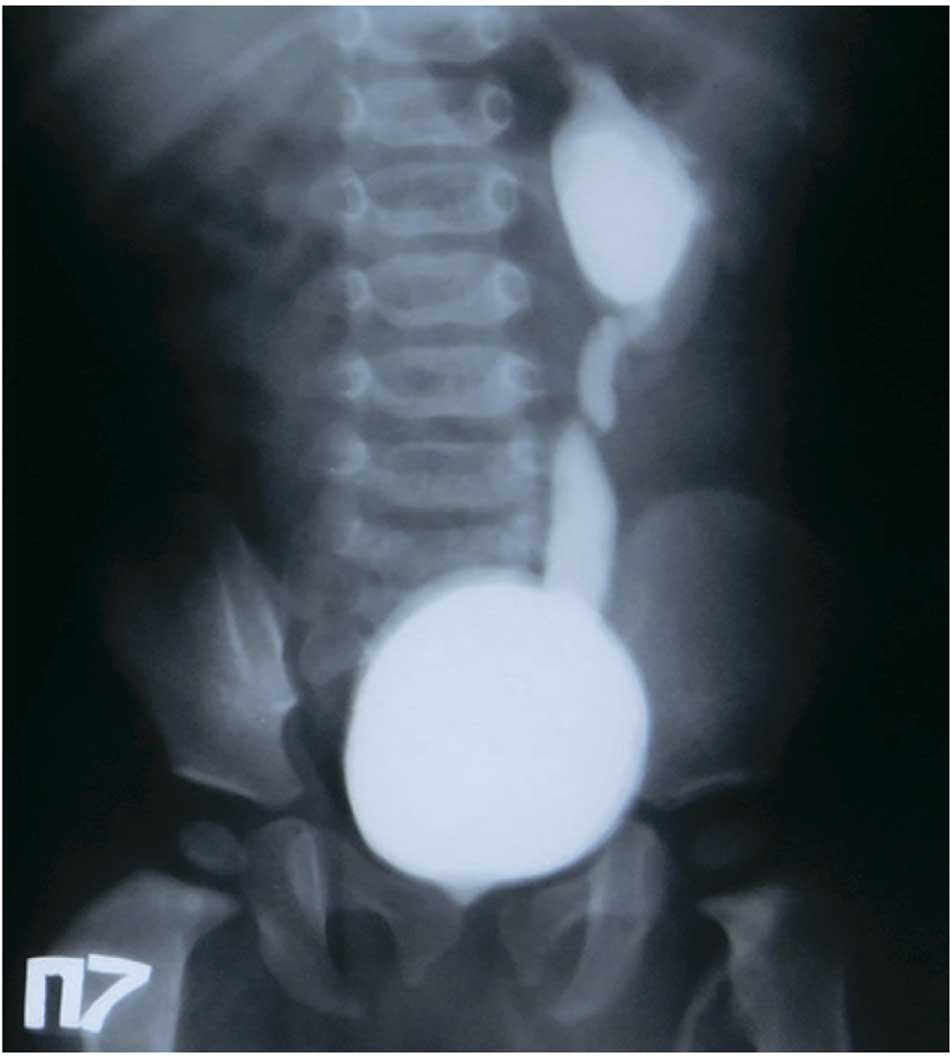
Рис. 8. Пациент Б. Ретроградная цистограмма с ПМР 5 степени в гипоплазированную левую почку после РМ с функцией по статической нефросцинтиграфии 16%
Fig. 8. Patient B. Retrograde cystogram with grade 5 VUR in the hypoplastic left kidney after UR with function according to static nephroscintigraphy of 16%
ЗАКЛЮЧЕНИЕ
Выполнение хирургической коррекции мегауретера при исходно широком (более 25 мм) коротком мочеточнике с несоблюдением правил формирования антирефлюксного механизма (формирование недостаточного по длине подслизистого туннелем) приводит к возникновению ПМР. Протяженная продольная пликация, фиксация мочеточника в двух точках (место входа мочеточника в мочевой пузырь и в области неоустья) используется для увеличения длины подслизистого туннеля и, при необходимости, в сочетании с операцией Боари, снижает риск формирования послеоперационного ПМР и рецидива мегауретера. Органосохраняющие операции при функции почки ниже 1517% с рецидивирующими инфекциями верхних мочевых путей очень сомнительны, так как прогрессирование нефросклероза в связи с наличием хронического очага инфекции в почечной паренхиме приводит в дальнейшем к выполнению нефроэктомии или геминефроэктомии. Адекватное дренирование верхних мочевых путей, контроль положения дренажа и надежная фиксация наружного дренажа остаются основой профилактики пиелонефрита в послеоперационном периоде. Понимание причин возможных осложнений реимплантации мочеточника позволяет более тщательно проводить этапы операции, обращать внимание на ключевые моменты и улучшать результаты коррекции мегауретера.
ЛИТЕРАТУРА
- Dekirmendjian A, Braga LH. Primary non-refluxing megaureter: analysis of risk factors for spontaneous resolution and surgical intervention. Front Pediatr 2019;7:126. https://doi.org/10.3389/fped.2019.00126.
- Braga LH, D'Cruz J, Rickard M, Jegatheeswaran K, Lorenzo AJ. The fate of primary nonrefluxing megaureter: a prospective outcome analysis of the rate of urinary tract infections, surgical indications and time to resolution. J Urol 2016;195(4Pt2):1300-5. https://doi.org/10.1016/j.juro.2015.11.049.
- Merlini E, Spina P. Primary non-refluxing megaureters. J Pediatr Urol 2005;1(6):409-17. https://doi.org/10.1016/j.jpurol.2005.04.007.
- Ranawaka R, Hennayake S. Resolution of primary non-refluxing megaureter: an observational study. J Pediatr Surg 2013;48(2):380-3. https://doi.org/10.1016/j.jpedsurg.2012.11.017.
- Gimpel C, Masioniene L, Djakovic N, Schenk JP, Haberkorn U, Tönshoff B, Schaefer F. Complications and long-term outcome of primary obstructive megaureter in childhood. Pediatr Nephrol 2010;25(9):1679-86. https://doi.org/10.1007/s00467-010-1523-0.
- Лебедев Д.А., Осипов И.Б., Комиссаров М.И., Сарычев С.А., Алексеева Л.А., Лифанова М.В, Нестерова Н.В. Лечение первичного обструктивного мегауретера у детей методом баллонной дилатации. Урология 2023;(1):76-82. [Lebedev D.A., Osipov I.B., Komissarov M.I., Sarychev S.A., Alekseeva L.A., Lifanova M.V., Nesterova N.V. Balloon dilation treatment of primary obstructive megaureter in children. Urologiya = Urologiia 2023;(1):76-82. (In Russan)] https://dx.doi.org/10.18565/urology.2023.1.76-82.
- Contini G, Mele E, Capozza N, Castagnetti M. Endoscopic balloon dilatation for the treatment of primary obstructive megaureter <24 months of age: Does the size of the balloon influence results? J Pediatr Urol 2023;19(2):198.e1-198.e9. https://doi.org/10.1016/j.jpurol.2022.11.021.
- Ortiz R, Burgos L, Fernández-Bautista B, Parente A, Ordóñez J, Angulo JM. Endoscopic balloon dilation of primary obstructive megaureter: is fluoroscopic guidance necessary? World J Urol 2023;41(10):2861-7. https://doi.org/10.1007/s00345-023-04572-z.
- Babu R. 'Mini reimplantation' for the management of primary obstructed megaureter. J Pediatr Urol 2016;12(2):103.e1-4. https://doi.org/10.1016/j.jpurol.2015.08.017.
- Babu R. Laparoscopic nipple invagination combined extravesical (NICE) reimplantation technique in the management of primary obstructed megaureter. J Pediatr Urol 2023;19(4):425.e1425.e6. https://doi.org/10.1016/j.jpurol.2023.03.023.
- Bustangi N, Kallas Chemaly A, Scalabre A, Khelif K, Luyckx S, Steyaert H, et al. Extravesical ureteral reimplantation following lich-gregoir technique for the correction of vesico-ureteral reflux retrospective comparative study open vs. laparoscopy. Front Pediatr 2018;6:388. https://doi.org/10.3389/fped.2018.00388.
- Babu R, Chandrasekharam VVS. A systematic review and meta-analysis comparing outcomes of laparoscopic extravesical versus trans vesicoscopic ureteric reimplantation. J Pediatr Urol 2020;16(6):783-789. https://doi.org/10.1016/j.jpurol.2020.09.006.
- Molinaro F, Nascimben F, Todesco C, Fusi G, Chiarella E, Planchamp T, et al. Robotic approach to the uretero-vesical junction in children: An international multicentric retrospective study. Int J Med Robot 2023;19(5):e2539. https://doi.org/10.1002/rcs.2539.
- Comez I, Ucar T, Telli O, Gunaydin B, Silay MS. Does previous endoscopic subureteric injection (STING) effect the outcomes of robot-assisted laparoscopic ureteral reimplantation surgery (RALUR) in children? J Pediatr Urol 2023;19(6):800.e1-800.e6. https://doi.org/10.1016/j.jpurol.2023.07.013.
- Рудин Ю.Э., Марухненко Д.В., Галицкая Д.А., Алиев Д.К., Лагутин Г.В., Вардак А.Б. Возможности пневмовезикоско-пического доступа при коррекции патологии уретеровезикального сегмента мочеточника и мочевого пузыря у детей. Урология 2021;(1):95-102. [Rudin Yu.E., Maruhnenko D.V., Galickaya D.A., Aliev D.K., Lagutin G.V., Vardak A.B. The opportunities of pneumovesicoscopic approach for correction of disorders of vesicoureteral junction in children. Urologiya = Urologiia 2021;(1):95-102. (In Russian)]. https://doi.org/10.18565/urology.2021.1.95-102.
- Rudin YE, Marukhnenko DV, Galitskaya DA, Aliev JK, Lagutin GV, Vardak AB. Pneumovesicoscopic ureteral reimplantation with intravesical tailoring of obstructive megaureter in pediatric patient. J Pediatr Urol 2022;18(2):224.e1-224.e8. https://doi.org/10.1016/j.jpurol.2021.12.004.
- Liu X, Liu J-H, Zhang D-Y, Hua Y, Lin T, Wei G-H., et al. Retrospective study to determine the short-term outcomes of a modified pneumovesical Glenn-Anderson procedure for treating primary obstructing megaureter. J Pediatr Urol 2015;11(5):266.e1-6. https://doi.org/10.1016/j.jpurol.2015.03.020.
- Hutflesz N, Boettcher M, Deeg S, Stein R, Wessel LM, Zahn K. Use of temporary double-J stent placement for children with congenital hydronephrosis: a long-term single-center cohort study. Urology 2023;172:165-169. https://doi.org/10.1016/j.urology.2022.11.024.
- Оганисян А.А., Врублевский А.С., Галкина Я.А., Валиев Р.Ю., Ахметжанов И.С., Врублевский С.Г., Врублевская Е.Н. Хирургическое лечение девочки 10 лет с мегауретером единственной почки. Детская хирургия 2022;26(3):177-83. [Oganisyan A.A., Vrublevskiy A.S., Galkina YA.A., Valiev R.YU., Ahmetzhanov I.S., Vrublevskiy S.G., Vrublevskaya E.N. A clinical case of surgical treatment of a 10-year-old girl with megaureter of the single kidney Detskaya Khirurgiya = Russian journal of Pediatric Surgery 2022;26(3):177-83. (In Russian)].
- Филатов А.И., Колесова Н.Н., Филатов И.А. Особенности лечения новорожденных при обструктивной уропатии. Педиатрический вестник Южного Урала 2012;(1):118-19. [Filatov A.I., Kolesova N.N., Filatov I.A. Features of treatment of newborns with obstructive uropathy. Pediatricheskiy vestnik Yuzhnogo Urala = Pediatric Bulletin of the South Ural 2012;(1):118-9. (In Russian)].
- Сальников В.Ю., Зоркин С.Н., Губарев В.И., Филинов И.В., Петров Е.И., Акопян А.И., и др. Современные аспекты малоинвазивного лечения первичного обструктивного мегауретера у детей. Детская хирургия 2016;20(3):155-9. [Sal'nikov V.YU., Zorkin S.N., Gubarev V.I., Filinov I.V., Petrov E.I., Akopyan A.I., et al. Modern aspects of low-invasive treatment of primary obstructive megaloureter in children. Detskaya Khirurgiya = Russian journal of Pediatric Surgery 2016;20(3):155-9. (In Russian)].
- Павлов А.Ю., Сабирзянова З.Р., Симонян Г.В. Тактика амбулаторного ведения пациентов с различными видами деривации мочи. Педиатрия. Журнал им. Г.Н. Сперанского 2016;95(5):58-62. [Pavlov A.Yu., Sabirzyanova Z.R., Simonyan G.V. Tactics of outpatient management of patients with various types of urine derivation. Pediatriya. Zhurnal im. G.N. Speranskogo= Pediatrics. Journal named after G.N. Speransky 2016;95(5):58-62. (In Russian)].
- Сальников В.Ю., Зоркин С.Н. Первый опыт применения рефлюксирующей реимплантации мочеточника в этапном лечении первичного обструктивного мегауретера у детей первого года жизни. Детская xирургия 2017;21(5):244-8. [Sal'nikov V.YU., Zorkin S.N. The first experience with refluxing ureteral reimplantation in the staged treatment of obstructive megaureter in children during the first year of life. Detskaya Khirurgiya = Russian journal of Pediatric Surgery 2017;21(5):244-8.(In Russian)].
- Сальников В.Ю., Зоркин С.Н. Оптимизация Тактики хирургического лечения первичного обструктивного мегауретера у детей первых лет жизни. Детская хирургия 2019;23(3):128-33. [Sal'nikov V.Yu., Zorkin S.N. Optimization of surgical treatment of primary obstructive megaureter in young children. Detskaya Khirurgiya = Russian journal of Pediatric Surgery 2019;23(3):128-33. (In Russian)].
- Arena S., Magno C., Montalto A.S., Russo T., Mami C., Baldari S., Romeo C., Arena F. Longterm follow-up of neonatally diagnosed primary megaureter: rate and predictors of spontaneous resolution. Scand J Urol Nephrol 2012;46(3):201-7. https://doi.org/10.3109/00365599.2012.662695.
- Calisti A, Oriolo L, Perrotta ML, Spagnol L, Fabbri R. The fate of prenatally diagnosed primary nonrefluxing megaureter: do we have reliable predictors for spontaneous resolution? Urology 2008;72(2):309-12. https://doi.org/10.1016/j.urology.2008.02.032.
- Di Renzo D, Aguiar L, Cascini V, Di Nicola M, McCarten KM, Ellsworth PI, et al. Long-term follow up of primary nonrefluxing megaureter. J Urol 2013;190(3):1021-6. https://doi.org/10.1016/j.juro.2013.03.008.
- Галицкая Д.А., Рудин Ю.Э. Совершенствование техники пневмовезикоскопического доступа для коррекции врожденных пороков развития нижних мочевых путей у детей. Экспериментальная и клиническая урология 2020;(3):154-60. [Galickaya D.A., Rudin Yu.E. Improving the technique of pneumovesicoscopic access for the correction of congenital malformations of the lower urinary tract in children. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and clinical urology 2020;(3):154-60. (In Russian)]. https://doi.org/10.29188/2222-8543-2020-12-3-154-160.
- Рудин Ю.Э., Марухненко Д.В., Галицкая Д.А., Лагутин Г.В., Вардак А.Б., Алиев Д.К. Современные возможности применения пневмовезикоскопического доступа при лечении урологической патологии у детей. Российский вестник детской хирургии, анестезиологии и реаниматологии 2020;10(S):137. [Rudin Yu.E., Marukhnenko D.V., Galitskaya D.A., Lagutin G.V., Vardak A.B., Aliev D.K. Modern possibilities of using pneumovesiscopic access in the treatment of urological pathology in children. Rossijskij vestnik detskoj hirurgii, anesteziologii i reanimacii = Russian journal of pediatric surgery, anesthesia and intensive care 2020;10(S):137. (In Russian)].
- Starr A. Ureteral plication. A new concept in ureteral tailoring for megaureter. Invest Urol 1979;17(2):153–158.
- Рудин Ю.Э., Галицкая Д.А. Способ эндовидеохирургического моделирования мочеточника при пневмовезиоксопической реимплантации у детей с мегауретером. Патент на изобретение № 2724870 от 25.06.2020. [Rudin Yu.E., Galitskaya D.A. Method for endovideosurgical modeling of the ureter during pneumovesioxopic reimplantation in children with megaureter. Patent for invention № 2724870 dated July 25,2020. (In Russian)].
- Патент № RU 2 813 946 С2 Российская Федерация, МПК A61B 17/00. Способ увеличения длины подслизистого туннеля при пневмовезикоскопической реимплантации мочеточника у детей с обструктивным мегауретером / Рудин Ю.Э., Галицкая Д.А., Каприн А.Д.; заявитель и патентообладатель Москва. Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации (ФГБУ «НМИЦ радиологии» Минздрава России). № 2 RU 2 813 946 С2; заявл. 06.07.2023; опубл. 21.08.2023 Бюл. № 24. [Patent No. RU 2 813 946 C2 Russian Federation, IPC A61B 17/00. Method for increasing the length of the submucosal tunnel during pneumovesiscopic reimplantation of the ureter in children with obstructive megaureter / Rudin Yu.E., Galitskaya D.A., Kaprin A.D.; applicant and patent holder Moscow. Federal State Budgetary Institution «National Medical Research Center of Radiology» of the Ministry of Health of the Russian Federation (FSBI «NMRIC of Radiology» of the Ministry of Health of the Russian Federation). No. 2 RU 2 813 946 C2; appl. 07/06/2023; publ. 08/21/2023 Bulletin. No. 24.
- Adam A. A Simple and Novel Method to Attain Retrograde Ureteral Access after Previous Cohen Cross-Trigonal Ureteral Reimplantation. Curr Urol 2017;11(1):42-47. https://doi.org/10.1159/000447193.







