ВВЕДЕНИЕ
Одним из перспективных развивающихся направлений терапии хронических заболеваний жизненноважных органов, в том числе почек, является стимуляция регенерации поврежденных клеточных и тканевых структур с использованием пересадки культивированных низкодифференцированных стволовых/ прогениторных клеток различного происхождения или с помощью терапии продуктами их секреции [1-3]. При этом накоплено много данных о том, что терапевтический эффект клеточной терапии реализуется преимущественно за счет секреции этими клетками комплекса биоактивных (сигнальных) молекул (низкомолекулярных белков и пептидов), регулирующих направленность клеточного метаболизма (цитокинов, факторов роста, стимуляторов ангиогенеза, антиапоптотических факторов и др.), получившего название «секретом» [4, 5]. Изучению эффективности терапии с использованием пептидов, выделенных из разных тканей, уделяется большое внимание как в зарубежных центрах [6], так и в России [7, 8]. Разработан целый ряд подобных препаратов. Показано, что на молекулярном уровне пептиды, составляющие активный компонент этих препаратов, взаимодействуют со специфическими сайтами ДНК, регулируют экспрессию генов, что обеспечивает направленную дифференцировку стволовых/прогениторных клеток с активацией синтеза специфических белков, стимулирующих клеточную пролиферацию и оказывающих антиапоптотическое и противовоспалительное действие [8].
К такому роду препаратов относится препарат Целлекс, представляющий собой белково-пептидный комплекс, хроматографически выделенный из нейрональных клеток головного мозга эмбрионов свиней. В ранее проведенных исследованиях нами было показано, что терапия этим препаратом крыс с индуцированной постишемической острой почечной недостаточностью и хронической почечной недостаточностью уменьшает выраженность функциональных расстройств и морфологических изменений в клубочках и канальцах почки, а также препятствует прогрессированию хронического патологического процесса [9, 10].
Учитывая, что источником комплекса сигнальных молекул, стимулирующих репаративные процессы, являются низкодифференцированные клетки функционально и анатомически незрелых органов, находящихся в состоянии развития, возникает вопрос, насколько возможно заменить технологически сложные методики выделения секретома стволовых/прогениторных клеток на трансплантацию неонатальных тканей, содержащих низкодифференцированные клетки в большом количестве.
Дополнительным аргументом целесообразности такой постановки вопроса является то, что, согласно современным представлениям для обеспечения функциональной активности стволовых/прогениторных клеток, необходимо сохранение специфического их микроокружения («ниши»), состоящего из внеклеточного матрикса и специфических сигнальных молекул, поддерживающих жизнеспособность, секреторную активность и направленную дифференцировку этих клеток, что имеет место при тканевой трансплантации [11-13]. Принцип формирования микрониши для стволовых клеток в настоящее время широко используется в исследованиях по созданию биоинженерных конструкций, имитирующих различные тканевые структуры с целью их последующей имплантации [14-16].
Сохранение специфического микроокружения может улучшить выживаемость клеток в чужеродном организме и продлить их функциональную активность при условии минимизации иммунологической реакции на аллогенные или ксеногенные ткани. Уменьшения иммунной реакции можно достичь путем пересадки аллогенной или ксеногенной ткани в иммунопривелегированные зоны, в том числе под капсулу почки, под белочную оболочку яичка, в переднюю камеру глаза [17, 18].
Учитывая эти данные, нами ранее были проведены эксперименты по изучению способности ткани неонатальных почек, полученных от новорожденных крысят (1-2 сутки после рождения), пересаженной под капсулу почек взрослых крыс после их ишемического/реперфузионного повреждения, в которых было показано, что при этом достигался выраженный нефропротективный эффект [19]. Возможность длительного выживания пересаженного под капсулу почки неонатального трансплантата была продемонстрирована нами в опытах по пересадке ткани неонатального яичка, как свежеудаленной, так и криоконсервированной. Пересаженная тестикулярная ткань не только сохраняла жизнеспособность в течение 6 месяцев, но и происходило развитие незрелой ткани с формированием полноценных семенных канальцев, а также зачатков придатка яичка и семявыносящего протока, что свидетельствовало о паракринной стимуляции органогенеза [20]. При трансплантации под белочную оболочку крипторхированного яичка пересаженная ткань неонатального тестикула стимулировала регенерацию семенных канальцев с восстановлением нарушенного сперматогенеза и активировала нарушенный синтез тестостерона [21].
Учитывая эти предпосылки, целью данного исследования явилась оценка нефропротективного действия трансплантации неонатальных тканей (почки и яичка), пересаженных под капсулу почки в резекционной модели хронической почечной недостаточности в сравнении с терапией протеомным ксеногенным секретомом нейрональных клеток эмбрионального головного мозга (препарат Целлекс). Использование неонатальных тканей разных органов обусловлено наличием данных об орган-неспецифическом действии их секретома [22-24].
МАТЕРИАЛЫ И МЕТОДЫ
Опыты проведены на 40 аутбредных крысах-самцах массой 260-290г. Животные содержались в стандартных условиях вивария с неограниченным доступом к полнорационному комбикорму для лабораторных грызунов (ООО «Лабораторкорм», Россия) и питьевой воде. Все манипуляции с животными выполняли в соответствии с Европейской конвенцией о гуманном обращении с животными, используемыми для экспериментов или в иных научных целях (ETS N 123) и Директивой Европейского парламента и Совета Европейского Союза 2010/63/ЕС о защите животных, использующихся для научных целей.
Для моделирования ХПН использовали «редукционную» модель. В условиях общей анестезии (внутрибрюшинное введение смеси Золетил-100 («Valdefarm», Франция) и Рометар («Биовета», Чешская республика) в соотношении 1:1 при расчетной дозе Золетила 15 мг/кг) выполняли правостороннюю нефрэктомию и резекцию верхнего и нижнего полюсов левой почки, в результате чего оставалось 18-25% функционирующей паренхимы органа.
Проведено 4 серии экспериментов по 10 животных в каждой серии. Первая серия служила контролем, и у этих крыс никаких лечебных мероприятий не проводили. Во 2-й серии животные получали терапию протеомным комплексом, хроматографически выделенным из нейрональных клеток головного мозга эмбрионов свиньи (ПКЭК), являющимся активным компонентом препарата «Целлекс», в виде двух десятидневных курсов с 10-дневным перерывом между ними с ежедневными подкожными инъекциями препарата в дозе 0,1 мл на крысу (0,1 мг действующего компонента). В 3-й и 4-й сериях сразу после моделирования ХПН под капсулу резецированной почки вводили ткань почки или яичка, полученных от новорожденных крысят (1-2 суток после рождения).
Субкапсулярную пересадку тканей выбрали в связи с тем, что эта локализация считается иммунологически привилегированной и уменьшает риск развития отторжения, которое неизбежно развивается при трансплантации аллогенного материала. При этом мы также учитывали, что, по ряду данных, эмбриональные, плодные и неонатальные ткани обладают меньшей иммуногенностью.
Органы новорожденных крысят удаляли в условиях эфирного наркоза в стерильных условиях. Эвтаназию проводили передозировкой паров эфира. Удаленные почки новорожденных крысят (3-я серия) после отмывания от крови измельчали до фрагментов порядка 0,5 мм и подвергали щадящей гомогенизации в физ. растворе в соотношении ткань/физ. раствор 1:1 до консистенции, позволяющей проходить через внутривенный катетер 18G Гомогенат вводили пункционно под капсулу почки в объеме 0,1 мл. Удаленные яички (4-я серия) освобождали от окружающей жировой ткани и с помощью микрохирургического инструментария, разрезали пополам и вводили в предварительно сформированный канал в подкапсулярном пространстве почки.
Оценку динамики биохимических показателей крови и мочи, характеризующих выраженность патологического процесса, оценивали через 7 дней после моделирования ХПН для характеристики ближайшей реакции на резко повышенную нагрузку на орган, а также через 1 и 2 месяца. Для получения биоматериала животных (по 5 крыс из разных серий на каждый срок) высаживали в обменные клетки на 24 часа для определения суточного диуреза, после чего животных подвергали эвтаназии передозировкой наркотических средств, брали пробы крови и удаляли почки для гистологического исследования. Биохимические показатели крови и мочи проводили на автоматическом анализаторе «ADVIA-2000» (Siemens). Определяли концентрацию креатинина, мочевины, натрия, кальция, а также активность ряда ферментов (аспартатаминотрансферазу (АСТ), щелочную фосфатазу (ЩФ), лактатдегидрогеназу (ЛДГ)). Из полученных данных с помощью общеизвестных формул рассчитывали такие функциональные показатели, как скорость клубочковой фильтрации (СКФ), канальцевая реабсорбция натрия и кальция, суточная экскреция креатинина и ферментов. Гистологическое исследование проводили по стандартной методике с окрашиванием препаратов гематоксилином и эозином.
Статистическую обработку цифрового материала выполняли с помощью компьютерных программ Excel и Statistica.10. Цифровые данные для каждой серии выражали в виде среднего значения и ошибки средней (M±m). Статистически значимыми различиями между сравниваемыми группами признавались при р<0,05.
РЕЗУЛЬТАТЫ
Все животные после выполнения моделирования ХПН выжили и были выведены из эксперимента в запланированные сроки.
У всех подопытных крыс развилась полиурия, выраженность которой значительно возрастала в течение 1-ого месяца примерно в равной степени во всех сравниваемых группах. При этом в опытах с пересадкой ткани неонатального яичка через 2 месяца выявилась достоверная тенденция к нормализации диуреза, тогда как в остальных группах существенной динамики не произошло (табл. 1). В отношении концентрации мочевины в крови выявлена несколько иная динамика: максимальный подъем в первые 7 суток (примерно в 2,5 раза) с тенденцией к постепенному снижению через 1 и 2 месяца. При этом более выраженное снижение уровня мочевины в крови через 1 и 2 месяца также выявлено в серии опытов, где производили трансплантацию неонатальной тестикулярной ткани. В отношении концентрации креатинина также обнаружено значительное (почти в 2 раза) увеличение этого показателя через 7 суток с некоторым его снижением через 1 месяц и стабилизацией через 2 месяца. При этом существенных различий между всеми группами не было обнаружено.
Таблица 1. Динамика диуреза и концентрации мочевины и креатинина в крови в сравниваемых группах
Table 1. Dynamics of diuresis and concentrations of urea and creatinine in the blood in the compared groups
| Показатель Parameter |
Норма Normal |
Вид терапии Therapy |
7 дней 7days |
1 мес. 1month | 2 мес. 2 months |
|---|---|---|---|---|---|
| Диурез (мл/сутки) Diresis (ml/day) | 11,3±0,2 | Контроль Control |
14,3±0,2 | 27,5±0,6 | 28,5±0,6 |
| ПКЭК PCEC |
15,1±0,3 | 29,5±0,7 | 24,7±0,5* | ||
| Ткань почки Renal tissue |
14,9±0,3 | 32,5±0,7 | 32,1±0,7* | ||
| Ткань яичка Testicular tissue |
13,9±0,2 | 28,5±0.6 | 20±0,4*** | ||
| Мочевина крови (мМ/л) Blood Urea (mM/L) | 6,8±0,2 | Контроль Control |
16,7±0,9 | 13,6±0,7 | 11,5±0,4 |
| ПКЭК PCEC |
13,9±0,7 | 13,3±0,4 | 10,5±0,3 | ||
| Ткань почки Renal tissue |
14,8±0,7 | 12,5±0,6 | 12,8±0,4 | ||
| Ткань яичка Testicular tissue |
13,9±0,6 | 9,6±0,5* | 8,3±0,4** | ||
| Креатинин крови (мкмоль/л) Blood creatinine (mcmol/L) | 60±2 | Контроль Control |
112±5 | 80±3 | 82±4 |
| ПКЭК PCEC |
98±3 | 81±2 | 73±3 | ||
| Ткань почки Renal tissue |
116±5 | 89±3 | 94±4 | ||
| Ткань яичка Testicular tissue |
103±4 | 80±2 | 76±4 |
Примечание. Различия достоверны по сравнению с контролем при: * p<0,05, **p<0,01, *** p<0,001
ПКЭК – протепомный комплекс эмбриональных клеток
Note. The differences are significant compared to the control at: * p<0.05, ** p<0.01, *** p<0.001
PCEC – proteomic complex of embryonic cells
Более информативными параметрами состояния функции поврежденного органа и влияния проводимой терапии являются расчетные показатели, такие как СКФ (оценка фильтрационной функции) и реабсорбция натрия и кальция (оценка функции почечных канальцев).
Через 7 дней после резекции почки значения СКФ резко снижались с 1,64±0,22 мл/мин в норме до 0,63-0,78 мл/мин в разных сериях. При этом степень снижения в разных сериях достоверно не различалась (рис. 1). Через 1 месяц в контроле и в сериях 2 и 3 отмечено умеренное возрастание этого показателя примерно в равной степени, тогда как в 4-й серии (трансплантации тестикулярной ткани) происходила полная нормализация СКФ. Через 2 месяца в контрольной серии СКФ вновь снижалась, а во всех опытных сериях она достоверно превышала контрольные значения, в том числе и в 4-й серии, где отмечено снижение СКФ по сравнению с 1-ым месяцем.
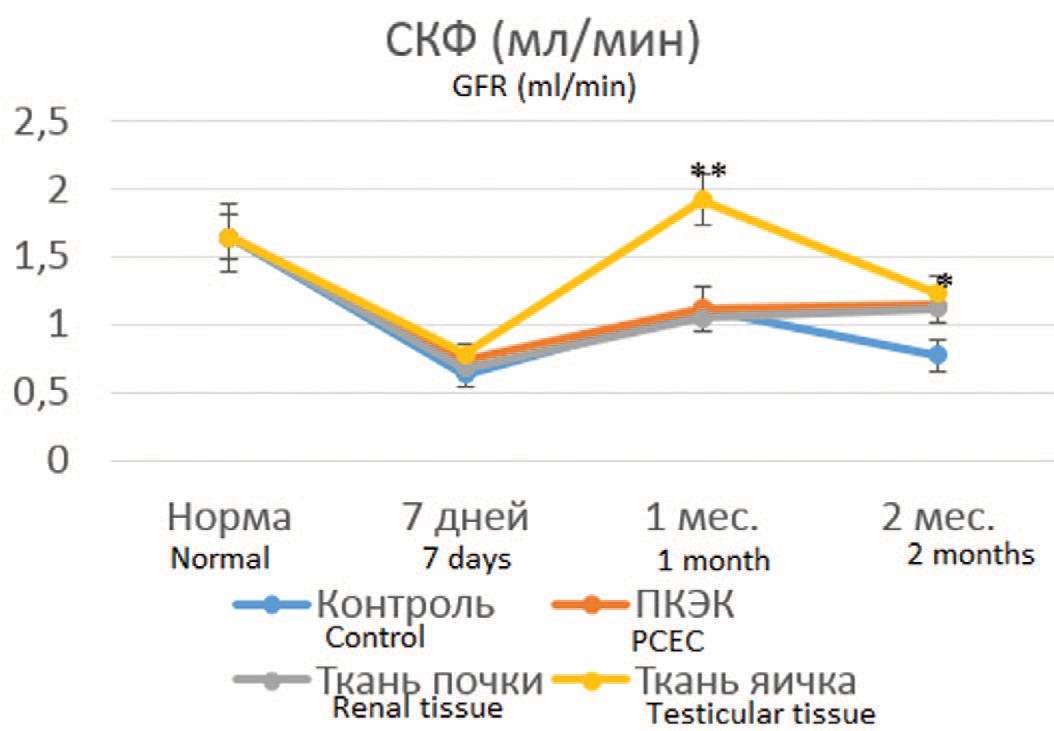
Рис. 1. Динамика СКФ в сравниваемых группах
Fig. 1. The dynamics of GFR in the compared groups
В отношении канальцевой реабсорбции натрия отмечалась похожая динамика (рис. 2). Через 7 дней после резекции почки во всех сериях происходило значительное уменьшение процентной доли реабсорбированного натрия без достоверных различий между контрольной и всеми опытными сериями (с 99,32% до 98,64%-98,84%). Через 1 и 2 месяца в контрольной серии отмечено незначительная тенденция к улучшению этого показателя, тогда как во всех опытных сериях через 1 месяц отмечено достоверное его возрастание, особенно выраженное в опытах с пересадкой тестикулярной ткани, где отмечена полная его нормализация, но ко 2-му месяцу различия между контрольной и опытным сериями сглаживались, оставаясь в серии с пересадкой тестикулярной ткани на достоверно более высоком уровне.
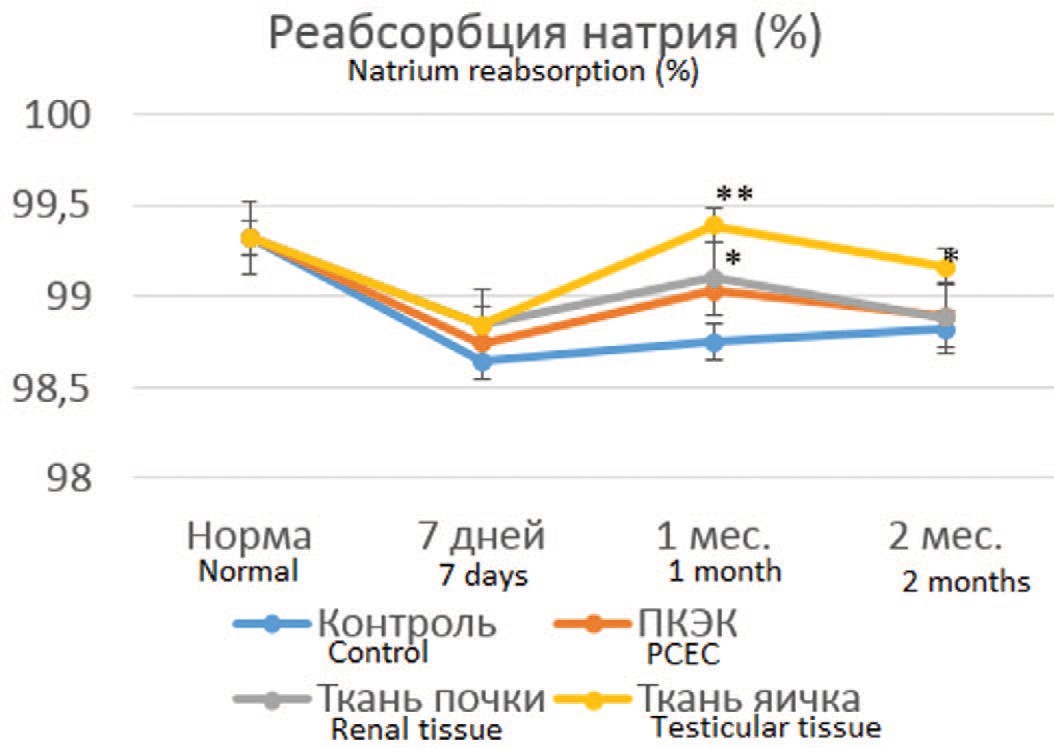
Рис. 2. Динамика канальцевой реабсорбции натрия (в процентах от профильт- рованного количества) в сравниваемых группах.
Fig. 2. Dynamics of tubular sodium reabsorption (as a percentage of the filtered amount) in the compared groups
Реабсорбция кальция в контрольной серии нарушалась более значительно, уменьшаясь к 7 суткам с 99,68% до 95,94%, тогда как во всех опытных сериях степень снижения оказалась достоверно менее выраженной (p<0,05 в опытах с пересадкой ткани неонатальной почки и p<0,001 в опытах с терапией ПКЭК и пересадкой ткани неонатальных тестикул) (рис. 3). Через 1 месяц выраженный положительный эффект сохранялся во всех опытных сериях (p<0,001), тогда как к 2 месяцам различия между контролем и опытными сериями исчезали за счет компенсации нарушений реабсорбции кальция в контрольных опытах.
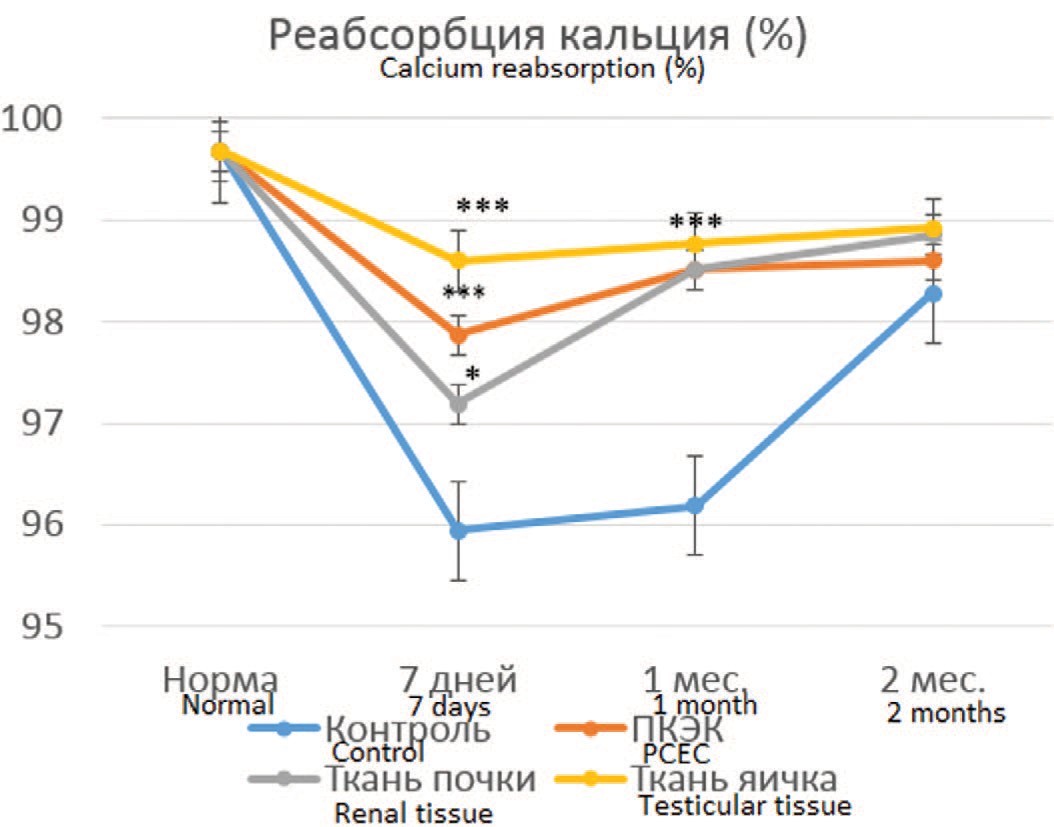
Рис. 3. Динамика канальцевой реабсорбции кальция (в процентах от профильт- рованного количества) в сравниваемых группах
Fig. 3. Dynamics of tubular calcium reabsorption (as a percentage of the filtered amount) in the compared groups
Хотя процентное отношение реабсорбированных катионов по отношению к общему количеству профильтрованного в клубочках натрия и кальция является стандартным показателем состояния канальцевого аппарата почки, тем не менее при выраженном повреждении клубочков со снижением СКФ (что мы наблюдали в наших опытах) нагрузка на канальцевый эпителий по реабсорбции электролитов может значительно различаться. Чем в большей степени снижена СКФ, тем меньшая масса катионов поступает в первичную мочу эти катионы могут реабсорбироваться, тогда как при повышенной нагрузке на эпителий канальцев процент реабсорбции может быть снижен, но общая масса сохраненных организмом электролитов может оставаться высокой. Поэтому мы также вычислили абсолютную массу реабсорбированного натрия и кальция, считая этот показатель более точным.
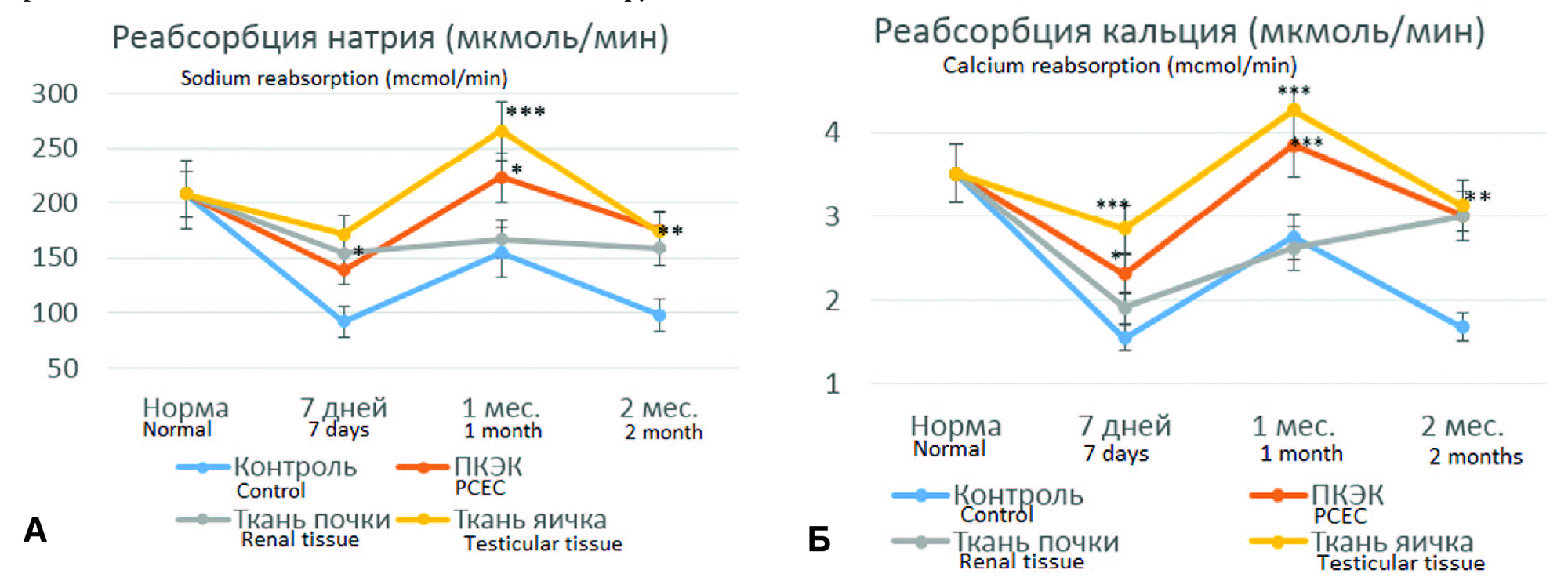
Рис. 4. Абсолютные значения скорости реабсорбции натрия (А) и кальция (Б)
в сравниваемых группах
Fig. 4. Absolute values of the reabsorption rates of sodium (A) and calcium (Б) in the compared groups
С этой целью мы рассчитали для каждой серии опытов количество профильтрованного в клубочках натрия и кальция, умножив показатель СКФ на концентрацию этих катионов в крови (фильтрационный заряд) и на процент реабсорбции этих катионов, и получили искомый показатель. Оказалось, что, действительно, имеются существенные различия между процентным и абсолютным количеством реабсорбированных натрия и кальция в сериях опытов (рис. 4А, Б). Если в контрольной серии процент реабсорбированных натрия и кальция с увеличением сроков наблюдения возрастал (более выраженно в отношении реабсорбции кальция), что можно было бы рассматривать как свидетельство компенсации дисфункции (фильтрационный заряд), и тем полнее канальцев, то в пересчете на абсолютное количество этих реабсорбированных катионов, после некоторого улучшения показателя через 1 месяц, к 2-м месяцам наступало снижение этих показателей, что, наоборот, указывает на декомпенсацию функциональных резервов эпителиальных клеток. При этом во всех опытных сериях уже через 7 дней после моделирования ХПН абсолютное количество реабсорбированного натрия в единицу времени оказалось достоверно больше, чем в контроле, что отличалось от процентных показателей, где различия оказались статистически недостоверными. Реабсорбция кальция в опытных сериях на этом сроке наблюдения оказалась выше контрольных значений при обоих вариантах расчета этого показателя. Через 2 месяца во всех опытных сериях показатель абсолютной реабсорбции как натрия, так и кальция, оказался достоверно выше контрольных значений, в отличии от процентного показателя, где различия с контролем оказались достоверными только для реабсорбции натрия в серии с пересадкой тестикулярной ткани.
Таким образом, все изучаемые варианты нефропротекции оказали существенный положительных эффект, уменьшив выраженность нарушения функции как клубочкового, так и канальцевого аппарата почки и предотвращая прогрессирование патологического процесса в отдаленном периоде.
Также важными показателями выраженности повреждения почки является активность внутриклеточных ферментов в крови, которая отражает масштабность цитолиза. Определение активности изученных ферментов в крови показало, что их активность, за исключением АЛТ, через 7 суток после резекции почки возрастала, что указывало на выраженное клеточное повреждение, вызванное острой функциональной перегрузкой органа. При этом достоверных различий между всеми сериями выявлено не было (табл. 2).
Таблица 2. Динамика активности ферментов в крови крыс в сравниваемых сериях (МЕ/л)
Table 2. Dynamics of enzyme activity in the blood of rats in the compared series (IU/l)
| Вид терапии Therapy |
Норма Normal |
7 дней 7days |
1 мес. 1month | 2 мес. 2 months |
|---|---|---|---|---|
| АСТ / AST | ||||
| Контроль Control |
68±14 | 140±25 | 85±14 | 90±15 |
| ПКЭК PCEC |
123±19 | 87±16 | 78±12 | |
| Ткань почки Renal tissue |
165±22 | 86±17 | 83±14 | |
| Ткань яичка Testicular tissue |
109±19 | 38±11* | 73±11 | |
| АЛТ / ALT | ||||
| Контроль Control |
36±4 | 34±3 | 58±5 | 42±5 |
| ПКЭК PCEC |
32±3 | 37±3* | 38±3 | |
| Ткань почки Renal tissue |
45±4 | 40±4 | 32±3 | |
| Ткань яичка Testicular tissue |
34±2 | 38±2* | 27±2* | |
| ЩФ / Alcaline phosphatase | ||||
| Контроль Control |
169±29 | 256±36 | 172±27 | 190±22 |
| ПКЭК PCEC |
218±31 | 253±33 | 180±19 | |
| Ткань почки Renal tissue |
315±44 | 226±30 | 158±18 | |
| Ткань яичка Testicular tissue |
197±29 | 155±19 | 121±14* | |
| ЛДГ / LDH | ||||
| Контроль Control |
320±33 | 569±41 | 378±31 | 928±122 |
| ПКЭК PCEC |
517±39 | 313±28 | 339±41** | |
| Ткань почки Renal tissue |
673±54 | 402±38 | 370±48** | |
| Ткань яичка Testicular tissue |
497±36 | 548±41 | 339±37** | |
Через 1 месяц активность всех ферментов снижалась до субнормального или нормального уровня, причем в опытах с пересадкой ткани неонатальной почки активность АЛТ снижалась более значительно, чем в контрольной серии, а в опытах с пересадкой тестикулярной ткани достоверные различия с контролем получены в отношении степени снижения АСТ и АЛТ. Через 2 месяца в контрольной группе опытов происходило резкое повышение активности ЛДГ в крови, тогда как активность остальных ферментов оставалась на значениях, близких к норме. Во всех опытных сериях активность ЛДГ была на уровне нормальных значений и достоверно отличалась от значений контрольных опытов (p<0,01). При определении активности остальных изученных ферментов достоверные различия с контролем получены лишь в опытах с пересадкой тестикулярной ткани в отношении АЛТ и ЩФ.
Для определения состояния пересаженной неонатальной ткани и прилегающей паренхимы почки провели гистологическое исследование удаленного органа через 1 и 2 месяца после трансплантации. Оказалось, что в опытах с трансплантацией гомогената ткани неонатальной почки происходила прогрессирующая деструкция пересаженной ткани. Через 1 месяц сохранялись лишь единичные группы почечных канальцев в разной степени деградации (рис. 5А). Трансплантат отделялся от паренхимы почки выраженной капсулой. Ткань почки, прилежащей к трансплантату, выглядела малоизмененной при умеренной степени воспалительной инфильтрации интерстиция. Через 2 месяца происходила полная деструкция трансплантата, но при этом сохранялись единичные жизнеспособные канальцы (рис. 5Б). В ткани почки, непосредственно прилежащей к трансплантату, наблюдалась умеренно выраженная воспалительная инфильтрация. Эпителий почечных канальцев был в состоянии дистрофии разной степени выраженности. В более отдаленной зоне гистологическая картина была близка к норме.
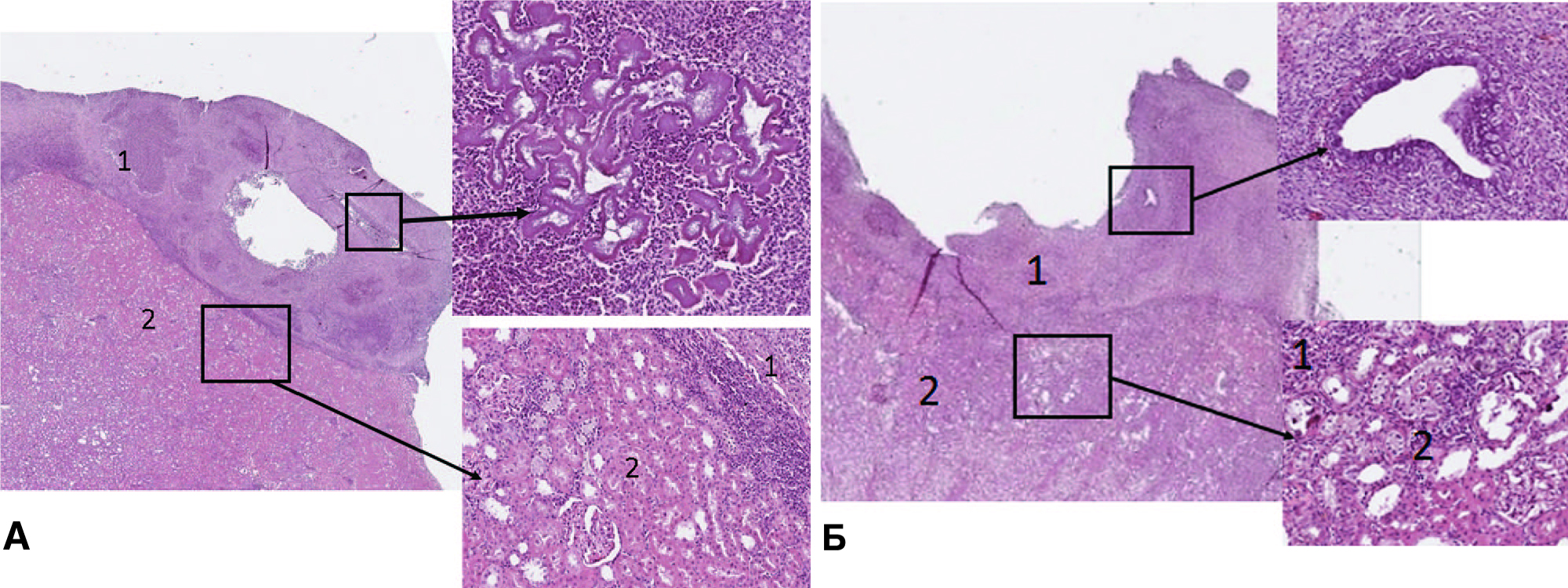
Рис. 5. Почка с трансплантатом неонатальной почечной ткани. А – через 1 месяц после пересадки. Субтотальная деструкция с массивной воспалительной инфильтрацией и с сохранившимися отдельными группами дистрофически измененных канальцев. Б – через 2 месяца после пересадки. Полная деструкция трансплантата с единичным сохранившимся почечным канальцем. Окраска гематоксилином и эозином. 1 – трансплантат неонатальной ткани почки. 2 – ткань почки реципиента. Ув. 60х. В выделенных фрагментах – Ув. 100х
Fig. 5. Kidney from neonatal renal tissue transplants. A – 1 month after the transplant. Subtotal destruction with massive inflammatory infiltration and with preserved separate groups of dystrophically altered tubules. B – 2 months after the transplant. Complete destruction of the graft with a single preserved renal tubule. H&E. 1 – neonatal kidney tissue transplant. 2 – recipient's kidney tissue. х 60. In the selected fragments – x 100
Совершенно иная гистологическая картина выявлена при трансплантации ткани неонатального яичка. Через 1 месяц под капсулой почки выявлены группы жизнеспособных семенных канальцев на ранних стадиях развития с сохраненным сперматогенным эпителием с наличием диффузного воспалительного инфильтрата в окружающей интерстициальной ткани. При этом прилежащая ткани почки выглядит практически нормальной (рис. 6А). Через 2 месяца выявляются множественные семенные канальцы с признаками активного сперматогенеза при незначительно выраженной инфильтрации интерстиция. Прилегающая к трансплантату ткань почки выглядит гистологически нормальной при полнокровии кровеносных сосудов (рис. 6Б).
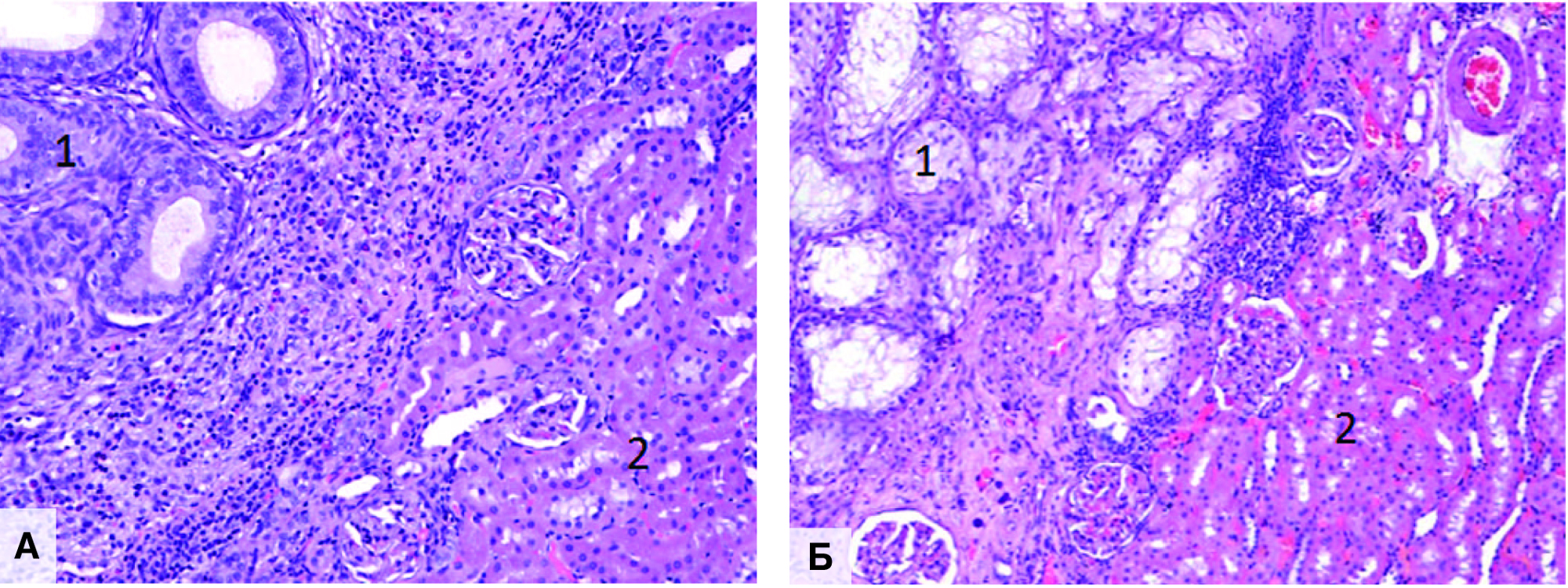
Рис. 6. Почка с трансплантатом ткани неонатального яичка. А – через 1 месяц после пересадки. Б – через 2 месяца после пересадки. 1 – трансплантат неонатального яичка. 2 – ткань почки реципиента. Окраска гематоксилином и эозином. Ув. 100х
Fig. 6. The kidney with a neonatal testicular tissue transplant. A – 1 month after the transplant. B – 2 months after the transplant. 1 – neonatal testicular transplant. 2 – recipient's kidney tissue. H&E. x 100
Таким образом, если пересаженная неонатальная почечная ткань подвергается отторжению и деструкции, то неонатальная тестикулярная ткань длительное время сохраняет не только жизнеспособность, но и способность к дальнейшему развитию.
ОБСУЖДЕНИЕ
Возможности «бесклеточной терапии» продуктами секреции стволовых/прогениторных клеток (секретомом) для восстановления функции органов, в том числе почек, при их хронических заболеваниях привлекают все большее внимание исследователей [3, 4]. Секретом низкодифференцированных клеток можно выделять из среды культивирования этих клеток, а также непосредственно из тканей эмбрионов и плодов, что является более эффективным. Учитывая это, сами плодные ткани можно рассматривать как потенциальный инструмент паракринной стимуляции клеточной регенерации при их пересадке в организм при условии сохранения их жизнеспособности.
В последние две декады 20-го века трансплантация тканей, полученных от эмбрионов и плодов, рассматривалась как потенциальный метод лечения различных заболеваний [25]. Хотя в то время только начиналось изучение роли стволовых/прогениторных клеток в органогенезе и регенерации тканей, тем не менее были получены данные о способности клеток плодных тканей к активной регенерации, направленной дифференцировке, способности стимулировать неангиогенез, секретировать нейротрофические факторы [26]. Проводились исследования по трансплантации плодной ткани поджелудочной железы и выделенных из нее островков Лангерганса, как в эксперименте, так и в клинической практике больным диабетом [27-30], пересаживали фрагменты ткани плодной печени для стимуляции гемопоэза или коррекции метаболических нарушений, связанных с дисфункцией печени [31, 32], микрофрагменты надпочечников или участков головного мозга для лечения болезни Паркинсона [33, 34], трансплантации ткани неонатальных яичников [35], тестикулярной ткани [36] и ткани гипофиза [37]. При этом авторы отмечали положительный эффект, однако в большинстве случаев он носил относительно кратковременный характер в связи с тем, что, хотя плодные ткани обладают меньшей иммуногенностью, чем ткани взрослого организма, тем не менее они все же со временем подвергаются отторжению и деструкции [38].
В 21-м веке в связи с развитием клеточных технологий и изменением юридических норм возможности использования тканей эмбрионов и плодов интерес к тканевой трансплантации плодных тканей существенно уменьшился, но все же появляются публикации по этой теме, в частности, по трансплантации овариальной ткани [39], композитных сосудистых комплексов [40], фрагментов головного мозга [41].
В связи с этим мы посчитали важным сравнить нефропротективное действие препарата Целлекс, активным компонентом которого является секретом нейрональных клеток эмбрионов свиньи (ПКЭК), и эффект от трансплантации органоспецифичной (почка) и орган-неспецифичной (тестикул) плодной ткани, пересаженной в иммунопривилегированную зону (под капсулу почки), что должно было способствовать длительному выживанию клеток трансплантата.
Результаты проведенных экспериментов показали, что такая трансплантация ткани неонатальных органов оказывает не менее выраженный нефропротективный эффект при экспериментально вызванной ХПН, что и терапия ПКЭК, а трансплантация ткани неонатального тестикула приводит к даже более значительному улучшению функции почки. На наш взгляд, более раннее улучшение всех показателей функции поврежденной почки в опытах с пересадкой ткани неонатального яичка может быть связано с действием в ранний период секретируемого трансплантатом тестостерона, обладающего, как известно, вазодилатирующими свойствами [42, 43], что может улучшать внутрипочечную гемодинамику, и, как следствие, увеличивать СКФ. В более отдаленном периоде за счет регулирующих эндокринных механизмов этот эффект нивелируется.
Проведенное гистологическое исследование показало, что неонатальный почечный трансплантат через 1 месяц подвергался субтотальной деструкции с сохранением отдельных групп жизнеспособных почечных канальцев, а через 2 месяца выявлялись лишь единичные жизнеспособные канальцы с сохраненной эпителиальной выстилкой. Однако при этом нефропротективный эффект пересадки сохранялся на протяжении длительного срока даже с тенденцией к его возрастанию к 2-месячному сроку наблюдения. Это может свидетельствовать, что стимуляция репаративных процессов в почке, индуцированная продуктами секреции неонатального трансплантата, может продолжаться и после прекращения их влияния вследствие гибели трансплантата за счет происшедшей перестройки клеточного метаболизма. При пересадке ткани неонатального яичка трансплантат длительно сохранял свою жизнеспособность, что может объяснять более выраженный нефропротективный эффект, выявленный через 1 месяц после пересадки за счет непрерывной поступления сигнальных молекул, стимулирующих регенерацию почечных структур. Некоторое снижение функциональных показателей к 2-месячному сроку может быть обусловлено как со снижением стимуляции в связи с более зрелой дифференцировкой структур трансплантата, так и с включением собственных механизмов регуляции метаболизма в клетках почки. В опытах с терапией крыс ПКЭК также наблюдали, что нефропротективный эффект сохранялся после прекращения терапии, продолжающейся в течение 1 месяца, и возрастал к 2-месячному сроку.
То есть, при всех вариантах терапии, использованных в наших экспериментах, индукция метаболической перестройки в клетках поврежденной почки проводит к стойкой активации компенсаторно-приспособительных процессов, обеспечивающих улучшение и стабилизацию функцию органа после прекращения терапевтического воздействия, что предупреждает прогрессирование ХПН.
Деструкция пересаженной ткани неонатальной почки может быть связана как с гипоксическим повреждением, поскольку почка плода уже участвует в образовании мочи, что является энергозатратным процессом и требует адекватной оксигенации ткани, так и за счет развивающегося иммунного отторжения в связи с иммуногенностью почечной ткани [44]. В то же время, эндокринные ткани, к которым можно отнести плодный тестикул, состоящий преимущественно из интерстииальной ткани, содержащей гормон-продуцирующе клетки Лейдига и ограниченное количество незрелых семенных канальцев, в которых пока отсутствует сперматогенез, более устойчивы к гипоксии и менее иммуногенны (эпителий семенных канальцев защищен от иммунного конфликта клетками Сертоли). Это позволяет длительно сохранять жизнеспособность тестикуляного трансплантата и способность секретировать клетками биологически активные субстанции.
Гистологическое исследование также показало, что вокруг некротизированного почечного трансплантата через 1 месяц формировалась выраженная фиброзная капсула, а в прилежащих отделах ткани собственной почки выявляли выраженный воспалительный инфильтрат, который становился более интенсивным через 2 месяца после пересадки. В зоне воспалительного инфильтрата почечные канальцы находились в состоянии дистрофии разной степени выраженности. При этом в остальной части почечной паренхимы воспалительных изменений не выявляли, а почечные структуры выглядели малоизмененными. В опытах с пересадкой тестикулярной ткани воспалительные изменения были значительно менее выражены, а паренхима почки выглядела нормальной даже в участках, прилегающих к трансплантату. Эти данные свидетельствуют, что даже полная деструкция трансплантата приводит лишь к локальному воспалительному эффекту, не оказывая существенного негативного влияния на орган, также как и при сохранении жизнеспособности пересаженной ткани.
ЗАКЛЮЧЕНИЕ
Проведенное исследование показало, что трансплантация неонатальной ткани (почки, яичка) позволяет предотвратить прогрессирование ХПН в сопоставимой степени (а по некоторым параметрам в большей степени) с терапией ПКЭК. При этом подтвердился тезис об орган-неспецифичном действии продуктов секреции низкодифференированных клеток в отношении стимуляции регенерации и восстановления функции поврежденных органов.
ЛИТЕРАТУРА
- Li JS, Li B. Renal injury repair: how about the role of stem cells. Adv Exp Med Biol 2019;1165:661-70. https://doi.org/10.1007/978-981-13-8871-2_32.
- Rota C, Morigi M, Cerullo D, Introna M, Colpani O, Corna D, et al. Therapeutic potential of stromal cells of non-renal or renal origin in experimental chronic kidney disease. Stem Cell Res Ther 2018;9(1):220. https://doi.org/10.1186/s13287-018-0960-8.
- Golle L, Gerth HU, Beul K, Heitplatz B, Barth P, Fobker M, et al. Bone marrow-derived cells and their conditioned medium induce microvascular repair in uremic rats by stimulation of endogenous repair mechanisms. Sci Rep 2017;7(1):9444. https://doi.org/10.1038/s41598-017-09883-x.
- Beer L, Mildner M, Ankersmit HJ. Cell secretome based drug substances in regenerative medicine: When regulatory affairs meet basic science. Ann TranslMed 2017;5:170. https://doi.org/10.21037/atm.2017.03.50.
- Xia J, Minamino S, Kuwabara K, Arai S. Stem cell secretome as a new booster for regenerative medicine. Biosci Trends 2019;13(4):299-307. https://doi.org/10.5582/ bst.2019.01226.
- Chouaib B, Haack-Sørensen M, Chaubron F, Cuisinier F, Collart-Dutilleul PY. Towards the standardization of mesenchymal stem cell secretome-derived product manufacturing for tissue regeneration. Int J Mol Sci 2023;24(16):12594. https://doi.org/10.3390/ijms241612594.
- Пушкарь Д.Ю., Гамидов С.И., Гомберг В.Г., Гураль А.К., Евдокимов М.С., Касян Г.Р., и соавт. Везустим: первые результаты применения в рамках клинического исследования у пациентов с гиперактивным мочевым пузырем. Экспериментальная и клиническая урология 2020;(3):34-5. [Pushkar D.Ju., Gamidov S.I., Gomberg V.G., Gural A.K., Evdokimov M.C., Kasyan G.R., et al. Vesustim: the first results of use in a clinical trial in patients with an overactive bladder. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2020;(3):34-5. (In Russian)]. https://doi.org/10.29188/2222-8543-2020-12-3-34-35
- Хавинсон В.Х. Лекарственные пептидные препараты: прошлое, настоящее, будущее. Клиническая медицина 2020;98(3):165-77. [Khavinson V.H. Medicinal peptide preparations: past, present, future. Klinicheskaya meditsina = Clinical medicine 2020;98(3):165-77. (In Russian)].
- Кирпатовский В.И., Сивков А.В., Голованов С.А., Дрожжева В.В., Самойлова С.И., Рабинович Э.З., и соавт. Профилактика развития острой постишемической почечной недостаточности с использованием белково-пептидного комплекса эмбриональной ткани. Экспериментальная и клиническая урология 2019;(3):32-9. [Kirpatovsky V.I., Sivkov A.V., Golovanov S.A., Drozhzheva V.V., Samoilova S.I., Rabinovich E.Z., et al. Prevention of the development of acute post-ishemic renal insufficiency using a protein-peptide complex of embryonal tissue. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2019;(3):32-9. (In Russian)]. https://doi.org/10.29188/2222-8543-2019-11-3-32-39.
- Кирпатовский В.И., Сивков А.В., Соколов М.А., Голованов С.А., Дрожжева В.В., Синюхин В.Н., и соавт. Терапия ксеногенным протеомным комплексом из эмбриональных клеток головного мозга тормозит прогрессирование экспериментально вызванной хронической почечной недостаточности. Экспериментальная и клиническая урология 2023;16(3):26-37. [Kirpatovsky V.I., Sivkov A.V., Sokolov M.A., Golovanov S.A., Drozhzheva V.V., Sinyukhin V.N., et al. Therapy with xenogenic proteomic complex from embryonic brain cells inhibits the progression of experimentally induced chronic renal failure. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2023;16(3):26-37. (In Russian)]. https://doi.org/10.29188/2222-8543-2023-16-3-26-37
- Hicks MR, Pyle AD. The emergence of the stem cell niche. Trends Cell Biol 2023;33(2):112-23. https://doi.org/10.1016/j.tcb.2022.07.003.
- . Hurwitz SN, Jung SK, Kurre P. Hematopoietic stem and progenitor cell signaling in the niche. Leukemia 2020;34(12):3136-48. https://doi.org/10.1038/s41375-020-01062-8.
- Chacón-Martínez CA, Koester J, Wickström SA Signaling in the stem cell niche: regulating cell fate, function and plasticity. Development 2018;145(15):dev165399. https://doi.org/10.1242/dev.165399.
- Cosgriff-Hernandez E, Timmins LH. Model-directed design of tissue engineering scaffolds. ACS Biomater Sci Eng 2022;8(11):4622-4. https://doi.org/10.1021/ acsbiomaterials.1c01386.
- Hassanzadeh P, Atyabi F, Dinarvand R. Tissue engineering: Still facing a long way ahead. J Control Release 2018;279:181-97. https://doi.org/10.1016/ j.jconrel.2018.04.024.
- Zhang X, Zhang Y. Tissue engineering applications of three-dimensional bioprinting. Cell Biochem Biophys 2015;72(3):777-82. https://doi.org/10.1007/ s12013-015-0531-x.
- Janeway CA Jr, Travers P, Walport M, Shlomchik MJ. Immunobiology: the immune system in health and disease. 6th Edition. 2004. Garland Science. 848 p.
- Куликов А.В., Кирпатовский И.Д., Куликов Д.А., Архипова Л.В., Смирнова Г.Н., Куликова П.А. Пересадка алло- и ксеногенных эндокринных тканей в иммунопривилегированные области организма. Клеточная трансплантология и тканевая инженерия 2013;8(3):36. [Kulikov A.V., Kirpatovsky I.D., Kulikov D.A., Arkhipova L.V., Smirnova G.N., Kulikova P.A. Transplantation of allo- and xenogenic endocrine tissues into immunoprivileged areas of the body. Kletochnaya transplantologia I tkanevaa inzheneria = Cellular Transplantation and Tissue Engineering 2013;8(3):36. (In Russian)].
- Кирпатовский В.И., Сивков А.В., Голованов С.А., Дрожжева В.В., Фролова Е.В. Сравнительная характеристика протективного действия терапии белково-пептидным секретомом эмбриональной ткани и трансплантации ткани неонатальной почки при острой постишемической почечной недостаточности. Экспериментальная и клиническая урология 2020;(1):28-35. [Kirpatovskiy V.I., Sivkov A.V., Golovanov S.A., Drozhzheva V.V., Frolova E.V. Comparative analisis of the protective therapectic effect between embryonic tissue secretome – mixture proteins and peptides – and transplantation of neonatal kidney tissue in acute post-ishemic renal failure. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2020;(1):28-35. (In Russian)]. https://doi.org/10.29188/2222-8543-2020-12-1-28-35
- Кирпатовский В.И., Ефремов Г.Д., Фролова Е.В. Эктопический органогенез при аллотрансплантации ткани свежеудаленного или криоконсервированного неонатального яичка под капсулу почки крыс.
Бюллетень экспериментальной биологии и медицины 2018;166(8):230-5. [Kirpatovskiy V.I., Efremov G.D., Frolova E.V. Ectopic organogenesis during allotransplantation of freshly removed or cryopreserved neonatal testis tissue under the capsule of a kidney of rats. Byulleten' eksperimental'noy biologii i meditsiny = Bulletin of Experimental Biology and Medicine 2018;166(8):230-5. (In Russian)].
- Кирпатовский В.И., Ефремов Г.Д., Фролова Е.В., Кудрявцева Л.В. Стимуляция сперматогенеза и синтеза тестостерона путем аллотрансплантации неонатальной тестикулярной ткани под белочную оболочку крипторхированного яичка. Бюллетень экспериментальной биологии и медицины 2018;166(10):495-501. [Kirpatovskiy V.I., Efremov G.D., Frolova E.V., Kudrjavtseva L.V. Stimulation of spermatogenesis and synthesis of testosterone by allotransplantation of neonatal testicular tissue under the casing of the cryptorchid testis. Byulleten' eksperimental'noy biologii i meditsiny = Bulletin of Experimental Biology and Medicine 2018;166(10):495-501. (In Russian)].
- Sagaradze G, Monakova A, Efimenko A. Potency assays for mesenchymal stromal cell secretome-based products for tissue regeneration. Int J Mol Sci 2023;24(11):9379. https://doi.org/10.3390/ijms24119379.
- Rahimi B, Panahi M, Saraygord-Afshari N, Taheri N, Bilici M, Jafari D, Alizadeh E. The secretome of mesenchymal stem cells and oxidative stress: challenges and opportunities in cell-free regenerative medicine. Mol Biol Rep 2021;48(7):5607-19. https://doi.org/10.1007/s11033-021-06360-7.
- Harrell CR, Fellabaum C, Jovicic N, Djonov V, Arsenijevic N, Volarevic V. Molecular mechanisms responsible for therapeutic potential of mesenchymal stem cell-derived secretome. Cells 2019;8(5):467. https://doi.org/10.3390/ cells8050467.
- Fine A. Transplantation of fetal cells and tissue: an overview. Can Med Assoc J 1994;151(9):1261-68.
- Edwards RG. Fetal Tissue Transplants in Medicine, Cambridge University Press, Cambridge, England, 1992. 366 p.
- Shumakov V.I., Shal'nev B.I., Blyumkin V.N., Shaletskii N.N., Babikova R.A., Danilov M.A. Heterografting cultures of human pancreatic islet cells in rats with experimental diabetes mellitus. Bulletin Of Experimental Biology And Medicine 1980;89(1):63-5.
- Groth CG, Andersson A, Bjorken C, Gunnarsson R, Hellerström C, Lundgren G, et al. Transplantation of fetal pancreatic microfragments via the portal vein to a diabetic patient. Diabetes 1980;29(suppl 1):80-3.
- Hu YF, Zhang H, Zhang HD, Shao AH, Li LX, Zhao BH. Clinical researches on islet transplantation in 20 patients with insulin-dependent diabetes mellitus. Acta Acad Med Wuhan 1984;4(3):145-51. https://doi.org/10.1007/BF02856867.
- Розенталь Р. Л., Штифт А. К., Ильинский И. М., Бицанс Я.Б., Фомина О.А. Лечение лабильных форм сахарного диабета трансплантацией культур островковых клеток поджелудочной железы. Проблемы эндокринологии 1988;34(1):10-2 [Rozental' RL, Shtift AK, Il'inskiĭ IM, Bitsans Ia.B, Fomina O.A. Treatment of labile forms of diabetes mellitus by transplantation of cultured pancreatic islet cells. Problemi Endocrinologii = Problems of Endocrinology 1988;34(1):10-2. (In Russian)].
- Harousseau JL, Devergie A, Lawler S, Gluckman E, Schaison G. Implant of fetal liver in severe bone marrow aplasia. Nouv Rev Francaise D'Hemato- logie 1980;22(Suppl.):572.
- Zhu RP, Lin XY, Wang JT. Fetal hepatocellular suspension transfusion (FHST) in the treatment of chronic active hepatitis B. Chung Hua Nei Ko Tsa Chih 1990;29:419-21.
- Hitchcock ER, Clough CG, Hughes RC, Kenny BG. Transplantation in Parkinson's disease: stereotactic implantation of adrenal medulla and foetal mesencephalon. Acta Neurochir Suppl (Wieni) 1988;46:48-50. https://doi.org/10.1007/978-3-7091-9029-6_11.
- Савельев С.В. Трансплантация эмбрионального головного мозга. Архив патологии 1992;54(11):43-6. [Saveliev S.V. Transplantation of the embryonic brain. Arkhiv Patologii = Archive of Pathology 1992;54(11):43-6. (In Russian)].
- Carroll J, Gosden RG. Transplantation of frozen-thawed mouse primordial follicles. Hum Reprod 1993;8(8):1163-7. https://doi.org/10.1093/oxfordjournals.humrep.a138221.
- Кирпатовский И.Д., Дендеберов Е.С. Способ лечения вторичного гипогонадизма. Патент на изобретение RUS № 2177735. 2002 [Kirpatovskiy I.D., Dendeberov E.S. Sposob lechenija vtorichnogo gipogonadizma. Patent RUS № 2177735.2002 (In Russian)].
- Дендеберов Е.С., Кирпатовский И.Д., Михалева Л.М. Новые подходык лечению крипторхизма, сочетающегося с вторичным гипогонадизмом. Проблемы репродукции 2001;(2):68. [Dendeberov E.S., Kirpatovsky I.D., Mikhaleva L.M. New approaches to the treatment of cryptorchidism combined with secondary hypogonadism. Problemi reproduktsii = Russian Journal of Human Reproduction 2001;(2):68. (In Russian)].
- Pidwell DJ, Burns C. The immunology of composite tissue transplantation. Clin Plast Surg 2007;34(2):303-17. https://doi.org/10.1016/j.cps.2006.12.002.
- Meirow D, Roness H, Kristensen SG, Andersen CY. Optimizing outcomes from ovarian tissue cryopreservation and transplantation; activation versus preservation. Hum Reprod 2015;30(11):2453-6. https://doi.org/10.1093/humrep/dev210.
- Tullius SG. Vascular composite tissue transplantation: achievements and challenges in a rapidly developing field. Transpl Int 2016;29(6):643. https://doi.org/10.1111/tri.12792.
- Shen H, Chen X, Li X, Jia K, Xiao Z, Dai J. Transplantation of adult spinal cord grafts into spinal cord transected rats improves their locomotor function. Sci China Life Sci 2019;62(6):725-33. https://doi.org/10.1007/s11427-019-9490-8.
- Kelly DM, Jones TH. Testosterone: a vascular hormone in health and disease. J Endocrinol 2013;217(3):R47-71. https://doi.org/10.1530/JOE-12-0582.
- Davis SR. Testosterone and the heart: friend or foe? Climacteric 2024;27(1):53-9. https://doi.org/10.1080/13697137.2023.2250252
- Gaunt G, Ramin K. Immunological tolerance of the human fetus Am J Perinatol 2001;18(6):299-312. https://doi.org/10.1055/s-2001-17861.







