Доброкачественная гиперплазия предстательной железы (ДГПЖ) – наиболее частая патология предстательной железы (ПЖ). Основные цели лечения ДГПЖ – улучшение качества жизни больных, страдающих от расстройств мочеиспускания (симптомы нижних мочевых путей, СНМП) и предотвращение прогрессирования заболевания [1]. Медикаментозная терапия ДГПЖ должна проводиться длительно, иногда в течение всей жизни пациента. Поэтому одним из требований, предъявляемых к фармакологическим средствам для лечения ДГПЖ, является низкая токсичность и отсутствие серьезных побочных эффектов. В настоящее время препаратами выбора для лечения ДГПЖ являются α1-адреноблокаторы и ингибиторы 5α-редуктазы; применяется комбинация α1-адреноблокаторов и ингибиторов 5α-редуктазы, которая является более эффективной по сравнению с приемом этих препаратов по отдельности [1, 2]. Указанные группы лекарственных препаратов имеют ряд значимых побочных эффектов, обусловленных их механизмом действия, тропностью к рецепторам, а также возрастными особенностями организма мужчины. Антиандрогенный эффект ингибиторов 5α-редуктазы проявляется в виде нарушения сексуальной функции у мужчин; нежелательные побочные эффекты α1-адреноблокаторов обусловлены их гипотензивными эффектами, также необходимо учитывать возможное хирургическое лечение катаракты у пациентов с ДГПЖ и в связи с этим необходимость отложить назначение α1-адреноблокаторов [2]. Новый селективный α1А-адреноблокатор силодозин является наиболее эффективным препаратом данной группы. Однако возникновение ретроградной эякуляции при приеме силодозина заставляет еще раз провести анализ соотношения "рискпольза" для этого препарата [3].
Фитотерапия является одной из неотъемлемых частей медикаментозной терапии ДГПЖ на ранних стадиях заболевания. Фитопрепараты, применяемые сегодня для лечения ДГПЖ, практически лишены значимых побочных эффектов, однако при их назначении имеется определенный субъективизм, связанный с тем, что препараты из растительного сырья сложнее подвергаются стандартизации и контролю качества, а разные серии одного препарата могут отличаться по количественному составу действующих веществ. Однако именно фитотерапия способна ингибировать прогрессию ДГПЖ, а также уменьшать выраженность симптомов, связанных с ДГПЖ, на ранних стадиях при отсутствии значимых побочных эффектов. В настоящее время широкое распространение получили растительные препараты, представляющие собой экстракты из плодов пальмы ползучей Serenoa repens (Простамол Уно, Пермиксон, Простаплант и др.) [4]. Лекарственное растительное сырье для получения этих препаратов произрастает в основном в США. На отечественном фармацевтическом рынке данная группа препаратов представлена препаратами, производимыми за рубежом (Франция, Германия), что, безусловно, отражается на их цене.
Учитывая несомненную актуальность разработки импортозамещающих конкурентоспособных фитопрепаратов для лечения ДГПЖ, целью представленной работы явилась сравнительная доклиническая оценка эффективности комплекса биологически активных веществ, выделенных из древесной зелени хвойных пород (хвойный провитаминный концентрат, ХПК), в сравнении с экстрактом Serenoa repens, на модели ДГПЖ, индуцированной сульпиридом. Выбор ХПК в качестве объекта исследования был сделан, исходя из данных о биологической активности компонентов, входящих в его состав, широкой доступности сырья для производства, а также наличия действующих предприятий по производству ХПК на территории Российской Федерации.
МАТЕРИАЛЫ И МЕТОДЫ
Эксперимент был проведен на 44 половозрелых крысах самцах Вистар с начальной массой 250–300 г разводки питомника "Рапполово" РАМН (Ленинградская область). Животные содержались в виварии барьерного типа в стандартных условиях. Содержание и все манипуляции с животными проводились в соответствии с требованиями действующих стандартов по содержанию и использованию лабораторных животных. Индукция ДГПЖ проводилась ежедневным введением сульпирида согласно методическим рекомендациям, принятым в России [5].
После 14-дневного карантина животные были рандомизированы и распределены на 4 группы:
1-я группа – интактный контроль, 10 крыс не получали никаких воздействий до конца эксперимента;
2-я группа – ДГПЖ-контроль, 12 крысам ежедневно вводили сульпирид в физиологическом растворе (ООО "Органика", Россия) внутрибрюшинно в дозе 40 мг/кг массы тела в течение 40 дней и носитель (растительное масло) внутрижелудочным зондом перорально по 0,5 мл на крысу;
3-я группа – ДГПЖ-ХПК, 12 крысам ежедневно вводили сульпирид, так же как во 2-й группе, и ХПК (ООО "Тихвинский лесхимзавод", Россия) в растительном масле внутрижелудочным зондом перорально в дозе 400 мг/кг массы тела;
4-я группа – ДГПЖ-Serenoa repens, 10 крысам ежедневно вводили сульпирид, так же как во 2-й группе, и спиртовой экстракт плодов Serenoa repens (Простамол Уно, Берлин-Хеми АГ, Германия), предварительно смешанный с растительным маслом, внутрижелудочным зондом перорально в дозе 200 мг/кг массы тела.
Выбор дозы ХПК был сделан, исходя из результатов предварительных доклинических испытаний его эффективности на модели ДГПЖ и оценки токсикологического профиля. Выбор дозы экстракта Serenoa repens основывался на литературных данных [6]. Длительность эксперимента составила 40 дней. По окончании эксперимента животные подвергались эвтаназии и взвешивались. При аутопсии ПЖ крыс извлекалась в виде комплекса дорсолатерального отдела (ДЛП), двух вентральных долей (ВП), двух семенных пузырьков с тесно прилежащими к ним передними долями или коагуляционными железами (ПП) (рис.1). Вычисляли объем дорсолатерального отдела ПЖ по формуле: V = a × b2, где а – больший линейный размер ПЖ; b – меньший линейный размер ПЖ. Отделы ПЖ взвешивались, для каждого из отделов и для всей ПЖ рассчитывали простатический индекс (ПИ) как отношение массы отдела ПЖ или всей ПЖ (в мг) к 100 г массы тела животного. Весь материал фиксировался в 10% забуференном растворе формальдегида и подвергался стандартной гистологической обработке с окраской гематоксилин/эозином; анализ гистологических препаратов проводился при световой микроскопии.
Результаты подвергались статистической обработке с использованием стандартного набора функций программы Microso Excel. Числовые данные приводятся в виде M±m, где M – среднее арифметическое; m – стандартная ошибка среднего арифметического. Для оценки статистической достоверности использовали критерий Стьюдента и Фишера с 95% уровнем значимости.
РЕЗУЛЬТАТЫ
На рис. 2 представлен макроскопический вид ПЖ крыс контрольных и экспериментальных групп. Во 2-й, 3-й и 4-й группах животных, подвергавшихся воздействию сульпирида, ДЛП и ВП в результате гиперплазии имели большие размеры по сравнению с группой интактного контроля. При гистологическом исследовании во всех отделах ПЖ крыс в результате действия сульпирида диагностирована гиперплазия преимущественно железистого типа.
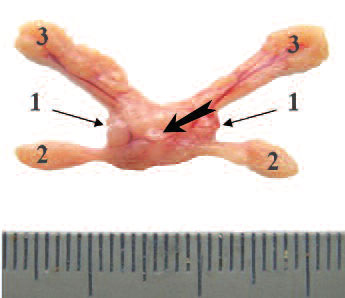
Рис. 1. Макроскопический вид нормальной предстательной железы крысы.
1 – дорсолатеральный отдел, 2 – вентральный отдел в виде двух вентральных
долей, 3 – передний отдел в виде двух
передних долей, прилежащих к семенным
пузырькам. Большой жирной стрелкой
обозначена простатическая часть уретры
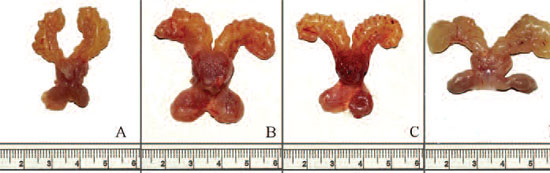
Рис. 2. Макроскопический вид предстательных желез крыс из разных групп. А – интактный
контроль; B – ДГПЖ-контроль; С – ДГПЖ-ХПК; D – ДГПЖ-Serenoa repens
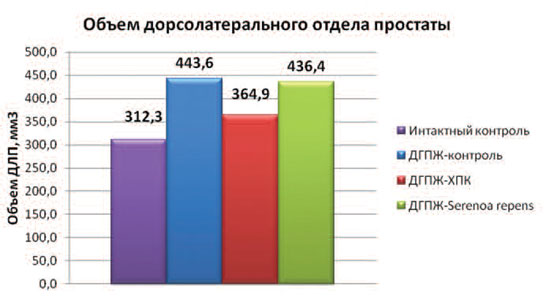
Рис. 3. Влияние ХПК и экстракта Serenoa repens на объем дорсолатерального отдела ПЖ у крыс
с экспериментальной ДГПЖ
В таблице 1 приведены данные о влиянии тестируемых средств на величину ПИ различных отделов и всей ПЖ крыс.
Как видно из таблицы, субхроническое внутрибрюшинное введение сульпирида вызывает увеличение массы отделов ПЖ по сравнению с интактными животными. По сравнению с интактным контролем, у крыс из группы "ДГПЖ-контроль" наблюдали достоверное увеличение ПИ ДЛП (на 44,7%), ВП (на 36,4%) и для всех отделов ПЖ (на 34,5%); увеличение ПИ ПП на 6,9% было недостоверным.
По сравнению с ДГПЖ-контролем, экстракт Serenoa repens достоверно снижал ПИ ВП, ПП и всей ПЖ соответственно на 27,9%, 40,5% и 24,2%; уменьшение ПИ ДЛП на 19,6% было статистически недостоверным (табл. 1). ХПК, в отличие от экстракта Serenoa repens, достоверно снижал ПИ всех отделов ПЖ и ПЖ в целом. По сравнению с ДГПЖ-контролем, ХПК достоверно снижал ПИ ДЛП, ВП, ПП и всей ПЖ соответственно на 28,9%, 31,8%, 32,7% и 29,7%. Лечебные эффекты ХПК на ДГПЖ, особенно на гиперлазию ДЛП, были более выраженными, чем у экстракта Serenoa repens (таб. 1).
На рисунке 3 представлены данные о влиянии тестируемых средств на объем ДЛП крыс.
Длительное введение сульпирида вызвало увеличение и объема ДЛП. По сравнению с интактной группой, в группе "ДГПЖ-контроль" объем ДЛП был достоверно выше на 42%. По сравнению с ДГПЖ-контролем, ХПК и экстракт Serenoa repens проявили лишь тенденцию к снижению данного показателя. При этом более выраженным было уменьшение объема ДЛП в группе животных, получавших ХПК (на 17,7%), в то время как экстракт Serenoa repens снижал объем ДЛП лишь на 1,6% (рис. 3).
Таблица 1. Влияние ХПК и экстракта Serenoa repens на величину простатического индекса у крыс с экспериментальной ДГПЖ
| Группа | Масса тела в день забоя, г |
Простатический индекс ( мг/ 100 г массы тела) | |||
|---|---|---|---|---|---|
| ДЛП | ВП | ПП | Вся ПЖ | ||
| Интактный контроль | 318,5±12,6 | 162,9±9,31 | 118,9±11,65 | 50,9±2,82 | 332,7±22,02 |
| ДГПЖ-контроль | 319,0±13,0 | 235,7±18,5* | 162,1±14,6* | 54,4±3,5 | 447,5±34,6* |
| ДГПЖ-ХПК | 366,2±13,7** | 167,6±7,6** | 110,5±6,7** | 36,6±3,4** | 314,8±14,2** |
| ДГПЖ-Serenoa repens | 321,1±14,8 | 189,9±13,6 | 116,9±6,6** | 32,4±3,6** | 339,2±18,1** |
ОБСУЖДЕНИЕ
Субхроническое внутрибрюшинное введение раствора сульпирида крысам вызывает у животных гиперпролактинемию, на фоне которой происходит увеличение массы отделов ПЖ и развивается ацинарная гиперплазия, причем показан синергический эффект пролактина и тестостерона на рост ПЖ [7]. Пролактин способен увеличивать число андрогеновых рецепторов в цитозоле и ядерных элементах клеток ПЖ у крыс [8]. Кроме того, пролактин продуцируется клетками ПЖ, где, вероятно, способен оказывать аутокринные или паракринные эффекты через модуляцию андрогенных воздействий [9].
Экстракт Serenoa repens получил в последние годы широкое распространение в качестве средства фитотерапии ДГПЖ в Европе и Америке. Фармакологические эффекты экстракта Serenoa repens на ПЖ весьма разнообразны и до конца не изучены. Это объясняется мультикомпонентным составом экстракта. Однако можно выделить основные эффекты, имеющие отношение к ПЖ: антиандрогенный, антипролиферативный, противоотечный, противовоспалительный [1, 4]. Лечебное действие экстракта Serenoa repens на ДГПЖ доказано в экспериментах на модели ДГПЖ, индуцированной как сульпиридом [10], так и тестостероном [11]. Результаты клинических исследований экстракта Serenoa repens у больных ДГПЖ противоречивые. Метаанализы, проведенные в 2004 г., показали эффективность экстракта Serenoa repens в отношении СНМП, ассоциированных с ДГПЖ [12, 13]. Однако метаанализ 17 рандомизированных клинических исследований, опубликованный в 2012 г., свидетельствует об отсутствии у экстракта Serenoa repens, применяемого в режиме монотерапии, эффектов в отношении СНМП по сравнению с плацебо [14].
В нашей работе простатотропные эффекты экстракта Serenoa repens проявились в виде достоверного снижения величины ПИ ВП, ПП и всей ПЖ. На ПИ ДЛП экстракт проявил лишь тенденцию к снижению, а на объем ДЛП практически не влиял. Учитывая тот факт, что экстракт Serenoa repens (препарат Простамол Уно) был выбран в качестве препарата сравнения, для тестируемого ХПК необходимо было получить сравнимые или более выраженные фармакологические эффекты. В целом, лечебное действие ХПК на ДГПЖ было более выраженным, чем у экстракта Serenoa repens.
Сырьем для получения ХПК служит хвоя ели европейской (Picea abies L.), которая фактически является отходом в лесоперерабатывающей промышленности. ХПК производят по специальной технологии путем выделения нейтральной фракции из хвои [15]. Широкий ареал распространения ели европейской на территории России делает сырье для получения ХПК дешевым и легкодоступным по сравнению с зарубежными фитопрепаратами, содержащими экстракт плодов Serenoa repens. Наиболее ценными биологически активными веществами в составе ХПК являются фитостерины (β-ситостерин, кампестерин, стигмастерин), витамин Е (α-токоферол, бета, гамма, дельта-токоферолы, альфа, бета, гамма, дельтатокотриенолы), каротиноиды (β-каротин, α-каротин, лютеин, ксантофиллы), полипренолы, фитол, сквален, витамин К [15]. Влияние ХПК на развитие экспериментальной ДГПЖ объясняется комплексными разнонаправленными механизмами действия входящих в его состав веществ. Среди всего комплекса биологически активных веществ ХПК следует выделить пять основных: фитостерины, фитол, β-каротин, витамин Е и полипренолы. Рассмотрим их возможные эффекты в отношении ДГПЖ.
Анализ результатов четырех рандомизированных плацебо-контролируемых клинических исследований, включавших в общей сложности 519 мужчин, показал, что β-ситостерин (основной представитель фитостеринов) вызывает регрессию СНМП у пациентов с ДГПЖ, хотя и не влияет на размеры ПЖ [16]. При анализе результатов семи контролируемых и неконтролируемых клинических исследований выявлено положительное влияние фитостеринов на качество жизни пациентов с ДГПЖ в шести исследованиях [17].
Фитол представляет собой длинноцепочечный алифатический спирт и входит в химическую структуру молекул токоферолов, хлорофилла, витамина К. Влияние самого фитола на развитие ДГПЖ в настоящее время не изучено. Фитол является лигандом для клеточных ядерных ре-цепторов PPAR (proliferator-activated receptor) и активирует данные рецепторы. Активация рецепторов PPAR в клетках является антипролиферативным и антиангиогенным сигналом [18], что может уменьшать гиперплазию ткани ПЖ.
β-каротин – соединение с известными антиоксидантными свойствами. ПЖ чувствительна к оксидативному стрессу ввиду того, что последний играет важную роль в развитии хронического интрапростатического воспаления [19]. Потребление β-каротина ассоциируется со снижением риска развития ДГПЖ и ее симптоматики [20, 21]. Еще одним известным антиоксидантом является витамин Е, что может объяснять его положительное влияние на ДГПЖ и СНМП. Комплекс препаратов, в состав которого входил витамин Е, у 144 пациентов с ДГПЖ уменьшал ноктурию и частоту мочеиспускания по сравнению с пациен
О влиянии полипренолов на развитие ДГПЖ литературных данных в настоящее время нет. Однако у полипренолов и их 2,3-дигидропроизводных (долихолов) выявлены многообразные эффекты, которые могут положительно влиять на ДГПЖ. Полипренолы, попадая в животный организм, метаболизируются в печени в активные долихолы. Функции полипренолов и долихолов связаны с транспортом гидрофильных молекулярных фрагментов через мембраны клеток в процессе синтеза полисахаридов, глюкопротеинов и других биополимеров; долихолы стереохимически взаимодействуют с витамином Е, образуя транспортные цепи по удалению свободных радикалов; полипренолы стимулируют синтез коэнзима Q, который является сильным антиоксидантом, нормализуют липидный обмен, стимулируют репарацию клеток [23].
ЗАКЛЮЧЕНИЕ
Впервые на модели ДГПЖ, индуцированной сульпиридом у крыс самцов, изучены простатотропные эффекты ХПК в сравнении с известным фитопрепаратом для лечения ДГПЖ – экстрактом Serenoa repens. ХПК уменьшал относительную массу всех отделов ПЖ и ПЖ в целом. Лечебные эффекты ХПК были более выраженными, чем у экстракта Serenoa repens. Полученные экспериментальные данные свидетельствуют о перспективах дальнейшего изучения ХПК, а также о возможности создания на его основе отечественного импортозамещающего лекарственного препарата растительного происхождения для лечения ранних стадий ДГПЖ у мужчин.
ЛИТЕРАТУРА
- Практическая урология. Руководство для врачей [под ред. П.В. Глыбочко, Ю.Г. Аляева]. М.: Медфорум, 2012. 352 с.
- Клинические рекомендации Европейской ассоциации урологов. М.: ООО "ИД АБВ-пресс", 2011. С. 8–35.
- Rossi M., Roumeguère T. Silodosin in the treatment of benign prostatic hyperplasia // Drug Des. Devel. Ther. 2010. Vol. 4. P. 291–297.
- Болезни предстательной железы [Под ред. Ю.Г. Аляева]. – М.: ГЭОТАР-Медиа, 2009. С. 126–152.
- Боровская Т.Г., Фомина Т.И., Дурнев А.Д., Удут В.В., Пахомова А.В., Юрмазов З.А. Дыгай А.И. Методические рекомендации по доклиническому изучению простатотропной активности лекарственных средств // Руководство по проведению доклинических исследований лекарственных средств. Часть первая [Под общей ред. А.Н. Миронова]. М.: ФГБУ "НЦЭМСП" Минздравсоцразвития России, 2012. С. 727–739.
- Duborija-Kovacevic N., Jakovljevic V., Sabo A., Tomic Z., Pajovic B., Perovic D. Tolerability and toxicity of lipidosterolic extract of American dwarf palm Serenoa repens in Wistar rats: well-known extract, new insight // Eur. Rev. Med. Pharmacol. Sci. 2011. Vol. 15. P. 1311–1317.
- Van Coppenolle F., Slomianny C., Carpentier F., Le Bourhis X., Ahidouch A., Croix D., Legrand G., Dewailly E., Fournier S., Cousse H., Authie D., Raynaud J.P., Beauvillain J.C., Dupouy J.P., Prevarskaya N. Effects of hyperprolactinemia on rat prostate growth: evidence of androgeno-dependence // Am. J. Physiol. Endocrinol. Metab. 2001. Vol. 280. P. 120–129.
- Prins G. Prolactin influence of cytosol and nuclear androgen receptors in the ventral, dorsal and lateral lobes of the rat prostate // Endocrinology. 1987. Vol. 120. P. 1457–1464.
- Nevalainen M., Valve E., Ingleton P., Nurmi M., Martikainen P., Harkonen P. Prolactin and prolactin receptors are expressed and functioning in human prostate // J. Clin. Invest. 1997. Vol. 99. P. 618–627.
- Van Coppenolle F., Le Bourhis X., Carpentier F., Delaby G., Cousse H., Raynaud J.P., Dupouy J.P., Prevarskaya N. Pharmacological effects of the lipidosterolic extract of Serenoa repens (Permixon) on rat prostate hyperplasia induced by hyperprolactinemia: comparison with finasteride // Prostate. 2000. Vol. 43. P. 49–58.
- Talpur N., Echard B., Bagchi D., Bagchi M., Preuss H.G. Comparison of Saw Palmetto (extract and whole berry) and Cernitin on prostate growth in rats // Mol. Cell. Biochem. 2003. Vol. 250. P. 21–26.
- Boyle P., Robertson C., Lowe F., Roehrborn C. Updated meta-analysis of clinical trials of Serenoa repens extract in the treatment of symptomatic benign prostatic hyperplasia // BJU Int. 2004. Vol. 93. P. 751–756.
- Gerber G.S., Fitzpatrick J.M The role of a lipido-sterolic extract of Serenoa repens in the management of lower urinary tract symptoms associated with benign prostatic hyperplasia // BJU Int. 2004. Vol. 94. P. 338–344.
- MacDonald R., Tacklind J.W., Rutks I., Wilt T.J. Serenoa repens monotherapy for benign prostatic hyperplasia (BPH): an updated Cochrane systematic review // BJU Int. 2012. Vol. 109. P. 1756–1761.
- Беспалов В.Г., Некрасова В.Б., Шевченко И.А., Вершинин А.С. Провитам – биоактивный комплекс из хвои сосны и ели. СПб.: Нордмедиздат, 2012. 52 с.
- Wilt T., Ishani A., MacDonald R., Mulrow C., Lau J. Betasitosterols for benign prostatic hyperplasia // Cochrane Database Syst. Rev. 2000. No. 2. CD001043.
- Coleman C.I., Hebert J.H., Reddy P. The effect of phytosterols on quality of life in the treatment of benign prostatic hyperplasia // Pharmacotherapy. 2002. Vol. 22. P. 1426–1432.
- Ondrey F. Peroxisome proliferator-activated receptor gamma pathway targeting in carcinogenesis: implications for chemoprevention // Clin. Cancer Res. 2009. Vol. 15. P. 2–8.
- De Marzo A.M., Coffey D.S., Nelson W.G. New concepts in tissue specificity for prostate cancer and benign prostatic hyperplasia // Urology. 1999. Vol. 53. P. 29–42.
- Rohrmann S., Giovannucci E., Willett W.C., Platz E.A. Fruit and vegetable consumption, intake of micronutrients, and benign prostatic hyperplasia in US men // Am. J. Clin. Nutr. 2007. Vol. 85. P. 523–529.
- Tavani A., Longoni E., Bosetti C. et al. Intake of selected micronutrients and the risk of surgically treated benign prostatic hyperplasia: a case-control study from Italy // Eur. Urol. 2006. Vol. 50. P. 549–554.
- Preuss H.G., Marcusen C., Regan J. Klimberg I.W., Welebir T.A., Jones W.A. Randomized trial of a combination of natural products (cernitin, saw palmetto, B-sitosterol, vitamin E) on symptoms of benign prostatic hyperplasia (BPH) // Int. Urol. Nephrol. 2001. Vol. 33. P. 217–225.
- Surmacz L., Swiezewska E. Polyisoprenoids – secondary metabolites or physiologically important superlipids? // Biochem. Biophys. Res. Commun. 2011. Vol. 22. P. 627–632.






