Мочекаменная болезнь занимает важное место в повседневной практике уролога и практикующих врачей общего профиля. В основе развития мочекаменной болезни (МКБ) лежат нарушения обменных процессов в организме, зачастую возникающие на фоне морфофункциональных изменений в мочевыделительной системе пациента, наследственной предрасположенности, заболеваний эндокринной системы. В среднем риск заболеваемости уролитиазом колеблется в пределах 5-10%. Коралловидный нефролитиаз является тяжелой формой мочекаменной болезни и составляет от 3 до 30% всех случаев диагностики камней почек [1].
По данным статистических исследований ежегодно в России по поводу МКБ выполняется около 200 000 операций, из них только 17% – высокотехнологичных [2]. Благодаря развитию альтернативных миниинвазивных методов оперативного лечения доля открытых методик (уретеро, пиело, нефролитотомия) неуклонно уменьшается. В клинических центрах, имеющих оборудование для проведения дистанционной ударно – волной литотрипсии (ДУВЛТ), уретероскопии, контактной литотрипсии (КЛТ), а также перкутанной нефролитолапаксии (ПНЛЛ), накопивших знания и значительный опыт по хирургическому лечению нефролитиаза, потребность в открытых операциях снизилась до 1-5,4% [1]. Несмотря на использование навигационных методов интраоперационного выявления бессосудистых участков при нефротомии, позволяющих удалять даже коралловидные камни без существенного нарушения функции почки, показания к открытой операции в настоящее время ограничены. К ним относятся как абсолютные, так и относительные:
1) значительный объем поражения, 2) неэффективность лечения методами ДУВЛТ, ПНЛЛ, КЛТ, 3) стеноз шейки чашечки, камень дивертикула, 4) ожирение, 5) нефункционирующий сегмент почки (резекция), 6) нефункционирующая почка (нефрэктомия), 7) выбор пациента – предпочтение одномоментного удаления конкремента [3].
Однако в последнее время по мере развития комбинированных эндоскопических интраренальных технологий к абсолютным показаниям открытого доступа можно отнести только нефункционирующую почку, при этом можно использовать лапароили ретроперитонеоскопический доступ. К тому же, на современном этапе доказано, что метод ПНЛЛ является наиболее предпочтительным способом извлечения камней чашечковых дивертикулов (stone free rates 69100%) [4].
Экстракорпоральная и чрескожная нефролитотрипсия являются альтернативой открытых оперативных методик. Мотивами для разработки новых миниинвазивных направлений при лечении МКБ явилось следующее: 1. несоответствие времени, затрачиваемого на выполнение доступа и основного этапа операции; 2. высокий травматизм и значимое уменьшение объема функционирующей паренхимы почки; 3. отсутствие интраоперационной визуализации внутренних структур объекта вмешательства; 4. высокий уровень осложнений после стандартных операций и длительный срок реабилитации.
Развитие дистанционных и перкутанных методов лечения МКБ происходило параллельно с начала 50-х годов прошлого столетия благодаря разработке оборудования для литодеструкции в водной среде, основанного на электро-гидравлическом принципе воздействия (рис. 1), а также возможностям осуществления пункционного доступа в полостную систему почки.

Рис. 1. Аппарат для дробления камней Урат
Первоначально большие надежды возлагались на дистанционные технологии по причине их малой травматичности.
В 80-е годы частота применения хирургических методов лечения МКБ в развитых (в отношении уровня здравоохранения) странах мира выглядела следующим образом: ДУВЛТ – 87%, ПНЛЛ – 9%, открытый доступ – 4% [5]. Однако по мере накопления опыта, несмотря на разработку и использование более эффективных видов формирования ударной волны (электро-магнитных, пьезо-электрических, электрокондуктивных), выявлены существенные ограничения ДУВЛТ. Выяснено, что результативность данного метода зависит от исходных размеров конкремента, его плотности, с увеличением которых эффективность метода снижается и увеличивается число послеоперационных осложнений (обострение хронического пиелонефрита, наличие «каменной дорожки» мочеточника, возникновение субкапсулярных и паранефральных гематом) [6]. Доказано, что ДУВЛТ при коралловидном нефролитиазе малопродуктивна, а в некоторых случаях абсолютно противопоказана. После многолетнего периода использования дистанционной технологии определена целесообразность ее применения только при неосложненных формах МКБ, размерах камня не более 2,0 см с плотностью до 1000 единиц HU [7]. Даже в Германии, называемой «матерью ударно-волновых технологий», некоторые крупные госпитали приняли решение не приобретать новые аппараты. С целью увеличения эффективности лечения и ускорения периода реабилитации на современном этапе происходит постепенное замещение экстракорпоральных операций минии микроперкутанными технологиями, предполагающими литодеструкцию и экстракцию высокоплотных камней малых (менее 1 см) размеров.
Для понимания и оценки текущих направлений развития терапевтической стратегии МКБ обратимся к истории. Основой совершенствования чрескожной технологии и расширения показаний для ее применения закономерно послужили следующие краеугольные исторические события, открытия и технические разработки:
- 3000 лет до н.э. – чрескожная катетеризация мочевого пузыря (Древний Египет);
- 1865 г. – простая чрескожная пункция почки (T. Hillier) [8];
- 1925 г. – разработка метода троакарного дренирования почки при гидронефрозе ( J. Israel, W. I srael) [9];
- 1941 г. – первая экстракция камня почки через сформированный нефростомический тракт (E. Rupel, R. Brown)[10];
- 1951 г. – антеградная чрескожная пиелография под рентгеноскопическим контролем (N. Ainsworth, Vest) [11];
- 1953 г. – разработка метода чрескожной пункции кровеносных сосудов (S. Seldinger) [12];
- 1955 г. – чрескожная пункционная нефростомия под рентгеновским контролем c совместным участием радиологов (W. Goodwin) [13];
- 1970 г. – электрогидравлическая дезинтеграция крупных камней мочевой системы (H. Sachse) [14];
- 1974 г. – пункционная нефростомия под ультразвуковой навигацией (J. Pedersen) [15];
- 1976 г. – двухэтапное удаление камня почки с использованием дилатационной методики (I. Fernstrom, B. Johansson) [16];
- 1977 г. – применение ультразвукового литотриптера для разрушения и экстракции камня через нефростому (K. Kurth, R. Hohenfellner, J. Altwein) [17];
- 1980-1982 гг. – разработка технологий кожно-почечного доступа (бужи и дилататоры P. Alken, K. Amplatz) [18,19];
- 1983 г. – формирование кожно-почечного тракта с использованием баллонного дилататора для ангиопластики (К. Сlayman) [20];
- 1985 г. – первая публикация об опыте проведения 1000 процедур перкутанной нефролитолапаксии (W. Segura) [21];
- 1985 г. – первый опыт чрескожной хирургии нефролитиаза в России (А.В. Морозов, А.Г. Мартов) [22];
- 1989 г. – новая эра лечения уролитиаза методом экстракорпоральной литотрипсии (внедрение литотриптора Dornier HM4) [23];
- 1990 г. – развитие перкутанной почечной хирургии в положении на спине (supine position) (JG. Valdivia) [24];
- 2008 г. – использование многопортовой техники чрескожного лечения коралловидного нефролитиаза (М. Desai) [25];
- 2012 г. – метод ПНЛЛ определен как первая линия терапии коралловидных и крупных камней почек [26].
Побуждающим стимулом для разработки нового направления и усовершенствования минимально-инвазивных технологий также явились особенности анатомии мочевых путей, обуславливающие разнообразие оперативных доступов и, бесспорно, открытие задне-латеральной аваскулярной зоны почки Brodel-Zondeka (рис. 2).
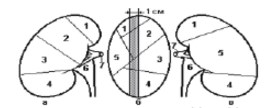
Рис. 2. Бессосудистая зона почки Brodel-Zondeka [27] Сегменты почки (правая): а – вид спереди, б – сбоку, в – сзади. 1 – segmentum superius; 2 – segmentum anterius superius; 3 – segmentum anterius inferius; 4 – segmen-tum inferius; 5 – segmentum posterius; 6 – pelvis; 7 – a. renalis; заштрихована «бессосудистая зона».
Конструирование и развитие специализированной эндоскопической техники в начале 80-х годов (M. Marberger совместно с Richard Volf GmbH, Germany [28], K. Korth совместно с Olympus Winter und Ibe, Germany [29], Hautmann совместно с K. Storz, Germany [23]), создание контактных литотрипторов (электрогидравлический – 1955 г., ультразвуковой, лазерный – 60-80-е годы, пневматический – 1988 г.) [23] позволили расширить показания для применения малотравматичных вмешательств в урологии, в том числе при осложненном течении нефролитиаза. Благодаря совершенствованию и внедрению в лечебный процесс новых компьютерных навигационных технологий, перспективы хирургии уролитиаза выросли многократно. На данном этапе развития техники передовые радиологические станции обеспечили возможность получения трехмерного изображения высокого разрешения, оптимального выбора точки пункции и планирования траектории движения инструмента в режиме реального времени.
С учетом вышеуказанного, на современном этапе наиболее рациональным методом лечения при коралловидном нефролитиазе является перкутанная нефролитолапаксия, использующая пункционно-дилятационную технику доступа в сочетании с тремя видами навигации и визуализации (ультразвуковой, рентген-телевизионной и эндоскопической) и различные технологии дезинтеграции конкрементов (рис. 3). Данная методика позволила значимо уменьшить площадь травмируемой паренхимы, сохранить ее функциональную способность, нивелировать риски интраи послеоперационных осложнений, сократить сроки анальгезии и госпитального периода.
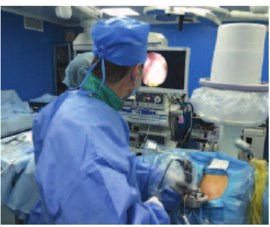
Рис. 3. Перкутанная нефролитолапаксия, этап нефролитотрипсии
В результате проведенных научных исследований установлено, что:
1. Одной из основных проблем МКБ является высокая частота рецидивов, которые могут встречаться у 50% пациентов в течении 5-летнего периода, а ежегодный риск рецидива камнеобразования достигает 14,415,2% [2];
2. На долю чрескожных пособий при нефролитиазе как монотерапии приходится от 45 до 60% оперативных вмешательств [30];
3. После перкутанного доступа функциональная способность почки восстанавливается в среднем через 72 часа [31];
4. При исследовании пациентов после формирования кожно-почечного канала и нефролитотрипсии фокальный дефект паренхимы при сканировании с технецием обнаружен только у 18% [32];
5. При глобальном изучении результатов и осложнений перкутанной нефролитолапаксии в 96 центрах Европы, Азии и Америки сделаны выводы о высокой эффективности и безопасности метода (CROES PCNL Study Group, 2011) [33];
6. Распределение осложнений по Clavien: без осложнений – 79%, I – 11,1%, II – 5,3%, IIIa – 2,3%, IIIb – 1,3%, IV – 0,5%, V – 0,03% [34];
7. Для освоения ПНЛЛ необходимо выполнить не менее 50 операций, а очень хорошие навыки приобретаются после выполнения более 100 вмешательств [35];
8. В настоящее время чрескожная нефролитотрипсия является широко известной и высокоэффективной методикой лечения МКБ, однако в США не более 11% урологов владеют соответствующей квалификацией для проведения данного оперативного вмешательства [36], в России, по мнению экспертов, – не более 3-5%.
Существующие альтернативные методы миниинвазивного лечения нефролитиаза широко известны. Их преимущества и недостатки представлены в таблице 1.
Таблица 1. Миниинвазивные методы лечения МКБ
| Методы | Преимущества | Недостатки |
|---|---|---|
| Многопортовая ПНЛЛ (multitube) |
Возможность одномоментного удаления камней |
Травма паренхимы, увеличение времени облучения, срока госпитализации |
| Бездренажная ПНЛЛ (tubeless) | Сокращение сроков анальгезии, госпитализации |
Опасность пролонгированного кровотечения с риском повторной операции |
| ПНЛЛ на спине (supine position) | Уменьшение времени операции (экономия на разворот), использование одновременно ретроградных интраренальных технологий, низкий риск повреждения соседних органов |
Неудобство формирования доступа и эндоскопического этапа |
| Мини, ультра-мини, микро ПНЛЛ | Уменьшение травмы паренхимы и рисков осложнений, увеличение свободы манипулирования, возможность применения tubeless методики |
Удлинение времени фрагментации и экстракции, ограничение методики при камнях более 1,5-2,0 см |
| Ранняя повторная нефроскопия (second-look) | Ликвидация резидуальных камней | Увеличение частоты инфекционно-воспалительных осложнений |
| Комбинированные методы – ПНЛЛ+ДУВЛ (sandwitch therapy) | Полная элиминация конкрементов | Удлинение сроков лечения и реабилитации |
Многопортовая технология заключается в формировании дополнительных доступов для удаления компонентов камня недоступных из основного канала. Операция заканчивается установкой двух и более нефростом (рис. 4).
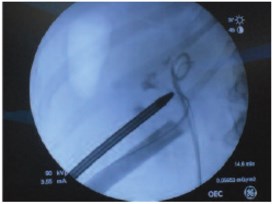
Рис. 4. Двухпортовая методика при коралловидном нефролитиазе (доступ через среднюю и нижнюю чашечки)
Бездренажная, вернее безнефростомная, методика предполагает только внутреннее дренирование мочевых путей. Нефролитолапаксия в положении на спине (supine position) обеспечивает уменьшение времени на укладку пациента, но создает трудности манипулирования инструментами (рис. 5).
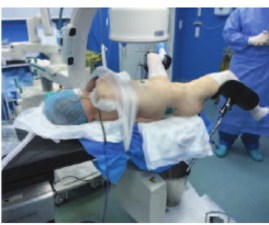
Рис. 5. Укладка пациента в положение на спине
Методы с использованием ранней повторной нефроскопии и сочетанием чрескожных методик с экстракорпоральными методами фрагментации позволяют уменьшить частоту резидуальных камней. Миди, мини, ультра-мини микронефролитолапаксия с использованием нефроскопов от 17 Ch до 5 Ch дает возможность разрушать и извлекать камни, несмотря на анатомические трудности. Стремление к миниатюризации процедуры существует уже более 15 лет. По данным многочисленных исследований выяснено, что традиционная ПНЛЛ (26 Ch) имеет ряд осложнений, которые в 29-83% случаев обусловленны дилатацией кожно-почечного тракта и ренальными манипуляциями [33]. Поэтому мини-технологии, разработанные с целью нивелирования травматичности доступа, уменьшают риски, в основном, геморрагических осложнений, но удлиняют время оперативных вмешательств по причине необходимости более мелкой фрагментации камня и длительности их извлечения через тубус малого диаметра, несмотря на использование вакуумного феномена Bernoulli. Микротехнологии заключаются в использовании 3-х компонентной иглы 4,85 Ch (1,6 мм) с оптической системой 0,9 мм и рабочим каналом, пропускающим лазерный световод 200 мкм, и предполагающие наиболее мелкую фрагментацию камней с возможностью их самостоятельного отхождения, не требующие их экстракции или применение ирригационноаспирационной автоматизированной системы для их отмывания.
С целью улучшения результатов данного вида операций в настоящее время назрела необходимость осуществления мероприятий по оптимизации технологического процесса и дальнейшему развитию всех этапов вмешательства: 1 этап (чрескожный доступ) – а) навигация, б) пункция, в) дилатация; 2 этап (деструкция и экстракция) – а) дезинтеграция конкрементов, б) извлечение фрагментов с оценкой полноты освобождения; 3 этап (дренирование) – а) нефростомия, б) методы закрытия кожно-почечного канала и внутреннее дренирование.
Рентгенологическая, ультразвуковая навигация и эндовидеоскопия являются основными и единственными методами контроля, как первого, так и последующих этапов перкутанного вмешательства, имея при этом значительные ограничения для осуществления безопасных манипуляций. Бипланарная флюороскопия с использованием С-дуги до сих пор является наиболее часто (до 60%) применяемым методом [37]. Ультрасонография в виде процедуры мононавигации применима в ограниченных ситуациях (у 10%), и чаще используется у детей, молодых женщин, у лиц астеничного телосложения и имеет такие значимые преимущества, как отсутствие лучевой нагрузки и наличие визуального контроля за окружающими висцеральными тканями и органами [38]. Комбинированные технологии навигации, используемые в менее чем в 15% случаев, предполагают осуществление следующих шагов: а) поиск заинтересованной чашечки, безопасной зоны направления пункционного канала и точки кожного входа при УЗ сканировании, б) виртуальное проектирование и формирование плана доступа, осмысление «дорожной карты», определение угла наклона иглы при биплановой рентгеноскопии, в) ретроградное контрастирование ЧЛС и собственно пункция выбранной чашечки под контролем фронтальной флюороскопии [39]. При отсутствии дилатации полостной системы почки, множественном или комбинированном нефролитиазе, аномалиях положения почек и морбидном ожирении возможно применение сочетанной навигации с использованием эндовидеоскопии. Гибкая уретероскопия позволяет осуществить точную антеградную пункцию через бессосудистую зону чашечки и исключить потерю ориентации при геморрагических изменениях прозрачности среды, а также произвести формирование ретроградного почечно-кожного канала при использовании техники Lawson. Уретероскопически ассистированная ретроградная нефростомия, как первый этап ПНЛЛ, применима при невозможности антеградного доступа, при отсутствии ретенции верхних мочевых путей [40]. Прорывом совершенствования технологии доступа явилось развитие философии минитюаризации хирургии нефролитиаза. Однако, «всевидящая» игла с микрооптикой 0,6 мм, улучшая возможности пункционного этапа, требует применения вспомогательных методов визуализации (ультразвуковых или рентгенологических).
Идеальная пункция подразумевает процедуру с максимальной результативностью освобождения от камней и минимальным риском кровотечения и повреждения висцеральных органов. Поэтому последние научные и технические разработки направлены на совершенствование технологий навигации и методов пункционно-дилатационного доступа. Получила развитие ротационная флюороскопия высокого разрешения с интраоперационной 3D реконструкцией, позволяющая обеспечить точную топическую картину камня и планирование оптимального пункционного канала. Специальные алгоритмы конструирования КТ-подобных изображений обеспечивают нужной информацией менее чем за минуту непосредственно у операционного стола. Программа интегрированной навигации отображает длину, угол траектории иглы, точку кожного входа, автоматически перемещает С-дугу для оптимальной визуализации, а система лазерного перекрестия указывает зону позиционирования инструментов доступа. Разработан и широко используется набор средств для уменьшения лучевой нагрузки на пациента и медицинский персонал – адаптация частоты импульсов, выбор фильтра с учетом телосложения, регулировка коллиматора, позиционирование объекта без включения источника излучения и др., обеспечивающий снижение радиологического скрининга на 67% [41]. 3D сонография с новой роботизированной системой пункционной навигации имеет ряд преимуществ в виде отсутствия лучевой нагрузки и точности манипуляций, однако эта методика в настоящее время находится на стадии клинических испытаний и носит экспериментальный характер [42]. Виртуальная проекция ультразвукового пункционного тракта на флюороскопическую картину обеспечивает безопасность этапа формирования кожно-почечного канала и также находится на стадии клинических исследований [43]. Данная система может служить симуляционным тренажером на этапе обучения чрескожным методам хирургии МКБ. Разработка специальной конструкции игл позволяет улучшить успешность пенетрации ЧЛС благодаря оценке биоимпеданса на границе тканей и сред [44]. В рутинной практике предоперационное планирование доступа основывается на мультиспиральной КТ-пиелографии и объемной реконструкции органа, а контроль во время процедуры базируется на ультрасонографии и рентгеноскопии, в редких ситуациях – на КТ и МРТ навигации (рис. 6 а-в).
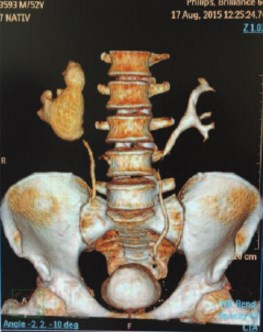
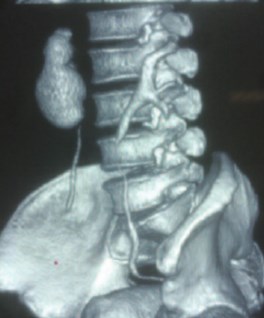
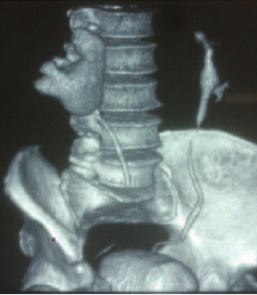
Рис. 6. Мультиспиральная компьютерная томография мочевыделительной системы с 3D реконструкцией а – фронтальная проекция, б, в – косые правая и левая проекция
Благодаря техническим разработкам в последнее время появились работы о проведении перкутанного доступа с новыми видами визуального наблюдения. Метод предполагает рентгеноскопическую мультиплановую реконструкцию с контрастным усилением, интегрированную с изображением, полученным при КТ/МРТ исследовании, а лазерная система фокусировки Syngo-iGuide обеспечивает точность и безопасность траектории пункционной иглы. Преимуществом данной системы является малая величина дозовой нагрузки и уменьшение времени этапа пенетрации [45]. Компьютерная программа наложения 3D-параметров КТ/МРТ на УЗ изображение в режиме реального времени в сочетании с экспериментальным использованием электромагнитного сенсора на кончике иглы позволит в недалеком будущем добиться оптимальных результатов в осуществлении доступа [46]. Также представляет интерес работа испанских ученых, посвященная разработке электромагнитной системы определения траектории доступа, предполагающая ретроградную установку проводника и антеградное проведение пункционной иглы с помощью навигационных сенсоров под эндовизуальным и УЗ контролем [47]. Данная система прошла успешное экспериментальное исследование на животных моделях в 2013 году. Также проходит тестирование «роботическая рука» для перкутанной почечной пункции в сочетании с УЗ навигацией [48]. Следующим этапом развития компьютер-ассистированной хирургии, нашедшей свое применение при лапароскопических вмешательствах, является внедрение новой технологии в перкутанной хирургии нефролитиаза. Суть процедуры следующая: во время МСКТ цветные радио-маркеры фиксируются к коже, интраоперационно они служат навигационными точками для формирования виртуальной анатомии зоны интереса. Инновационная программа, разработаннная в Научно-исследовательском центре рака (Германия), позволяет получить 3D реконструкцию КТ сканирования собирательной системы почки и окружающих органов в различных позициях пациента. Камера iPad получает изображение от стороны доступа, форматирует его и передает через беспроводную локальную сеть серверу устройства управления флюороскопическим столом. Сервер анализирует расположение маркеров относительно iPad и сопоставляет их с позицией видеои КТ-изображения. Далее сервер создает картину дополненной реальности и передает информацию на iPad [47] (рис. 7).

Рис. 7. IPad навигация
В настоящее время после пункции заинтересованной чашечки и оптимальной установки рабочего проводника рутинно осуществляется фасциальная дилатация бужами 810 Ch с последующим определением метода формирования кожно-почечного канала. Выбор инструментария и технологии дилатации зависит от величины и конфигурации камня, его мобильности, диаметра и длины шейки чашечки, типа строения и степени ретенции ЧЛС, отечно-инфильтративных изменений эндотелия, толщины и плотности паренхимы в зоне пункции, а также величины пространства между камнем и стенкой чашечки. В большинстве случаев используется методика прогрессивного бужирования телескопическими металлическими дилататорами Alken или пластиковыми дилататорами Amplatz с последующей установкой одноименного кожуха, выбор диаметра которого определяется величиной эндоскопа [18]. Среди преимуществ кожуха можно отметить следующие: стабильность доступа, невозможность абсорбции и экстравазации ирригационной жидкости, обеспечение низкого интраренального давления, возможность извлечения крупных фрагментов и гемостатическая интубация паренхиматозного тракта. Однако необходимость смены дилататоров и их количество сопряжены с пролонгированием данного этапа и времени рентгенологического скрининга, с риском потери доступа, а также кровотечения с развитием гемотампонады ЧЛС. Данных осложнений лишена методика одномоментного доступа (one-shot), которая имеет относительные ограничения только при склеротических изменениях паранефрия и паренхимы почки. Лучшим методом дилатации на данном этапе является баллонная технология, имеющая неоспоримые преимущества в виде применения одношаговой техники, низкого риска паренхиматозного кровотечения и травматических повреждений по причине радиальной силы воздействия [20]. К наиболее значимым проблемам этапа доступа можно отнести невозможность продвижения внешнего кожуха до просвета чашечки в случаях отсутствия пространства для его проникновения, особенно при коралловидном нефролитиазе. При этом достижение просвета чашечки возможно только под эндовизуальным контролем, что при возникшем паренхиматозном кровотечении крайне затруднительно. В данной ситуации наиболее предпочтительно использование телескопических дилататоров Alken.
Представляется закономерным развитие второго этапа чрескожной технологии – дезинтеграции конкремента, основной целью которой является сокращение времени фрагментации и замена экстракции на аспирацию. Рутинно применяемые методы, такие как электрогидравлический, пневматический и даже ультразвуковой (в меньшей мере) требуют использования, зачастую продолжительной, инструментальной экстракции высокоплотных крупных фрагментов. Современные разработки оборудования, использующие энергию высокочастотного гольмиевого лазера, демонстрируют фрагментацию в «пыль», что в сочетании с автоматизированной ирригационно-аспирационной системой обеспечивает полное калькулезное освобождение без необходимости их извлечения. Стратегия фрагментации и экстракции зависит от трех равноценно-значимых факторов: 1. калькулезный фактор включает плотность, локализацию, размер и конфигурацию камня; 2. инструментальный фактор определяется калибром рабочего канала эндоскопа, диаметром внешнего кожуха и моделью нефроскопа; 3. фактор укладки пациента – положение на спине (supine pos.) предполагает позицию инструмента с наклоном вниз, что облегчает спонтанную миграцию фрагментов.
Традиционно ПНЛЛ заканчивается установкой нефростомического дренажа с целью гемостатической интубации паренхиматозного канала, обеспечения низкого внутрипросветного давления и адекватной уродинамики, исключения паранефральной экстравазации мочи и формирования уриномы, а также для перспектив осуществления прямого доступа (методика second-look) и проведения контрастного антеградного исследования. За годы применения методики использовалось множество дренирующих устройств различных размеров и модификации. Если на ранних этапах совершенствования технологии преимущественно устанавливались трубки, сопоставимые с диаметром сформированного канала, то в настоящее время наибольшее распространение получили нефростомы малого диаметра. Доказана возможность минидренирования (10-12 Ch) при инфекционном, коралловидном нефролитиазе, изначальной дилатации ЧЛС, не полном калькулезном освобождении, в случае интраоперационных осложнений (перфорация, паренхиматозное кровотечение, повреждение висцеральных органов), а также при осуществлении макси-доступов (30-36 Ch). Известно, что использование нефростомы малого диаметра (до 10-12 Ch) при доступе 30 Ch приводит к геморрагическим осложнениям только в 1% случаев [49]. В последнее время получили развитие безнефростомная и бездренажная методики, продиктованные рядом факторов – длительное заживление кожно-почечного канала при пролонгированной нефростомии, отсутствие компрессионного гемостатического эффекта и геморрагических осложнений при использовании дренажа малого диаметра, быстрое закрытие свища и спонтанный гемостаз при дислокации нефростомы в раннем послеоперационном периоде [50-51]. Преимущества данной методики (одномоментное закрытие кожно-почечного канала, уменьшение потребности в послеоперационной анальгезии, сокращение сроков госпитального периода и реабилитации, сопоставимость периоперационных осложнений по количеству, характеру и степени тяжести в сравнении с дренажной техникой) оценены рядом авторов при проведении рандомизированных исследований [52]. Уже накоплен опыт бездренажной ПНЛЛ у детей, пациентов с ожирением, старческого возраста, при коралловидном нефролитиазе, в случаях единственной почки, аномалий развития (дистопии, подковообразной почки), хронической почечной недостаточности, синхронной билатеральной процедуре [53-54]. Благодаря многоцентровым исследованиям определены критерии возможности применения метода – отсутствие инфекции мочевых путей, использование менее 2 портов, размер камня менее 3 см, время операции менее 2 часов, отсутствие осложнений (перфорация, кровотечение), полное калькулезное освобождение, отсутствие органической инфраренальной обструкции [55]. К альтернативным tubeless методам, нивелирующим риски паренхиматозного кровотечения, относятся следующие процедуры:
- механическая компрессия кожно-почечного канала;
- ушивание свищевого хода;
- криоаблация паренхиматозного тракта;
- монои биполярная коагуляция паренхиматозных сосудов;
- аппликация абсорбируемых гемостатических материалов (фибрин, желатиновый матрикс с тромбином и без) [56-57].
Изучение проблем перкутанной хирургии нефролитиаза продолжается и по сей день. Что же нас ждет в будущем, какие технологические разработки и инструментальные усовершенствования позволят решить такие существующие проблемы перкутанной хирургии нефролитиаза, как выбор оптимально-физиологического положения пациента на операционном столе, уменьшение риска респираторных и кардиологических осложнений, увеличение эффективности и безопасности доступа, возможность монопортовой техники, скорость фрагментации и экстракции, полнота элиминации, необходимость дренирования, низкая доза облучения, профилактика осложнений (полноценный гемостаз, мочевая инфекция)?
Новшества должны коснуться всех этапов ПНЛЛ, от пункции и навигации до дренирования или клеевой тампонады паренхиматозного канала. Необходимость дальнейшего развития метода также продиктована определенным спектром наиболее часто встречающихся осложнений и особенностями периоперационного периода.
Немного пофантазируем…
Давайте представим 20… год. В больницу поступает пациент с диагнозом коралловидный камень почки. Пациент после предоперационной подготовки попадает в операционную будущего. Медицинский персонал укладывает пациента на операционный стол с окном для пункции в положение лежа на спине. Ассистент подводит роботическую установку к пациенту. Хирург, находясь в пультовой и управляя джойстиком, расположенным на дистанционном пульте управления, точными движениями манипулятора робота с фиксированной иглой и сложным механизмом обратной связи проводит пункцию полостной системы почки (рис. 8).

Рис. 8. Роботизированное устройство для пункции при перкутанной нефролитотомии [58]
При этом навигация осуществляется с помощью компьютерной программы, позволяющей интегрировать 3D-параметры КТ/МРТ на 3D сонографическое изображение в режиме реального времени и отслеживать положение иглы по отношению к чашечке-мишени и корректировать продвижение иглы при ее отклонении. Формирование пункционного доступа проводится с помощью баллонного дилататора с наличием в центральной части просвета с изменяемым диаметром канала для проведения оптики и инструментов. С помощью лазерного дезинтегратора производится фрагментация камней в мелкодисперсную пыль. Автоматизированная ирригационно-аспирационная система подает подогретую жидкость и аспирирует каменную мелкодисперсную взвесь, контролируя давление в полостной системе почки. Закрытие пункционно-дилатационного доступа производится с помощью клеевых материалов.
Таким образом, учитывая современное состояние проблемы, мы предполагаем, что перспективными направлениями будущего перкутанной техники могут быть:
- сочетанные навигационные технологии с использованием данных МСКТ, МРТ, рентгеновского и УЗ сканирования на этапе осуществления доступа и формирования кожно-почечного канала;
- использование дистанционных роботизированных технологий на этапе дезинтеграции и экстракции камня;
- применение автоматизированной подачи подогреваемого раствора и аспирации фрагментов при поддержании низкого внутриполостного давления;
- новые технологии литодеструкции с использованием лазерной энергии в режиме абляции и микрофрагментации;
- использование гибкой цифровой нефроскопии с целью оптимизации доступа в труднодоступные зоны ЧЛС и полного калькулезного освобождения;
- сочетание антеградных и ретроградных интраренальных технологий;
- термальные или биологические методы паренхиматозного гемостаза и закрытия кожно-почечного свища;
- технологические разработки и усовершенствования инструментария (баллонный кожух-дилататор с изменяемым диаметром (просветом), трансформирующийся мочеточниковый катетер в стент, конструктивное изменение операционного стола для оптимального и физиологического положения пациента и др.).
ЛИТЕРАТУРА
1. Аляев Ю.Г., Григорян В.А., Руденко В.И., Григорьев Н.А., Еникеев М.Э., Сорокин Н.И. Современные технологии в диагностике и лечении мочекаменной болезни. М.: Литтерра, 2007. 144 с.
2. Кривонос О.В., Скачкова Е.И., Малхасян В.А., Пушкарь Д.Ю. Состояние, проблемы и перспективы развития Российской урологической службы. Вестник Российского общества урологов. 2012:2.
3. Аляев Ю.Г. Мочекаменная болезнь. Современные методы диагностики и лечения. М: ГЭОТАР – Медиа, 2010. 103 с.
4. Okeke Waingankar N, Hayek S, Smith AD, Okeke Z. Calyceal diverticula: a comprehensive review. Rev Urol 2014;16(1): 29–43.
5. Paik ML, Resnick MI. Is there a role for open stone surgery? Urologic Clinics 2000; 27(2):323-331
6. Donaldson JF, Lardas M, Scrimgeour D, Stewart F, MacLennan S, Lam TB, et al. (2015) Systematic review and meta-analysis of the clinical effectiveness of shock wave lithotripsy, retrograde intrarenal surgery, and percutaneous nephrolithotomy for lower-pole renal stones. Eur Urol 2015;67(4):612-616
7. Мочекаменная болезнь в «Клинические рекомендации Европейской ассоциации урологов». 2011. 28-31с.
8. Bloom DA, Morgan JR, Scardino PL. Thomas Hillier and percutaneous nephrostomy. Urology 1989; 33:346-350
9. Israel J, Israel W. Chirurgie der Niere und des Harnleiters. Thieme, Leipzig, 1925. 222 p.
10. Rupel E, Brown R. Nephroscopy with remowal of stone following nephrostomy for obstructive calculus anuria. J Urol 1941;46:177-182
11. Ainsworth WL, Vest SA. The differential diagnosis between renal tumors and cysts. J Urol 1951;66(6): 740-749
12. Seldinger SI. Catheeter replacement of the needle in percutaneous arteriography; a new technique. Acta radiol 1953;39(5): 368-376
13. Goodwin WE, Casey WS, Woolf W. Percutaneous trocar (needle) nephrostomy in hydronephrosis. JAMA 1955;157:891-894
14. Sachse H. Erfahrungen mit der Electrolithotripsie. Verh Deutsche Ges Urologie 1970;23:171-173
15. Pedersen JF. Percutaneous nephrostomy guided by ultrasound. J Urol 1974;112:157-159
16. Fernstrom I, Johannson B. Percutaneous pyelolithotomy: a new extraction technique. Scand J Urol Nephrol 1976;10:257-259
17. Kurth KH, Hohenfellner R, Altwein J. Ultrasound litholapaxy of a staghorn calculus. J Urol 1977;117:242-243
18. Alken P. The telescope dilators. World J Urol 1985;3:7-10
19. Rusnak B, Castaneda-Zuniga W, Kotula F. An improved dilator system for percutaneous nephrostomies. Radiology 1982; 144:174
20. Clayman RV, Castaneda-Zuniga W, Hunter DW. Rapid balloon dilatation of the nephrostomy tract for nephrostolithotomy. Radiology 1983;147:884-885
21. Segura W, Patterson OE, Le Roy AJ. Percutaneous removal of kidney stones: review of 1000 cases. J Urol 1985; 1134:1077-1081
22. Морозов А.В. Мартов А.Г. Удаление камней почек и мочеточников через нефростомический свищ. Урология и нефрология 1985;4:30-32.
23. Supine percutaneous nephrolithotomy and ECIRS: the new way of interpreting PNL. [Editors Scoffone CM, Hoznek A, Cracco CM]. Springer-Verlag, France. 2014
24. Valdivia JD, Valle J, Villarroya S, LÓPEZ JA, BAYO A, LANCHARES E, et al. Why is percutaneous nephroscopy still performed with the patients prone? J Endourol 1990; 4:269-272
25. Desai M, Ganpule A, Manohar T. ''Multiperc'' for complete staghorn calculus. t om y J Endourol 2008;22(2):267-271 J Endourol 2008;22:1831-1833
26. Turk C, Knoll T, Petrik A. Guidelines on urolithiasis, European Association of Urology. 2012: 102 p. URL: https://uroweb.org/wp-content/uploads/20_Urolithiasis_LR-March-13-2012.pdf
27. Хинман Ф. Оперативная урология. Атлас. М.: ГЭОТАР – Медиа, 2001. 1192 с.
28. Marberger M, Stack I, Hruby W. Percutaneous litholapaxy of renal calculi with ultrasound. Eur Urol 1982;8:236-242
29. Korth K. A new percutaneous pyeloscope with permanent irrigation. BJU Suppl 1983:31-33
30. Мартов А.Г., Ергаков Д.В., Серебрянный С.А., Дзеранов Н.К., Лисовченко С.А. Перкутанная хирургия коралловидного нефролитиаза в эпоху ДЛТ. Материалы Пленума правления Российского общества урологов (Сочи, 28-30 апреля 2003). М., 2003, C. 411-412.
31. Handa RK, Evan AP, Willis LR, Connors BA, Gao S, Kim SC, et al. Time – course for recovery of renal function after unilateral (single-tract) percutaneous access in the pig. J Endourol 2010;24(2):283-288.
32. Unsal A, Koca G, Resorlu B, Bayindir M, Korkmaz M. Effect of percutaneous nephrolithotomy and tract dilatation methods on renal function: assessment by quantitative single-photon emission computed tomography of technetium – 99m – dimercaptosuccinic acid uptake by the kidneys. J Endourol 2010; 24(9):1497-1502
33. De La Rosette J, Assimos D, Desai M, Gutierres J, Lingeman J, Scarpa R, et al. The clinical research office of the endourological society percutaneous nephrolithotomy Global Study: indications, complications and outcomes in 5803 patients. J Endourol 2011;25(1): 11-17
34. Ozden E, Mercimek MN, Bostanci Y, Yakupoglu YK, Sirtbas A, Sarikaya S. Long-term outcomes of percutaneous nephrolithotomy in patients with chronic kidney disease: a single-center experience. Urology 2012;79(5):990-994
35. Allen D, O’Brien T, Tiptath R, Glass J. Defining the Learning Curve for percutaneous nephrolithotomy. J Endourol 2005;19(3):279-282.
36. Schilling D, Gakis G, Walcher U, Stenzl A, Nagele U. The learning curve in minimally invasive percutaneous nephrolitholapaxy: a 1-year retrospective evaluation of a novice and an expert. World J Urol 2011;29(6):749-753
37. Tepeler A, Binbay M, Yuruk E, Sari E, Kaba M, Muslumanoglu AY, et al. Factor affecting the fluoroscopic screening time during percutaneous nephrolithotomy. J Endourol 2009;23(11):1825-1829
38. Desai M. Ultrasonography-guided punctures – with and without puncture guide. J Endourol 2009;23:1641-1643
39. Ritter M, Krombach P, Michel MS. Percutaneous stone removal. Eur Urol Suppl 2011;10:433-439
40. Kawahara T, Ito H, Terao H, Yoshida M, Ogawa T, Uemura H, Kubota Y, Matsuzaki J. Ureteroscopy assisted retrodrade nephrostomy: a new technique for percutaneous nephrolithotomy. BJU Int 2012;110:588-590
41. Portis AJ, Laliberte MA, Drake S, Holtz C, Rosenberg MS, Bretzke CA. Intraoperative fragment detection during percutaneous nephrolithotomy: evaluation of high magnification rotational fluoroscopy combined with aggressive nephroscopy. J Urol 2006;175:162-166
42. Boctor EM, Choti MA, Burdette EC, Webster RJ. Three-dimensional ultrasound-guided robotic needle placement: an experimental evaluation. Int J Med Robot Comput Assist Surg 2008;4:180-191
43. Mozer P, Conort P, Leroy A, Baumann M, Payan Y, Troccaz J, et al. Aid to percutaneous renal access by virtual projection of the ultrasound puncture tract onto fluoroscopic images. J Endourol 2007;21:460-465
44. Hernandez DJ, Sinkov VA, Roberts WW, Allaf ME, Patriciu A, Jarrett TW, Kavoussi LR, Stoianovici D. Measurement of bio-impedance with a smart needle to confirm percutaneous kidney access. J Urol 2001;166:1520-1523
45. Ritter M, Rassweiler MC, Haecker A, Michel MS. Laser-guided percutaneous kidney access with the UroDyna-CT: first experience of three-dimensional puncture planning with an ex-vivo model. World J Urol 2013;31:1147-1151
46. Appelbaum L, Solbiati L, Sosna J, Nissenbaum Y, Greenbaum N, Goldberg SN. Evaluation of an electromagnetic image-fusion navigation system for biopsy of small lesions: assessment of accuracy in an in vivo swine model. Acad Radiol 2013; 20:209-217
47. Müller M, Rassweiler MC, Klein J, Seitel A, Gondan M, Baumhauer M, et al. Mobile augmented reality for computer-assisted percutaneous nephrolithotomy. Int J Comput Assist Radio Surg 2013;8:663-675
48. Challacombe B, Patriciu A, Glass J, Aron M, Jarrett T, Kim F, et al. A randomized controlled trial of human versus robotic and telerobotic access to the kidney as the first step in percutaneous nephrolithotomy. Comput Aided Surg 2005;10:165-171
49. De Sio M, Autorino R, Quattrone C, Giugliano F, Balsamo R, D'Armiento M. Choosing the nephrostomy size after percutaneous nephrolithotomy. World J Urol 2011;29:707-711
50. Shen P, Liu Y, Wang J. Nephrostomy tube-free versus nephrostomy tube for renal drainage after percutaneous nephrolithotomy: a systematic review and meta-analysis. Urol Int 2012;88:298-306
51. Сrook TJ, Lockyer CR, Keoghane SR, Walmsley BH. otally tubeless percutaneous nephrolithot om y J Endourol 2008;22(2):267-271
52. Agrawal MS, Agrawal M. Tubeless percutaneous nephrolithotomy. Indian Urol 2019;26:16-24
53. Falahatkar S, Khosropanah I, Roshani A, Neiroomand H, Nikpour S, Nadjafi-Semnani M, et al. Tubeless percutaneous nephrolithotomy for staghorn stones. J Endourol 2008 22:1447-1451
54. Aghamir SM, Hamidi M, Aloosh M, Mohammadi A, Nikoobakht MR, Meysamie A Efficacy and morbidity following PCNL in patients with renal anomalies: the outcome from a randomized study comparing different imaging modalities for assessment. Minerva Urol Nefrol 2011;63:207-212
55. Wang J, Zhao C, Zhang C, Fan X, Lin Y, Jiang Q. Tubeless vs standard percutaneous nephrolithotomy: a meta-analysis. BJU Int 2011;109:918-924
56. Li R, Louie MK, Lee HJ, Osann K, Pick DL, Santos R. Prospective randomized trial of three different methods of nephrostomy tract closure after percutaneous neprolithotripsy. BJU Int 2010;107:1660-1665
57. Choe CN, L’Esperance JO, Auge BK. The use of adjunctive hemostatic agents for tubeless percutaneous nephrolithotomy. J Endourol 2009 23:1733-1738
58. Rodrigues PL, Rodrigues NF, Fonseca J, Lima E, Vilaça JL. Kidney Targeting and Puncturing During Percutaneous Nephrolithotomy: Recent Advances and Future Perspectives J Endourol 2013;27: 826–834







