ВВЕДЕНИЕ
Несмотря на успехи ранней диагностики рака предстательной железы (РПЖ), представительство местнораспространенных и метастатических форм заболевания остается высоким. Так, за десятилетний период 2012- 2022 гг. удельный вес больных РПЖ III стадии снизился с 31,8% до 15,0%, при том, что доля больных РПЖ IV стадии возросла с 17,8% до 21,6% [1]. Пятилетняя выживаемость при распространенном РПЖ составляет всего 28% [2, 3]. При этом, востребованным методом лечения распространенного рака по-прежнему остается гормональная терапия (ГТ) с использованием агонистов гонадо-ропинрилизинг-гормона (ГнРГ), а время до наступления резистентности к ГТ составляет по данным разных авторов 2-3 года [4-7].
Развитие устойчивости к ГТ клеток РПЖ происходит, главным образом, из-за возникновения генетических изменений в андрогенных рецепторах (АР), что ведет к росту пула андроген-независимых клеток [8]. Изучение механизмов резистентности АР, а именно ферментов, участвующих в синтезе тестостерона, в том числе CYP17, привело к разработке новых лекарственных препаратов – антиандрогенов второго поколения, таких как абиратерон, способного вызывать селективное и необратимое ингибирование CYP17, а также энзалутамида, апалутамида и даролутамида, которые являются низкомолекулярными антагонистами АР [8].
Хотя данные препараты доказали свою приемлемую эффективность и безопасность у больных кастрационно-резистентным раком предстательной железы (КРПРЖ), но и к ним через некоторое время развивается первичная либо вторичная резистентность [9].
Считают, что под влиянием антиандрогенов, в том числе нового поколения, клетки РПЖ могут приобретать различные фенотипы, приводящие к резистентности. Основные пути развития КРРПЖ: утрата опухолевыми клетками андрогенных рецепторов, а также нейроэндокринная трансформация (дифференцировка) (НЭД) раковых клеток, что также приводит к потере рецепторов к андрогенам [10-12].
Важным механизмом возникновения резистентности РПЖ к гормональной терапии, как с применением агонистов ГнРГ, так и новых антиандрогенов, является НЭД опухолевых клеток, которую наблюдают у 25% пациентов с метастатическим РПЖ [13]. В экспериментах in vitro и in vivo было показано, что в условиях кастрационного уровня тестостерона клетки предстательной железы (ПЖ) приобретают фенотипические признаки нейронов, форма их становится более вытянутой, в цитоплазме появляются секреторные гранулы, что сопровождается увеличением экспрессии нейроэндокринных маркеров, снижением экспрессии АР и уровня ПСА [14, 15].
Для выявления НЭД РПЖ используют специфические маркеры, в частности, хромогранин А (ХгА), синаптофизин, нейрон-специфичную енолазу, CD56 (NCAM), экспрессия которых существенно возрастает при наличии НЭД опухоли ПЖ. При этом считают, что наибольшей диагностической ценностью обладает ХгА [16, 17], чувствительность которого по разным данным составляет 60-90%, а специфичность 10-35% [18, 19]. Есть исследования, которые показывают, что нейроэндокринный статус очень важен для эффективного лечения КРРПЖ. Пациенты с РПЖ с высоким уровнем ХгА имели достоверно худший прогноз, по сравнению с пациентами, у которых НЭД опухоли не была выявлена [19, 20]. При этом, снижение ХгА на фоне лечения свидетельствует о терапевтическом эффекте [10, 16].
Установлено, что при развитии НЭД в опухолевых клетках повышается экспрессия рецепторов соматостатина SSTR 2 и SSTR 5 [21-25], а выявленные мутации этих рецепторов обладают проонкогенным эффектом [26]. Визуализация распределения рецепторов соматостатина у больных с КРРПЖ с использованием лигандов, меченых радиоактивным изотопом, подтверждает целесообразность включение в схему комбинированного лечения аналогов соматостатина (АС): октреотид, ланреотид, пасиреотид [24, 27, 28]. При этом наибольшее число исследований по применению АС у больных КРРПЖ было проведено с использованием октреотида в форме депо [24, 27, 29-31]. Более того, с 2023 г. в инструкции по применению депо-формы октреотида отечественного производства в качестве одного из показаний указан КРРПЖ [32].
Роль и терапевтический потенциал АС при опухолях с нейроэндокринным статусом, включая РПЖ, изучены недостаточно. Один из механизмов связывают со снижением уровня IGF-1: или непосредственно, путем подавления экспрессии гена IGF-1 (прямой эффект) или косвенно – вследствие ингибирования печеночной экскреции [33]. Однако публикаций по этому вопросу немного, что требует дополнительных исследований.
Современные подходы к лечению КРРПЖ подразумевают применение антиандрогенов нового поколения, либо химиотерапии в различных комбинациях. Наиболее эффективными режимами химиотерапии для лечения НЭД РПЖ считают комбинации доцетаксела и карбоплатина или карбоплатина и кабазитаксела, однако прогноз для таких пациентов по-прежнему неблагоприятный, а медиана общей выживаемости не превышает 1,5–2 лет [34].
Несмотря на имеющуюся связь НЭД с КРРПЖ и мнение ряда авторов о перспективности комбинации АС с другими противоопухолевыми препаратами [24, 25, 35], этот лечебный подход пока не нашел широкого применения при КРРПЖ и находится на этапе изучения. Если в клинических рекомендациях по РПЖ 2014- 2016 года АС были включены в схему лечения больных КРРПЖ [36], то в клинических рекомендациях последующих лет АС, как терапевтическая опция при КРРПЖ, отсутствует [17].
Интересно вспомнить, что ранее было доложено несколько исследований о сочетанном применении агонистов ГнРГ и АС у больных КРРПЖ, не показавших впечатляющих результатов [27, 37], что несколько снизило общий интерес к этому направлению терапии. Однако необходимо учитывать, что в указанных исследованиях не стратифицировали пациентов в зависимости от исходного уровня маркеров НЭД, например, ХгА. При этом, в опубликованной нами ранее работе было показано, что комбинированное применение агониста ГнРГ, АС и дексаметазона у больных КРРПЖ с исходно повышенным ХгА сыворотки крови продемонстрировало достоверно лучший ответ по динамике ПСА в сравнении с пациентами, имевшими нормальные значения ХгА [35]. В то же время нам не удалось найти других публикаций, где авторы проводили терапию КРРПЖ с применением АС на основе оценки нейроэндокринного статуса опухоли.
С учетом того, что проблема НЭД РПЖ, несмотря на появление новых методов лечения, не потеряла своей актуальности, а также, что использование АС в комбинации с другими лекарственными средствами потенциально способно улучшить результаты лечения больных КРРПЖ с повышенным уровнем ХгА, мы решили опубликовать результаты исследования, проведенного ранее, до периода широкого применения антиандрогенов нового поколения.
МАТЕРИАЛЫ И МЕТОДЫ
C 2014 по 2018 гг. в исследование было включено 89 пациентов с КРРПЖ в возрасте 72,2±1,4 года. Локализованный РПЖ был диагностирован у 6 (6,7%), местнораспространенный РПЖ (T3-4N0M0) диагностирован у 12 (13,5%) больных, метастатический (T3- 4N0-1M1) – у 71 (79,8%). У всех пациентов на этапе включения был подтвержден кастрационный уровень тестостерона сыворотки крови (менее 1,7 нмоль/л или 50 нг/дл). Кроме соматических заболеваний, влияющих на уровень ХгА (нарушение функции почек, гипертензия, лечение глюкокортикоидами, атрофический гастрит типа А, лечение ингибиторами протонной помпы или блокаторами Н2-рецепторов), критерием исключения из исследования была предшествовавшая химиотерапия.
Все пациенты до включения в исследование получали гормональное лечение в режиме максимальной андрогенной блокады по месту жительства. Наступление кастрационной резистентности было выявлено в онкодиспансере по месту наблюдения и подтверждено нами на основании трех последовательных подъемов ПСА более 50% с интервалом более двух недель, либо при прогрессии по метастазам. Пациенты были включены в исследование на этапе решения вопроса о дальнейшем лечении в связи с развившейся кастрационной резистентностью: химиотерапия или участие в исследовании с продолжением комбинированной ГТ в комплексе с аналогами соматостатина и дексаметазоном. Во время набора пациентов доступность антиандрогенов 2 поколения и ингибиторов стероидогенеза носила крайне ограниченный характер и была практически недоступна для большинства пациентов.
Уровень ПСА определяли иммунохемилюминисцентным методом на анализаторе «Access 2» («Beckman Coulter», США) с использованием оригинальных тестсистем, а ХгА – методом иммуноферментного анализа с использованием наборов «Human Chromogranin-A ELISA Kit» («Eu-rodiagnostica», Швеция) на анализаторе «Gemini» («Stratec Biomedical Systems», Швейцария). Референсные значения ХгА для данного метода составляют от 0 до 3 нмоль/л.
Повышение ХгА наблюдали у 31,5% (n=28) больных КРРПЖ. С целью оценки влияния ХгА на эффективность терапии пациенты были разделены на 3 группы: 1-я группа – 61 пациент с нормальным уровнем ХгА (<3 нмоль/л); 2-я группа – 18 больных с повышением уровня ХгА в пределах 3-7 нмоль/л и 3-я группа – 10 больных с уровнем ХгА выше 7 нмоль/л. Выделение групп с разным уровнем ХгА было основано на данных о взаимосвязи степени повышения этого маркера и выраженности прогрессирования РПЖ [38]. Все три группы оказались сопоставимы по возрасту, стадиям РПЖ, медианным значениям суммы баллов Gleason (p>0,05, U тест Манна–Уитни, ДИ 95%, t-критерий). Значение медианы ПСА у пациентов с нормальным ХгА было ниже, чем у больных с его повышенным уровнем, а у лиц с ХгА > 7 нмоль/л было выше, чем при ХгА 3-7 нмоль/л (табл. 1). Во всех группах достоверно отличались между собой медианные значения ХгА (p<0,05, ДИ 95%, U тест Манна–Уитни), остальные показатели во всех группах статистически не отличались (p>0,05, U тест Манна–Уитни, ДИ 95%, t-критерий).
Таблица 1. Сопоставимость групп больных с нормальным и повышенным уровнем ХгА в крови
Table 1. Comparability of patients with normal and elevated levels of serum CgA
| Группы больных Patient groups |
ХгА < 3 моль/л (n=61) CgA < 3 nmol/l (n=61) | ХгА ≥ 3 нмоль/л (n=28) CgA ≥ 3 nmol/l (n=28) | |
|---|---|---|---|
| ХгА 3-7 нмоль/л (n=18) CgA 3-7 nmol/l (n=18) | ХгА >7 нмоль/л (n=10) CgA >7 nmol/l (n=10) | ||
| Средний возраст (лет) Age, years | 71,3 ± 1,6 | 72,8 ± 1,5 | 70,4 ± 1,9 |
| Доля больных с локализованным РПЖ, % Patients with localized prostate cancer, % | 6,6 | 5,5 | 10 |
| Доля больных с местнораспространенным РПЖ, % Patients with locally advanced prostate cancer, % | 13,1 | 16,7 | 10 |
| Доля больных с метастатическим РПЖ, % Patients with metastatic prostate cancer, % | 80,3 | 77,8 | 80 |
| Медиана ПСА (нг/мл) Median PSA (ng/ml) | 57,0 [29,8; 94] | 169,5 [66,3; 235,3] | |
| 160,5 [59,6; 292,8] | 195,5 [34,7; 383,6] | ||
| Медиана ХгА (нмоль/л) Median CgA (nmol/l) | 2,1 [1,9; 2,2] | 5,2 [3,6; 7,1] | |
| 3,6 [3,2; 5,2] | 12,1 [7,5; 14,2] | ||
Комбинированную терапию проводили препаратом Октреотид-депо (ЗАО «Фарм-Синтез», Россия) по следующей схеме: по 20 мг п/к 1 раз в 28 дней в комбинации с дексаметазоном в дозе 4 мг в сутки в течение 1 месяца. Затем дозу дексаметазона снижали до 2 мг в сутки в течение 2 недель, переходя, в последующем, к поддерживающему режиму по 1 мг в сутки. Наряду с этим все больные продолжали получать лечение агонистами ГнРГ.
В настоящее время есть несколько протоколов для оценки эффективности лечения пациентов КРРПЖ, одним из современных является PCWG 3.0. В нашем пилотном исследовании, исходя из его ограниченности по времени и учитывая фактор безопасности (потеря времени до развития метастазов), в качестве критерия оценки эффективности использовали динамику показателя ПСА сыворотки крови, а не прогрессию по метастазам, что ранее применено и в других исследованиях со схожим дизайном [39-41].
Пациентов наблюдали каждые 28 дней. Оценку эффективности лечения проводили на основании ответа по динамике уровня ПСА и ХгА, а также по данным ультразвукового исследования (УЗИ) органов мочеполовой системы, мультиспиральной томографии (МСКТ) брюшной полости, магнитно-резонансной томографии (МРТ) органов таза и остеосцинтиграфии, которые выполняли в том числе в онкологических диспансерах по месту жительства. По динамике ПСА ответом считали снижение медианы ПСА, либо отсутствие роста более 10%. Согласно клиническим рекомендациям, три последовательных увеличения ПСА выше 50% с интервалом более двух недель, расценивают как прогрессию заболевания [17]. Однако в нашем протоколе для повышения безопасности рост ПСА выше 10% уже считали поводом для исключения пациента из исследования, как и появление признаков прогрессирования по данным методов визуализации. Этих пациентов выводили из исследования и направляли на химиотерапию по месту жительства. Продолжительность терапии октреотидом пролонгированного действия у всех пациентов составила не менее трех месяцев, а максимальная – 32 месяца.
Статистическую обработку цифрового материала проводили с помощью компьютерной программы Statistica 13.3 и MedCalc 18. Для оценки средних значений, определения статистической значимости количественных различий между группами применяли t-критерий Стьюдента. При сравнении медианных значений зависимых групп использовали W-критерий (Уилкоксона) и Z-тест Фишера, для сравнения независимых групп U тест Манна–Уитни. Достоверность различий между независимыми группами оценивали при помощи χ2 Пирсона. Динамику сроков наступления прогрессии и выживаемость пациентов оценивали методом Каплана-Мейера. Достоверными считали различия при р<0,05. Построение матрицы рисков оценивали методом определения абсолютного риска (АР) и относительного риска (ОР) при доверительном интервале (ДИ) 95%.
РЕЗУЛЬТАТЫ
Об эффективности терапии Октреотидом-депо судили по 3 параметрам: динамике уровня ПСА в первые 3 месяца после начала терапии, длительности периода без прогрессии заболевания и общей выживаемости пациентов.
При анализе ближайших результатов лечения (через 3 месяца) в группе больных с нормальным уровнем ХгА медиана ПСА достоверно увеличилась: с 57,0 [29,8; 94] нг/мл исходно, до 89,0 [47,4; 131,9] нг/мл, что составило 56,1% (р<0,05, Z-тест Фишера, ДИ 95%). При этом у больных с повышенным уровнем ХгА было отмечено снижение медианного значения ПСА на 35,7%, хотя и статистически незначимое: со 169,5 [66,3; 235,3] нг/мл до 109,0 [44,8; 236,9] нг/мл (р=0,7, W-критерий, ДИ 95%) (рис. 1А).
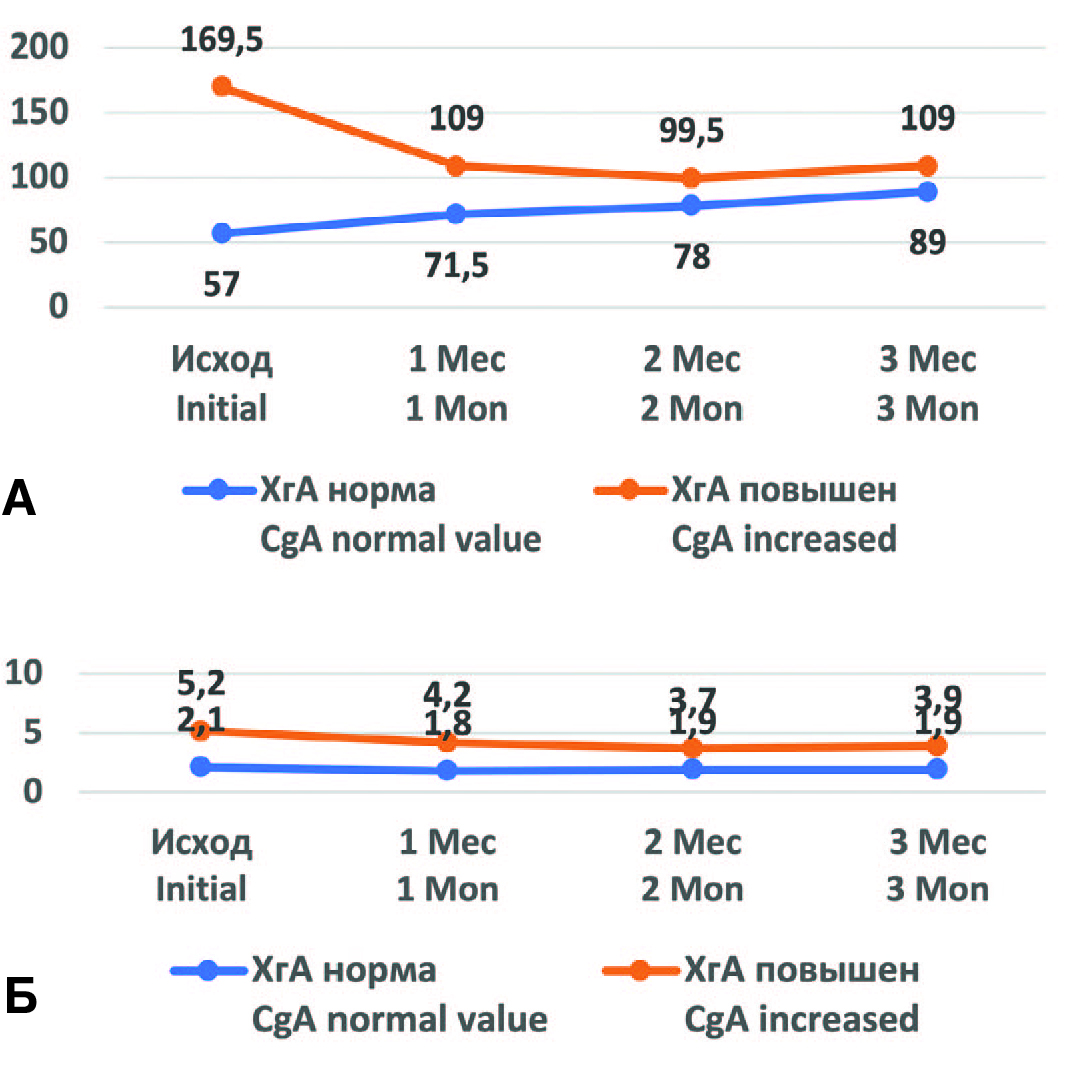
Рис. 1. Динамика уровней ПСА (нг/мл) (А) и ХгА (нмоль/л) (Б) в первые 3 месяца комбинированной терапии у пациентов с исходно нормальным и повышенным уровнем ХгА
Fig. 1. Dynamics of PSA (ng/ml) (A) and CgA (nmol/L) (Б) Dynamics in the first 3 months of combination therapy in patients with initially normal and elevated levels of CgA
При этом у больных с исходно нормальным уровнем ХгА его значения на фоне лечения практически не изменились: 2,1 [1,9; 2,2] нмоль/л в начале и 1,9 [1,7; 2,2] нмоль/л или снижение на 9,5% после 3-х месяцев терапии (р=0,4, Z-тест Фишера, ДИ 95%), тогда как в группе пациентов с изначально повышенным ХгА отмечено его достоверное уменьшение на 25,0% с исходных 5,2 [3,6; 7,1] нмоль/л до 3,9 [2,3; 5,2] нмоль/л (р=0,01, W-критерий, ДИ 95%) (рис. 1Б).
Поскольку мы предполагали, что степень повышения уровня ХгА отражает выраженность злокачественного процесса, были раздельно проанализированы подгруппы пациентов с исходно умеренным повышением ХгА (3-7 нмоль/л) и более значительным увеличением его уровня (> 7 нмоль/л). Характерно, что в первом случае к 3-м месяцам лечения наблюдали снижение ПСА на 45,5%, со 160,5 [59,6; 292,8] нг/мл до 87,5 [34,0; 217,4] нг/мл (р<0,05, W-критерий, ДИ 95%), тогда как во втором – на 31,7%, со 195,5 [34,7; 383,6] нг/мл до 133,5 [31,1; 611,4] нг/мл, однако, разница в последнем случае оказалась статистически недостоверной (р>0,05, W-критерий, ДИ 95%).
Анализ ближайших результатов лечения выявил, что в группе больных с ХгА 3-7 нмоль/л, у 44,4% пациентов на проводимую комбинированную терапию был получен ответ в виде снижения ПСА на 50% и более, а у 11,1% – стабилизация уровня ПСА (снижение менее 50%), тогда как при ХгА < 3 нмоль/л и ХгА > 7 нмоль/л ответ наблюдали у 8,2% и 20,0%, а стабилизацию – у 11,2% и 20,0% больных (табл. 2).
Таблица 2. Сравнительная эффективность терапии больных с нормальным повышенным и уровнем ХгА
Table 2. Comparative effectiveness of therapy in patients with normal elevated and CgA levels
| Параметры Parameters |
Всего больных Patients in total |
1-я группа, n=61 (ХгА < 3 нмоль/л) 1st group, n=61 (CgA < 3 nmol/l) | 2-я группа, n=18 (ХгА - 3-7 нмоль/л) Group 2, n=18 (CgA - 3-7 nmol/l) | 3-я группа, n=10 (ХгА > 7 нмоль/л) Group 3, n=10 (CgA > 7 nmol/l) |
|---|---|---|---|---|
| Снижение ПСА <50%, n (%) PSA decrease <50%, n (%) | 10 (11,2) | 6 (9,8) | 2 (11,1) | 2 (20,0)* |
| Снижение ПСА >50%, n (%) Decrease in PSA >50%, n (%) | 15 (16,9) | 5 (8,2) | 8 (44,4) | 2 (20,0)* |
| Прогрессия РПЖ, n (%) PC progression, n (%) | 64 (71,9) | 50 (82) | 8 (44,4) | 6 (60,0)* |
Достоверность различий между группами p=0,01* (χ2)
The significance between groups is p=0.01* (χ2)
Соответствующе выглядела и динамика ХгА: у пациентов 2-й группы отмечено снижение среднего показателя на 30,6%, с 3,6 [3,2; 5,2] нмоль/л до 2,5 [1,6; 4,2] нмоль/л (р<0,05, W-критерий, ДИ 95%), тогда как в 3-й группе уменьшение ХгА составило всего 5,0%, с 12,1 [7,5; 14,2] нмоль/л до 11,5 [4,5; 14,1] нмоль/л (р>0,05, W-критерий, ДИ 95%), однако, разница в последнем случае оказалась статистически недостоверной. Примечательно, что если на фоне лечения у большинства исследуемых группы 2 значения ХгА вернулись к нормальным значениям, то в 3-й группе таких пациентов практически не было (табл. 3).
Таблица 3. Динамика ПСА и ХгА в течение 3х месяцев лечения в подгруппах с разным исходным уровнем ХгА (ДИ 95%)
Table 3. PSA and CgA dynamics during 3 months of treatment in subgroups with different baseline levels of CgA (95% CI)
| Показатели Parameters |
ХгА < 3 нмоль/л (n = 61) CgA < 3 nmol/l (n = 61) | ХгА 3-7 нмоль/л (n = 18) CgA 3-7 nmol/l (n = 18) |
ХгА > 7 нмоль/л (n = 10) CgA > 7 nmol/L (n = 10) | |
|---|---|---|---|---|
| ПСА (нг/мл) PSA (ng/ml) | до лечения initial |
57,0 [29,8; 94] | 160,5 [59,6; 292,8] | 195,5 [34,7; 383,6] |
| через 1 месяц in 1 month |
71,5 [36,9; 87,2] | 87,5 [54,9; 253,5] | 159,5 [50,3; 482,4] | |
| через 2 месяца in 2 month |
78,0 [40,9; 129,2] | 90,4 [35,8; 214,9] | 147,0 [33,7; 429,5] | |
| через 3 месяца in 3 month |
89,0 [47,4; 131,9] | 87,5 [34,0; 217,4] | 133,5 [31,1; 611,4] | |
| ХгА (нмоль/л) CgA (nmol/l) | до лечения initial |
2,1 [1,9; 2,2] | 3,6 [3,2; 5,2] | 12,1 [7,5; 14,2] |
| через 1 месяц in 1 month |
1,8 [1,5; 2,0] | 3,1[2,3; 4,2] | 8,2 [6,5; 11,8] | |
| через 2 месяца in 2 month |
1,9 [1,6; 2,2] | 2,5 [1,7; 4,2] | 11,2 [4,8; 12,5] | |
| через 3 месяца in 3 month |
1,9 [1,7; 2,2] | 2,5 [1,6; 4,2] | 11,5 [4,5; 14,1] | |
Показательно, что в группе больных с исходно нормальным уровнем ХгА, спустя 3 месяца на другой вид лечение были переведены 50 (82%) пациентов, ввиду прогрессии РПЖ, соответственно, доля ответивших на лечение снижением или стабилизацией ПСА (n=11), составила всего 18%, тогда как среди лиц с ХгА> 3 нмоль/л – уже 50% (n=14) (p=0,004, χ2 Пирсона).
В подгруппе пациентов с ХгА (3-7 нмоль/л) спустя 3 месяца лечения 8 пациентов были исключены из исследования ввиду прогрессии РПЖ, соответственно, доля пациентов, ответивших на лечение снижением или стабилизацией ПСА, составила 56% (n=10). В подгруппе с повышенным ХгА более 7 нмоль/л в этот же период времени из исследования по аналогичной причине были исключены 6 больных, остальные 40% (n=4) продолжили участие (рис. 2). Различия между группами были недостоверны.
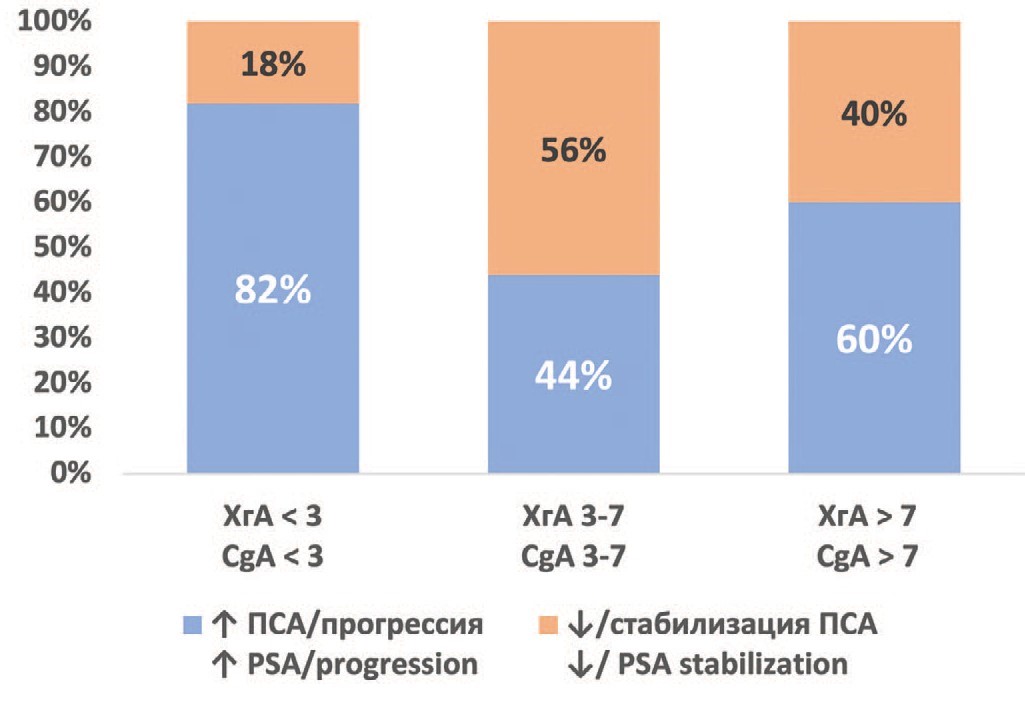
Рис. 2. Доля пациентов (в %) ответивших на лечение снижением или стабилизацией ПСА через 3 месяца терапии октреотидом-депо: группа А – ХгА ниже 3 (нмоль/л), группа Б – ХгА 3-7 (нмоль/л), группа В – ХгА от 7 (нмоль/л)
Fig. 2. Patients (in %) responded to treatment with a decrease or stabilization of PSA after 3 months of octreotide-depot therapy: group A - CgA < 3 (nmol/l), B – CgA 3-7 (nmol/l), C – CgA > 7 (nmol/l)
Таким образом, общая доля пациентов, ответивших снижением или стабилизацией ПСА на комбинированную терапию, составила 28% (n=25). Медианные значения и доля снижения ПСА в группе «ответчиков», стратифицированных по уровню ХгА, до и после 3-х месяцев лечения составили, соответственно:
- в группе с нормальными значениями ХгА – 43,0 [16,5; 154,3] нмоль/л и 15,2 [7,2; 48,8] нмоль/л или 64,7% (р<0,02, W-критерий, ДИ 95%);
- при ХгА 3-7 нмоль/л – 160,5 [35,1; 278,6] нмоль/л и 42,4 [14,1; 88,4] нмоль/л или 73,6% (р=0,004, W-критерий, ДИ 95%);
- у больных с ХгА более 7 нмоль/л – 166,5 [28,0; 222,0] нмоль/л и 81,7 [16,4; 151,0] нмоль/л или 50,9%, что, однако, оказалась статистически недостоверным (р>0,05, Z-тест Фишера, ДИ 95%) (табл. 4).
Таблица 4. Динамика ПСА и ХгА в течение трех месяцев лечения в подгруппах «ответчиков» (показавших снижение или стабилизацию ПСА) с разным исходным уровнем ХгА (ДИ 95%)
Table 4. PSA and CgA dynamics during 3 months of treatment in subgroups of «responders» (who showed a decrease or stabilization of PSA) with different baseline levels of CgA (95% CI)
| Показатели Parameters |
ХгА < 3 нмоль/л (n = 11) CgA < 3 nmol/l (n = 11) | ХгА 3-7 нмоль/л (n = 10) CgA 3-7 nmol/l (n = 10) |
ХгА > 7 нмоль/л (n = 4) CgA > 7 nmol/L (n = 4) | |
|---|---|---|---|---|
| ПСА (нг/мл) PSA (ng/ml) | до лечения initial |
43,0 [16,5; 154,3] | 160,5 [35,1; 278,6] | 166,5 [28,0; 222,0] |
| через 1 месяц in 1 month |
62,5 [13,5; 145,6] | 66,5 [32,7; 172,0] | 132,5 [50,0; 176,0] | |
| через 2 месяца in 2 month |
15,0 [9,0; 173,0] | 55,0 [19,5; 92,3] | 115,5 [14,0; 169,0] | |
| через 3 месяца in 3 month |
15,2 [7,2; 48,8] | 42,4 [14,1; 88,4] | 81,7 [16,4; 151,0] | |
| ХгА (нмоль/л) CgA (nmol/l) | до лечения initial |
1,7 [1,3; 2,2] | 3,6 [3,1; 5,5] | 12,3 [10,0; 16,0] |
| через 1 месяц in 1 month |
1,4 [0,9; 1,8] | 2,4 [1,8; 3,8] | 8,3 [6,0; 13,2] | |
| через 2 месяца in 2 month |
1,2 [0,9; 2,0] | 2,1 [1,1; 2,5] | 9,4 [2,4; 12,0] | |
| через 3 месяца in 3 month |
1,2 [0,6; 1,7] | 1,9 [1,2; 3,0] | 9,9 [2,3; 14,0] | |
Снижение ХгА в подгруппах «ответчиков» через 3 месяца лечения также различалось и составило:
- у пациентов с исходно нормальными значениями ХгА (n=11): 1,7 [1,3; 2,2] нмоль/л → 1,2 [0,6; 1,7] нмоль/л или 29,4% (р=0,01, W-критерий, ДИ 95%);
- при ХгА 3-7 нмоль/л (n=10) : 3,6 [3,1; 5,5] нмоль/л → 1,9 [1,2; 3,0] нмоль/л или 47,2% (р=0,02, W-критерий, ДИ 95%);
- при ХгА более 7 нмоль/л (n=4): 12,3 [10,0; 16,0] нмоль/л → 9,9 [2,3; 14,0] нмоль/л или 19,5% (р<0,02, Z-тест, ДИ 95%).
Таким образом, анализ ближайших результатов терапии больных КРРПЖ октреотидом-депо в комбинации с агонистами ГнРГ и дексаметазоном показал, что ее эффективность выше у пациентов с исходно увеличенным уровнем ХгА, причем достигнутые результаты выглядят предпочтительнее у пациентов с умеренным повышением этого маркера (в пределах 3- 7 нмоль/л).
В дальнейшем, пациенты-«ответчики» продолжили проводимую терапию до возникновения прогрессии по ПСА или по данным методов визуализации. Критериями оценки отдаленных результатов считали длительность выживаемости без прогрессирования (ВБП), которую определяли, как период времени от начала лечения до прогрессирующего роста уровня ПСА на 50% и более при 3х-кратном измерении с интервалом 2-4 недели или при получении данных МРТ и/или ОСГ о прогрессировании злокачественного процесса и общую выживаемость пациентов. Для их оценки был использован статистический метод Каплана-Мейера с построением соответствующих кривых, а также показателей медианы и определение индивидуального АР и сравнительного ОР при ДИ 95%.
Средняя длительность ВБП в группе больных с нормальным уровнем ХгА, с учетом продолживших лечение, составила 6 [5,66-9,79] месяцев (ДИ 95%, АР=0,836), тогда как у пациентов с повышенным значением этого маркера – 9,5 [8,04-12,25] месяцев (ДИ 95%, АР=0,64, ОР 0,77 [0,51-1,15], ДИ 95%, W-критерий, p=0,096). При сравнении ВБП у пациентов с разной степенью повышения маркера оказалось, что средний период ремиссии был достоверно продолжительнее при ХгА 3-7 нмоль/л – 12 [9,50-13,09] месяцев (АР=0,444, ОР=0,53 [0,31-0,90], ДИ – 0,95%, W-критерий, p=0,021). В группе пациентов с ХгА > 7 нмоль/л медиана ВБП составила 5 месяцев [4,54-9,09] (ДИ – 0,95%). Эти значения статистически значимо не отличались от значений в группе с нормальным ХгА (Z- тест, p=0,123), но были достоверно хуже, чем в группе пациентов с ХгА 3-7 нмоль/л (Z-тест, p=0,038). Также продолжительность ВБП у больных с исходным уровнем ХгА 3-7 нмоль/л оказалась достоверно больше (W-критерий, p=0,042), чем у пациентов с нормальным уровнем маркера (рис. 3).
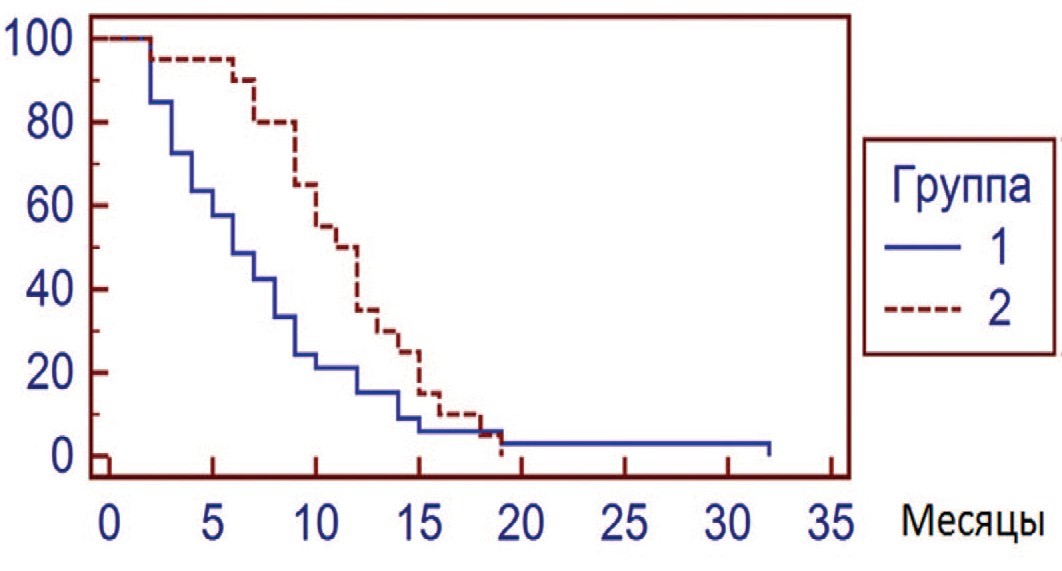
Рис. 3. Кривые Каплана-Мейера ВБП по ПСА на фоне комбинированной терапии больных КРРПЖ в группах нормальным уровнем ХгА (Группа 1) и ХгА 3-7 нмоль/л (Группа 2) (W-критерий, р=0,042)
Fig. 3. Kaplan-Meyer curves of PFS for PSA against the background of combination therapy of CRPC patients in groups with normal levels of CgA (Group 1) and CgA 3-7 nmol/l (Group 2) (W-criterion, р=0.042)
То есть, отсутствие достоверных различий по ВБП между группами с нормальным и повышенным уровнем ХгА, вероятно, обусловлено снижением эффективности комбинированной терапии у больных с высокими значениями этого маркера.
ОБСУЖДЕНИЕ
Лечение больных с КРРПЖ остается существенной проблемой в связи с высокой летальностью в этой группе пациентов, несмотря на появление новых противоопухолевых средств [42]. Существенную роль может играть нейроэндокринная трансформация опухолевых клеток с изменением их рецепторного аппарата, в частности, повышением экспрессии рецепторов соматостатина [25]. Учитывая частую связь КРРПЖ с НЭД, в ряде исследований в схему лечения этой категории больных включали аналоги (агонисты) соматостатина (октреотид, ланреотид, пасиреотид), в том числе в комбинации с агонистами ГнРГ и дексаметазоном [43].
По данным исследований, эффективность применения АС в комбинированной терапии КРРПЖ показала некоторую эффективность [40]. Однако в большинстве работ такое лечение показало «скромные» результаты, так как его проводили без оценки наличия или отсутствия НЭД РПЖ и не используя определение экспрессии специфических маркеров, в частности, ХгА [24, 29, 31, 44]. Считаем, что такой недифференцированный подход негативно повлиял на показатели эффективности терапии.
Ранее нами получены данные, что у больных с КРРПЖ и повышенным уровнем ХгА в крови эффективность терапии окреотидом-депо в сочетании с агонистом ГнРГ и дексаметазоном, оцененная в раннем периоде после начала терапии по степени снижения уровня ПСА, существенно выше, чем у аналогичных больных с нормальным уровнем этого маркера [35]. Однако данные о роли стратификации пациентов по уровню ХгА и ее связи с более отдаленными результатами и ВБП в литературе отсутствуют.
В связи с этим несколько лет назад нами было проведено данное исследование, в котором удалось показать, что определение уровня ХгА в крови пациентов с КРРПЖ, как маркера НЭД, позволяет выделить мужчин, которым целесообразно назначение аналогов соматостатина в комплексной терапии КРРПЖ. У больных с нормальным уровнем ХгА лечение октреотидом-депо в комбинации с агонистом ГнРГ и дексаметазоном оказалось малоэффективно, что проявилось низкой (18%) частотой положительного ответа по ПСА к трем месяцам лечения, тогда как при повышенном значении ХгА положительный результат был достоверно выше – у 50% исследуемых. Показательный результат дала стратификация пациентов по уровню исходного повышения ХгА: доля «ответчиков» во 2-й группе больных достигла 56%, тогда как в 3-й группе – всего 40%.
Это также наглядно проявилось динамикой ПСА, который на фоне лечения достоверно вырос у пациентов 1-й группы на 56,1%, но статистически значимо снизился на 45,5% во 2-й и на 31,7% (недостоверно) в 3-й группах соответственно. Изменение уровня ПСА сопровождалось характерной динамикой ХгА: незначительное уменьшение на 9,5% и 5,0% у пациентов 1-й и 3-й групп соответственно и достоверное снижение на 30,6% во 2-й группе.
Пациенты, положительно ответившие на лечение, продемонстрировали более значимое снижение ПСА (на 50,9-73,6 нг/мл), причем наилучший результат был достигнут при исходном ХгА 3-7 нмоль/л: достоверное снижение уровня ПСА>50% у 44,4% больных, по сравнению с 8,2% и 20,0% в 1-й и 2-й группах. В последнем случае уменьшение уровня ХгА также было наибольшим – 47,2%, тогда как у больных с исходно нормальным ХгА – 29,4%, при ХгА 3-7 нмоль/л – всего 19,5%.
Следует отметить, что в настоящем исследовании с целью безопасности мы применили достаточно жесткие критерии, считая неудовлетворительным результатом повышение ПСА>10%, хотя в ряде других работ рост ПСА до 50% не обозначали как прогрессию, рассчитывая на более отдаленный эффект октреотида [31]. Достижение некоторого эффекта комбинированной терапии у больных с исходно нормальным уровнем ХгА может быть объяснено или уже наличием субклинической НЭД, не определяемой маркерами в крови, или противоопухолевыми эффектами октреотида, непосредственно не связанными с соматостатиновыми рецепторами, что было описано ранее [45]. Сообщают, что АС обладают прямым и непрямым механизмами действия на опухолевые клетки. Прямое противоопухолевое действие реализуется через рецепторы соматостатина и включают блокаду митогенных сигналов, обусловленных факторами роста и индукцию апоптоза. Непрямые противоопухолевые эффекты заключаются в ингибировании высвобождения факторов роста и гормонов, стимулирующих рост опухоли, в антиангиогенном действии, уменьшающим приток крови и в иммуномодуляции, стимулирующей естественные противоопухолевые механизмы организма [45, 46]. Таким образом, несмотря на недостаточность рецепторов соматостатина при нормальном уровне ХгА, часть пациентов КРРПЖ все же достигает терапевтического эффекта (рис. 4).
![Прямой и непрямой механизмы противоопухолевого действия аналогов соматостатина [45]](https://ecuro.ru/sites/default/files/issue/1-2024/ecu1_2024_029.jpg)
Рис. 4. Прямой и непрямой механизмы противоопухолевого действия аналогов соматостатина [45]
Fig. 4. Direct and indirect mechanisms of antitumor action of somatostatin analogues [45]
Безрецидивная выживаемость у больных, продолживших лечение, также оказалась связана с исходным уровнем маркера. Она составила: при нормальных значениях ХгА – 6 месяцев; при ХгА > 3 нмоль/л – 9,5 месяцев; при ХгА 3-7 нмоль/л – 12 месяцев; при ХгА > 7 нмоль/л – 5 месяцев. Причем, продолжительность ВБП в группе 2 оказалась статистически выше. При этом, в исследованиях без стратификации пациентов по исходному уровню ХгА продолжительность ВБП равна, в среднем, 7-8 месяцев [29, 30, 27, 44].
Таким образом, при наличии умеренно выраженной нейроэндокринной трансформации клеток РПЖ комбинированная терапия с октреотидом-депо демонстрирует обнадеживающие результаты, тогда как при значительных изменениях с высоким уровнем ХгА эффективность лечения не отличается от таковой при отсутствии НЭД. На наш взгляд, это различие может быть связано с тем, что у пациентов с более высоким уровнем ХгА к моменту начала терапии произошли более значительные патологические изменения, активирующие другие механизмы прогрессии КРРПЖ, помимо рецепторов соматостатина. Подтверждением этой точки зрения являются данные об индивидуальной динамике ХгА в процессе терапии в группах с разной степенью его исходного повышения. Если при ХгА нмоль/л наблюдали прогрессивное снижение маркера до нормы у всех больных, то при повышении выше 7 нмоль/л он нормализовался лишь у 1 пациента, свидетельствуя о персистенции НЭД. Эти данные косвенно указывают на значимость степени начального повышения ХгА в отношении прогноза эффективности данного вида терапии, поскольку отсутствие нормализации маркера НЭД в ответ на ингибирование рецепторов соматостатина может свидетельствовать об утрате контроля этого пути прогрессии КРРПЖ.
Важный вопрос связан с влиянием лечения октреотидом-депо на назначаемую в последующем противоопухолевую терапию. По-видимому, комбинированная терапия с включением АС у больных с НЭД на какое-то время тормозит патологический процесс, подавляя в той или иной степени НЭД – один из механизмов прогрессирования КРРПЖ. При этом, по мнению ряда авторов, эффективность дальнейшей терапии после прекращения действия октреотида-депо не снижается. Продемонстрировано, что лечение октреотидом-депо не оказывает негативного действия на эффективность последующего применения доцетаксела или абиратерона [30]. Оно демонстрирует большую результативность до назначения химиотерапии 1-й линии: полный или частичный ответ был получен в 70,9% и 60,5% случаев, соответственно [31].
Применение АС в комбинированной терапии КРРПЖ также может иметь и экономическую целесообразность. Более позднее начало последующей терапии оказывает выраженный экономический эффект за счет использования менее дорогостоящих препаратов, что позволяет сэкономить до 17% средств в первый год лечения и еще более значительную сумму в дальнейшем [47].
И, наконец, недавние исследования показывают, что резистентность к антиандрогенам второй линии у некоторых больных при лечении КРРПЖ также возникает через механизм НЭД [48]. То есть появление новых методов гормонального лечения РПЖ не снимает с повестки дня проблему НЭД, которая, по нашему мнению, должна оставаться в поле зрения специалистов.
ЗАКЛЮЧЕНИЕ
Нейроэндокринная дифференцировка клеток, возникающая в результате гормональной терапии РПЖ – важная научная и клиническая проблема, не теряющая актуальности и в настоящее время «новых» антиандрогенов. Раннее выявление НЭД при КРРПЖс применением маркера ХгА позволяет стратифицировать больных по ее выраженности и предложить комбинированную терапию с включением АС. Анализ ближайших результатов лечения КРРПЖ октреотидом-депо в комбинации с агонистами ГнРГ и дексаметазоном показал достоверно более высокую эффективность у пациентов с исходно увеличенным уровнем ХгА, причем достигнутые результаты выглядят предпочтительнее у пациентов с умеренным повышением этого маркера (в пределах 3-7 нмоль/л).
Cчитаем, что изучение нейроэндокринного статуса опухоли перспективно у больных КРРПЖ, получающих антиандрогены нового поколения, у которых применение АС в комбинации оправдано «включением» независимого механизма воздействия на опухоль.
ЛИТЕРАТУРА
- Каприн А.Д., Старинский В.В., Шахзадова А.О. Состояние онкологической помощи населению России в 2022 году. М.: МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России 2022, c. 1-239. [Kaprin A.D., Starinsky V.V., Shakhzadova A.O. Th state of oncological care for the population of Russia in 2022. Moscow: P.A. Herzen Moscow State Medical Research Institute – branch of the Federal State Budgetary Institution «NMIC of Radiology» of the Ministry of Health of Russia 2022, p. 1-239. (In Russian)].
- Попов С.В., Гусейнов Р.Г., Хижа В.В., Язенок А.В., Орлов И.Н., Сивак К.В., и соавт. Рак предстательной железы: современная ситуация в России и г. Санкт-Петербурге по данным медико-статистических показателей. Онкоурология 2023;19(1):102-14. [Popov S.V., Guseynov R.G., Khizha V.V., Yazenok A.V., Orlov I.N., Sivak K.V., et al. Prostate cancer: current situation in Russia and Saint Petersburg according to medical statistical indicators. Onkourologiya = Cancer Urology 2023;19(1):102-14. (In Russian)] https://doi.org/10.17650/1726-9776-2023-19-1-102-114.
- Siegel DA, O’Neil ME, Richards TB, Dowling NF, Weir HK. Prostate Cancer Incidence and Survival, by Stage and Race/Ethnicity – United States, 2001-2017. MMWR Morb Mortal Wkly Rep 2020;69(41):1473-80. https://doi.org/10.15585/mmwr.mm6941a1.
- Desai K, McManus JM, Sharifi N. Hormonal therapy for prostate cancer. Endocr Rev
2021;42(3):354-73. https://doi.org/10.1210/endrev/bnab002.
- McDonald J, O’Brien J, Kostos L, Lawrentschuk N, Azad AA, Murphy D, Chen K. Systemic ther-apy in metastatic hormone-sensitive prostate cancer. Curr Opin Support Palliat Care 2022;16(4):234-9. https://doi.org/10.1097/SPC.0000000000000622.
- Menges D, Yebyo HG, Sivec-Muniz S, Haile SR, Barbier MC, Tomonaga Y, et al. Treatments for metastatic hormone-sensitive prostate cancer: systematic review, network metaanalysis, and benefitharm assessment. Eur Urol Oncol 2022;5(6):605-16. https://doi.org/10.1016/j.euo.2022.04.007.
- Omrčen T. Systemic triple therapy in metastatic hormone sensitive prostate cancer (MHSPC). Acta clinica Croatica 2022;61(Suppl 3):81–5. https://doi.org/10.20471/acc.2022.61.s3.12.
- Pienta KJ, Bradley D. Mechanisms underlying the development of androgen-independent prostate cancer. Clin Cancer Res 2006;12(6):1665-71. https://doi.org/10.1158/1078-0432.CCR-06-0067.
- Aurilio G, Cimadamore A, Mazzucchelli R, Lopez-Beltran A, Verri E, Scarpelli M, et al. Androgen receptor signaling pathway in prostate cancer: from genetics to clinical applications. Cells 2020;9(12):2653. https://doi.org/10.3390/cells9122653.
- Conteduca V, Scarpi E, Salvi S, Casadio V, Lolli C, Gurioli G, et al. Plasma androgen receptor and serum chromogranin A in advanced prostate cancer. Scientific Reports 2018;8(1):15442. https://doi.org/10.1038/s41598-018-33774-4.
- Montironi R, Cimadamore A, Lopez-Beltran A, Scarpelli M, Aurilio G, Santoni M, et al. Mor- phologic, molecular and clinical features of aggressive variant prostate cancer. Cells 2020;9(5):1073. https://doi.org/10.3390/cells9051073.
- Beltran H, Demichelis F. Th py considerations in neuroendocrine prostate cancer: what next?
Endocr Relat Cancer 2021;28(8):T67–T78. https://doi.org/10.1530/ERC-21-0140.
- Patel GK, Chugh N, Tripathi M. Neuroendocrine Differentiation of prostate cancer-an intriguing example of tumor evolution at play. Cancers (Basel) 2019;11(10):1405. https://doi.org/10.3390/cancers11101405.
- Lin D, Wyatt AW, Xue H, Wang Y, Dong X, Haegert A, et al. High fidelity patient-derived xeno-grafts for accelerating prostate cancer discovery and drug development. Cancer research 2014;74(4):1272–83. https://doi.org/10.1158/0008-5472.CAN-13-2921-T.
- Yang X, Yang Y, Li Z, Cheng C, Yang T, Wang C, et al. Diagnostic value of circulating c hro-mogranin a for neuroendocrine tumors: a systematic review and meta-analysis. PloS One 2015;10(4):e0124884. https://doi.org/10.1371/journal.pone.0124884.
- Szarvas T, Csizmarik A, Fazekas T, Hüttl A, Nyirády P, Hadaschik B, et al. Comprehensive analysis of serum chromogranin A and neuron-specifi enolase levels in localized and castration-resistant prostate cancer. BJU Int 2021;127(1):44–55. https://doi.org/10.1111/bju.15086.
- Носов Д.А., Волкова М.И., Гладков О.А., Карабина Е.В., Крылов В.В., Матвеев В.Б., Митин Т., Попов А.М. Практические рекомендации по лечению рака предстательной железы. Злокачественные опухоли 2022;12(3S2-1):607–26. [Nosov D.A., Volkova M.I., Gladkov O.A., Karabina E.V., Krylov V.V., Matveev V.B., Mitin T., Popov A.M. Practical recommendations for the treatment of prostate cancer. Zlokachestvennyye opukholi = Malignant Tumousis 2022;12(3S2-1):607-26 (In Russian)]. https://doi.org/10.18027/2224-5057-2022-12-3s2-607-626.
- Marotta V, Nuzzo V, Ferrara T, Zuccoli A, Masone M, Nocerino L, et al. Limitations of Chromogranin A in clinical practice. Biomarkers 2012;17(2):186–91. https://doi.org/10.3109/1354750X.2012.654511.
- Guo Z, Wang Y, Xiang S, Wang S, Chan FL. Chromogranin A is a predictor of prognosis in patients with prostate cancer: a systematic review and meta-analysis. Cancer Manag Res 2019;11:2747–58. https://doi.org/10.2147/CMAR.S190678.
- Ischia R, Hobisch A, Bauer R, Weiss U, Gasser RW, Horninger W, et al. Elevated levels of serum secretoneurin in patients with therapy resistant carcinoma of the prostate. J Urol 2000;163(4):1161–5.
- Pedraza-Arévalo S, Hormaechea-Agulla D, Gómez-Gómez E, Requena MJ, Selth LA, Gahete MD, et al. Somatostatin receptor subtype 1 as a potential diagnostic marker and therapeutic target in prostate cancer. Prostate 2017;77(15):1499–511. https://doi.org/10.1002/pros.23426.
- Dos Santos G, García Fontes M, Engler H, Alonso O. Intraindividual comparison of 68Ga-DOTATATE PET / CT vs 11C-Choline PET / CT in patients with prostate cancer in biochemical relapse: in vivo evaluation of the expression of somatostatin receptors. Comparación intraindividual de la PET/TC con 68Ga-DOTATATE vs. PET/TC con 11C-colina en pacientes con cáncer de próstata en recaída bioquímica: evaluación in vivo de la expresión de receptores de la somatostatina. Rev Esp Med Nucl Imagen Mol (Engl Ed) 2019;38(1):29–37. https://doi.org/10.1016/j.remn.2018.08.005.
- Werner RA, Bundschuh RA, Bundschuh L, Javadi MS, Higuchi T, Weich A, et al. Molecular imaging reporting and data systems (MI-RADS): a generalizable framework for targeted radiotracers with theranostic implications. Ann Nucl Med 2018;32(8):512–22. https://doi.org/10.1007/s12149-018-1291-7.
- Алексеев Б.Я., Нюшко К.М. Роль аналогов соматостатина в лечении больных кастрационно-рефрактерным раком предстательной железы. Онкология. Журнал им. П.А. Герцена 2012;1(2):100-2. [Alekseev B.Ya., Niushko K.M. Role of somatostatin analogues in the treatment of patients with castration-refractory prostate cancer. Onkologiya. Zhurnal imeni P.A. Gertsena =
P.A. Herzen Journal of Oncology 2012;1(2):100-2. (In Russian)].
- Kitajima K, Yamamoto S, Ikeda M, Yamasaki T, Kawanaka Y, Komoto H, et al. Pelvic MRI, FDG-PET/CT, and somatostatin receptor scintigraphy fi gs of treatment-related neuroendocrine-differentiated prostate cancer. Case Rep Oncol 2021;14(1):397–402. https://doi.org/10.1159/000511070
- Hormaechea-Agulla D, Jiménez-Vacas JM, Gómez-Gómez E, L-López F, Carrasco-Valiente J, Valero-Rosa J, et al. Th oncogenic role of the spliced somatostatin receptor sst5TMD4 variant in prostate cancer. FASEB J 2017;31(11):4682–96. https://doi.org/10.1096/fj.201601264RRR
- Mitsiades CS, Bogdanos J, Karamanolakis D, Milathianakis C, Dimopoulos T, Koutsilieris
M. Randomized controlled clinical trial of a combination of somatostatin analog and dexamethasone plus zoledronate vs. zoledronate in patients with androgen ablation-refractory prostate cancer. Anticancer Res 2006;26(5B):3693–700.
- Тищенко В.К., Петриев В.М., Крылов В.В., Власова О.П., Шегай П.В., Иванов С.А., Каприн А.Д. Аналоги соматостатина, меченные радионуклидами, для терапии онкологических заболеваний. Обзор. Радиация и риск (Бюллетень Национального радиационно-эпидемиологического регистра) 2022;31(2):76-96. [Tishchenko V.K., Petriev V.M., Krylov V.V., Vlasova O.P., Shegai P.V., Ivanov S.A., Kaprin A.D. Radiolabeled somatostatin analogs for cancer treatment. Review. Radiatsiya i risk (Byulleten' Natsional'nogo radiatsionno-epidemiologicheskogo registra) = Radiation and Risk (Bulletin of the National Radiation and Epidemiological Register) 2022;31(2):76-96 (In Russian)]. https://doi.org/10.21870/0131-3878-2022-31-2-76-96
- Ганов Д. И., Варламов С. А. Опыт применения октреотида у пациентов с кастрационно-рефрактерным раком предстательной железы. Онкоурология 2011;(4):71-4. [Ganov D. I., Varlamov S. A. Experience with Octreotide in patients with castration refractory prostate cancer. Onkourologiya = Cancer urology 2011;(4):71-4. (In Russian)].







