ВВЕДЕНИЕ
Мочекаменная болезнь (МКБ) – широко распространенное заболевание, довольно значимое в здравоохранении и в социальной сфере. Одна из форм уролитиаза – фосфатная. Доля фосфатных конкрементов достигает 35% от всех случаев МКБ. Пациенты с фосфатной формой МКБ – сложная категория больных, требующих пристального внимания врачей, так как фосфатные камни в большинстве своем имеют инфекционную природу, и, помимо метаболических нарушений, в организме происходит воспалительный инфекционный процесс. Причина столь сложного механизма – инфекции, вызываемые бактериями, продуцирующими фермент уреаза, который, в свою очередь, расщепляет мочевину, защелачивая мочу и способствуя дальнейшему размножению бактерий и формированию камня.
Стоит отметить, что особого отношения требуют пациенты с различными дренажами мочевыводящих путей, так как при постоянных или длительно стоящих дренажах невозможно добиться стерильности мочи. По данным российского исследования ЭРГИНИ, катетерассоциированные инфекции составляют порядка 35% от всех внутрибольничных инфекций мочевыводящих путей (ИМП) [1]. В США катетер-ассоциированные инфекции мочевыводящих путей являются наиболее распространенными ИМП и ежегодно приводят к 13 000 смертей [2]. При лечении подобных пациентов не стоит забывать, что снижение роста фосфатных камней не менее значимо, чем антибиотикотерапия.
Сложная клиническая картина при фосфатной форме мочекаменной болезни обуславливает постоянный поиск различных вариантов пероральной терапии. Одним из комплексов, которые врачи могут взять на вооружение, является «Фосфалит®», в состав которого входят бергенин, карбонат кальция, ниацинамид и экстракт клюквы.
Цель настоящего исследования – оценить эффективность комплекса «Фосфалит®» в качестве средства коррекции метаболических нарушений при фосфатной форме МКБ.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводилось на базе кафедры урологии и андрологии с курсом ДПО ФГБОУ ВО «Алтайский ГМУ» Минздрава России, ГБУЗ НО «Нижегородская областная клиническая больница им. Н.А. Семашко» и ЧУЗ Центральная клиническая больница «РЖД-Медицина».
Данное клиническое исследование было проведено как проспективное рандомизированное контролируемое когортное. Исследуемая популяция состояла из пациентов с лабораторно верифицированным фосфатным уролитиазом (витлоткит, апатит, гидроксиапатит, октакальция фосфат, трипельфосфат (струвит), карбонат апатит, брушит). Диагноз фосфатного уролитиаза устанавливался одним из трех способов: анализ химического состава конкремента, биохимический анализ мочи, обнаружение кристаллов фосфатов при исследовании осадка мочи
На старте исследования было сформировано две когорты пациентов: пациенты с фосфатным уролитиазом и пациенты с фосфатным уролитиазом либо фосфатурией на фоне имеющихся постоянных дренажей мочевыводящих путей (нефростомы, цистостомы, уретеростомы).
Всего в исследование было рекрутировано 135 пациентов. Для статистического анализа были доступны данные по 131 пациенту.
Все пациенты, соответствующие критериям включения, были рандомизированы в четыре группы (рис. 1).
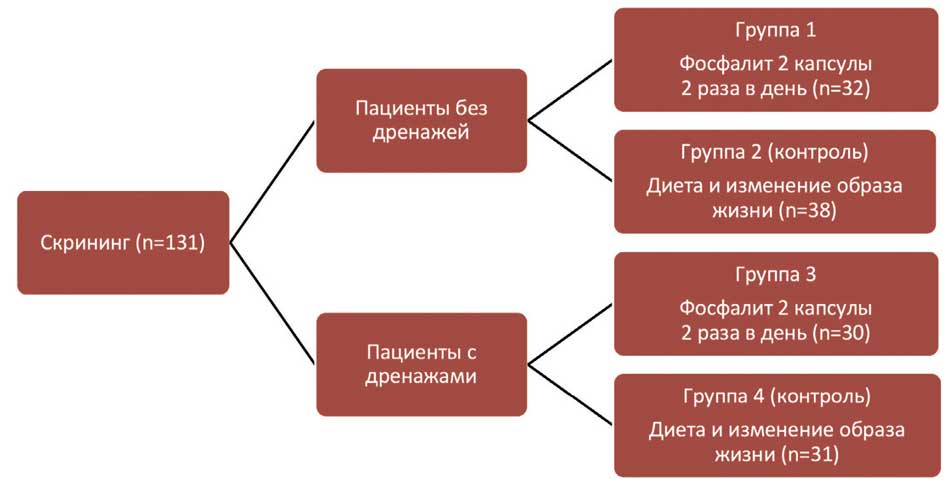
Рис. 1. Распределение исследуемой популяции по группам
Fig. 1. Distribution of the studied population by groups
Группа 1 – пациенты с фосфатным уролитиазом, получавшие препарат «Фосфалит®» на регулярной основе по 2 капсулы (в 1 капсуле – 480 мг) 2 раза в день. Группа 2 – пациенты с фосфатным уролитиазом, получавшие общие рекомендации по изменению образа жизни и диеты. Группа 3 – пациенты с фосфатным уролитиазом на фоне имеющихся постоянных дренажей мочевыводящих путей (нефростомы, цистостомы, уретеростомы), получающие препарат «Фосфалит®» на регулярной основе по 2 капсулы (в 1 капсуле – 480 мг) 2 раза в день. Группа 4 – пациенты с фосфатным уролитиазом на фоне имеющихся постоянных дренажей мочевыводящих путей (нефростомы, цистостомы, уретеростомы), получившие общие рекомендации по изменению образа жизни и диеты. Длительность вмешательства составила 90 дней.
В качестве критериев эффективности вмешательства оценивалась динамика показателей общего анализа мочи (степень кристаллурии, уровень лейкоцитов, рН, уровень белка и др.) и степень изменения уровня фосфатов в крови и суточной экскреции фосфатов с мочой. Также в исследуемых группах оценивалось число и размер конкрементов.
Статистическая обработка данных выполнялась с использованием программного пакета IBM SPSS Statistics версии 23.0.0.0. Для облегчения статистической обработки данных при изучении числа лейкоцитов в полях зрения вычислялось среднее арифметическое из минимального и максимального числа значений. При оценке динамики размера конкрементов, при наличии нескольких конкрементов, вычислялся среднеарифметический размер.
РЕЗУЛЬТАТЫ
Для облегчения интерпретации результатов ниже раздельно представлены суммарные данные по пациентам из групп 1 и 2 (без дренажей) и групп 3 и 4 (с дренажами).
Среди пациентов с фосфатным уролитиазом в группах 1 и 2 после 3-х месяцев наблюдения достоверно снижался уровень фосфатов в крови (p<0,001; исходно vs 3 мес. лечения). При этом в группе, получавшей «Фосфалит®», уровень фосфатов в крови снизился на 16,1%, а в контрольной группе – на 10,8% (р=0,04 для межгруппового различия).
Среди пациентов с дренажами мочевой системы различие между группами было более выраженным. Так, в группе, получавшей «Фосфалит®», уровень фосфатов в крови снизился на 28%, а в контрольной группе – на 12,7% (p<0,001 при сравнении до и после лечения). Однако, из-за значимых различий в изначальном уровне фосфатов в крови, несмотря на более выраженную динамику в группе «Фосфалита®», через 3 месяца различия между группами нет (р=0,152 для межгруппового различия). Общая эффективность «Фосфалита®» в отношении снижения уровня фосфатов в крови в обеих группах пациентов составила 90,1%. При этом у пациентов с дренажами мочевых путей эффективность составила 100,0%, а у пациентов без дренажей – 83,3%. Более подробно данные по динамике уровня фосфатов в крови отображены в таблице 1 и на рисунке 2.
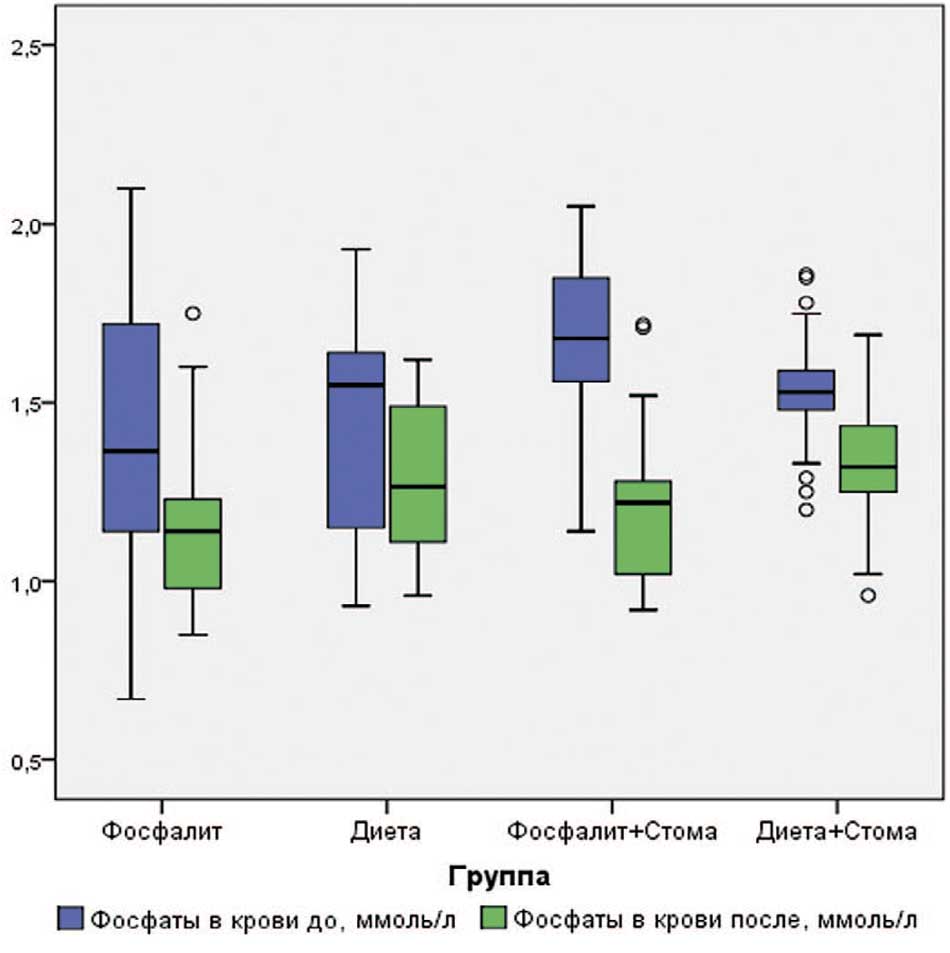
Рис. 2. Уровень фосфатов в крови, ммоль/л
Fig. 2. The level of phosphates in the blood, mmol/l
Другим показателем, характеризующим обмен фосфора, является его суточная экскреция с мочой. И изучаемое, и контрольное вмешательства достоверно снижали суточную экскрецию фосфатов с мочой. Вместе с тем, среди пациентов без дренажей в опытной группе суточная экскреция фосфатов с мочой снизилась на 34,4%, а в контрольной – на 14,1% (р=0,005 для межгруппового различия). В группах пациентов с дренажами экскреция фосфатов среди получавших «Фосфалит®» также снижалась сильнее по сравнению с контролем (36,2% vs 17,2%, р=0,04 для межгруппового различия). Общая эффективность «Фосфалита®» в отношении снижения экскреции фосфатов в обеих группах пациентов составила 93,3%. При этом у пациентов с дренажами мочевых путей эффективность составила 100,0%, а у пациентов без дренажей – 86%. Более подробно динамика суточной экскреции фосфатов отображена в таблице 2 и на рисунке 3.
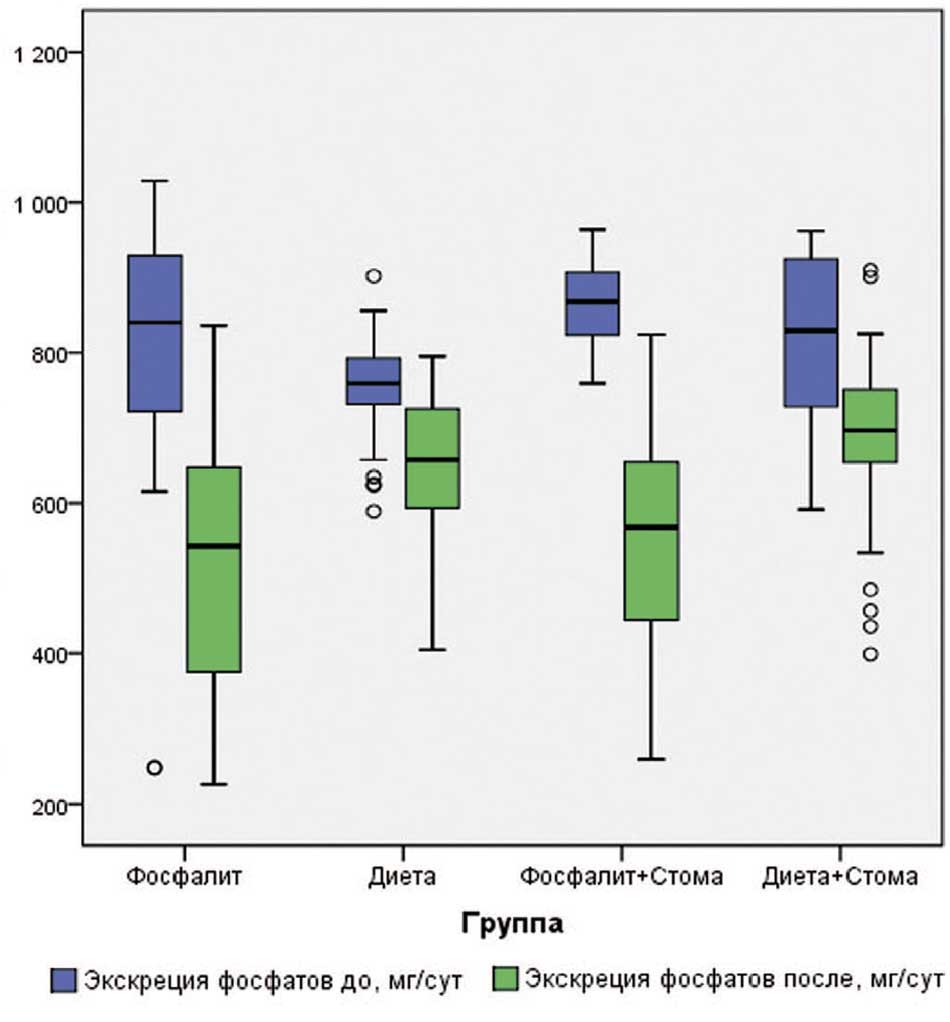
Рис. 3. Динамика суточной экскреции фосфатов с мочой, мг/сут
Fig. 3. Dynamics of daily excretion of phosphates in urine, mg/day
Таблица 1. Динамика уровня фосфатов в крови, ммоль/л
Table 1. Dynamics of blood phosphate levels, mmol/l
| Среднее ± стандартное отклонение Average ± standard deviation |
Разница, % Difference, % |
Значимость изменений во времени The significance of changes over time |
|||||
|---|---|---|---|---|---|---|---|
| До Before |
Различие между группами Significance of the difference between groups |
После After |
Различие между группами Significance of the difference between groups |
||||
| Без стомы Without сatheter |
Фосфалит® Phosphalit® (n=30) |
1,39±0,38 | р=0,588 | 1,17±0,24 | р=0,04 | -16,1% | р<0,001 |
| Диета Diet (n=38) |
1,44±0,29 | 1,28±0,21 | -10,8% | р<0,001 | |||
| Стома With сatheter |
Фосфалит® Phosphalit® (n=30) |
1,67±0,23 | р=0,02 | 1,20±0,23 | р=0,152 | -28% | р<0,001 |
| Диета Diet (n=31) |
1,53±0,15 | 1,34±0,17 | -12,7% | р<0,001 | |||
Динамика степени кристаллурии также показала положительные изменения во всех изучаемых группах. Так, доля лиц с полным отсутствием кристаллов фосфатов в осадке мочи в группе, принимавшей «Фосфалит®», выросла с 6,3% до 46,7%, и в контрольной группе также выросла с 3,7% до 48,1%. В группе пациентов с дренажами, принимавших «Фосфалит®» (группа 3), доля лиц с полным отсутствием кристаллов фосфатов в осадке мочи после лечения увеличилась с 3,7% до 40,7%, а в контрольной группе – с 3,4% до 31,0%. Более подробно данное распределение отображено в таблице 3 и на рисунке 4.
Во всех исследуемых группах отмечалось уменьшение размера конкрементов (табл. 4). При этом наиболее выраженная динамика отмечалась в группе пациентов, не имеющих дренажей и получавших «Фосфалит®» (снижение на 63,3%). В то же время, как среди пациентов с дренажами, так и без таковых, отмечалось достоверное различие между опытной и контрольной группой. У пациентов с нефростомами и цистостомами применение «Фосфалита®» снижало объем конкрементов в 3,1 раза быстрее по сравнению с диетой (р=0,01). У пациентов без дренажей «Фосфалит®» уменьшал средний размер конкремента в 2,7 раза быстрее (р=0,002).
Таблица 2. Экскреция фосфатов с мочой, мг/сут
Table 2. Urinary excretion of phosphates, mg/day
| Среднее ±стандартное отклонение Average ± standard deviation |
Разница,% Difference, % |
Значимость изменений во времени The significance of changes over time |
|||||
|---|---|---|---|---|---|---|---|
| До Before |
Различие междугруппами Significance of the difference between groups |
После After |
Различие между группами Significance of the difference between groups |
||||
| Без стомы Without сatheter |
Фосфалит® Phosphalit® (n=20) |
794±214 | р=0,323 | 521±173 | р=0,005 | -34,4% | р<0,001 |
| Диета Diet (n=27) |
750±74 | 644±113 | -14,1% | р<0,001 | |||
| Стома With сatheter |
Фосфалит® Phosphalit® (n=27) |
865±56 | р=0,130 | 552±149 | р=0,001 | -36,2% | р<0,001 |
| Диета Diet (n=29) |
829±109 | 686±127 | -17,2% | р<0,001 | |||
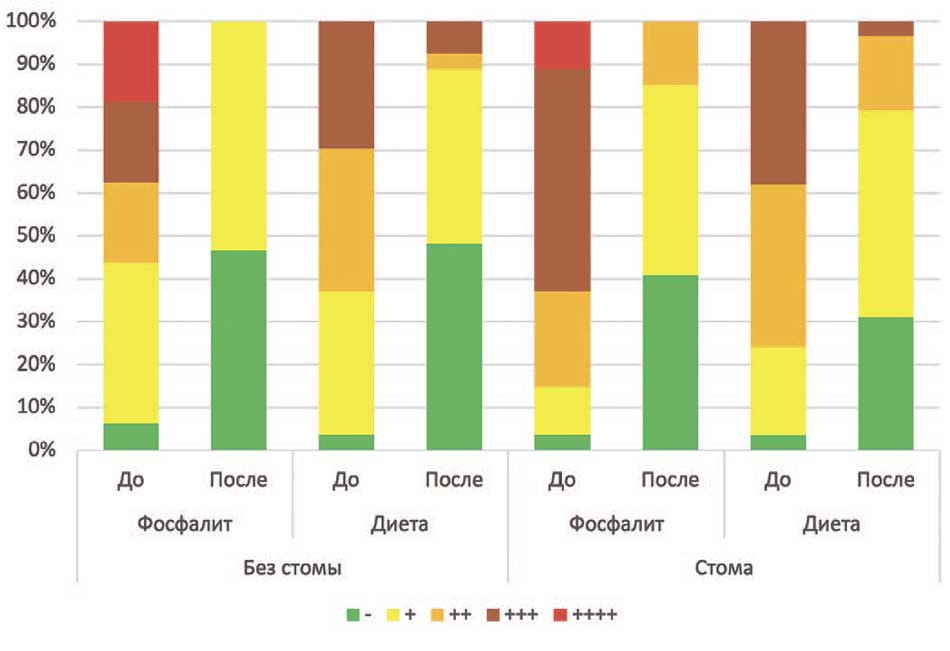
Рис. 4. Распределение пациентов по степени фосфатной кристаллурии в осадке мочи
Fig. 4. Patients’ distribution according to the degree of phosphate crystalluria in urine sediment
Таблица 3. Распределение пациентов по степени фосфатной кристаллурии в осадке мочи
Table 3. Patients’ distribution according to the degree of phosphate crystalluria in the urine sediment
| Группа Group |
Степень кристаллурии Crystalluria degree |
||||||
|---|---|---|---|---|---|---|---|
| – | + | ++ | +++ | ++++ | |||
| Без стомы Without сatheter |
Фосфалит® Phosphalit® (n=16) |
До / Before | 1 | 6 | 3 | 3 | 3 |
| После / After | 7 | 8 | 0 | 0 | 0 | ||
| Диета Diet (n=27) |
До / Before | 1 | 9 | 9 | 8 | 0 | |
| После / After | 13 | 11 | 1 | 2 | 0 | ||
| Стома With сatheter |
Фосфалит® Phosphalit® (n=27) |
До / Before | 1 | 3 | 6 | 14 | 3 |
| После / After | 11 | 12 | 4 | 0 | 0 | ||
| Диета Diet (n=29) |
До / Before | 1 | 6 | 11 | 11 | 0 | |
| После / After | 9 | 14 | 5 | 1 | 0 | ||
Для оценки функции почек в ходе исследования оценивались концентрация белка в моче, уровень лейкоцитов и эритроцитов в анализе мочи (табл. 5). В группах 1 и 3 отмечалось достоверное снижение концентрации белка и содержания форменных элементов в осадке мочи. В группе 3 отмечалось достоверное снижение концентрации белка в моче (p<0,001). В остальных группах достоверных изменений не было.
ОБСУЖДЕНИЕ
Повышение уровня фосфатов в крови является большой проблемой не только с точки зрения повышенного риска камнеобразования, в том числе у пациентов с постоянными дренажами мочевых путей, но и для лиц, находящихся на гемодиализе в связи с терминальной стадией хронической болезни почек.
Таблица 4. Динамика размеров конкрементов на фоне лечения
Table 4. Stone size dynamics during treatment
| Среднее ± стандартное отклонение Average ± standard deviation |
Разница,% Difference, % |
Значимость изменений во времени The significance of changes over time |
|||||
|---|---|---|---|---|---|---|---|
| До Before |
Различие между группами Significance of the difference between groups |
После After |
Различие между группами Significance of the difference between groups |
||||
| Без стомы Without сatheter |
Фосфалит® Phosphalit® (n=32) |
4,9±3,1 | р=0,584 | 1,8±2,0 | р=0,002 | -63,3% | р<0,001 |
| Диета Diet (n=38) |
5,2±1,7 | 4,0±3,2 | -23,1% | р=0,001 | |||
| Стома With сatheter |
Фосфалит® Phosphalit® (n=30) |
6,9±2,3 | р=0,269 | 4,7±3,0 | р=0,01 | -31,9% | р<0,001 |
| Диета Diet (n=31) |
7,8±3,3 | 7,0±3,8 | -10,3% | р=0,001 | |||
Таблица 5. Динамика показателей общего анализа мочи
Table 5. Urinalysis dynamics
| Показатель Parameter |
Группа Group |
Среднее ± стандартное отклонение Average ± standard deviation |
Значимость изменений во времени The significance of changes over time |
|
|---|---|---|---|---|
|
До |
После |
|||
|
Белок, г/л |
Фосфалит® Phosphalit® |
0,11±0,15 | 0,06±0,11 | 0,015* |
| Диета Diet |
0,14±0,15 | 0,13±0,16 | 0,512 | |
| Фосфалит® (дренажи) Phosphalit® (with catheters) |
0,26±0,21 | 0,14±0,12 | <0,001* | |
| Диета (дренажи) Diet (with catheters) |
0,19±0,15 | 0,11±0,14 | <0,001* | |
| Лейкоциты, в п/зр Leucocytes |
Фосфалит® Phosphalit® |
6,8±6,4 | 4,6±5,6 | 0,035* |
| Диета Diet |
7,5±6,5 | 6,6±7,1 | 0,410 | |
| Фосфалит® (дренажи) Phosphalit® (with catheters) |
42,2±42,7 | 16,2±35,2 | 0,008* | |
| Диета (дренажи) Diet (with catheters) |
36,4±46,8 | 25,2±35,0 | 0,257 | |
| Эритроциты, в п/зр Erythrocytes |
Фосфалит® Phosphalit® |
2,5±2,3 | 1,2±1,1 | <0,001* |
| Диета Diet |
2,8±2,1 | 2,7±2,6 | 0,684 | |
| Фосфалит® (дренажи) Phosphalit® (catheters) |
29,1±47,8 | 7,3±5,5 | 0,016* | |
| Диета (дренажи) Diet (with catheters) |
18,3±35,8 | 16,7±35,7 | 0,440 | |
Кокрановский обзор, проведенный в 2015 году, показал, что диетические рекомендации не способны значимо снизить уровень фосфатов в крови [3]. В целом, авторы обзора пришли к выводу, что существует лишь ограниченное количество доказательств низкого качества, указывающих на то, что диетические вмешательства могут положительно влиять на контроль уровня фосфатов в сыворотке.
Это было подтверждено в недавних исследованиях, в которых различные методы диетического обучения пациентов приводили к снижению уровня фосфатов в сыворотке крови от незначимого до -0,4 ммоль/л (-1,24 мг/дл) [4]. Кроме того, все эти исследования были краткосрочными, а долгосрочное поддержание более низких уровней фосфатов с помощью диетических мер после окончания вмешательства сомнительно [5]. Кроме того, риск недостаточности питания при хроническом ограничении фосфатов в рационе до сих пор недостаточно изучен.
Бергенин из экстракта Bergenia ligulata, входящий в состав «Фосфалита®», показал свою способность достоверно уменьшать скорость кристаллизации карбоната и гидрофосфата кальция in vitro [6]. Кроме того, в эксперименте in vivo Bergenia ligulate уменьшал объем кристаллурии в 8,5 раз [7].
Бергенин в эксперименте оказывает восстановительное действие на функцию почек при модельном уролитиазе за счет повышения активности ферментов с антиоксидантной активностью (каталазы, супероксиддисмутазы, глутатионпероксидазы) [8]. Другим возможным антилитогенным механизмом действия бергенина является восстановление нормального функционирования комплекса I, II и IV цепи переноса электронов в митохондриях, а также за счет снижения продукции IL-1β и экспрессии KIM-1 (Kidney Injury Molecule-1) и MCP-1 (Monocyte chemoattractant protein-1) в почечной ткани [9]. Карбонат кальция традиционно используется в качестве антацида или источника кальция, однако он обладает и выраженным фосфат-связывающим действием. Принимаемый с едой кальций и фосфаты образуют нерастворимый комплекс, который выводится с фекалиями.
Многочисленные исследования показали, что прием карбоната кальция эффективно и стабильно снижает избыточный уровень фосфатов в крови [10]. При этом карбонат кальция обладает хорошим профилем безопасности и низким уровнем неблагоприятных реакций, сравнимым с более современными и высокотехнологичными фосфат-связывающими агентами [11].
Отдельные исследования показывают безопасность непрерывного приема карбоната кальция с целью снижения уровня фосфатов в крови на протяжении 24 месяцев [12].
Никотиновая кислота (Ниацин, витамин РР, витамин В3) чаще всего в медицинской практике применяется также при гиперлипидемии, дислипидемии, гипертриглицеридемии и с целью снижения риска инфаркта миокарда. Ниацин снижает уровень липопротеинов очень низкой плотности (ЛПОНП) и липопротеинов низкой плотности (ЛПНП), одновременно увеличивая уровни липопротеинов высокой плотности (ЛПВП). Никотиновая кислота и ее метаболиты могут эффективно снижать абсорбцию фосфора в желудочнокишечном тракте, тем самым снижая концентрацию фосфора в сыворотке [13].
Данные in vitro и in vivo показывают, что никотинамид и никотиновая кислота снижают гиперфосфатемию за счет ингибирования натрий-зависимого совместного транспорта фосфата в проксимальных канальцах почек и в кишечнике. Соответственно, нацеливание на натрий-зависимый переносчик фосфата 2b с использованием никотинамида в качестве альтернативы или дополнения к классическим фосфатсвязывающим средствам может быть терапевтическим вариантом для модуляции сывороточного фосфата при фосфатных формах мочекаменной болезни [14].
Более того, рандомизированное исследование показало, что сочетание никотинамида и карбоната кальция при длительности приема в 6 месяцев и более существенно снижает уровень кальция и фосфора в сыворотке крови, по сравнению с монотерапией [15]. Клюква (лат. Vaccinium oxycoccus) и различные ее формы широко применяются в урологии как для борьбы с инфекциями нижних мочевых путей, так и при мочекаменной болезни. Она содержит большое число органических кислот, которые изменяют кислотность мочи, тем самым снижая ее литогенную способность. Так, еще в 2004 году было показано, что употребление большого количества сока клюквы вызывает снижение рН мочи [16].
В рандомизированном исследовании было показано, что употребление сока клюквы достоверно увеличивает содержание одного из низкомолекулярных антилитогенных веществ – магния, а также снижает рН мочи на 0,3, вероятно, за счет кислотной нагрузки [17]. Кишечнорастворимая форма капсул «Фосфалита®» позволяет избежать развития желудочно-кишечных побочных эффектов некоторых компонентов и увеличить эффективность комплекса в целом.
ЗАКЛЮЧЕНИЕ
Благодаря комплексному действию активных компонентов на множество механизмов развития заболевания, «Фосфалит®» является эффективным и безопасным средством коррекции метаболических нарушений при фосфатных формах мочекаменной болезни. Эффективность комплекса при катетерах и стентах позволяет сделать вывод, что «Фосфалит®» можно включать в схему терапии фосфатных камней на фоне катетер-ассоциированных инфекций ИМП.
ЛИТЕРАТУРА
- Яковлев С.В., Суворова М.П., Белобородов В.Б., Басин Е.Е., Елисеева Е.В., Ковеленов С.В., и соавт. Распространенность и клиническое значение нозокомиальных инфекций в лечебных учреждениях России: исследование ЭРГИНИ. Антибиотики и Химиотерапия 2016;61(5-6):32-42. [Yakovlev S.V., Suvorova M.P., Beloborodov V.B., Basin E.E., Eliseeva E.V., Kovelenov S.V., et al. Multicentre Study of the Prevalence and Clinical Value of Hospital-Acquired Infections in Emergency Hospitals of Russia: ERGINI Study. Antibiot Khimioter = Antibiotics and Chemotherapy 2016;61(5-6):32-42. (In Russian)].
- Menegueti MG, Ciol MA, Bellissimo-Rodrigues F, Auxiliadora-Martins M, Gaspar GG, Canini SRMDS, et al. Long-term prevention of catheter-associated urinary tract infections among critically ill patients through the implementation of an educational program and a daily checklist for maintenance of indwelling urinary catheters A quasiexperimental study. Medicine (United States) 2019;98(8):e14417. https://doi.org/10.1097/MD.0000000000014417.
- Liu Z, Su G, Guo X, Wu Y, Liu X, Zou C, et al. Dietary interventions for mineral and bone disorder in people with chronic kidney disease. Cochrane Database Syst Rev 2015;2015(9):CD010350. https://doi.org/10.1002/14651858.CD010350.pub2.
- Duff EA, Chawke FM. A service review to assess if innovative intensive phosphate dietary education can help reduce phosphate levels to the recommended range in a hemodialysis population. Hemodial Int 2017;21(Suppl 2):S22-S26. https://doi.org/10.1111/hdi.12593.
- Vrdoljak I, Panjkota Krbavčić I, Bituh M, Leko N, Pavlović D, Vrdoljak Margeta T. The impact of education and cooking methods on serum phosphate levels in patients on hemodialysis: 1-year study. Hemodial Int 2017;21(2):256-64. https://doi.org/10.1111/hdi.12468.
- Joshi VS, Parekh B, Joshi MJ, Vaidya ADB. Herbal extracts of Tribulus terrestris and Bergenia ligulata inhibit growth of calcium oxalate monohydrate crystals in vitro. Journal of Crystal Growth 2005;275:1–2. https://doi.org/10.1016/j.jcrysgro.2004.11.240.
- Bashir S, Gilani AH. Antiurolithic effect of Bergenia ligulata rhizome: an explanation of the underlying mechanisms. J Ethnopharmacol 2009;122(1):106-16. https://doi.org/10.1016/j.jep.2008.12.004.
- Aggarwal D, Kaushal R, Kaur T, Bijarnia RK, Puri S, Singla SK. The most potent antilithiatic agent ameliorating renal dysfunction and oxidative stress from Bergenia ligulata rhizome. J Ethnopharmacol 2014;158:85-93. https://doi.org/10.1016/j.jep.2014.10.013.
- Aggarwal D, Gautam D, Sharma M, Singla SK. Bergenin attenuates renal injury by reversing mitochondrial dysfunction in ethylene glycol induced hyperoxaluric rat model. Eur J Pharmacol 2016;791:611-21. https://doi.org/10.1016/j.ejphar.2016.10.002.
- Miller D, Taber TE, Hegeman TF. Calcium carbonate powder as a phosphate binder. ASAIO Trans 1989;35(3):322-4. https://doi.org/10.1097/00002480-198907000-00047.
- Ogata H, Fukagawa M, Hirakata H, Kagimura T, Fukushima M, Akizawa T; LANDMARK Investigators and Committees. Effect of Treating Hyperphosphatemia With Lanthanum Carbonate vs Calcium Carbonate on Cardiovascular Events in Patients With Chronic Kidney Disease Undergoing Hemodialysis: The LANDMARK Randomized Clinical Trial. JAMA 2021;325(19):1946-54. https://doi.org/10.1001/jama.2021.4807.
- Malberti F, Surian M, Poggio F, Minoia C, Salvadeo A. Efficacy and safety of long-term treatment with calcium carbonate as a phosphate binder. Am J Kidney Dis 1988;12(6):487-91. https://doi.org/10.1016/s0272-6386(88)80099-4.
- Rennick A, Kalakeche R, Seel L, Shepler B. Nicotinic acid and nicotinamide: a review of their use for hyperphosphatemia in dialysis patients. Pharmacotherapy 2013;33(6):683-90. https://doi.org/10.1002/phar.1258.
- Lenglet A, Liabeuf S, Guffroy P, Fournier A, Brazier M, Massy ZA. Use of nicotinamide to treat hyperphosphatemia in dialysis patients. Drugs R D 2013;13(3):165-73. https://doi.org/10.1007/s40268-013-0024-6.
- El Borolossy R, El Wakeel LM, El Hakim I, Sabri N. Efficacy and safety of nicotinamide in the management of hyperphosphatemia in pediatric patients on regular hemodialysis. Pediatr Nephrol 2016;31(2):289-96. https://doi.org/10.1007/s00467-015-3208-1.
- Raz R, Chazan B, Dan M. Cranberry juice and urinary tract infection. Clin Infect Dis 2004;38(10):1413-9. https://doi.org/10.1086/386328.
- Gettman MT, Ogan K, Brinkley LJ, Adams-Huet B, Pak CY, Pearle MS. Effect of cranberry juice consumption on urinary stone risk factors. J Urol 2005;174(2):590-4. https://doi.org/10.1097/01.ju.0000165168.68054.f8.







