ВВЕДЕНИЕ
Лечение нарушений мочеиспускания у женщин является проблемой, широко обсуждаемой в медицинских кругах, а последствия несвоевременного и некорректного выбора лечебной тактики или неверного начала лечения делают данную проблему актуальной для исследований. Врачи многих специальностей – урологи, гинекологи, проктологи так же, как неврологи и реабилитологи сталкиваются с проблемами нарушения мочеиспускания в своей практике. Лечение нарушений мочеиспускания – это растущий и непрерывно совершенствующийся сектор медицинской индустрии. Опубликовано большое количество работ, посвященных данной проблеме. Для лечения нарушений мочеиспускания используют значительный арсенал методов, имеющих как достоинства, так и ограничения.
В связи с этим совершенствование методов лечения нарушений мочеиспускания является актуальной задачей современной функциональной женской урологии.
Распространенность нарушений мочеиспускания у женщин. Виды и терминология
По данным литературы приблизительно 24% женщин до 60 лет и более 50% женщин старше 60 лет испытывают проблемы, связанные с нарушением акта мочеиспускания [1]. По данным различных авторов, распространенность симптомов нарушенного мочеиспускания среди женщин в США достигает 37%, в Европе – 26%, в Великобритании – 29%, в странах восточного региона (Сингапур, Пакистан, Тунис) – 20% [2]. Различна и обращаемость за медицинской помощью данной категории женщин. Во Франции она составляет 33%, в Германии – 40%, в Испании – 24%, в Великобритании – 25% [3].
В России распространенность нарушений мочеиспускания у женщин составляет примерно 36%, а обращаемость пациенток за медицинской помощью сравнительно невысока [4]. В последние годы наметилась положительная тенденция увеличения числа обращений пациенток с нарушениями мочеиспускания за высококвалифицированной медицинской помощью. Особенно актуальна эта проблема для женщин, страдающих недержанием мочи. В нашей стране до последнего времени ее обсуждать было не принято. Многие женщины испытывали стеснение при обращении к врачу со столь «интимной проблемой». Было распространено заблуждение, что это обычное состояние для рожавших и женщин старшего возраста, а также что оно неизлечимо и т.п. [5]. Однако, недержание мочи не является естественным признаком старения. Оно может встречаться и у молодых женщин, в том числе во время беременности, а также в раннем послеродовом периоде.
Высокая распространенность нарушений мочеиспускания у женщин, как молодого, так и старшего возраста, обуславливает актуальность этой медицинской и социальной проблемы.
Наиболее частыми видами нарушений мочеиспускания являются недержание мочи различной степени тяжести и функциональная инфравезикальная обструкция, часто обозначаемая как дисфункциональное мочеиспускание.
Недержание мочи
Согласно определению Международного общества по проблемам недержания мочи (International Continence Society (ICS)), недержание мочи – это непроизвольное вытекание мочи по уретре. Выделяют три вида недержания: стрессовое, ургентное и смешанное. Недержанием мочи страдают 6-10% населения и 1/3 женщин [6]. По терминологии ICS стрессовое недержание мочи – это непроизвольное подтекание мочи при напряжении, физической нагрузке (исключая спортивные нагрузки) или при чихании и кашле. Стрессовое недержание мочи выявляют у 25-70% женщин [7].
Согласно данным российских публикаций, недержание мочи при напряжении наблюдали у 19% женщин из общего числа обратившихся за помощью в урологическую клинику [5]. Симптомы заболевания выявляли у каждой 10–15-й больной при обращении в женскую консультацию. Согласно нашим ранее опубликованным данным, частота клинических симптомов недержания мочи у женщин старше 25 лет достигает 30% случаев [8]. Самым распространенным видом недержания мочи по-прежнему остается стрессовая форма. У женщин старше 50 лет распространенность клинических симптомов возрастает в 2,5 раза, достигая 70% [9].
Имеются данные, что физическая активность увеличивает риск развития стрессового недержания мочи у женщин, хотя патофизиологические механизмы этого влияния неясны. У спортсменок, занимающихся спортом с тяжелыми физическими нагрузками, дисфункцию мочеиспускания отмечают чаще, чем в общей популяции женщин.
Наличие недержания мочи существенно влияет на психологическое состояние женщины. Часто развивается депрессия и постоянная тревожность, происходит снижение половой активности и работоспособности. В итоге, это приводит к значительному ухудшению качества жизни [10]. При этом, далеко не все женщины, страдающие недержанием мочи, обращаются за медицинской помощью, так как многие даже не предполагают, что это заболевание можно не только контролировать, но и лечить. По данным M. Sjöström и соавт., обращаемость к врачу в европейских странах не превышает 25%, а лечение получают только 6% женщин. Признано, что эффективность лечения во многом зависит от своевременности обращения за медицинской помощью: чем раньше начата терапия, тем лучших результатов можно добиться [11].
Функциональная инфравезикальная обструкция (дисфункциональное мочеиспускание)
Функциональную инфравезикальную обструкцию (фИВО) или дисфункциональное мочеиспускание у женщин в настоящее время рассматривают, как важную медицинскую проблему, о чем свидетельствует выделение этой темы в рекомендациях Европейской ассоциации урологов (EAU) в отдельную главу [12]. Согласно терминологии ICS, дисфункциональное мочеиспускание определяют, как прерывистое или неравномерное выделение мочи вследствие непроизвольных периодических сокращений периуретральных поперечнополосатых мышц в процессе мочеиспускания у неврологически здоровых пациенток.
Определение, терминология и классификация ИВО у женщин такие же, как для мужчин, что отражено в материалах комитета стандартизации ICS. Несмотря на то, что у женщин преобладают симптомы накопления, нередко они предъявляют жалобы и на задержку мочеиспускания, вялое мочеиспускание и чувство неполного опорожнения мочевого пузыря. При уродинамическом исследовании выявляют низкие показатели скорости мочеиспускания и повышенные значения объема остаточной мочи.
В отличие от проблемы недержания мочи, в специальной литературе встречаются лишь отдельные сообщения, посвященные попыткам стандартизации жалоб женщин с ИВО. A.J. Flisser, J.G. Blaivas указывают, что у пациенток со значительной обструкцией показатель шкалы IPSS (International Prostate Symptom Score – международная система суммарной оценки симптомов болезней предстательной железы в баллах) достоверно выше, чем при незначительной или умеренной обструкции. Средний показатель выраженности симптомов в группе с обструкцией составил 15,8±8,4 балла против 10,3±6,4 у женщин со стрессовым недержанием мочи и 2,1±2,7 – у здоровых женщин. Некоторые авторы считают возможным применение шкалы IPSS при симптомах нарушенного мочеиспускания у женщин. Такая шкала получила название IPSS women (IPSSw) [13].
Диагноз фИВО ставят после исключения механической причины обструкции, обусловленной такими клиническими состояниями, как цистоцеле, пролапс органов малого таза, стеноз и дивертикул уретры, предшествующие операции на органах таза, в том числе по поводу недержания мочи.
Также необходимо исключить гипотонию мочевого пузыря, что определяют при сопоставлении значений детрузорного давления и скорости мочеиспускания. Для упрощения оценки сократимости детрузора используют номограммы Abrams-Griffiths и часто номограммы BlaivasGroutz [14]. Нередко диагностика дисфункционального мочеиспускания требует специальных методов исследования, таких как видеоурография, электромиография или изучение профиля давления уретры в дополнение к стандартному определению и сопоставлению данных микционной цистометрии. Предложен метод диагностики этого состояния только на основании исследования с определением плато детрузорного давления. На основании этого показателя, с последующим расчетом индекса обструкции нижних мочевых путей (BOOI) и разницы между максимальным давлением детрузора и максимальными значениями давления детрузора при максимальном потоке мочи (PdetmaxpdetQmax), диагноз дисфункционального мочеиспускания устанавливают у 86% женщин с расстройством мочеиспускания [15].
По данным R. Terlikowski и соавт., обструкцию функционального генеза выявляют у 30-40% пациенток с симптомами затрудненного мочеиспускания [16].
Распространенность фИВО у женщин варьирует в широких пределах от 2,7 до 29% [17]. Столь значительная разница показателей, во многом, связана с неоднозначностью определений и отсутствием общепринятого диагностического алгоритма выявления инфравезикальной обструкции (ИВО). В зависимости от выбранного уродинамического критерия, частота выявления ИВО у пациенток с симптомами нарушения функции нижних мочевых путей колеблется от 2 до 8% [18]. По данным большинства исследователей, частота выявления ИВО, в том числе функционального характера, зависит от возраста [19]. У 16% пациенток причину ИВО точно установить не удается [20]. В этом случае говорят об «идиопатической инфравезикальной обструкции».
Несмотря на проводимое лечение, при выявлении дисфункционального мочеиспускания у девочек-подростков в 40% случаев дисфункция сохраняется во взрослом возрасте [21].
Патофизиологические аспекты развития нарушений мочеиспускания
В обеспечении нормальной функции тазовых органов существенную роль играет мышечно-связочный аппарат малого таза, обеспечивающий механическую поддержку тазовых органов, их нормальное взаиморасположение и механизм удержания мочи и кала. Различные варианты дисфункции мочеиспускания часто связаны с нарушением поддерживающей функции тазового дна.
Основными мышцами, формирующими тазовое дно, являются: мышца, поднимающая задний проход – лобково-копчиковая мышца, она же лобково-простатическая (у мужчин); лобково-влагалищная; лобковоанальная; лобково-ректальная; подвздошно-копчиковая (идет от сухожильной дуги к нижним копчиковым позвонкам ниже лобково-копчиковой мышцы); седалищно-копчиковая мышца. Взаиморасположение основных мышц тазового дна, связок и тазовых органов представлено на рис. 1.
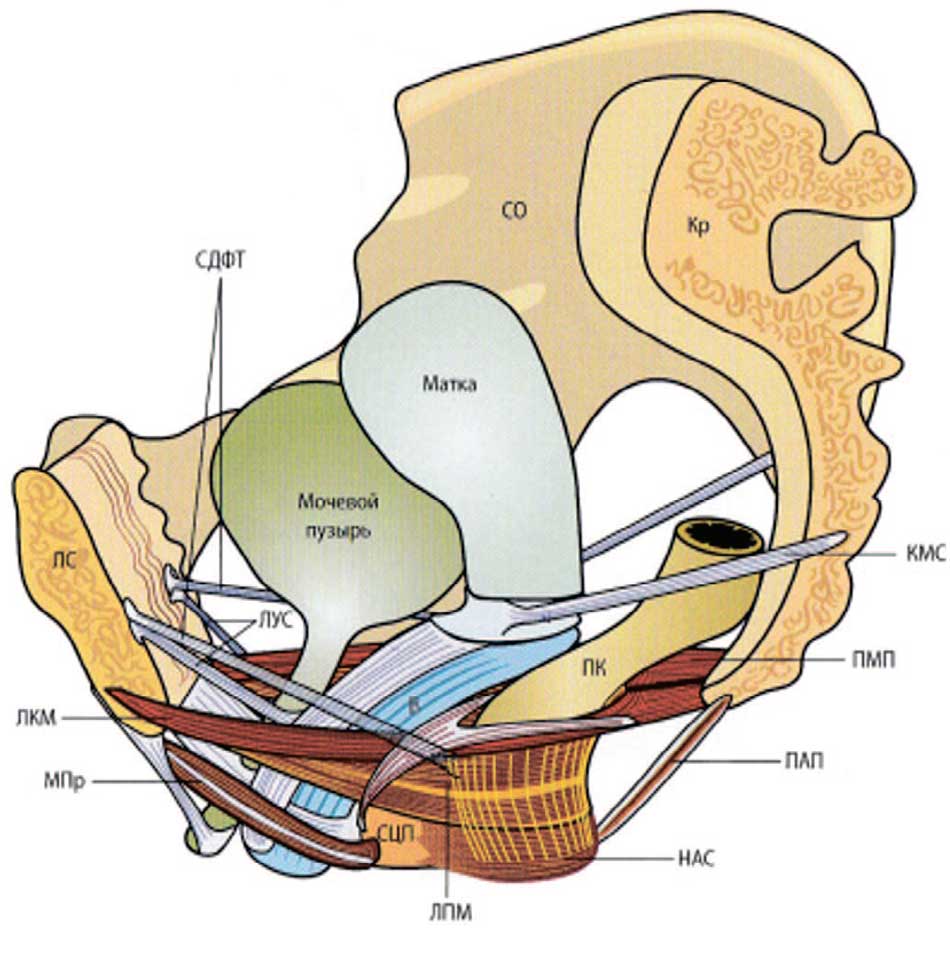
Рис. 1. Схема мышечно-связочного аппарата малого таза [22]. Обозначения: ЛС – лобковый симфиз, Кр – крестец, ЛКМ – лобково-копчиковая мышца, ПМП – поднимающая мышечная пластина, ПМА – продольная мышца ануса, ЛПМ – лобково-прямокишечная мышца, ЛУС – лобково-уретральная связка, СДФТ – сухожильная дуга фасции таза, КМС – крестцово-маточная связка, КСМ – кардиальная связка матки, ЛШФ – лобково-шеечная фасция, ВПФ – влагалищно-прямокишечная фасция, СЦП – сухожильный центр промежности, НАС – наружный анальный сфинктер
Fig. 1. Scheme of the muscular-ligamentous apparatus of the small pelvis [22] Designations: ЛС – pubic symphysis, Кр – sacrum, ЛКМ– pubococcygeus muscle, ПМП – levator muscular plate, ПМА – longitudinal muscle of the anus, ЛПМ – puborectalis muscle, ЛУС – pubourethral ligament, СДФТ – tendinous arcus of the pelvic fascia, КМС – sacrouterine ligament, KСМ – cardiac ligament of the uterus, ЛШФ– pubocervical fascia, ВПФ – vaginal-rectal fascia, СЦП – tendinous center of the perineum, НАС – external anal sphincter
Согласно интегральной теории P.E. Petros и U. Ulmsten, именно взаимодействие тазовых мышц и связок таза обеспечивает механизм удержания мочи. Нагрузка на связочный аппарат таза ведет к постепенному его растяжению, что нарушает механизм удержания мочи. В конечном итоге, это может приводить к изменению топографии органов малого таза и нарушению их функции, в том числе к дисфункции мочеиспускания в виде недержания мочи или инфравезикальной обструкции, а также к другим нарушениям, таким как пролапс тазовых органов, недержание кала, сексуальная дисфункция, диастаз прямых мышц живота, хроническая тазовая боль [23].
Ослабление мышечно-связочного аппарата ведет к опущению мочевого пузыря и изменению взаиморасположения шейки мочевого пузыря, уретры и влагалища. Хотя влагалище в норме не участвует в поддержании расположения мочевого пузыря, при опущении мочевого пузыря влагалище становится его опорой. Опущение передней стенки влагалища способствует дисфункции везико-уретрального сегмента и непроизвольному подтеканию мочи. Фиксация верхнего отдела влагалища восстанавливает функцию удержания мочи.
Основным фактором развития дисфункции тазового дна у женщин считается возраст. После наступления менопаузы частота развития недержания мочи, опущения тазовых органов и других видов дисфункции мочеиспускания возрастает. К причинам этих расстройств относят ослабление сфинктера уретры, мышц тазового дна, а также слабость фасциального и связочного аппарата таза.
В формировании дисфункции тазового дна также могут играть роль генетические факторы, такие как коллагеновая недостаточность, в том числе I и III типов. По данным некоторых исследователей, обнаружена прямая взаимосвязь генетических дефектов и стрессового недержания мочи.
Появляются публикации, подтверждающие роль полиморфизма гена COL3A1 в развитии этого состояния [24].
Подтверждением роли дисфункции мышц тазового дна в развитии симптомов нарушенного мочеиспускания является исследование L.P. Cacciari и соавт., в котором приняли участие 23 женщины с недержанием мочи и 31 женщина без недержания. В исследовании определяли профили влагалищного давления с использованием мультисенсорного устройства Pliance. Проводили регистрацию профиля давления в 10 участках вдоль влагалища. У женщин с недержанием мочи выявили более низкое вагинальное давление в покое и сниженную возможность поддерживать напряжение мышц в течение определенного времени. Особенно большая разница между группами выявлена в средней части влагалища на расстоянии 3-4 см от его входа, что соответствует проекции мышц тазового дна [25].В основе фИВО лежит гиперактивность мышц, участвующих в регуляции мочеиспускания (наружный сфинктер мочевого пузыря, лонно-копчиковая мышца, являющаяся частью мышцы, поднимающей анус), что было продемонстрировано в ряде исследований, в том числе с применением метода электромиографии. Показано, что затруднение мочеиспускания связано с недостаточным расслаблением уретры, шейки мочевого пузыря и мышц тазового дна во время акта мочеиспускания [26].
В норме продолжительное сокращение детрузора синхронизировано с релаксацией наружного сфинктера. «Неполноценная» работа периуретральных мышц во время мочеиспускания может явиться причиной функциональной обструкции. В свое время, это состояние получило название «ненейрогенного нейрогенного мочевого пузыря» или синдрома Hinman. A. Groutz и соавт. считают, что более правильными терминами в этой ситуации являются «псевдодиссенергия» или «дисфункциональное мочеиспускание» [27]. Однако, наряду с этими терминами, широко используют и понятие фИВО, подчеркивая, что нарушением является именно функциональная обструкция.
Вероятной причиной мышечного гипертонуса могут быть нарушения мышечно-тонических реакций, связанных как с заболеваниями органов таза, так и с дистрофическими или органическими поражениями позвоночника, учитывая, что органы, расположенные в полости таза и тазовое дно имеют общую систему иннервации. При этом все функции тазовых органов находятся под контролем центральной нервной системы (ЦНС), которая представляет собой сбалансированный механизм, но в определенных ситуациях предрасположенный к нейронной неустойчивости. Сбой, возникший в этой системе, может вызвать центральное функциональное нарушение или дисфункцию периферических нервов, в частности, органов таза. Такая взаимосвязь, в свою очередь, может привести к изменениям в ЦНС, в результате которых возникает нарушение обработки ноцицептивной сенсорной информации.
Косвенные указания на связь сбоев в ЦНС и дисфункции мочеиспускания описаны в публикации J. Panicker и соавт., где изучена роль психологического состояния и наличия определенных функциональных неврологических симптомов в развитии фИВО. Установлено, что у женщин с дисфункциональным мочеиспусканием чаще выявляют симптомы депрессии и тревожности, а также ослабление мышц бедра. Авторы полагают, что перенесенные стрессовые ситуации, особенно сексуального характера, повышают риск развития затрудненного мочеиспускания [28].
Методы лечения нарушений мочеиспускания у женщин
Консервативная терапия нарушений мочеиспускания
В основе дисфункции мочеиспускания у женщин значительную роль играет нарушение функционирования мышц тазового дна. В связи с этим основные методы лечения этих расстройств направлены на восстановление мышечного тонуса тренировочными или лекарственными средствами, а также восстановлением механической поддержки тазовых органов хирургическим путем.
Тренировочные подходы, укрепляющие мышцы тазового дна, являются методами лечения первой линии у женщин с дисфункцией мочеиспускания. Большинство женщин с недержанием мочи предпочитают именно этот вариант первичной терапии, и лишь немногие сразу соглашаются на хирургическое вмешательство.
При неэффективности тренировочных методов лечения назначают медикаментозную терапию с использованием препаратов различных механизмов действия. При недержании мочи применяют терапию М-холиноблокаторами, β3-адреномиметиками, антидепрессантами [29]. Отмечена высокая частота развития побочных эффектов лекарственной терапии, нередко приводящих к отказу от ее продолжения. Учитывая, что недержание мочи в большинстве случаев развивается у женщин в менопаузе при эстрогенной недостаточности, гинекологи широко применяют эстрогены в лечении стрессового недержания мочи, даже в режиме монотерапии, несмотря на то, что применение эстрогенов не обеспечивает необходимой эффективности, увеличивая риск возникновения сердечно-сосудистых заболеваний, злокачественных образований эндометрия и молочных желез [30].
Имеются немногочисленные работы, описывающие применение лекарственной терапии при фИВО у женщин. Если причину функциональной обструкции определить не удается, то назначают средства, способствующие расслаблению наружного сфинктера уретры и усиливающие сократительную способность детрузора.
Проведены исследования по изучению неселективных (феноксибензамин) или селективных (альфузозин, теразозин) α1-адреноблокаторов или М2-холиномиметиков (бетанехол хлорид) [31]. Анализ этих данных указывает на низкую эффективность лекарственной терапии.
Описан опыт применения малых доз миорелаксантов центрального действия, снижающих максимальное внутриуретральное давление в зоне наружного сфинктера уретры, которое обычно повышено у женщин с ИВО функционального типа. Среди нежелательных явлений данного метода отмечают снижение артериального давления, головокружение и мышечную слабость. Эти препараты противопоказаны при черепно-мозговой травме, сотрясениях головного мозга в анамнезе. Эффективность данного лечения не превышает 50% [32].
Хирургические методы лечения дисфункции мочеиспускания у женщин
При недостаточном эффекте консервативных методов терапии обычно прибегают к малоинвазивному и хирургическому методам лечения.
У женщин с недержанием мочи используют такие малоинвазивные методы лечения как: парауретральное введение объемообразующих субстанций на основе аутожира, препаратов коллагена, силикона и др. В последнее время широкое распространение получил метод парауретрального введения объемобразующего геля Bulkamid, который представляет собой гомогенный биосовместимый гидрогель (97,5% апирогенная вода и 2,5% полиакриламид). Эффективность его введения, составляет 65%. Через год наблюдения после введения повторные инъекции понадобились в 35% случаев [33].
Одним из вариантов малоинвазивного лечения у женщин с дисфункциональным мочеиспусканием является денервация сфинктера мочевого пузыря методом введения ботулотоксина. Ботулинотерапию можно рассматривать как метод терапии нарушенного мочеиспускания 3-й линии.
Применение ботулинического токсина при фИВО обладает высокой эффективностью. Основным показанием к проведению лечения данным методом является тяжелая степень функциональной обструкции. По данным НИИ урологии, средняя продолжительность действия ботулинического токсина при введении в зону наружного сфинктера уретры составляет от 3 до 8 месяцев, что влечет за собой необходимость неоднократных повторных введений [18, 32].
Y.H. Jiang и соавт. описали результаты видеоурографического обследования 81 женщины с дисфункциональным мочеиспусканием для выявления преимущественной локализации области обструкции с последующим введением ботулотоксина в эту зону. Эффективность данного метода составила 67,9%, авторы делают вывод о его высокой результативности [34].
При неэффективности малоинвазивного лечения прибегают к хирургическим вмешательствам, особенно при сочетании дисфункции мочеиспускания с пролапсом тазовых органов, поскольку восстановление нормальной топографии тазовых органов способствует устранению симптомов нарушенного мочеиспускания.
Для оперативного лечения недержания мочи у женщин предложено более 200 вариантов оперативных вмешательств. Эффективность большинства операций с использованием собственных тканей ограничена в силу изменений, приводящих к снижению их прочности и эластичности. Как известно, у женщин старшей возрастной группы, страдающих стрессовым недержанием мочи, снижена прочность и эластичность тканей тазового дна. Подобные изменения обуславливают неэффективность большинства вмешательств с использованием собственных тканей, направленных на восстановление функции тазового дна. В связи с этим при корректирующих операциях преимущественно используют синтетические материалы.
При недержании мочи наиболее частым вариантом малоинвазивной операции является установка среднеуретрального слинга (TVT, TVT-O), что в настоящее время считают «золотым стандартом». Однако, накопление опыта этих операций свидетельствует, что их долгосрочная эффективность составляет около 60%, а необходимость повторных вмешательств возникает у 17,7% пациенток в течение последующих 5 лет [35]. По данным различных исследований, частота рецидивов или сохранение стрессового недержания мочи после слинговых операций в ближнесрочном периоде варьирует от 10 до 55%, а в течение 5 лет возрастает до 70% [36]. В то же время, имеются более оптимистичные мнения. По данным исследований, проведенных в Англии и Шотландии, необходимость в повторных операциях возникает в 45% случаев [37]. По данным метаанализа, проведенного F. Fusco и соавт., частота развития осложнений при слинговой уретропексии варьирует от 0,5 до 11,5%, хотя при использовании метода позадилонного слинга частота осложнений оказалась ниже, чем при установке трансобтураторного слинга [38].
Из других вариантов хирургической коррекции недержания мочи при сочетании с опущением тазовых органов используют такие операции, как уретросуспензия, везикокольпосуспензия, а при выраженном пролапсе – везикосакропексию, цервикосакропексию, в том числе с использованием сетчатых имплантатов.
Для восстановления нормального расположения везико-уретрального сегмента доказана целесообразность таких операций, как кольпосуспензия (операция Burch). Эффективность кольпосуспензии, по данным I. Giarenis и соавт., составила 85-93% [39]. Международный и отечественный опыт лечения ИВО у женщин неоднозначен. Выбор метода лечения зависит от этиологии состояния. Оперативное лечение применяют у относительно небольшой группы пациенток. В случае анатомической/механической обструкции, связанной с пролапсом органов малого таза, выполняют оперативное пособие, направленное на ликвидацию опущения.
Ранние результаты баллонной дилатации уретры обнадеживали, однако в последующем долгосрочная эффективность метода не подтвердилась, а после 1994 года новых публикаций не было. При стенозе уретры или шейки мочевого пузыря может быть выполнена трансуретральная инцизия.
Оперативное лечение не потеряло своей значимости у пациенток, которые не способны выполнять интермиттирующую катетеризацию или имеют постоянный катетер/цистостому. Устранение ИВО методом сфинктеротомии может быть достигнуто без полного разрушения удерживающей функции сфинктера. У части больных операцию приходится периодически повторять, так как вторично могут развиться сужение шейки мочевого пузыря и фиброз [40].
Стентирование уретры при ИВО у женщин применяют в единичных случаях. Возможность их установки зависит от состоятельности шейки мочевого пузыря. Результаты применения уретральных стентов сопоставимы с таковыми при сфинктеротомии, но высокая стоимость, осложнения и необходимость повторения процедуры являются ограничивающими факторами для этого метода [41].
Тренировка мышц тазового дна, как метод терапии первой линии
Методом лечения первой линии при дисфункции мочеиспускания у женщин является тренировка мышц тазового дна. Целесообразность тренировочной терапии обоснована патогенезом стрессового недержания мочи, связанным с дисфункцией мышц тазового дна. Тренировки, направленные на произвольное сокращение и расслабление тазовых мышц, позволяют повысить «управляемость» ими, что повышает способность мышц к сокращению и является важным фактором удержания мочи. Тренировка на «расслабление» способствует релаксации сфинктерного аппарата нижних мочевых путей при фИВО.
У женщин с недержанием мочи комплекс упражнений, направленный на периодическое напряжение и расслабление мышц тазового дна (упражнения Кегеля, использование влагалищных конусов), способствует увеличению силы сокращений мышц диафрагмы таза и обеспечивает возможность более длительно удерживать мышцы в состоянии сокращения, что способствует функции удержания мочи. Метод используют при различных положениях тела – лежа, стоя, сидя, в зависимости от состояния пациента.
Имеется ряд исследований, подтверждающих положительное влияние тренировочных методов на состояние мочеиспускания у женщин с недержанием мочи. Однако информация об эффективности этого метода, по данным разных авторов, существенно различается – от 27% до 75% или даже до 90% при 12-недельной тренировке, тогда как при использовании только поведенческой терапии и коррекции образа жизни улучшение состояния мочеиспускания отмечали только 7,2% пациенток [42, 43].
В систематическом обзоре S. Alouini и соавт., охватывающем 15 рандомизированных контролируемых исследований (997 пациенток), проанализирована и выявлена эффективность методов тренировки мышц тазового дна у женщин со стрессовым недержанием мочи. У 21,8% достигнута полая континенция по padтесту, а у 50,5% отмечено существенное улучшение [44]. В исследовании P. Rygh и соавт. на основании результатов анкетирования 24602 женщин с недержанием мочи было показано, что тренировка мышц тазового дна позволяет уменьшить выраженность симптомов по опроснику ISIQ-UI SF (International Conférence on Incontinence Questionnaire Short Form – Международное соглашение по вопроснику о недержании мочи) в среднем на 1,31 балл, причем эффект был выше у пациенток с более выраженным недержанием: при тяжелой степени регистрировали улучшение на 3,23 балла, при средней тяжести – на 1,41 балл, а при легкой степени – на 0,24 балла. При оценке эффективности тренировочной терапии по анкете PGII (Patient Global Imression of Improvement – Общее впечатление пациента об улучшении) улучшение состояния отметили 65% женщин. В когорте пациенток в рандомизированном контролируемом исследовании подтверждена высокая эффективность: по опроснику ISIQ-UI SF сумма баллов уменьшилась на 3,9 пункта, а по анкете PGI-I улучшение удержания отметили 92% пациенток [45].
Имеются данные, что тренировка мышц тазового дна у женщин в период беременности и в раннем послеродовом периоде уменьшает риск развития недержания мочи, а у женщин с уже развившимся недержанием после родов тренировочные методы являются терапией первой линии.
Тренировочные методики также эффективны у женщин, занимающихся атлетическими видами спорта, у которых риск развития недержания мочи в 3 раза превышает риск в общей популяции, а также у физически активных женщин. Тренировки проводят как для профилактики развития недержания, так и в качестве лечебных мероприятий. Использование программы тренировок мышц тазового дна увеличивает силу мышечных сокращений и уменьшает объем теряемой при нагрузке мочи, повышая качество жизни. У женщин с недержанием мочи, обусловленным пролапсом тазовых органов, тренировочная терапия не только повышает степень удержания, но и уменьшает выраженность пролапса, оцененного по системе РОР.
Для повышения эффективности тренировочной терапии разработаны специальные вспомогательные программы с использованием дополнительных инструктирующих устройств (Femiscan, Myself и др.). В исследовании S.S. Hoseini и соавт. показано, что тренировка мышц тазового дна с использованием телеинструктора при выполнении упражнений Кегеля позволяет улучшить способность удерживать мочу даже у женщин старшего возраста, способствуя их социальной адаптации [46].
В проспективном рандомизированном исследовании, оценившем эффективность использования 4-недельной программы тренировок с дополнительным использованием устройств EmbaGYN (Великобритания) или Magic Kegel Master device (Китай) у 80 женщин с послеродовым недержанием мочи, продемонстрирована эффективность с уменьшением доли женщин с симптомами ургентного недержания с 35,3% до 8,8%, а со стрессовым недержанием – с 41,2% до 11,8% [47].
Многие авторы рекомендуют дополнять тренировки мышц тазового дна физиотерапевтическими методами. Показано, что использование электромагнитной стимуляции мышц тазового дна достоверно улучшает состояние женщин с недержанием мочи, оцененное методом анкетирования с использованием 8 опросников, характеризующих выраженность стрессового недержания мочи, пролапс тазовых органов, гиперактивность детрузора, ургентность и качество жизни без побочных эффектов [48].
Имеется ряд публикаций, свидетельствующих, что тренировка мышц тазового дна помогает не только повысить степень удержания, но и, наоборот, снизить повышенный тонус мышц, вызывающих затруднение мочеиспускания, что позволяет использовать этот метод для лечения женщин с дисфункциональным мочеиспусканием.
Вовлечение тазовых мышц в развитие дисфункционального мочеиспускания обусловило разработку специальных программ тренировок, направленных на снижение тонуса мышц тазового дна.
В проспективном исследовании, проведенном T. Lazaros и соавт., включающем 48 женщин с фИВО (Qmax < 12 мл/сек), оценили результаты тренировочной терапии, проводимой в течение 6 месяцев. Среднее значение максимальной скорости мочеиспускания увеличилось незначительно (с 7,5 до 8,5 мл/сек), объем остаточной мочи уменьшился с 110 до 65 мл. У 7 женщин параметры мочеиспускания нормализовались. Количество женщин с тяжелой степенью обструкции уменьшилось с 8 до 3, со средней степенью обструкции – с 16 до 8. Исходно 20 женщин отмечали 3 и более эпизодов мочевой инфекции в год, а 12 – эпизоды острой задержки мочи. После терапии эпизоды мочевой инфекции отмечены только у 4 пациенток, а случаев острой задержки мочи не было ни у кого [49].
Таким образом, тренировка мышц тазового дна оказывает существенный терапевтический эффект как при недержании мочи, так и при фИВО, хотя в последнем случае в литературе имеются ограниченные сведения.
Использование биологической обратной связи (БОС) как метода повышения эффективности тренировочной терапии при лечении женщин с нарушениями мочеиспускания
В большинстве исследований приводят данные о высокой эффективности тренировочной терапии у женщин с нарушенным мочеиспусканием, однако в ряде публикаций показано, что при самостоятельном применении 25-50% женщин не способны корректно управлять необходимыми мышцами, ошибочно напрягая мышцы антагонисты (ягодичные, мышцы бедра и передней брюшной стенки). Устные и письменные инструкции не повышают результативность таких тренировок. Для повышения эффективности тренировочных программ у этих женщин необходимо сочетание обычных самостоятельных тренировок с аппаратными тренировочными технологиями с медицинским контролем.
Для повышения эффективности тренировочных методов терапии все чаще используют тренировки, основанные на принципе БОС. Сущность БОС заключается в преобразовании биологических сигналов, получаемых от мышц с помощью электромиографии или датчиков давления, установленных во влагалище или на промежности, в аудио-, визуальные или вибрационные сигналы, что позволяет пациентке контролировать тренировочный процесс.
Разработаны специальные устройства, обеспечивающие функцию БОС и помогающие пациенткам контролировать степень напряжения тазовых мышц. БОС постоянно информирует женщин о состоянии их мышц, обеспечивая сознательный контроль их тонуса через обратную связь. Лучший контроль физиологического состояния мышц способствует формированию лучшего управления их тонусом, что улучшает результаты лечения.
В обзоре A.E. Matsi и соавт. проанализирована эффективность применения метода БОС при недержании мочи разных форм (стрессовое, ургентное или смешанное), и показано статистически значимое улучшение контроля мочеиспускания у женщин со стрессовым недержанием при использовании БОС по сравнению с другими вариантами тренировочной терапии, тогда как при ургентном и смешанном недержании эффективность БОС существенно ниже [50].
В обзоре F. Fitz и соавт. приведены данные о повышении способности влиять на тонус мышц тазового дна при использовании технологии БОС по сравнению с традиционными тренировками у женщин со стрессовым недержанием мочи [51].
В работе T.A. Ong и соавт. выявили достоверное повышение возможности напрягать мышцы тазового дна и более быстрое улучшение качества мочеиспускания после 4-недельного курса тренировочной терапии с использованием БОС, по сравнению с аналогичной терапией без БОС. Похожие результаты получены в исследовании M.M. Weinstein и соавт. Быстрое достижение результатов при использовании БОС объясняют более быстрой и более точной идентификацией пациенткой мышц, которые необходимо тренировать, что позволяет целенаправленно влиять на сокращение мышц. Таким образом, БОС может ускорить повышение мышечного тонуса и нейромышечного взаимодействия, способствуя повышению функции удержания мочи. Кроме того, более ранее улучшение степени континенции повышает мотивацию пациенток к продолжению терапии. К таким же выводам приходят F. Goulart и соавт., считающие, что использование БОС улучшает произвольную функцию мышц, усиливает нейропластичность или активирует механизм формирования новых нейронных связей в центральной нервной системе, за счет создания для нее новых потребностей. Процесс нейропластичности позволяет пациенткам постоянно контролировать мышечную активность и управлять ею, давая возможность обеспечивать функцию удержания мочи [52-54].
Помимо более быстрого увеличения силы сокращений, использование принципа БОС позволяет увеличить способность удерживать напряжение тазовых мышц в течение определенного времени, что также повышает возможность удерживать мочу, в том числе при смешанной форме недержания.
В исследовании S. Firinci и соавт. сравнили эффективность тренировочной терапии у женщин с идиопатической гиперактивностью мочевого пузыря и недержанием мочи в сравнении с терапий, дополненной БОС, электростимуляцией или БОС+электростимуляцией. Было показано преимущество комбинированной терапии в группе тренировки+БОС+ электростимуляция, хотя определенное улучшение состояния функции мочеиспускания отмечено во всех группах пациенток. Уменьшались частота мочеиспусканий, частота эпизодов недержания, выраженность ноктурии, повышалась оценка качества жизни [55, 56].
В Национальных рекомендациях Великобритании указано, что использование БОС при тренировках мышц тазового дна в бóльшей степени способствует улучшению качества жизни пациенток, чем применение только тренировочной терапии [57].
Об удовлетворенности результатами лечения с использованием БОС как дополнения к тренировочной терапии свидетельствуют данные о том, что около 60% женщин не прибегают к другим методам лечения и, при необходимости, проходят повторные курсы тренировок [58].
На результаты лечения могут влиять субъективные факторы восприятия пациентками процесса терапии. В частности, использование поверхностных миографических датчиков для осуществления БОС более предпочтительно, чем использование вагинальных датчиков, поскольку при их применении нередко отмечалось жжение во влагалище, болезненное мочеиспускание, раздражение кожи вблизи влагалища. Преимуществом поверхностных электродов является наличие облегченных высокочувствительных моделей, надежно фиксируемых на теле пациентки, что позволяет проводить исследование в различных положениях тела и более точно оценивать динамику лечебного процесса.
Важным вопросом является длительность сохранения эффекта тренировок в отношении способности удерживать мочу. По данным M. Gameiro и соавт., эффект тренировки сохранялся в течение 6 месяцев, но постепенно исчезал к 12 месяцам. По другим данным, уменьшение степени удержания сохранялось в течение 1 года у 70-74% пациенток [59].
В отношении оценки эффективности БОС при терапии дисфункционального мочеиспускания имеется существенно меньше публикаций. C.H. Chiang и соавт. оценили клиническую эффективность БОС в составе тренировочной терапии у женщин с фИВО и установили, что через 3 месяца улучшение качества мочеиспускания и, соответственно, качества жизни отметили более 80% женщин [60].
О более высокой эффективности использования БОС в программе тренировок мышц тазового дна у женщин с фИВО, по сравнению с традиционной тренировочной терапией, сообщается в публикации E. Sam и соавт. При использовании БОС как компонента тренировочной терапии, достигали значительного увеличения максимальной и средней скоростей мочеиспускания, а также значительного уменьшения объема остаточной мочи, по сравнению с группой, где использовались только тренировки. Также в группе с использованием БОС, выраженность симптомов, оцененная по шкале UDI-6 (Urinary Distress Inventory-6 – Шкала оценки расстройств мочеиспускания), оказалась достоверно ниже. Электромиографическая активность мышц тазового дна также уменьшалась в большей степени в группе женщин при использовании метода БОС [61].
Таким образом, суммируя вышеизложенные данные, можно сделать заключение, что применение метода БОС повышает эффективность тренировочной терапии стрессового недержания мочи, но в отношении ургентного или смешанного вариантов недержания данные неоднозначны. Технология БОС также позволяет улучшить результаты лечения пациенток с дисфункциональным мочеиспусканием.
ЗАКЛЮЧЕНИЕ
Проблема лечения женщин с различными функциональными нарушениями является актуальной. Из методов консервативного лечения наиболее часто используют тренировку мышц тазового дна в различных модификациях (самостоятельные тренировки, дополнительное использование телеили аудио-инструктирующих устройств), считающуюся методом терапии первой линии. Тренировка мышц тазового дна позволяет увеличить силу их сокращений и возможность более длительно удерживать мышцы в сокращенном состоянии, что способствует улучшению функции удержания мочи. При этом, не все исследователи находили прямую связь между увеличением мышечного тонуса и улучшением функции нижних мочевыводящих путей, придавая значение психологической составляющей тренировочного процесса. Дополнительное использование метода биологической обратной связи (БОС) позволяет лучше контролировать процесс тренировки и достижения необходимой степени сокращения или расслабления, особенно для тех женщин, у которых самостоятельное управление необходимыми мышцами вызывает трудности. Во многих публикациях приводятся данные о большей эффективности включения БОС в схему тренировок, тогда как в других сообщениях авторы не выявляли различий между группами женщин с тренировками, дополненными БОС или изолированными тренировками. Однако, в части из них оценка проводилась только на основании изменения тонуса тазовых мышц. В отношении тренировочных методов, в том числе с использованием БОС, у женщин с функциональной ИВО данные литературы крайне ограничены, хотя в имеющихся публикациях отмечается положительный эффект включения БОС в схему тренировок.
БОС терапия относится к высокотехнологичным методам лечения, совершенствуется аппаратное сопровождение, в том числе по программе импортозамещения, что открывает широкие перспективы его использования и обеспечения большей доступности в различных звеньях оказания медицинской помощи (поликлиники, женские консультации, санатории, реабилитационные центры).
ЛИТЕРАТУРА
- 1. Abdel Raheem A, Madersbacher H. Voiding dysfunction in women: How to manage it correctly. Arab J Urol 2013;11(4):319-30. https://doi.org/10.1016/j.aju.2013.07.005.
- Gormley EA, Lightner DJ, Faraday M, Vasavada SP. Diagnosis and treatment of overactive bladder (non-neurogenic) in adults: AUA/SUFU guideline amendment. J Urol 2015;193(5):1572-80. https://doi.org/10.1016/j.juro.2015.01.087.
- García-Sánchez E, Rubio-Arias JA, Ávila-Gandía V, Ramos-Campo DJ, López-Román. Effectiveness of pelvic floor muscle training in treating urinary incontinence in women: A current review. J Actas Urol Esp 2016;40(5):271-8. https://doi.org/10.1016/j.acuro.2015.09.001.
- Сивков А.В., Ромих В.В. Инфравезикальная обструкция у женщин. Урология 2006;(5):90-4. [Sivkov A.V., Romikh V.V. Infravesical obstruction in women. Urologiya = Urologiia 2006;(5):90-4. (In Russian)].
- Ермакова Е.И., Балан В.Е., Краснопольская И.В., Тихомирова Е.В. Консервативная терапия недержания мочи у женщин. Российский вестник акушера-гинеколога 2014;(4):113-5. [Ermakova E.I.,Balan V.E., Krasnopol'skaia I.V., Tikhomirova E.V. Medical therapy for female urinary incontinence. Rossiyskiy vestnik akushera-ginekologa = Russian Bulletin of Obstetrician-Gynecologis 2014;(4):113-5. (In Russian)].
- Weber-Rajek M, Strączyńska A, Strojek K, Piekorz Z, Pilarska B, Podhorecka M, et al. A. Assessment of the Effectiveness of Pelvic Floor Muscle Training (PFMT) and Extracorporeal Magnetic Innervation (ExMI) in treatment of stress urinary incontinence in women: A randomized controlled trial. BioMed Res Int 2020;2020:1019872. https://doi.org/10.1155/2020/1019872.
- Milsom I, Gyhagen M. The prevalence of urinary incontinence. Climacteric 2019;22(3):217-22. https://doi.org/10.1080/13697137.2018.1543263
- Ромих В.В. Клиническая уродинамика и нейроурология: от диагностики к эффективному лечению и реабилитации. Экспериментальная и клиническая урология 2010(4):92-8. [Romih V.V. Clinical urodynamics and neurourology: from diagnosis to effective treatment and rehabilitation. Eksperimentalnaya i Klinicheskaya Urologiya = Experimental and Clinical Urology 2010(4):92-8. (In Russian)].
- Серегин А.В., Синякова Л.А., Довлатов З.А., Матвеевская Т.А. Недержание мочи: возможности консервативной терапии. Проблемы женского здоровья 2010;5(1):74-6. [Seryogin A.V., Sinyakova L.A., Dovlatov Z.A., Matveyevskaya T.A. Urinary incontinence: opportunities of conservative treatment. Problemy zhenskogo zdorov'ya = Women's Health Issues 2010;5(1):74-6. (In Russian)].
- Caruso S, Brescia R, Matarazzo MG, Giunta G, Rapisarda AMC, Cianci A. Effects of urinary incontinence subtypes on women's sexual function and quality of life. Urology 2017;108:59-64. https://doi.org/10.1016/j.urology.2017.06.025.
- Sjöström M, Umefjord G, Stenlund H, Carlbring P, Andersson G, Samuelsson E. Internet-based treatment of stress urinary incontinence: 1and 2-year results of a randomized controlled trial with a focus on pelvic floor muscle training. BJU Int 2015;116(6):955-64. https://doi.org/10.1111/bju.13091.
- Harding CK, Lapitan MC, Arlandis S, Cobussen-Boekhorst, E. Costantini, J. Groen, et. al. Management of non-neurogenic female lower urinary tract symptoms. EAU Guidelines 2022:148.
- Flisser AJ, Blaivas JG. Using urodynamics to diagnose bladder outlet obstruction in women. Contemporary Urology 2002:223-5.
- Mytilekas KV, Oeconomou A, Sokolakis I, Kalaitzi M, Mouzakitis G, Nakopoulou E, et al. Defining voiding dysfunction in women: bladder outflow obstruction versus detrusor underactivity. Int Neurourol J 2021;25(3):244-51. https://doi.org/10.5213/inj.2040342.171.
- Agarwal MM, Sharma S, Jain S, Prasad D, Bhaskar V, Gupta S, et al. Can urodynamic diagnosis of dysfunctional voiding/external sphincter nonrelaxation be made on two-channel pressure-flow study without video-urodynamics, electromyography, or urethral pressure profilometry? Plateau detrusor pattern in perspective. Neurourol Urodyn 2022;41(4):935-44. https://doi.org/10.1002/nau.24897.
- Terlikowski R, Dobrzycka B, Kinalski M, Kuryliszyn-Moskal A, Terlikowski SJ. Transvaginal electrical stimulation with surface-EMG biofeedback in managing stress urinary incontinence in women of premenopausal age: a double-blind, placebo-controlled, randomized clinical trial. Int Urogynecol J 2013;24(10):1631-8. https://doi.org/10.1007/s00192-013-2071-5.
- Brucker BM, Fong E, Shah S, Kelly C, Rosenblum N, Nitti VW. Urodynamic differences between dysfunctional voiding and primary bladder neck obstruction in women. Urology 2012;80(1):55-60. https://doi.org/10.1016/j.urology.2012.04.011.
- Hickling D, Aponte M, Nitti V. Evaluation and management of outlet obstruction in women without anatomical abnormalities on physical exam or cystoscopy. Curr Urol Rep 2012t;13(5):356-62. https://doi.org/10.1007/s11934-012-0267-8.
- Vo A, Kielb SJ. Female voiding dysfunction and urinary incontinence. Med Clin North Am 2018;102(2):313-24. https://doi.org/10.1016/j.mcna.2017.10.006.
- Imamura M, Jenkinson D, Wallace S, Buckley B, Vale L, Pickard R. Conservative treatment options for women with stress urinary incontinence: clinical update. Br J Gen Pract 2013;63(609):218-20. https://doi.org/10.3399/bjgp13X665477.
- van Geen FJ, van de Wetering EHM, Nieuwhof-Leppink AJ, Klijn AJ, de Kort LMO. Dysfunctional voiding: exploring disease transition from childhood to adulthood. Urology 2023;177:60-4. https://doi.org/10.1016/j.urology.2023.03.018.
- Petros PE. The pelvic floor muscle training manoeuvre works by increasing intraurethral resistance. Comment on «Influence of voluntary pelvic floor muscle contraction and pelvic floor muscle training on urethral closure pressures: a systematic literature review». Int Urogynecol J 2016;27(12):1943-4. https://doi.org/10.1007/s00192-016-3182-6.
- Petros PE, Ulmsten U. An integral theory of female urinary incontinence. Acta Obstet Gynecol Scand Suppl 1990;153:7-31. https://doi.org/10.1111/j.1600-0412.1990.tb08027.x.
- Касян Г.Р., Вишневский Д.А., Акуленко Л.В., Козлова Ю.О., Шарова Е.И., Тупикина Н.В., Пушкарь Д.Ю. Ассоциация полиморфизма 1800255 гена СОL3A1 с развитием пролапса тазовых органов и недержания мочи у женщин: предварительные данные. Урология 2017;(6):30-3. [Kasyan G.R., Vishnevskii D.A., Akulenko L.V., Kozlova Yu.O., Sharova E.I., Tupikina N.V., Pushkar D.Yu. association of polymorphism of 1800255 COL3A1. Urologiya = Urologiia 2017;(6):30-3. (In Russian)]. https://doi.org/10.18565/urology.2017.6.30-33.
- Cacciari LP, Amorim AC, Pyssaro AC, Dumoulin C, Sacco ICN. Intravaginal pressure profile of continent and incontinent women. J Biomech 2020;99:10972. https://doi.org/10.1016/j.jbiomech.2019.10972.
- Deindl FM, Vodusek DB, Bischoff C, Hofmann R, Hartung R. Dysfunctional voiding in women: which muscles are responsible? Br J Urol 1998;2(6):814-9. https://doi.org/10.1046/j.1464-410x.1998.00866.x.
- Groutz A, Blaivas JG, Pies C, Sassone AM. Learned voiding dysfunction (nonneurogenic, neurogenic bladder) among adults. Neurourol Urodyn 2001;20(3):259-68. https://doi.org/10.1002/nau.1003.
- Panicker JN, Selai C, Herve F, Rademakers K, Dmochowski R, Tarcan T, et al. Psychological comorbidities and functional neurological disorders in women with idiopathic urinary retention: International Consultation on Incontinence Research Society (ICI-RS) 2019. Neurourol Urodyn 2020;39(Suppl 3):S60-S69. https://doi.org/10.1002/nau.24233.
- Peyronnet B, Lapitan MC, Tzelves L, O'Connor E, Nic An Riogh A, et al. Benefits and harms of conservative, pharmacological, and surgical management options for women with bladder outlet obstruction: A systematic review from the European Association of Urology Non-neurogenic Female LUTS Guidelines Panel. Eur Urol Focus 2022;8(5):1340-61. https://doi.org/10.1016/j.euf.2021.10.006.
- Cody JD, Jacobs ML, Richardson K, Moehrer B, Hextall A. Oestrogen therapy for urinary incontinence in post-menopausal women. Cochrane Database Syst Rev 2012;10(10):CD001405. https://doi.org/10.1002/14651858.CD001405.pub3.
- Minardi D, Pellegrinelli F, Conti A, Fontana D, Mattia M, Milanese G, et al. α1Blockers for the treatment of recurrent urinary tract infections in women with dysfunctional voiding: a prospective randomized study. Int J Urol 2015;22(1):115-21. https://doi.org/10.1111/iju.12601.
- Ромих В.В., Захарченко А.В., Коршунова Е.С., Кукушкина Л.Ю. Использование ботулинического токсина тина А у пациентов с нейрогенными нарушениями мочеиспускания. Экспериментальная и клиническая урология 2010;(1):81-4. [Romikh V.V., Zaharchenko A.V., Korshunova E.S., Kukushkina L.U. Using of botulinum a toxin in treatment of neurogenic voiding desorders patients. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2010;(1):81-4. (In Russian)].
- Sokol ER, Karram MM, Dmochowski R. Efficacy and safety of polyacrylamide hydrogel for the treatment of female stress incontinence: a randomized, prospective, multicenter North American study. J Urol 2014;192(3):843-9. https://doi.org/10.1016/j.juro.2014.03.109.
- Jiang YH, Lee CL, Chen SF, Kuo HC. Therapeutic Effects of Urethral Sphincter Botulinum Toxin A Injection on Dysfunctional Voiding with Different Videourodynamic Characteristics in Non-Neurogenic Women. Toxins (Basel) 2021;13(5):362. https://doi.org/10.3390/toxins13050362.
- Ford AA, Rogerson L, Cody JD, Aluko P, Ogah JA. Mid-urethral sling operations for stress urinary incontinence in women. Cochrane Database Syst Rev 2017;7(7):CD006375. https://doi.org/10.1002/14651858.CD006375.pub4.
- Колотева Е.В., Чаркина О.В., Шилина А.В., Бельских О.Л. Результат использования TVT-петли при пролапсе тазовых органов, осложненном недержанием мочи. Молодежный инновационный вестник 2018;7(S1):109. [Koloteva E.V., Charkina O.V., Shilina A.V., Belskikh O.L. The result of using TVT-loop in pelvic organ prolapse complicated by urinary incontinence. Molodozhnyy innovatsionnyy vestnik 2018;7(S1):109. (In Russian)].
- Gurol-Urganci I, Geary RS, Mamza JB, Duckett J, El-Hamamsy D, Dolan L, et al. Long-term rate of mesh sling removal following midurethral mesh sling insertion among women with stress urinary incontinence. JAMA 2018;320(16):1659-69. https://doi.org/10.1001/jama.2018.14997.
- Fusco F, Abdel-Fattah M, Chapple CR, Creta M, La Falce S, Waltregny D, et al. Updated systematic review and meta-analysis of the comparative data on colposuspensions, pubovaginal slings, and midurethral tapes in the surgical treatment of female stress urinary incontinence. Eur Urol 2017;72(4):567-91. https://doi.org/10.1016/j.eururo.2017.04.026.
- Giarenis I, Mastoroudes H, Cardozo L, Robinson D. Rediscovery of open colposuspension as a salvage continence operation. Int Urogynecol J 2012;23(8):1117-22. https://doi.org/10.1007/s00192-012-1720-4.
- Utomo E, Groen J, Blok BF. Surgical management of functional bladder outlet obstruction in adults with neurogenic bladder dysfunction. Cochrane Database Syst Rev 2014;2014(5):CD004927. https://doi.org/10.1002/14651858.CD004927.pub4.
- Brasure M, Fink HA, Risk M, MacDonald R, Shamliyan T, Ouellette J, et al. Chronic urinary retention: Comparative effectiveness and harms of treatments. Rockville (MD): AHRQ (US) 2014.
- Leong BS, Mok NW. Effectiveness of a new standardized urinary continence physiotherapy program for community-dwelling older women in Hong Kong. Hong Kong Med J 2015;21(1):30-7. https://doi.org/10.12809/hkmj134185.
- Curillo-Aguirre CA, Gea-Izquierdo E. Effectiveness of pelvic floor muscle training on quality of life in women with urinary incontinence: A systematic review and meta-analysis. Medicina (Kaunas) 2023;59(6):1004. https://doi.org/10.3390/medicina59061004.
- Alouini S, Memic S, Couillandre A. Pelvic floor muscle training for urinary incontinence with or without biofeedback or electrostimulation in women: A systematic review. Int J Environ Res Public Health 2022;19(5):2789. https://doi.org/10.3390/ijerph19052789.
- Rygh P, Asklund I, Samuelson E. Real-world effectiveness of app-based treatement for urinary incontinence: a cohort study. BMJ Open 2021;11(1):e040819. https://doi.org/10.1136/bmjopen-2020-040819.
- Hoseini SS, Ghahremani L, Khorasani F, Yarelahi M, Asadollahi A. Training of pelvic floor muscle training improves the severity and quality of urine incontinence and increases social participation of older women in Southern Iran. Curr Aging Sci 2024;17(1):68-73. https://doi.org/10.2174/1874609816666230816125026.
- Artymuk NV, Khapacheva SY. Device-assisted pelvic floor muscle postpartum exercise programme for the management of pelvic floor dysfunction after delivery. J Matern Fetal Neonatal Med 2022;35(3):481-5. https://doi.org/10.1080/14767058.2020.1723541.
- Борисенко Л.Ю., Сивков А.В., Ромих В.В., Захарченко А.В., Пантелеев В.В., Костин А.А., Аполихин О.И. Результаты исследования метода биологической обратной связи с тестовой электростимуляцией мышц тазового дна в качестве монотерапии и в сочетании с экстракорпоральной магнитной стимуляцией мышц тазового дна при функциональной инфравезикальной обструкции у женщин. Экспериментальная и клиническая урология 2019;(2):146-51. [Borisenko L.Yu., Sivkov A.V., Romikh V.V., Zakharchenko A.V., Panteleyev V.V., Kostin A.A., Apolikhin O.I. The results of the comparative study of biofeedback with test electrostimulation of the pelvic floor muscles as monotherapy and in combination with extracorporeal magnetic stimulation of the pelvic floor muscles with functional infravesical obstruction in women. Eksperimentalnaya i Klinicheskaya Urologiya = Experimental and Clinical Urology 2019;(2):146-51. (In Russian)].
- Lazaros T, Ioannis T, Vasileios S, Christina P, Michae S. The effect of pelvic floor muscle training in women with functional bladder outlet obstruction. Arch Gynecol Obstet 2023;307(5):1489-94. https://doi.org/10.1007/s00404-023-06930-z.
- Matsi AE, Billis E, Lampropoulou S, Xergia SA, Tsekoura M, Fousekis K. The effectiveness of pelvic floor muscle exercise with biofeedback in women with urinary incontinence: A systematic review. Appl Sci 2023;23:12743. https://doi.org/10.3390/app132312743.
- Fitz FF, Resende AP, Stüpp L, Costa TF, Sartori MG, Girão MJ, et al. Effect the adding of biofeedback to the training of the pelvic floor muscles to treatment of stress urinary incontinence. Rev Bras Ginecol Obstet 2012;34(11):505-10. https://doi.org/10.1590/s0100-72032012001100005.
- Ong TA, Khong SY, Ng KL, Ting JR, Kamal N, Yeoh WS, et al. Using the Vibrance Kegel Device with pelvic floor muscle exercise for stress urinary incontinence: A randomized controlled pilot study. Urology 2015;86(3):487-91. https://doi.org/10.1016/j.urology.2015.06.022.
- Weinstein MM, Collins S, Quiroz L, Anger JT, Paraiso MFR, DeLong J, et al. Multicenter randomized controlled trial of pelvic floor muscle training with a motionbased digital therapeutic device versus pelvic floor muscle training alone for treatment of stress-predominant urinary incontinence. Female Pelvic Med Reconstr Surg 2022;28(1):1-6. https://doi.org/10.1097/SPV.0000000000001052.
- Goulart F, Vasconcelos KS, de Souza MR, Pontes PB. Physical therapy for facial paralysis using the biofeedback. Acta Fisiátr 2002(9):134-40.
- Firinci S, Yildiz N, Alkan H, Aybek Z. Which combination is most effective in women with idiopathic overactive bladder, including bladder training, biofeedback, and electrical stimulation? A prospective randomized controlled trial. Neurourol Urodyn 2020;39(8):2498-508. https://doi.org/10.1002/nau.24522.
- Özengin N, Bakar Y, Özdemir C, Duran B. The comparison of EMGbiofeedback and extracorporeal magnetic innervation treatments in women with urinary incontinence. Clin Exp Obstet Gynecol 2016;43(4):550-4.
- National Guideline Alliance UK. Urinary Incontinence and Pelvic Organ Prolapse in Women: Management 2019. [Electronic resource]. URL: www.nice.ork.uk/guidance/ng123.
- Yoo EH, Kim YM, Kim D. Factors predicting the response to biofeedback-assisted pelvic floor muscle training for urinary incontinence. Int J Gynaecol Obstet 2011;112(3):179-81. https://doi.org/10.1016/j.ijgo.2010.09.016.
- Sigurdardottir T, Steingrimsdottir T, Geirsson RT, Halldorsson TI, Aspelund T, Bø K. Can postpartum pelvic floor muscle training reduce urinary and anal incontinence? An assessor-blinded randomized controlled trial. Am J Obstet Gynecol 2020;222(3):247.e1-247.e8. https://doi.org/10.1016/j.ajog.2019.09.011.
- Chiang CH, Jiang YH, Kuo HC. Therapeutic efficacy of biofeedback pelvic floor muscle exercise in women with dysfunctional voiding. Sci Rep 2021;11(1):13757. https://doi.org/10.1038/s41598-021-93283-9.
- Hagen S, Elders A, Stratton S, Sergenson N, Bugge C, Dean S, et al. Effectiveness of pelvic floor muscle training with and without electromyographic biofeedback for urinary incontinence in women: Multicentre randomised controlled trial. BMJ 2020;371:m3719. https://doi.org/10.1136/bmj.m3719.







