Новый радиофармацевтический препарат, Резоскан 99m Tc в диагностике патологических изменении скелета у больных раком предстательной железы
 23996
23996 В широкой медицинской практике в настоящее время применяются различные радиофармацевтические препараты (РФП) с целью радионуклидной диагностики метастатического поражения костей. Основным изотопом в составе этих РФП является технеций-99м (99mTc), имеющий идеальный для сцинтиграфии моноэнергетический спектр гамма-излучения (140 кэВ) и малый период полураспада (6 ч.), что позволяет минимизировать облучение пациента. Кроме того, 99mTc удобен для клинического применения, так как получается из генератора непосредственно в условиях клинической радиоизотопной лаборатории, легко образует комплексы с химическими соединениями, тропными к различным органам и тканям.
В начале семидесятых годов прошлого столетия G. Subramanian и J.G. Agfee впервые предложили использовать для остеосцинтиграфии фосфатные комплексы технеция-99м полифосфат, трифосфат и пирофосфат [1]. Было найдено, что накопление в костях обратно пропорционально длине цепи полифосфата, что объясняло наилучшее накопление в костях комплекса 99mTc с пирофосфатом [2].
В костной ткани фосфатные соединения 99шТс связываются с кристаллами гидроксиапатита и незрелым коллагеном [3]. Однако в связи с тем, что в неорганических фосфатах присутствует связь Р-О-Р, они подвергаются энзиматическому гидролизу in vivo под воздействием фосфатазы. Известными особенностями фармакокинетики фосфатов неорганической природы являются медленный клиренс крови, а также замедленные сроки максимального накопления в скелете при невысоких отношениях активности в костях к активности в мышцах [1]. Кроме того, как правило, наблюдается накопление препарата в печени до 10-15% от введенной активности. Это создает определенные ограничения для применения препаратов, содержащих пирофосфат, для остеосцинтиграфии [4].
Впоследствии было установлено, что определенными преимуществами перед вышеперечисленными фосфатными комплексами обладают 99шТс-дифосфонаты [5], которые не подвержены гидролизу in vivo, а также характеризуются более низким уровнем связывания с белками плазмы и эритроцитами, что, в свою очередь, позволяет получить высокое соотношение костная ткань-окружающие ткани. При обсуждении механизма накопления радиофармацевтического препарата (РФП) в костной ткани показано [5], что на накопление 99mTc-HEDP (99™Тсгидроксиэтилидендифосфонат) положительно влияет повышенный уровень кальция в сыворотке крови. Другие возможные механизмы накопления, такие как высокое сродство к органической составляющей костной ткани или белкам окружающей ткани [6], к фосфатазе [5], имеют меньшее значение для накопления РФП в костях.
Структурное сходство дифос фонатов с минералом кости гидрокси-апатитом, составляющим почти 2/3 общего веса кости в сочетании с органической матрицей связи Р-С-Р, делает их устойчивыми к химическому и ферментативному гидролизу [2]. Кроме того, их аффинность к гидроксиапатиту, определяющая способность дифосфонатов откладываться в местах образования новой кости, имеет фундаментальное значение. Дифосфонаты сохраняются в местах нового костеобразования до тех пор, пока не произойдет замена старой кости на новую. Благодаря этим свойствам комплексы дифосфонатов с технецием-99м могут быть использованы в качестве радиофармацевтических средств диагностики патологических состояний костной ткани, сопровождающихся остеобластическими процессами.
В настоящее время в мировой радиологической практике наиболее широко применяются 99шТс-метилендифосфонат (99шТсMDP) и 99шТс-гидроксиэтилидендифосфонат ("'^Ix-HEDP, в русскоязычной литературе ОЭДФ), а также некоторые другие производные органических дифосфонатов [7]. В Институте биофизики в начале 80-х годов прошлого века были получены данные по распределению остеотропных препаратов в организме лабораторных животных [8, 9].
Фармакокинетика препаратов технеция с такими органическими фосфатами, как гидроксиэтилидендифосфонат (этидронат) и метилендифосфонат (медронат), характеризуется быстрым клиренсом крови, высоким накоплением в скелете уже через 1 час после внутривенного введения и быстрым выведением через мочевыделительную систему организма. G. Subramanian с соавт. [10] еще в середине 70-х годов XX века провели сравнительное изучение остеотропных препаратов технеция-99м и пришли к выводу, что наилучшие результаты по визуализации скелета получены с препаратом 99mTc-MDP, который до настоящего времени считают «золотым стандартом» при диагностических исследованиях скелета.
В настоящее время активно продолжается поиск новых остеотропных препаратов с большей чувствительностью, разрешающей способностью при визуализации и высокой скоростью выведения радиоизотопа из организма с целью повышения эффективности дифференциальной диагностики злокачественных поражений скелета, остеомиелита и других патологических состояний.
На IX Конгрессе Всемирной федерации ядерной медицины и биологии (2006 г.) группа китайских исследователей [11] сообщила о разработке нового радиодиагностического препарата на основе золедроновой кислоты, меченной технецием-99м. Накопление препарата в кости нормальных мышей составило 13,45% от введенной дозы/г, соотношения кость-мышцы и кость-кровь 28,01 и 16,96 через 30 мин. после инъекции соответственно. Рассчитано кинетическое уравнение кровяного клиренса: С = 30,789е 0,460t + 1,553е 0,013t. Четкая визуализация костной системы кролика была получена через 75 мин. после инъекции.
Золедроновая кислота является самым современным бисфос фонатом IV поколения и обладает максимальной способностью подавлять костную резорбцию за счёт наибольшей аффинности к участкам усиленной резорбции костной ткани [16]. In vitro золедроновая кислота ингибирует активность и индуцирует апоптоз остеокластов, блокирует остеокластическую резорбцию минерализированной костной и хрящевой ткани, ингибирует повышение активности остеокластов и высвобождения кальция из костной ткани под влиянием стимулирующих факторов, освобождающихся из опухолевых клеток.
В настоящее время в России зарегистрированы препараты на основе золедроновой кислоты Зoмета (Novartis) и Резорба (ЗАО «Фарм-Синтез»). Мировой опыт использования меченых бисфосфонатов в ядерной медицине с одной стороны, а также позитивные результаты последних лет в клиническом применении золедроновой кислоты с другой стороны явились основанием для создания РФП на основе золедроновой кислоты для радионуклидной диагностики и терапии. Препарат Резоскан,99™^ был разработан в ЗАО «Фарм-Синтез» (Москва) и испытан в ГНЦ «Институт биофизики» в 2006-2007 гг.
Исследование фармакокинетики радиофармацевтического препарата Резоскан, 99mTc показало, что для физиологического распределения исследуемого РФП характерна выраженная остеотропность. После внутривенного введения препарата интактным животным через 1 ч. до 52,5% введенной активности локализуется в скелете и 40% выводится из организма с мочой. Через 3 ч. после введения накопление в скелете составляет 48,9%, выведение 40%. Уровень активности в крови не превышает 1,9% через 1 ч. после введения, снижаясь к 24 ч. после начала исследования до фоновых величин. В остальных органах также не происходит значимого накопления препарата.
Согласно «Руководству по экспериментальному (доклиническому) изучению новых радиофармацевтических препаратов» [14] препарат Резоскан,9911^: можно отнести к РФП на основе химических соединений с изученными фармакологическими свойствами, т.к. одним из основных веществ является золедроновая кислота, которая относится к фармакологической группе 8.8 (Корректоры метаболизма костной и хрящевой ткани) [15]. В то же время в состав радиофармацевтического препарата Резоскан,99mTc не идентичен известным лекарственным формам на основе золедроновой кислоты.
Изученные образцы препарата Резоскан,9911'^ были стерильны, апирогенны и не вызывали у животных нежелательных реакций при внутривенном введении. Экспериментальное исследование показало безвредность применения данного препарата.
Из всего вышесказанного можно заключить, что Резоскан,99"'^ первый в мировой практике коммерческий радиофармацевтический препарат (РФП) на основе золедроновой кислоты, предназначенный для выявления патологических изменений костной системы методами ядерной медицины.
Основным отличием от существующих РФП подобного типа является использование в качестве основной субстанции (таргетного носителя) бисфосфоната последнего поколения золедроновой кислоты, которая обладает максимальной аффинностью (по сравнению с другими используемыми бисфосфонатами) к участкам патологически повышенной резорбции костной ткани, в том числе к очагам метастатического происхождения при новообразованиях различной локализации и происхождения.
С целью оценки эффективности и безопасности препарата Резоскан,9911'^ при патологических изменениях скелета у больных раком предстательной железы нами было предпринято открытое мультицентровое сравнительное исследование результатов остеосцинтиграфии с препаратами Резоскан, 99mTc и Технефор, 99mTc.
МАТЕРИАЛЫ И МЕТОДЫ
Для оценки чувствительности и безопасности препарата Резоскан в исследование было включено 20 пациентов с диагнозом «распространенный рак предстательной железы» после его первоначального обнаружения методами УЗИ, КТ и морфологического подтверждения. В исследование отбирались пациенты с клиническими и/или рентгенологическими признаками патологических изменений костной системы. Изучалась частота совпадений результатов остеосцинтиграфии, проведенной с препаратами Резоскан, 99mTc и Технефор, 99mTc. Безопасность препаратов оценивалась на основании анализа частоты нежелательных явлений и побочных эффектов.
У всех больных исследуемой группы в разные сроки до включения в исследование был установлен рак предстательной железы. Ранг значений уровня ПСА в сыворотке крови составил 110-2150 нг/ мл. У больных было выявлено или предполагалось поражение скелета метастатическим процессом по клиническим данным, а также в результате рентгенологического и радиоизотопного исследований. Больные получали специфическую терапию, согласно установленной стадии и форме основного заболевания.
Все пациенты дали письменное информированное согласие на участие в исследовании и соблюдали указания врача. Из протокола были исключены пациенты: с установленной повышенной чувствительностью к препаратам, содержащим 99mTc; прошедшие радиологическое исследование с 111In или 67Ga в течение 10 дней перед включением в исследование, а также пациенты, которые, по мнению исследователя, по какой-либо причине не подходили для участия в нем.
Резоскан, 99mTc вводился внутривенно, исходя из расчета 5 МБк на 1 кг массы тела. В данном исследовании сцинтиграфию у всех пациентов проводили через 1 час после инъекции препарата. Технефор,99шТс вводился внутривенно в количестве 5 МБк на 1 кг массы тела пациента, сканирование проводилось через 3 часа после инъекции препарата. Исследование проводилось с использованием гамма-камеры. Интервал между сцинтиграфией с применением Резоскана, 99mTc и Технефора,99mTc составлял не менее чем 72 часа.
Изображения, полученные при остеосцинтиграфии с препаратами Резоскан,99mTc и Технефор,99mTc анализировались врачом-радиологом, оценивались на наличие или отсутствие захвата 99mTc в костях скелета. Изображения, полученные с применением препаратов Резоскан,99mTc и Технефор,99mTc считались положительными, если определялись очаги накопления в костях скелета с разницей накопления радиофармпрепарата в симметричной области более 40% (КДН > 140%). Изображения считались отрицательными в случае отсутствия очагов гиперфиксации радионуклида.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
По нашим данным и данным литературы чувствительность остеосцинтиграфии существенно превышает чувствительность рентгенологических методов при выявлении метастатического поражения скелета у больных раком предстательной железы. В связи с этим рентгенография не должна применяться в качестве рутинного метода диагностики.
В рамках настоящего исследования визуализация изображений при сцинтиграфии с препаратом Резоскан,99'1'^ проводилась через 1 час после его введения у всех пациентов и, дополнительно, у отдельных пациентов через 3 часа, с целью сравнения его разрешающей способности с таковой у препарата Технефор,99mTc, для которого в соответствии с инструкцией по применению визуализация изображений осуществлялась через 3 часа после введения.
Полученные результаты свидетельствуют о равноэффек тивной диагностической значимости исследуемого препарата Резоскан,99mTc (через 1 час после введения) и Технефор,99mTc (через 3 часа после введения). Так, не было зарегистрировано существенных различий по минимальным значениям КДН 1,48 ± 0,29 против 1,41 ± 0,52 соответственно (достоверность различий р = 0,668 по критерию Стьюдента с поправкой Йетса), и по максимальным значениям КДН 2,22 ± 1,19 против 1,88 ± 0,82 соответственно (достоверность различий р = 0,381). При этом было выявлено лучшее разрешение при сцинтиграфии препаратом Резо^ан,^^, как через 1 час, так и через 3 часа после введения, по сравнению с препаратом Технефор,99mTc через 3 часа после введения. Данная закономерность установлена как по минимальным, так и по максимальным значениям КДН (р = 0,06 по критерию МаннаУитни). При этом корреляционный анализ показал высокую степень сопряженности в парных выборках (R = 0,9102).
Сцинтиграфия с препаратом Резоскан,99тТс оказалась достоверно более чувствительной, чем аналогичное исследование с Технефором,99тТс. Так, у отдельных больных удалось визуализировать очаги накопления с препаратом Резоскан,99тТс, не обнаруженные с препаратом Технефор,99тТс (p < 0,05, критерий х2 Пирсона). Важно отметить, что данные отличия были зарегистрированы при сцинтиграфии препаратом Резоскан,99тТс уже через 1 час после введения.
Особый интерес представляет случай выявления одиночного метастаза литической природы при первичной сцинтиграфии у больного гормонорезистентным раком предстательной железы с препаратом Резоскан,99тТс, не выявленного с препаратом Технефор,99тТс (рисунок 1, А, Б). Данный факт позволил обосновать и назначить больному раннюю терапию препаратом золедроновой кислоты (Резорба).
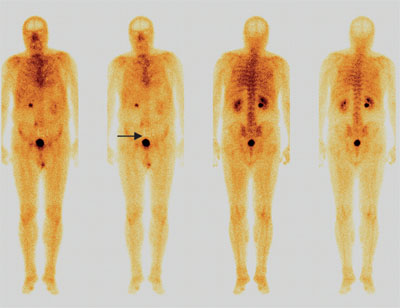
Рисунок 1, А. Визуализация очага накопления в L5 с препаратом Резоскан, 99mTc через 1 час
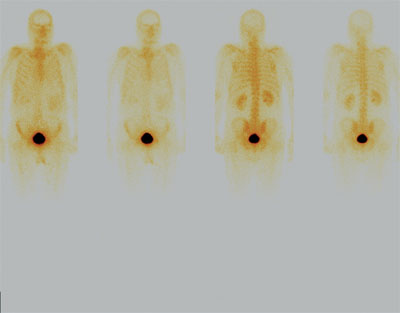
Рисунок 1, Б. Тот же больной, отсутствие визуализации с препаратом Технефор, 99mTc через 3 часа
Резоскан,99тТс продемонстрировал лучшую диагностическую ценность при дифференциальной диагностике локальных и множественных очаговых поражений костного скелета по сравнению с Технефором,99тТс. Так, у одного больного была проведена дифференциальная диагностика множественных очаговых поражений костного скелета, характерных для тотального метастатического поражения при раке предстательной железы или болезни Педжета. Были выявлены поражения скелета, характерные для метастатического рака предстательной железы, но не для болезни Педжета (рисунок 2). У другого больного раком предстательной железы, с выраженным болевым синдромом, исследование с Резосканом,99тТс позволило провести дифференциальную диагностику между специфическим поражением скелета и артрозом (рисунок 3).
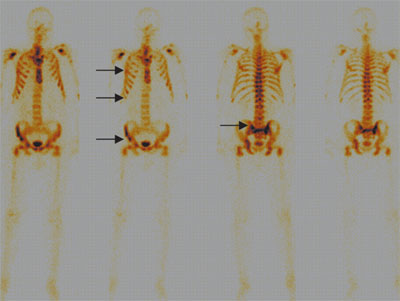
Рисунок 2. Визуализация метастатических очагов с препаратом Резоскан, 99mTc через 1 час
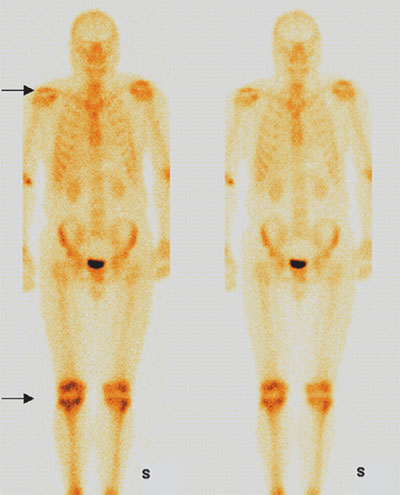
Рисунок 3. Типичная картина артроза, выявленная при сканировании с Резосканом, 99mTc через 1 час
Важным является факт получения более четких сцинтиграмм при использовании препарата Резоскан,99тТс по сравнению с Технефором,99тТс при костнодегенеративных состояниях. Это обусловлено как более высокой чувствительностью, так и значительно большей скоростью выведения Резоскана,99тТс из мягких тканей и крови, как было показано при изучении фармакокинетики в доклинических исследованиях.
В ходе исследования нами установлено, что применение коротких курсов терапии препаратами золедроновой кислоты (до 3 мес.) существенно не влияет на эффективность визуализации очагов метастатического поражения скелета (рисунок 4). В то же время проведение длительных курсов химиотерапии в сочетании с применением препаратов золедроновой кислоты приводит к прекращению накопления радиофармпрепарата в ранее выявленных и, вероятно, подавленных очагах метастатического поражения (рисунок 5). Данный факт позволяет применять препарат Резоскан,99тТс для контроля степени подавления специфической резорбции костной ткани при терапии препаратами золедроновой кислоты и/или химиотерапии и, следовательно, оценивать эффективность различных видов терапии метастатических поражений скелета в динамике.
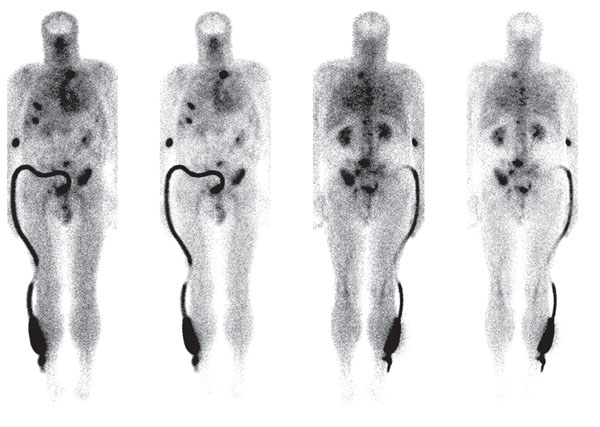
Рис. 4 Визуализация очагов поражения скелета с Резосканом, 99mTc у больного РПЖ на фоне лечения препаратом золедроновой кислоты в течение 2 месяцев
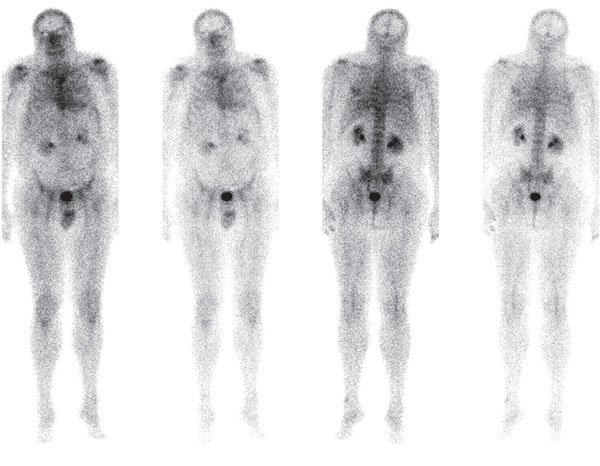
Рисунок 5. Прекращение накопления Резоскана, 99тТс в очагах поражения скелета у того же больного РПЖ на фоне лечения доцетакселом и препаратом золедроновой кислоты в течение 8 месяцев
Согласно протоколу клинического исследования Резоскана,99тТс должны были регистрироваться любые нежелательные события с момента его инъекции и до завершения исследования. Каких-либо нежелательных событий, вызванных введением исследуемого препарата, в течение всего времени исследования не было зарегистрировано.
ВЫВОДЫ
- Препарат Резоскан,99тТс превосходит препаратТехнефор,99тТс по разрешающей способности и, соответственно, по чувствительности при остеосцинтиграфии метастатических поражений скелета у онкологических больных.
- Сцинтиграфия с препаратом Резоскан,99mTc позволяет выявлять литические метастазы при первичной диагностике костных поражений скелета при раке предстательной железы, что позволяет рекомендовать раннее назначение препаратов золедроновой кислоты для лечения и предупреждения дальнейшего метастазирования.
- Сцинтиграфия с препаратом Резоскан^^Г:, в отличие от Технефора^^Г:, обеспечила возможность дифференциальной диагностики между метастатическим поражением скелета и костнодегенеративными изменениями неонкогенной природы, что определило выбор дальнейшей терапии.
- Препарат Резоскан,99тТс, в отличие от Технефора,99тТс, позволил диагностировать активность деструктивного процесса при дегенеративных поражениях скелета неонкогенной природы, в частности при заболеваниях суставов и позвоночника.
- Сцинтиграфия с препаратом Резоскан,99тТс позволила контролировать степень подавления резорбции косной ткани при терапии препаратами золедроновой кислоты и при их комбинации с химиотерапией и тем самым оценивать эффективность лечения пациентов с метастатическими поражениями скелета в динамике.
- Сцинтиграфия с препаратом Резоскан,99тТс экономически целесообразна, так как позволяет примерно на 67% сократить время исследования по сравнению с Технефором.
Таким образом, в результате клинического исследования была доказана высокая эффективность и безопасность нового препарата для остеосцинтиграфии у больных с патологическим процессом в костном скелете. Препарат Резоскан,99тТс может быть рекомендован к широкому клиническому использованию в клинической практике лечебных учреждений на территории РФ.
Ключевые слова: рак предстательной железы, костные метастазы, радиоизотопная диагностика, золедроновая кислота, Резоскан.
ЛИТЕРАТУРА
- G. Subramanian, J.G. Agfee // Radiology. 1971. Vol. 99. P. 192.
- Nuclear Medicine. Diagnosis and Therapy // J.C. Harbert, W.C. Eckelman, R.D. Neumann Eds. Thieme Medical Publishers, Inc., New York. 1996.
- Радионуклидная диагностика для практических врачей / Под ред. Ю.Б. Лишманова, В.И. Чернова. Томск: SST 2004. С. 279-292.
- Rosenhall L., Kaye M. Technetium-99m pyrophosphate kinetics an imaging in metabolic bone disease // J. Nucl. Med. 1975. Vol. 16. P. 33.
- Schmitt G.H., Holmes R.A., Isitman А.Т. A proposed mechanism for 99mTc-labeled polyphosphate and diphosphonate uptake by human breast tissue // Radiology. 1974. Vol. 112. P. 733.
- Dewanjee M.K., Kahn P.C. Mechanism of localization of 99mTc-labeled pyrophosphate and tetracycline in infarcted myocardium. // J. Nucl. Med. 1976. Vol. 17. P. 639.
- WC. Eckelman, WA. Volkert. In vivo chemistry of 99mTc-chelates // Int. J. Appl. Radiat. Isotopes. 1982. Vol. 33. P. 945.
- Изыскание новых остеотропных препаратов с технецием-99м на основе полиметиленффосфоновых кислот: Отчет о НИР (заключительный) / Институт биофизики (ИБФ МЗ СССР); Руководитель И.А. Володин. Инв. № Б-4388. М. 1983. 30 с ил. Отв. исполнитель Г.Е. Кодина, М.А. Грачева.
- We A.J., Francis M.D. In vitro stabilization of a low-tin bone-imaging agent (99mTcSn-HEDP) by ascorbic acid. // J. Nucl. Med. 1976. Vol. 17. P. 820.
- G. Subramanian, J.G. McAfee et al. Tc-99m-methylenediphosphonate a superior agent for skeletal imaging: comparison with other technetium complexes. // J.Nucl. Med. 1975. Vol. 16. P. 744.
- S Luo H.-Y. / Wang M.-H. Xie et al The study on the preparation and biodistribution of Tc-99m-ZL // World J.Nucl.Med. 2006. Vol. 5. Suppl. 1. S65.
- ОСПОРБ
- Методические указания МУ 2.6.1.1892-04 «Гигиенические требования по обеспечению радиационной безопасности при проведении радионуклидной диагностики с помощью радиофармпрепаратов»
- Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / под ред. члена-корреспондента РАМН, профессора Хабриева. Москва 2005.
- Энциклопедия лекарств. 12-й выпуск / Гл. ред. Г.Л. Вышковский. М. РЛС-2005. С. 366.
- Золедроновая кислота новый бисфосфонат в лечении костных метастазов и опухоль-индуцированной гиперкальциемии. // Современная онкология. 2001. Т 3№ 4 С 1-5



















































































