Первый опыт оценки регионарных показателей вегетативной нервной регуляции и кровообращения мочевого пузыря пациентов после локального введения ботулинического токсина (Лантокс)
 8155
8155 Инъекции ботулинического токсина (БТ) все шире применяются в урологии для лечения гиперактивного мочевого пузыря (ГАМП), тем не менее, дозы, пути введения и эффективность лечения все еще недостаточно выяснены [1, 2]. Клинические эффекты БТ, ограничивающего высвобождение ацетилхолина в парасимпатических синапсах, связывают с изменениями регуляции ГАМП, осуществляемой центральной и автономной нервной системой [2, 3]. Оценка эффективности лечения производится на основании опросников, а также объективных ультразвуковых и уродинамиче- ских исследований, позволяющих оценить анатомию и уродинамику мочевых путей [1]. Для исследования нервной регуляции мочевого пузыря требуется специальное неврологическое обследование пациента, включающее оценку урогенитальных рефлексов [4]. О вегетативной регуляции ГАМП судят по состоянию рецепторов симпатической и парасимпатической нервной системы и нейропептидов [5-7].
В настоящей работе мы попытались оценить состояние регионарной
активности вегетативной нервной системы у пациентов с ГАМП, получавших лечение БТ, используя новый метод гармонического анализа микровариаций биоимпеданса, апробированный в экспериментах на животных [8-10].
МАТЕРИАЛ И МЕТОДЫ
Неинвазивные исследования методом гармонического анализа биоимпеданса (ГАБ) мочевого пузыря выполнены у 5 пациентов непосредственно перед введением БТ в мочевой пузырь и/или сфинктер мочевого пузыря, а также на 1 - 4 день после процедуры.
Регистрацию биоимпеданса осуществляли оригинальным аппаратно - программным комплексом, включающим малошумящий высокочувствительный импедансметр («Биола», Россия), посредством двух серебряных (Ag-AgCl) электродов. Электроды, покрытые смоченнымифизиологическим раствором салфетками, располагали на передней брюшной стенке в области проекции мочевого пузыря.
Количественную оценку регионарной гемодинамической и нейрогенной активности производили по специальной программе с использованием быстрого Фурье-преобразова- ния. Оценивали ритмичную (РА) и асинхронную (АА) активность мочевого пузыря (рис. 1).
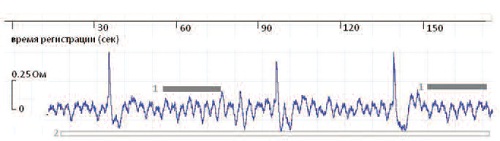 |
| Рис.1. Пример записи переменного компонента биоимпеданса мочевого пузыря у пациента К. в реальном времени. 1- участок записи, включающий ритмические и асинхронные вариации импеданса (RMS), 2- участки ритмичной активности (РА). |
Для этого на записях переменного импеданса автоматически вычисляли эффективное сопротивление (среднеквадратичное значение микровариаций биоимпеданса) для всей записи, включающей как ритмические, так и асинхронные изменения импеданса (RMS, рис. 1. 1), а также для участков суммарной ритмической активности - РА (рис.1. 2). Для вычленения асинхронной активности (АА) применяли формулу:
AA=√RMS – PA2
Спектр микровариаций биоимпеданса, получаемый быстрым Фурье-преобразованием участков записей, соответствующих РА (12.8-25.6 сек), анализировали в диапазоне частот 0.05 - 15.0 Гц. Показателями регионарной нейрогенной активности служили спектральные параметры: пик Майера на частоте очень низких частот (0.1 Гц) и респираторный пик на частоте 0.3 - 0.7 Гц (R). Сердечный пик (С1), регистрируемый на частоте сердцебиений 0.8 - 1.5 Гц, и его гармоники (С2 - С7) служили показателями кровообращения и регионарной сосудодвигательной активности, на основании которых рассчитывали полную пульсовую активность (ППА):
ППА=√(С1)2+(С2)2+(С3)2+(Сn)2
Все показатели выражали в единицах эффективного сопротивления - Омах.
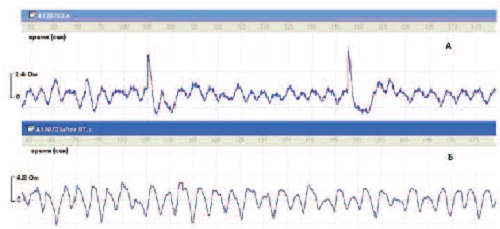 |
| Рис.2. Примеры записей переменного компонента биоимпеданса мочевого пузыря у пациентки К. перед введением БТ (А) и на третий день после инъекций (Б). |
РЕЗУЛЬТАТЫ
На записях импеданса мочевого пузыря, полученных высокочувствительным импедансметром, можно различить всплески двигательной активности, следующие с разной частотой и амплитудой, а также малые вариации биоимпеданса, отражающие стационарную активность в связи с пульсовыми колебаниями артериального давления и микровариациями нейрогенного генеза. Например, у пациентки К. регистрация импеданса мочевого пузыря перед лечением (рис. 2, А) выявила выраженные колебания импеданса (в) с частотой приблизительно 1 раз в минуту, наблюдавшиеся на фоне малых регулярных колебаний. Всплески двигательной активности, вероятно, соответствовали непроизвольным сокращениям детрузора, что может быть характерным признаком гиперактивности мочевого пузыря. После локального введения БТ эти сокращения исчезли (рис.2, Б). В обоих случаях записи произведены при умеренном наполнении мочевого пузыря до появления позывов к мочеиспусканию. Такой результат может указывать на угнетение сократительной активности мышцы мочевого пузыря в результате действия БТ.
Фрагменты стационарной записи колебаний биоимпеданса автоматически обрабатывались быстрым Фурье-преобразованием для получения амплитудных спектров (рис.3). Спектры микровариаций биоимпеданса, зарегистрированные с передней брюшной стенки в проекции умеренно наполненного мочевого пузыря, были аналогичны спектрограммам, полученным прямым наложением регистрирующих электродов на стенку мочевого пузыря у экспериментальных животных. Схожесть записей биоимпеданса мочевого пузыря и их спектрограмм у пациентов с таковыми у экспериментальных животных, позволила провести аналогию в трактовке физиологической значимости спектральных параметров с результатами наших экспериментальных исследований [8-10] для объяснения особенностей регуляции мочевого пузыря у человека. Гармонический анализ микровариаций биоимпеданса мочевого пузыря позволяет выявить ритмичности, отражающие регуляторные процессы, происходящие в организме с постоянной частотой, а именно, сердечно-сосудистую, дыхательную и нейрогенную ритмичность.
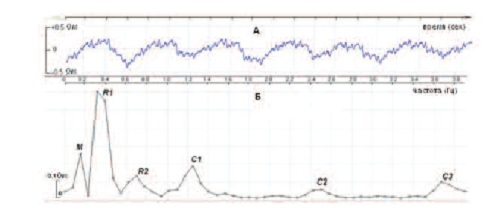 |
| Рис. 3. Пример записи колебаний биоимпеданса мочевого пузыря человека в реальном времени (А) и спектрограмма (Б), полученная быстрым Фурье преобразованием этой короткой записи. М- пик Майера, R1 и R2- гармоники респираторного пика, С1, С2, С3 - гармоники кардиального (сердечного) пика. |
На спектрограмме мочевого пузыря ритмичная активность проявляется пиками, соответственно, сердечным (С1), респираторным (R1) и их гармониками (C2, C3; R2), а также пиком Майера (М) на очень низкой частоте (0.1 Гц). Согласно нашим предыдущим иследованиям, пик С1 характеризует кровообращение в органе, пик R1 отражает активность парасимпатического, а пик М - симпатического отделов автономной нервной системы.
Обзорные спектры биоимпеданса мочевого пузыря для анализа низкочастотных колебаний на частотах волны Майера (М) и дыхания (R) выполнены с частотным разрешением 0.04 Гц (получены анализом фрагментов записи переменного импеданса длительностью 25.6 сек, включающие 4096 точек). На рис.4 представлены примеры спектрограмм, зарегистрированных у пациентки С. до (А) и на 4-й день после (Б) локальных инъекций БТ. Выявленная высокая регионарная активность парасимпатического отдела вегетативной нервной системы, которая проявлялась выраженными респираторными гармониками, существенно превышающими пик Майера (М), снизилась после лечения БТ. Учитывая, что парасимпатическим влияниям приписывается существенная роль в формировании гиперактивности детрузора, приведенный пример объективно демонстрирует угнетение регионарной парасимпатической активности после лечения БТ, что можно расценить как ожидаемый положительный эффект терапии.
Снижение регионарной парасимпатической активности после локального введения БТ было зарегистрировано у 3 из 5 пациентов. У них вырос показатель М/R с 0.12 до 0.42, указывая на сдвиг регионарного симпато-парасимпатического баланса в пользу повышения симпатических влияний.
У остальных 2 пациентов симпатопарасимпатический баланс изменился в пользу парасимпатического компонента - показатель М/R снизился с 0.50 до 0.16. Усиление регионарной парасимпатической активности у этих пациентов происходило на фоне увеличения общей ритмической (РА) и сосудодвигательной (ППА) активности, которые возрастали в 3.3. раза. Для сравнения, у пациентов с уменьшением парасимпатического компонента эти показатели выросли в 1.5 и 2.0 раза, соответственно. Усиление нейрогенной РА (увеличение пиков М, R) можно объяснить регионарной реакцией на денервацию мочевого пузыря в результате действия БТ.
Другой эффект БТ, выявленный у всех обследованных пациентов методом гармонического анализа микровариаций биоимпеданса, состоял в изменении спектральных параметров на частоте сердечнососудистой активности, характеризующих состояние кровообращения и регионарную вазоактивность.
Для анализа колебаний биоимпеданса на частоте работы сердца и сердечных гармоник обрабатывали участки записи, соответствующие РА, длительностью 12.8 сек (2048 точек) с разрешением 0.08 Гц (рис.5).
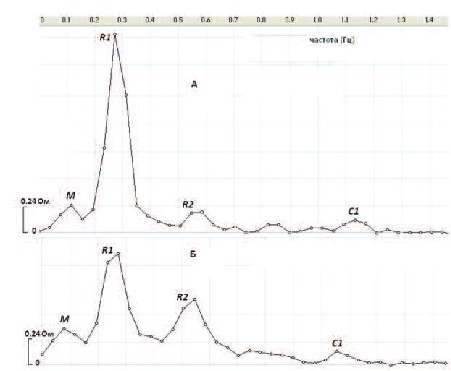 |
| Рис.4. Спектрограммы биоимпеданса мочевого пузыря, демонстрирующие изменения фундаментальных гармоник, отражающих регионарную нейрогенную активность (М и R1) у пациентки С. перед(А) и после (Б) локального введения БТ. |
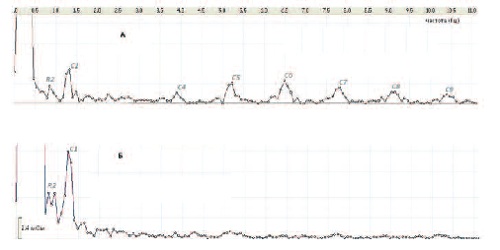 |
| Рис.5. Спектрограммы импеданса мочевого пузыря демонстрирующие изменения сердечного пика (С1) и его гармоник (С4-С9) у пациентки К. перед (А) и после (Б) локального введения БТ. |
Так, до лечения у пациентов наблюдали высокие ближние резонансы (С5-С7), сопоставимые или даже превышающие С1. Следует отметить, что для нормального мочевого пузыря здоровых людей характерно равномерное убывание амплитуды следующих за фундаментальным пиком гармоник (С1>С2>С3>С4>С5>С6>С7). После локального введения БТ зарегистрирован рост первого пика на частоте сердечной активности (С1), а остальные гармоники существенно снизились или пропали (рис.5, Б). Такие результаты свидетельствуют об улучшении регионарного кровообращения после действия БТ и о снижении сосудистого тонуса. Это объясняется тем, что пульсовые гармоники C2, C3 и C..., амплитуды которых выше основной пульсовой гармоники C1, представляют собой резонансы, обусловленные усилением тонуса артерий разного калибра и, соответственно, увеличением жесткости их стенки, что сопровождается увеличением добротности колебательной структуры и увеличением спектральных пиков (рис. 5, А).
После локального действия БТ увеличение С1 может быть показателем улучшенного кровоснабжения мочевого пузыря, а уменьшение и исчезновение резонансных гармоник указывает на повышение эластичности артериального русла. Лишь у одного из обследованных пациентов имело место усиление как фундаментального сердечного пика (С1), так и последующих его гармоник, что может свидетельствовать об органических (атеросклеротических) изменениях сосудистого русла мочевого пузыря у этого пациента.
В среднем непосредственный эффект введения БТ в детрузор и сфинктер состоял в усилении регионарной нейрогенной и сосудистой активности мочевого пузыря у обследованных пациентов (табл. 1). По данным метода гармонического анализа микровариаций биоимпеданса ритмичная активность (РА) мочевого пузыря в течение 1-го дня после локального действия БТ усилилась (+133%) значительно больше, чем асинхронная активность (АА, +20%). Усиление нейрогенной активности происходило как за счет симпатической (пик Майера возрастал на 88%), так и парасимпатической (R-пик увеличивался на 75%) активности, по сравнению с начальным, до введения токсина, уровнем. Полная пульсовая активность (ППА) увеличивалась в 3,3 раза, по сравнению со значением до лечения, а фундаментальная сердечная гармоника (С1) возрастала в 4 раза.
Изменение этих показателей, а также указанное ранее снижение резонансных гармоник у большинства обследованных пациентов свидетельствует об улучшении кровообращения в мочевом пузыре после введения БТ, а отмеченное ранее снижение резонансных гармоник у 4 из 5 обследованных пациентов может быть связано с улучшением эластичных свойств сосудистого русла.
Зарегистрированные изменения являются начальными, вероятно характеризующими переходные процессы, происходящие в мочевом пузыре. Так, у пациентки С., обследованной на 1-е затем на 4-е сутки после локального введения БТ выявлены изменения исследуемых параметров, произошедшие даже за этот короткий срок, но свидетельствующие о положительной динамике лечения. Как демонстрируют результаты, представленные в табл.2 первоначальный эффект инъекций БТ вызвал усиление ритмической (РА), парасимпатической (R) и сосудистой (ППА, С1) активности. В последующем (на 4-е сутки) зарегистрированы изменения, ожидаемые после химической денервации мочевого пузыря в результате действия токсина, целью которой, собственно, и является угнетение регионарной парасимпатической активности (R). Показатель регионарного симпато - парасимпатического баланса возрос с 0.16 (исходный) и 0.13 (на 1-е сутки) до 0.48 (на 4-е сутки), т.е. сместился в пользу регионарной симпатической активности. Следовательно, уменьшение нейрогенной ритмичной активности произошло за счет парасимпатического компонента (R), без изменений симпатического (М), а показатель ППА указывал на хорошее состояние регионарного кровообращения. Кроме того, у этой пациентки исчезли резонансные гармоники С3- С6, которые регистрировались перед лечением, свидетельствуя о снижении ригидности сосудистого русла.
Таблица 1. Показатели нейрогенной и сосудистой активности мочевого пузыря, полученные методом гармонического анализа микровариаций биоимпеданса у 5 пациентов с ГАМП на 1-4 сутки после локального введения БТ (Лантокс)
| Время регистрации | Исследуемые параметры | |||||
| Исходные |
PA |
M |
R |
ППА |
C1 |
AA |
| 253.0 ± 122.1 | 28.9 ± 7.5 | 238.8 ± 125.2 | 16.6 ± 4.4 | 50.8 ± 17.4 | 382.4 ± 207.6 | |
| После БТ | 589.3 ± 271.2 | 54.6 ± 20.4 | 384.0± 173.0 |
55.2 ± 20.7 | 204.0 ± 85.2 | 457.6 ± 168.2 |
Таблица 2. Динамика показатели нейрогенной и сосудистой активности мочевого пузыря у пациентки С. через 1-4 сутки после локального введения БТ
| Время регистрации |
Исследуемые параметры | ||||
| PA |
M |
R |
ППА |
C1 | |
| Исходные | 219.1 | 36.0 | 217.7 | 16.0 | 48.0 |
| 1-й день после БТ % изменения |
252.0 +15% |
30.7 -15% |
236.5 +9% |
22.3 +39% |
+71% |
| 4-й день после БТ % изменения |
105.6 -45% |
36.5 +2% |
76.3 -60% |
19.3 +15% |
39.0 +15% |
В заключение следует отметить, что не у всех обследованных пациентов зарегистрированы схожие и ожидаемые изменения параметров функциональной регуляции после инъекций БТ. Это объясняется неясной природой исходных различий исследуемых показателей, т.к. патогенез ГАМП включает миогенные, нейрогенные и уретелиогенные факторы [3], роль и степень выраженности которых может быть разной. Используемый нами метод гармонического анализа микровариаций биоимпеданса основан на регистрации и количественной оценке биоэлектрической активности мочевого пузыря. Известно, что общим свойством органов мочевого тракта, мочевого пузыря и мочеиспускательного канала включительно, является способность к ритмичной электрической и механической активности, происходящей от самопроизвольно возбуждающихся клеток (ICC), а координирующая роль нервной системы в пейсмейкерной активности этих клеток призвана обеспечивать полноценность механизма удержания и эвакуации мочи [11]. Несмотря на объективные гистологические и электрофизиологические доказательства биоэлектрических свойств урогенитального тракта, в клинической практике до настоящего времени не существует метода, позволяющего в динамике in situ наблюдать изменения функциональной регуляции отдельных органов. Проведенные исследования продемонстрировали возможность объективно и неинвазивно оценивать индивидуальные особенности нейрогенной активности мочевого пузыря и состояние регионарного кровообращения в процессе лечения.
Литература
- Wen Ji Li, Seung-June Oh. Management of Lower Urinary Tract Dysfunction in Patients with Neurological Disorders. // Korean J Urol. 2012. V. 53. P. 583-592.
- Apostolidis A, Dasgupta P, Denys P, Elneil S, Fowler CJ, Giannantoni A, Karsenty G, Schulte-Baukloh H, Schurch B, Wyndael J-J. Recommendations on the Use of Botulinum Toxin in the Treatment of Lower Urinary Tract Disorders and Pelvic Floor Dysfunctions: A European Consensus Report. // Eur Urol. 2009. Vol. 55. N 1, P. 100-120.
- Meng En, Lin Wei-Yu, Lee Wei-Chia, Chuang Yao-Chi. Pathophysiology of Overactive Bladder LUTS: Lower Urinary Tract Symptoms. // Special Issue: Recent Advances in the Understanding of LUTS. 2012. Vol. 4, Suppl. s1. P. 48-55.
- Коган М И. Нейрофизиологическая оценка пациентов с хроническим простатитом (синдром хронической тазовой боли). // Урология. 2012. № 4. С. 37-42.
- Apostolidis A, Popat R, Yiangou Y, Cockayne D, Ford AP DW, Davis JB, Dasgupta P, Fowler CJ, Anand P. Decreased Sensory Receptors P2X3 and TRPV1 in suburotelial nerve fibers following intradetrusor injections of Botulinum toxin for human detrusor overactivity. // J Urol. 2005. Vol. 174, N 3. P. 977-983.
- Chancellor MB, Fowler CJ, Apostolidis A, de Groat WC, Smith C P, Somo- gyi GT, Aoki KR. Drug Insight: biological effects of botulinum toxin A in the lower urinary tract. // Nat Clin Pract Urol. 2008. Vol. 5, N 6. P. 319-328.
- Ochodnicky P, Uvelius B, Andersson K-E, Michel M C. Autonomic nervous control of the urinary bladder. // Acta Physiologica. 2012. Vol. 206, N 3. Accepted Article.
- Мудрая И.С., Ибрагимов А.Р., Кирпатовский В.И., Ревенко С.В., Несторов А.В., Гаврилов И.Ю. Оценка функционального состояния мочевого пузыря крыс методов Фурье-импедансной цистометрии. // Экспер и клинич урология. 2010. № 3. С. 21-27.
- Mudraya IS, Revenko SV, Nesterov AV, Gavrilov IY, Kirpatovsky VI. Bioimpedance harmonic analysis as a tool to simultaneously assess circulation and nervous control. // Physiol Meas. 2011, Vol. 32, N 7. С. 959-976.
- Кирпатовский В.И., Мудрая И.С., Ревенко С.В., Нестеров А.В., Гаврилов И.Ю., Хромов Р.А., Баблумян А.Ю. Оценка интрамурального кровотока и нейрогенной регуляции в интактном и гипертрофированном мочевом пузыре крыс с помощью гармонического анализа биоимпеданса. // Бюлл. экспер. биол. мед. 2012, Т. 153, № 4. С. 422-427.
- McHale NG, Hollywood MA , Sergeant GP, Shafei M, Thornbury KT, Ward SM. Organization and function of ICC in the urinary tract. // J. Physiol. 2006. Vol. 576. N. 3, P. 689-694.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью в pdf формате | 280.06 кб |















































































