ВВЕДЕНИЕ
Новообразования яичка (НЯ) наиболее часто встречается у лиц молодого возраста [1]. Это заболевание возникает в пиковый период репродуктивной жизни, в ключевой период для карьеры и семейной жизни.
Подход к активному лечению у этих пациентов начинается с орхифуникулэктомии (ОФЭ), что позволяет удалить первичную опухоль и получить гистологическую верификацию заболевания. Приблизительно 50% больных в дальнейшем нуждаются в дополнительной лучевой терапии (ЛТ) или полихимиотерапии (ПХТ) при диссеминированном заболевании [2]. По данным литературы, эти методы лечения увеличивают риск дефицита тестостерона (ДТ) [3-6]. Однако другие авторы подчеркивают, что риск ДТ у этих пациентов не зависит от лечения, а связан с тестикулярным микролитиазом и тестикулярной атрофией, которые присутствуют у таких пациентов еще до лечения [3, 7]
В настоящее время мало что известно об уровне половых гормонов в сыворотке крови у мужчин с НЯ до лечения. В работах, посвященных этому вопросу, указывается, что концентрации этих гормонов в сыворотке крови аналогичны таковым у здоровых людей [8]. Другие исследователи считают, что при использовании комбинированной оценки лютенизирующего гормона (ЛГ) и общего тестостерона (Т) более чем у 25% пациентов с НЯ отмечаются изменения в гипоталамо-гипофизарноонадной оси (ГГГО) [9]. Это состояние характеризуется повышенным уровнем ЛГ, в то время уровень Т либо нормальный, либо сниженный.
Таким образом, необходимы дополнительные исследования для оценки ГГГО у мужчин новообразованием в яичке.
Цель исследования. Оценить степень гормональных нарушений, влияющих на ГГГО у мужчин с НЯ до лечения.
МАТЕРИАЛЫ И МЕТОДЫ
Характеристика пациентов
За период с декабря 2021 по март 2023 г. на базе МНИОИ им. П.А. Герцена – филиала НМИЦ радиологии в отделении урологии обратились 49 мужчин с НЯ. Пациенты были обследованы по стандартной методике (компьютерная томография органов грудной клетки, брюшной полости и забрюшинного пространства с внутривенным контрастированием, магнитнорезонансная томография/ультразвуковое исследование (МРТ/УЗИ) органов мошонки, определение уровня онкомаркеров – альфа-фетопротеина (АФП), бета-хорионического гонадотропина (β-ХГЧ), лактатдегидрогеназы (ЛДГ). После обследования и при подозрении на злокачественное новообразование всем пациентам была выполнена орхифуникулэктомия для гистологической верификации опухоли и определения дальнейшей тактики лечения.
В качестве факторов, влияющих на гормональный статус пациентов до хирургического лечения, мы оценивали такие параметры как: возраст, степень ожирения, курение, объем яичек, размер опухолевого образования, отягощенный онкологический семейный анамнез, наличие хирургического вмешательства в анамнезе по поводу крипторхизма, микролитиаз яичек и уровень β-ХГЧ. При этом размер опухоли, объем и наличие микролитиаза яичек определяли по результатам методов лучевой диагностики (МРТ/УЗИ).
Гормональный анализ
Забор крови для определения уровня гонадотропных (ЛГ, ФСГ, ПРЛ) и стероидных гормонов (общий тестостерона, эстрадиол), а также глобулин-связывающих половых гормонов (ГСПГ) производился натощак между 8 и 10 часами утра. Анализ уровня гормонов в сыворотке выполнена на оборудовании Beckman Coulter UniCel DxI 800, Immulite 2000XPi.
Пороговым значением, позволяющим разграничить нормальное состояние и потенциальный ДТ, считали уровень 8 нмоль/л для общего тестостерона (Т) сыворотки крови. При уровне общего Т от 8 до 12 нмоль/л учитывали уровень ГСПГ с дальнейшим расчетом уровня свободного Т по формуле (описанной в работе A. Vermeulen и соавт), нижняя граница нормы которого принята <243 пмоль/л [10].
Для дифференциации первичной и вторичной форм гипогонадизма, а также выявления субклинического гипогонадизма определяли уровень гонадотропных гормонов (ЛГ, ФСГ, пролактин) в сыворотке крови.
Так как повышенный уровень хорионического гонадотропина человека для мужчин (β-ХГЧ) можно наблюдать при НЯ [11], а данный гормон оказывает значительное влияние на гормональный уровень пациента, то по этой причине мы разделили пациентов на две группы: 1 группа – с высоким уровнем β-ХГЧ (n=19); 2 группа – с нормальным уровнем β-ХГЧ (n=30).
Методы статической обработки данных
Статистический анализ проводился с использованием пакета программы IBM SPSS v.27 и StatTech v. 3.1.6 (разработчик – ООО «Статтех», Россия).
Количественные показатели, имеющие нормальное распределение, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95% доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1 – Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей.
Сравнение двух групп по количественному показателю, имеющему нормальное распределение, при неравных дисперсиях выполнялось с помощью t-критерия Уэлча. Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с помощью U-критерия Манна-Уитни.
Направление и теснота корреляционной связи между двумя количественными показателями оценивались с помощью коэффициента ранговой корреляции Спирмена (при распределении показателей, отличном от нормального).
Статистически значимыми различия считали при уровне p≤0,05.
РЕЗУЛЬТАТЫ
Клиническая характеристика обследуемых пациентов представлена в таблице 1. Среди всей наблюдаемой когорты мужчин большая часть пациентов (81,6%), была молодого возраста, остальные были лица среднего возраста. Повышенный индекс массы тела был лишь у 6 (12,2%) мужчин. Операции в области мошонки в анамнезе имелись у 11 (22,4%) человек. Большая часть пациентов имели вредную привычку – табакокурение (32; 65,3%).
Таблица 1. Клиническая характеристика пациентов с НЯ (n=49)
Table 1. Clinical characteristics of patients with testicular tumors (n=49)
| Показатели Indicators |
M ± SD / Me | 95% ДИ / Q₁ – Q₃ |
|---|---|---|
| Возраст, (лет)/Age (years) | 34 ± 10 | 32 – 37 |
| Вес, (кг)/Weight (kg) | 83 ± 18 | 78 – 88 |
| Рост, (см)/Height (cm) | 180 ± 7 | 178 – 182 |
| Размер опухоли, (см)/Tumor size (cm) | 3,88 ± 2,07 | 3,28 – 4,47 |
| Объем пораженного яичка, (см3) Affected testicle volume (cm3) | 31,80±11,9 | 20,10 – 62,40 |
| Объем здорового ячика, (см3) Healthy testicle volume (cm3) | 16,10±2,4 | 12,35 – 19,25 |
| Общий объем яичек, (см3) Total testicular volume (cm3) | 49,95±9,6 | 31,62 – 77,17 |
По данным лабораторных исследований, до лечения уровень β-ХГЧ был высоким у 19 (38,8%) пациентов, и у 30 (61,2%) пациентов с НЯ он был в пределах референсных значений. Лабораторные признаки дефицита тестостерона (ДТ) наблюдали у 15 (30,6%) из 49 пациентов, что 86,7% случаев приходиться на долю пациентов без повышенного уровня β-ХГЧ.
Гонадотропные гормоны: ЛГ, ФСГ, пролактин
Концентрация ЛГ в крови была ниже границы нормы у 18 (36,7%), в пределах референсных значений у 23 (46,9%) и выше границы нормы у 8 (16,3%) пациентов с НЯ (рис. 1).
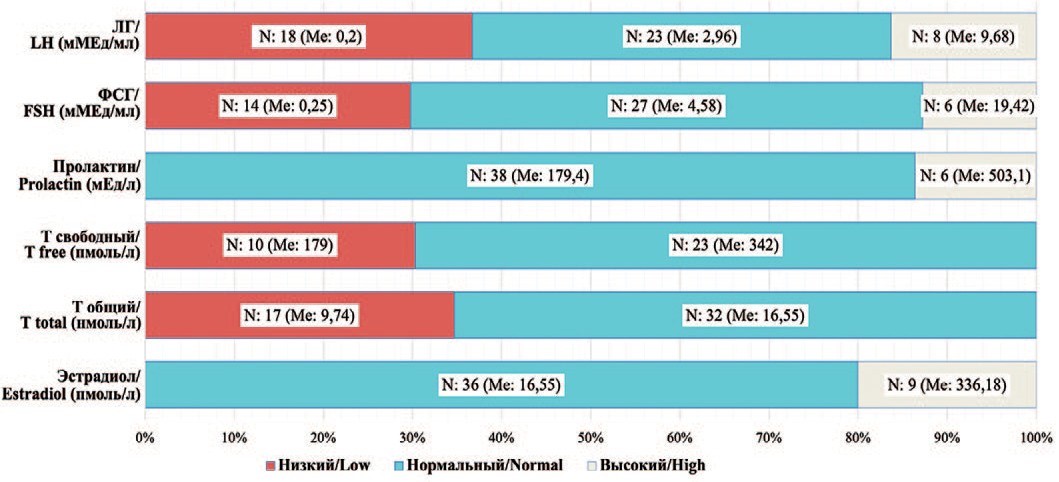
Рис. 1. Распределение пациентов с новообразованием яичка в зависимости от уровней гормонов.
Fig. 1. Distribution of patients with testicular tumors depending on hormone levels.
Были установлены существенные различия при сопоставлении уровня ЛГ в зависимости от уровня β- ХГЧ (p<0,001) и наличие крипторхизма (p=0,023). Выявленные различия объясняются более низким уровнем ЛГ у пациентов с высокими уровнями β-ХГЧ по сравнению с пациентами с отрицательными уровнем данного онкомаркера (рис. 2). Напротив, высокий уровень ЛГ наблюдался у пациентов с наличием крипторхизмом в анамнезе.
Концентрация ЛГ в крови была ниже границы нормы у 18 (36,7%), в пределах референсных значений у 23 (46,9%) и выше границы нормы у 8 (16,3%) пациентов с НЯ (рис. 1).
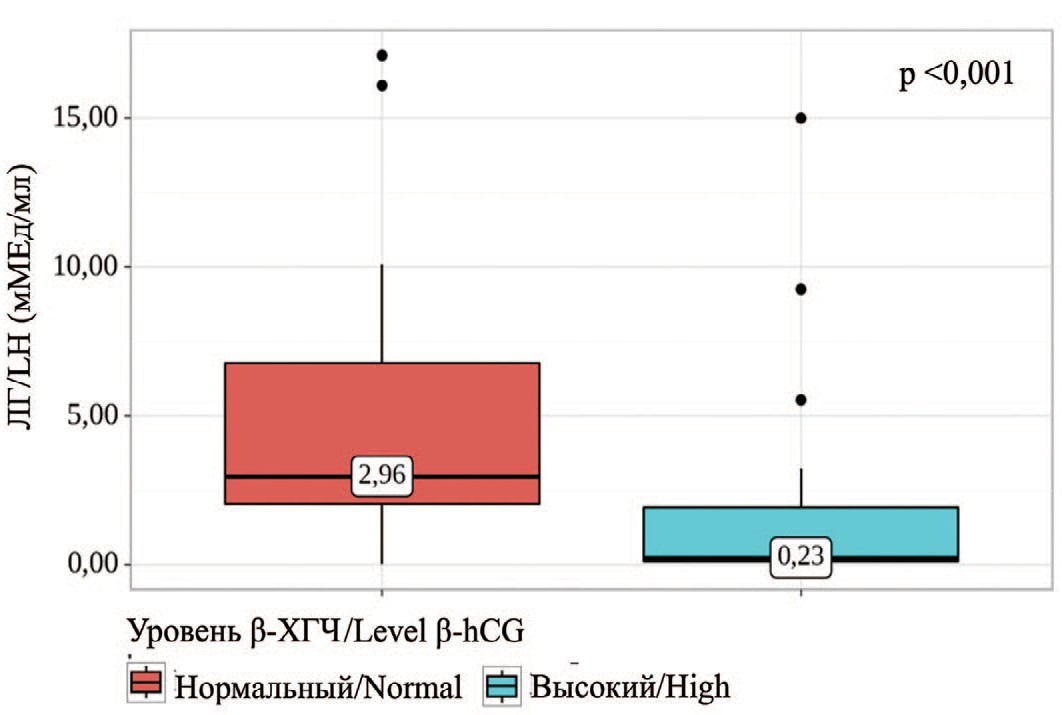
Рис. 2. Сравнение значений ЛГ в зависимости от уровня β-ХГЧ
Fig. 2. Comparison of LH values depending on β-hCG levels
Концентрация ФСГ в крови была низкой у 14 (28,6%), нормальной у 29 (59,2%) и повышенной у 6 (12,2%) пациентов с НЯ (рис. 1).
При анализе уровня ФСГ в зависимости от β-ХГЧ и наличия крипторхизма, также были выявлены существенные различия (p<0,001). Высокий уровень β-ХГЧ был сопряжен со снижением уровня ФСГ в крови (рис. 3). Напротив, наличие крипторхизма в анамнезе сопровождалось повышением уровня данного гонадотропного гормона в крови.
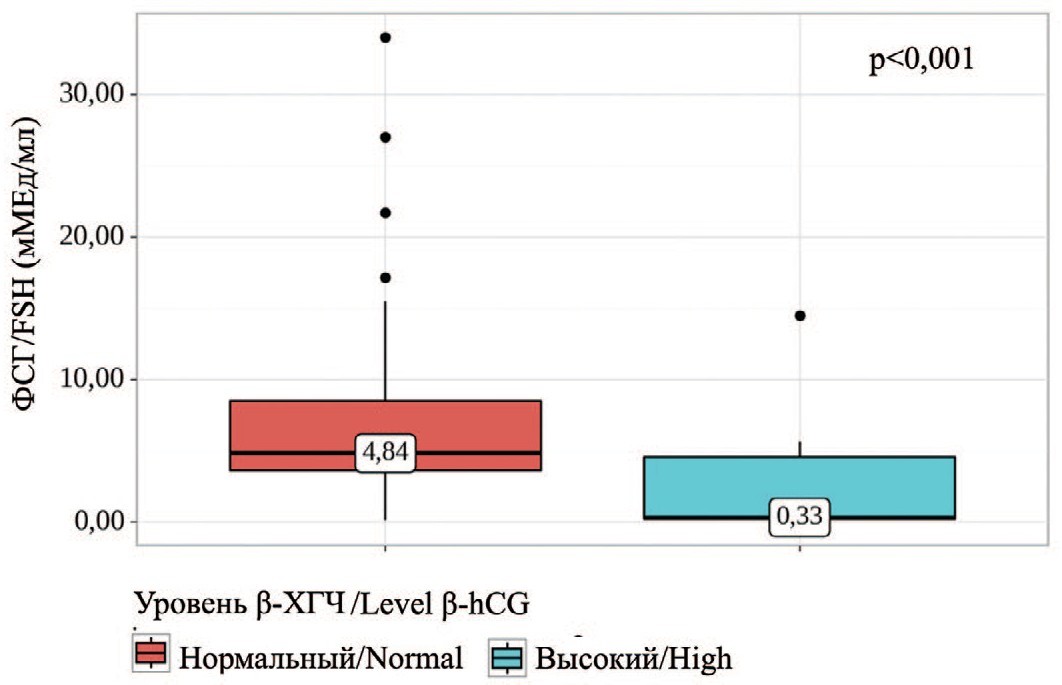
Рис. 3. Сравнение значений ФСГ в зависимости от уровня β-ХГЧ
Fig. 3. Comparison of FSH values depending on β-hCG levels
Уровень пролактина был высоким у 6 (12,2%), нормальным – у 43 (87,8%) пациентов. Однако причинно-следственная связь установлена не была.
При корреляционном анализе выявлена связь между уровнем ЛГ (p=-0,351; p=0,014), ФСГ (p=-0,3; p=0,041) и размер опухолевого образования. При анализе зависимости уровня гонадотропных гормонов от возрастной группы, курения и ожирения статические значимые различия получены не были (p>0,05).
Стероидные гормоны: общий тестостерон, свободный тестостерон, эстрадиол
Концентрация общего Т ниже 8 нмоль/л обнаружена у 3 (6,1%) пациентов. Значения тестостерона от 8-12 нмоль/л выявлены у 14 (28,6%) пациентов. Значения тестостерона выше 12,1 нмоль/л (>3,46 нг/мл) зарегистрированы у 32 (65,3%) пациентов.
Уровень свободного Т ниже 243 пмоль/л отмечался у 10 (30,3%), в пределах референсных значений – у 23 (69,7%) пациеннтов.
Уровень эстрадиола был высоким у 9 (20%), нормальным у 36 (80%) пациентов.
Согласно полученным данным, при сопоставлении уровня общего Т, свободного Т и эстрадиола (E2) с бета-ХГЧ нам удалось установить статистически значимые различия (p=0,019, p=0,01; p=0,003) (рис. 4-6). Данное различие было обусловлено наиболее высокой концентрацией половых гормонов в крови у пациентов с уровнем β-ХГЧ выше референсного значения.
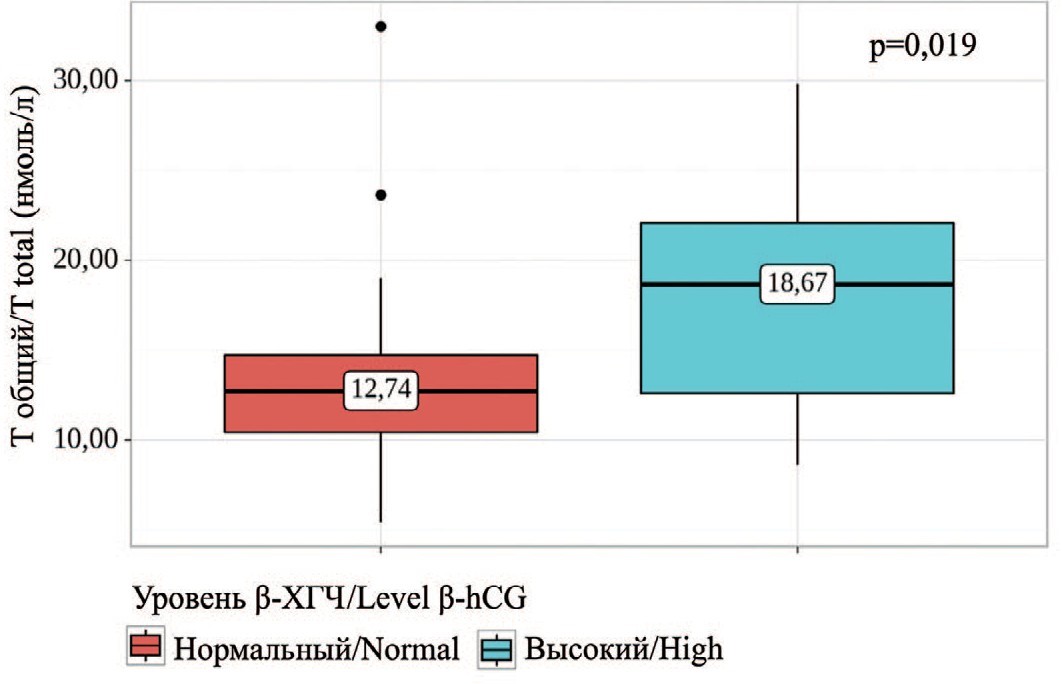
Рис. 4. Сравнение значений общего тестостерона в зависимости от уровня β-ХГЧ
Fig. 4. Comparison of total testosterone values depending on β-hCG levels
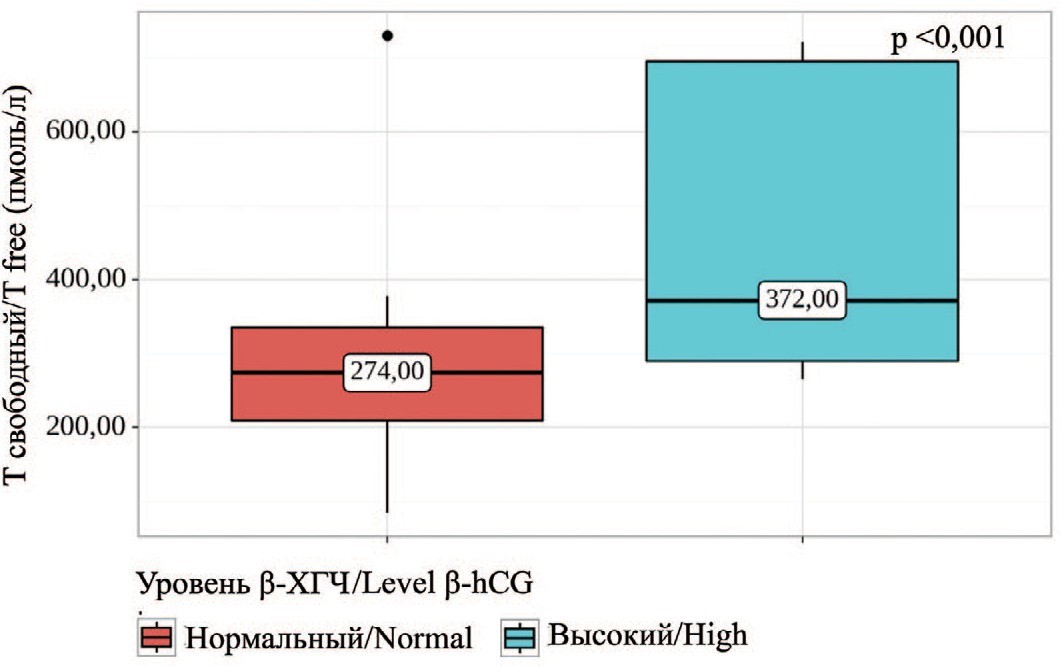
Рис. 5. Сравнение значений свободного тестостерона в зависимости от уровня β-ХГЧ
Fig. 5. Comparison of free testosterone values depending on β-hCG levels
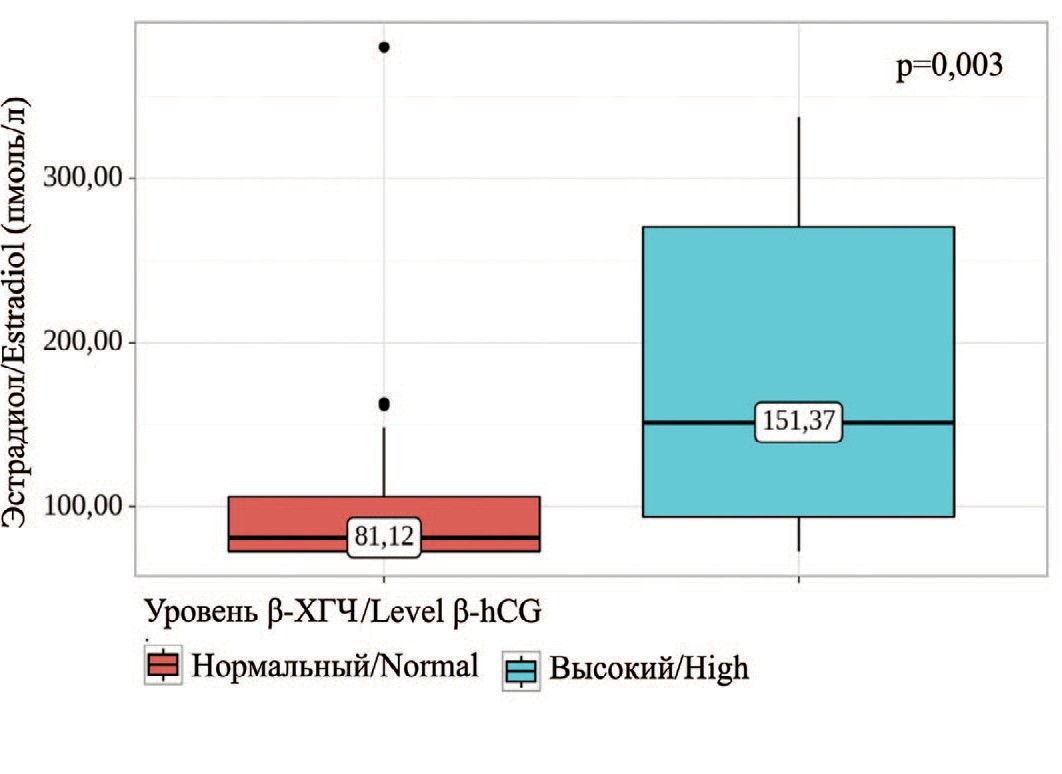
Рис. 6. Сравнение значений эстрадиола в зависимости от уровня β-ХГЧ
Fig. 6. Comparison of estradiol values depending on β-hCG levels
Также при анализе общего Т, свободного Т и Е2 в зависимости от наличия орхипексии в анамнезе, были установлены статистически значимые различия (p=0,016, p=0,022, p=0,034 соответственно).
При оценке связи размера опухоли и Е2 была установлена умеренная прямая связь.
При анализе зависимости уровня стероидных гормонов от возраста пациентов, употребления ими табачных изделий, лишней массы тела статические значимые различия не были получены (p>0,05).
ОБСУЖДЕНИЕ
В настоящее время важными целями при НЯ являются минимизация последствий самого заболевания и его лечения для улучшения качества жизни (КЖ) пациента в долгосрочной перспективе. Одним из наиболее важных аспектов КЖ у молодых мужчин, пролеченных по поводу НЯ, является сохранение функции яичек (сперматогенез/стероидогенез).
В течение многих десятилетий наибольшее внимание уделялось нарушению фертильности у пациентов с НЯ, разработаны меры профилактики [12, 13]. В последнее время появляется все больше данных, свидетельствующих о том, что у этой группы пациентов также повышен риск развития гипогонадизма, связанного с лечением [14, 15]. В то же время на сегодняшний день не существует научно обоснованных рекомендаций для практикующих врачей по скринингу гипогонадизма у пациентов с НЯ [16].
По мнению других специалистов, развитие гипогонадизма у этих пациентов не зависит от методов лечения, а связано с тестикулярным микролитиазом и тестикулярной атрофией, которые присутствуют у пациентов еще до начала лечения [17, 18].
В многочисленных исследованиях изучали гормональный фон у мужчин с НЯ до лечения, и лишь немногие из них касались факторов риска, приводящих к гипогонадизму.
P.J. Wiechno и соавт. проанализировали уровень общего Т у 62 пациентов до ОФЭ и у 120 пациентов через 1 месяц после ОФЭ. Пороговым значением для ДТ считался уровень общего Т ниже 8 нмоль/л. Авторы пришли к выводу о том, что 5% пациентов имели ДТ до ОФЭ по сравнению с 16% пациентов через месяц после ОФЭ [19]. Это свидетельствует о том, что у пациентов с НЯ до начала активного лечения уже имеется нарушения гормонального статуса.
P.M. Petersen и соавт. оценили качество спермы и репродуктивные гормоны (ЛГ, ФСГ, тестостерон, эстрадиол, ГСПГ) у 83 мужчин с НЯ перед ОФЭ. ДТ определялся как уровень ЛГ выше 10 МЕ/л и/или уровень общего Т ниже 10 нмоль/л. Проанализировав результаты, специалисты не наблюдали нарушения функции клеток Лейдига у этих пациентов. С другой стороны, авторы почеркнули, что из-за высокого уровня β-ХГЧ, который в свою очередь стимулирует клетки Лейдига, сложно исключить такое нарушение [20].
В литературе есть указания на то, что ЛГ и β-ХГЧ являются морфологически сходными полипептидными гормонами, стимулирующими одни и те же рецепторы [7] Этот факт объясняет разрушающее действие высоких концентраций бета-ХГЧ на ГГГО. Другие исследователи также предполагают, что концентрация β-ХГЧ у больных раком яичка коррелирует с концентрацией тестостерона, пролактина, эстрадиола и гонадотропинов [21].
Учитывая данную закономерность, M. Bandak и соавт. оценили функцию клеток Лейдига до и после ОФЭ у пациентов с 1 стадии НЯ [8]. До ОФЭ не было значительных различий в уровнях ЛГ и Т между пациентами с нормальными уровнями β-ХГЧ и контрольной группой. Однако, при оценке соотношении ЛГ/Т более чем у 30% пациентов имеется дисфункция клеток Лейдига. Кроме того, пациенты с повышенным уровнем β-ХГЧ перед ОФЭ имели заметное нарушение гипофизарно-гонадной оси (ГГО) на исходном уровне с подавлением ЛГ, повышением T и E2 по сравнению с контрольной группой. Эти выводы согласуются с предположением P.M. Petersen и соавт. [19].
При дальнейшем изучении этой проблемы в другом своем исследовании M. Bandak и соавт. показали, что примерно у четверти пациентов с НЯ, у которых нормальный уровень бета-ХГЧ, дисфункция клеток Лейдига наблюдается уже до лечения. Также, была обнаружена значимая корреляционная связь между дисфункцией клеток Лейдига и размером опухоли, наличием неоплазии зародышевых клеток in situ и возрастом [9].
J. Eberhard и соавт. изучали факторы риска гипогонадизма у 143 пациентов с НЯ после лечения. Авторы подчеркивали, что у мужчин наличие микролитиаза яичка до лечения является сильным предиктором последующего гипогонадизма [3]. Однако в этих работах есть свои недостатки: небольшое количество пациентов, проблемы с измерением уровня тестостерона и различные методики в определении ДТ.
Анализ отечественных литературных источников показал, что в России до сих пор не проводились подобного рода наблюдения. Полученные нами результаты исследования демонстрируют, что у трети пациентов наблюдались лабораторные признаки ДТ, преимущественно у пациентов (в 87% случаев) с нормальным уровнем β-ХГЧ. У мужчин c высоким уровнем β-ХГЧ мы наблюдали изменение ГПГ с подавлением уровня гонадотропинов (ЛГ, ФСГ) и повышением общего/свободного T и эстрадиола, что согласуется с результатами исследования M. Bandak и соавт. [9] и P.M. Petersen и соавт. [19]. Однако, НЯ не позволяет однозначно оценить гонадную функцию исходно, что требует дальнейшего наблюдения за этой когортой пациентов с последующей повторной оценкой гормонального статуса после активного лечения и нормализации опухолевого маркера (β-ХГЧ).
ЗАКЛЮЧЕНИЕ
Таким образом, результаты проведенного нами исследования демонстрируют, что функция ГГГО нарушена у 30% пациентов с НЯ до лечения. У одной трети мужчин наблюдались лабораторные признаки ДТ. Требуется проведение дальнейших исследований с включением большего числа пациентов для выработки практических рекомендаций.
ЛИТЕРАТУРА
- Ghoreifi A, Djaladat H. Management of primary testicular tumor. Urol Clin North Am 2019;46(3):333-9. https://doi.org/10.1016/j.ucl.2019.04.006.
- Chovanec M, Cheng L. Advances in diagnosis and treatment of testicular cancer.
BMJ 2022;379:e070499. https://doi.org/10.1136/bmj-2022-070499.
- Eberhard J, Ståhl O, Cwikiel M, Cavallin-Ståhl E, Giwercman Y, Salmonson EC, et al. Risk factors for post-treatment hypogonadism in testicular cancer patients. Eur J Endocrinol 2008;158(4):561-70. https://doi.org/10.1530/EJE-07-0684.
- Huddart RA, Norman A, Moynihan C, Horwich A, Parker C, Nicholls E, Dearna- ley DP. Fertility, gonadal and sexual function in survivors of testicular cancer. Br J Cancer 2005;93(2):200-7. https://doi.org/10.1038/sj.bjc.6602677.
- Ondrusova M, Spanikova B, Sevcikova K, Ondrus D. Testosterone deficiency and bone metabolism damage in testicular cancer survivors. Am J Mens Health 2018;12(3):628-33. https://doi.org/10.1177/1557988316661986.
- La Vignera S, Cannarella R, Duca Y, Barbagallo F, Burgio G, Compagnone M, et al. Hypogonadism and sexual dysfunction in testicular tumor survivors: a systematic review. Front Endocrinol (Lausanne) 2019;10:264. https://doi.org/10.3389/fendo.2019.00264.
- Pühse G, Wachsmuth JU, Kemper S, Husstedt IW, Evers S, Kliesch S. Chronic pain has a negative impact on sexuality in testis cancer survivors. J Androl 2012;33(5):886-93. https://doi.org/10.2164/jandrol.110.012500.
- Bandak M, Aksglaede L, Juul A, Rørth M, Daugaard G. The pituitary-Leydig cell axis before and after orchiectomy in patients with stage I testicular cancer. Eur J Cancer 2011;47(17):2585-91. https://doi.org/10.1016/j.ejca.2011.05.026.
- Bandak M, Jørgensen N, Juul A, Lauritsen J, Gundgaard Kier MG, Mortensen MS, et al. Preorchiectomy Leydig cell dysfunction in patients with testicular cancer. Clin Genitourin Cancer 2017;15(1):e37-e43. https://doi.org/10.1016/j.clgc.2016.07.006.
- Vermeulen A, Verdonck L, Kaufman JM. A Critical Evaluation of Simple Methods for the Estimation of Free Testosterone in Serum. J Clin Endocrinol Metab 1999;84(10):3666-72. https://doi.org/10.1210/jcem.84.10.6079.
- Duffy MJ. Clinical uses of tumor markers: a critical review. Crit Rev Clin Lab Sci 2001;38(3):225-62. https://doi.org/10.1080/20014091084218.
- Djaladat H, Burner E, Parikh PM, Beroukhim Kay D, Hays K. The association between testis cancer and semen abnormalities before orchiectomy: a systematic re- view. J Adolesc Young Adult Oncol 2014;3(4):153-9. https://doi.org/10.1089/ jayao.2014.0012.
- Sineath RC, Mehta A. Preservation of fertility in testis cancer management. Urol Clin North Am 2019;46(3):341-51. https://doi.org/10.1016/j.ucl.2019.04.010.
- Ni FD, Hao SL, Yang WX. Molecular insights into hormone regulation via sig- naling pathways in Sertoli cells: with discussion on infertility and testicular tumor. Gene 2020;753:144812. https://doi.org/10.1016/j.gene.2020.144812.
- Oldenburg J. Hypogonadism and fertility issues following primary treatment for testicular cancer. Urol Oncol 2015;33(9):407-12. https://doi.org/10.1016/j.urolonc.2015.01.014.
- Jacobs LA, Vaughn DJ. Hypogonadism and infertility in testicular cancer survivors. J Natl Compr Canc Netw 2012;10(4):558-63. https://doi.org/10.6004/jnccn.2012.0053.







