ВВЕДЕНИЕ
В настоящее время нервосберегающая расширенная радикальная гистерэктомия (РГЭ С1 типа) принята в качестве новой стандартной методики хирургического вмешательства при инвазивном раке шейки матки (РШМ). Ее онкологические результаты сопоставимы со стандартной техникой операции (РГЭ С2 типа) [1]. В послеоперационном периоде перед хирургом встает вопрос о возможностях оценки сохранности функции нижних мочевыводящих путей (НМП). Возникающие симптомы нарушения функции нижних мочевыводящих путей (СНМП) оказывают большое влияние на качество жизни пациенток и должны приниматься во внимание при оценке общеклинического статуса пациенток в послеоперационнном периоде. В подавляющем большинстве исследований контроль проводится на основании субъективных данных – с помощью оценки жалоб больных, в том числе с использованием оценочных шкал. Объективная оценка чаще проводится посредством измерения объема остаточной мочи (ООМ) при катетеризации или ультразвуковым методом [2, 3, 4].
Известно, что нарушение функции НМП может возникать как в раннем послеоперационном периоде, так и в отдаленные сроки – через год и более после проведенного хирургического лечения. У части пациенток нарушения уродинамики протекают субклинически или на фоне отсутствия клинической симптоматики [5]. Проведение симптоматической оценки расстройства мочеиспускания не позволяет поставить точный диагноз, так как многие симптомы являются субъективными и неспецифичными для определенного заболевания или нарушения. Субъективная оценка симптомов также бывает затруднена в связи с наличием у одной пациентки нескольких уродинамических нарушений одновременно, что нередко встречается в клинической практике.
Уродинамическое исследование позволяет оценить состояние мочевыделительной системы, детализировать характер нарушения и определить дальнейшую тактику урореабилитации. Внедрение уродинамического исследования в практику обследования пациентов, перенесших лечение по поводу онкологических заболеваний органов таза, улучшило понимание изменений функции мочевого пузыря и уретры после радикальных гинекологических операций. Ввиду трудоемкости и факультативности метода инвазивного уродинамического исследования на первом этапе обычно проводят урофлоуметрию, как метод неинвазивного уродинамического скрининга нарушений функции НМП.
Целью настоящего исследования является оценка динамики мочеиспускания на основании показателей урофлоуметрии у пациенток после радикального хирургического лечения РШМ.
Статистический анализ
Статистическая обработка полученных данных проводилась с помощью R (R Foundation for Statistical Computing, Vienna, Austria; версия 3.2). Проверка данных на нормальность распределения выполнялась с помощью теста Шапиро–Уилка. В качестве описательных статистик для количественных показателей посчитаны средние ± средние квадратические отклонения [(M (±SD)]; минимальные и максимальные значения в выборке. Сравнение медиан в группах проводили при помощи теста Манна–Уитни, частот – с помощью точного теста Фишера. Статистически значимые различия признавались на уровне р<0,05.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включено 173 пациентки с морфологически верифицированным РШМ IB1-IIВ стадий, которым в период 2017-2022 гг. на базе отделения онкогинекологии МНИОИ им. П.А. Герцена, отделения гинекологии с химиотерапией НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина – филиалов ФГБУ «НМИЦ радиологии» Минздрава России проведена расширенная РГЭ. Основную группу составили 42 пациентки, которым выполнена расширенная РГЭ С1 типа с тазовой и парааортальной лимфаденэктомией с применением метода водоструйной диссекции. В группу контроля А вошло 79 пациенток, которым проведена операция в объеме расширенной РГЭ С1 типа с тазовой и парааортальной лимфаденэктомией. Группу контроля B составили 52 пациентки, которым проведено хирургическое вмешательство в объеме расширенной РГЭ С2 типа с тазовой и парааортальной лимфаденэктомией. Уродинамическое исследование проводилось как на дооперационном этапе, так и через 2 месяца после хирургического вмешательства. Исследование выполнялось на урофлоуметре «Urocap», входящем в уродинамический комплекс «Aquarius TT» (Laborie, Канада), с целью изучения статуса мочеиспускания и изменений урофлоуметрической кривой и параметров урофлоуметрии. Основные оцениваемые урофлоуметрические параметры:
- максимальная скорость потока мочи – Qмакс (мл/с);
- средняя скорость потока мочи – Qср (мл/с);
- время достижения максимального потока мочи (с);
- время потока мочи (с);
- объем выделенной мочи – VV (мл);
- объем остаточной мочи – PVR (мл).
Данные уродинамического исследования оценивались с учетом клинических данных о состоянии пациенток.
РЕЗУЛЬТАТЫ
В основной группе средний возраст пациенток составил 44,6 (10,6) года, в группе контроля А – 46,5 (10,8), в группе контроля В – 48,7 (9,3). Распределение по стадиям в основной группе по стадиям FIGO (2018): IB стадия определена у 38/42 (91%) пациенток, IIA – у 2/42 (4%), IIB – 2/42 (5%). В группе контроля А распределение по стадиям: IB стадия – 72/79 (91%) пациенток, IIA – у 3/79 (4%), IIB – 4/79 (5%). В группе контроля В распределение по стадиям: IB стадия – 43/52 (83%) пациенток, IIA – у 2/52 (4%), IIB – 7/52 (13%). По данным морфологического исследования во всех группах преобладал плоскоклеточным тип опухоли – 36 (86%), 65 (82%) и 44 (85%) в основной и контрольных группах соответственно (р>0,05) (табл. 1).
Таблица 1. Клинико-морфологическая характеристика исследуемых групп
Table 1. Clinical and morphological characteristics of the studied groups
| Основная группа, n=42 Main group, n=42 |
Контрольная группа А, n=79 Control group A, n=79 |
Контрольная группа B, n=52 Control group B, n=52 |
р | |
|---|---|---|---|---|
| Возраст / Age | ||||
| 44,6 (10,6) | 46,5(10,8) | 48,7 (9,3) | >0,05 | |
| FIGO (2018), n (%) | ||||
| IB1 | 23 (55%) | 55 (69%) | 29 (56%) | >0,05 |
| IB2 | 13 (31%) | 14 (18%) | 10 (19%) | |
| IB3 | 2 (5%) | 3 (4%) | 4 (8%) | |
| IIA1 | 1 (2%) | 2 (3%) | 1 (2%) | |
| IIA2 | 1 (2%) | 1 (1%) | 1 (2%) | |
| IIB | 2 (5%) | 4 (5%) | 7 (13%) | |
| Гистологический тип опухоли, n (%) / Histological type of tumor, n (%) | ||||
| Аденокарцинома Аdenocarcinoma |
5 (12%) | 12 (15%) | 8 (15%) | >0,05 |
| Плоскоклеточный рак Squamous cell carcinoma |
36 (86%) | 65 (82%) | 44 (85%) | |
| Аденоплоскоклеточный рак Adenosquamous carcinoma |
1 (2%) | 2 (3%) | — | |
| Гистологический тип опухоли, n (%) / Histological type of tumor, n (%) | ||||
| Grade1 | 7 (17%) | 7 (9%) | 7 (13%) | >0,05 |
| Grade2 | 24 (57%) | 46 (58%) | 27 (52%) | |
| Grade3 | 11 (26%) | 26 (33%) | 18 (35%) | |
Всем пациенткам на дооперационном этапе с целью исключения нарушения функции НМП выполнялась урофлоуметрия с оценкой ее основных цифровых показателей – максимальной и средней скоростей потока мочи, времени достижения максимального потока мочи, времени потока мочи, времени мочеиспускания, объема выделенной мочи, объема остаточной мочи. Дооперационные показатели урофлоуметрии были равнозначными и не имели статистически значимых отличий между группами (р>0,05) (табл. 2).
Таблица 2. Результаты урофлоуметрии до операции у пациенток основной и контрольных групп
Table 2. The results of uroflowmetry before surgery in patients of the main and control groups
| Показатель урофлоуметрии Uroflowmetry index |
Основная группа, n=42 Main group, n=42 |
Контрольная группа А, n=79 Control group A, n=79 |
Контрольная группа B, n=52 Control group B, n=52 |
P |
|---|---|---|---|---|
| Максимальная скорость потока мочи, мл/с Maximum urine flow rate, ml/s |
29,8±11,6 | 28,3±14,6 | 29,2±10,7 | >0,05 |
| Средняя скорость потока мочи, мл /с Average urine flow rate, ml/s |
12,0±5,13 | 15,2±6,5 | 16,2±6,2 | >0,05 |
| Время достижения максимального потока мочи, с Time to reach maximum urine flow, s |
9,4±5,8 | 8,1±7,4 | 6,7±6,4 | >0,05 |
| Время потока мочи, с Urine flow time, s |
23,1±10,6 | 20,2±8,2 | 19,3± 8,4 | >0,05 |
| Время мочеиспускания, с Urination time, s |
30,8±13,5 | 26,1±11,7 | 26,1±8,9 | >0,05 |
| Объем выделенной мочи, мл Urine output, ml |
301,1±122,4 | 253,2±137,2 | 269,2±140,1 | >0,05 |
| Объем остаточнойй мочи, мл Post-void residual urine, ml |
21,5±22,5 | 22,2±12,3 | 21,4±7,8 | >0,05 |
Особое диагностическое значение в урофлометрии имеет графическое изображение мочеиспускания в виде урофлоуметрической кривой (урофлоуграмма). В норме на графике урофлоуметрии наблюдается симметричная кривая в виде параболы/колокола. В норме значение максимальной скорости потока в 1,5–2 раза превышает среднюю скорость (рис. 1). В случае нарушения мочеиспускания на графике регистрируются неравномерные всплески амплитуды в виде отдельных пиков максимальной скорости мочеиспускания или пологая кривая. Такой тип потока мочи считается обструктивным (рис. 2). В других случаях, например, при гиперактивном мочевом пузыре, кривая мочеиспускания имеет «стремительный» вид: отмечается быстрое нарастание потока и быстрое его снижение. При этом максимальная скорость мочеиспускания превышает нормативную. Такой тип мочеиспускания является вариантом «необструктивного» (рис. 3).
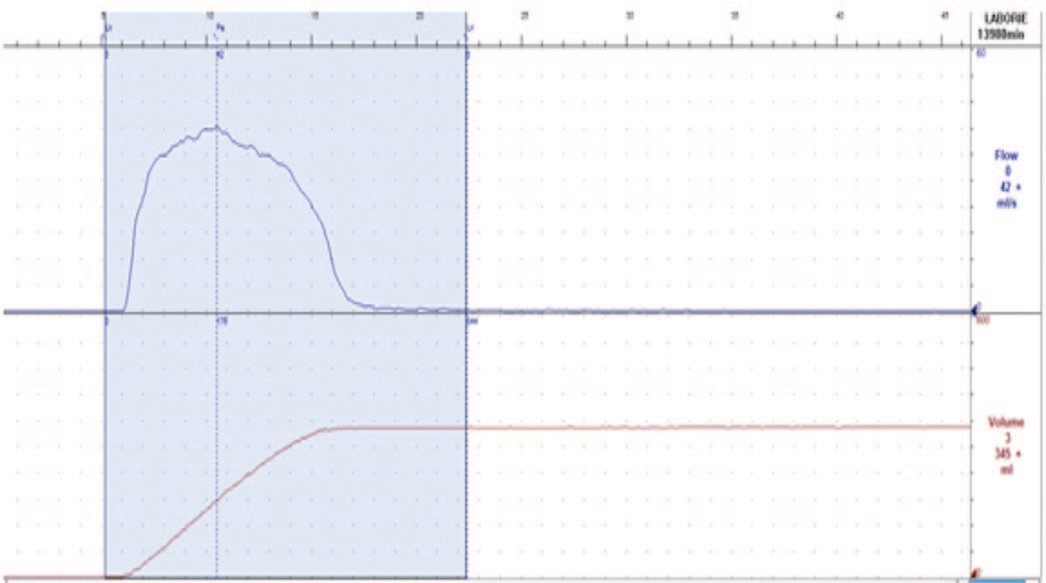
Рис.1. Нормальный физиологический тип урофлоуметрической кривой в послеоперационном периоде
Fig 1. Normal physiological type of uroflowmetric curve in the postoperative period
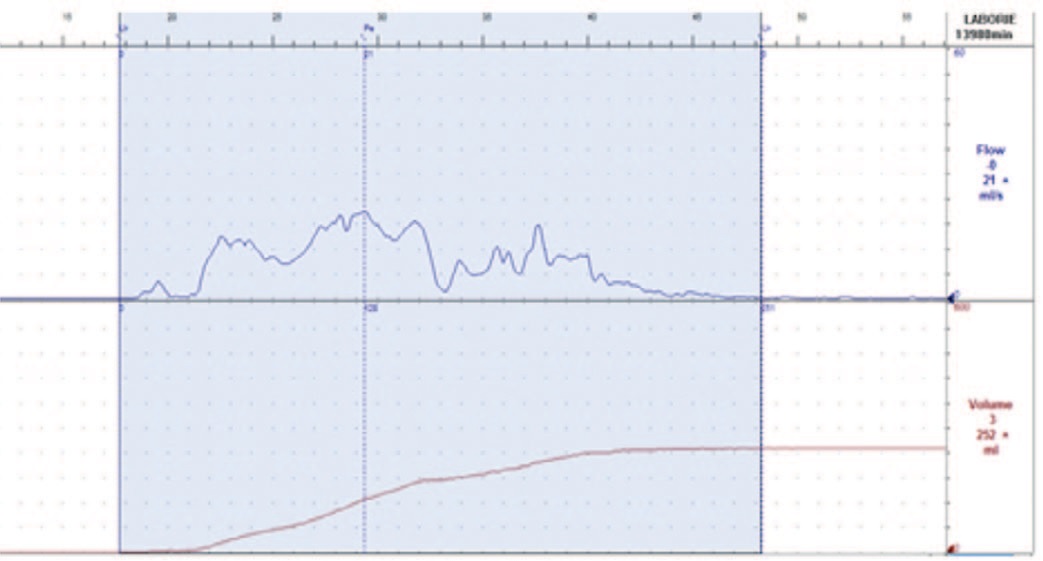
Рис. 2. Обструктивный тип урофлоуметрической кривой в послеоперационном периоде
Fig 2. Obstructive type of uroflowmetric curve in the postoperative period
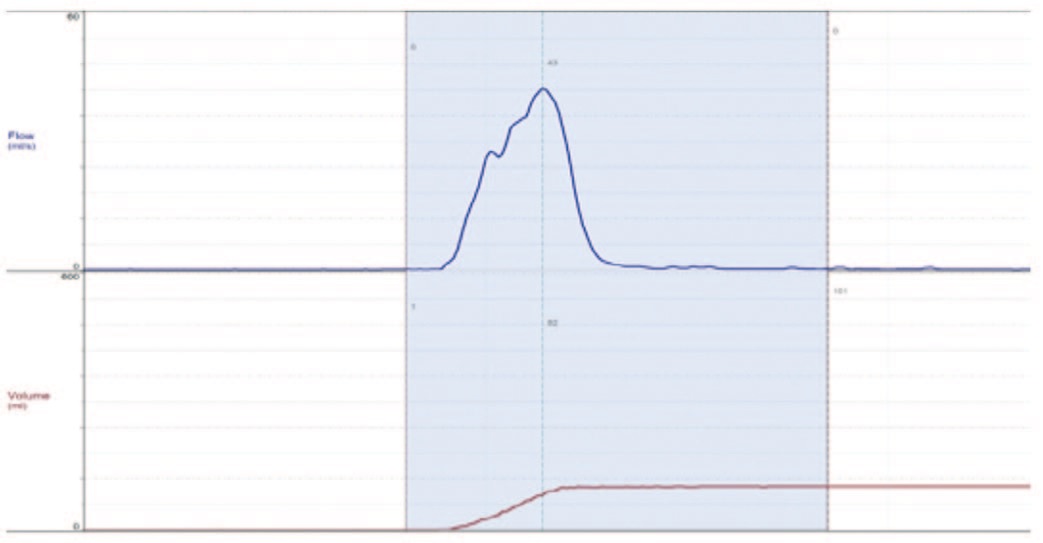
Рис. 3. «Стремительный» тип урофлоуметрической кривой в послеоперационном периоде
Fig. 3. «Impetuous» type of uroflowmetric curve in the postoperative period
При оценке типов кривой мочеиспускания в основной группе нормальный физиологический тип выявлен в 90,5% случаев, в то время как обструктивный тип выявлен только в 9,5% (р>0,05). В группе контроля А нормальная физиологическая урофлоуграмма зафиксирована в 80,8% случаев, обструктивная – в 19,2% (р>0,05). В группе контроля В нормальная физиологическая урофлоуграмма определялась в 39,4% наблюдений, в большинстве случаев (60,6%) зарегистрирован обструктивный тип мочеиспускания (р<0,001).
При оценке СНМП в послеоперационном периоде отмечены наиболее частые жалобы в виде порционного мочеиспускания при ощущении наполненности мочевого пузыря, вялого мочеиспускания с напряжением мышц брюшной стенки, чувства неполного опорожнения и частого мочеиспускание малыми порциями. В раннем послеоперационном периоде СНМП в основной группе наблюдались в 7,1% (3 пациентки), что статистически не имело отличий от группы контроля А – 7,6% (6 пациенток) (р>0,05). В группе контроля В данный показатель составил 26,9% (21 пациентка) (р<0,001). Согласно опросу через 3 месяца после хирургического вмешательства СНМП в основной группе и контрольной группе А не выявлены ни у одной пациентки. Обструктивное мочеиспускание по данным урофлоуметрии зарегистрировано у 4 из них (9,5%). В группе контроля В СНМП присутствовали в 17,3% (9 пациенток) (р<0,001). При урофлоуметрии обструктивное мочеиспускание отмечено у 31 пациентки (60,6%).
С целью оценки восстановления функции нижних мочевых путей опрос пациенток проводился также через 6 месяцев после хирургического вмешательства. В контрольной группе В СНМП выявлены у 15,4% (8 пациенток), в основной группе и группе контроля А клинические проявления нарушений отсутствовали.
Согласно результатам урофлометрии до операции при сравнении между исследуемыми группами не было выявлено статистически значимых отличий по таким показателям как средняя скорость потока мочи, время достижения максимального потока мочи, время мочеиспускания и объем выделенной мочи (p>0,05) (табл. 2).
Максимальная скорость потока мочи через 2 дня после операции была значительно выше в основной группе и группе контроля А в сравнении с группой контроля В – 24,1±8,10 мл/с, 25,1±13,3 мл/с и 19,3±10,1 мл/с соответственно (р<0,001). Такой показатель, как время потока мочи, был достоверно ниже в основной группе (20,2±5,58 с) в сравнении с группой контроля А (24,0±11,3 с) (р=0,007) и группой контроля В (23,5± 9,5 с) (р<0,001). Параметр объема остаточной мочи был значительно выше в контрольной группе В по сравнению с основной группой и группой контроля А – 85,1±56,5 мл, 34,0±9,45 мл и 32,2±11,2 соответственно (р<0,001) (табл. 3). Таким образом, показатели урофлоуметрии не имели достоверных отличий при сравнении групп А, где выполнялась операция по стандартной нервосберегающей технике, и нервосберегающей техники с использованием водоструйного диссектора в основной группе.
Таблица 3. Результаты урофлоуметрии через 2 месяца после операции у пациенток основной и контрольных групп
Table 3. The results of uroflowmetry 2 months after surgery in patients of the main and control groups
| Показатель урофлоуметрии Uroflowmetry index |
Основная группа, n=42 Main group, n=42 |
Контрольная группа А, n=79 Control group A, n=79 |
Контрольная группа B, n=52 Control group B, n=52 |
P | ||
|---|---|---|---|---|---|---|
| Основная и группа А Main and control group A |
Основная и группа В Main and control group B |
Группа А и группа В Control groups A and B |
||||
| Максимальная скорость потока мочи, мл/с Maximum urine flow rate, ml/s |
24,1±8,10 | 25,1±13,3 | 19,3±10,1 | 0,279 | <0,001 | <0,001 |
| Средняя скорость потока мочи, мл /с Average urine flow rate, ml/s |
12,1±5,08 | 12,3±8,4 | 11,8±5,5 | 0,369 | 0,002 | 0,669 |
| Время достижения максимального потока мочи, с Time to reach maximum urine flow, s |
7,69±3,04 | 9,2±8,8 | 8,8±7,5 | 0,175 | 0,108 | 0,936 |
| Время потока мочи, с Urine flow time, s |
20,2±5,58 | 24,0±11,3 | 23,5± 9,5 | 0,007 | <0,001 | 0,755 |
| Время мочеиспускания, с Urination time, s |
27,0±10,6 | 25,3±16,1 | 31,0±8,1 | 0,540 | 0,025 | 0,016 |
| Объем выделенной мочи, мл Urine output, ml |
268,2 ±109,1 | 241,2 ±111,2 | 265,5 ±125,5 | 0,496 | 0,678 | 0,184 |
| Объем остаточнойй мочи, мл Post-void residual urine, ml |
34,0±9,45 | 32,2±11,2 | 85,1±56,5 | 0,503 | <0,001 | <0,001 |
При сравнительном анализе параметров урофлоуметрии до и через 2 месяца после операции у пациенток основной группы получены достоверные отличия по показателям максимальной и средней скоростей потока мочи. В группе контроля А получены статически значимые различия по показателям максимальной скорости потока мочи, средней скорости потока мочи, времени потока мочи, а также объема остаточной мочи. В группе контроля В все показатели имели достоверные отличия за исключением объема выделенной мочи (табл. 4). Сравнительные результаты до и через 2 месяца после хирургического лечения в основной группе свидетельствуют о преимуществе техники водоструйной диссекции, как о наиболее прецизионном и нервосберегающем методе.
Таблица 4. Сравнение результатов урофлоуметрии до и через 2 месяца после хирургического лечения в исследуемых группах
Table 4. Comparison of uroflowmetry results before and 2 months after surgical treatment in the study groups
| Показатель урофлоуметрии Uroflowmetry index |
Основная группа, n=42 Main group, n=42 |
P | Контрольная группа А, n=79 Control group A, n=79 |
P | Контрольная группа B, n=52 Control group B, n=52 |
P | |||
|---|---|---|---|---|---|---|---|---|---|
| До Before | После After | До Before | После After | До Before | После After | ||||
| Максимальная скорость потока мочи, мл/с Maximum urine flow rate, ml/s |
29,8±11,6 | 24,1±8,10 | 0,004 | 28,3±14,6 | 25,1±13,3 | <0,001 | 29,2±10,7 | 19,3±10,1 | <0,001 |
| Средняя скорость потока мочи, мл /с Average urine flow rate, ml/s |
12,0±5,13 | 9,52±3,13 | 0,013 | 15,2±6,5 | 12,3±8,4 | <0,001 | 16,2±6,2 | 11,8±5,5 | <0,001 |
| Время достижения максимального потока мочи, с Time to reach maximum urine flow, s |
9,4±5,8 | 7,69±3,04 | 0,071 | 8,1±7,4 | 9,2±8,8 | 0,063 | 6,7±6,4 | 8,8±7,5 | <0,001 |
| Время потока мочи, с Urine flow time, s |
23,1±10,6 | 20,2±5,58 | 0,088 | 20,2±8,2 | 24,0±11,3 | <0,001 | 19,3± 8,4 | 23,5±9,5 | <0,001 |
| Время мочеиспускания, с Urination time, s |
30,8±13,5 | 27,0±10,6 | 0,171 | 26,1±11,7 | 25,3±16,1 | 0,697 | 26,1±8,9 | 31,0±8,1 | 0,001 |
| Объем выделенной мочи, мл Urine output, ml |
301,1±122,4 | 268,2±109,1 | 0,103 | 253,2±137,2 | 241,2±111,2 | 0,411 | 269,2 ±140,1 | 265,5±125,5 | 0,742 |
| Объем остаточнойй мочи PVR, мл Post-void residual urine, ml |
21,5±22,5 | 34,0±9,45 | 0,006 | 22,2±12,3 | 32,2±11,2 | <0,001 | 21,4±7,8 | 85,1±56,5 | <0,001 |
С целью патогенетического обоснования симптомов со стороны мочевыделительных путей в клинической практике проводится цистометрия наполнения и опорожнения, что было выполнено в основной группе. Согласно результатам проведенного инвазивного уродинамического обследования у 5 (11,9%) пациенток выявлено снижение чувствительности мочевого пузыря, у 2 (4,7%) пациенток – детрузорная гиперактивность. При этом пациентки с выявленными изменениями не предъявляли выраженных жалоб со стороны мочеиспускания. В группе контроля А и группе контроля В углубленная уродинамическая оценка не проводилась.
ОБСУЖДЕНИЕ
Обширная радикальная гинекологическая операция является причиной повреждения периферических нервов области таза, а также сосудистых сплетений, сопровождающих мочеточник и мочевой пузырь, что неизбежно приводит к дисфункции НМП. Частота клинически значимых нарушений, проявляющихся СНМП в виде поллакиурии, императивности, недержания мочи или задержки мочеиспускания, после радикальных гистерэктомий колеблется от 8 до 80%. Такой широкий диапазон обусловлен отличающимися техниками операции, вариабельностью способов диагностической оценки, различиями во времени наблюдения [6].
Ранние послеоперационные СНМП характеризуются снижением функциональной емкости мочевого пузыря, повышением активности детрузора, гиперчувствительностью и снижением комплаентности мочевого пузыря. Поздняя дисфункция проявляется затруднением мочеиспускания с напряжением живота, снижением сократимости детрузора, иногда в сочетании с его гиперактивностью, недержанием мочи [7]. Основным патоморфологическим субстратом СНМП является повреждение нервных волокон в ходе хирургического вмешательства. Нарушение проведения импульса может быть обусловлено временной блокадой передачи сигнала без поражения аксонов (нейропраксия), в результате чего потенциал действия блокируется в месте повреждения. В данном случае функциональные нарушения являются временными, а функциональная целостность нерва восстанавливается в период от нескольких часов до нескольких недель после операции. Возможно пересечение аксона с сохранением интактности нервных оболочек (аксонотмезис), обеспечивающих регенерацию и рост нерва от 0,25 мм/сут до 4 мм/сут. В случае полного пересечения нерва без сохранения аксонов и нервных оболочек регенеративная способность волокна утрачивается [8]. Повреждение сосудистого сплетения идущего рядом с нервными волокнами также играет большую роль в развитии дисфункции НМП. Сочетание растяжения и ишемии делает нерв более уязвимым к повреждению. Поэтому ряд авторов говорит о необходимости сохранения мезоуретральных тканей, в составе которых проходят гипогастральные нервы, и исключают отдельную обработку нервных сплетений [9, 10].
Однако травматическое повреждение нерва не является единственным механизмом, приводящим к дисфункции НМП после расширенной РГЭ. Непосредственное повреждение мочевого пузыря, лимфокисты, нарушение кровоснабжения и фиброз стенки мочевого пузыря, менопаузальный возраст пациенток, отягощенный акушерский анамнез – факторы, играющие роль в развитии послеоперационных нарушений мочеиспускания [11, 12].
Важность проведения уродинамического исследования в послеоперационном периоде обусловлена необходимостью получения достоверной объективной информации об имеющихся нарушениях. Одно из первых исследований, посвященных вопросу уродинамического исследования как метода диагностики и предупреждения нарушений со стороны мочевыделительной системы, опубликовано P. Benedetti-Panici и соавт. [13]. 84 пациенткам через 18 месяцев (медиана наблюдения 13-25 месяцев) после радикального хирургического лечения РШМ проведено уродинамическое исследование. Даже при отсутствии жалоб со стороны мочевыделительных путей у 58 (76%) пациенток были обнаружены уродинамические нарушения. В результате выявлено три основных нарушения мочеиспускания: гиперактивность детрузора (21%), смешанное недержание мочи (24%), стрессовое недержание мочи (21%). Таким образом, авторы сделали вывод, что наличие субъективных клинических симптомов, как и их отсутствие, не может достоверно свидетельствовать о степени восстановления функции НМП. При этом высоко информативным объективным методом оценки является уродинамическое исследование.
В периодической литературе опубликован ряд работ, посвященных уродинамическому исследованию после расширенной РГЭ [4, 5, 14, 15]. J. Kruppa и соавт. провели исследование в небольшой когорте из 12 пациенток, которым проведена расширенная РГЭ С1 типа. Перед хирургическим лечением, а также через неделю и через 22 месяца после операции пациенткам выполнялось уродинамическое исследование. Проводилась оценка таких показателей как максимальная скорость потока мочи, цистометрическая емкость, объем остаточной мочи, а также измерялось давление детрузора при наполнении. Через 1 неделю после операции у 6 пациенток выявлена гиперактивность детрузора, через 22 месяца данное патологическое состояние сохранилось у 3 пациенток. При проведении опроса у пациенток отсутствовали выраженные клинические симптомы имеющихся нарушений. Авторы сделали вывод, что несмотря на отсутствие симптомов уродинамическое исследование имеет важное клиническое значение для достоверной оценки функции НМП [14].
На сегодняшний день опубликовано единственное исследование, посвященное методу нервосберегающей гистерэктомии – НСГЭ (РГЭ С1 типа) с использованием метода водоструйной диссекции [15]. В 2019 году L. Lei и соавт. в исследуемой группе пациенток с целью послеоперационной оценки функции НМП проводили уродинамическое исследование через 4 месяца после хирургического лечения. В исследовании проводилось сравнение показателей мочеиспускания после НСГЭ с использованием водоструйного диссектора (основная группа) и стандартной расширенной РГЭ С1 типа (группа контроля). В группе контроля по данным уродинамического исследования различные дисфункции НМП наблюдалась у 7 пациенток (8,8%), в основной группе – у 4 (3,8%). В данном исследовании авторы продемонстрировали преимущества расширенной РГЭ С1 типа с использованием водоструйного диссектора, которая приводит к более быстрому функциональному восстановлению НМП в послеоперационном периоде.
Таким образом, предоперационная оценка уродинамических параметров является крайне важной для понимания влияния операции на функцию мочевыведения и исключения или возможной объективной констатации наличия нарушения функции НМП на дооперационном этапе [11].
Уродинамическое исследование не используется изолированно и всегда оценивается совокупно с другими клиническими данными. Важна роль опроса пациенток для изучения жалоб на нарушения мочеиспускания как на дооперационном этапе, так и после проведенного хирургического лечения. Тщательное анкетирование и использование оценочных шкал позволит избежать ошибок в оценке исходов операции, а также определить правильный подход в коррекции СНМП. Урофлоуметрия является базовым скрининговым методом выявления функциональных нарушений со стороны НМП. Данное исследование позволяет получить графический и цифровой отчет о мочеиспускании [16, 17]. При необходимости детализации нарушения у части пациентов проводят комбинированное уродинамическое исследование. Инвазивное уродинамическое исследование (цистометрия наполнения, цистометрия опорожнения, профилометрия уретры) проводится с целью патогенетического обоснования симптомов или выявления нарушения при отсутствии жалоб, а также определения факторов риска. Наиболее часто встречающимися нарушениями, выявляемыми при комбинированном уродинамическом исследовании, являются детрузорная гиперактивность, низкая комплаэнтность, инфравезикальная обструкция и гипоактивность детрузора [17]. Урофлоуметрия является базовым скрининговым методом диагностики патологических состояний НМП [18]. Данные урофлоуметрии помогают объективно определить показания к инвазивному уродинамическому исследованию вне зависимости от наличия или отсутствия сформулированных жалоб и характера их субъективной оценки. Урофлоуметрия, являясь доступным и незатратным методом исследования, также важна при динамическом наблюдении и оценке функциональных результатов лечения, как собственно хирургического, так и любого консервативного метода, в том числе в урореабилитации.
ЗАКЛЮЧЕНИЕ
Анализ полученных данных позволяет утверждать, что субъективная оценка жалоб недостаточна для определения СНМП, у части пациенток нарушения функции НМП протекают бессимптомно и могут быть выявлены только при помощи объективного уродинамического тестирования. Основным скрининговым исследованием является урофлоуметрия. Внедрение уродинамического исследования в практику пред- и послеоперационного обследования улучшило понимание изменений функции мочевого пузыря и уретры после радикальных гинекологических операций и позволило выделить группы риска. Достоверная информация о пред- и послеоперационных нарушениях определяет дальнейшую тактику ведения пациенток и позволяет предупредить усугубление нарушений и снижение качества жизни.
ЛИТЕРАТУРА
1. Kietpeerakool C, Aue-Aungkul A, Galaal K, Ngamjarus C, Lumbiganon P. Nerve-sparing radical hysterectomy compared to standard radical hysterectomy for women with early stage cervical cancer (stage Ia2 to IIa). Cochrane Database Syst Rev 2019;12;2(2):CD012828. https://doi.org/10.1002/14651858.CD012828.pub2.
2. Komatsu H, Okawa M, Hikino K, Iida Y, Osaku D, Kudoh A, et al. A simplified procedure of nerve-sparing radical hysterectomy. J Obstet Gynaecol Res 2022;48(3):766-73. https://doi.org/10.1111/jog.15154.
3. Li L, Ma S, Tan X, Zhong S, Wu M. Surgical, urinary, and survival outcomes of nerve-sparing versus traditional radical hysterectomy: a retrospective cohort study in China. Am J Clin Oncol 2019;42(10):783-8. https://doi.org/10.1097/COC.0000000000000593.
4. Liu Q, Li P, Sun Y, Zhang S, Liu K. Effect of laparoscopic nerve-sparing radical hysterectomy on bladder function recovery. J Invest Surg 2020;33(4):381-6. https://doi.org/10.1080/08941939.2018.1502377.
5. Cao TT, Wen HW, Gao YN, Lyu QB, Liu HX, Wang S, Wang SY, et al. Urodynamic assessment of bladder storage function after radical hysterectomy for cervical cancer. Chin Med J (Engl) 2020;133(19): 2274-80. https://doi.org/10.1097/CM9.0000000000001014.
6. Yoshikawa H, Nerve-sparing radical hysterectomy: Kobayashi's method. Surg J 2021;7(2):70- 6. https://doi.org/10.1055/s-0041-1728751.
7. Wang S, Wen H, Gao Y, Lv Q, Cao T, Wang S, et al. Assessment of pelvic floor function and quality of life in patients treated for cervical cancer: a multicenter retrospective study. Gynecol Obstet Invest 2021;86(4):353-60. https://doi.org/10.1159/000517995.
8. Eicke M., Hohenfellner R., Leissner J. Nerve injuries in urologic surgery. in book Advanced Urologic Surgery. Third Edition. [Ed. Hohenfellner R, Fitzpatrick J, McAninch J.] 2005; 488-93 р. https://doi.org/10.1002/9780470755914.
9. Cosma S, Ferraioli D, Mitidieri M, Ceccaroni M, Zola P, Micheletti L, Benedetto C. A simplified fascial model of pelvic anatomical surgery: going beyond parametrium-centered surgical anatomy. Anat Sci Int 2021; 96(1):20-9. https://doi.org/10.1007/s12565-020-00553-z.
10. Yang XF, Luo GH, Ding ZH, Li GX, Chen XW, Zhong SZ.The urogenital-hypogastric sheath: an anatomical observation on the relationship between the inferomedial extension of renal fascia and the hypogastric nerves. Int J Colorectal Dis 2014;29(11):1417-26. https://doi.org/10.1007/s00384-014-1973-0.
11. Aoun F, Peltier A, van Velthoven R. Lower Urinary tract dysfunction in pelvic gynecologic cancer: the role of urodynamics. Adv Urol 2014;2014:303958. https://doi.org/10.1155/2014/303958.
12. Мухтарулина С.В., Каприн А.Д., Востров А.Н. Причины развития урологических осложнений у больных инвазивным раком шейки матки после радикальной гистерэктомии. Онкология. Журнал им. П.А. Герцена 2017;6(5):100-2. https://doi.org/10.17116/ onkolog201765100-102. [Mukhtarulina S.V., Kaprin A.D., Vostrov A.N. Reasons of urological complications in patients with invasive cervical cancer after radical hysterectomy. Onkologiya. Zhurnal imeni P.A. Gertsena = P.A. Herzen Journal of Oncology 2017;6(5):100-102. (In Russian)].
13. Benedetti-Panici P, Zullo MA, Plotti F, Manci N, Muzii L, Angioli R.. Long-term bladder function in patients with locally advanced cervical carcinoma treated with neoadjuvant chemotherapy and type 3-4 radical hysterectomy. Cancer 2004;100(10):2110-7. https://doi.org/10.1002/cncr.20235.
14. Kruppa J, Kavvadias T, Amann S, Baessler K, Schuessler B.. Short and long-term urodynamic and quality of life assessment after nerve sparing radical hysterectomy: a prospective pilot study. Eur J Obstet Gynecol Reprod Biol 2016;201:131-4. https://doi.org/10.1016/j.ejogrb.2016.03.026.
15. Li L, Ma S, Tan X, Zhong S, Wu M. The urodynamics and survival outcomes of different methods of dissecting the inferior hypogastric plexus in laparoscopic nerve-sparing radical hysterectomy of type C: a randomized controlled study. Ann Surg Oncol 2019;26(5):1560-8. https://doi.org/10.1245/s10434-019-07228-8.
16. Chapple CR, Osman NI, Birder L, Dmochowski R, Drake MJ, van Koeveringe G,et al. Terminology report from the International Continence Society (ICS) working group on Underactive Bladder (UAB). Neurourol Urodyn 2018;37(8):2928-2931. https://doi.org/10.1002/ nau.23701.
17. Ромих В.В., Клиническая уродинамика и нейроурология: от диагностики к эффективному лечению и реабилитации. Экспериментальная и клиническая урология 2010;( 4):92-8. [Romih V.V. Clinical urodynamics and neurourology: from diagnosis to effective treatment and rehabilitation. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and clinical urology 2010;(4):92-8. (In Russia)].
18. Arlandis S, Bø K, Cobussen-Boekhorst H, Costantini E, de Heide M, Farag F, Groen J, Karavitakis M, et al. European Association of Urology guidelines on the management of female non-neurogenic lower urinary tract symptoms. Part 2: underactive bladder, bladder outlet obstruction, and nocturia. Eur Urol 2022;82(1):60-70. https://doi.org/10.1016/ j.eururo.2022.01.044.







