Распространенность бесплодия в различных странах варьирует от 8 до 29% и составляет в среднем во всем мире около 15%. При этом отмечено, что каждая восьмая пара имеет проблемы с зачатием первого ребенка, каждая шестая пара – второго и последующего ребенка [1,2]. Примерно у половины бездетных пар бесплодие связано с «мужским фактором», т.е. измененными параметрами спермы [3, 4]. Следует отметить, что за последние два десятилетия наблюдается негативная тенденция в этой области в виде увеличения доли инфертильных мужчин с 30 до 50% [5, 6].
Мужское бесплодие представляет собой многофакторный синдром, включающий широкий спектр нарушений и различных патологических состояний, затрагивающих как половую, так и другие системы организма: эндокринную, нервную, кровеносную, иммунную и т.д. Однако в 25-75% случаев мужского бесплодия не удается выявить этиологический фактор (идиопатическое бесплодие) [7-10].
Одной из теорий, объясняющих снижение фертильного потенциала у данной категории пациентов, является повышение допустимой концентрации сперматозоидов с фрагментацией ДНК, представляющей собой одноили двухцепочечный разрыв молекул ДНК. Во многих исследованиях показана обратная корреляционная связь между вероятностью достижения беременности (естественным путем или с помощью вспомогательных репродуктивных технологий) и степенью фрагментации ДНК сперматозоидов [11-13]. Например, при низкой степени фрагментации ДНК вероятность успешной беременности естественным способом была выше в 6,5-10,0 раз, с помощью процедуры экстракорпорального оплодотворения (ЭКО) – выше в 2 раза по сравнению с высокой степенью фрагментации ДНК [14, 15].
К настоящему времени среди специалистов нет единого мнения относительно тактики по коррекции повышенного уровня фрагментации ДНК сперматозоидов, а исследования, посвященные изучению возможностей различных методов лечения мужчин с бесплодием в сочетании с высокой степенью фрагментации ДНК сперматозоидов, основаны на малой выборке пациентов и краткосрочных наблюдениях. Кроме того, в мировой литературе отсутствуют работы, направленные на изучение влияния гипербарической оксигенации (ГБО) на изменение показателей фрагментации ДНК сперматозоидов, и, следовательно, на вероятность наступления беременности у половых партнерш. Таким образом, все вышеуказанные факторы обусловили актуальность настоящего исследования.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование носило проспективный характер и основано на материалах обследования и лечения 90 мужчин с идиопатическим бесплодием и повышенным уровнем фрагментации ДНК сперматозоидов. Данная когорта пациентов была подразделена на две группы: основная группа (60 человек) и контрольная группа (30 человек). Пациентам основной группы на базе ГБУЗ ГКБ им. С.П. Боткина г. Москвы проведен курс лечения с помощью ГБО перед выполнением ЭКО, пациентам контрольной группы – не проводили ГБО перед ЭКО. Возраст больных варьировал от 25 до 37 лет, а его медиана составила 30,5 лет. Продолжительность срока мужского бесплодия в исследуемой выборке колебалась от 1 года до 5 лет и составила в среднем 2,4 года.
Пациентам основной группы ГБО выполняли по стандартной методике с помощью барокамеры отечественного производства БЛКС-303. Для работы данной барокамеры использовали медицинский кислород. Сеансы проводили ежедневно (с понедельника по пятницу, суббота и воскресенье – выходные, затем повторно с понедельника по пятницу, всего – десять сеансов). Общее время одного сеанса составляло 60 минут: компрессия – 5-10 минут, изопрессия – 40 минут, декомпрессия – 10 минут. Режимы баротерапии устанавливали с учетом индивидуальной переносимости пациентом повышенного давления внутри камеры. При этом давление кислорода в среднем составляло 1,2-2,0 АТА (в режиме изопрессии). Через 3 месяца после 10 сеансов ГБО пациентам основной группы выполняли процедуру ЭКО.
Базовое лечение пациентов обеих групп, кроме ГБО, не проводили из соображений обеспечения чистоты исследования.
Исследование спермограммы проводили по стандартной методике, при этом ее основные параметры оценивали в соответствии с требованиями руководства ВОЗ 5-го издания от 2010 года [16]. Фрагментацию ДНК сперматозоидов определяли с помощью метода TUNEL. Результат теста оценивали в виде индекса фрагментации ДНК сперматозоидов, выраженном в процентах, что означало долю сперматозоидов с поврежденной ДНК. Верхней границей нормальных показателей уровня (степени) фрагментации ДНК сперматозоидов считали 15%. Спермограмму и уровень фрагментации ДНК сперматозоидов оценивали у пациентов основной группы в момент включения в исследование (базовые данные) и через 3 месяца после курса ГБО, у пациентов контрольной группы – в момент включения в исследование и через 3 месяца после него.
Статистическую обработку результатов проводили с помощью программы Statistica v. 17.0. При характеристике признаков, распределение значений которых в выборке отличалось от нормального типа, использованы медиана (Me), нижний (Q25%) и верхний (Q75%) квартили, а признаков с нормальным типом распределения значений – среднее значение (M) со средним квадратическим отклонением (SD).
Таблица 1. Базовые значения ключевых параметров спермограммы и уровня фрагментации ДНК сперматозоидов у пациентов основной и контрольной групп
| Показатель | Основная группа | Контрольная группа | p |
|---|---|---|---|
| Общее количество сперматозоидов (106 в эякуляте), M±SD |
28,8±12,2 | 29,3±10,5 | 0,615 |
| Подвижность (a+b) сперматозоидов (%), Me [Q25%; Q75%] |
28 [19,5; 34] | 29 [24; 36] | 0,323 |
| Морфология сперматозоидов (% нормальных форм), Me [Q25%; Q75%] |
8 [5; 16] | 9 [6; 16] | 0,098 |
| Уровень фрагментации ДНК сперматозоидов (%), M±SD |
33,2±7,5 | 31,2±6,1 | 0,081 |
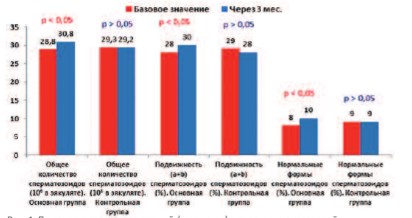
Рис. 1. Динамика средних значений (медианы) основных показателей спермограммы у пациентов основной и контрольной групп
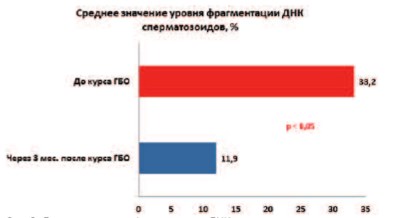
Рис. 2. Динамика уровня фрагментации ДНК сперматозоидов у пациентов основной группы
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По базовым значениям ключевых показателей спермограммы и уровня фрагментации ДНК сперматозоидов у пациентов основной и контрольной групп статистически значимых различий между собой не выявлено (табл. 1).
У пациентов основной группы через 3 месяца после сеансов ГБО отмечено небольшое, но достоверное (p< 0,05) увеличение среднего значения (медианы) всех основных параметров спермограммы, тогда как в контрольной группе без проведения курса с помощью ГБО такие положительные изменения в спермограмме не отмечены (рис. 1).
Проведение курса лечения с использованием ГБО привело к существенному уменьшению среднего значения уровня фрагментации ДНК сперматозоидов у пациентов основной группы относительно базовых данных. Оно после терапии составило 11,9± 5,9%, что соответствовало диапазону нормальных показателей данного параметра (рис. 2).
При этом также существенно уменьшилось число пациентов с тяжелой степенью (более 30%) фрагментации ДНК. Если таковых до лечения было 39 (65%) человек, то после курса ГБО – 2 (3,3%) человека (табл. 2).
В контрольной группе пациентов при отсутствии курсов ГБО среднее значение уровня фрагментации ДНК сперматозоидов осталось практически на прежнем уровне и составило 31,7± 6,3% (рис. 3).
При анализе уровня фрагментации ДНК сперматозоидов у пациентов контрольной группы было отмечено достоверное увеличение доли пациентов с тяжелой степенью фрагментации ДНК (табл. 3).
При выполнении процедуры ЭКО через 3 месяца после курса терапии с помощью ГБО у пациентов основной группы и в эти же сроки у пациентов контрольной группы положительный результат (наступление беременности) достигнут у половых партнерш 63,3% (38/60) мужчин из основной группы и у 36,7% (11/30) – из контрольной группы. Статистический тест оценил данное различие между указанными группами пациентов как достоверное (рис. 4).
Такой результат следует расценивать, прежде всего, как следствие положительного влияния ГБО на степень фрагментации ДНК сперматозоидов, а не изменений традиционных параметров спермы. Хотя вышеуказанная положительная динамика традиционных параметров спермы носила достоверный характер, средние величины двух параметров (общее количество и подвижность сперматозоидов) оставались ниже границ нормальных значений. Медиана третьего параметра (число нормальных форм сперматозоидов) и до лечения находилась в пределах границ нормы. Эти данные свидетельствуют о том, что с точки зрения фертильных возможностей спермограмма в целом осталась на прежнем уровне. Следовательно, данные изменения основных параметров спермограммы не могли оказать значимое влияние на повышение вероятности беременности у половых партнерш. В отличие от традиционных параметров спермы, показатели уровня фрагментации ДНК сперматозоидов претерпели существенные изменения и после лечения в целом оказались в рамках нормальных значений. Это обстоятельство, безусловно, должно было оказать значительное влияние на фертильный потенциал мужчин. Анализ результатов ЭКО в зависимости от различных значений параметров спермы и уровня фрагментации ДНК сперматозоидов (в зависимости от градаций: показатель в норме или вне рамок нормы) подтвердил нашу точку зрения о возможной роли уровня фрагментации ДНК сперматозоидов на наступление беременности (табл. 4).
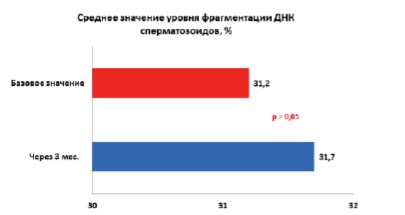
Рис. 3. Динамика уровня фрагментации ДНК сперматозоидов у пациентов контрольной группы
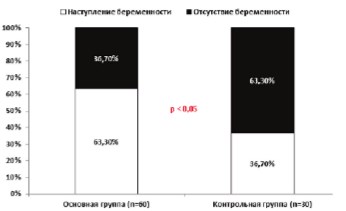
Рис. 4. Частота наступления беременности в результате ЭКО у половых партнерш пациентов основной и контрольной групп
Таблица 2. Уровень фрагментации ДНК сперматозоидов до и после курса ГБО у пациентов основной группы
| Уровень фрагментации ДНК сперматозоидов, % |
До курса ГБО | Через 3 мес. после ГБО | p | ||
|---|---|---|---|---|---|
| n | % | n | % | ||
| 0-15 | 0 | 0 | 55 | 91,7 | 0,005 |
| 16-30 | 21 | 35,0 | 3 | 5,0 | |
| > 30 | 39 | 65,0 | 2 | 3,3 | |
Таблица 3. Динамика уровня фрагментации ДНК сперматозоидов у пациентов контрольной группы за 3 месяца в отсутствии курса ГБО
| Уровень фрагментации ДНК сперматозоидов, % |
Базовое состояние | Через 3 мес. после ГБО | p | ||
|---|---|---|---|---|---|
| n | % | n | % | ||
| 16-30 | 12 | 40,0 | 9 | 30,0 | 0,021 |
| > 30 | 18 | 60,0 | 21 | 70,0 | |
На наш взгляд, причиной уменьшения степени фрагментации ДНК сперматозоидов после применения ГБО является снижение уровня активных форм кислорода в сперме, так как именно повышение концентрации последних в сперме служит одной из причин фрагментации ДНК.
В литературе представлены примеры положительного влияния ГБО на различные параметры спермы. Так, A. Mitrović и соавт. [17] сообщили об улучшении подвижности сперматозоидов после применения ГБО. В работе R.Q. Zheng и соавт. [18] продемонстрировано, что после варикоцелэктомии в сочетании с ГБО показатели качества спермы, пенетрационных способностей сперматозоидов и частоты наступления беременности у партнерш лучше, чем после варикоцелэктомии без ГБО. Однако, несмотря на положительный эффект ГБО на различные свойства спермы, опыт исследования взаимосвязи ГБО и фрагментации ДНК сперматозоидов в мире до сих пор не был описан. Поэтому наша работа открывает новое научное направление и должна стать толчком к продолжению аналогичных исследований, так как окончательные выводы об эффективности метода могут быть сделаны только на основании серии подобных работ.
Таблица 4. Результаты ЭКО в зависимости от показателей спермы у пациентов основной группы (указаны частота наступления беременности в % и число таких случаев от общего количества пациентов в виде дроби; анализ проведен по двум градациям: данный показатель спермы в норме или вне рамок нормы)
| Признак и его категории | Частота наступления беременности после одной процедуры ЭКО |
p |
|---|---|---|
| Общее количество сперматозоидов: | ||
| < 38*106 | 62,8% (27/43) | 0,079 |
| ≥ 39*106 | 64,7% (11/17) | |
| Подвижность (a+b) сперматозоидов: | ||
| < 40% | 63,3% (31/49) | 0,935 |
| ≥ 40% | 63,6% (7/11) | |
| Нормальные формы сперматозоидов: | ||
| < 4% | 58,3% (7/12) | 0,064 |
| < 4% | 64,6% (31/48) | |
| Фрагментация ДНК сперматозоидов: | ||
| ≤ 15% | 67,3% (37/55) | 0,001 |
| > 15% | 20,0% (1/5) |
ЗАКЛЮЧЕНИЕ
Уровень фрагментации ДНК сперматозоидов следует рассматривать как очень важный прогностический фактор, в значительной степени определяющий состояние мужской фертильности. Применение ГБО показало высокую эффективность в коррекции повышенного уровня фрагментации ДНК сперматозоидов. В результате лечения таких мужчин с помощью ГБО достоверно увеличивается вероятность наступления беременности у их половых партнерш после процедуры ЭКО. Полученные данные дают основание расценивать методику ГБО как перспективный способ лечения мужчин с идиопатическим бесплодием и, следовательно, рекомендовать ее к широкой клинической практике после проведения дальнейших исследований в этой области и комплексной оценки их результатов.
ЛИТЕРАТУРА
1. Корнеева И.Е. Общая концепция диагностики и классификации форм бесплодия. / Бесплодный брак: современные подходы к диагностике и лечению: руководство. 2-е изд., испр. и доп. [Под ред. Г.Т. Сухих, Т.А. Назаренко]. М.: ГЭОТАР-Медиа, 2010. С. 21-52.
2. Chandra A, Copen CE, Stephen EH. Infertility and impaired fecundity in the United States, 1982-2010: data from the National Survey of Family Growth. // Natl Health Stat Report. 2013. N 67. P. 1-18.
3. Jungwirth A, Diemer T, Dohle GR, Giwercman A, Kopa Z, Krausz C, Tournaye H. European Association of Urology Guidelines. Guidelines on male infertility. 2014 // URL: http://www.uroweb.org/gls/pdf/17%20Male%20Infertility_LR.pdf (Дата обращения: 10.02.2015 г.).
4. Богданов Ю.А., Карпунина Т.И., Зуева Т.В. К вопросу о распространенности мужского бесплодия. // Медицина и образование в Сибири. 2013. № 5. URL: http://ngmu.ru/cozo/mos/article/text_full.php?id=1135 (Дата обращения: 01.02.2015 г.).
5. Choy JT, Ellsworth P. Overview of current approaches to the evaluation and management of male infertility. // Urol Nurs. 2012. Vol. 32, N 6. P. 286-294.
6. Rouchou B. Consequences of infertility in developing countries. // Perspect Public Health. 2013. Vol. 133, N 3. P. 174-179.
7. Barazani Y, Katz BF, Nagler HM, Stember DS. Lifestyle, environment, and male reproductive health. // Urol Clin North Am. 2014. Vol. 41, N 1. P. 55-66.
8. Bachir BG, Jarvi K. Infectious, inflammatory, and immunologic conditions resulting in male infertility. // Urol Clin North Am. 2014. Vol. 41, N 1. P. 67-81.
9. Божедомов В.А., Рохликов И.М., Третьяков А.А., Липатова Н.А., Виноградов И.В., Никонов Е.Л. Актуальные вопросы оказания помощи парам с мужским фактором бездетного брака: клинические и организационно-методические аспекты. // Андрология и генитальная хирургия. 2013. № 4. С. 7-16.
10. Sabanegh EJ, Agarwal A. Male infertility. // Campbell-Walsh urology. 10th ed. [Eds., M.F. Campbell, P.C. Walsh, A.J. Wein]. Philadelphia: Saunders Elsevier, 2012. P. 616–647.
11. Muriel L, Garrido N, Fernández JL, Remohí J, Pellicer A, de los Santos MJ, Meseguer M. Value of the sperm deoxyribonucleic acid fragmentation level, as measured by the sperm chromatin dispersion test, in the outcome of in vitro fertilization and intracytoplasmic sperm injection. // Fertil. Steril. 2006. Vol. 85, N 2. P. 371-383.
12. Simon L, Brunborg G, Stevenson M, Lutton D, McManus J, Lewis SE. Clinical significance of sperm DNA damage in assisted reproduction outcome. // Hum. Reprod. 2010. Vol. 25, N 7. P. 1594-1608.
13. López G, Lafuente R, Checa MA, Carreras R, Brassesco M. Diagnostic value of sperm DNA fragmentation and sperm highmagnification for predicting outcome of assisted reproduction treatment. // Asian. J. Androl. 2013. Vol. 15, N 6. P. 790-794.
14. Wyrobek AJ, Eskenazi B, Young S, Arnheim N, Tiemann-Boege I, Jabs EW, Glaser RL, Pearson FS, Evenson D. Advancing age has differential effects on DNA damage, chromatin integrity, gene mutations, and aneuploidies in sperm. // Proc Natl Acad Sci USA. 2006. Vol. 103, N 25. P. 9601-9606.
15. Benchaib M, Lornage J, Mazoyer C, Lejeune H, Salle B, François Guerin J. Sperm deoxyribonucleic acid fragmentation as a prognostic indicator of assisted reproductive technology outcome. // Fertil. Steril. 2007. Vol. 87, N 1. P. 93-100.
16. World Health Organization. WHO laboratory manual for the examination and processing of human semen. Fifth ed. Geneva: WHO, 2010. 271 p.
17. Mitrović A, Brkić P, Jovanović T. The effects of hyperbaric oxygen treatment on vigility of spermatozoids: preliminary report. // Acta. Physiol Hung. 2011. Vol. 98, N 1. P. 85-90.
18. Zheng RQ, Wang XS, Wang PT. Effect of varicocelectomy with hyperbaric oxygenation in treating infertile patients with varicocele. // Zhonghua Nan Ke Xue. 2006. Vol. 12, N 1. P. 46-49.







