ВВЕДЕНИЕ
Выраженность симптомов нарушения функции нижних мочевых путей (СНМП) и снижение параметров мочеиспускания – ключевые показатели, характеризующие клиническую картину при доброкачественной гиперплазии предстательной железы (ДГПЖ) [1, 2]. Нередко при ДГПЖ обструктивные симптомы сочетаются с симптомами фазы накопления – поллакиурией, в том числе ночной, и ургентностью, что соответствует синдрому гиперактивного мочевого пузыря (ГМП). Самыми распространенными средствами лекарственной терапии, применяемыми в данной ситуации, являются α1-адреноблокаторы (α1-АБ) и Мхолинолитики (МХЛ).
Общей тенденцией клинических исследований α1-АБ и МХЛ у больных ДГПЖ и ГМП является оценка субъективного симптоматического эффекта и динамики показателя качества жизни [2]. В то же время, нами не найдено работ, в которых пациенты исходно были бы стратифицированы на группы в зависимости от урофлоуметрических показателей, объективно отражающих характер и степень нарушения мочеиспускания. Это представляет определенный научный и практический интерес, особенно с учетом возможного снижения сократимости мочевого пузыря под действием МХЛ и некоторого увеличения объема остаточной мочи, отмеченного в ряде исследований [3, 4].
Ранее было показано, что комбинация алфузозина и солифенацина демонстрирует высокую эффективность и безопасность у больных ДГПЖ в сочетании с ГМП, в том числе при выраженных симптомах нарушения функции нижних мочевых путей (СНМП), если исключить случаи инфравезикальной обструкции (ИВО) механического типа [5, 6]. Настоящее исследование призвано подтвердить эффективность и безопасность такой комбинированной терапии у пациентов с выраженными нарушениями мочеиспускания по данным урофлоуметрии (УФМ).
МАТЕРИАЛЫ И МЕТОДЫ
В наблюдательное мультицентровое исследование «АВИАТОР» – «Оценка влияния комбинированной терапии α1-адреноблокатором (алфузозин, Алфупрост® МР, 10 мг, один раз в сутки) и средством с антимускариновой активностью (солифенацин, Везигамп, 5 мг, один раз в сутки) на выраженность СНМП у амбулаторных пациентов с ДГПЖ и ГМП со средней и тяжелой симптоматикой», проведенное в 2022 – 2023 гг., было включено 208 мужчин старше 50 лет. В исследовании, приближенном к реальной клинической практике, приняли участие 15 специалистов из 8 медицинских учреждений Москвы, Санкт-Петербурга, Нижнего Новгорода, Ростова-на-Дону и Челябинска.
На этапе включения в исследование все пациенты прошли стандартизированное обследование, включавшее: сбор анамнеза; физикальный осмотр; пальцевое ректальное исследование; оценку симптомов по опросникам (IPSS – International Prostate Symptom Score, QoL – Quality of Life, OABSS – Overactive Bladder Symptom Score, PPIUSPatient Perception of Intensity of Urgency Scale); лабораторные исследования (общий анализ мочи, определение уровня простатспецифического антигена – ПСА, общий анализ крови, измерение концентрации креатинина и глюкозы в крови); ультразвуковое исследование (УЗИ) почек, мочевого пузыря, предстательной железы – ПЖ (объем, величина внутрипузырной протрузии – ВВП); УФМ (максимальная скорость потока мочи – Qmax, средняя скорость мочеиспускания – Qave, объем мочеиспускания – VV); определенный объем остаточной мочи (PVR) ультразвуковым методом.
Для оценки симптомов, не вошедших в стандартные опросники, была разработана оригинальная анкета, а для учета формы УФМ-кривых, что играет важную диагностическую роль, – шаблон с графическим изображением их основных типов: нормальный; обструктивный пологий; обструктивный платообразный; нерегулярный (неправильный); башенный (стремительный); прерывистый. Соответствие реальной формы УФМ-кривой шаблону определял врач.
В наблюдательное исследование включали мужчин с диагнозом ДГПЖ, объемом ПЖ по данным УЗИ более 30 см3 и величиной внутрипузырной протрузии (ВПП) менее 10 мм, наличием симптомов расстройства мочеиспускания умеренной и значительной степеней выраженности (≥ 8 баллов по IPSS), Qmax при УФМ ≥7 мл/с и < 15 мл/с, объемом остаточной мочи ≤ 150 мл, уровнем ПСА < 4 нг/мл, по опроснику QoL > 3 баллов. Критерием включения в исследование также было наличие жалоб на учащенное мочеиспускание ≥ 8 раз в сутки и императивные позывы к мочеиспусканию ≥ 2 за сутки в течение 3-х и более месяцев. Все пациенты подписали информированное согласие на участие в исследовании и обработку деперсонифицированных данных, протокол и другие документы исследования были утверждены локальным этическим комитетом НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина.
В исследование не включали пациентов с предшествующей терапией в течение 6 месяцев любым α1-АБ, MХЛ, антагонистом β3рецепторов, ингибитором 5α-редуктазы, ингибитором фосфодиэстеразы 5 типа, препаратами на основе растительных экстрактов, применяемыми для лечения расстройств мочеиспускания и мочегонными средствами. В наблюдательную программу не вошли пациенты: с абсолютными показаниями к оперативному лечению ДГПЖ (повторяющаяся после удаления катетера или рецидивирующая острая задержка мочеиспускания, парадоксальная ишурия, устойчивая к терапии макрогематурия, двухсторонний уретерогидронефроз c почечной недостаточностью или без нее, камни и дивертикулы мочевого пузыря); с хронической мочевой инфекцией; с внутрипузырной протрузией предстательной железы ≥10 мм, определенной при УЗИ, а также пациенты, не способные по своему состоянию обеспечить регулярный прием исследуемых препаратов и/или посещать врача в указанное время.
За два дня до включения в исследование пациенты должны были начать прием препаратов: алфузозин (Алфупрост® МР) 10 мг/сут. и солифенацин (Везигамп) 5 мг/сут в строгом соответствии с действующими инструкциями по медицинскому применению.
Контрольные обследования, включавшие оценку жалоб, заполнение опросников IPSS, QoL, OABSS, PPIUS, выполнение УФМ с определением объема остаточной мочи, как и мониторинг нежелательных явлений (НЯ) и контроль терапии, проводили на визитах V1 и V2: через один и три месяца лечения. Анализ приверженности и удовлетворенности лечением пациентов и врачей осуществили с использованием стандартизированной шкалы Лайкерта.
Клинически значимую эффективность оценивали по следующим критериям: уменьшение общего показателя IPSS на 25%; на 50%; на 75% и/или > 3 баллов; увеличение Qmax более, чем на 30%.
Исследование по подгруппам
Цель настоящего ретроспективного подгруппового анализа стала сравнительная оценка влияния комбинированной терапии алфузозином (Алфупрост® МР, 10 мг, один раз в сутки) и солифенацином (Везигамп, 5 мг, одни раз в сутки) на выраженность СНМП и объективных показателей мочеиспускания у пациентов с ДГПЖ и ГМП со средней и тяжелой выраженностью нарушений мочеиспускания по данным УФМ.
Задачи исследования:
- оценка влияния комбинированного применения препаратов через один и три месяца терапии на СНМП по изменению баллов шкалы IPSS, других специализированных анкет, анкеты качества жизни QoL и УФМ показателей;
- оценка у больных частоты и тяжести нежелательных реакций и связанных с ними отказов от лечения (комплаентность).
Для этого общую группу пациентов разделили на две подгруппы, в зависимости от показателя Qmax: Подгруппа 1 (ПГ1) – c выраженным снижением потока мочи, Qmax < 12 мл/с (n=102); Подгруппа 2 (ПГ2) – с умеренными/незначительными нарушениями, Qmax ≥ 12 мл/с (n=106).
Статистический анализ
Для обработки полученных результатов были применены методы описательной статистики. Количественные данные представлены центральными тенденциями и рассеянием: среднее арифметическое (M) и стандартное отклонения (SD) в формате М (SD). При распределении признаков, отличающемся от нормального, их описывали в виде медианы (Me) и квартилей Q1 и Q3 в формате Me (Q1; Q3). Величину порогового уровня значимости р принимали равной 0,05. Статистически значимыми считали различия при p<0,05.
Частотный анализ и расчет процентной доли встречаемости признака применяли для качественных данных. Проверку выборок на нормальность осуществляли при помощи теста Колмогорова-Смирнова. U-критерий Манна-Уитни и Т-Стьюдента использовали для сравнения независимых выборок. Взаимосвязь параметров определяли с использованием метода корреляционного анализа Спирмена. Непараметрический критерий Хи-квадрат с поправкой Йеитса был использован для установления различия частот признаков в независимых группах. Математическую и статистическую обработку полученных данных проводили с использованием стандартных пакетов программ Statistica (V7.0) и SPSS Statistics (V17.0).
РЕЗУЛЬТАТЫ
Мужчины ПГ1 и ПГ2 достоверно не отличались по среднему возрасту (60,2 и 61,3 лет), росту (177,1 и 177,3 см), весу (85,1 и 86,8 кг), индексу массы тела (27,1 и 27,5), структуре и частоте сопутствующих заболеваний. Однако зарегистрированы значимые различия по ряду основных клинических характеристик, в том числе по объему ПЖ: 52,1+13,3 и 47,7+10,3 см3 (p=0,014). Также статистически достоверно отличались показатели общего балла IPSS и симптомов фазы опорожнения, общий балл OABSS и урофлоуметрические показатели: Qmax, Qave, VV, PVR. Не выявлено значимых различий по показателям, отражающим проявления гиперактивности мочевого пузыря и ургентности: симптомы фазы накопления по IPSS; ноктурия; QoL; частота ургентных позывов и недержания мочи по OABSS; балл опросника PPIUS (табл. 1).
В результате лечения у подавляющего числа пациентов обеих групп достигнут статистически достоверный и выраженный эффект по большинству субъективных и объективных клинических показателей, который был зарегистрирован уже через месяц после начала приема препаратов и усилился к 3-му месяцу наблюдения.
Влияние на СНМП
В результате лечения доля пациентов, предъявляющих какие-либо жалобы, снизилась в ПГ1 и ПГ2: через месяц – до 93,1% и 93,4%, а через три месяца – до 71,6% и 67,0% соответственно. В частности, процент мужчин, исходно отмечавших тяжесть/боль над лоном, уменьшился в ПГ1 с 8,8% до 1,0%, в ПГ2 – с 5,7% до 0,9%, а жаловавшихся на дискомфорт/боль при мочеиспускании – с 7,8% и 5,7% до 0,0.
Шкала IPSS/QoL. Исходно общая выраженность СНМП по IPSS, как и сумма баллов фазы опорожнения (IPSS-v) в ПГ1 были достоверно (p=0,001) выше, чем в ПГ2, при отсутствии различий (p=0,178) по симптомам фазы накопления (IPSS-s), в том числе ноктурии. Через один и три месяца наблюдения и в ПГ1 и ПГ2 выявлено статистически значимое (p=0,001) улучшение, соответственно: общего показателя IPSS на 45,2% и 70,5% против 46,0% и 74,3%; симптомов фазы накопления на 42,7% и 70,1% против 47,2% и 74,7%; симптомов фазы опорожнения на 45,8% и 70,0% против 44,8% и 74,0%; показателя QoL на 43,7% и 81,2% против 54,2% и 81,2% (табл. 1, рис. 1). Обращает на себя внимание более выраженная динамика показателей IPSS у пациентов ПГ2, по сравнению с ПГ1, при их достоверной разнице и через один, и через три месяца.
Таблица 1. Динамика основных клинических показателей в подгруппах на визитах 1-3
Table 1. Dynamics of the main clinical indicators in subgroups at visits 1-3
| Показатели Indicators | Подгруппа 1 (n = 102) Subgroup 1 (n = 102) | Подгруппа 2 (n = 106) Subgroup 2 (n = 106) | p | |
|---|---|---|---|---|
| IPSS, баллы IPSS, points | Исходно | 21,7 (±4,2) | 18,7 (±5,1) | 0,001 |
| 1 месяц | 11,9 (±4,0) | 10,1 (±3,7) | 0,001 | |
| 3 месяца | 6,4 (±3,9) | 4,8 (±2,5) | 0,004 | |
| IPSS накопления, баллы IPSS storage, points | Исходно | 9,6 (±2,1) | 9,1 (±2,1) | 0,187 |
| 1 месяц | 5,5 (±1,7) | 4,8 (±1,5) | 0,010 | |
| 3 месяца | 2,8 (±1,7) | 2,3 (±1,2) | 0,018 | |
| IPSS опорожнения, баллы IPSS (voiding), points | Исходно | 12,0 (±3,4) | 9,6 (±4,5) | 0,000 |
| 1 месяц | 6,5(±2,8) | 5,3 (±2,9) | 0,013 | |
| 3 месяца | 3,6(±2,5) | 2,5 (±1,8) | 0,005 | |
| IPSS ноктурия, баллы IPSS (nocturia), points | Исходно | 2,9 (±0,9) | 2,7 (±1,0) | 0,328 |
| 1 месяц | 1,6 (±0,7) | 1,4 (±0,8) | 0,151 | |
| 3 месяца | 0,8 (±0,6) | 0,8 (±0,7) | 0,421 | |
| QoL, баллы QoL, points | Исходно | 4,8 (±0,5) | 4,8 (±0,5) | 0,996 |
| 1 месяц | 2,7 (±1,1) | 2,2 (±0,9) | 0,001 | |
| 3 месяца | 0,9 (±0,9) | 0,9 (±0,8) | 0,928 | |
| OABSS, баллы OABSS, points | Исходно | 10,9 (±2,5) | 10,1 (±2,3) | 0,022 |
| 1 месяц | 5,6 (±3,0) | 4,7 (±2,4) | 0,040 | |
| 3 месяца | 2,3 (±2,1) | 1,8 (±1,6) | 0,214 | |
| PPIUS, баллы PPIUS, points | Исходно | 2,6 (±0,7) | 2,4 (±0,6) | 0,299 |
| 1 месяц | 1,3 (±0,7) | 1,1 (±0,6) | 0,172 | |
| 3 месяца | 0,4 (±0,5) | 0,3 (±0,4) | 0,066 | |
| Qmax, мл/с Qmax, ml/s | Исходно | 9,7 (±1,3) | 13,2 (±1,0) | 0,001 |
| 1 месяц | 13,8 (±3,9) | 16,6 (±5,2) | 0,001 | |
| 3 месяца | 16,9 (±5,4) | 18,1 (±4,6) | 0,001 | |
| Qave, мл/с Qave, ml/s | Исходно | 5,8 (±1,0) | 7,3 (±1,6) | 0,001 |
| 1 месяц | 7,6 (±2,4) | 8,8 (±2,8) | 0,001 | |
| 3 месяца | 8,7 (±2,4) | 9,4 (±2,4) | 0,021 | |
| Объем мочеиспускания, мл Voided volume, ml | Исходно | 195,4 (±49,8) | 212,4 (±51,8) | 0,017 |
| 1 месяц | 203,1 (±41,6) | 223,0 (±45,2) | 0,001 | |
| 3 месяца | 214,9 (±43,9) | 219,8 (±50,7) | 0,496 | |
| Остаточная моча, мл PVR, ml | Исходно | 56,6 (±35,1) | 43,0 (±34,4) | 0,001 |
| 1 месяц | 27,8 (±23,6) | 22,4 (±22,8) | 0,061 | |
| 3 месяца | 13,1 (±15.8) | 11,1 (±16,6) | 0,049 | |
* различия между подгруппами статистически достоверны при p<0,05
* differences between subgroups are statistically significant at p<0.05
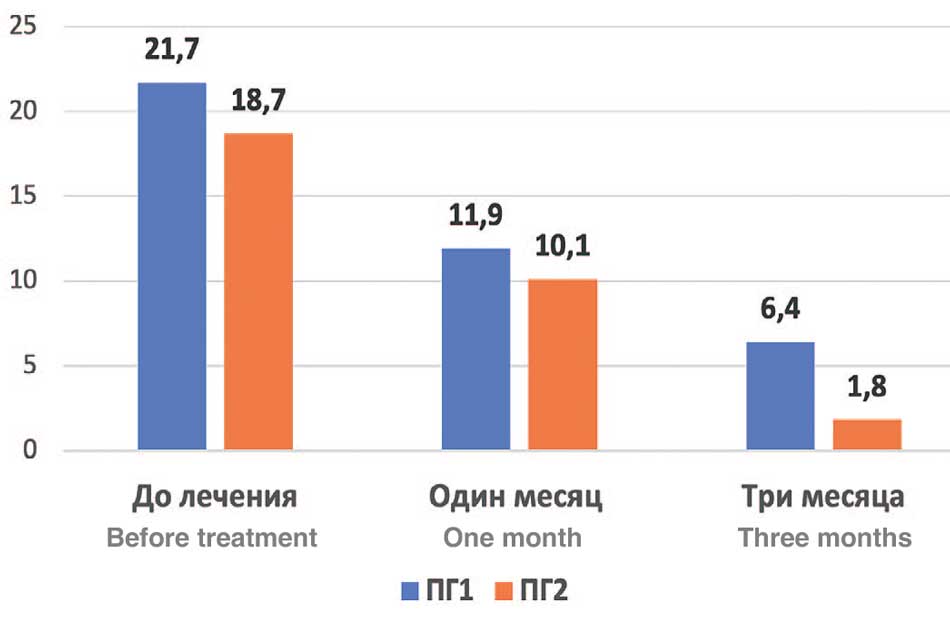
Рис. 1. Сравнительная динамика симптомов по шкале IPSS между ПГ1 и ПГ2 на визитах 1-3
Fig. 1. Comparative dynamics of symptoms according to the IPSS scale between PG1 and PG2 at visits 1-3
Средний показатель ноктурии по шкале IPSS исходно статистически не различался (p=0,328). В последующие месяцы он достоверно (p=0,001) снизился на 44,8% и 72,4% в ПГ1 против 48,2% и 70,4% в ПГ2, без различий между подгруппами в течение всего исследования. Значения QoL в начале программы также были очень близки (p=0,996), статистически значимо (p=0,001) улучшились по ее результатам, но без статистических различий между подгруппами на каждом этапе исследования (табл. 1).
Шкалы OABSS и PPIUS. Симптомы ГМП по шкале OABSS исходно у пациентов ПГ1 были представлены достоверно (p=0,022) выше. Интересно, что исходные различия между подгруппами были достоверными только по частоте мочеиспусканий (p =0,009), тогда как показатели ноктурии (p=0,439), повелительных позывов (p=0,177) и императивного недержания мочи (p=0,082) не достигли статистической значимости. В течение срока лечения отмечено последовательное достоверное (p=0,001) снижение общего балла OABSS на 48,6% и 78,9%, против 53,5% и 82,0%, соответственно, причем к трем месяцам различий между показателями не наблюдали (p=0,214).
Проявления ургентности по шкале PPIUS в начале исследования не различались (p=0,299). В ходе лечения в обеих подгруппах также зарегистрировано высокозначимое (p=0,001) уменьшение симптомов через один и три месяца соответственно, на 50,0% и 84,6% против 54,2% и 87,5%, без достоверных отличий между ними (табл. 1).
Влияние на объективные показатели мочеиспускания
Согласно идее исследования и порядку формирования подгрупп, они исходно различались по основным объективным параметрам: Qmax (p=0,001); Qave (p=0,001); объему мочеиспускания (p=0,017) и остаточной мочи (p=0,001). В результате комбинированной терапии отмечено достоверное (p=0,001) улучшение всех показателей у пациентов ПГ1 и ПГ2 через один и три месяца, соответственно: Qmax – на 42,3% и 74,2% против 25,8% и 37,1%; Qave – на 31,0% и 50,0% против 20,5% и 28,8% (табл. 1, рис. 2).
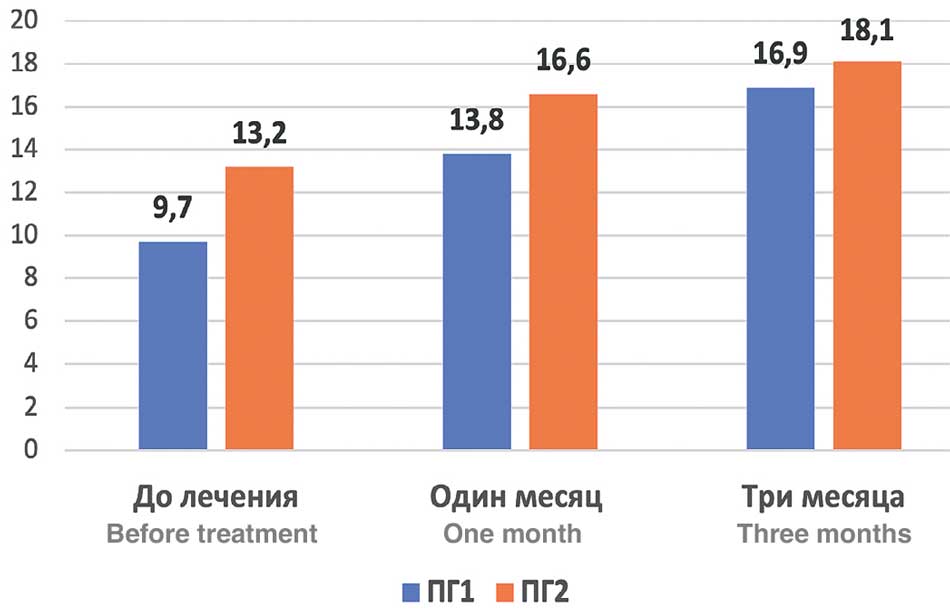
Рис. 2. Сравнительная динамика Qmax между ПГ1 и ПГ2 на визитах 1-3
Fig. 2. Comparative dynamics of Qmax between PG1 and PG2 at visits 1-3
Объем мочеиспускания значимо (p=0,037; p=0,001) увеличился в ПГ1 на 3,4% и 10,0% против изменения на грани статистических различий на 5,0% и 3,5% в ПГ2 (p=0,019; p=0,223). К третьему месяцу наблюдения статистические различия между подгруппами по этому показателю исчезли (p=0,496).
Важным фактором, связанным с безопасностью лечения, является объем остаточной мочи. Исходно этот параметр достоверно различался между группами (p=0,001). В ходе лечения он высокодостоверно (p <0,001) снизился через один и три месяца и в ПГ1 и в ПГ2, соответственно: на 50,9% и 76,8% против 47,9% и 74,2%. Различия между подгруппами оказались на грани статистической значимости (p=0,061; p=0,049). Форма УФМ кривой – важный комплексный визуальный критерий оценки результатов урофлоуметрии. Показательно, что если до начала лечения у большинства пациентов наблюдали обструктивные и нерегулярный типы кривых, а в ПГ1 нормальный тип кривой отсутствовал вовсе, то через три месяца комбинированного лечения 36,3% мужчин в ПГ1 и 51,9% – в ПГ2 демонстрировали нормальную форму кривой, что свидетельствует у них о нормализации мочеиспускания (табл. 2).
Таблица 2. Распределение типов УФМ кривых (%) в подгруппах на визитах 1 и 3
Table 2. Distribution of UFM curve types (%) in subgroups at visits 1 and 3
| Показатели Indicators | Подгруппа 1 Subgroup 1 | Подгруппа 2 Subgroup 2 | ||
|---|---|---|---|---|
| До лечения Before treatment | 3 месяца After 3 months | До лечения Before treatment | 3 месяца After 3 months | |
| Нормальный Normal | 0 | 36,3 | 10,4 | 51,9 |
| Обструктивный пологий Obstructive gentle curve | 30,4 | 39,2 | 45,3 | 36,8 |
| Обструктивный платообразный Obstructive plateau | 32,3 | 16,7 | 20,8 | 1,9 |
| Нерегулярный (неправильный) Irregular (irregular) | 29,4 | 6,8 | 17,9 | 9,4 |
| Башенный (стремительный) Tower-shaped (rapid) | 1,0 | 0 | 0,9 | 0 |
| Прерывистый Intermittent | 6,9 | 1,0 | 4,7 | 0 |
Клинически значимый ответ
Клинически значимый ответ – это изменение состояния пациента, которое является не просто статистически значимым, но ощутимым и важным и для пациента, и для врача. Достижение клиническизначимого ответа при лекарственной терапии ДГПЖ имеет принципиальное значение, как с клинической, так и с медико-экономической точек зрения. Считают, что экономически целесообразными являются именно те подходы, где достигается клиническизначимый результат. Критерии такого ответа при лечении ДГПЖ – это комплекс объективных и субъективных показателей, свидетельствующих об эффективности лечения. Они применены в ряде работ и обобщенно могут быть сгруппированы по следующим категориям:
- улучшение симптоматики по валидированному опроснику IPSS:
- снижение на ≥ 3 балла или ≥ 25-30%;
- переход в более легкую категорию симптомов;
- улучшение объективных уродинамических показателей:
- улучшение Qmax на ≥ 30% от исходного значения;
- в абсолютных цифрах – увеличение на ≥ 3-4 мл/с;
- нормализация показателя до >15 мл/с;
- остаточная моча (PVR – Post-Void Residual Urine Volume):
- снижение объема остаточной мочи на ≥ 30-50%;
- снижение значительного объема до 50-70 мл;
- полное исчезновение остаточной мочи;
- качество жизни QoL:
- улучшение ≥ 1 балла.
В настоящем исследовании уменьшение общего балла IPSS > 25% в ПГ1 и ПГ2 через один и три месяца комбинированной терапии наблюдали у 87,2% и 90,6%, а через три месяца – у 98,0% и 100,0%. Улучшение IPSS > 50% к V1 имело место у 39,2% и 44,3%, а к V2 – у 86,3% и 97,2%. Показательно, что если снижение IPSS >75% через месяц отметили всего у 2,9% и 1,9%, то к трем месяцам их доля возросла до 46,1% и 46,2%, соответственно. Улучшение IPSS > 3 баллов в обеих подгруппах продемонстрировали 100% участников программы. Доля пациентов ПГ1 и ПГ2, у которых зарегистрировали увеличение Qmax > 30%, составила: на визите V1 55,9% и 15,1%, а на визите V2 – 92,2% и 50,0% соответственно. Такое различие между подгруппами, вероятно, обусловлено разной «стартовой базой», а также достижением, в среднем, нормальных показателей Qmax в ПГ2 уже через один месяц лечения (табл. 1). Таким образом, подавляющее число пациентов обеих подгрупп достигли клинически значимого ответа по ведущим клиническим показателям.
Безопасность и удовлетворенность лечением
Комбинированное лечение, как было показано ранее, продемонстрировало высокий уровень безопасности: в течение 3-х месяцев лечения было зарегистрировано всего 3 НЯ у двух (1,0%) пациентов: сухость во рту – 2 (1,0%), ретроградная эякуляция – 1 (0,5%). Пациенты не прервали лечения из-за развития нежелательных явлений. Эпизодов задержки мочеиспускания не было.
Анкетирование пациентов и врачей с использованием шкалы Лайкерта подтвердило их высокую удовлетворенность результатами комбинированного лечения и его хорошую переносимость [5].
ОБСУЖДЕНИЕ
Уникальными отличительными особенностями настоящего наблюдательного исследования являются:
- использование комбинации алфузозина и солифенацина у больных ДГПЖ и ГМП с умеренными и выраженными симптомами;
- исключение из программы пациентов с внутрипузырной простатической протрузией ≥ 10 мм, то есть имевших выраженную ИВО механического типа, что является неблагоприятным прогностическим фактором эффективности лекарственной терапии;
- комплексная оценка динамики симптомов с использованием пакета валидизированных анкет (IPSS/QoL, OABSS, PPIUS);
- исходная стратификация подгрупп пациентов по показателю Qmax;
- оценка изменений характера мочеиспускания не только по цифровым показателям, но и по форме УФМ кривой;
- оценка эффективности лечения по достижению «клинически значимого ответа».
Подавляющее большинство исследований лекарственной терапии СНМП/ДГПЖ фокусируются на достижении симптоматического эффекта и улучшении качества жизни пациентов. Однако объективные показатели мочеиспускания не менее важны при комплексной оценке результативности лечения и, наряду с оценкой симптомов по шкале IPSS и качества жизни QoL, учитываются в большинстве исследований [2]. Однако нами не найдено работ, где бы пациентов исходно стратифицировали по объективным параметрам мочеиспускания.
Важнейшим УФМ критерием является Qmax – максимальная объемная скорость мочеиспускания. Значения Qmax превышающие 15 мл/сек для пациентов с ДГПЖ считают нормальными, уменьшение до 10-15 мл/сек расценивают, как умеренное нарушение, а ниже 10 мл/сек – как значительное. Снижение Qmax у больных СНМП/ДГПЖ чаще ассоциируют с ИВО, реже – с гипотонией детрузора, в том числе вторичной природы. Однако только по результатам УФМ невозможно достоверно судить о наличии или отсутствии ИВО: необходимо выполнить комбинированное уродинамическое исследование с расчетом показателей «давление/поток». Особенно это касается группы пациентов с Qmax 10-15 мл/сек, где число больных с ИВО и без таковой разделилось примерно поровну [7]. Диагностическая ценность УФМ в выявлении ИВО значительно варьирует и в большой степени зависит от выбранных пороговых показателей. При пороге Qmax=10 мл/с специфичность критерия в отношении ИВО составляет 70%, положительная прогностическая ценность – 70%, а чувствительность – 47%. При пороговом значении Qmax=15 мл/с специфичность равна 38%, чувствительность – 82%, а положительная прогностическая ценность – 67% [8]. Более поздний систематический обзор приводит близкие значения для критерия Qmax=10 мл/с при диагностике ИВО: чувствительность – 68,3%; специфичность – 70,5%; позитивная прогностическая значимость – 74,3% и негативная прогностическая ценность – 68,0% [9].
В описываемое исследование были отобраны пациенты и с умеренными и тяжелыми симптомами по шкале IPSS (8 и более баллов) и показателем Qmax в диапазоне от 7 до 15 мл/с. Пациенты были стратифицированы в зависимости от величины Qmax на подгруппы с выраженными (ПГ1) и умеренными нарушениями мочеиспускания (ПГ2). Показательно, что исходно средние значения общего показателя IPSS в обеих подгруппах находились в зоне выраженных изменений (21,7 и 18,7 баллов). При этом, снижение среднего показателя Qmax в ПГ1 было расценено, как значительное (9,7 мл/с), а в ПГ2 – как умеренное (13,2 мл/с).
Ожидаемо, подгруппы исходно достоверно отличались по среднему баллу IPSS симптомов фазы опорожнения. Значимые различия показателей по мере их улучшения сохранились на всех этапах исследования, достигнув к трем месяцам 70,1% и 74,7% в ПГ1 и ПГ2. Напротив, выраженность симптомов фазы накопления в начале программы между подгруппами не различалась (p>0,05), как и выраженность отдельных симптомов, что говорит об отсутствии четкой взаимосвязи между ними и Qmax в ситуации отсутствия явной механической ИВО. В дальнейшем, по мере улучшения Qmax на фоне лечения наблюдали появление достоверных различий между величиной общего балла IPSS-s и выраженности отдельных симптомов в подгруппах, кроме ноктурии. Несмотря на снижение других показателей, различий между подгруппами по выраженности ноктурии не удалось достигнуть в течение всего исследования (табл. 1).
Интересно, что при этом исходно были отмечены достоверные различия по величине общих баллов шкалы гиперактивности OABSS (p<0,05) за счет большей частоты мочеиспусканий у пациентов ПГ1, тогда как остальные показатели характеризующие ургентность, как и общий балл PPIUS статистически не различались (p>0,05). На фоне лечения наблюдали последовательное и достоверное снижение всех этих показателей, но без достижения статистической разницы между подгруппами (p>0,05).
Принципиальной инновацией настоящего исследования является исключение из него пациентов с ВПП ≥ 10 мм. Этот подход обусловлен данными о жесткой связи величины ВПП и ИВО механического типа. Серией исследований продемонстрировано, что величина ВПП является высокодостоверным предиктором ИВО при ДГПЖ, превосходящим другие неинвазивные критерии, включая объем ПЖ [10-15]. Значение ВПП в 10 мм общепринято в качестве пограничного критерия, поскольку оно обладает хорошей чувствительностью в отношении наличия ИВО [12, 16]. Важно, что пациенты с СНМП/ДГПЖ и ВПП выше 10 мм, по-видимому, чаще плохо реагируют на медикаментозное лечение тамсулозином [17]. Было показано, что конфигурация ПЖ, наличие средней доли и степень ВПП влияют на ИВО в большей степени, чем собственно размер ДГПЖ. Чрезмерная протрузия ПЖ в мочевой пузырь вызывает большую обструкцию из-за деформации и сдавления области шейки мочевого пузыря, чем гиперплазия боковых долей, которые вызывают ИВО только при большом увеличении [18-20].
L.S. Lee и соавт. исследовали показатель ВПП, как предиктор клинической прогрессии ДГПЖ. Они наблюдали 259 пациентов с ДГПЖ на протяжении, в среднем, 32 месяцев. Прогрессирование заболевания определяли как ухудшение IPSS на 4 балла и более, увеличение объема остаточной мочи > 100 мл или возникновение острой задержки мочеиспускания (ОЗМ). В группе исследуемых прогрессирование заболевания произошло у 7% при ВПП < 5 мм и у 49% при ВПП > 10 мм. Авторы пришли к выводу, что ВПП является важным неинвазивным предиктором клинического прогрессирования СНМП/ДГПЖ [21].
Некоторые авторы справедливо считают, что степень ИВО, наряду с выраженностью симптомов, является определяющим фактором при выборе метода лечения больных СНМП/ДГПЖ. Еще в 2004 г. при определении тактики ведения этих больных мы предложили классифицировать их на 11 подгрупп, в зависимости от наличия осложнений и/или неблагоприятных факторов прогноза, выраженности симптомов по IPSS и величины Qmax. После исключения пациентов с осложнениями ДГПЖ и признаками механической ИВО, были определены подгруппы, где можно ожидать высокую эффективность различных методов лекарственной терапии, в том числе комбинации α1-А Б и МХЛ [22, 23]. K.T. Foo и соавт. предложили классифицировать клинические проявления ДГПЖ на 4 стадии, в зависимости от выраженности ИВО и СНМП. Пациентам со стадией II, у которых нет существенной обструкции, но присутствуют беспокоящие симптомы, рекомендована лекарственная терапия [20].
Известно, что значительная часть пациентов с СНМП/ДГПЖ не реагирует на лечение первой линии α1-АБ. В многочисленных исследованиях рассматривали предикторы неэффективности медикаментозной терапии с использованием неинвазивных тестов: ВПП, простато-уретральный угол (PUA), неинвазивные уродинамические параметры, объем остаточной мочи, толщина стенки мочевого пузыря, выраженность симптомов по IPSS и т.д. [9, 15, 24, 25]. Было показано, что величина ВПП непосредственно влияет на результаты лекарственной терапии ДГПЖ.
H.Y. Park и соавт. продемонстрировали, с одной стороны, прямую корреляцию величины ВПП с объемом ПЖ, длиной простатической уретры, ПСА, Qmax и объемом остаточной мочи (p< 0,05), но не c баллом по IPSS, а с другой – неэффективность терапии α1-АБ тамсулозином при ВПП > 10 мм [26]. Другие группы исследователей также подтвердили низкую результативность применения тамсулозина у больных ДГПЖ и ВПП >10 мм [17,27]. L. Topazio и соавт. установили, что лечение тамсулозином было успешным у 38,5% больных с ВПП 5-10 мм и лишь у 7,1% – при ВПП > 10 мм. С помощью многофакторной регрессии выявили зависимость между степенью ВПП и успехом лечения СНМП/ДГПЖ. Показатели УФМ и симптомы наиболее значимо улучшились у пациентов с низкой величиной ВПП. Объем ПЖ, повидимому, не влиял на эту взаимосвязь. Авторы подтвердили, что ВПП в значительной степени обратно коррелирует с успехом лечения СНМП/ДГПЖ у пациентов получающих терапию α1-АБ [28]. В исследовании K. Hirayama и соавт. у 21% пациентов ДГПЖ комбинированная терапия α1-АБ и дутастеридом оказалась неэффективной, что потребовало оперативного лечения. При последующем анализе оказалось, что при отсутствии статистических различий по объему ПЖ у пациентов, не ответивших на лечение, величина ВПП была достоверно выше. Этот критерий стал самым значимым прогностическим фактором перехода от лекарственной терапии к хирургическому вмешательству (AUC 0,9): для ВПП = 8 мм чувствительность составила 91% при специфичности – 72% [29]. Именно поэтому, с учетом имеющихся фактов и клинического опыта, ряд авторов указывают, что пациенты с ВПП > 10 мм нуждаются в более агрессивной стратегии ведения – оперативному лечению ДГПЖ [22, 23, 25].
Исключение из наблюдательной программы
«АВИАТОР» пациентов с ВВП ≥ 10 мм, наряду с использованной комбинацией препаратов, позволило добиться впечатляющего симптоматического эффекта и улучшения уродинамических показателей, как в общей группе, так и у пациентов с выраженными СНМП [5, 6]. В настоящем исследовании у пациентов с умеренными и выраженными нарушениями мочеиспускания, определенными по показателю Qmax, применение комбинации алфузозина и солифенацина в течение трех месяцев также привело к высокодостоверному снижению симптомов по шкале IPSS на 74,3% и 70,5% и увеличению Qmax на 37,1% и 74,2%, соответственно, что является уникальным для других подобных наблюдений. Показательно, что к концу 3х-месячного периода лечения, средние значения общего балла IPSS у пациентов обеих групп расценили, как слабо выраженные, а показатели Qmax, как соответствующие возрастной норме.
Некоторые исследователи считают среднюю скорость мочеиспускания Qave, а не Qmax, УФМ-параметром, тесно связанным с СНМП, ГМП и качеством жизни у пожилых мужчин [30]. Показано, что увеличение продолжительности сокращения детрузора, связано с ухудшением симптомов. И если Qmax условно отражает максимальную производительность детрузора в момент мочеиспускания, то Qave – условно работу детрузора во времени. Показатель Qmax широко используют в клинической практике при диагностике функции мочеиспускания у больных ДГПЖ, однако по мнению ряда авторов, критерий Qave также следует учитывать при оценке результатов лечения [31, 32]. В настоящем исследовании показатель Qave мы учитывали, как дополнительный критерий, демонстрирующий общую эффективность лечения. Исходно и на всех этапах наблюдения он достоверно отличался между подгруппами. Его высокодостоверное увеличение через один и три месяца составило 31,0% и 50,0% в ПГ1 против 20,5% и 28,8% в ПГ2 соответственно (табл. 1).
Доподлинно известна связь ИВО и ГМП у больных ДГПЖ [33]. Однако вопрос о связи ВПП и ГМП остается открытым. K.H. Kim и Y.S. Kim при анализе группы больных ДГПЖ с использованием метода множественного линейного регрессионного анализа выявили статистически достоверную зависимость выраженности ВПП и симптомов ГМП по шкале IPSS (4-й вопрос > 2 баллов) и частоты ОЗМ [34]. Позже, Y. Matsukawa и соавт. уродинамически установили, что величина ВПП является действенным предиктором наличия детрузорной гиперактивности у мужчин с СНМП [35]. При этом, C.H. Tsai и соавт. в ходе открытого проспективного исследования не смогли подтвердить прогностическую ценность ВПП в отношении ГМП, но доказали связь ВПП > 10 мм с более высокой частотой ночных мочеиспусканий [36]. Тем не менее, можно с достаточной уверенностью заявить, что исключение из исследования пациентов с ВПП > 10 мм вследствие снижения вероятности механической ИВО, привело и к уменьшению проявлений ГМП, ассоциированной с такой обструкцией. То есть, в программе остались пациенты с ИВО, преимущественно функционального типа и гиперактивностью, не связанной с обструкцией механического типа.
Менее изученным является вопрос о влиянии первичного ГМП на ИВО. У пациентов в нашем исследовании были умеренные или выраженные нарушения мочеиспускания, проявлявшиеся соответствующим снижением Qmax. То есть, присутствовала ИВО преимущественно функционального типа в сочетании с ГМП. И хотя сама ГМП не создает анатомического препятствия оттоку мочи, она может содействовать функциональным нарушениям, которые имитируют или усугубляют симптомы обструкции, особенно при их совместном существовании. При сильном ургентном (повелительном) позыве, вызванном ГМП, может происходить непроизвольное сокращение не только детрузора, но и наружного уретрального сфинктера (диссинергия). Это – защитный рефлекс организма, чтобы предотвратить недержание мочи. В результате возникает функциональное сопротивление току мочи, которое напоминает обструкцию. Также хроническая гиперактивность детрузора может сопровождаться повышенным тонусом гладких мышц шейки мочевого пузыря, что также добавляет элемент функционального сопротивления. Результаты настоящего исследования наглядно показали эффективность комбинации алфузозина (α1-АБ) и солифенацина (МХЛ), выступающих синергично при нарушениях мочеиспускания подобного типа.
Считают, что возникновению вторичного ГМП при ДГПЖ способствует дисфункция мочевого пузыря, связанная с ИВО, что приводит к высокому давлению при мочеиспускании, чрезмерному растяжению детрузора и ишемии стенки мочевого пузыря. Известно, что а1-АБ снижают степень ИВО, тем самым улучшая симптомы ГМП у пациентов с ДГПЖ [37, 38]. При этом, уменьшение ургентности тесно связано с улучшением оттока мочи: снижение функциональной обструкции и уменьшение уретрального сопротивления на фоне приема а1-АБ улучшают симптомы ГМП [32]. O. Yokoyama и соавт. связали нарушения фазы накопления у больных ДГПЖ с повышением активности афферентных путей от простатического отдела уретры [39]. Позже этот же автор сообщил, что механизм, с помощью которого а1-АБ улучшают симптомы ГМП у пациентов с ДГПЖ, заключается в ингибирующем действие на С-волокна афферентных нервов уретры [40]. Иными словами, возбуждение чувствительных волокон (нервов) уретры и ПЖ может способствовать нарушению процесса накопления и удержания мочи. Эти сообщения подтверждают результаты, демонстрирующие значительную корреляцию между снижением ургентности и улучшением оттока мочи [32]. В обсуждаемой программе высокодостоверному улучшению УФМ-показателей сопутствовало значимое снижение симптомов ГМП по шкалам IPSS и OABSS и ургентности по PPIUS (табл. 1).
Антихолинергические препараты эффективны для лечения симптомов ГМП у пациентов с ДГПЖ, но могут вызвать нежелательные явления, такие как затрудненное мочеиспускание или ОЗМ. Стойкие симптомы ГМП у пациентов с ДГПЖ, безусловно, способствуют возникновению патологических состояний, связанных с нарушенным оттоком мочи, и могут еще больше осложнить обструкцию. Показано, что МХЛ, применяемые для лечения ГМП у мужчин, статистически недостоверно изменяли параметры мочеиспускания и приводили к увеличению объема остаточной мочи и частоты ОЗМ [3, 41]. Однако солифенацин в сочетании с α1-АБ не вызывал достоверного ухудшения Qmax у мужчин с симптомами ГМП [42, 43], повышение объема остаточной мочи не было клинически значимым, а риск развития ОЗМ – низким до одного года наблюдения [43]. В целом, Европейская ассоциация урологов (EAU) указывает, что существует низкий риск развития ОЗМ при использовании α1-АБ и МХЛ у мужчин с СНМП/ДГПЖ и ГМП, при объеме остаточной мочи менее 150 мл [2].
В исследованиях комбинированной терапии α1-АБ и МХЛ, представленных S.A. Kaplan и соавт. и H.J. Cho и соавт., на фоне увеличения Qmax на 19,4% и 18,4% к концу наблюдения зарегистрирован рост объема остаточной мочи на 68,2% и 94,6% соответственно, что, однако, не было клинически значимым [44, 45]. В настоящей наблюдательной программе в ПГ1 и ПГ2 к третьему месяцу наблюдения на фоне увеличения Qmax на 37,1% и 74,2% и объема мочеиспускания на 10,0% и 3,5%, выявлено уменьшение остаточной мочи на 76,9% и 74,2% соответственно, что подтверждает высокую безопасность лечения.
Форма урофлоуметрической кривой – важный, но трудно оцениваемый в клинических исследованиях критерий. Нами не найдено работ, в которых на фоне лечения оценивали бы типы УФМ-кривых и их динамику. В настоящей работе это удалось благодаря использованию оригинального специально разработанного шаблона. Ранее нами было показано, что в общей группе, наряду с улучшением урофлоуметрических показателей, доля пациентов с формой кривой приближенной к норме за три месяца комбинированного лечения увеличилась с 5,3% до 44,2%. Также произошло перераспределение в пользу обструктивной кривой пологого типа, достигшей 38%, за счет других типов кривых [5]. В настоящем исследовании нормализация формы УФМ-кривых произошла с 0% до 36,3% в ПГ1 и с 10,4% до 51,9% в ПГ2. Обструктивные кривые пологого типа к концу исследования наблюдали у 39,2% и 36,8% соответственно (табл. 2).
ЗАКЛЮЧЕНИЕ
Таким образом, обсуждаемое исследование продемонстрировало высокую результативность и безопасность комбинированной терапии алфузозином (Алфупрост® МР) и солифенацином (Везигамп) пациентов с СНМП/ДГПЖ с умеренными и выраженными нарушениями мочеиспускания по данным УФМ. Успех лечения достигнут благодаря как при-менению эффективной комбинации препаратов, так и корректному отбору больных на лечение, с исключением из программы случаев ИВО механического типа.
ЛИТЕРАТУРА
- Раснер П.И., Сивков А.В., Харчилава Р.Р. Клинические рекомендации. Доброкачественная гиперплазия предстательной железы. Согласованы Научным Советом Министерства здравоохранения Российской Федерации 13.06.2024. 95 с. URL: https://cr.minzdrav.gov.ru/view-cr/6_2.
- Cornu JN, Gacci M, Hashim H, Herrmann TRW, Malde S, Netsch C, et al. EAU guidelines on nonneurogenic male lower urinary tract symptoms (LUTS). Limited update April 2024. Guidelines Office. https://uroweb.org/guidelines/managementof-non-neurogenic-male-luts/chapter/disease-management.
- Kaplan SA, Roehrborn CG, Rovner EC, Carlsson M, Bavendam T., Guan Z. Tolterodine and tamsulosin for treatment of men with lower urinary tract symptoms and overactive bladder: a randomized controlled trial. JAMA 2006;296(19):2319-28. https://doi.org/10.1001/jama.296.19.2319
- Blake-James BT, Rashidian A, Ikeda Y, Emberton M. The role of anticholinergics in men with lower urinary tract symptoms suggestive of benign prostatic hyperplasia: a systematic review and meta-analysis. BJU Int 2007;99(1):85–96. https://doi.org/10.1111/j.1464-410X.2006.06574.x
- Сивков А.В. и исследовательская группа «АВИАТОР». Эффективность и безопасность комбинированной терапии препаратами алфузозин (Алфупрост® МР) и солифенацин (Везигамп) у больных доброкачественной гиперплазией предстательной железы и гиперактивным мочевым пузырем: первые результаты наблюдательного многоцентрового исследования «АВИАТОР». Экспериментальная и клиническая урология 2023;16(4):44-56. [Sivkov A.V. and the AVIATOR research group. Efficacy and safety of combination therapy with alfuzosin (Alfuprost® MR) and solifenacin (Vesigamp) in patients with benign prostatic hyperplasia and overactive bladder: first results of the observational multicenter «AVIATOR» study. Eksperimentalnaya i klinicheskaya urologiya= Experimental and Clinical Urology 2023;16(4):44-56. (In Russian)]. https://doi.org/10.29188/2222–8543–2023–16–4–44–56
- Сивков А.В., Пантелеев В.В., Ромих В.В., Кукушкина Л.Ю., Захарченко А.В., Аполихин О.И., Каприн А.Д. Сравнительная эффективность комбинированной терапии препаратами алфузозин (Алфупрост® МР) и солифенацин (Везигамп) у больных ДГПЖ и гиперактивным мочевым пузырем с умеренными и выраженными симптомами нарушения функции нижних мочевых путей. Экспериментальная и клиническая урология 2024;17(4):56-66. [Sivkov A.V., Panteleev V.V., Romikh V.V., Kukushkina L.Yu., Zakharchenko A.V., Apolikhin O.I., Kaprin A.D. Comparative effectiveness of alfuzosin (Alfuprost® MR) and solifenacin (Vesigamp) combination therapy in patients with BPH and overactive bladder, with moderate and severe symptoms of lower urinary tract dysfunction. Eksperimentalnaya i klinicheskaya urologiya= Experimental and Clinical Urology 2024;17(4):56-66. (In Russian)]. https://doi.org/10.29188/2222-8543-2024-17-4-56-66
- IdzengaT, Pel JJ, van Mastrigt R. Accuracy of maximum flow rate for diagnosing bladder outlet obstruction can be estimated from the ICS nomogram. Neurourol Urodyn 2008;27(1): 97-8. https://doi.org/10.1002/nau.20480
- Reynard JM, Yang Q, Donovan JL, Peters TJ, Schafer W, de la Rosette JJ, et al. The ICS-’BPH’ Study: uroflowmetry, lower urinary tract symptoms and bladder outlet obstruction. Br J Urol 1998;82(5):619-23.
- Malde S, Nambiar AK, Umbach R, Lam TB, Bach T, Bachmann F, et al. Systematic review of the performance of noninvasive tests in diagnosing bladder outlet obstruction in men with lower urinary tract symptoms. Eur Urol 2017;71(3):391-402. https://doi.org/10.1016/j.eururo.2016.09.026
- Mehraban D. Clinical value of intravesical prostatic protrusion in the evaluation and man-agement of prostatic and other lower urinary tract diseases. Asian J Urol 2017;4(3):174-80. https://doi.org/10.1016/j.ajur.2016.10.001
- Yuen JSP, Ngiap JTK, Cheng CWS, Foo KT. Effects of bladder volume on transabdominal ultrasound measurements of intravesical prostatic protrusion and volume. Int J Urol 2002;9(4):225-9. https://doi.org/10.1046/j.1442-2042.2002.00453.x.9:225e9.
- Chia SJ, Heng CT, Chan SP, Foo KT. Correlation of intravesical prostatic protrusion with bladder outlet obstruction. BJU Int 2003;91(4):371-4. https://doi.org/10.1046/j.1464-410x.2003.04088.x
- Kuo TL, Teo JS, Foo KT. The role of intravesical prostatic protrusion (IPP) in the evaluation and treatment of bladder outlet obstruction (BOO). Neurourol Urodyn 2016;35(4):535-7. https://doi.org/10.1002/nau.22741
- Wang D, Huang H, Law YM, Foo KT. Relationships between prostatic volume and intravesical prostatic protrusion on transabdominal ultrasound and benign prostatic obstruction in patients with lower urinary tract symptoms. Ann Acad Med Singap 2015;44(2):60-5.
- Кривобородов Г.Г., Ефремов Н.С., Болотов А.Д. Ультразвуковые показатели предстательной железы, мочевого пузыря и данные урофлоуметрии в диагностике инфравезикальной обструкции у мужчин с доброкачественной гиперплазией предстательной железы. Урология 2017;(5):9-14. [Krivoborodov G.G., Efremov N.S., Bolotov A.D. Ultrasound indicators of the prostate, urinary bladder and uroflowmetry parameters in the diagnosis of infravesical obstruction in men with benign prostatic hyperplasia. Urologiya = Urologiia 2017;(5):9-14. (In Russian)]. https://dx.doi.org/10.18565/urology.2017.5.9-14
- Doo CK, Uh HS. Anatomic configuration of prostate obtained by noninvasive ultrasonography can predict clinical voiding parameters for determining BOO in men with LUTS. Urology 2009;73(2):232-6. https://doi.org/10.1016/j.urology.2008.09.055
- Cumpanas AA, Botoca M, Minciu R, Bucuras V. Intravesical prostatic protrusion can be a predicting factor for the treatment outcome in patients with lower urinary tract symptoms due to benign prostatic obstruction treated with tamsulosin. Urology 2013;81(4):859-63. https://doi.org/10.1016/j.urology.2012.12.007
- Gandhi J, Weissbart SJ, Kim AN, Joshi G, Kaplan SA, Khan SA. Clinical considerations for intravesical prostatic protrusion in the evaluation and management of bladder outlet obstruction secondary to benign prostatic hyperplasia. Current Urol 2018;12(1):6-12.https://doi.org/10.1159/000447224
- Eze BU, Amu OC, Edeh JA. A review of intravesical prostatic protrusion in the evaluation and treatment of benign prostatic enlargement. European Journal of Medical and Health Sciences 2021;3(1):13-7. https://doi.org/10.24018/ejmed.2021.3.1.648
- Foo KT. Pathophysiology of clinical benign prostatic hyperplasia. Asian J Urol 2017;4(3):152-7. https://doi.org/10.1016/j.ajur.2017.06.003
- Lee LS, Sim HG, Lim KB, Wang D, Foo KT. Intravesical prostatic protrusion predicts clinical progression of benign prostatic enlargement in patients receiving medical treatment. Int J Urol 2010;17(1):69-74. https://doi.org/10.1111/j.1442-2042.2009.02409.x
- Сивков А.В., Аполихин О.И., Патаки К.В. Современный алгоритм обследования и лечения больных доброкачественной гиперплазией предстательной железы. Consilium Medicum 2004;6(7):516-24. [Sivkov A.V., Apolikhin O.I., Pataki K.V. Modern algorithm for examination and treatment of patients with benign prostatic hyperplasia. Consilium Medicum 2004;6(7):516-24.(In Ruissan)].
- Аполихин О.И., Сивков А.В., Ромих В.В., Положенцева М.О. Аденома предстательной железы и гиперактивный мочевой пузырь: оценка симптомов и выбор терапии. Урология 2009;(2):78-84. [Apolikhin O.I., Sivkov A.V., Romikh V.V., Polozhentseva M.O. Prostatic adenoma and overactive urinary bladder: assessment of symptoms and choice of therapy. Urologiya = Urologiia 2009;(2):78-84. (In Russian)].
- Mangat R, Ho HS, Kuo TL. Non-invasive evaluation of lower urinary tract symptoms (LUTS) in men. Asian J Urol 2017,(5):42-7. https://doi.org/10.1016/j.ajur.2017.12.002
- Lim KB, Ho H, Foo KT, Wong MY, Fook-Chong S. Comparison of intravesical prostatic protrusion, prostate volume and serum prostatic‐specific antigen in the evaluation of bladder outlet obstruction. Int J Urol 2006;13(12):1509-13. https://doi.org/10.1111/j.1442-2042.2006.01611.x
- Park HY, Lee JY, Park SY, Lee SW, Kim YT, Choi HY, et al. Efficacy of alpha blocker treatment according to the degree of intravesical prostatic protrusion detected by transrectal ultrasonography in patients with benign prostatic hyperplasia. Korean J Urol 2012;53(2):92-7. https://doi.org/10.4111/kju.2012.53.2.92
- Kalkanli A, Tandogdu Z, Aydin M, Karaca AS, Hazar AI, Balci MB, et al. Intravesical prostatic protrusion: a potential marker of alpha-blocker treatment success in patients with benign prostatic enlargement. Urology 2016;88:161-5. https://doi.org/10.1016/j.urology.2015.11.029
- Topazio L, Perugia C, De Nunzio C, Gaziev G, Iacovelli V, Bianchi D, et al. Intravescical prostatic protrusion is a predictor of alpha blockers response: results from an observational study. BMC Urology 2018;18(1):6. https://doi.org/10.1186/s12894-018-0320-0
- Hirayama K, Masui K, Hamada A, Shichiri Y, Masuzawa N, Hamada S. Evaluation of intravesical prostatic protrusion as a predictor of dutasteride-resistant lower urinary tract symptoms/benign prostatic enlargement with a high likelihood of surgical intervention. Urology 2015;86(3):565-9. https://doi.org/10.1016/j.urology.2015.05.021
- Itoh H., Kojima M., Okihara K., Ukimura O, Ushijima S, Kawauchi A, Miki T. Significant relationship of time-dependent uroflowmetric parameters to lower urinary tract symptoms as measured by the International Prostate Symptom Score. Int J Urol 2006;13(8):1058-65. https://doi.org/10.1111/j.1442-2042.2006.01496.x
- Kaplan SA, Reis RB. Significant correlation of the American Urological Association symptom score and a novel urodynamic parameter: detrusor contraction duration. J Urol 1996;156(5):1668-72.
- Matsukawa Y, Takai S, Asai K, Kasugai S, Narita H, Komatsu T, et al. A slow stream is pathophysiologically related to a poor response to a1-adrenoceptor therapy in the treatment of storage symptoms associated with benign prostatic hyperplasia. Urology 2015;86(3):558-64. https://doi.org/10.1016/j.urology.2015.03.060
- Moss MC, Rezan T, Karaman UR, Gomelsky A. Treatment of concomitant OAB and BPH. Curr Urol Rep 2017;18(1):1. https://doi.org/10.1007/s11934-017-0649-z
- Kim KH, Kim YS. Correlation of male overactive bladder with intravesical prostatic protrusion. Korean J Urol 2010;51(12):843-6.https://doi.org/10.4111/kju.2010.51.12.843
- Matsukawa Y, Majima T, Ishida S, Funahashi Y, Kato M, Gotoh M. Useful parameters to predict the presence of detrusor overactivity in male patients with lower urinary tract symptoms. Neurourol Urodyn 2020;39(5):1394-1400. https://doi.org/10.1002/nau.24352
- Tsai CH, Lee WC, Shen YC, Wang HJ, Chuang YC. The role of intravesical prostatic protrusion in the evaluation of overactive bladder in male patients with LUTS. Int Urol Nephrol 2020;52(5):815-20. https://doi.org/10.1007/s11255-019-02370-4
- Nishino Y, Masue T, Miwa K, Takahashi Y, Ishihara S, Deguchi T. Comparison of two al-pha1adrenoceptor antagonists, naftopidil and tamsulosin hydrochloride, in the treatment of lower urinary tract symptoms with benign prostatic hyperplasia: a randomized crossover study. BJU Int 2006;97(4):747-51. https://doi.org/10.1111/j.1464-410X.2006.06030.x
- Matsukawa Y, Gotoh M, Komatsu T, et al. Efficacy of silodosin for relieving benign prostatic obstruction: prospective pressure flow study. J Urol 2009;182:2831-5.
- Yokoyama O, Nagano K, Kawaguchi K, et al. The influence of prostatic urethral anesthesia in overactive detrusor in patients with benign prostatic hyperplasia. J Urol 1994;151:1554-6.
- Yokoyama O, Yusup A, Oyama N, Aoki Y, Miwa Y, Akino H. Improvement in bladder storage function by tamsulosin depends on suppression of C-fiber urethral afferent activity in rats. J Urol 2007;177(2):771-5. https://doi.org/10.1016/j.juro.2006.09.076
- van Kerrebroeck P, Chapple C, Drogendijk T, Klaver M, Sokol R, Speakman M. et al. Combination therapy with solifenacin and tamsulosin oral controlled absorption system in a single tablet for lower urinary tract symptoms in men: efficacy and safety results from the randomised controlled NEPTUNE trial. Eur Urol 2013;64(6):1003-12. https://doi.org/10.1016/j.eururo.2013.07.034
- Gong M, Dong W, Huang H, Gong Z, Deng D, Qiu S, et al. Tamsulosin combined with solifenacin versus tamsulosin monotherapy for male lower urinary tract symptoms: a meta-analysis. Curr Med Res Opin 2015; 31(9):1781-92. https://doi.org/10.1185/03007995.2015.1074067
- Drake MJ, Oelke M, Snijder R, Klaver M, Traudtner K, van Charldorp K. et al. Incidence of urinary retention during treatment with single tablet combinations of solifenacin+tamsulosin OCAS for up to 1 year in adult men with both storage and voiding LUTS: A subanalysis of the NEPTUNE/NEPTUNE II randomized controlled studies. PLoS One 2017;12(2):e0170726. https://doi.org/10.1371/journal.pone.0170726
- Kaplan SA, He W, Koltun WD, Cummings J, Schneider T, Fakhoury A. Solifenacin plus tamsulosin combination treatment in men with lower urinary tract symptoms and bladder outlet obstruction: a randomized controlled trial. Eur Urol 2013; 63(1):158–65. https://doi.org/10.1016/j.eururo.2012.07.003
- Cho HJ, Shin SC, Seo DY, Cho JM, Kang JY, Yoo TK. et al. Comparison of alfuzosin 10 mg with or without propiverine 10 mg, 20 mg in men with lower urinary tract symptom and an overactive bladder: randomised, single-blind, prospective study. Int J Clin Pract 2014;68(4):471–7. https://doi.org/10.1111/ijcp.12339








 Скачать
Скачать