Эректильная функция у больных раком предстательной железы
Е.А. Ефремов
НИИ урологии Минздравсоцразвития РФ, Москва
Проблема эректильной дисфункции (ЭД) у больных
раком предстательной железы (РПЖ) в настоящее время очень актуальна. По данным разных авторов, из ста больных, обращающихся к урологам с проблемой ЭД, в 3,5% случаях диагностируется высокий уровень простатспецифического антигена (ПСА), который практически всегда свидетельствует о наличии онкологического диагноза. В то время как одним из главных современных показателей качества жизни у больных раком предстательной железы является отсутствие ЭД (Burger В. et al., 1999; Singer P.A. et al., 1991).
Сексуальная функция при РПЖ
Изменения в сексуальной сфере мужчины наступают сразу после начала обследования по поводу РПЖ. Процесс обследования всегда вызывает стресс и обеспокоенность по поводу результатов биопсии и дальнейших перспектив лечения, что, несомненно, оказывает существенное влияние на либидо и качество жизни (Visser, 2006).
Следует отметить, что беспокойство и ухудшение сексуальной функции появляются уже сразу приобнаружении повышенных значений ПСА еще до биопсии (Katz, 2007; McGovern, 2004). А после верификации диагноза РПЖ большинство пациентов испытывают депрессию и отмечают снижение потребности в сексе (Turns, 2001). Психологические проблемы у многих пациентов основаны на канцерофобии (Fossa S.D., 1997; Schover L.R., 2002; Roos I.A.G., 2003).
Определение исходного уровня сексуальной функции по данным, полученным в период подготовки к оперативному лечению, в большинстве случаев неверно. Такой способ дает заниженные по отношению к истинному уровню показатели (Раднаев Л.Г., Пушкарь Д.Ю., 2011).
В настоящее время известно, что в зависимости от метода лечения РПЖ частота ЭД варьирует в диапазоне от 14 до 96% (Thüroff S. et al., 2000; Kao T., 2000; Stanford J.L., 2000; Schover L.R., 2002; Matthew A.G., 2005; Eastham J.A., 2008; Sanda M.G., 2008) (таблица 1).
Таблица 1. Частота осложнений после применения различных методов лечения РПЖ
| Метод | Свищи | Императивные позывы | Недержание мочи | ЭД |
| Радикальная простатэктомия | < 0,5-4% | 6-16% | 7-52% | 14-96% |
| Дистанционная лучевая терапия | Нет данных | 19-43% | 0-15% | 50-61% |
| Брахитерапия | 0-3% | 19-43% | 0-19% | 14-66% |
| HIFU | < 0,5-5% | Нет данных | 0-2% | 28-30% |
| Криоабляция | 0-0,5% | Нет данных | 1-7% | 47-95% |
Эректильная функция после лечения РПЖ
Что касается сохранности эректильной функции после применения различных методов лечения РПЖ (рисунок 1), то минимально инвазивными являются дистанционная радиотерапия, позволяющая избежать ЭД в 78% случаев, брахитерапия (75%), андрогенная депривация (50%). Что же касается РПЭ и криотерапии, то, по данным Robinson J.W. et al., 2001, 29-30% больных остаются с сохранной эректильной функцией.
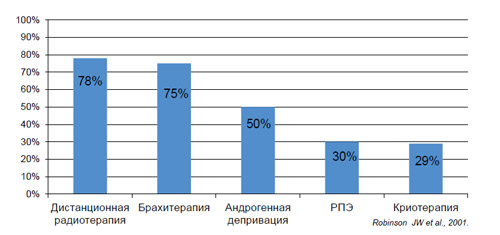
Рисунок 1. Сохранность эректильной функции после применения различных методов лечения РПЖ (n=1051, срок наблюдения 3 года)
Осложнения после РПЭ – наиболее изученный вопрос по сравнению с другими методами лечения, учитывая богатый опыт использования этой методики в отношении больных с РПЖ.
Осложнения делятся на ранние и поздние. К ранним относятся: значительная кровопотеря, повреждение прямой кишки (< 1%), смертность (0,3%), тромбоз глубоких вен (1,1%), тромбоэмболия легочной артерии (1,3%), инфекционные осложнения (1,5%), лимфоцеле (3,4%). Среди поздних осложнений особое внимание следует обратить на недержание мочи и ЭД преимущественно нейрогенной и васкулогенной формы (таблица 2). Эти два осложнения, в основном, и определяют качество жизни пациентов.
Таблица 2. Частота ЭД после РПЭ
| Автор | N | Наблюдение | Методика | % ЭД п/о |
|---|---|---|---|---|
| Gralnek, 2000 | 83 46 |
>12 мес. >12 мес. |
NNSP UNSP |
95 % 61 % |
| Kao, 2000 | 887 | >6 мес. | – | 88 % |
| Rabbani, 2000 | 314 | >36 мес. | BNSP (181), UNSP (107), NNSP (26) |
50 % |
| Stanford, 2000 | 1291 | >18 мес. | BNSP UNSP NNSP |
56 % 59 % 66 % |
| Thukral, 2000 | 143 | 12 мес. | NSP (64%), NNSP (36%) |
61 % |
| Michl, 2001 | 226 63 |
19 мес. | UNSP BNSP |
84 % 54 % |
Частота встречаемости ЭД после РПЭ в зависимости от методики выполнения варьирует от 50 до 95%
Кроме того, эти мужчины психологически отягощены, поэтому нужно учитывать также и данные аспекты.
Частота встречаемости ЭД после РПЭ в зависимости от методики выполнения варьирует от 50 до 95% (Gralnek, 2000; Kao, 2000; Rabbani, 2000; Stanford, 2000; Thukral, 2000; Michl, 2001).
По данным российских исследований процент наличия эректильных расстройств в послеоперационном периоде практически равен 100 (Велиев Е.И., 2003; Алексеев Б.Я., 2003; Пушкарь Д.Ю., 2003).
Что касается вопроса восстановления эректильной функции после РПЭ, то очень интересным в этом плане является исследование, проведенное Б. Джаваном в 2006 г., в котором автор показал, что в сроки до двенадцати месяцев после выполнения РПЭ происходит реиннервация и реваскуляризация, на фоне чего эректильная функция постепенно несколько улучшается.
Briganti A. et al. (2006), Велиев Е.И. (2008) в своих работах показали, что ухудшение эрекции в раннем послеоперационном периоде после нервосохраняющей РПЭ связано с развитием нейропраксии, возникающей вследствие неизбежного повреждения кавернозных нервов.
А Shrader-Bogen C.L. (1997), Cooperberg M.R. (2003), Meyer J.P. (2003) обратили внимание на то, что при относительно удовлетворительном качестве жизни пациентов в послеоперационном периоде у 60,0% из них послеоперационная ЭД является причиной эмоциональных нарушений и конфликтов с половыми партнерами.
Особое внимание следует уделить прогнозу сохранения сексуальной функции в отношении всех методик, которые используются при обследовании и лечении больных РПЖ. Разные авторы (Osterling J.E., 1997; Borghede G., 1997; Flanigan R.C., 1998; Eastham J., 2003; Hollenbeck B.K., 2003; Dubbelman Y.D., 2006; Giuliano F., 2008) выделяют определенные факторы, влияющие на прогноз сохранения эректильной функции при этом заболевании. К таким факторам относятся: метод лечения РПЖ, нервосбережение при РПЭ,стадия заболевания, возраст, отсутствие ЭД до операции, отсутствие недержания мочи в послеоперационном периоде, отсутствие рецидива РПЖ, хирургические навыки вра-
ча, отсутствие канцерофобии и тяжелых форм депрессии, отсутствие «острых» осложнений, уровень ПСА менее 10 нг/мл, сумма Глисона менее 6, отсутствие пальпаторных признаков заболевания при пальцевом ректальном исследовании.
В зависимости от методики оперативного лечения, эффективность применения ингибиторов фосфодистеразы пятого типа (ФДЭ-5), как первой линии терапии в лечении ЭД после РПЭ располагается в диапазоне от 0 до 80%.
По данным НИИ урологии (2010) у 82% больных, которые перенесли РПЭ, отмечалась ЭД, в основном, в виде тяжелых форм (68%).
При рассмотрении динамики показателей эректильной функции в течение первого года после РПЭ отмечается резкое снижение эректильной функции сразу после операции. Но, в результате реваскуляризации, реиннервации и разрешений нейропраксии улучшение эректильной функции наблюдается в сроки от 12 до 18 месяцев даже при отсутствии лекарственной терапии(таблица 3). Иная ситуация наблюдается после применения HIFU и брахитерапии – после операции практически в течение месяца отмечается незначительное снижение эректильной функции с последующим ее восстановлением до исходного уровня, но, в дальнейшем, в течение года эректильная функция постепенно снижается.
Таблица 3. Восстановление ЭФ после РПЭ
| Срок наблюдения после БлНСРПЭ, билатеральной, нервосберегающей РПЭ |
Сохранность эректильной функции без лечения |
|---|---|
| 3 мес. | 9-16% |
| 6 мес. | 21-29% |
| 12 мес. | 56-86% |
Djavan B. et al., 2006
Особое внимание следует обратить на сочетание нейрогенного и васкулогенного компонента ЭД. При фармакодопплерографии сосудов полового члена диагностируется снижение скорости кровотока по пенильным артериям, а при мониторинге ночных пенильных тумесценций выявляется их урежение и снижение по амплитуде и времени.
При выполнении электромиографии в 75,8% наблюдений отмечаются изменения в виде нерегулярных потенциалов низкой частоты и амплитуды, а у 24,2% пациентов выявлено практически полное отсутствие электрической активности при сочетании с положительным фармакотестом, что расценивается как денервация кавернозной ткани в результате проведенной операции (таблица 4).
Таблица 4. Данные электромиографии полового члена у пациентов до и через 1 год после РПЭ (n = 62)
| Показатели ЭМГ | До операции | После операции | ||||
|---|---|---|---|---|---|---|
| Фаза покоя | Фаза тумесценции |
Фаза эрекции | Фаза покоя | Фаза тумесценции |
Фаза эрекции | |
| Амплитуда (мкВ) | 142,7±21,7 | 89,4±16,8 | 0 | 76,8±20,3 | 34,2±14,6 | 0 |
| Частота потенциалов в минуту | 5,2±1,8 | 15,2±3,8 | 0 | 4,8±1,2 | 12,6±3,4 | 0 |
| Длительность (сек.) | 9,2±3,3 | 1,2±1,8 | 0 | 6,9±2,1 | 3,8±1,2 | 0 |
| Количество фаз | 5,2±0,9 | 3,2±0,5 | 0 | 3,7±0,9 | 3,1±0,9 | 0 |
При проведении анализа данных госпитальной шкалы депрессии и тревоги было выявлено, что еще до выполнения РПЭ у 86% больных отмечалась депрессия. Через год после операции происходило снижение депрессивных расстройств не до нормы, но до субклинических ее проявлений (рисунок 2).
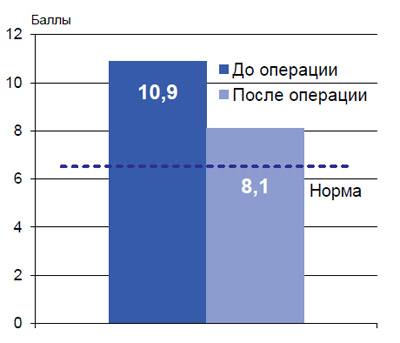
Рисунок 2. Анализ госпитальной шкалы депрессии и тревоги (сроки наблюдения 12 месяцев после РПЭ, n=62)
Что касается брахитерапии, которая позиционируется как неагрессивный метод лечения, в качестве осложнений после ее выполнения, кроме ЭД (14-49,5%) чаще всего встречаются симптомы нижних мочевых путей и симптомы поражения кишечника (Ash D. et al., 2007; Bottomley D. et al., 2007).
Причем существует достоверная корреляция между уровнем эректильной функции в до- и послеоперационном периоде (Merrick G.S., 2002; Fujioka H., 2004; Merrick G.S., 2005; Stock R.G., 2006). Также большое значение имеют величина радиационной дозы, использование адъювантной – неоадъювантной химиотерапии (прежде всего, гормональной терапии, андрогенной депривации) и возраст пациентов (Stock R.G., 2001; Valicenti R.K., 2002; Merrick G.S., 2005; Macdonald A.G., 2005).
Выводы
1. ЭД – часто встречаемое осложнение, возникающее в послеоперационном периоде при использовании любого метода лечения
РПЖ.
2. Продолжительное использование ингибиторов ФДЭ-5, начатое в ранние сроки и на регулярной основе в качестве эффективного перорального препарата значительно повышает параметры, определяющие эректильную функцию и удовлетворение сексуальной жизнью пациентов при длительном наблюдении.
3. Сексуальная реабилитация пациентов может продолжаться долгое время (до 18-24 месяцев).
4. Методы коррекции могут варьировать от лекарственной, вакуумконстрикторной терапии, интракавернозного введения азоактивных препаратов при интактной васкулярной системе вплоть до эндофаллопротезирования при грубых органических изменениях.
РПЖ – это специфическое заболевание, влияющее на психическую и соматическую функцию организма, в том числе на сексуальную функцию, степень нарушения которой зависит от множества факторов и оказывает негативное влияние на физическое, эмоциональное состояние пациента, так и на его социальный статус. Решение данной проблемы и улучшение качества жизни, независимо от возраста и стадии заболевания, должно включаться в план общей терапевтической стратегии и должно быть согласовано с больным изначально.
Ключевые слова: эректильная дисфункция, рак предстательной железы, радикальная простатэктомия, брахитерапия, HIFU, криоабляция.
Keywords: erectile dysfunction, prostate cancer, radical prostatectomy, brachytherapy, HIFU, kryoablation.






